Фуллерены и их синтез.ppt
- Количество слайдов: 31

Фуллерены и их синтез
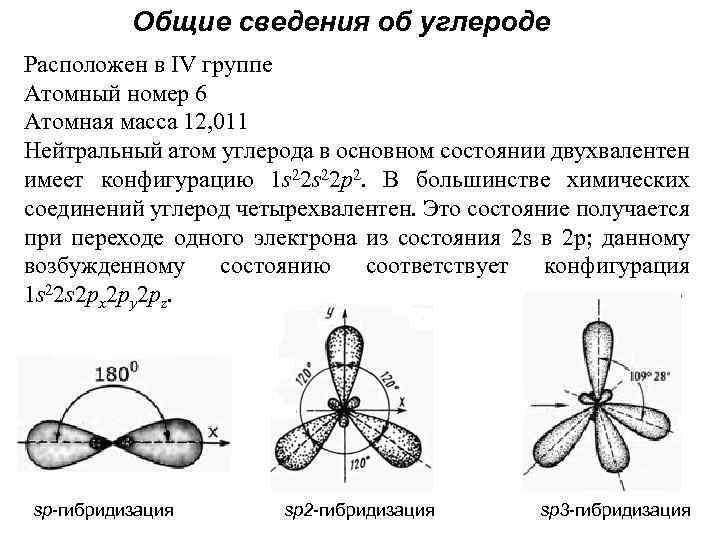
Общие сведения об углероде Расположен в IV группе Атомный номер 6 Атомная масса 12, 011 Нейтральный атом углерода в основном состоянии двухвалентен имеет конфигурацию 1 s 22 p 2. В большинстве химических соединений углерод четырехвалентен. Это состояние получается при переходе одного электрона из состояния 2 s в 2 p; данному возбужденному состоянию соответствует конфигурация 1 s 22 s 2 px 2 py 2 pz. sp-гибридизация sp 2 -гибридизация sp 3 -гибридизация
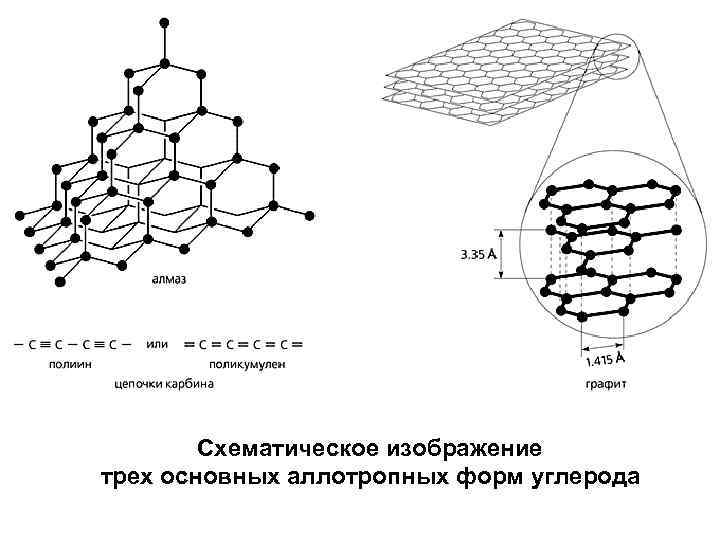
Схематическое изображение трех основных аллотропных форм углерода
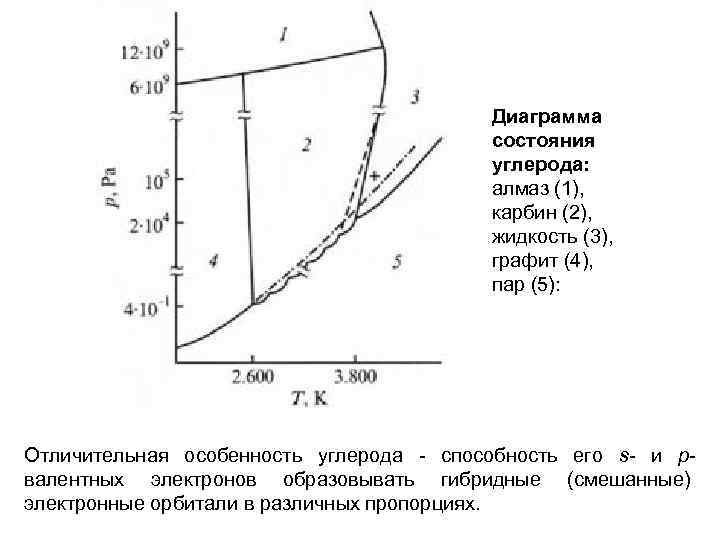
Диаграмма состояния углерода: алмаз (1), карбин (2), жидкость (3), графит (4), пар (5): Отличительная особенность углерода - способность его s- и pвалентных электронов образовывать гибридные (смешанные) электронные орбитали в различных пропорциях.
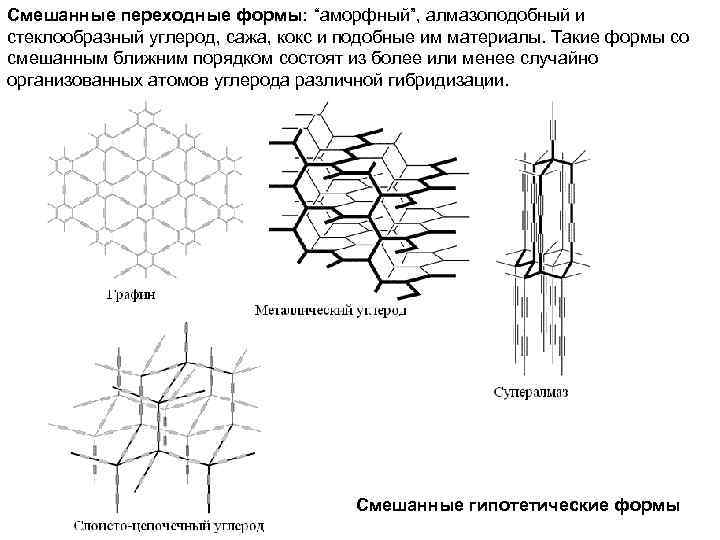
Смешанные переходные формы: “аморфный”, алмазоподобный и стеклообразный углерод, сажа, кокс и подобные им материалы. Такие формы со смешанным ближним порядком состоят из более или менее случайно организованных атомов углерода различной гибридизации. Смешанные гипотетические формы
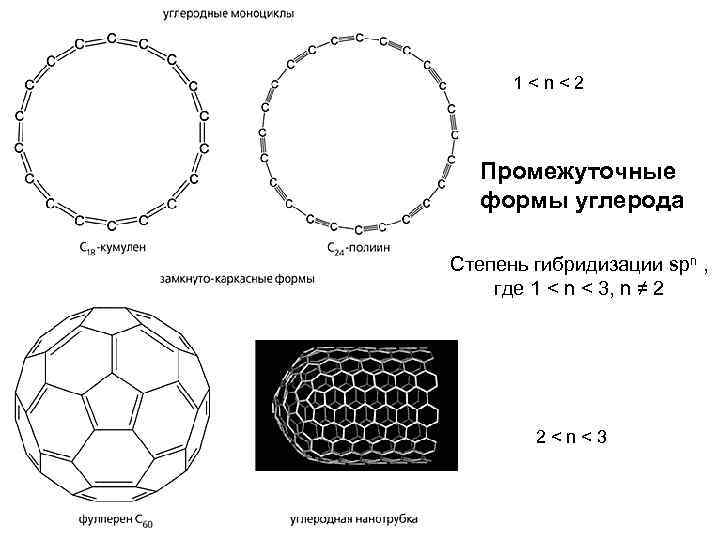
1 < n < 2 Промежуточные формы углерода Степень гибридизации spn , где 1 < n < 3, n ≠ 2 2 < n < 3
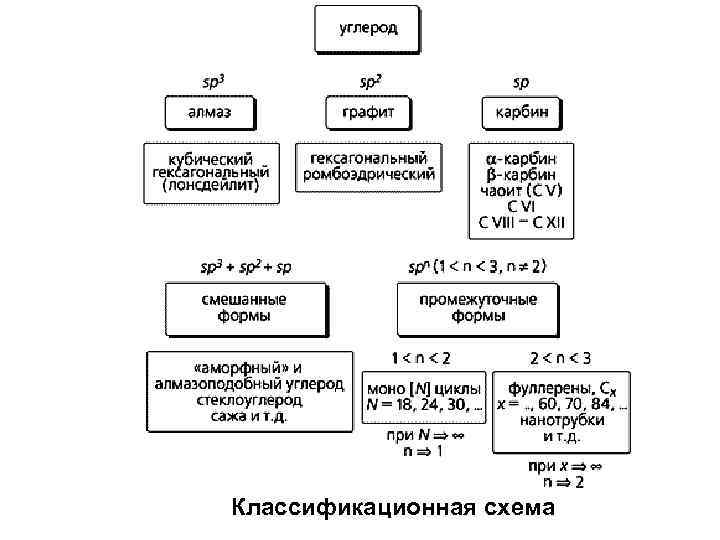
Классификационная схема
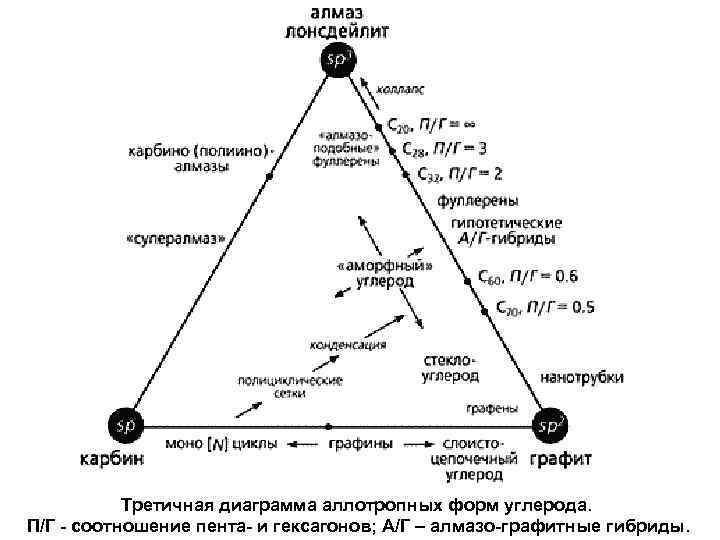
Третичная диаграмма аллотропных форм углерода. П/Г - соотношение пента- и гексагонов; А/Г – алмазо-графитные гибриды.

Масс-спектр углеродных кластеров
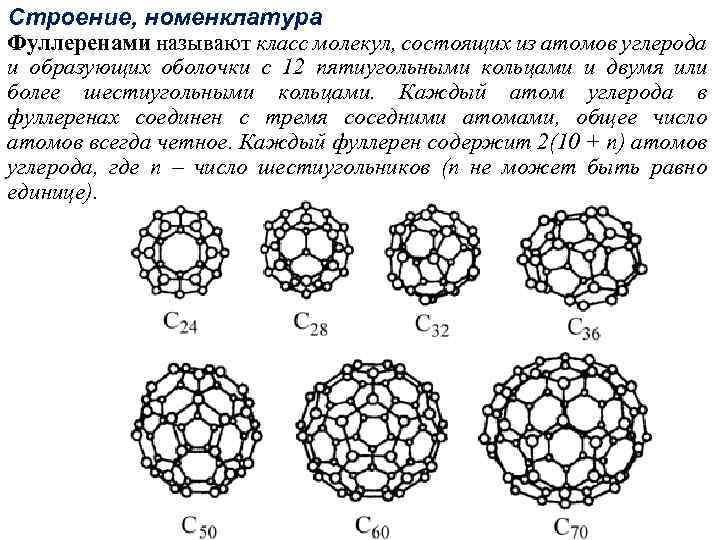
Строение, номенклатура Фуллеренами называют класс молекул, состоящих из атомов углерода и образующих оболочки с 12 пятиугольными кольцами и двумя или более шестиугольными кольцами. Каждый атом углерода в фуллеренах соединен с тремя соседними атомами, общее число атомов всегда четное. Каждый фуллерен содержит 2(10 + n) атомов углерода, где n – число шестиугольников (n не может быть равно единице).
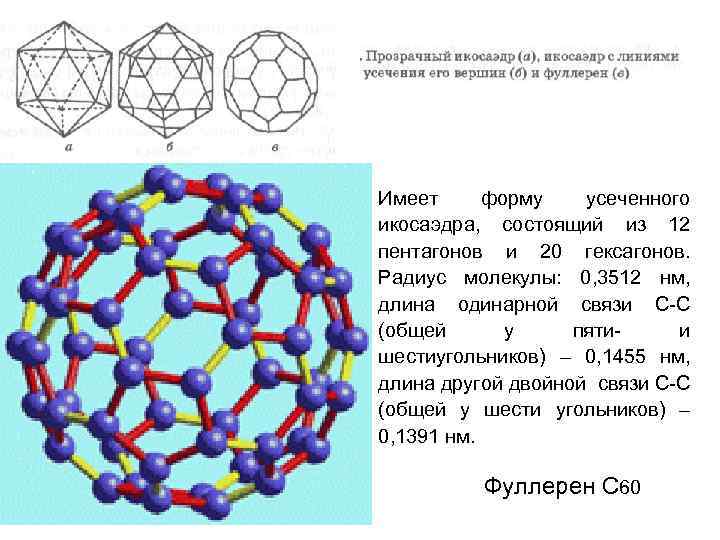
Имеет форму усеченного икосаэдра, состоящий из 12 пентагонов и 20 гексагонов. Радиус молекулы: 0, 3512 нм, длина одинарной связи С-С (общей у пяти- и шестиугольников) – 0, 1455 нм, длина другой двойной связи С-С (общей у шести угольников) – 0, 1391 нм. Фуллерен С 60
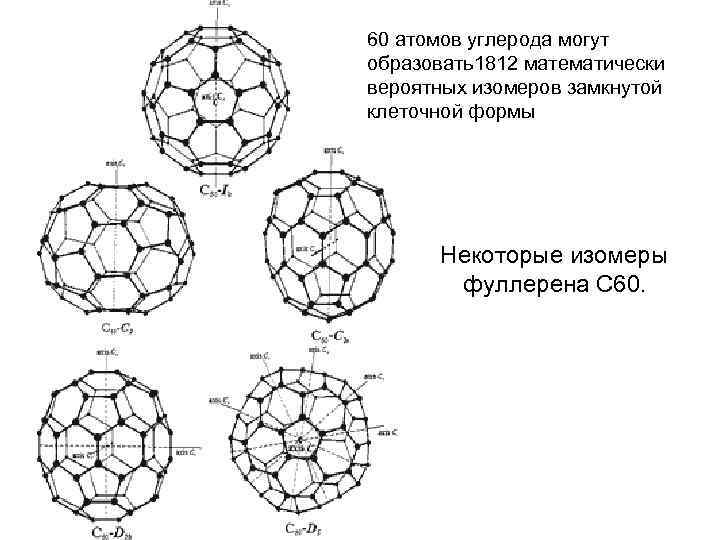
60 атомов углерода могут образовать1812 математически вероятных изомеров замкнутой клеточной формы Некоторые изомеры фуллерена С 60.
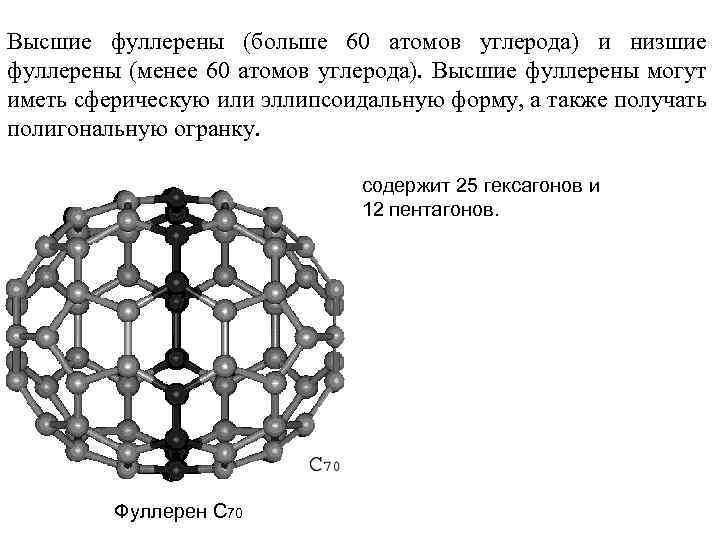
Высшие фуллерены (больше 60 атомов углерода) и низшие фуллерены (менее 60 атомов углерода). Высшие фуллерены могут иметь сферическую или эллипсоидальную форму, а также получать полигональную огранку. содержит 25 гексагонов и 12 пентагонов. Фуллерен С 70
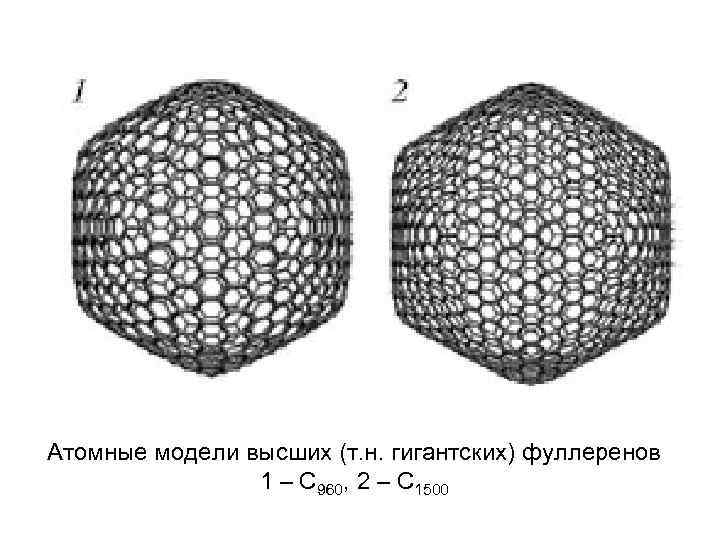
Атомные модели высших (т. н. гигантских) фуллеренов 1 – С 960, 2 – С 1500

Гиперфуллерены или онионы имеют несколько углеродных оболочек, вложенных друг в друга, так называемые луковичные углеродные структуры или онионы, многослойные фуллерены, гиперфуллерены. Могут содержать более 10 концентрических слоев.
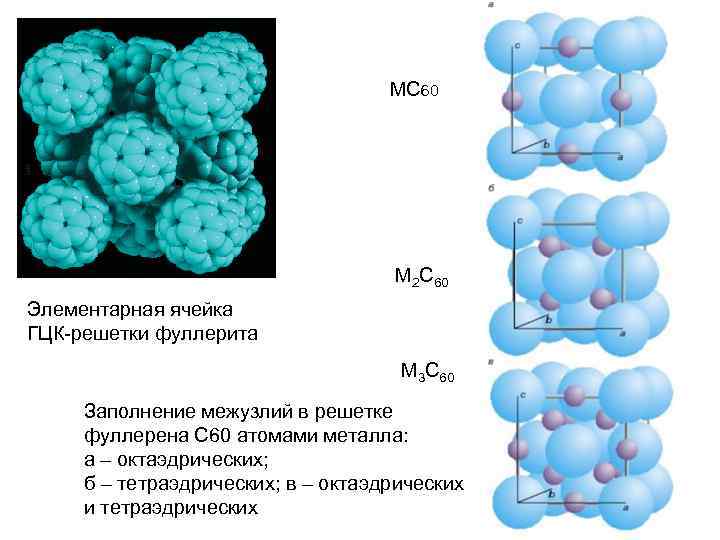
МС 60 М 2 С 60 Элементарная ячейка ГЦК-решетки фуллерита М 3 С 60 Заполнение межузлий в решетке фуллерена С 60 атомами металла: а – октаэдрических; б – тетраэдрических; в – октаэдрических и тетраэдрических
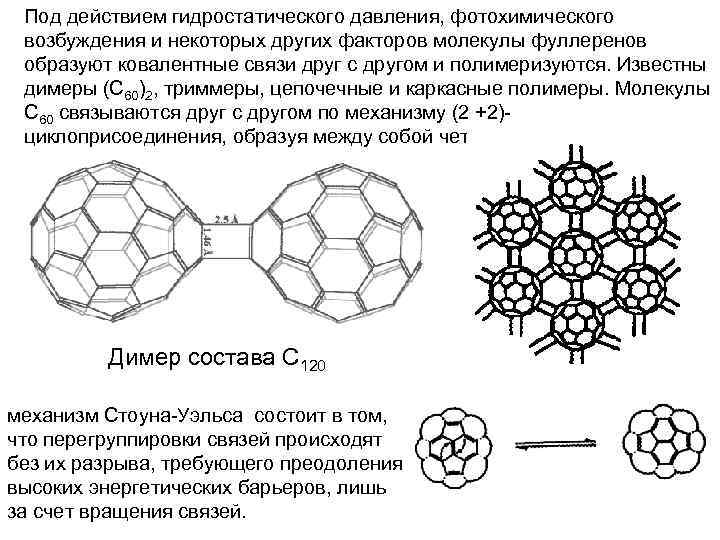
Под действием гидростатического давления, фотохимического возбуждения и некоторых других факторов молекулы фуллеренов образуют ковалентные связи друг с другом и полимеризуются. Известны димеры (С 60)2, триммеры, цепочечные и каркасные полимеры. Молекулы С 60 связываются друг с другом по механизму (2 +2)циклоприсоединения, образуя между собой четырехчленный цикл. Димер состава C 120 механизм Стоуна-Уэльса состоит в том, что перегруппировки связей происходят без их разрыва, требующего преодоления высоких энергетических барьеров, лишь за счет вращения связей.
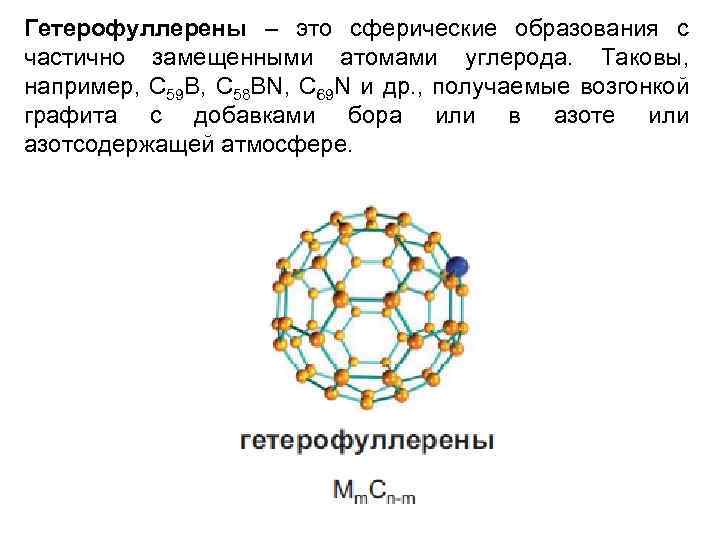
Гетерофуллерены – это сферические образования с частично замещенными атомами углерода. Таковы, например, C 59 B, C 58 BN, C 69 N и др. , получаемые возгонкой графита с добавками бора или в азоте или азотсодержащей атмосфере.
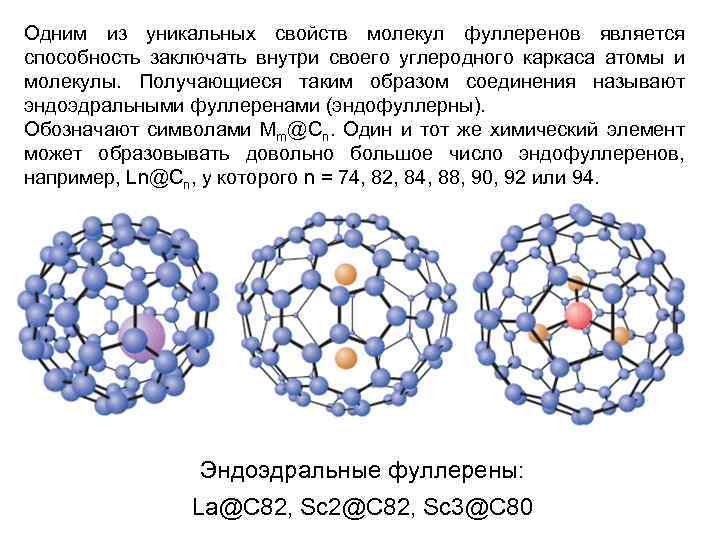
Одним из уникальных свойств молекул фуллеренов является способность заключать внутри своего углеродного каркаса атомы и молекулы. Получающиеся таким образом соединения называют эндоэдральными фуллеренами (эндофуллерны). Обозначают символами Mm@Cn. Один и тот же химический элемент может образовывать довольно большое число эндофуллеренов, например, Ln@Cn, у которого n = 74, 82, 84, 88, 90, 92 или 94. Эндоэдральные фуллерены: La@C 82, Sc 2@C 82, Sc 3@C 80
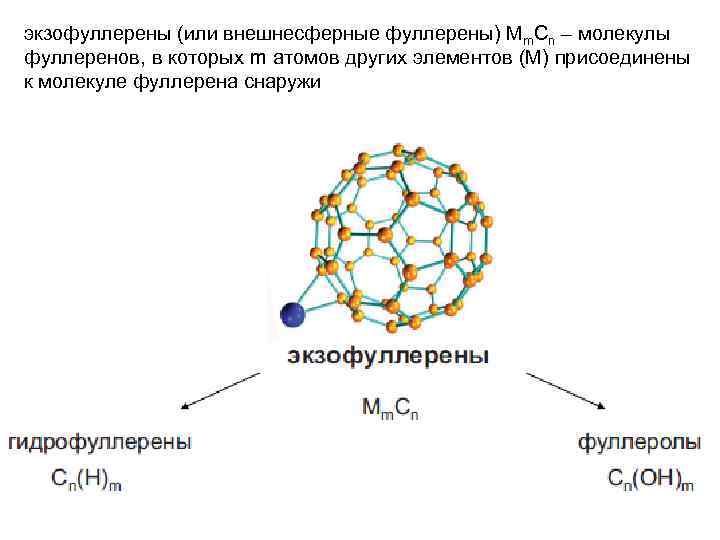
экзофуллерены (или внешнесферные фуллерены) Мm. Cn – молекулы фуллеренов, в которых m атомов других элементов (М) присоединены к молекуле фуллерена снаружи

Методы получение фуллеренов Известны две группы методов получения фуллеренов: возгонка графита с последующей десублимацией и пиролиз углеводородов. При возгонке графита, требующей температур выше 2000 К, используют несколько способов нагревания: • с помощью электрической дуги (дуговой), • резистивное (за счет джоулева тепла), • лучевое (с помощью лазерного излучения, солнечных концентраторов или электронного пучка), • плазменное, • индукционное (токами высокой частоты).
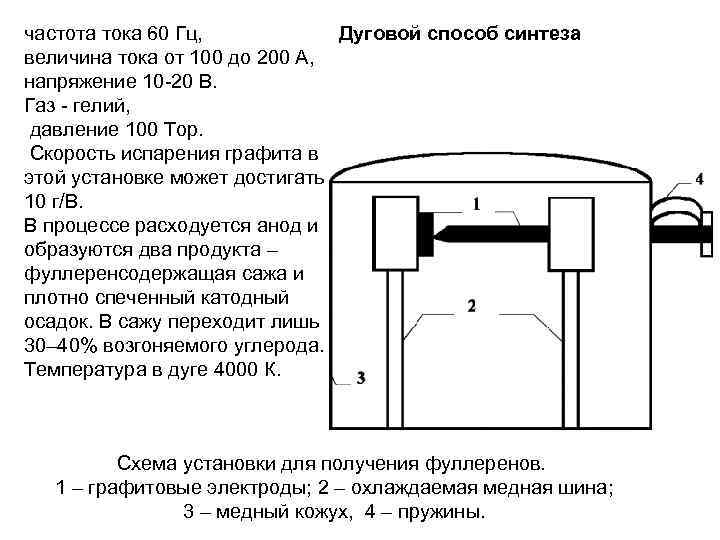
Дуговой способ синтеза частота тока 60 Гц, величина тока от 100 до 200 А, напряжение 10 -20 В. Газ - гелий, давление 100 Тор. Скорость испарения графита в этой установке может достигать 10 г/В. В процессе расходуется анод и образуются два продукта – фуллеренсодержащая сажа и плотно спеченный катодный осадок. В сажу переходит лишь 30– 40% возгоняемого углерода. Температура в дуге 4000 К. Схема установки для получения фуллеренов. 1 – графитовые электроды; 2 – охлаждаемая медная шина; 3 – медный кожух, 4 – пружины.
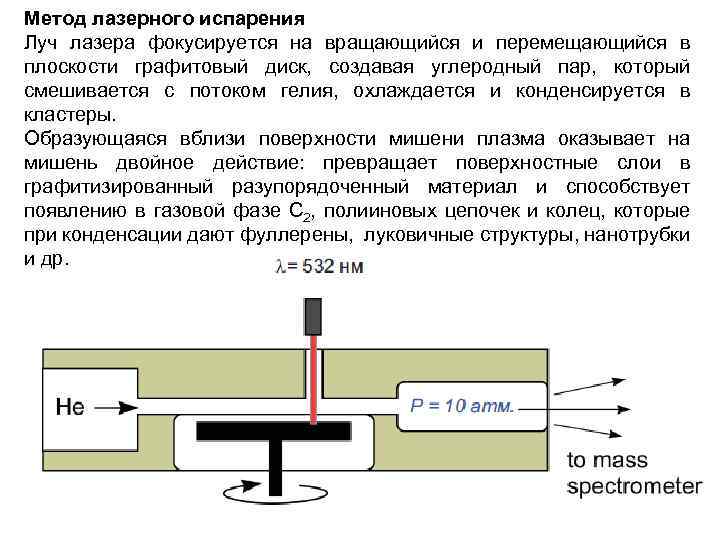
Метод лазерного испарения Луч лазера фокусируется на вращающийся и перемещающийся в плоскости графитовый диск, создавая углеродный пар, который смешивается с потоком гелия, охлаждается и конденсируется в кластеры. Образующаяся вблизи поверхности мишени плазма оказывает на мишень двойное действие: превращает поверхностные слои в графитизированный разупорядоченный материал и способствует появлению в газовой фазе С 2, полииновых цепочек и колец, которые при конденсации дают фуллерены, луковичные структуры, нанотрубки и др.

Пиролиз углеводородов с образованием фуллеренов реализован в двух основных вариантах: • при нагревании углеводородов без окислителей (в частности, с использованием микроволновой плазмы, индуктивно-связанной плазмы или лазерного излучения); • при частичном сжигании углеводородов. Пиролизу подвергают ароматические углеводороды. Недостаток: очень низкий выход фуллеренов от общего количества углерода, используемого для сжигания (около 1%). Повышение выхода сажи возможно при снижении температуры, но тогда понижается концентрация фуллеренов в саже. На выход фуллеренов влияют соотношение углеводорода (горючее) и окислителя, а также общее давление в системе. Выход, кроме того, растет пропорционально скорости газов. Механизм процесса образования сажи определяется встраиванием молекул С 2 в структуры молекул полициклических ароматических углеводородов (ПАУ), а также реакционной коагуляцией самих ПАУ. При образовании фуллеренов дополнительно действует механизм сжатия бензольных колец, приводящий к миграции пятичленных циклов в ароматических молекулах.

Синтез фуллереновых производных возможен двумя способами: • естественным путем – непосредственно при плазменном синтезе; • искусственным путем – при добавлении атомов других элементов к уже синтезированной молекуле. Синтез эндо- и гетерофуллеренов ведется при термическом испарении графита либо методом лазерного испарения. В графитовом электроде (либо в мишени) делают отверстие и заполняют его смесью металлического и графитового порошков, оксидами металлов, либо пропитывают их солями соответствующих элементов и затем отжигают. Внедрение летучего вещества можно осуществить в результате выдерживания фуллеренов в атмосфере этого вещества при повышенных температуре и давлении. Процесс внедрения достигается так же в результате облучения кристалла атомами или ионами элемента-допанта, ускоренными до энергии, при которой возможно проникновение частиц внутрь фуллереновой клетки. Эндоэдральные фуллерены так же можно получить с использованием реакций ядерных превращений.
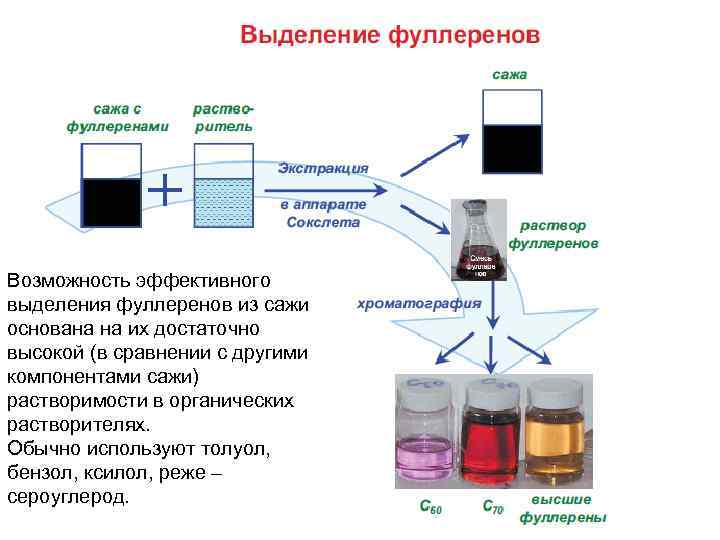
Возможность эффективного выделения фуллеренов из сажи основана на их достаточно высокой (в сравнении с другими компонентами сажи) растворимости в органических растворителях. Обычно используют толуол, бензол, ксилол, реже – сероуглерод.
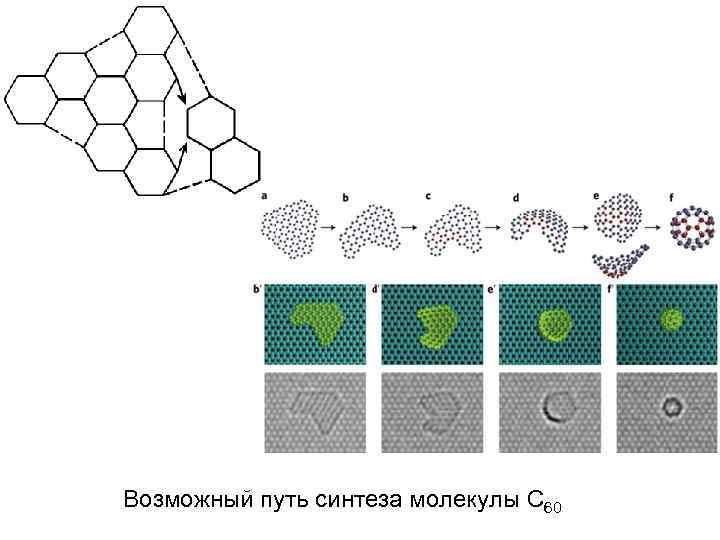
Возможный путь синтеза молекулы С 60
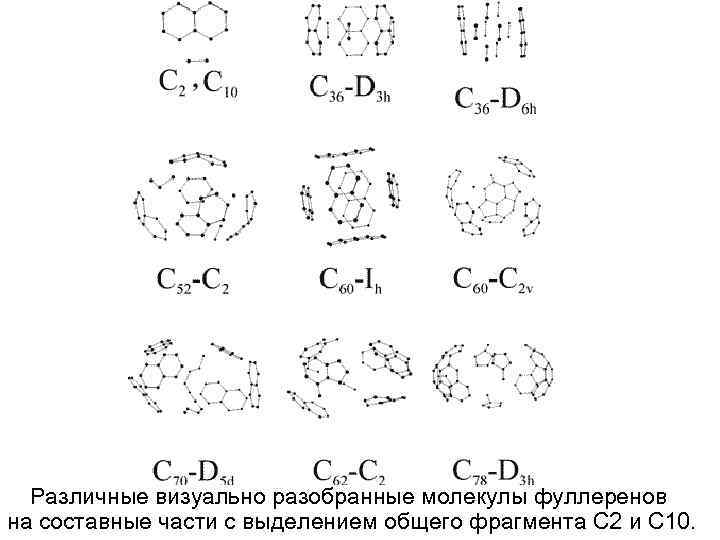
Различные визуально разобранные молекулы фуллеренов на составные части с выделением общего фрагмента С 2 и С 10.
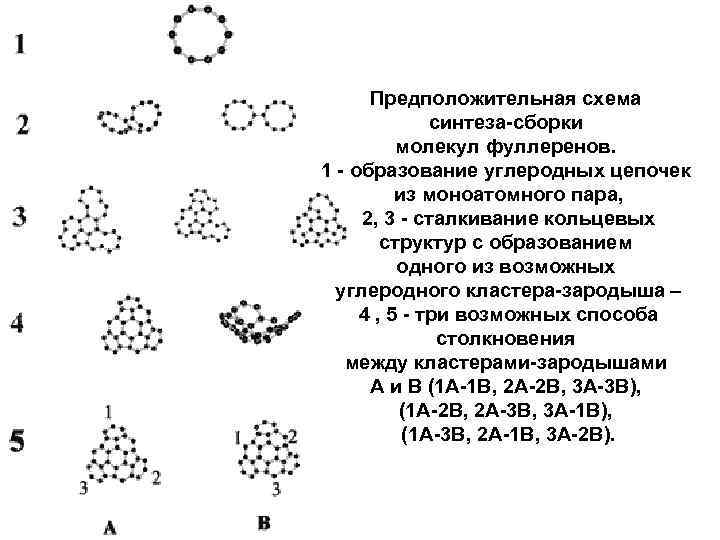
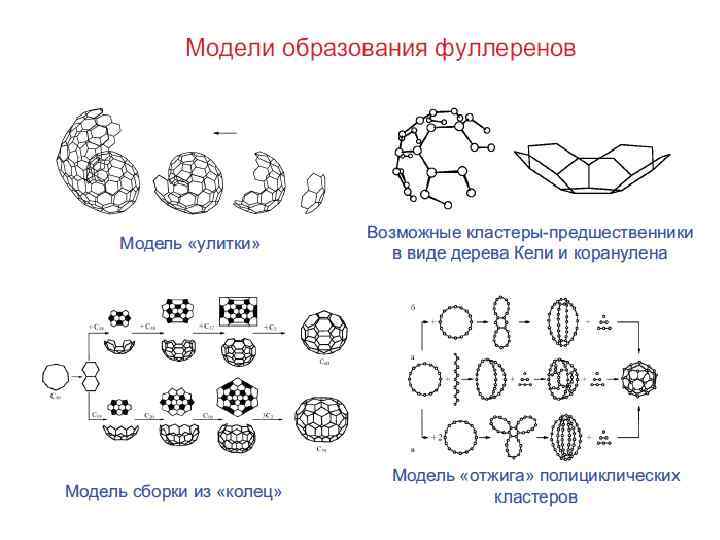
Предположительная схема синтеза-сборки молекул фуллеренов. 1 - образование углеродных цепочек из моноатомного пара, 2, 3 - сталкивание кольцевых структур с образованием одного из возможных углеродного кластера-зародыша – 4 , 5 - три возможных способа столкновения между кластерами-зародышами А и В (1 А-1 В, 2 А-2 В, 3 А-3 В), (1 А-2 В, 2 А-3 В, 3 А-1 В), (1 А-3 В, 2 А-1 В, 3 А-2 В).
Фуллерены и их синтез.ppt