Фотосинтез: что делать, когда все, что можно, уже











03_fotosintez.ppt
- Размер: 14.0 Мб
- Автор: Эля Алиева
- Количество слайдов: 73
Описание презентации Фотосинтез: что делать, когда все, что можно, уже по слайдам
 Фотосинтез: что делать, когда все, что можно, уже окислилось? а/ умереть от отсутствия энергии б/ найти способ «регенерации» восстановленных соединений : СО 2 + Н 2 О → (СН 2 О) + О 2 Для этого необходимо: 1. Найти «псевдонеиссякаемый» источник энергии (вспоминая первую лекцию – безотказного кредитора для безнадежной игры…) 2. Придумать систему трансформации этой энергии в энергию восстановленных соединений. Псевдонеиссякаемый источник энергии на Земле – только энергия звезды по имени Солнце… Таким образом, основные задачи : • поймать энергию солнечных квантов • преобразовать ее в энергию восстановленных соединений.
Фотосинтез: что делать, когда все, что можно, уже окислилось? а/ умереть от отсутствия энергии б/ найти способ «регенерации» восстановленных соединений : СО 2 + Н 2 О → (СН 2 О) + О 2 Для этого необходимо: 1. Найти «псевдонеиссякаемый» источник энергии (вспоминая первую лекцию – безотказного кредитора для безнадежной игры…) 2. Придумать систему трансформации этой энергии в энергию восстановленных соединений. Псевдонеиссякаемый источник энергии на Земле – только энергия звезды по имени Солнце… Таким образом, основные задачи : • поймать энергию солнечных квантов • преобразовать ее в энергию восстановленных соединений.
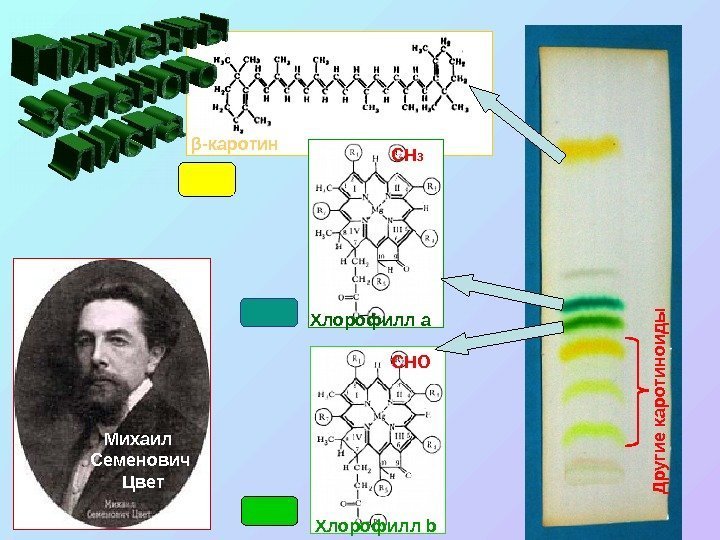
 β — каротин Михаил Семенович Цвет СНО Хлорофилл b. СН 3 Хлорофилл a. Д р уги е ка р о ти н о и д ы
β — каротин Михаил Семенович Цвет СНО Хлорофилл b. СН 3 Хлорофилл a. Д р уги е ка р о ти н о и д ы
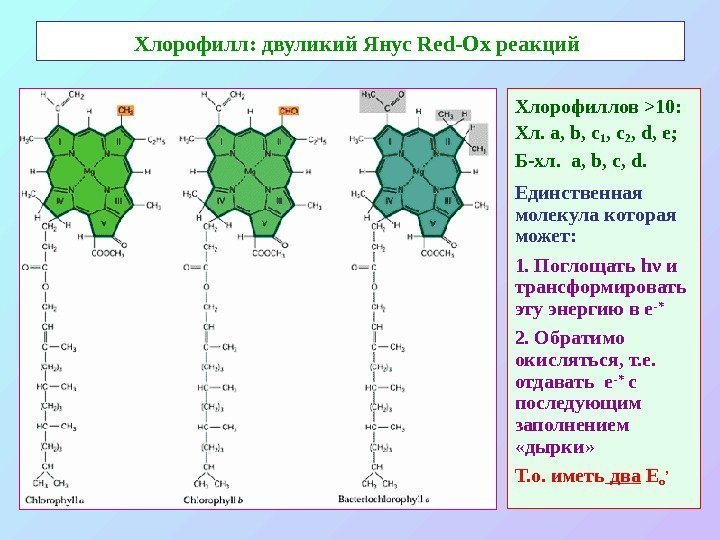
 Хлорофилл: двуликий Янус Red-Ox реакций Хлорофиллов > 10: Хл. а, b, c 1 , с 2 , d, e ; Б-хл. a, b, c, d. Единственная молекула которая может: 1. Поглощать h ν и трансформировать эту энергию в е-* 2. Обратимо окисляться, т. е. отдавать е -* с последующим заполнением «дырки» Т. о. иметь два Е o ’
Хлорофилл: двуликий Янус Red-Ox реакций Хлорофиллов > 10: Хл. а, b, c 1 , с 2 , d, e ; Б-хл. a, b, c, d. Единственная молекула которая может: 1. Поглощать h ν и трансформировать эту энергию в е-* 2. Обратимо окисляться, т. е. отдавать е -* с последующим заполнением «дырки» Т. о. иметь два Е o ’
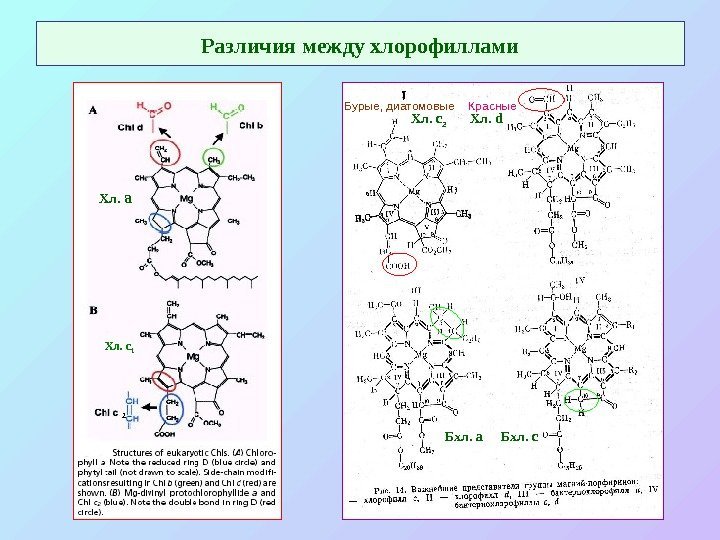
 Различия между хлорофиллами Хл. а Хл. с 2 Хл. d Бхл. а Бхл. с. Хл. с 1 2 Бурые, диатомовые Красные
Различия между хлорофиллами Хл. а Хл. с 2 Хл. d Бхл. а Бхл. с. Хл. с 1 2 Бурые, диатомовые Красные
 Основные структурные особенности молекулы хлорофилла • Конъюгированная система двойных связей: основная 18 -членная π — система + дополнителные в I, II, V кольцах. • Mg – минимум электроотрицательности; изменяет симметрию молекулы хлорофилла; «активирует» электроны пиррольных азотов • V -кольцо – «форбиновая структура» : две важных группы: карбонильная при С 9 (участвует в n – π переходах) и кетоэфирная при С 10 – транс- (хл-л а) или цис- (хл-л а ’ ). • Гидрофобный «хвост» (обычно С 20 – фитол). Структурная роль.
Основные структурные особенности молекулы хлорофилла • Конъюгированная система двойных связей: основная 18 -членная π — система + дополнителные в I, II, V кольцах. • Mg – минимум электроотрицательности; изменяет симметрию молекулы хлорофилла; «активирует» электроны пиррольных азотов • V -кольцо – «форбиновая структура» : две важных группы: карбонильная при С 9 (участвует в n – π переходах) и кетоэфирная при С 10 – транс- (хл-л а) или цис- (хл-л а ’ ). • Гидрофобный «хвост» (обычно С 20 – фитол). Структурная роль.
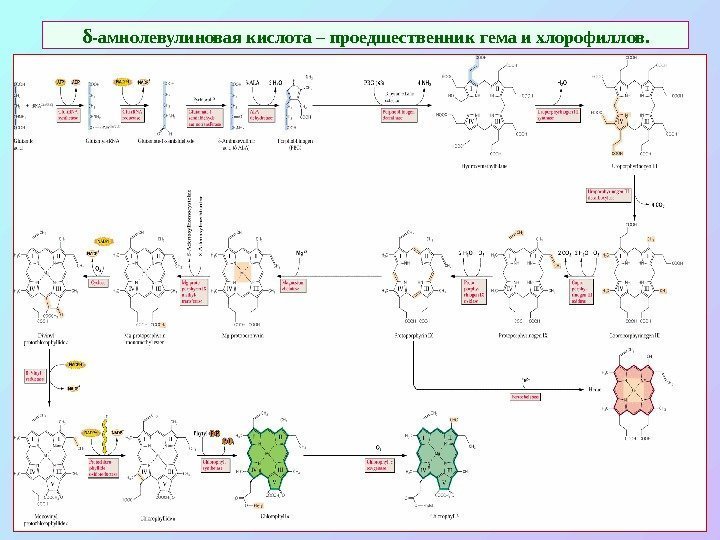
 δ -амнолевулиновая кислота – проедшественник гема и хлорофиллов.
δ -амнолевулиновая кислота – проедшественник гема и хлорофиллов.
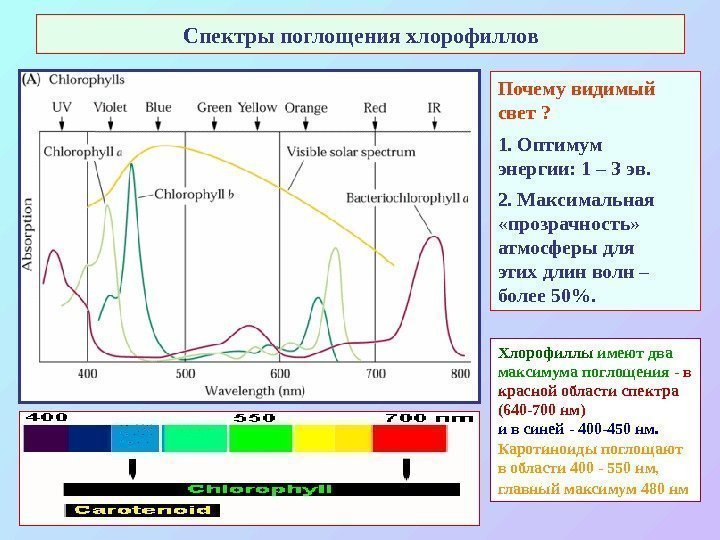
 Спектры поглощения хлорофиллов Почему видимый свет ? 1. Оптимум энергии: 1 – 3 эв. 2. Максимальная «прозрачность» атмосферы для этих длин волн – более 50%. Хлорофиллы имеют два максимума поглощения — в красной области спектра (640 -700 нм) и в синей — 400 -450 нм. Каротиноиды поглощают в области 400 — 50 нм, главный максимум 480 нм
Спектры поглощения хлорофиллов Почему видимый свет ? 1. Оптимум энергии: 1 – 3 эв. 2. Максимальная «прозрачность» атмосферы для этих длин волн – более 50%. Хлорофиллы имеют два максимума поглощения — в красной области спектра (640 -700 нм) и в синей — 400 -450 нм. Каротиноиды поглощают в области 400 — 50 нм, главный максимум 480 нм
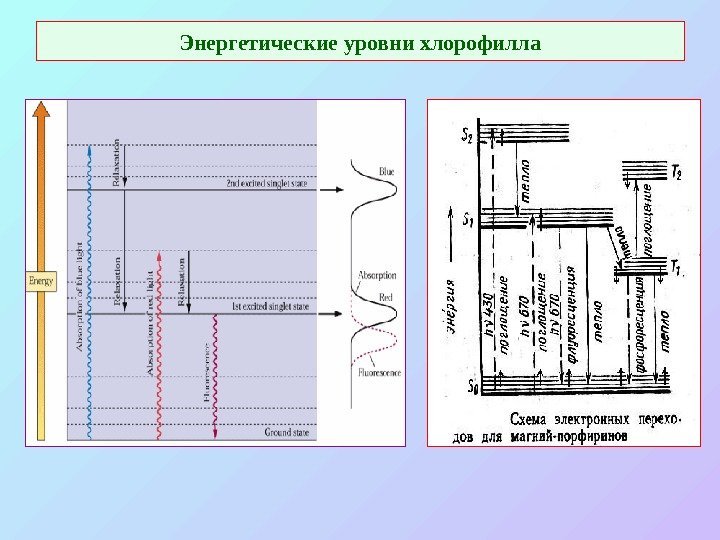
 Энергетические уровни хлорофилла
Энергетические уровни хлорофилла
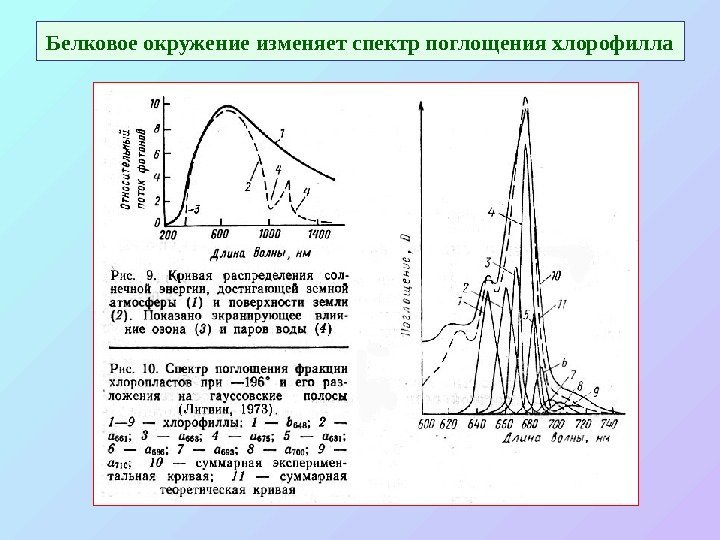
 Белковое окружение изменяет спектр поглощения хлорофилла
Белковое окружение изменяет спектр поглощения хлорофилла
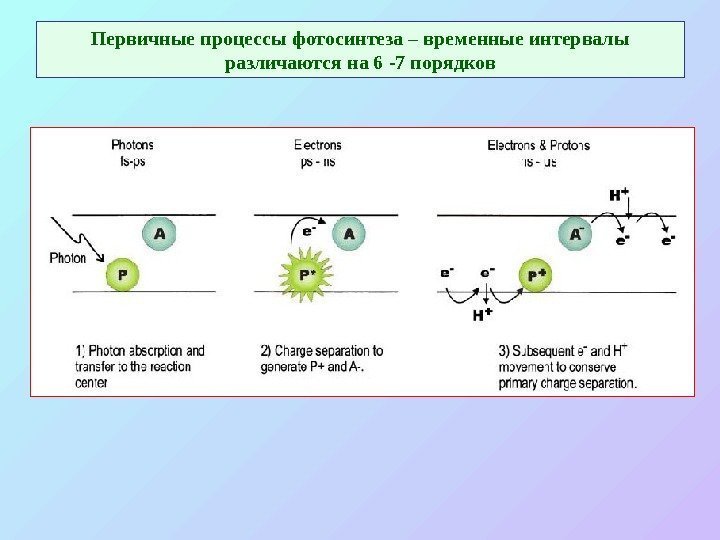
 Первичные процессы фотосинтеза – временные интервалы различаются на 6 -7 порядков
Первичные процессы фотосинтеза – временные интервалы различаются на 6 -7 порядков
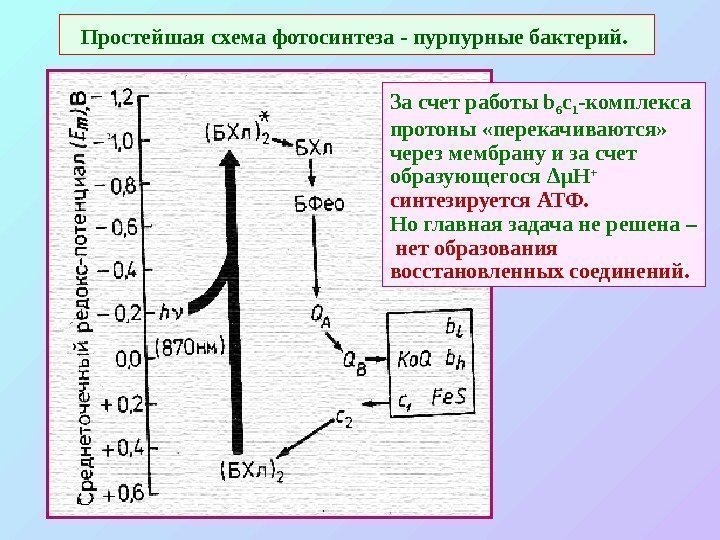
 Простейшая схема фотосинтеза — пурпурные бактерий. За счет работы b 6 c 1 -комплекса протоны «перекачиваются» через мембрану и за счет образующегося Δ µ Н + синтезируется АТФ. Но главная задача не решена – нет образования восстановленных соединений.
Простейшая схема фотосинтеза — пурпурные бактерий. За счет работы b 6 c 1 -комплекса протоны «перекачиваются» через мембрану и за счет образующегося Δ µ Н + синтезируется АТФ. Но главная задача не решена – нет образования восстановленных соединений.
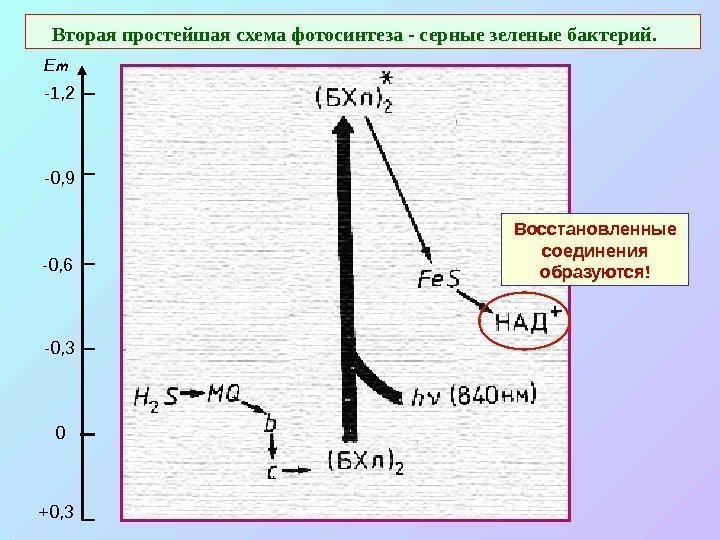
 Вторая простейшая схема фотосинтеза — серные зеленые бактерий. Восстановленные соединения образуются! +0, 3 0 -0, 3 -0, 6 -0, 9 -1, 2 E m
Вторая простейшая схема фотосинтеза — серные зеленые бактерий. Восстановленные соединения образуются! +0, 3 0 -0, 3 -0, 6 -0, 9 -1, 2 E m
 Основные требования к донору электронов: 1. Ео’ меньше Ео’ хл+ (т. е. может отдавать е- на хл+ ) 2. Продукты окисления нетоксичны (желательно) 3. Его должно быть много Н 2 S – хорош по всем параметрам, кроме последнего: 1. Е о’ н 2 S = — 0, 23 – электрон достаточно легко «забрать» 2. Продукт окисления (сера) — легко уводится из реакции Н 2 О – отвратителен по всем параметрам, кроме последнего: 1. Е о’ н 2 о = +0, 82 – очень много, электрон «оторвать» трудно 2. Продукт окисления (кислород) — очень токсичен. Но последний фактор оказался решающим. Очередная проблема: где взять источник (донор) электронов (окисляемое соединение)?
Основные требования к донору электронов: 1. Ео’ меньше Ео’ хл+ (т. е. может отдавать е- на хл+ ) 2. Продукты окисления нетоксичны (желательно) 3. Его должно быть много Н 2 S – хорош по всем параметрам, кроме последнего: 1. Е о’ н 2 S = — 0, 23 – электрон достаточно легко «забрать» 2. Продукт окисления (сера) — легко уводится из реакции Н 2 О – отвратителен по всем параметрам, кроме последнего: 1. Е о’ н 2 о = +0, 82 – очень много, электрон «оторвать» трудно 2. Продукт окисления (кислород) — очень токсичен. Но последний фактор оказался решающим. Очередная проблема: где взять источник (донор) электронов (окисляемое соединение)?
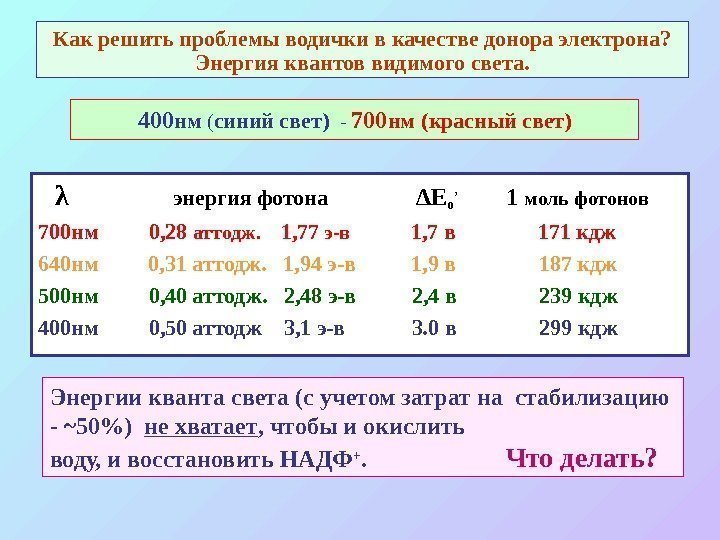
 Как решить проблемы водички в качестве донора электрона? Энергия квантов видимого света. 400 нм ( синий свет) — 700 нм (красный свет) λ энергия фотона Δ Ео’ 1 моль фотонов 700 нм 0, 28 аттодж. 1 , 77 э-в 1 , 7 в 171 кдж 640 нм 0, 31 аттодж. 1, 94 э-в 1, 9 в 187 кдж 500 нм 0, 40 аттодж. 2, 48 э-в 2, 4 в 239 кдж 400 нм 0, 50 аттодж 3, 1 э-в 3. 0 в 299 кдж Энергии кванта света (с учетом затрат на стабилизацию — ~ 50%) не хватает , чтобы и окислить воду, и восстановить НАДФ +. Что делать?
Как решить проблемы водички в качестве донора электрона? Энергия квантов видимого света. 400 нм ( синий свет) — 700 нм (красный свет) λ энергия фотона Δ Ео’ 1 моль фотонов 700 нм 0, 28 аттодж. 1 , 77 э-в 1 , 7 в 171 кдж 640 нм 0, 31 аттодж. 1, 94 э-в 1, 9 в 187 кдж 500 нм 0, 40 аттодж. 2, 48 э-в 2, 4 в 239 кдж 400 нм 0, 50 аттодж 3, 1 э-в 3. 0 в 299 кдж Энергии кванта света (с учетом затрат на стабилизацию — ~ 50%) не хватает , чтобы и окислить воду, и восстановить НАДФ +. Что делать?
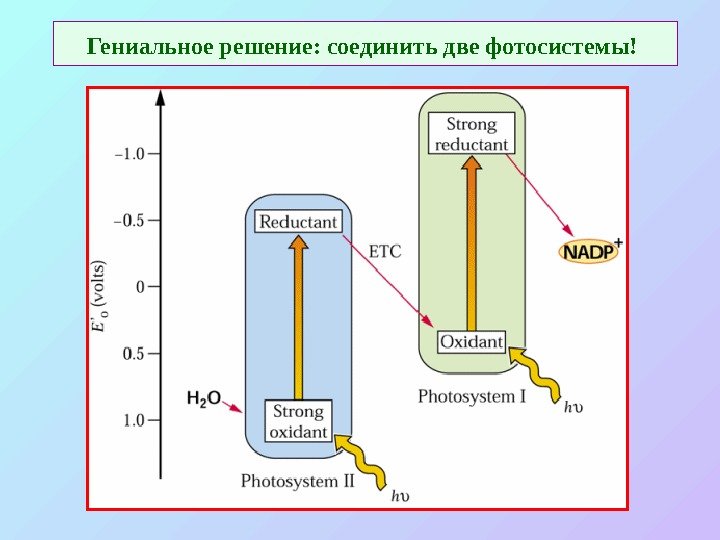
 Гениальное решение: соединить две фотосистемы!
Гениальное решение: соединить две фотосистемы!
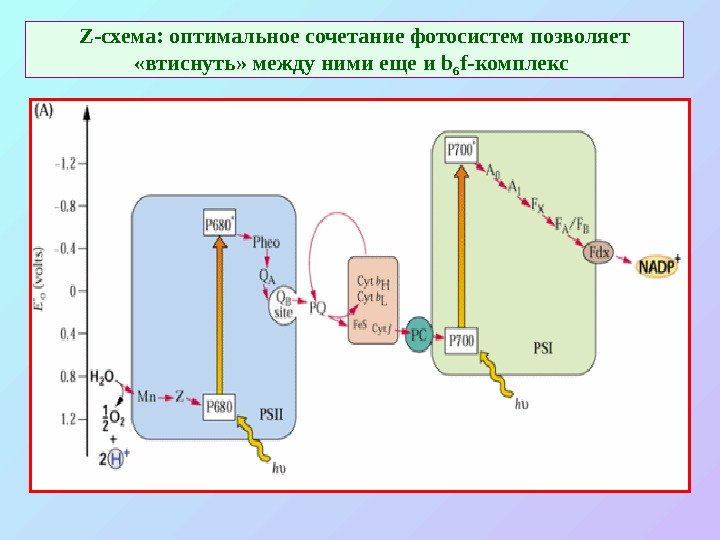
 Z -схема: оптимальное сочетание фотосистем позволяет «втиснуть» между ними еще и b 6 f- комплекс
Z -схема: оптимальное сочетание фотосистем позволяет «втиснуть» между ними еще и b 6 f- комплекс
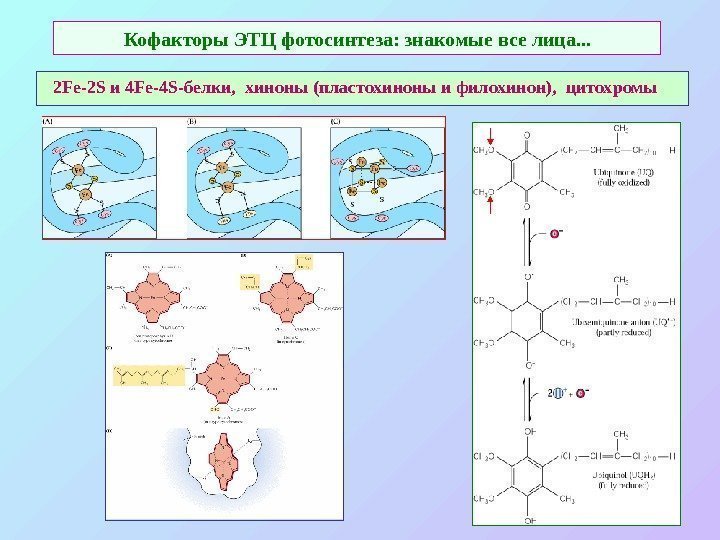
 Кофакторы ЭТЦ фотосинтеза: знакомые все лица. . . 2 Fe-2 S и 4 Fe-4 S -белки, хиноны (пластохиноны и филохинон), цитохромы
Кофакторы ЭТЦ фотосинтеза: знакомые все лица. . . 2 Fe-2 S и 4 Fe-4 S -белки, хиноны (пластохиноны и филохинон), цитохромы
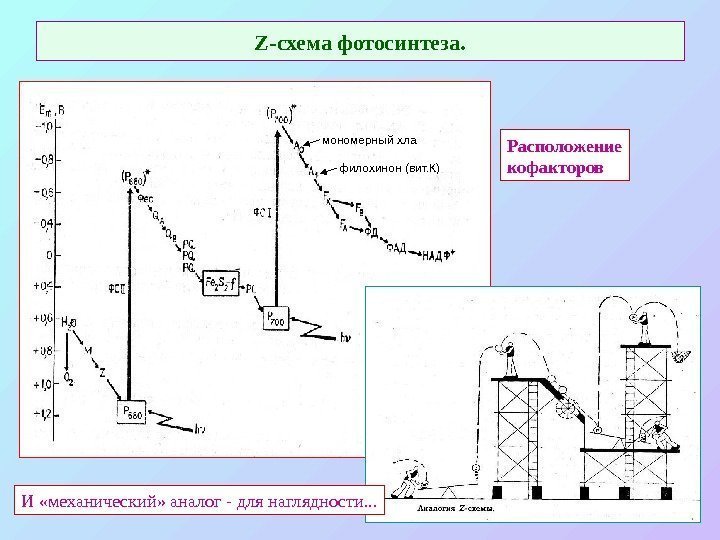
 Z- схема фотосинтеза. Расположение кофакторов И «механический» аналог — для наглядности. . . мономерный хла филохинон (вит. К)
Z- схема фотосинтеза. Расположение кофакторов И «механический» аналог — для наглядности. . . мономерный хла филохинон (вит. К)
 Red-Ox потенциалы компонентов ЭТЦ хлоропластов ФС II P 680 * — 0. 7 Pheo — 0. 6 Q A — 0. 1 Q B ~ 0 cytb 559 L + 0. 08 cytb 559 H + 0. 38 H 2 O/O 2 + 0. 82 P 680 +1. 12 ФС I P 700 * ~ 1. 2 A 0 (P 695 ) — 1. 1 0 A 1 ( вит К ) — 0. 88 F x — 0. 73 F A — 0. 59 F B — 0. 5 P 700 + 0. 52 Cyt b/f Cyt b. L — 0. 15 Cyt b. H — 0. 05 Fe. S Риске + 0. 30 Cyt f + 0. 34 PQ ~ 0 Fd — 0. 42 FMN — 0. 36 NADPH — 0. 32 PC +0.
Red-Ox потенциалы компонентов ЭТЦ хлоропластов ФС II P 680 * — 0. 7 Pheo — 0. 6 Q A — 0. 1 Q B ~ 0 cytb 559 L + 0. 08 cytb 559 H + 0. 38 H 2 O/O 2 + 0. 82 P 680 +1. 12 ФС I P 700 * ~ 1. 2 A 0 (P 695 ) — 1. 1 0 A 1 ( вит К ) — 0. 88 F x — 0. 73 F A — 0. 59 F B — 0. 5 P 700 + 0. 52 Cyt b/f Cyt b. L — 0. 15 Cyt b. H — 0. 05 Fe. S Риске + 0. 30 Cyt f + 0. 34 PQ ~ 0 Fd — 0. 42 FMN — 0. 36 NADPH — 0. 32 PC +0.
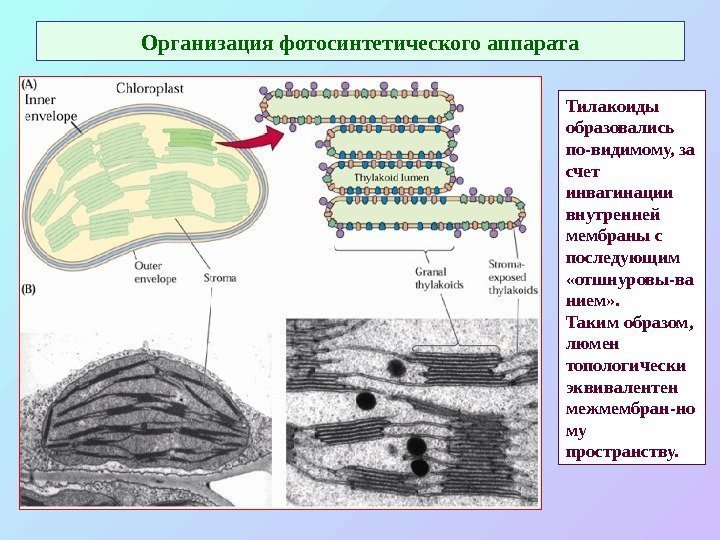
 Организация фотосинтетического аппарата Тилакоиды образовались по-видимому, за счет инвагинации внутренней мембраны с последующим «отшнуровы-ва нием» . Таким образом, люмен топологически эквивалентен межмембран-но му пространству.
Организация фотосинтетического аппарата Тилакоиды образовались по-видимому, за счет инвагинации внутренней мембраны с последующим «отшнуровы-ва нием» . Таким образом, люмен топологически эквивалентен межмембран-но му пространству.
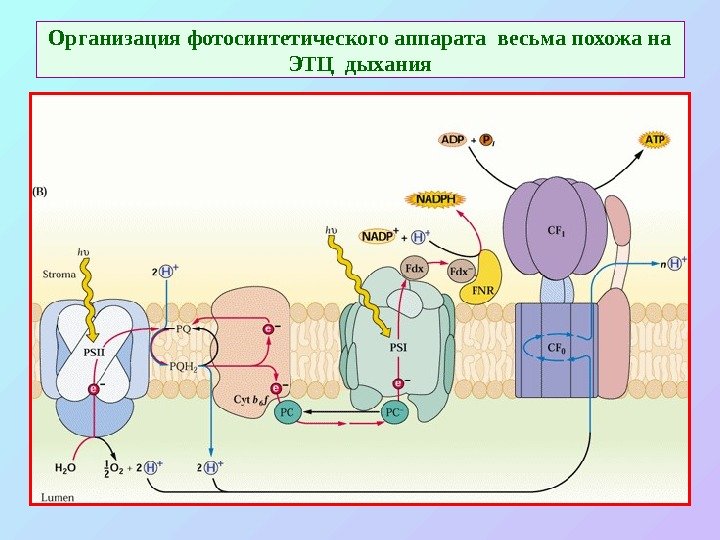
 Организация фотосинтетического аппарата весьма похожа на ЭТЦ дыхания
Организация фотосинтетического аппарата весьма похожа на ЭТЦ дыхания
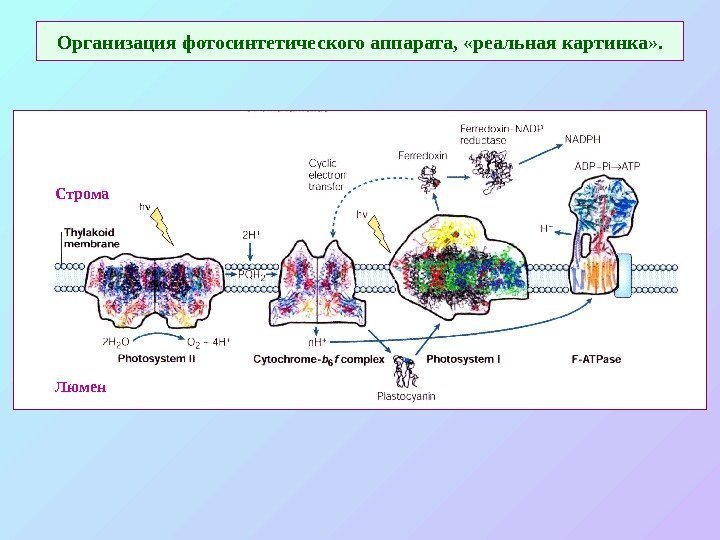
 Организация фотосинтетического аппарата, «реальная картинка» . Строма Люмен
Организация фотосинтетического аппарата, «реальная картинка» . Строма Люмен
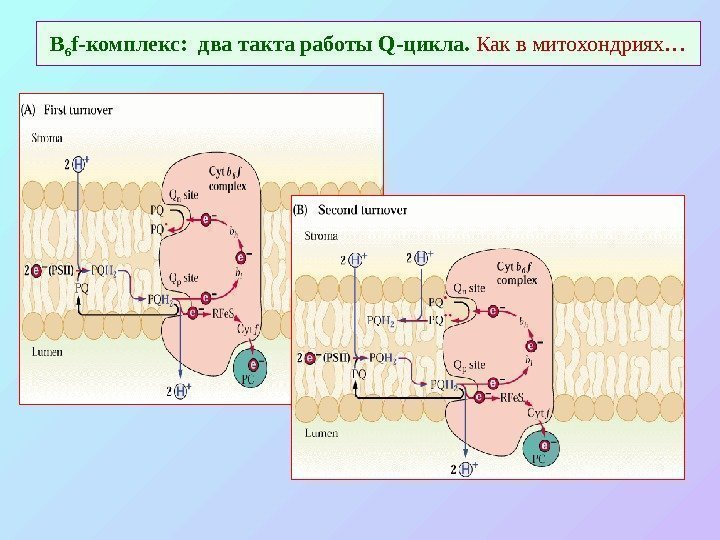
 В 6 f- комплекс: два такта работы Q -цикла. Как в митохондриях…
В 6 f- комплекс: два такта работы Q -цикла. Как в митохондриях…
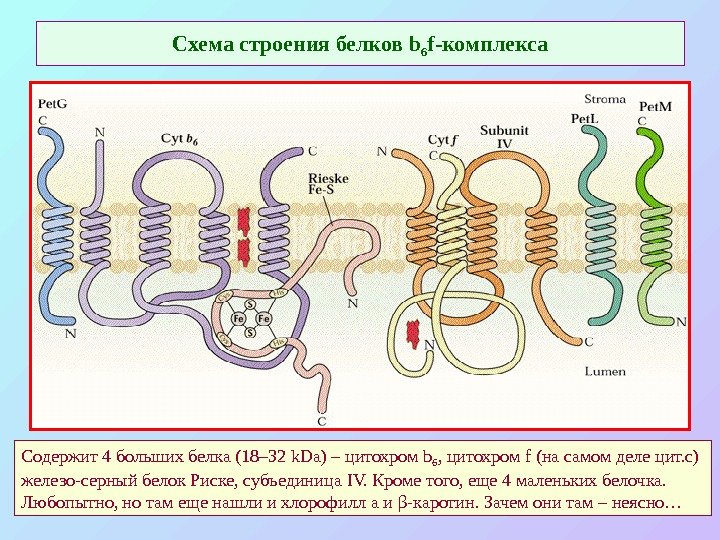
 Схема строения белков b 6 f -комплекса Содержит 4 больших белка (18– 32 k. Da) – цитохром b 6 , цитохром f (на самом деле цит. с) железо-серный белок Риске, субъединица IV. Кроме того, еще 4 маленьких белочка. Любопытно, но там еще нашли и хлорофилл а и β — каротин. Зачем они там – неясно…
Схема строения белков b 6 f -комплекса Содержит 4 больших белка (18– 32 k. Da) – цитохром b 6 , цитохром f (на самом деле цит. с) железо-серный белок Риске, субъединица IV. Кроме того, еще 4 маленьких белочка. Любопытно, но там еще нашли и хлорофилл а и β — каротин. Зачем они там – неясно…
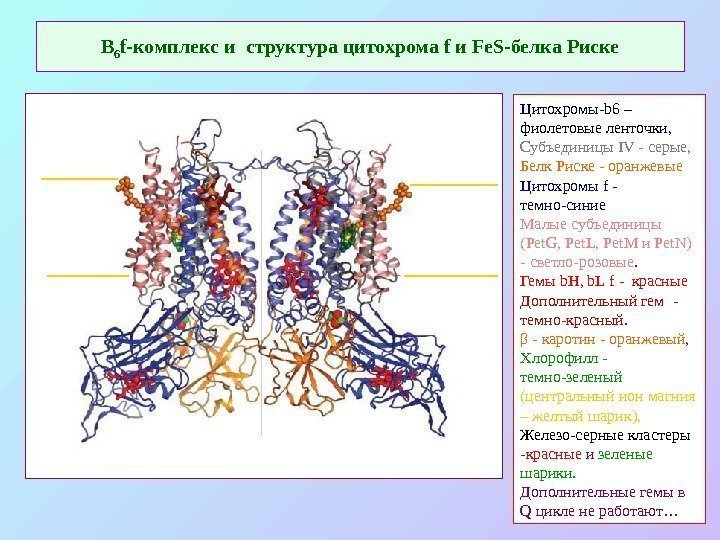
 В 6 f -комплекс и структура цитохрома f и Fe. S -белка Риске Цитохромы-b 6 – фиолетовые ленточки, Субъединицы IV — серые, Белк Риске — оранжевые Цитохромы f — темно-синие Малые субъединицы ( Pet. G , Pet. L , Pet. M и Pet. N ) — светло-розовые. Гемы b. H , b. L f — красные Дополнительный гем — темно-красный. β — каротин — оранжевый , Хлорофилл — темно-зеленый (центральный ион магния – желтый шарик), Железо-серные кластеры — красные и зеленые шарики. Дополнительные гемы в Q цикле не работают…
В 6 f -комплекс и структура цитохрома f и Fe. S -белка Риске Цитохромы-b 6 – фиолетовые ленточки, Субъединицы IV — серые, Белк Риске — оранжевые Цитохромы f — темно-синие Малые субъединицы ( Pet. G , Pet. L , Pet. M и Pet. N ) — светло-розовые. Гемы b. H , b. L f — красные Дополнительный гем — темно-красный. β — каротин — оранжевый , Хлорофилл — темно-зеленый (центральный ион магния – желтый шарик), Железо-серные кластеры — красные и зеленые шарики. Дополнительные гемы в Q цикле не работают…
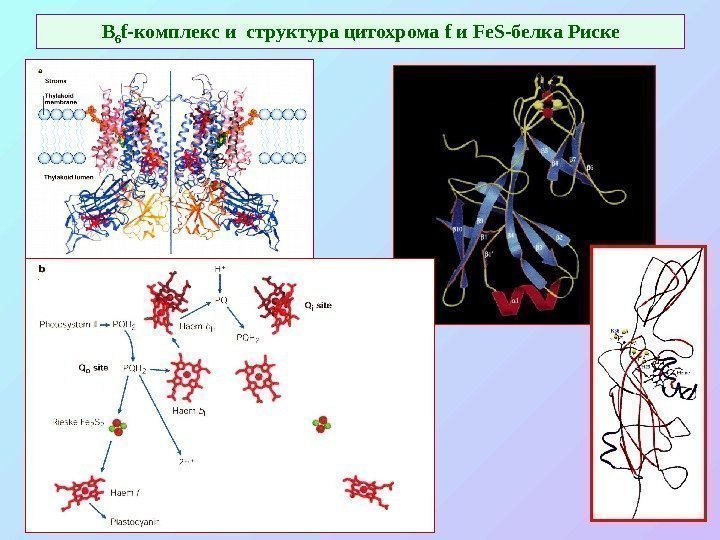
 В 6 f -комплекс и структура цитохрома f и Fe. S -белка Риске
В 6 f -комплекс и структура цитохрома f и Fe. S -белка Риске
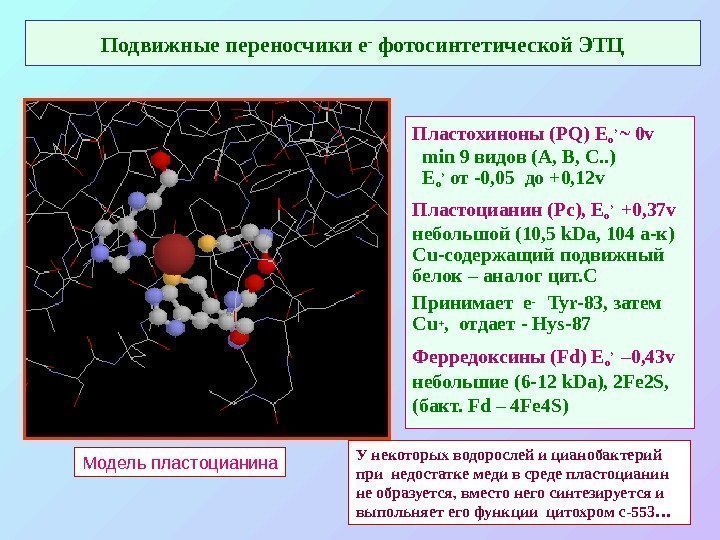
 Подвижные переносчики е — фотосинтетической ЭТЦ Пластохиноны ( PQ) E o ’ ~ 0 v min 9 видов (А, В, С. . ) E o ’ от -0, 05 до +0, 12 v Пластоцианин ( Pc), E o ’ +0, 37 v небольшой (10, 5 k. Da, 104 а-к) Cu -содержащий подвижный белок – аналог цит. С Принимает е — Tyr-83, затем Cu + , отдает — Hys-87 Ферредоксины ( Fd) E o ’ – 0, 43 v небольшие (6 -12 k. Da), 2 Fe 2 S, ( бакт. Fd – 4 Fe 4 S) Модель пластоцианина У некоторых водорослей и цианобактерий при недостатке меди в среде пластоцианин не образуется, вместо него синтезируется и выпольняет его функции цитохром с-553…
Подвижные переносчики е — фотосинтетической ЭТЦ Пластохиноны ( PQ) E o ’ ~ 0 v min 9 видов (А, В, С. . ) E o ’ от -0, 05 до +0, 12 v Пластоцианин ( Pc), E o ’ +0, 37 v небольшой (10, 5 k. Da, 104 а-к) Cu -содержащий подвижный белок – аналог цит. С Принимает е — Tyr-83, затем Cu + , отдает — Hys-87 Ферредоксины ( Fd) E o ’ – 0, 43 v небольшие (6 -12 k. Da), 2 Fe 2 S, ( бакт. Fd – 4 Fe 4 S) Модель пластоцианина У некоторых водорослей и цианобактерий при недостатке меди в среде пластоцианин не образуется, вместо него синтезируется и выпольняет его функции цитохром с-553…
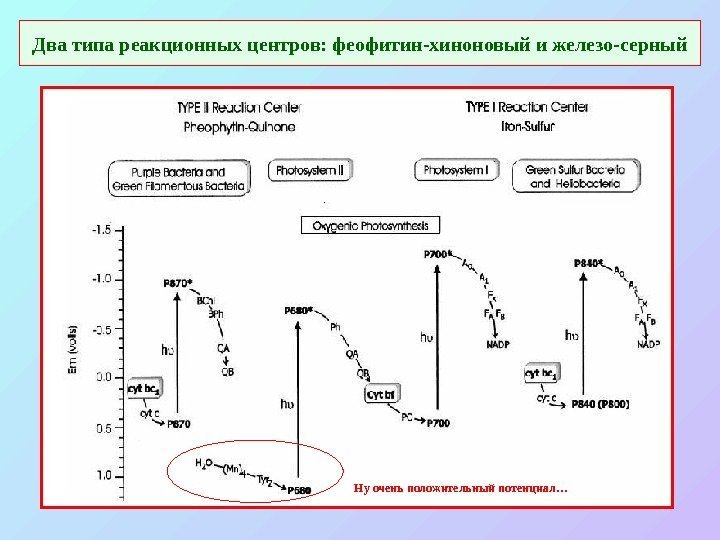
 Два типа реакционных центров: феофитин-хиноновый и железо-серный Ну очень положительный потенциал…
Два типа реакционных центров: феофитин-хиноновый и железо-серный Ну очень положительный потенциал…
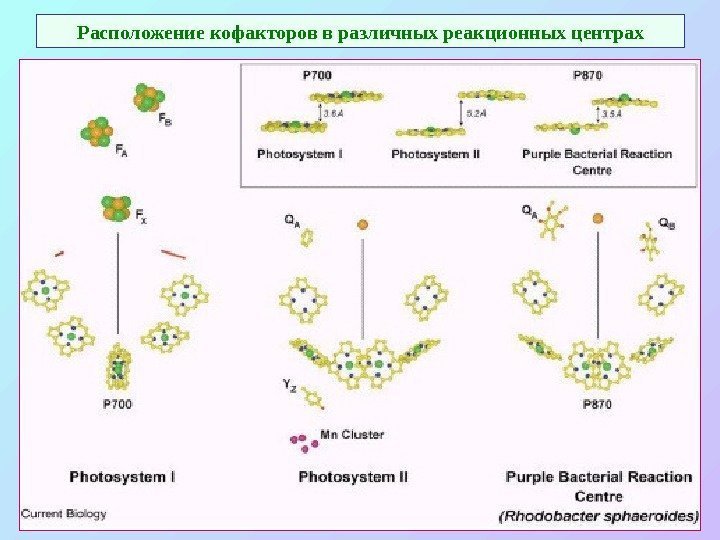
 Расположение кофакторов в различных реакционных центрах
Расположение кофакторов в различных реакционных центрах
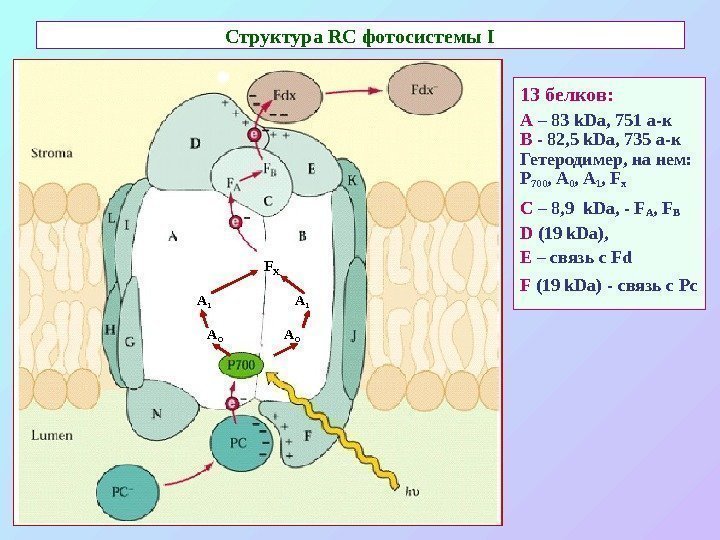
 Структура RC фотосистемы I 13 белков: А – 83 k. Da, 751 a- к В — 82, 5 k. Da , 7 35 a- к Гетеродимер, на нем: Р 700 , А 1 , Fx С – 8, 9 k. Da, — F A , FB D (19 k. Da), E – связь с Fd F (19 k. Da) — связь с Pc A O A OA 1 A 1 F X
Структура RC фотосистемы I 13 белков: А – 83 k. Da, 751 a- к В — 82, 5 k. Da , 7 35 a- к Гетеродимер, на нем: Р 700 , А 1 , Fx С – 8, 9 k. Da, — F A , FB D (19 k. Da), E – связь с Fd F (19 k. Da) — связь с Pc A O A OA 1 A 1 F X
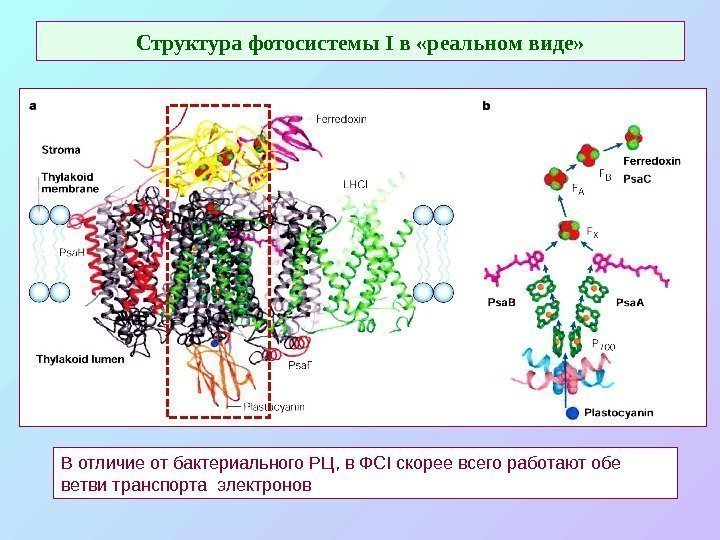
 Структура фотосистемы I в «реальном виде» В отличие от бактериального РЦ, в ФС I скорее всего работают обе ветви транспорта электронов
Структура фотосистемы I в «реальном виде» В отличие от бактериального РЦ, в ФС I скорее всего работают обе ветви транспорта электронов
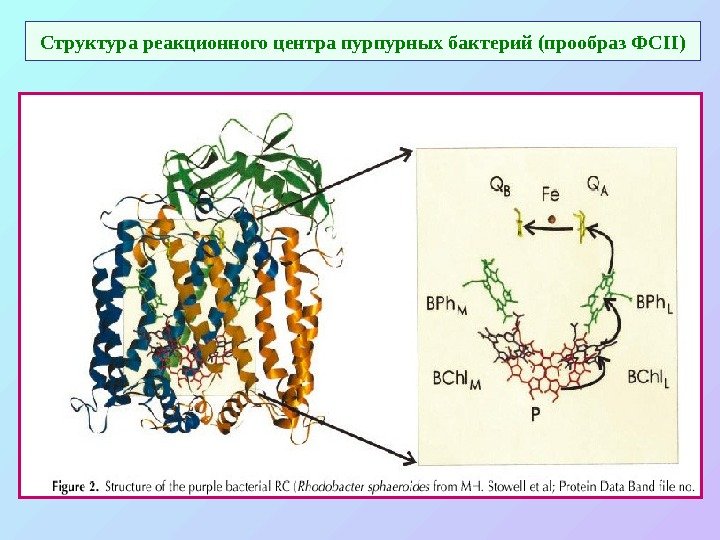
 Структура реакционного центра пурпурных бактерий (прообраз ФС II)
Структура реакционного центра пурпурных бактерий (прообраз ФС II)
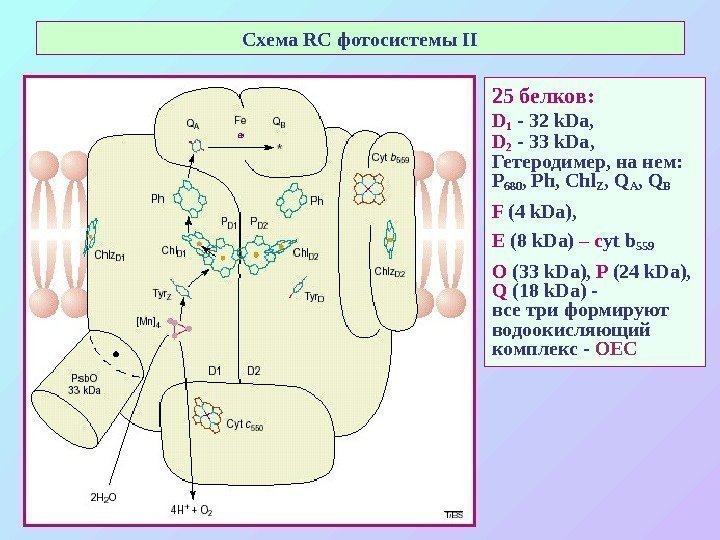
 Схема RC фотосистемы II 25 белков: D 1 — 3 2 k. Da, D 2 — 33 k. Da , Гетеродимер, на нем: Р 680 , Ph , Chl Z , Q A , Q B F (4 k. Da) , E (8 k. Da) – с yt b 559 O (3 3 k. Da), P (24 k. Da), Q (18 k. Da) — все три формируют водоокисляющий комплекс — O
Схема RC фотосистемы II 25 белков: D 1 — 3 2 k. Da, D 2 — 33 k. Da , Гетеродимер, на нем: Р 680 , Ph , Chl Z , Q A , Q B F (4 k. Da) , E (8 k. Da) – с yt b 559 O (3 3 k. Da), P (24 k. Da), Q (18 k. Da) — все три формируют водоокисляющий комплекс — O
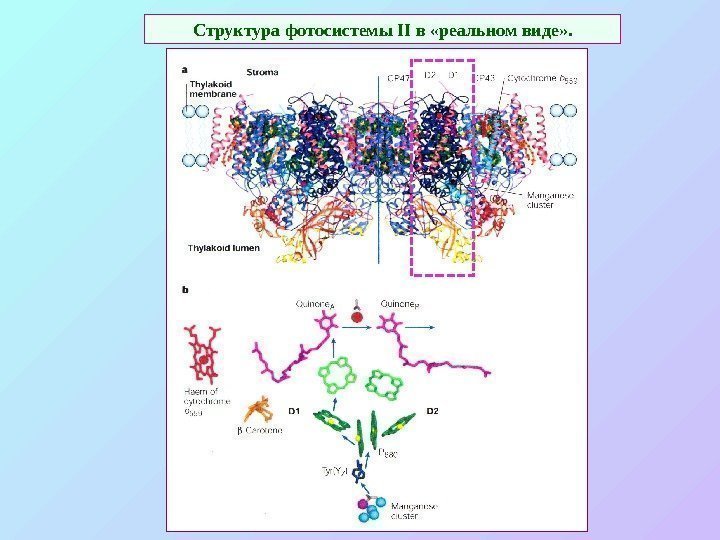
 Структура фотосистемы II в «реальном виде» .
Структура фотосистемы II в «реальном виде» .
 Структура белка D 1 RC фотосистемы II
Структура белка D 1 RC фотосистемы II
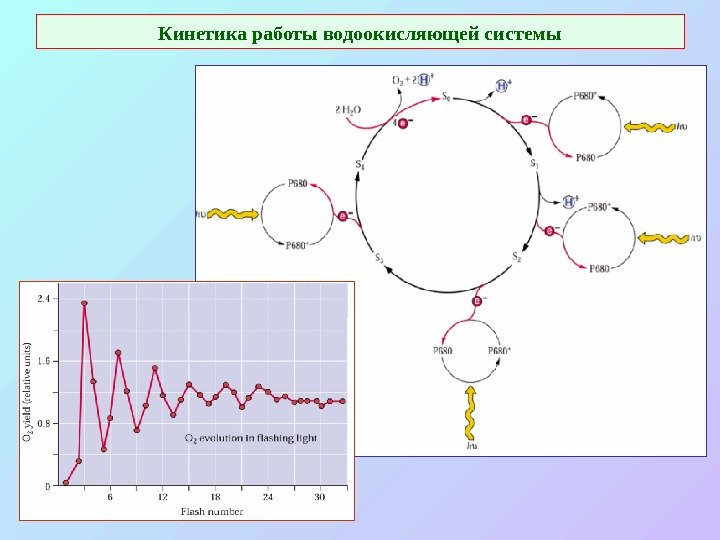
 Кинетика работы водоокисляющей системы
Кинетика работы водоокисляющей системы
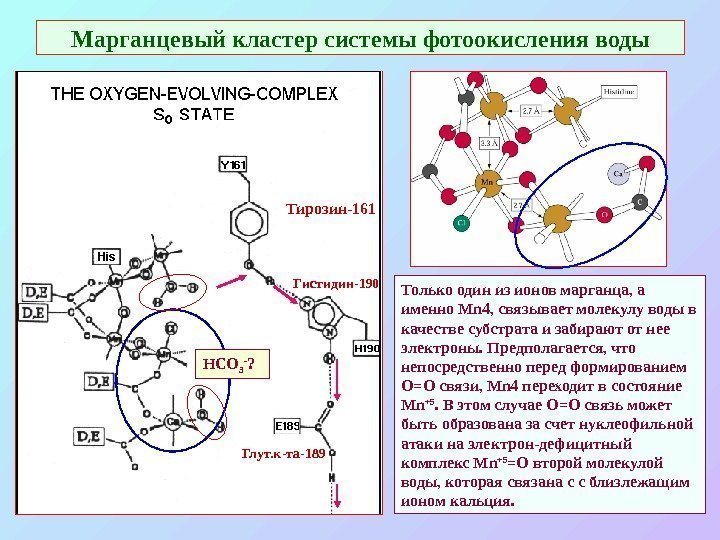
 Марганцевый кластер системы фотоокисления воды Тирозин-161 Гистидин-190 Глут. к-та-189 Только один из ионов марганца, а именно Mn 4, связывает молекулу воды в качестве субстрата и забирают от нее электроны. Предполагается, что непосредственно перед формированием O=O связи, Mn 4 переходит в состояние М n +5. В этом случае O=O связь может быть образована за счет нуклеофильной атаки на электрон-дефицитный комплекс М n +5 =O второй молекулой воды, которая связана с с близлежащим ионом кальция. HCO 3 — ?
Марганцевый кластер системы фотоокисления воды Тирозин-161 Гистидин-190 Глут. к-та-189 Только один из ионов марганца, а именно Mn 4, связывает молекулу воды в качестве субстрата и забирают от нее электроны. Предполагается, что непосредственно перед формированием O=O связи, Mn 4 переходит в состояние М n +5. В этом случае O=O связь может быть образована за счет нуклеофильной атаки на электрон-дефицитный комплекс М n +5 =O второй молекулой воды, которая связана с с близлежащим ионом кальция. HCO 3 — ?
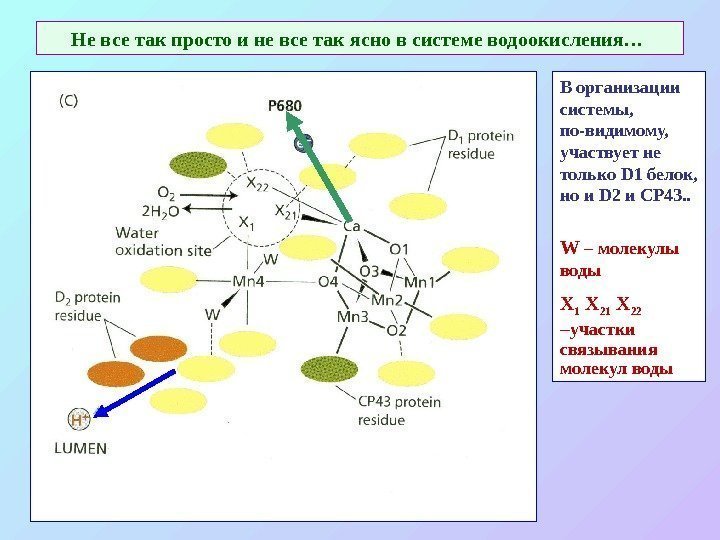
 Не все так просто и не все так ясно в системе водоокисления… В организации системы, по-видимому, участвует не только D 1 белок, но и D 2 и CP 43. . W – молекулы воды Х 1 Х 22 – участки связывания молекул воды
Не все так просто и не все так ясно в системе водоокисления… В организации системы, по-видимому, участвует не только D 1 белок, но и D 2 и CP 43. . W – молекулы воды Х 1 Х 22 – участки связывания молекул воды
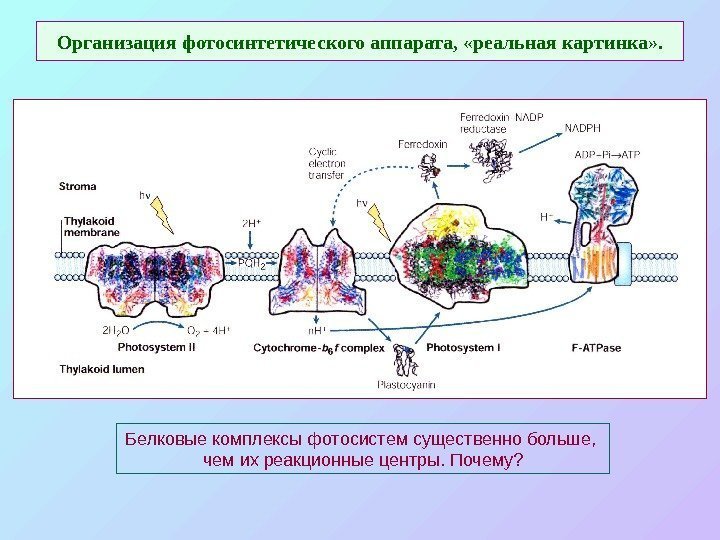
 Организация фотосинтетического аппарата, «реальная картинка» . Белковые комплексы фотосистем существенно больше, чем их реакционные центры. Почему?
Организация фотосинтетического аппарата, «реальная картинка» . Белковые комплексы фотосистем существенно больше, чем их реакционные центры. Почему?
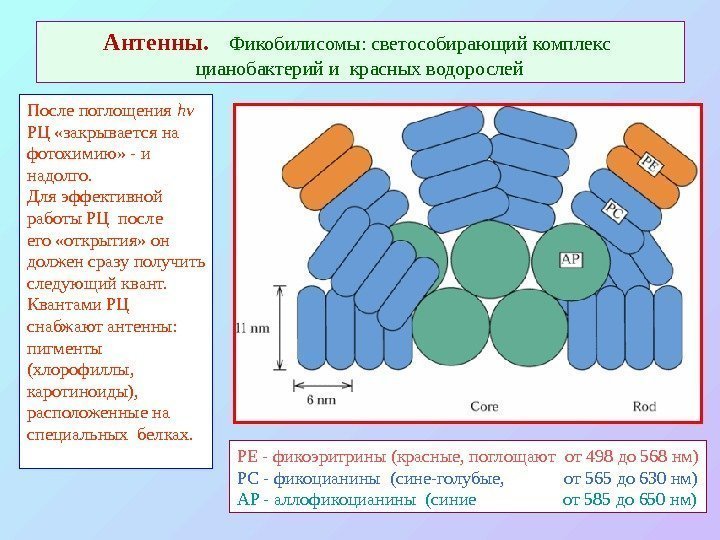
 Антенны. Фикобилисомы: светособирающий комплекс цианобактерий и красных водорослей После поглощения h ν РЦ «закрывается на фотохимию» — и надолго. Для эффективной работы РЦ после его «открытия» он должен сразу получить следующий квант. Квантами РЦ снабжают антенны: пигменты (хлорофиллы, каротиноиды), расположенные на специальных белках. PE — фикоэритрины (красные, поглощают от 498 до 568 нм) PC — фикоцианины (сине-голубые, от 565 до 630 нм) AP — аллофикоцианины (синие от 585 до 650 нм)
Антенны. Фикобилисомы: светособирающий комплекс цианобактерий и красных водорослей После поглощения h ν РЦ «закрывается на фотохимию» — и надолго. Для эффективной работы РЦ после его «открытия» он должен сразу получить следующий квант. Квантами РЦ снабжают антенны: пигменты (хлорофиллы, каротиноиды), расположенные на специальных белках. PE — фикоэритрины (красные, поглощают от 498 до 568 нм) PC — фикоцианины (сине-голубые, от 565 до 630 нм) AP — аллофикоцианины (синие от 585 до 650 нм)
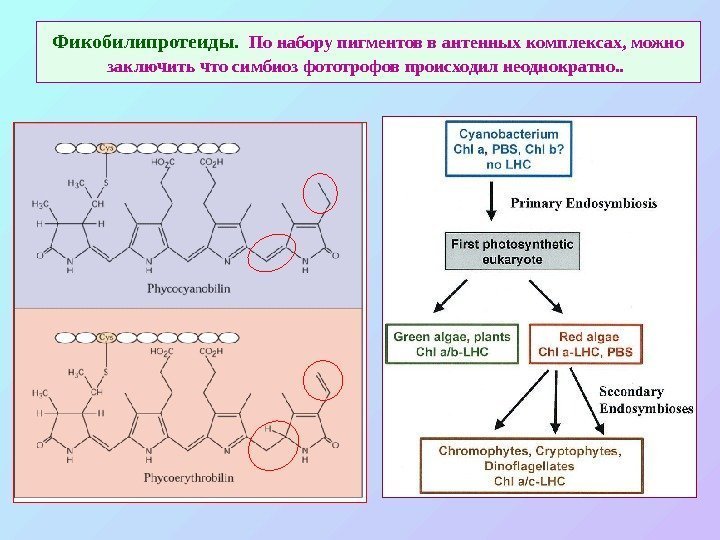
 Фикобилипротеиды. По набору пигментов в антенных комплексах, можно заключить что симбиоз фототрофов происходил неоднократно. .
Фикобилипротеиды. По набору пигментов в антенных комплексах, можно заключить что симбиоз фототрофов происходил неоднократно. .
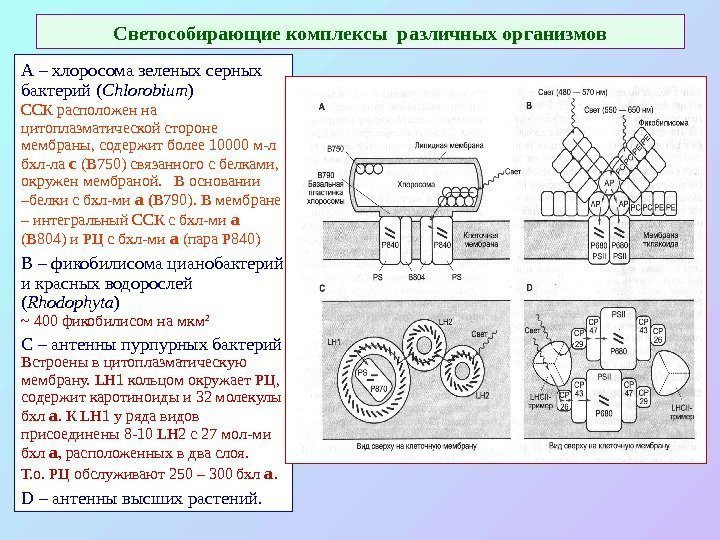
 Светособирающие комплексы различных организмов А – хлоросома зеленых серных бактерий ( Chlorobium ) ССК расположен на цитоплазматической стороне мембраны, содержит более 10000 м-л бхл-ла с (В 750) связанного с белками, окружен мембраной. В основании –белки с бхл-ми а ( В 790). В мембране – интегральный ССК с бхл-ми а ( B 804) и РЦ с бхл-ми а (пара P 840) B – фикобилисома цианобактерий и красных водорослей ( Rhodophyta ) ~ 400 фикобилисом на мкм 2 C – антенны пурпурных бактерий Встроены в цитоплазматическую мембрану. LH 1 кольцом окружает РЦ, содержит каротиноиды и 32 молекулы бхл а. К LH 1 у ряда видов присоединены 8 -10 LH 2 с 27 мол-ми бхл а , расположенных в два слоя. Т. о. РЦ обслуживают 250 – 300 бхл а. D – антенны высших растений.
Светособирающие комплексы различных организмов А – хлоросома зеленых серных бактерий ( Chlorobium ) ССК расположен на цитоплазматической стороне мембраны, содержит более 10000 м-л бхл-ла с (В 750) связанного с белками, окружен мембраной. В основании –белки с бхл-ми а ( В 790). В мембране – интегральный ССК с бхл-ми а ( B 804) и РЦ с бхл-ми а (пара P 840) B – фикобилисома цианобактерий и красных водорослей ( Rhodophyta ) ~ 400 фикобилисом на мкм 2 C – антенны пурпурных бактерий Встроены в цитоплазматическую мембрану. LH 1 кольцом окружает РЦ, содержит каротиноиды и 32 молекулы бхл а. К LH 1 у ряда видов присоединены 8 -10 LH 2 с 27 мол-ми бхл а , расположенных в два слоя. Т. о. РЦ обслуживают 250 – 300 бхл а. D – антенны высших растений.
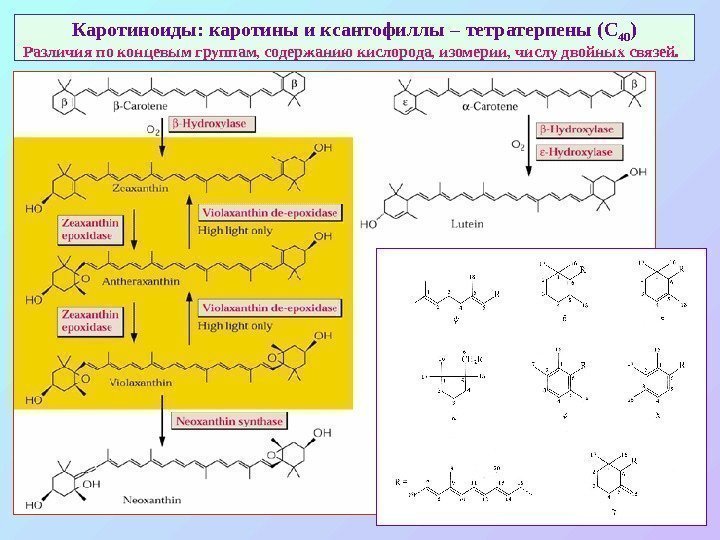
 Каротиноиды: каротины и ксантофиллы – тетратерпены (С 40 ) Различия по концевым группам, содержанию кислорода, изомерии, числу двойных связей.
Каротиноиды: каротины и ксантофиллы – тетратерпены (С 40 ) Различия по концевым группам, содержанию кислорода, изомерии, числу двойных связей.
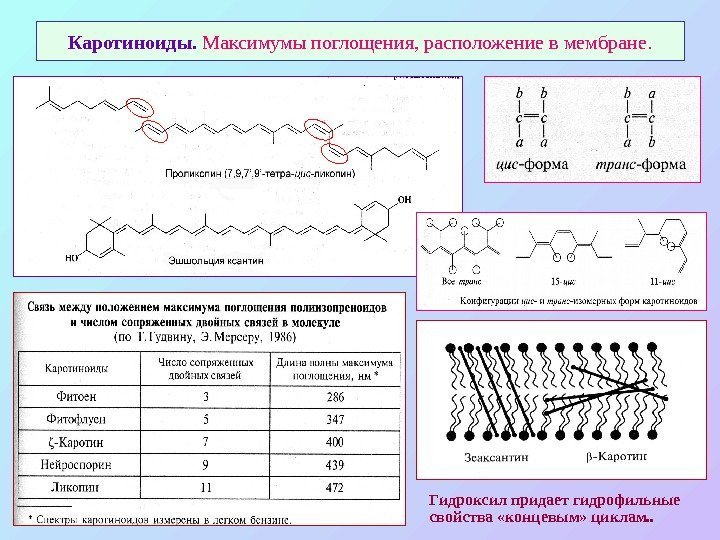
 Каротиноиды. Максимумы поглощения, расположение в мембране. Гидроксил придает гидрофильные свойства «концевым» циклам. .
Каротиноиды. Максимумы поглощения, расположение в мембране. Гидроксил придает гидрофильные свойства «концевым» циклам. .
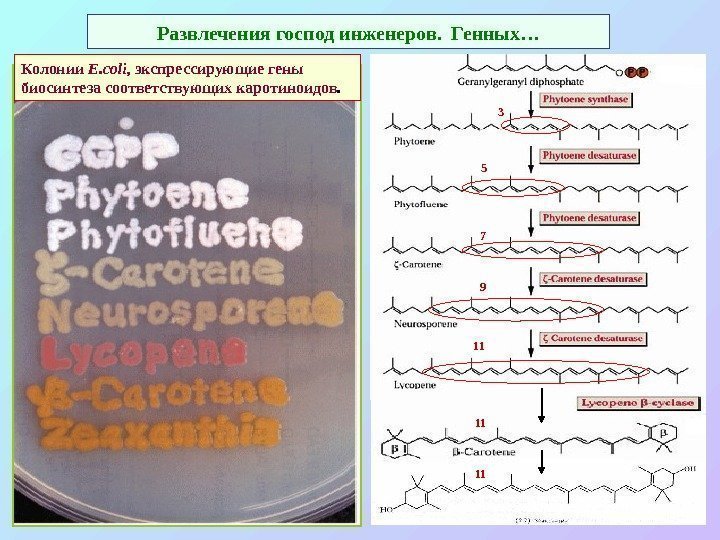
 Развлечения господ инженеров. Генных… Колонии E. coli, экспрессирующие гены биосинтеза соответствующих каротиноидов.
Развлечения господ инженеров. Генных… Колонии E. coli, экспрессирующие гены биосинтеза соответствующих каротиноидов.
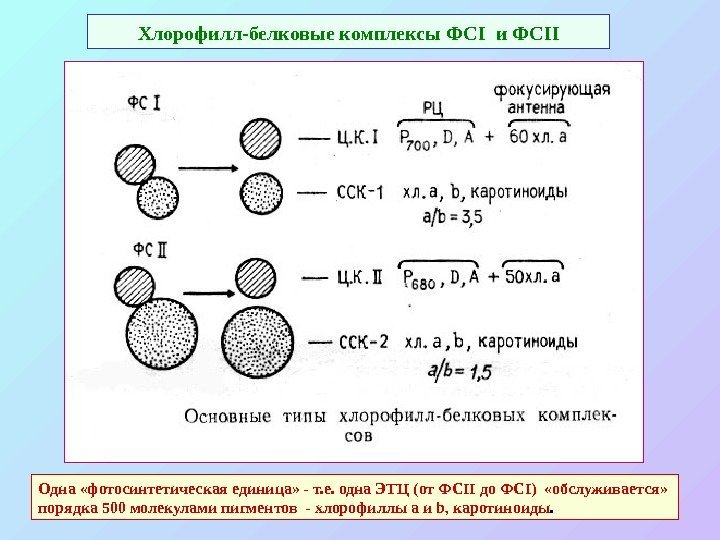
 Хлорофилл-белковые комплексы ФС I и ФС II Одна «фотосинтетическая единица» — т. е. одна ЭТЦ ( от ФС II до ФС I) «обслуживается» порядка 500 молекулами пигментов — хлорофиллы a и b , каротиноиды.
Хлорофилл-белковые комплексы ФС I и ФС II Одна «фотосинтетическая единица» — т. е. одна ЭТЦ ( от ФС II до ФС I) «обслуживается» порядка 500 молекулами пигментов — хлорофиллы a и b , каротиноиды.
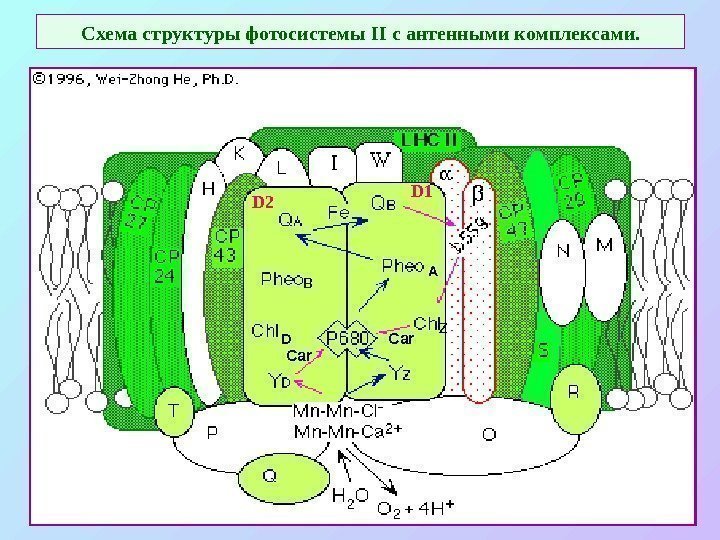
 Схема структуры фотосистемы II с антенными комплексами. в А D z Car.
Схема структуры фотосистемы II с антенными комплексами. в А D z Car.
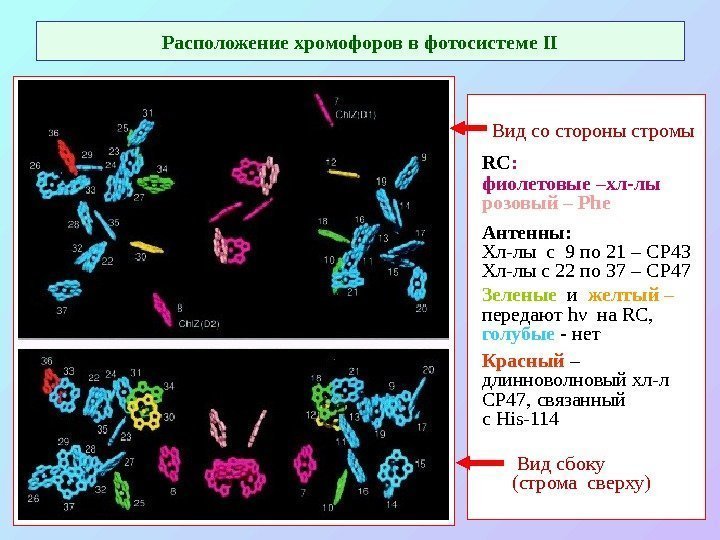
 Расположение хромофоров в фотосистеме II Вид со стороны стромы RC : фиолетовые –хл-лы розовый – Phe Антенны: Хл-лы с 9 по 21 – СР 43 Хл-лы с 22 по 37 – СР 47 Зеленые и желтый – передают h ν на RC, голубые — нет Красный – длинноволновый хл-л СР 47, связанный с His-114 Вид сбоку (строма сверху)
Расположение хромофоров в фотосистеме II Вид со стороны стромы RC : фиолетовые –хл-лы розовый – Phe Антенны: Хл-лы с 9 по 21 – СР 43 Хл-лы с 22 по 37 – СР 47 Зеленые и желтый – передают h ν на RC, голубые — нет Красный – длинноволновый хл-л СР 47, связанный с His-114 Вид сбоку (строма сверху)
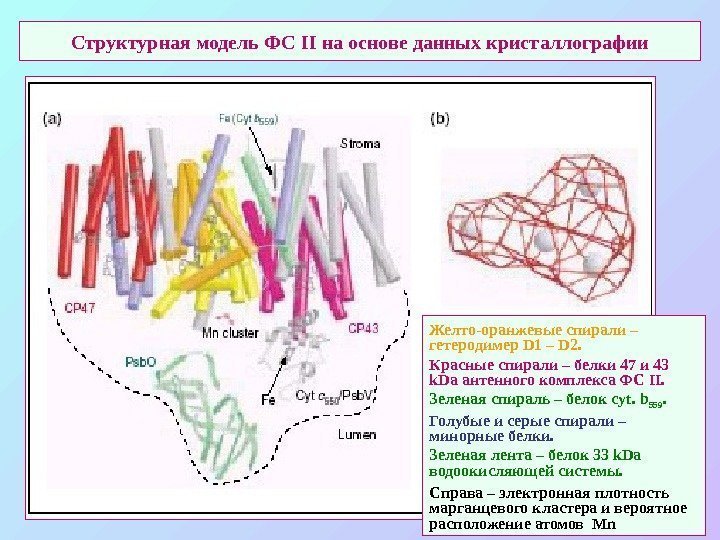
 Структурная модель ФС II на основе данных кристаллографии Желто-оранжевые спирали – гетеродимер D 1 – D 2. Красные спирали – белки 47 и 43 k. Da антенного комплекса ФС II. Зеленая спираль – белок cyt. b 559. Голубые и серые спирали – минорные белки. Зеленая лента – белок 33 k. Da водоокисляющей системы. Справа – электронная плотность марганцевого кластера и вероятное расположение атомов Mn
Структурная модель ФС II на основе данных кристаллографии Желто-оранжевые спирали – гетеродимер D 1 – D 2. Красные спирали – белки 47 и 43 k. Da антенного комплекса ФС II. Зеленая спираль – белок cyt. b 559. Голубые и серые спирали – минорные белки. Зеленая лента – белок 33 k. Da водоокисляющей системы. Справа – электронная плотность марганцевого кластера и вероятное расположение атомов Mn
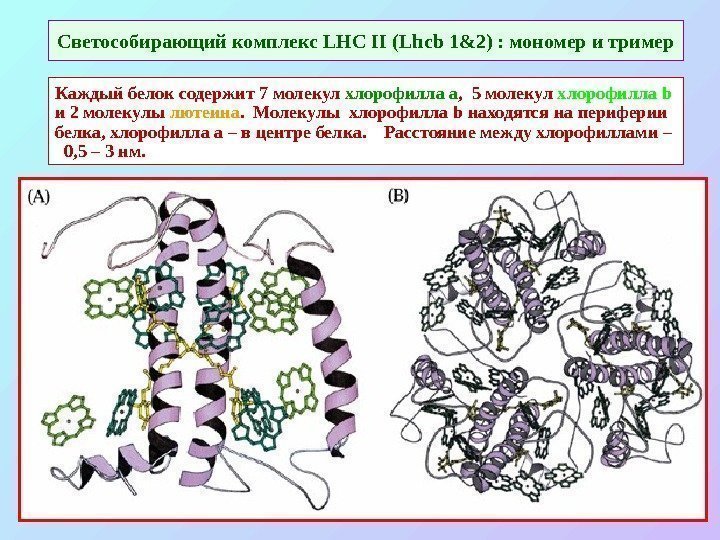
 Светособирающий комплекс LHC II ( Lhcb 1 &2) : мономер и тример Каждый белок содержит 7 молекул хлорофилла a , 5 молекул хлорофилла b и 2 молекулы лютеина. Молекулы хлорофилла b находятся на периферии белка, хлорофилла a – в центре белка. Расстояние между хлорофиллами – 0, 5 – 3 нм.
Светособирающий комплекс LHC II ( Lhcb 1 &2) : мономер и тример Каждый белок содержит 7 молекул хлорофилла a , 5 молекул хлорофилла b и 2 молекулы лютеина. Молекулы хлорофилла b находятся на периферии белка, хлорофилла a – в центре белка. Расстояние между хлорофиллами – 0, 5 – 3 нм.
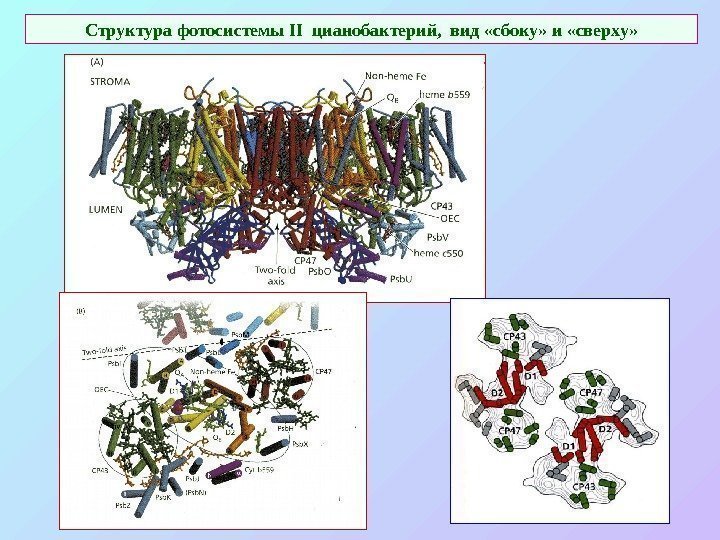
 Структура фотосистемы II цианобактерий, вид «сбоку» и «сверху»
Структура фотосистемы II цианобактерий, вид «сбоку» и «сверху»
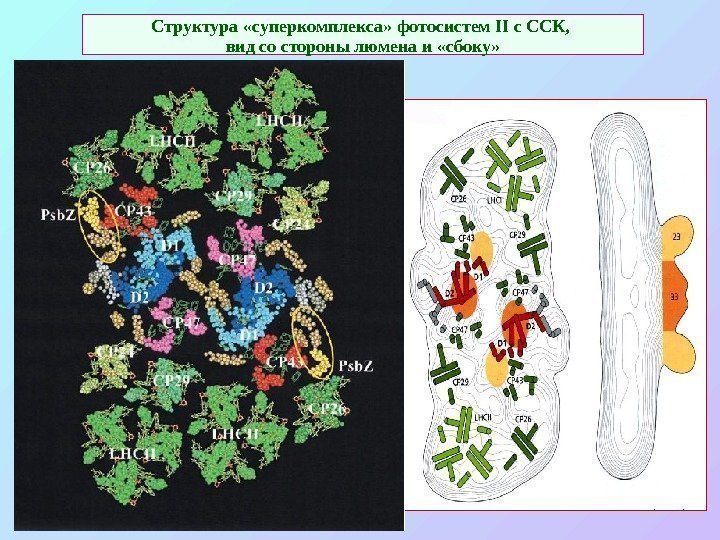
 Структура «суперкомплекса» фотосистем II c ССК, вид со стороны люмена и «сбоку»
Структура «суперкомплекса» фотосистем II c ССК, вид со стороны люмена и «сбоку»
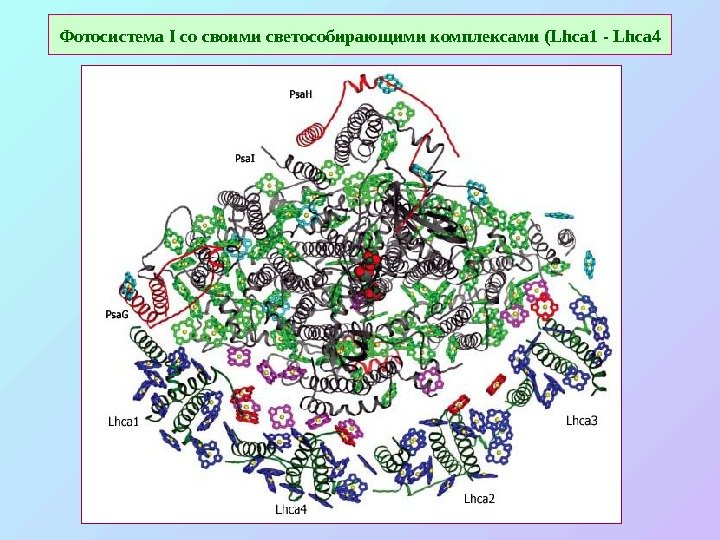
 Фотосистема I со своими светособирающими комплексами ( Lhca 1 — Lhca
Фотосистема I со своими светособирающими комплексами ( Lhca 1 — Lhca
 Фотосистема I скорее всего существует в виде тримера
Фотосистема I скорее всего существует в виде тримера
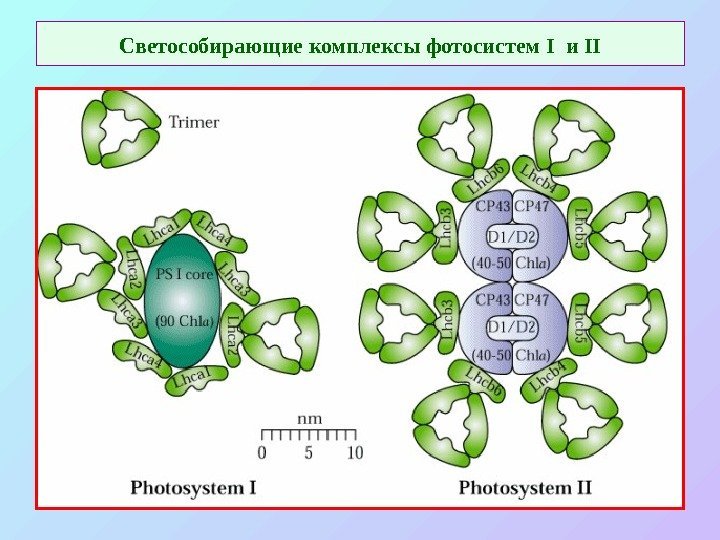
 Светособирающие комплексы фотосистем I и II
Светособирающие комплексы фотосистем I и II
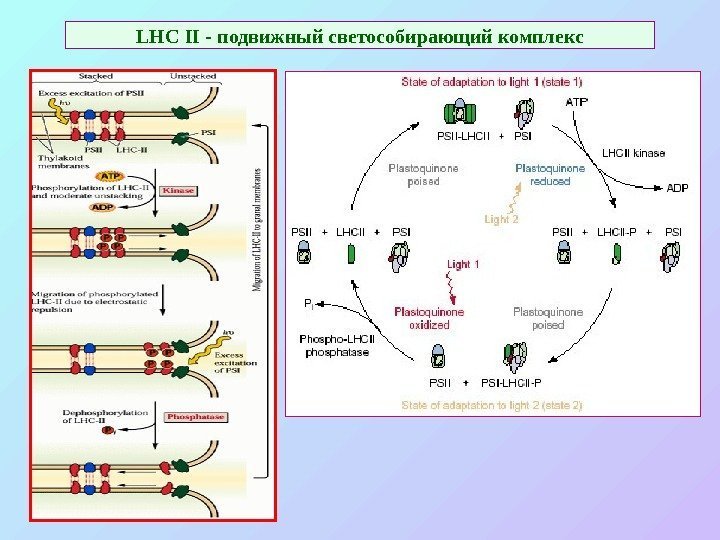
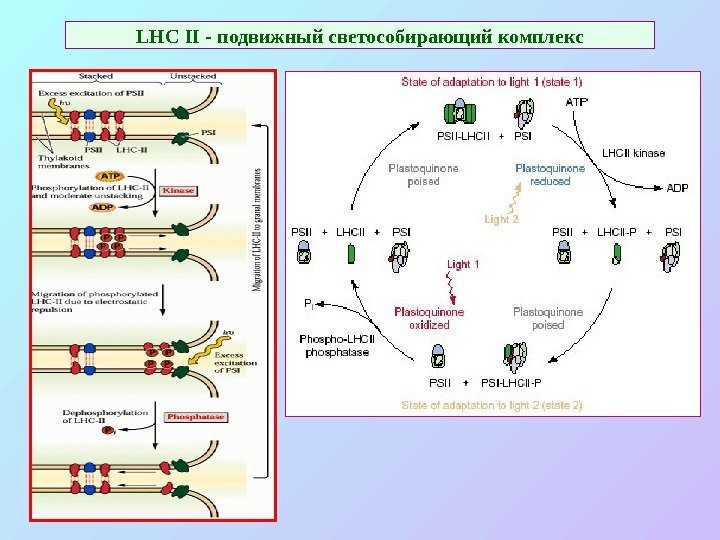
 LHC II — подвижный светособирающий комплекс
LHC II — подвижный светособирающий комплекс
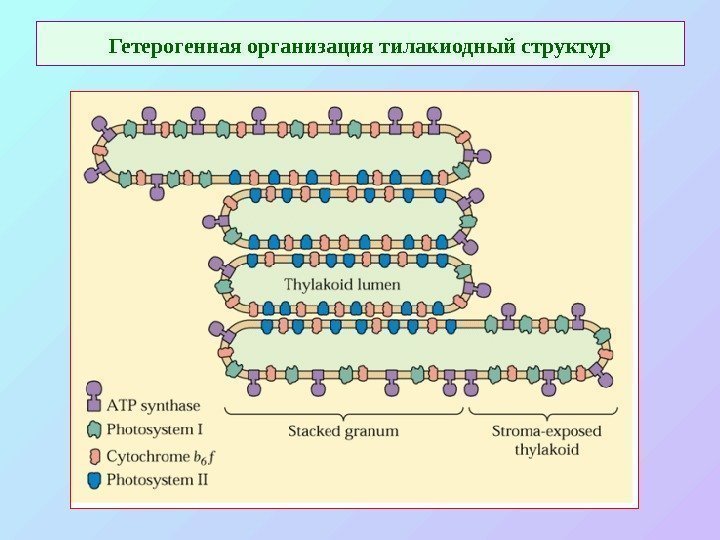
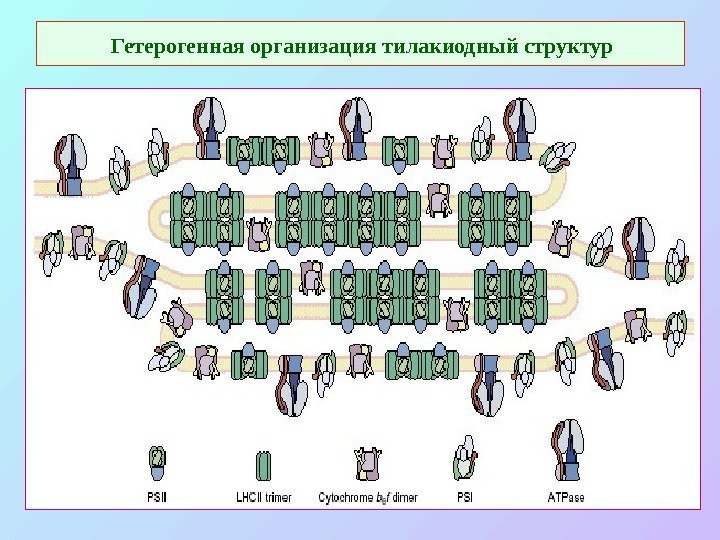
 Гетерогенная организация тилакиодный структур
Гетерогенная организация тилакиодный структур
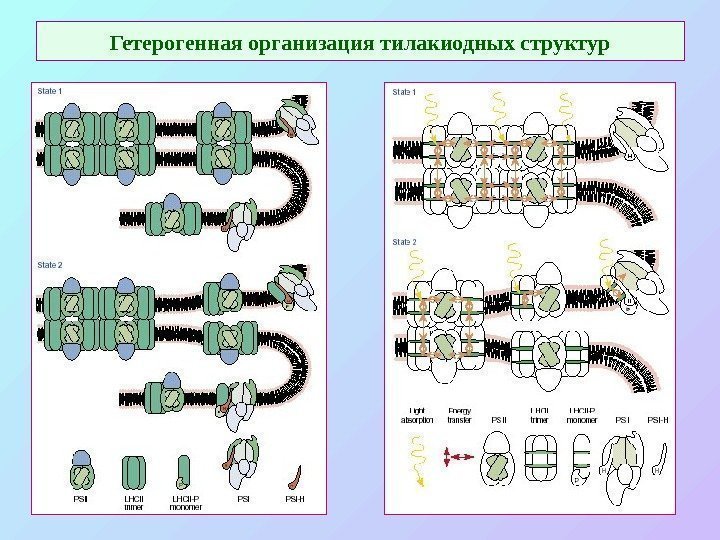
 Гетерогенная организация тилакиодных структур
Гетерогенная организация тилакиодных структур
 Гетерогенная организация тилакиодный структур
Гетерогенная организация тилакиодный структур
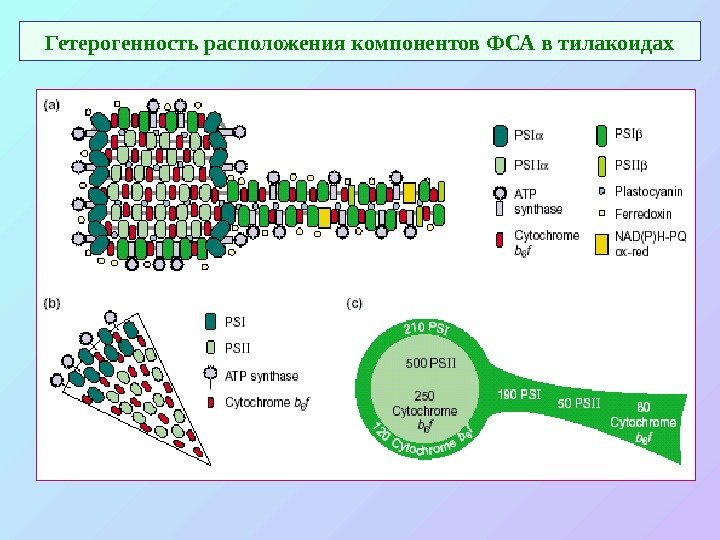
 Гетерогенность расположения компонентов ФСА в тилакоидах
Гетерогенность расположения компонентов ФСА в тилакоидах
 Hosta ‘ Piedmont Gold’ Hosta sieboldiana ‘ Elegans’ Hosta ‘ Golden Haze’
Hosta ‘ Piedmont Gold’ Hosta sieboldiana ‘ Elegans’ Hosta ‘ Golden Haze’
 Механизмы регулирования и защиты ФС II от фотодеструкции • нециклический поток , регулирование мобильными антеннами; • циклические потоки вокруг каждой фотосистемы; • псевдоциклический транспорт электронов • Хлоропластное дыхание — ? • виолоксантиновый цикл • «тушение» триплетного состояния хлорофилла каротиноидами • «обезвреживание» активных форм кислорода каротиноидами • каротиноиды «на заклание» • замена D 1 — белка
Механизмы регулирования и защиты ФС II от фотодеструкции • нециклический поток , регулирование мобильными антеннами; • циклические потоки вокруг каждой фотосистемы; • псевдоциклический транспорт электронов • Хлоропластное дыхание — ? • виолоксантиновый цикл • «тушение» триплетного состояния хлорофилла каротиноидами • «обезвреживание» активных форм кислорода каротиноидами • каротиноиды «на заклание» • замена D 1 — белка
 LHC II — подвижный светособирающий комплекс
LHC II — подвижный светособирающий комплекс
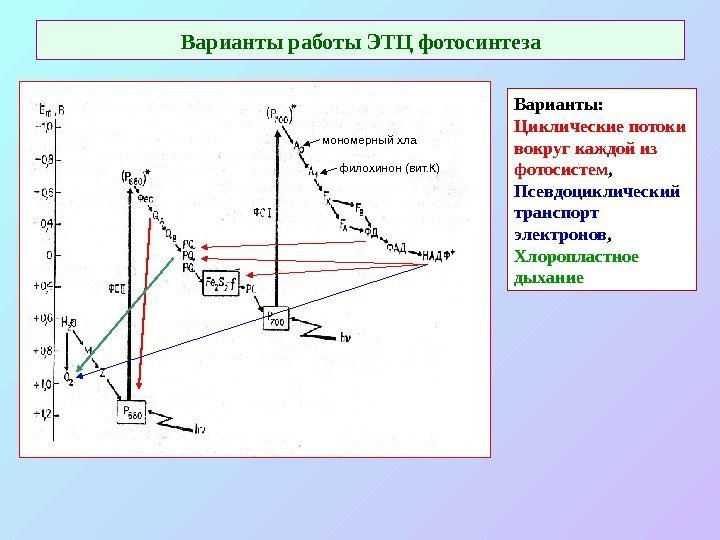
 Варианты работы ЭТЦ фотосинтеза мономерный хла филохинон (вит. К) Варианты: Циклические потоки вокруг каждой из фотосистем , Псевдоциклический транспорт электронов , Хлоропластное дыхание
Варианты работы ЭТЦ фотосинтеза мономерный хла филохинон (вит. К) Варианты: Циклические потоки вокруг каждой из фотосистем , Псевдоциклический транспорт электронов , Хлоропластное дыхание
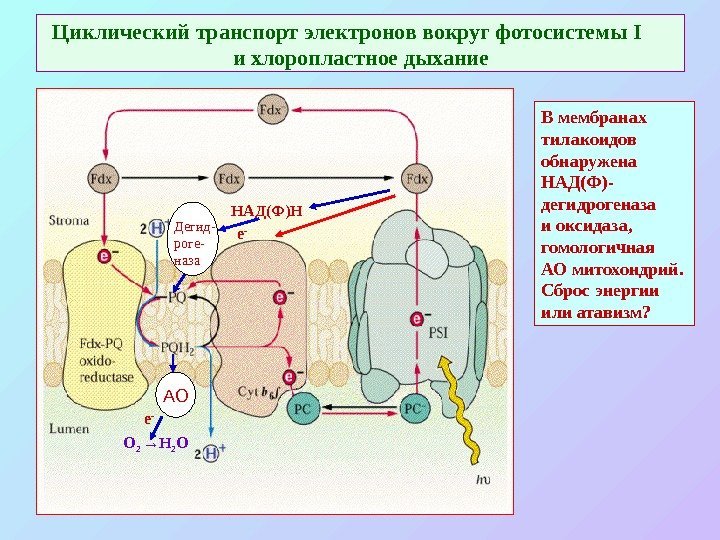
 Циклический транспорт электронов вокруг фотосистемы I и хлоропластное дыхание НАД(Ф)Н Дегид- роге- наза АО О 2 →Н 2 О е — В мембранах тилакоидов обнаружена НАД(Ф)- дегидрогеназа и оксидаза, гомологичная АО митохондрий. Сброс энергии или атавизм?
Циклический транспорт электронов вокруг фотосистемы I и хлоропластное дыхание НАД(Ф)Н Дегид- роге- наза АО О 2 →Н 2 О е — В мембранах тилакоидов обнаружена НАД(Ф)- дегидрогеназа и оксидаза, гомологичная АО митохондрий. Сброс энергии или атавизм?
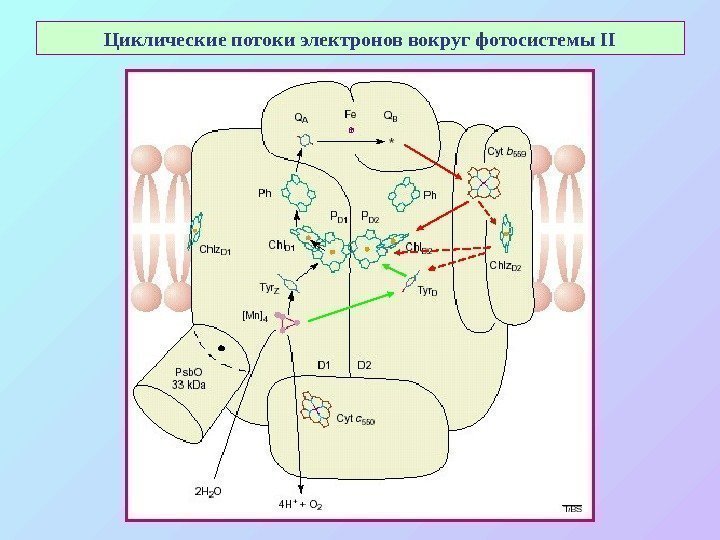
 Циклически e потоки электронов вокруг фотосистемы II
Циклически e потоки электронов вокруг фотосистемы II
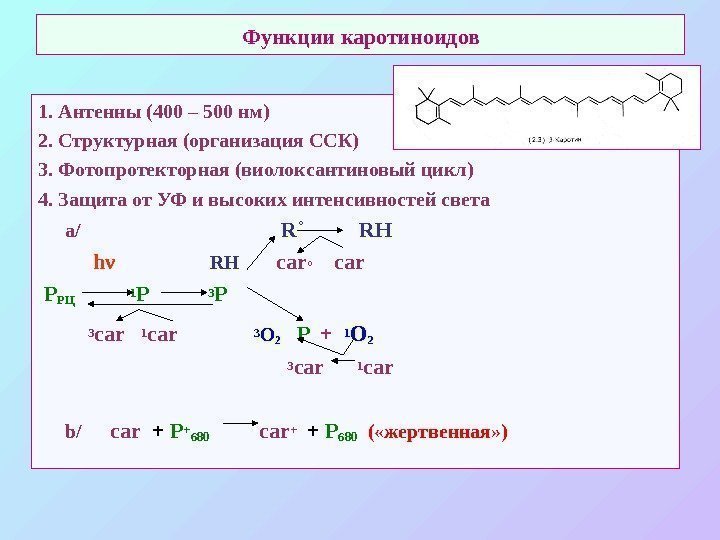
 Функции каротиноидов 1. Антенны (400 – 500 нм) 2. Структурная (организация ССК) 3. Фотопротекторная (виолоксантиновый цикл) 4. Защита от УФ и высоких интенсивностей света a/ R ˚ R Н h ν RH carо car P РЦ 1 Р 3 Р 3 car 1 car 3 O 2 P + 1 O 2 3 car 1 car b/ car + P +680 car+ + P 680 ( «жертвенная» )
Функции каротиноидов 1. Антенны (400 – 500 нм) 2. Структурная (организация ССК) 3. Фотопротекторная (виолоксантиновый цикл) 4. Защита от УФ и высоких интенсивностей света a/ R ˚ R Н h ν RH carо car P РЦ 1 Р 3 Р 3 car 1 car 3 O 2 P + 1 O 2 3 car 1 car b/ car + P +680 car+ + P 680 ( «жертвенная» )
 Каротиноиды в хлоропластах 1. Разные состояния: мономерная или агрегированная форма, связь с белками. 2. Изомеры: транс – в антеннах, цис – в РЦ. При этом в РЦ – β -каротины, в ССК – ксантофиллы. Ядро ФС I высших растений содержит 14 молекул β -каротина, 2 из них в РЦ, 12 – во внутренней антенне. Ядро ФС II : на D 1 и D 2 белках расположены симметрично 2 молекулы β -каротина. На D 1 – все-транс форма, на D 2 – 15 — цис форма. Внутренняя антенна (СР 43 и СР 47) – 2 -3 молекулы β -каротина и несколько молекул лютеина. ССК (СР 24, СР 26, СР 29) – в каждом 1 -2 молекулы лютеина, а также молекулы неоксантина, зеаксантина, антероксантина и виолоксантина. Антенная функция – все-транс форма. Защитные функции — все-транс форма β -каротина на D 1 белке – альтернативный донор е- для Р 680 при низких tо и нарушении работы OEC. 15 — цис форма на D 2 – тушение триплета Р 680 за счет изомеризации во все-транс- форму.
Каротиноиды в хлоропластах 1. Разные состояния: мономерная или агрегированная форма, связь с белками. 2. Изомеры: транс – в антеннах, цис – в РЦ. При этом в РЦ – β -каротины, в ССК – ксантофиллы. Ядро ФС I высших растений содержит 14 молекул β -каротина, 2 из них в РЦ, 12 – во внутренней антенне. Ядро ФС II : на D 1 и D 2 белках расположены симметрично 2 молекулы β -каротина. На D 1 – все-транс форма, на D 2 – 15 — цис форма. Внутренняя антенна (СР 43 и СР 47) – 2 -3 молекулы β -каротина и несколько молекул лютеина. ССК (СР 24, СР 26, СР 29) – в каждом 1 -2 молекулы лютеина, а также молекулы неоксантина, зеаксантина, антероксантина и виолоксантина. Антенная функция – все-транс форма. Защитные функции — все-транс форма β -каротина на D 1 белке – альтернативный донор е- для Р 680 при низких tо и нарушении работы OEC. 15 — цис форма на D 2 – тушение триплета Р 680 за счет изомеризации во все-транс- форму.
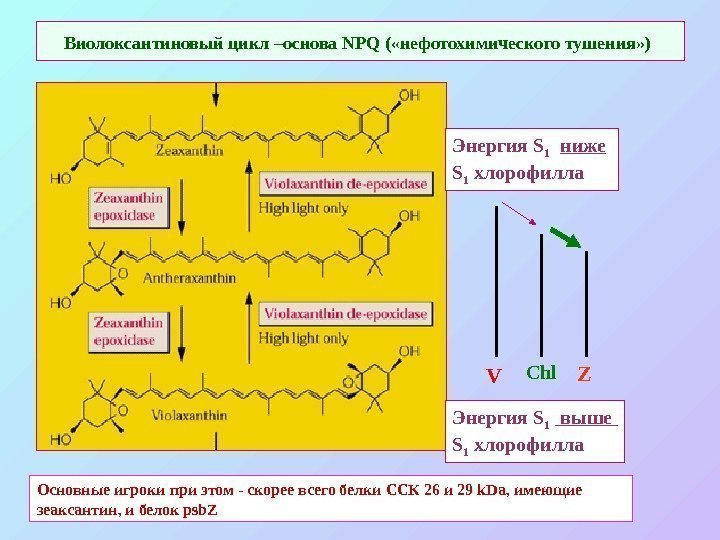
 Виолоксантиновый цикл –основа NPQ ( «нефотохимического тушения» ) Энергия S 1 ниже S 1 хлорофилла Энергия S 1 выше S 1 хлорофилла V Chl Z Основные игроки при этом — скорее всего белки ССК 26 и 29 k. Da , имеющие зеаксантин, и белок psb. Z
Виолоксантиновый цикл –основа NPQ ( «нефотохимического тушения» ) Энергия S 1 ниже S 1 хлорофилла Энергия S 1 выше S 1 хлорофилла V Chl Z Основные игроки при этом — скорее всего белки ССК 26 и 29 k. Da , имеющие зеаксантин, и белок psb. Z
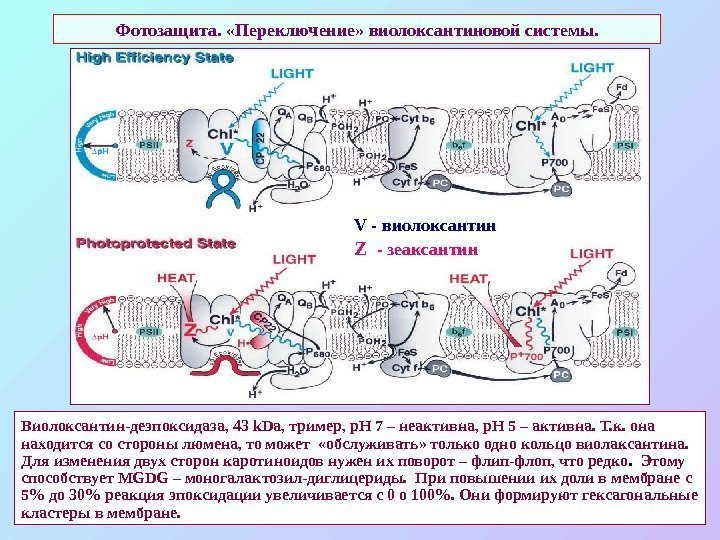
 Фотозащита. «Переключение» виолоксантиновой системы. Виолоксантин-деэпоксидаза, 43 k. Da , тример, р. Н 7 – неактивна, р. Н 5 – активна. Т. к. она находится со стороны люмена, то может «обслуживать» только одно кольцо виолаксантина. Для изменения двух сторон каротиноидов нужен их поворот – флип-флоп, что редко. Этому способствует MGDG – моногалактозил-диглицериды. При повышении их доли в мембране с 5% до 30% реакция эпоксидации увеличивается с 0 о 100%. Они формируют гексагональные кластеры в мембране. V — виолоксантин Z — зеаксантин
Фотозащита. «Переключение» виолоксантиновой системы. Виолоксантин-деэпоксидаза, 43 k. Da , тример, р. Н 7 – неактивна, р. Н 5 – активна. Т. к. она находится со стороны люмена, то может «обслуживать» только одно кольцо виолаксантина. Для изменения двух сторон каротиноидов нужен их поворот – флип-флоп, что редко. Этому способствует MGDG – моногалактозил-диглицериды. При повышении их доли в мембране с 5% до 30% реакция эпоксидации увеличивается с 0 о 100%. Они формируют гексагональные кластеры в мембране. V — виолоксантин Z — зеаксантин
 D 1 белок – «камикадзе» растительной клетки • Разборка ФС II : уходят белки OEC, снимаются атомы Mn, отсоединяются CP 43, CP 47 • Удаление «испорченного» белка: «отгрызаются» выступающие из мембраны участки D 1 белка ( работает специальная протеаза deg. P 2 ), специальный белок «выталкивает» его останки из мембраны • Синтез нового D 1 белка: синтез идет в ламеллах, процессинг (удаляется N- концевой метионин, оставшийся треонин ацетилируется, этот треонин может обратимо фосфориллироваться). • Миграция D 1 белка в граны: белок пальмитинируется и в таком виде мигрирует в граны. • Обратная сборка ФС II Время «полужизни» D 1 белка – 30 минут. Интенсивность синтеза D 1 белка — 50% от всех синтезируемых в хлоропласте белков, тогда как его доля – 0, 1% от белков хлоропласта
D 1 белок – «камикадзе» растительной клетки • Разборка ФС II : уходят белки OEC, снимаются атомы Mn, отсоединяются CP 43, CP 47 • Удаление «испорченного» белка: «отгрызаются» выступающие из мембраны участки D 1 белка ( работает специальная протеаза deg. P 2 ), специальный белок «выталкивает» его останки из мембраны • Синтез нового D 1 белка: синтез идет в ламеллах, процессинг (удаляется N- концевой метионин, оставшийся треонин ацетилируется, этот треонин может обратимо фосфориллироваться). • Миграция D 1 белка в граны: белок пальмитинируется и в таком виде мигрирует в граны. • Обратная сборка ФС II Время «полужизни» D 1 белка – 30 минут. Интенсивность синтеза D 1 белка — 50% от всех синтезируемых в хлоропласте белков, тогда как его доля – 0, 1% от белков хлоропласта
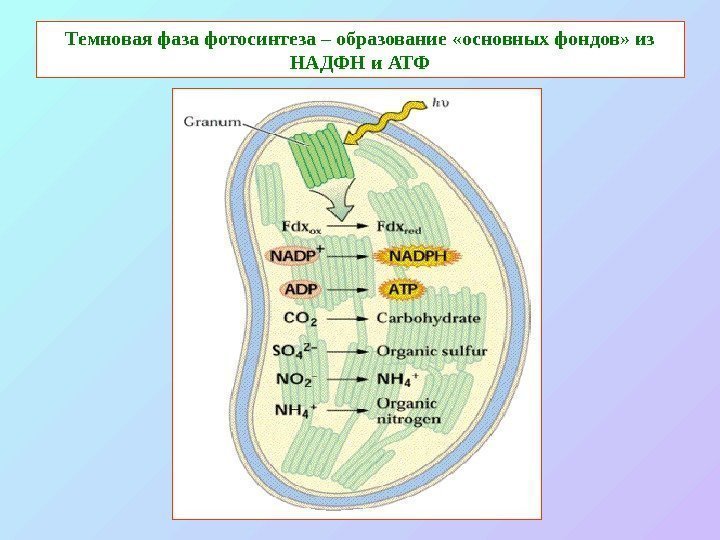
 Темновая фаза фотосинтеза – образование «основных фондов» из НАДФН и АТФ
Темновая фаза фотосинтеза – образование «основных фондов» из НАДФН и АТФ
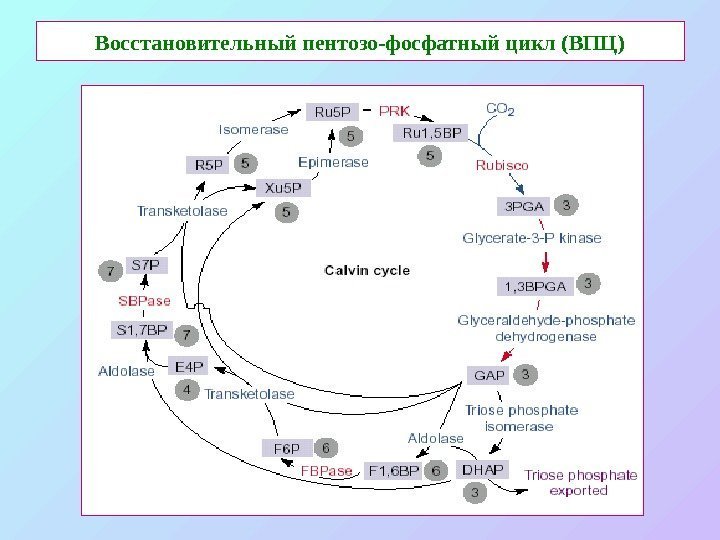
 Восстановительный пентозо-фосфатный цикл (ВПЦ)
Восстановительный пентозо-фосфатный цикл (ВПЦ)

