Фотометрические методы анализа.ppt
- Количество слайдов: 29
 ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
ФОТОМЕТРИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
 Фотометрические методы анализа, основаны на взаимодействии электромагнитного излучения с анализируемыми веществами. Это взаимодействие приводит к различным энергетическим переходам, которые регистрируются экспериментально в виде поглощения излучения, отражения и рассеяния электромагнитного излучения.
Фотометрические методы анализа, основаны на взаимодействии электромагнитного излучения с анализируемыми веществами. Это взаимодействие приводит к различным энергетическим переходам, которые регистрируются экспериментально в виде поглощения излучения, отражения и рассеяния электромагнитного излучения.
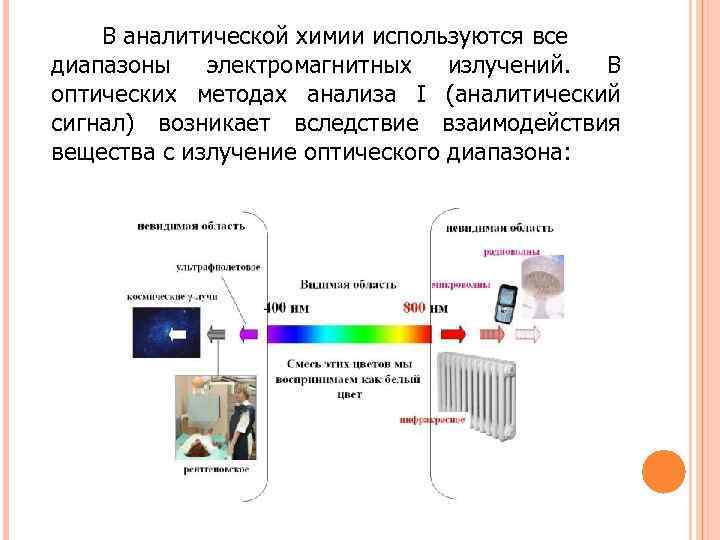 В аналитической химии используются все диапазоны электромагнитных излучений. В оптических методах анализа I (аналитический сигнал) возникает вследствие взаимодействия вещества с излучение оптического диапазона:
В аналитической химии используются все диапазоны электромагнитных излучений. В оптических методах анализа I (аналитический сигнал) возникает вследствие взаимодействия вещества с излучение оптического диапазона:
 Ø Ø В зависимости от вида поглощающих частиц и способа трансформирования поглощенной энергии различают: Атомно-абсорбционный анализ, основанный на поглощении световой энергии атомами анализируемых веществ; Молекулярный абсорбционный анализ, т. е. анализ поглощения света молекулами анализируемого вещества в ультрафиолетовой, видимой и инфракрасной областях спектра (спектрофотометрия, фотоколориметрия, ИК-спектроскопия); Анализ поглощения и рассеяния световой энергии взвешенными частицами анализируемого вещества (турбидиметрия, нефелометрия); Люминесцентный (флуорометрический) анализ, основанный на измерении излучения, возникающего в результате выделения энергии возбужденными молекулами анализируемого вещества.
Ø Ø В зависимости от вида поглощающих частиц и способа трансформирования поглощенной энергии различают: Атомно-абсорбционный анализ, основанный на поглощении световой энергии атомами анализируемых веществ; Молекулярный абсорбционный анализ, т. е. анализ поглощения света молекулами анализируемого вещества в ультрафиолетовой, видимой и инфракрасной областях спектра (спектрофотометрия, фотоколориметрия, ИК-спектроскопия); Анализ поглощения и рассеяния световой энергии взвешенными частицами анализируемого вещества (турбидиметрия, нефелометрия); Люминесцентный (флуорометрический) анализ, основанный на измерении излучения, возникающего в результате выделения энергии возбужденными молекулами анализируемого вещества.
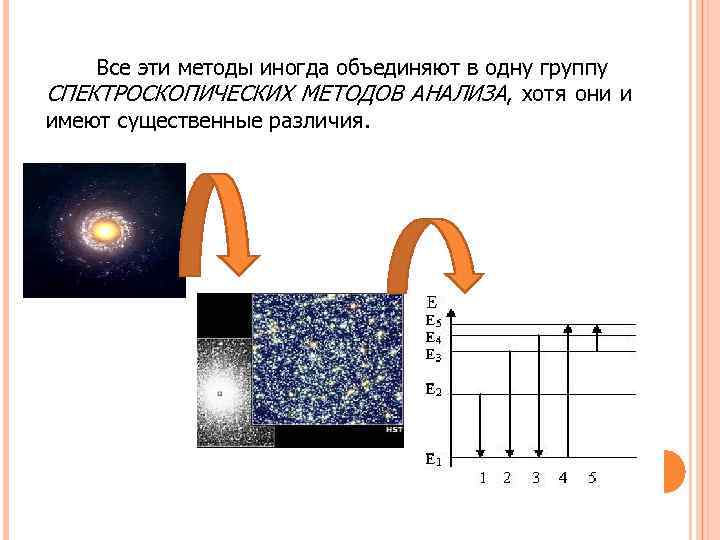 Все эти методы иногда объединяют в одну группу СПЕКТРОСКОПИЧЕСКИХ МЕТОДОВ АНАЛИЗА, хотя они и имеют существенные различия.
Все эти методы иногда объединяют в одну группу СПЕКТРОСКОПИЧЕСКИХ МЕТОДОВ АНАЛИЗА, хотя они и имеют существенные различия.
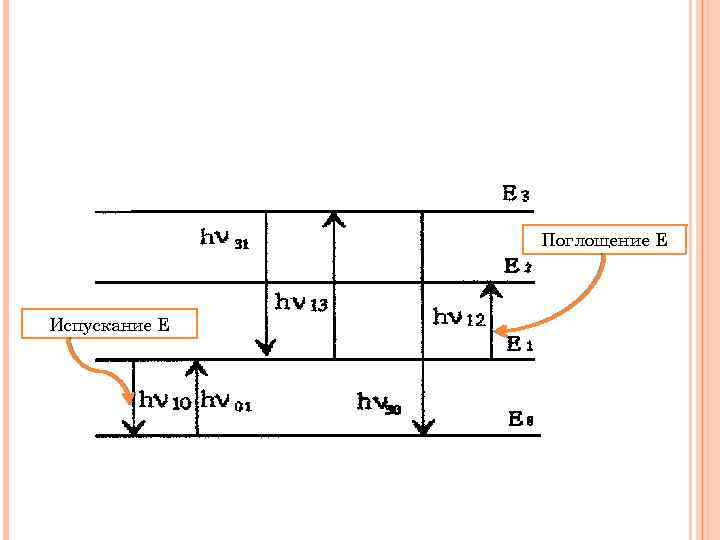 Поглощение Е Испускание Е
Поглощение Е Испускание Е
 В зависимости от используемой аппаратуры в фотометрическом анализе различают: Ø спектрофотометрический метод – анализ по поглощению монохроматического света; Ø фотоколориметрический – анализ по поглощению полихроматического (немонохроматического) видимой области спектра. света в Оба метода основаны на пропорциональной зависимости между светопоглощением и концентрацией поглощающего вещества.
В зависимости от используемой аппаратуры в фотометрическом анализе различают: Ø спектрофотометрический метод – анализ по поглощению монохроматического света; Ø фотоколориметрический – анализ по поглощению полихроматического (немонохроматического) видимой области спектра. света в Оба метода основаны на пропорциональной зависимости между светопоглощением и концентрацией поглощающего вещества.
 Фотометрические методы подразделяют на прямые и косвенные. В прямых методах определяемый ион М с помощью реагента R переводят в светопоглощающее соединение MR, а затем измеряют интенсивность светопоглощения раствора этого соединения. При косвенных определениях используют вспомогательные соединения, которые при взаимодействии с определяемым веществом либо разрушаются сами, либо образуют новые светопоглощающие соединения.
Фотометрические методы подразделяют на прямые и косвенные. В прямых методах определяемый ион М с помощью реагента R переводят в светопоглощающее соединение MR, а затем измеряют интенсивность светопоглощения раствора этого соединения. При косвенных определениях используют вспомогательные соединения, которые при взаимодействии с определяемым веществом либо разрушаются сами, либо образуют новые светопоглощающие соединения.
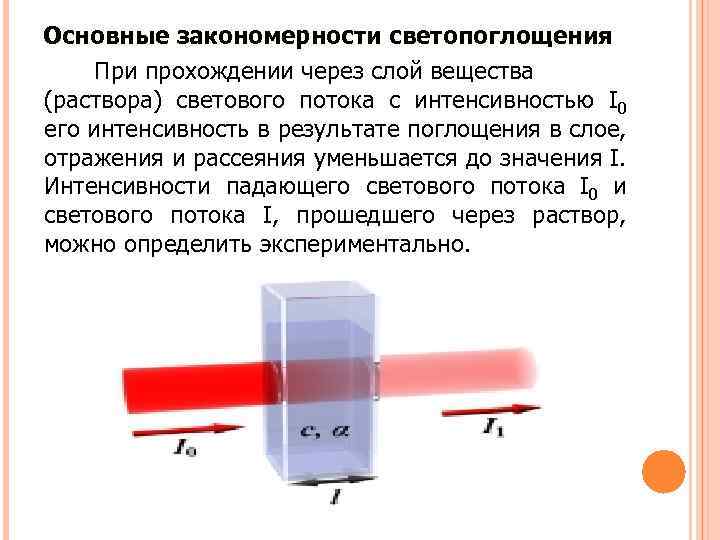 Основные закономерности светопоглощения При прохождении через слой вещества (раствора) светового потока с интенсивностью I 0 его интенсивность в результате поглощения в слое, отражения и рассеяния уменьшается до значения I. Интенсивности падающего светового потока I 0 и светового потока I, прошедшего через раствор, можно определить экспериментально.
Основные закономерности светопоглощения При прохождении через слой вещества (раствора) светового потока с интенсивностью I 0 его интенсивность в результате поглощения в слое, отражения и рассеяния уменьшается до значения I. Интенсивности падающего светового потока I 0 и светового потока I, прошедшего через раствор, можно определить экспериментально.
 Связь между интенсивностями световых потоков I 0 и I устанавливается законом Бугера-Ламберта, согласно которому однородные слои одного и того же вещества одинаковой толщины поглощают одну и ту же долю падающей на них световой энергии (при постоянной концентрации растворенного вещества). Математически этот закон выражается уравнением экспоненциальной зависимости: I = I 0 eal , где е – основание натуральных логарифмов; а – коэффициент поглощения; l 0 – толщина поглощающего слоя.
Связь между интенсивностями световых потоков I 0 и I устанавливается законом Бугера-Ламберта, согласно которому однородные слои одного и того же вещества одинаковой толщины поглощают одну и ту же долю падающей на них световой энергии (при постоянной концентрации растворенного вещества). Математически этот закон выражается уравнением экспоненциальной зависимости: I = I 0 eal , где е – основание натуральных логарифмов; а – коэффициент поглощения; l 0 – толщина поглощающего слоя.
 Поглощение излучения характеризуют оптической плотностью: D= lg(I 0/I) Связь между концентрацией поглощающего раствора и его оптической плотностью lg(I 0/I) выражается законом Бера, согласно которому оптическая плотность раствора прямо пропорциональна концентрации растворенного вещества при постоянной толщине слоя: Lg(I 0/I) = k 1 C , где k 1 – коэффициент пропорциональности; С – концентрация растворенного вещества.
Поглощение излучения характеризуют оптической плотностью: D= lg(I 0/I) Связь между концентрацией поглощающего раствора и его оптической плотностью lg(I 0/I) выражается законом Бера, согласно которому оптическая плотность раствора прямо пропорциональна концентрации растворенного вещества при постоянной толщине слоя: Lg(I 0/I) = k 1 C , где k 1 – коэффициент пропорциональности; С – концентрация растворенного вещества.
 Зависимость интенсивности монохроматического светового потока, прошедшего через слой окрашенного раствора, от интенсивности падающего потока света, концентрации окрашенного вещества и толщины слоя раствора определяется объединенным законом Бугера-Ламберта-Бера, который является основным законом светопоглощения и лежит в основе большинства фотометрических методов анализа: I = I 0 *10−ελCl , где ε – молярный коэффициент светопоглощения при длине λ, С – молярная концентрация, L – толщина поглощающего слоя I 0 – интенсивность падающего света.
Зависимость интенсивности монохроматического светового потока, прошедшего через слой окрашенного раствора, от интенсивности падающего потока света, концентрации окрашенного вещества и толщины слоя раствора определяется объединенным законом Бугера-Ламберта-Бера, который является основным законом светопоглощения и лежит в основе большинства фотометрических методов анализа: I = I 0 *10−ελCl , где ε – молярный коэффициент светопоглощения при длине λ, С – молярная концентрация, L – толщина поглощающего слоя I 0 – интенсивность падающего света.
 При соблюдении основного закона светопоглощения оптическая плотность раствора прямо пропорциональна молярному коэффициенту светопоглощения, концентрации поглощающего вещества и толщине слоя раствора: D = lg(I 0/I) =ελСl При графическом изображении зависимости оптической плотности от концентрации (при постоянном значении l) получается прямая линия. Эта прямая проходит через начало координат при отсутствии поглощения света растворителем и систематических погрешностей.
При соблюдении основного закона светопоглощения оптическая плотность раствора прямо пропорциональна молярному коэффициенту светопоглощения, концентрации поглощающего вещества и толщине слоя раствора: D = lg(I 0/I) =ελСl При графическом изображении зависимости оптической плотности от концентрации (при постоянном значении l) получается прямая линия. Эта прямая проходит через начало координат при отсутствии поглощения света растворителем и систематических погрешностей.
 УСЛОВИЯ СОБЛЮДЕНИЯ ЗАКОНА БУГЕРА-ЛАМБЕРТА-БЕРА 1 усл. Свет должен быть монохроматическим, т. е. с определенной длиной волны Dλ = ελl. Cx ; 2 усл. Концентрация поглощающего вещества < 10 -2 моль/л; 3 усл. Устранить влияние других поглощающих свет веществ (так как D – неселективный аналитический сигнал);
УСЛОВИЯ СОБЛЮДЕНИЯ ЗАКОНА БУГЕРА-ЛАМБЕРТА-БЕРА 1 усл. Свет должен быть монохроматическим, т. е. с определенной длиной волны Dλ = ελl. Cx ; 2 усл. Концентрация поглощающего вещества < 10 -2 моль/л; 3 усл. Устранить влияние других поглощающих свет веществ (так как D – неселективный аналитический сигнал);
 4 усл Должна существовать только одна поглощающая свет форма (в неё и нужно количественно переводить определяемый компонент); 5 усл Измерение оптической плотности проводят с использованием двух одинаковых кювет. Измеряют световой поток прошедший через раствор сравнения и анализируемый раствор.
4 усл Должна существовать только одна поглощающая свет форма (в неё и нужно количественно переводить определяемый компонент); 5 усл Измерение оптической плотности проводят с использованием двух одинаковых кювет. Измеряют световой поток прошедший через раствор сравнения и анализируемый раствор.
 Фотометрические методы определения концентрации вещества в растворе Фотометрические методы определения концентрации растворов основаны на сравнении поглощения при пропускании света стандартными и исследуемыми растворами. Степень поглощения света фотометрируемым раствором измеряют с помощью фотоколориметров и спектрофотометров. Измерение оптической плотности стандартного и исследуемого окрашенных растворов всегда производят по отношению к раствору сравнения (нулевому (контрольному) раствору).
Фотометрические методы определения концентрации вещества в растворе Фотометрические методы определения концентрации растворов основаны на сравнении поглощения при пропускании света стандартными и исследуемыми растворами. Степень поглощения света фотометрируемым раствором измеряют с помощью фотоколориметров и спектрофотометров. Измерение оптической плотности стандартного и исследуемого окрашенных растворов всегда производят по отношению к раствору сравнения (нулевому (контрольному) раствору).
 В качестве раствора сравнения можно использовать: Ø аликвотную часть исследуемого раствора, содержащего все добавленные компоненты, кроме реагента, образующего с определяемым веществом окрашенное соединение; Ø дистиллированную воду.
В качестве раствора сравнения можно использовать: Ø аликвотную часть исследуемого раствора, содержащего все добавленные компоненты, кроме реагента, образующего с определяемым веществом окрашенное соединение; Ø дистиллированную воду.
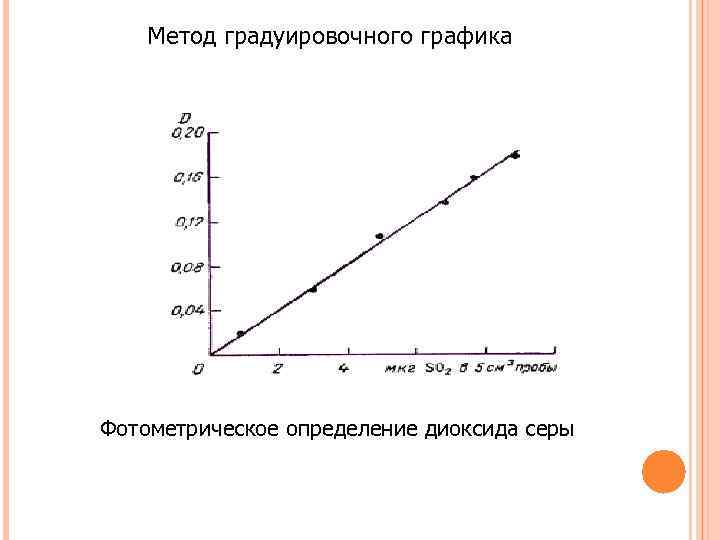 Метод градуировочного графика Фотометрическое определение диоксида серы
Метод градуировочного графика Фотометрическое определение диоксида серы
 Метод сравнения оптических плотностей стандартного и исследуемого растворов D
Метод сравнения оптических плотностей стандартного и исследуемого растворов D
 Принципиальная оптическая схема фотоэлектроколориметра (ФЭК) В фотоэлектроколориметрах приёмником световой энергии является прибор – фотоэлемент. В этом приборе световая энергия преобразует в электрическую. Фотоэлементы позволяют проводить колориметрические определения не только в видимой, но также в УФ- и ИКобластях спектра. Измерение световых потоков с помощью фотоэлектрических фотометров более точно и не зависит от особенностей глаза наблюдателя. Применение фотоэлементов позволяет автоматизировать определение концентрации веществ в химическом контроле технологических процессов. Вследствие этого фотоэлектрическая колориметрия значительно шире используется в практике заводских лабораторий, чем визуальная.
Принципиальная оптическая схема фотоэлектроколориметра (ФЭК) В фотоэлектроколориметрах приёмником световой энергии является прибор – фотоэлемент. В этом приборе световая энергия преобразует в электрическую. Фотоэлементы позволяют проводить колориметрические определения не только в видимой, но также в УФ- и ИКобластях спектра. Измерение световых потоков с помощью фотоэлектрических фотометров более точно и не зависит от особенностей глаза наблюдателя. Применение фотоэлементов позволяет автоматизировать определение концентрации веществ в химическом контроле технологических процессов. Вследствие этого фотоэлектрическая колориметрия значительно шире используется в практике заводских лабораторий, чем визуальная.
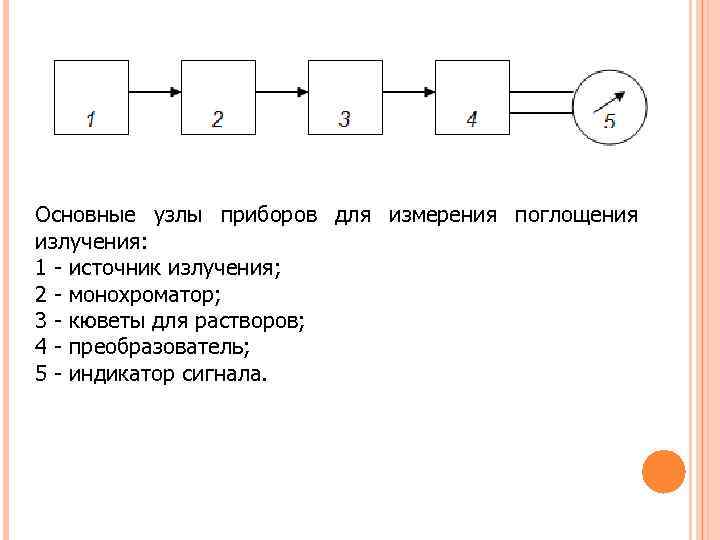 Основные узлы приборов для измерения поглощения излучения: 1 - источник излучения; 2 - монохроматор; 3 - кюветы для растворов; 4 - преобразователь; 5 - индикатор сигнала.
Основные узлы приборов для измерения поглощения излучения: 1 - источник излучения; 2 - монохроматор; 3 - кюветы для растворов; 4 - преобразователь; 5 - индикатор сигнала.
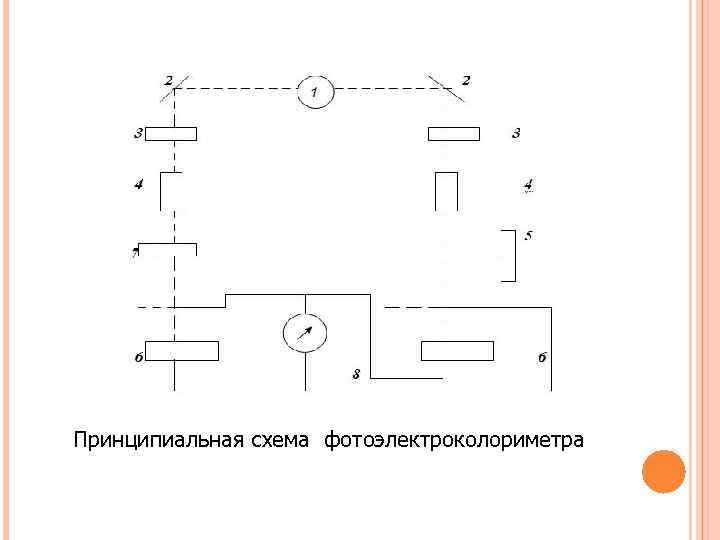 Принципиальная схема фотоэлектроколориметра
Принципиальная схема фотоэлектроколориметра
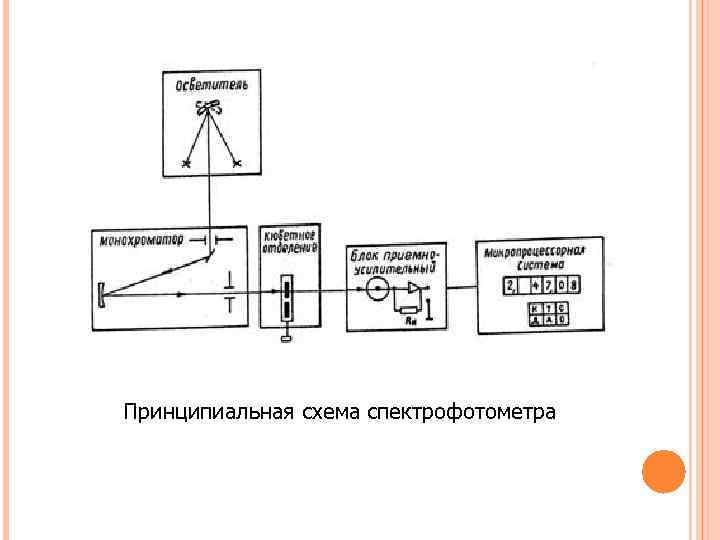 Принципиальная схема спектрофотометра
Принципиальная схема спектрофотометра
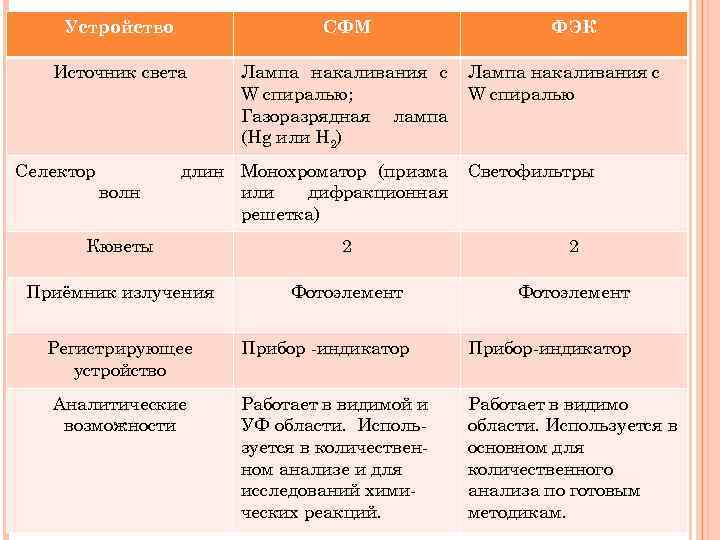 Устройство СФМ Источник света Лампа накаливания с W спиралью; Газоразрядная лампа (Hg или H 2) Селектор волн длин Монохроматор (призма или дифракционная решетка) ФЭК Лампа накаливания с W спиралью Светофильтры Кюветы 2 2 Приёмник излучения Фотоэлемент Регистрирующее устройство Аналитические возможности Прибор -индикатор Прибор-индикатор Работает в видимой и УФ области. Используется в количественном анализе и для исследований химических реакций. Работает в видимо области. Используется в основном для количественного анализа по готовым методикам.
Устройство СФМ Источник света Лампа накаливания с W спиралью; Газоразрядная лампа (Hg или H 2) Селектор волн длин Монохроматор (призма или дифракционная решетка) ФЭК Лампа накаливания с W спиралью Светофильтры Кюветы 2 2 Приёмник излучения Фотоэлемент Регистрирующее устройство Аналитические возможности Прибор -индикатор Прибор-индикатор Работает в видимой и УФ области. Используется в количественном анализе и для исследований химических реакций. Работает в видимо области. Используется в основном для количественного анализа по готовым методикам.
 Спектрофотометрические методы, по сравнению с фотоколориметрическими, позволяют решать более широкий круг задач: Ø проводить количественное определение веществ в широком интервал длин волн (185 -1100 нм); Ø осуществлять количественный анализ многокомпонентных систем (одновременное определение нескольких веществ); Ø определять состав и константы устойчивости светопоглощающих комплексных соединений; Ø определять фотометрические характеристики светопоглощающих соединений.
Спектрофотометрические методы, по сравнению с фотоколориметрическими, позволяют решать более широкий круг задач: Ø проводить количественное определение веществ в широком интервал длин волн (185 -1100 нм); Ø осуществлять количественный анализ многокомпонентных систем (одновременное определение нескольких веществ); Ø определять состав и константы устойчивости светопоглощающих комплексных соединений; Ø определять фотометрические характеристики светопоглощающих соединений.
 Фотометрические методы анализа являются универсальными методами по определяемым веществам. Если определяемое вещество само неспособно к поглощению света, то предварительно проводится фотометрическая реакция, в результате которой образуется соединение поглощающее свет. Для определения Kt+ металлов использую реакции с переносом заряда, или же реакции с фотометрическими органическими реагентами содержащими хромофорные группы.
Фотометрические методы анализа являются универсальными методами по определяемым веществам. Если определяемое вещество само неспособно к поглощению света, то предварительно проводится фотометрическая реакция, в результате которой образуется соединение поглощающее свет. Для определения Kt+ металлов использую реакции с переносом заряда, или же реакции с фотометрическими органическими реагентами содержащими хромофорные группы.
 Возможности данных методов: Dmin = 0, 01 Сmin = 10 -7 – 10 -2 моль/л
Возможности данных методов: Dmin = 0, 01 Сmin = 10 -7 – 10 -2 моль/л
 Задача При фотоколориметрическом определении Fe 3+ с сульфосалициловой кислотой из стандартного раствора с содержанием железа 10 мг/см 3 приготовили ряд разведений в мерных колбах вместимостью 100 см 3, измерили оптическое поглощение и получили следующие данные: Vст, см 3 А 1, 0 2, 0 3, 0 4, 0 5, 0 6, 0 0, 12 0, 25 0, 37 0, 50 0, 62 0, 75 Определите концентрацию Fе 3+ в анализируемых растворах, если их оптическое поглощение равно 0, 30 и 0, 50.
Задача При фотоколориметрическом определении Fe 3+ с сульфосалициловой кислотой из стандартного раствора с содержанием железа 10 мг/см 3 приготовили ряд разведений в мерных колбах вместимостью 100 см 3, измерили оптическое поглощение и получили следующие данные: Vст, см 3 А 1, 0 2, 0 3, 0 4, 0 5, 0 6, 0 0, 12 0, 25 0, 37 0, 50 0, 62 0, 75 Определите концентрацию Fе 3+ в анализируемых растворах, если их оптическое поглощение равно 0, 30 и 0, 50.
 Решение. Строим калибровочный график для стандартного раствора и находим концентрацию при оптическом поглощении 0, 30 и 0, 50. Она равна 24 и 40 мг/100 см 3 соответственно. Ответ: 24, 0 и 40, 0 мг/100 см 3
Решение. Строим калибровочный график для стандартного раствора и находим концентрацию при оптическом поглощении 0, 30 и 0, 50. Она равна 24 и 40 мг/100 см 3 соответственно. Ответ: 24, 0 и 40, 0 мг/100 см 3


