Тема 2.1.3. Главная подгруппа V группы.Фосфор.ppt
- Количество слайдов: 19
 Фосфор
Фосфор
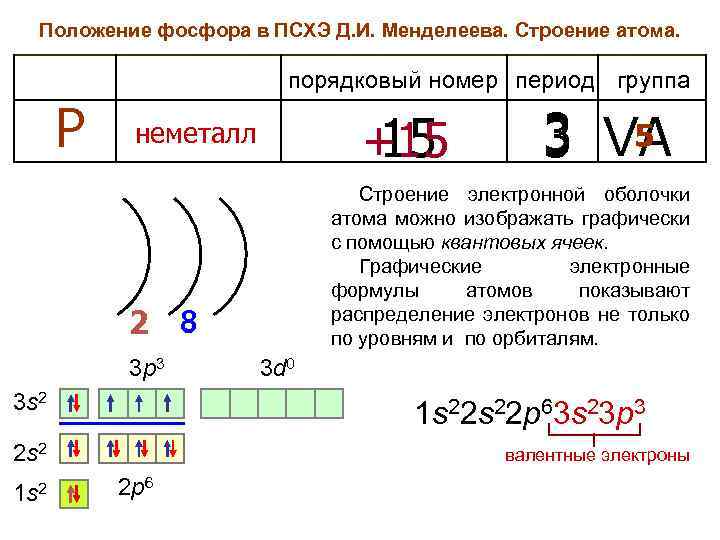 Положение фосфора в ПСХЭ Д. И. Менделеева. Строение атома. порядковый номер период группа Р +15 15 неметалл Строение электронной оболочки атома можно изображать графически с помощью квантовых ячеек. Графические электронные формулы атомов показывают распределение электронов не только по уровням и по орбиталям. 2 8 3 p 3 3 s 2 3 d 0 1 s 22 p 63 s 23 p 3 2 s 2 1 s 2 5 3 VA валентные электроны 2 p 6
Положение фосфора в ПСХЭ Д. И. Менделеева. Строение атома. порядковый номер период группа Р +15 15 неметалл Строение электронной оболочки атома можно изображать графически с помощью квантовых ячеек. Графические электронные формулы атомов показывают распределение электронов не только по уровням и по орбиталям. 2 8 3 p 3 3 s 2 3 d 0 1 s 22 p 63 s 23 p 3 2 s 2 1 s 2 5 3 VA валентные электроны 2 p 6
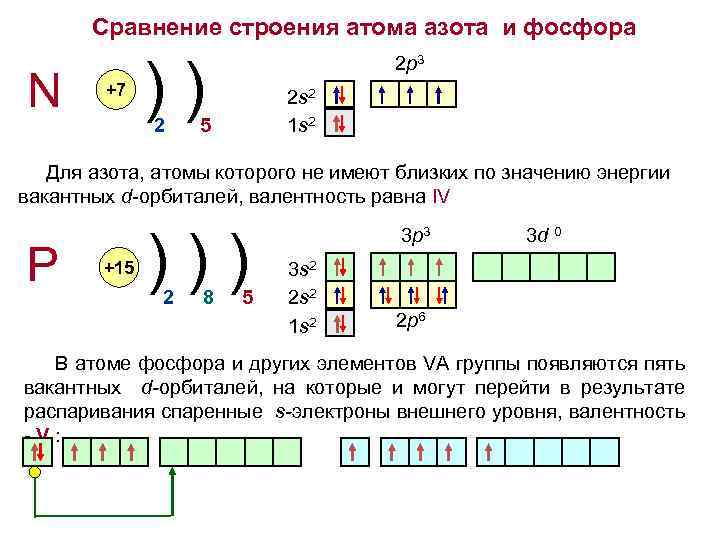 Сравнение строения атома азота и фосфора N +7 )) 2 2 p 3 2 s 2 1 s 2 5 Для азота, атомы которого не имеют близких по значению энергии вакантных d-орбиталей, валентность равна IV P +15 ))) 2 8 5 3 p 3 3 s 2 2 s 2 1 s 2 3 d 0 2 p 6 В атоме фосфора и других элементов VA группы появляются пять вакантных d-орбиталей, на которые и могут перейти в результате распаривания спаренные s-электроны внешнего уровня, валентность -V:
Сравнение строения атома азота и фосфора N +7 )) 2 2 p 3 2 s 2 1 s 2 5 Для азота, атомы которого не имеют близких по значению энергии вакантных d-орбиталей, валентность равна IV P +15 ))) 2 8 5 3 p 3 3 s 2 2 s 2 1 s 2 3 d 0 2 p 6 В атоме фосфора и других элементов VA группы появляются пять вакантных d-орбиталей, на которые и могут перейти в результате распаривания спаренные s-электроны внешнего уровня, валентность -V:
 Нахождение в природе Содержание фосфора в земной коре составляет 0, 093%. В природе фосфор встречается только в виде соединений, главным образом апатитов, фосфоритов.
Нахождение в природе Содержание фосфора в земной коре составляет 0, 093%. В природе фосфор встречается только в виде соединений, главным образом апатитов, фосфоритов.
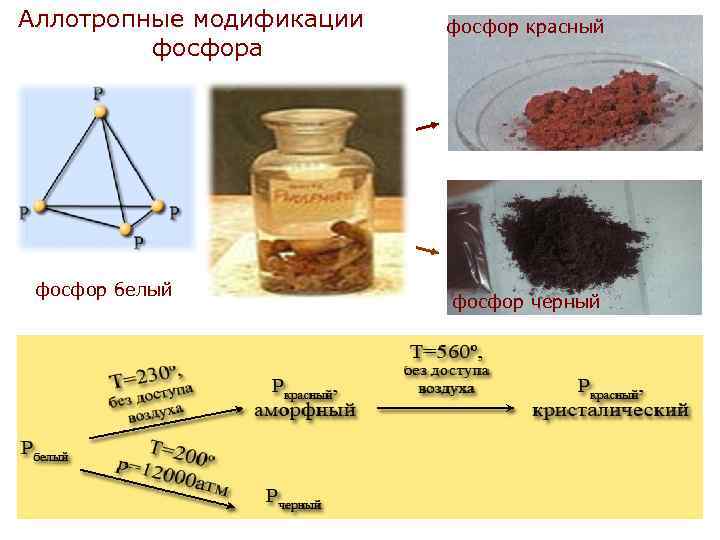 Аллотропные модификации фосфора фосфор белый фосфор красный фосфор черный
Аллотропные модификации фосфора фосфор белый фосфор красный фосфор черный
 • Белый фосфор - твердое кристаллическое вещество. На воздухе самовоспламеняется, в темноте светится. Получают быстрым охлаждением паров фосфора. Очень ядовит! • Красный фосфор - порошок темно-красного цвета. Получают длительным нагреванием белого фосфора без доступа воздуха при температуре 250 -300°С. Не ядовит. • Черный фосфор - твердое вещество, плотность его 2, 7 г/см 3. Образуется при нагревании белого фосфора при температуре 200 °С под высоким давлением. Используется в производстве спичек, снарядов и т. д.
• Белый фосфор - твердое кристаллическое вещество. На воздухе самовоспламеняется, в темноте светится. Получают быстрым охлаждением паров фосфора. Очень ядовит! • Красный фосфор - порошок темно-красного цвета. Получают длительным нагреванием белого фосфора без доступа воздуха при температуре 250 -300°С. Не ядовит. • Черный фосфор - твердое вещество, плотность его 2, 7 г/см 3. Образуется при нагревании белого фосфора при температуре 200 °С под высоким давлением. Используется в производстве спичек, снарядов и т. д.
 Превращение красного фосфора в белый • https: //www. youtube. com/watch? v=4 VPG 9 gv 08 g. Q • https: //www. youtube. com/watch? time_continue=102&v=f. KF Uvu. DI 26 g
Превращение красного фосфора в белый • https: //www. youtube. com/watch? v=4 VPG 9 gv 08 g. Q • https: //www. youtube. com/watch? time_continue=102&v=f. KF Uvu. DI 26 g
 Свечение белого фосфора • https: //www. youtube. com/watch? v=3 sl. QHDu. QVb. Q
Свечение белого фосфора • https: //www. youtube. com/watch? v=3 sl. QHDu. QVb. Q
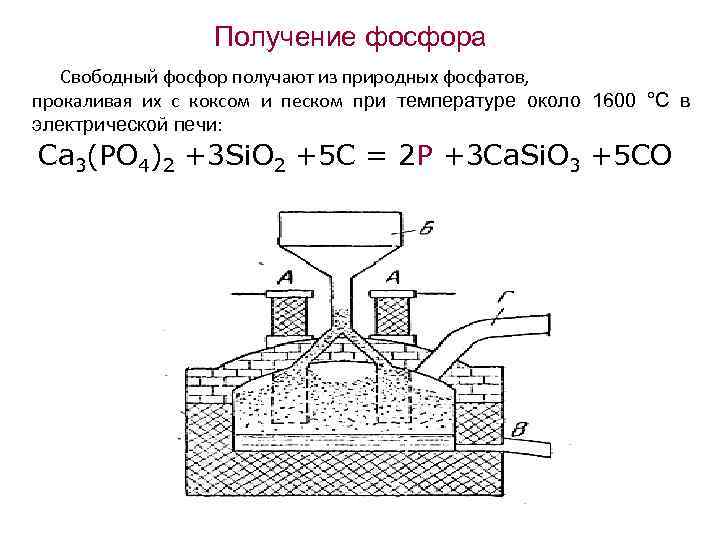 Получение фосфора Свободный фосфор получают из природных фосфатов, прокаливая их с коксом и песком при температуре около 1600 °С в электрической печи: Ca 3(PO 4)2 +3 Si. O 2 +5 C = 2 P +3 Ca. Si. O 3 +5 CO
Получение фосфора Свободный фосфор получают из природных фосфатов, прокаливая их с коксом и песком при температуре около 1600 °С в электрической печи: Ca 3(PO 4)2 +3 Si. O 2 +5 C = 2 P +3 Ca. Si. O 3 +5 CO
 Химические свойства фосфора P 0 восстановитель окислитель P + O 2 (S, Cl 2) P + Ме P+5 (P+3) P– 3 I. Взаимодействие фосфора с неметаллами 1) с кислородом 2) с серой 3) с хлором II. Взаимодействие фосфора с металлами III. Взаимодействие фосфора со сложными веществами
Химические свойства фосфора P 0 восстановитель окислитель P + O 2 (S, Cl 2) P + Ме P+5 (P+3) P– 3 I. Взаимодействие фосфора с неметаллами 1) с кислородом 2) с серой 3) с хлором II. Взаимодействие фосфора с металлами III. Взаимодействие фосфора со сложными веществами
 I. Взаимодействие фосфора с неметаллами Взаимодействие фосфора с кислородом 4 P 0 + 5 O 20 = 2 P 2+5 O 5– 2 При окислении фосфора в недостатке кислорода образуется 4 P 0 +3 O 20 =2 P 2+3 O 3– 2 Р 2 О 3
I. Взаимодействие фосфора с неметаллами Взаимодействие фосфора с кислородом 4 P 0 + 5 O 20 = 2 P 2+5 O 5– 2 При окислении фосфора в недостатке кислорода образуется 4 P 0 +3 O 20 =2 P 2+3 O 3– 2 Р 2 О 3
 Горение красного фосфора • https: //www. youtube. com/watch? time_conti nue=95&v=Uo 25 TO_Qt. Rc
Горение красного фосфора • https: //www. youtube. com/watch? time_conti nue=95&v=Uo 25 TO_Qt. Rc
 Так же, как с кислородом, фосфор реагирует и с другим халькогеном – серой: 4 P 0 + 3 S 0 = 2 P 2+3 S 3– 2 4 P 0 + 5 S 0 = 2 P 2+5 S 5– 2
Так же, как с кислородом, фосфор реагирует и с другим халькогеном – серой: 4 P 0 + 3 S 0 = 2 P 2+3 S 3– 2 4 P 0 + 5 S 0 = 2 P 2+5 S 5– 2
 Горение фосфора в хлоре 2 P 0 + 3 Cl 20 = 2 P+3 Cl 3– 1 При пропускании хлора через трубку с красным фосфором в приемнике собирается бесцветная жидкость – хлорид фосфора (III). 2 P 0 + 5 Cl 20 = 2 P+5 Cl 5– 1 В избытке хлора фосфор сгорает бледно-зеленым пламенем с образованием хлорида фосфора (V), которые при охлаждении конденсируются в светло-желтые кристаллы. https: //www. youtube. com/watch? v=z 1 Je. GYn. Kz. Yo
Горение фосфора в хлоре 2 P 0 + 3 Cl 20 = 2 P+3 Cl 3– 1 При пропускании хлора через трубку с красным фосфором в приемнике собирается бесцветная жидкость – хлорид фосфора (III). 2 P 0 + 5 Cl 20 = 2 P+5 Cl 5– 1 В избытке хлора фосфор сгорает бледно-зеленым пламенем с образованием хлорида фосфора (V), которые при охлаждении конденсируются в светло-желтые кристаллы. https: //www. youtube. com/watch? v=z 1 Je. GYn. Kz. Yo
 III. Взаимодействие фосфора с металлами Взаимодействие фосфора с кальцием 2 P 0 + 3 Ca 0 = Ca 3+2 P 2– 3 фосфид кальция https: //www. youtube. com/watch? v=5 lw. UXYlghxs Фосфиды энергично разлагаются водой с выделением фосфина. Фосфин очень ядовитый газ с чесночным запахом. Ca 3 P 2 + 6 H 2 O = 3 Ca(OH)2 + ↑ 2 PH 3
III. Взаимодействие фосфора с металлами Взаимодействие фосфора с кальцием 2 P 0 + 3 Ca 0 = Ca 3+2 P 2– 3 фосфид кальция https: //www. youtube. com/watch? v=5 lw. UXYlghxs Фосфиды энергично разлагаются водой с выделением фосфина. Фосфин очень ядовитый газ с чесночным запахом. Ca 3 P 2 + 6 H 2 O = 3 Ca(OH)2 + ↑ 2 PH 3
 III. Взаимодействие фосфора со сложными веществами: 1. С концентрированными кислотами (азотной и серной); P + 5 HNO 3 = H 3 PO 4 + 5 NO 2 + H 2 O https: //www. youtube. com/watch? time_continue=13&v=GVtc. BNp. FJp. M 2 P + 5 H 2 SO 4= 2 H 3 PO 4 + 5 SO 2 + 2 H 2 O 2. Раствором щелочи; 4 P + 3 Na. OH + 3 H 2 O = PH 3 + 3 Na. H 2 PO 2 3. Хлоратом калия. 6 P + 5 KCl. O 3 = 5 KCl + 3 P 2 O 5 бертолетова соль (хлорат калия)
III. Взаимодействие фосфора со сложными веществами: 1. С концентрированными кислотами (азотной и серной); P + 5 HNO 3 = H 3 PO 4 + 5 NO 2 + H 2 O https: //www. youtube. com/watch? time_continue=13&v=GVtc. BNp. FJp. M 2 P + 5 H 2 SO 4= 2 H 3 PO 4 + 5 SO 2 + 2 H 2 O 2. Раствором щелочи; 4 P + 3 Na. OH + 3 H 2 O = PH 3 + 3 Na. H 2 PO 2 3. Хлоратом калия. 6 P + 5 KCl. O 3 = 5 KCl + 3 P 2 O 5 бертолетова соль (хлорат калия)
 Применение фосфора 1 Белый фосфор применяется для получения красного фосфора 2 Фосфор применяется для получения фосфорных кислот и их производных. 3 Основная область применения красного фосфора – производство спичек 4 Фосфор применяется как раскислитель и компонент некоторых металлических сплавов 5 Производство лекарственных препаратов 6 Средства борьбы с вредителями сельского хозяйства 7 Производство моющих средств 8 Органический синтез 9 Р 2 О 5 как осушитель газов и жидкостей
Применение фосфора 1 Белый фосфор применяется для получения красного фосфора 2 Фосфор применяется для получения фосфорных кислот и их производных. 3 Основная область применения красного фосфора – производство спичек 4 Фосфор применяется как раскислитель и компонент некоторых металлических сплавов 5 Производство лекарственных препаратов 6 Средства борьбы с вредителями сельского хозяйства 7 Производство моющих средств 8 Органический синтез 9 Р 2 О 5 как осушитель газов и жидкостей
 1. В каком из перечисленных соединений степень окисления фосфора В +3 А) Р 2 О 5; Б) Na. PO 3; В) PCl 3 2. В какой из приведенных пар оба вещества взаимодействуют с фосфором: Б А) кальций и соляная кислота; Б) натрий и хлор; В) кислород и соляная кислота. 3. Составьте уравнение реакции фосфора с кальцием. Коэффициент перед формулой окислителя: А) 2; Б) 3); В) 1. А 4. Как хранят красный фосфор в лаборатории: А) под слоем воды; Б) под слоем керосина; В) в обычных условиях. В 5. Фосфор образует простое вещество с молекулярной кристаллической решеткой, в узлах которой находятся молекулы Р 4. какой цвет имеет такой фосфор: Б А) красный; Б) желтый; В) зеленый. 6. Степень окисления фосфора увеличивается в ряду: А) PH 3, P 2 O 3, H 3 PO 4; Б) Na 3 PO 4, P 2 O 5, HPO 3; В) Ca 3 P 2, PH 3, Na. PO 3 А 7. Какое из утверждений неверно: «Атом фосфора по сравнению с атомом азота имеет» : В А) больший радиус; Б) больший заряд ядра; В) более ярко выраженные неметаллические свойства.
1. В каком из перечисленных соединений степень окисления фосфора В +3 А) Р 2 О 5; Б) Na. PO 3; В) PCl 3 2. В какой из приведенных пар оба вещества взаимодействуют с фосфором: Б А) кальций и соляная кислота; Б) натрий и хлор; В) кислород и соляная кислота. 3. Составьте уравнение реакции фосфора с кальцием. Коэффициент перед формулой окислителя: А) 2; Б) 3); В) 1. А 4. Как хранят красный фосфор в лаборатории: А) под слоем воды; Б) под слоем керосина; В) в обычных условиях. В 5. Фосфор образует простое вещество с молекулярной кристаллической решеткой, в узлах которой находятся молекулы Р 4. какой цвет имеет такой фосфор: Б А) красный; Б) желтый; В) зеленый. 6. Степень окисления фосфора увеличивается в ряду: А) PH 3, P 2 O 3, H 3 PO 4; Б) Na 3 PO 4, P 2 O 5, HPO 3; В) Ca 3 P 2, PH 3, Na. PO 3 А 7. Какое из утверждений неверно: «Атом фосфора по сравнению с атомом азота имеет» : В А) больший радиус; Б) больший заряд ядра; В) более ярко выраженные неметаллические свойства.
 Фосфор был открыт немецким алхимиком X. Брэндом в 1669 г. Позже А. Лавуазье доказал, что фосфор самостоятельный химический элемент. Ж. Пруст и М. Клапорт установили его широкое распространение в земной коре, в основном в виде фосфата кальция.
Фосфор был открыт немецким алхимиком X. Брэндом в 1669 г. Позже А. Лавуазье доказал, что фосфор самостоятельный химический элемент. Ж. Пруст и М. Клапорт установили его широкое распространение в земной коре, в основном в виде фосфата кальция.


