6-2014. Субстратные циклы, обратные связи.pptx
- Количество слайдов: 28
 Фосфатазы
Фосфатазы
 Соотношение киназ и фосфатаз Киназы Фосфатазы (~520) (~140) Sir Philip Cohen Tyr (РТК) Shi Y (2009) Cell 139: 468 -484 (428) Tyr (РТР) Ser/Thr (РSР) ≈ РТК (90) Ser/Thr (РSK) << РТК (107) (30)
Соотношение киназ и фосфатаз Киназы Фосфатазы (~520) (~140) Sir Philip Cohen Tyr (РТК) Shi Y (2009) Cell 139: 468 -484 (428) Tyr (РТР) Ser/Thr (РSР) ≈ РТК (90) Ser/Thr (РSK) << РТК (107) (30)
 Фосфорилирование – основной инструмент регуляции The story of protein phosphatases, and of protein phosphorylation as a regulatory mechanism, can be traced back to research conducted in the 1930 s and 1940 s, referred to in those early days as ‘mechanisms of hormone action’, which was later called ‘signal transduction’, eventually becoming known as ‘cell signalling’. The basic issue was to understand how blood glucose is regulated by hormones. Gerty (Radnitz) & Carl Cori Nobel Prize 1947 Brautigan DL (2013) Febs J 280: 324 -5
Фосфорилирование – основной инструмент регуляции The story of protein phosphatases, and of protein phosphorylation as a regulatory mechanism, can be traced back to research conducted in the 1930 s and 1940 s, referred to in those early days as ‘mechanisms of hormone action’, which was later called ‘signal transduction’, eventually becoming known as ‘cell signalling’. The basic issue was to understand how blood glucose is regulated by hormones. Gerty (Radnitz) & Carl Cori Nobel Prize 1947 Brautigan DL (2013) Febs J 280: 324 -5
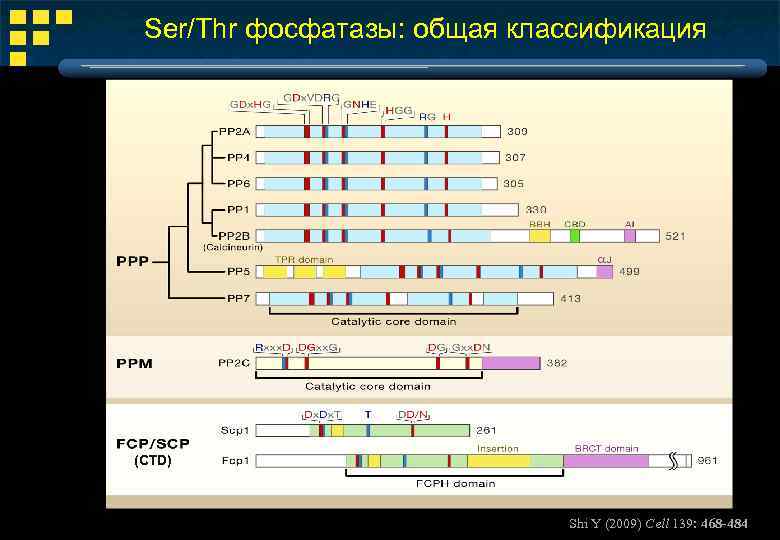 Ser/Thr фосфатазы: общая классификация (CTD) Shi Y (2009) Cell 139: 468 -484
Ser/Thr фосфатазы: общая классификация (CTD) Shi Y (2009) Cell 139: 468 -484
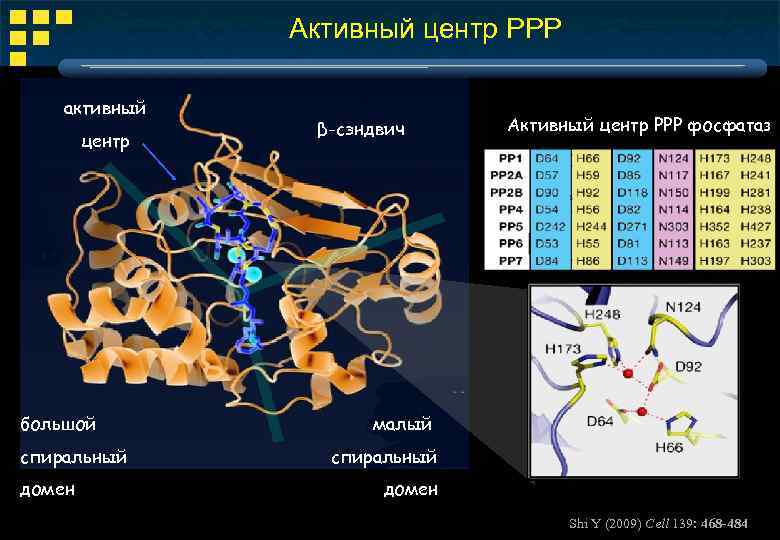 Активный центр РРР активный центр большой спиральный домен β-сэндвич Активный центр РРР фосфатаз малый спиральный домен Shi Y (2009) Cell 139: 468 -484
Активный центр РРР активный центр большой спиральный домен β-сэндвич Активный центр РРР фосфатаз малый спиральный домен Shi Y (2009) Cell 139: 468 -484
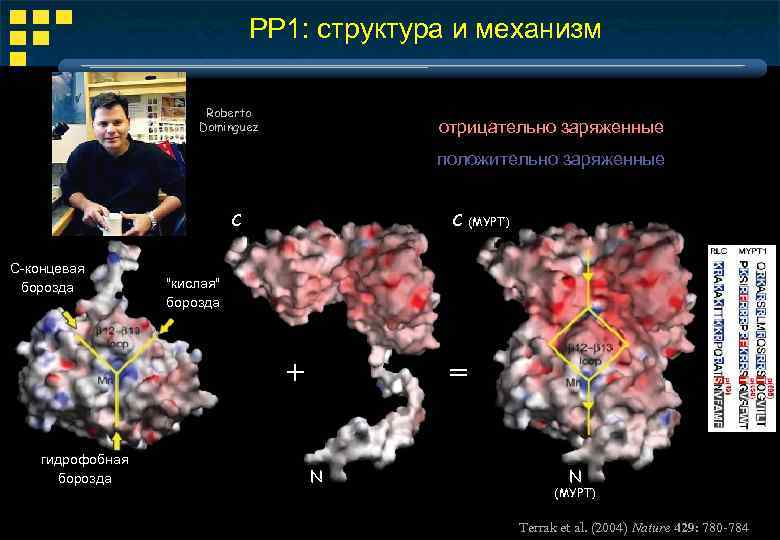 РР 1: структура и механизм Roberto Dominguez отрицательно заряженные положительно заряженные C С-концевая борозда С (MYPT) "кислая" борозда + гидрофобная борозда = N N (MYPT) Terrak et al. (2004) Nature 429: 780 -784
РР 1: структура и механизм Roberto Dominguez отрицательно заряженные положительно заряженные C С-концевая борозда С (MYPT) "кислая" борозда + гидрофобная борозда = N N (MYPT) Terrak et al. (2004) Nature 429: 780 -784
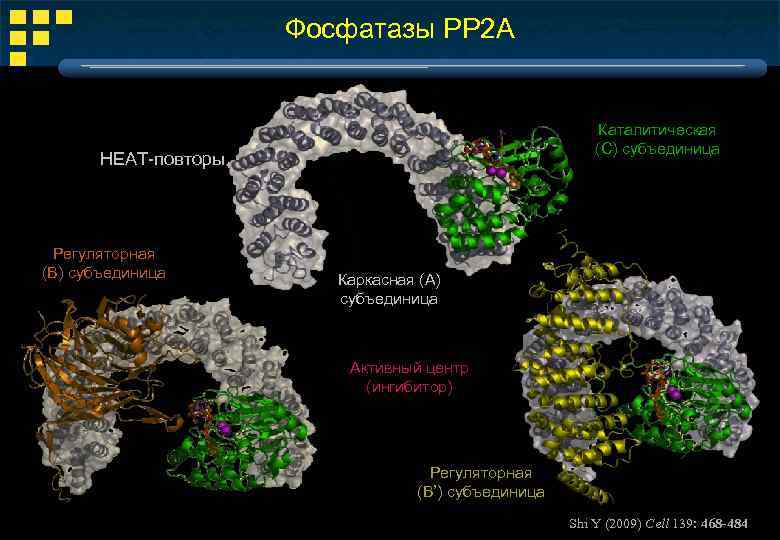 Фосфатазы РР 2 А Каталитическая (С) субъединица HEAT-повторы Регуляторная (В) субъединица Каркасная (А) субъединица Активный центр (ингибитор) Регуляторная (В’) субъединица Shi Y (2009) Cell 139: 468 -484
Фосфатазы РР 2 А Каталитическая (С) субъединица HEAT-повторы Регуляторная (В) субъединица Каркасная (А) субъединица Активный центр (ингибитор) Регуляторная (В’) субъединица Shi Y (2009) Cell 139: 468 -484
 Регуляция
Регуляция
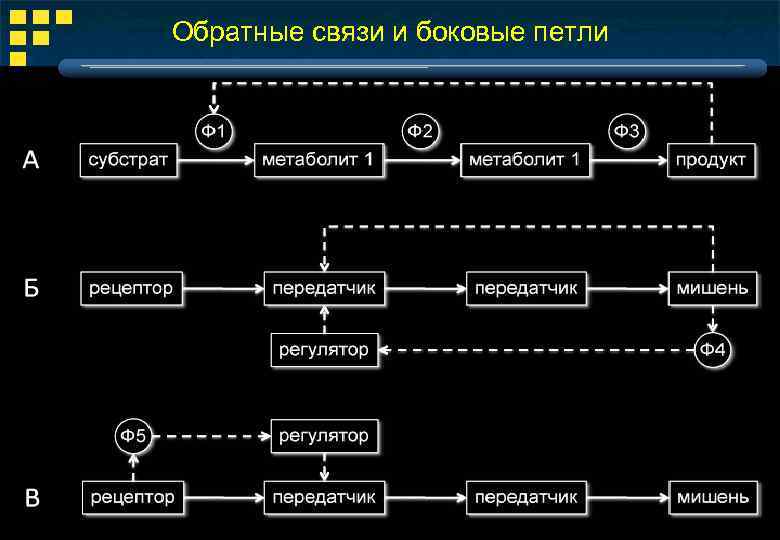 Обратные связи и боковые петли
Обратные связи и боковые петли
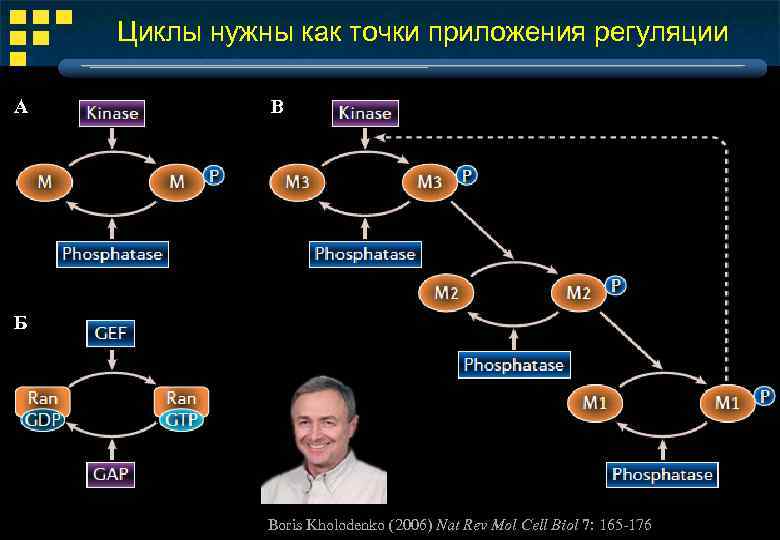 Циклы нужны как точки приложения регуляции А В Б Boris Kholodenko (2006) Nat Rev Mol Cell Biol 7: 165 -176
Циклы нужны как точки приложения регуляции А В Б Boris Kholodenko (2006) Nat Rev Mol Cell Biol 7: 165 -176
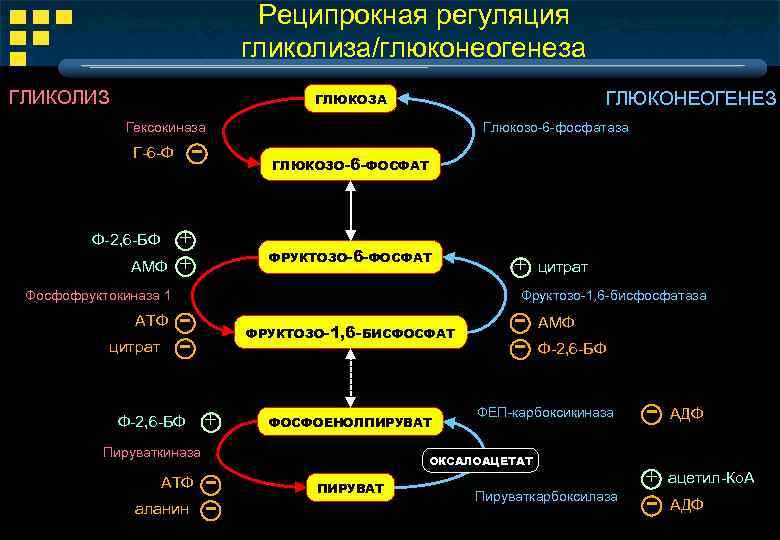 Реципрокная регуляция гликолиза/глюконеогенеза ГЛИКОЛИЗ ГЛЮКОНЕОГЕНЕЗ ГЛЮКОЗА Гексокиназа - Г-6 -Ф Ф-2, 6 -БФ АМФ Фосфофруктокиназа 1 АТФ цитрат ГЛЮКОЗО-6 -ФОСФАТ + + ФРУКТОЗО-6 -ФОСФАТ Пируваткиназа АТФ аланин + цитрат Фруктозо-1, 6 -бисфосфатаза - Ф-2, 6 -БФ Глюкозо-6 -фосфатаза ФРУКТОЗО-1, 6 -БИСФОСФАТ + - ФОСФОЕНОЛПИРУВАТ - АМФ Ф-2, 6 -БФ ФЕП-карбоксикиназа ОКСАЛОАЦЕТАТ ПИРУВАТ Пируваткарбоксилаза - АДФ + ацетил-Ко. А - АДФ
Реципрокная регуляция гликолиза/глюконеогенеза ГЛИКОЛИЗ ГЛЮКОНЕОГЕНЕЗ ГЛЮКОЗА Гексокиназа - Г-6 -Ф Ф-2, 6 -БФ АМФ Фосфофруктокиназа 1 АТФ цитрат ГЛЮКОЗО-6 -ФОСФАТ + + ФРУКТОЗО-6 -ФОСФАТ Пируваткиназа АТФ аланин + цитрат Фруктозо-1, 6 -бисфосфатаза - Ф-2, 6 -БФ Глюкозо-6 -фосфатаза ФРУКТОЗО-1, 6 -БИСФОСФАТ + - ФОСФОЕНОЛПИРУВАТ - АМФ Ф-2, 6 -БФ ФЕП-карбоксикиназа ОКСАЛОАЦЕТАТ ПИРУВАТ Пируваткарбоксилаза - АДФ + ацетил-Ко. А - АДФ
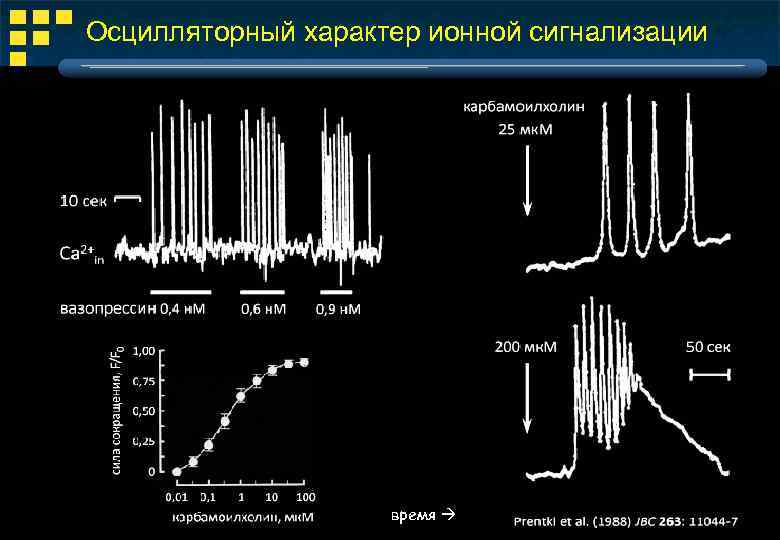 Осцилляторный характер ионной сигнализации время
Осцилляторный характер ионной сигнализации время
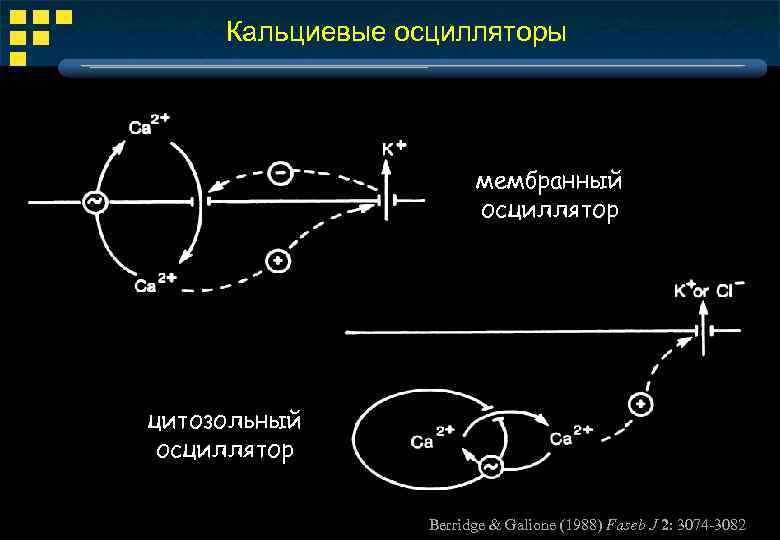 Кальциевые осцилляторы мембранный осциллятор цитозольный осциллятор Berridge & Galione (1988) Faseb J 2: 3074 -3082
Кальциевые осцилляторы мембранный осциллятор цитозольный осциллятор Berridge & Galione (1988) Faseb J 2: 3074 -3082
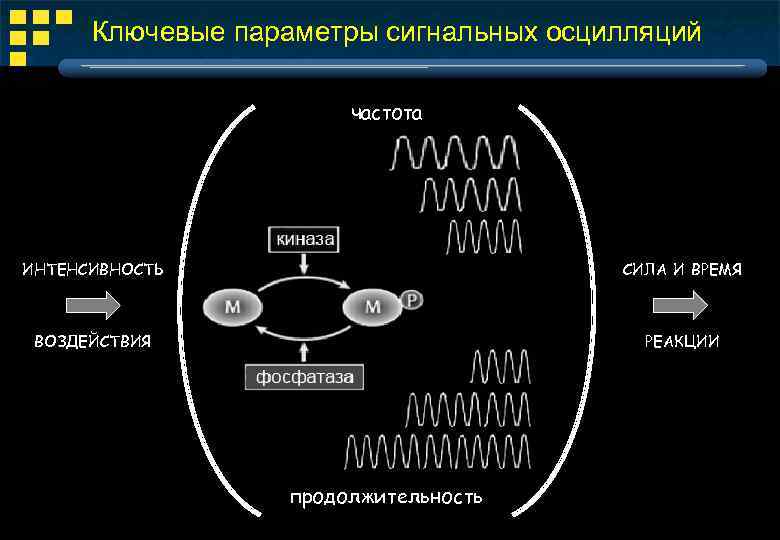 Ключевые параметры сигнальных осцилляций частота ИНТЕНСИВНОСТЬ СИЛА И ВРЕМЯ ВОЗДЕЙСТВИЯ РЕАКЦИИ продолжительность
Ключевые параметры сигнальных осцилляций частота ИНТЕНСИВНОСТЬ СИЛА И ВРЕМЯ ВОЗДЕЙСТВИЯ РЕАКЦИИ продолжительность
 Моделирование Бистабильный включатель Осциллятор
Моделирование Бистабильный включатель Осциллятор
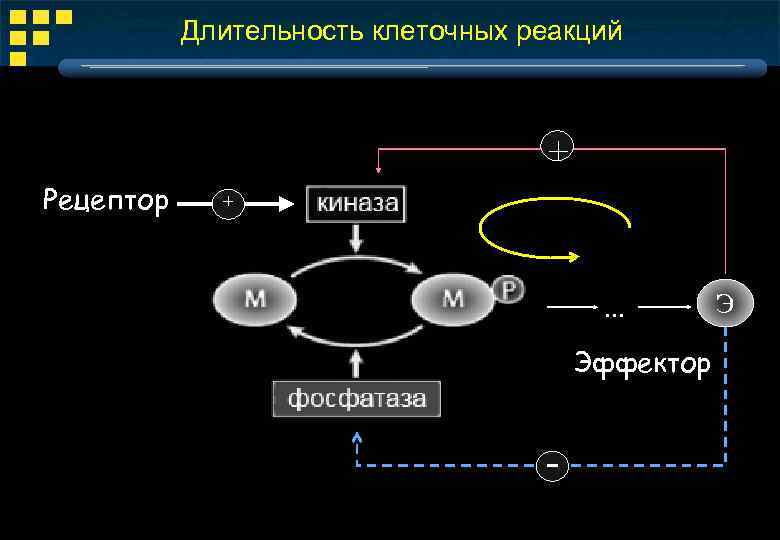 Длительность клеточных реакций + Рецептор + . . . Эффектор - Э
Длительность клеточных реакций + Рецептор + . . . Эффектор - Э
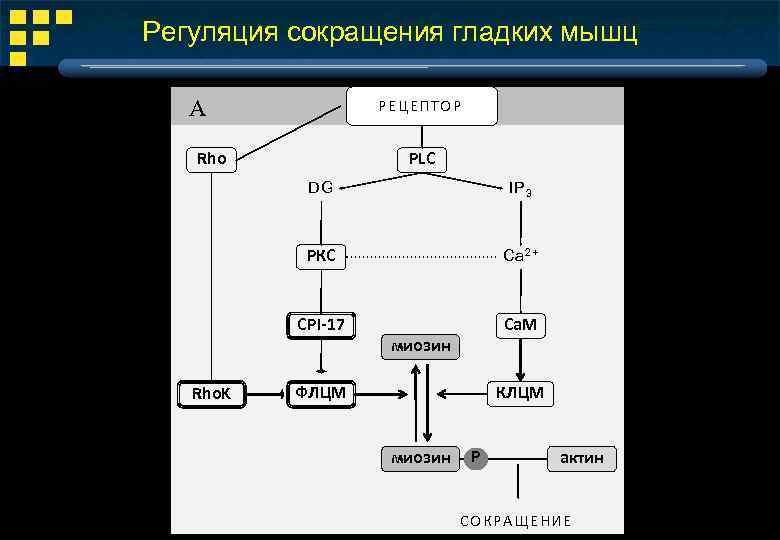 Регуляция сокращения гладких мышц А РЕЦ Е ПТ ОР PLC Rho DG РКС Ca 2+ CPI-17 Rho. K IP 3 Са. М миозин КЛЦМ ФЛЦМ миозин Р актин СОК РА ЩЕН ИЕ
Регуляция сокращения гладких мышц А РЕЦ Е ПТ ОР PLC Rho DG РКС Ca 2+ CPI-17 Rho. K IP 3 Са. М миозин КЛЦМ ФЛЦМ миозин Р актин СОК РА ЩЕН ИЕ
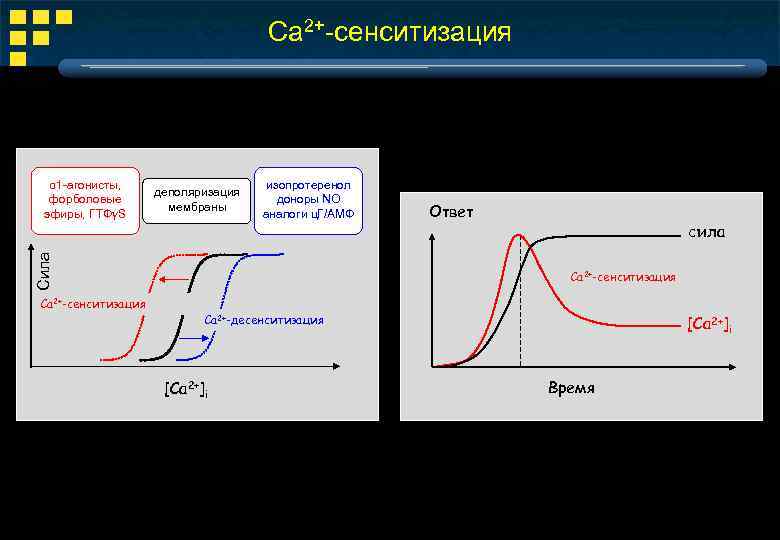 Ca 2+-сенситизация деполяризация мембраны изопротеренол доноры ΝΟ аналоги ц. Г/АМФ Сила α 1 -агонисты, форболовые эфиры, ГТФγS Ca 2+-сенситизация Ответ сила Ca 2+-сенситизация Ca 2+-десенситизация [Са 2+]i [Ca 2+]i Время
Ca 2+-сенситизация деполяризация мембраны изопротеренол доноры ΝΟ аналоги ц. Г/АМФ Сила α 1 -агонисты, форболовые эфиры, ГТФγS Ca 2+-сенситизация Ответ сила Ca 2+-сенситизация Ca 2+-десенситизация [Са 2+]i [Ca 2+]i Время
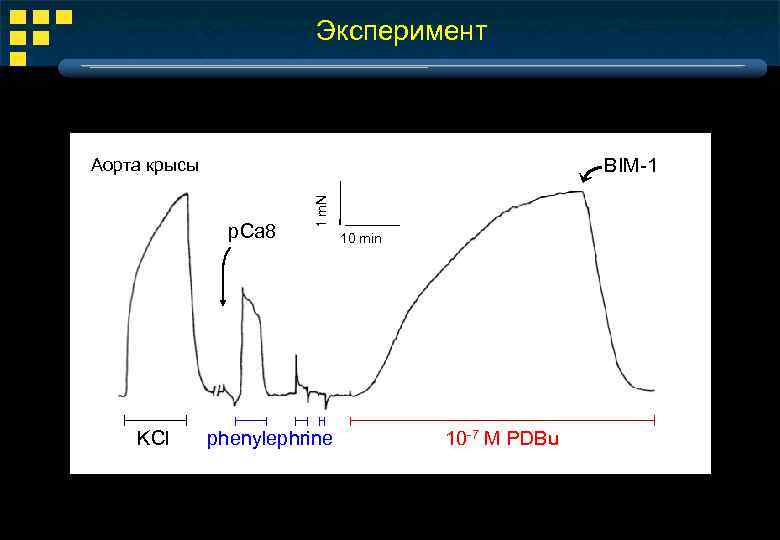 Эксперимент BIM-1 p. Ca 8 KCl 1 m. N Аорта крысы phenylephrine 10 min 10 -7 М PDBu
Эксперимент BIM-1 p. Ca 8 KCl 1 m. N Аорта крысы phenylephrine 10 min 10 -7 М PDBu
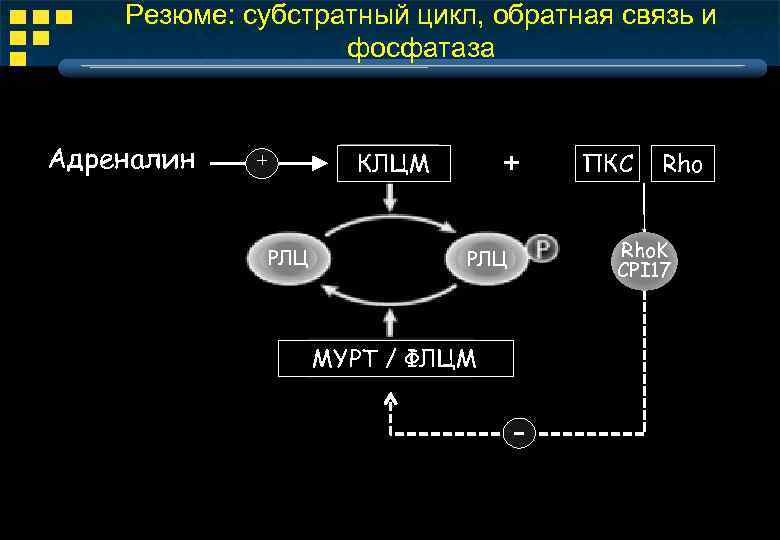 Резюме: субстратный цикл, обратная связь и фосфатаза Адреналин + КЛЦМ + РЛЦ ПКС Rho. K CPI 17 РЛЦ MYPT / ФЛЦМ -
Резюме: субстратный цикл, обратная связь и фосфатаза Адреналин + КЛЦМ + РЛЦ ПКС Rho. K CPI 17 РЛЦ MYPT / ФЛЦМ -
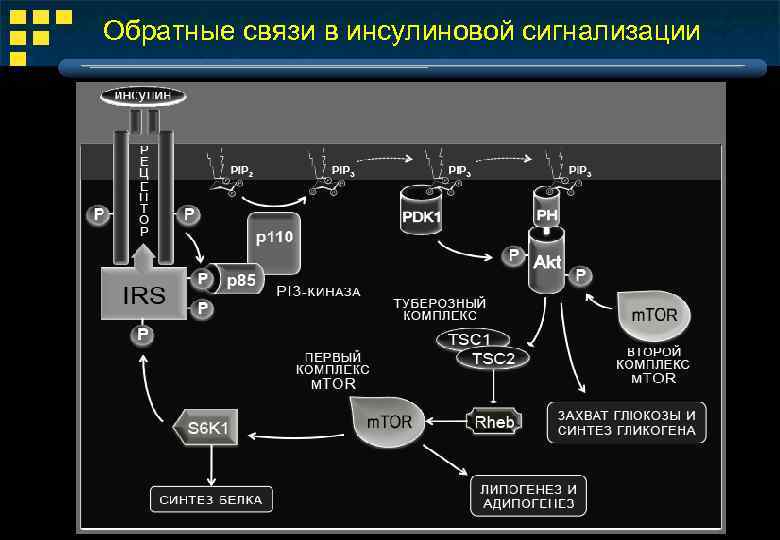 Обратные связи в инсулиновой сигнализации
Обратные связи в инсулиновой сигнализации
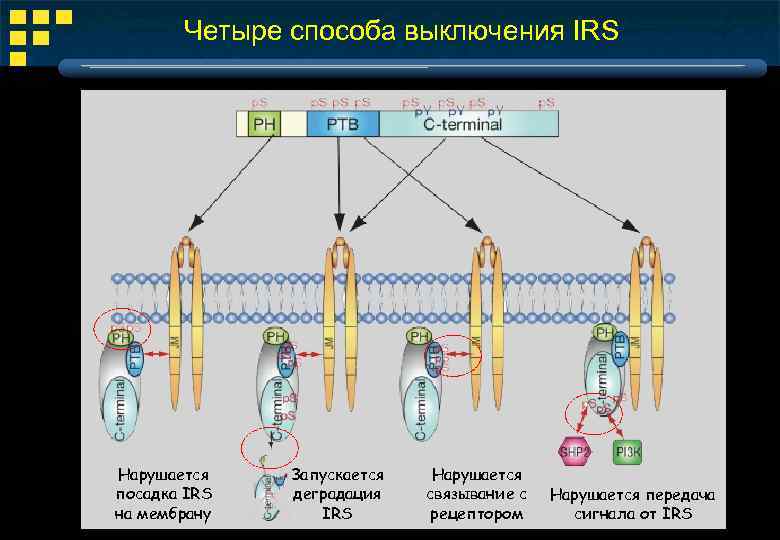 Четыре способа выключения IRS Нарушается посадка IRS на мембрану Запускается деградация IRS Нарушается связывание с рецептором Нарушается передача сигнала от IRS
Четыре способа выключения IRS Нарушается посадка IRS на мембрану Запускается деградация IRS Нарушается связывание с рецептором Нарушается передача сигнала от IRS
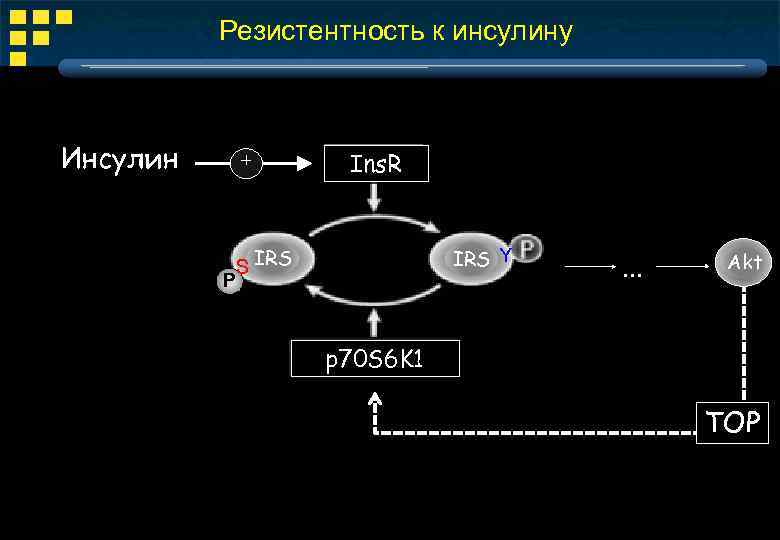 Резистентность к инсулину Инсулин + Ins. R S IRS P IRS Y . . . Akt Р p 70 S 6 K 1 ТОР
Резистентность к инсулину Инсулин + Ins. R S IRS P IRS Y . . . Akt Р p 70 S 6 K 1 ТОР
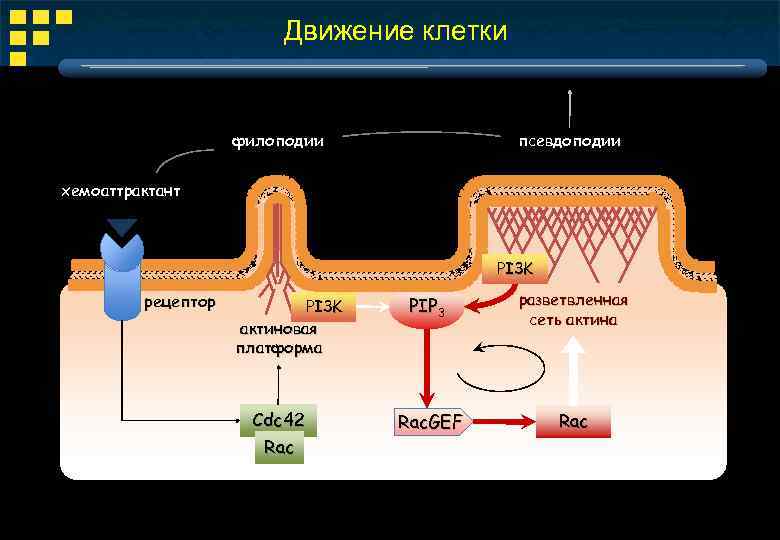 Движение клетки филоподии псевдоподии хемоаттрактант PI 3 K рецептор PI 3 K актиновая платформа Cdc 42 Rac PIP 3 разветвленная сеть актина Rac. GEF Rac
Движение клетки филоподии псевдоподии хемоаттрактант PI 3 K рецептор PI 3 K актиновая платформа Cdc 42 Rac PIP 3 разветвленная сеть актина Rac. GEF Rac
 H 2 O 2 как вторичный посредник и регулятор фосфатаз лиганд плазматическая мембрана NOX рецептор 1 -5 мин 15 -60 мин p 4 0 ph Rac ox p 67 phox x pho p 47 ФАД НАДФ H 2 O 2 Киназа Y Киназа неактивная Y-P активные PTP SH PTP SOH неактивная миграция e-
H 2 O 2 как вторичный посредник и регулятор фосфатаз лиганд плазматическая мембрана NOX рецептор 1 -5 мин 15 -60 мин p 4 0 ph Rac ox p 67 phox x pho p 47 ФАД НАДФ H 2 O 2 Киназа Y Киназа неактивная Y-P активные PTP SH PTP SOH неактивная миграция e-
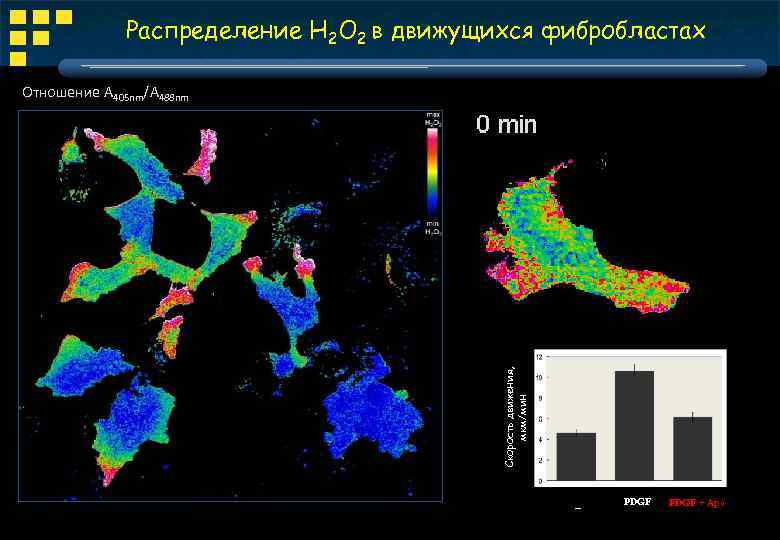 Распределение Н 2 О 2 в движущихся фибробластах Отношение А 405 nm/А 488 nm PIP 3 Скорость движения, мкм/мин λвозб = 405 nm − PDGF + Apo
Распределение Н 2 О 2 в движущихся фибробластах Отношение А 405 nm/А 488 nm PIP 3 Скорость движения, мкм/мин λвозб = 405 nm − PDGF + Apo
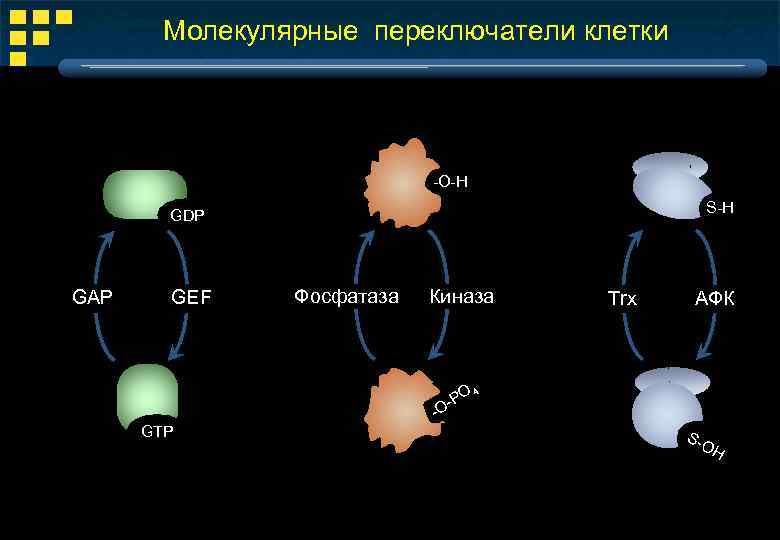 Молекулярные переключатели клетки -O-H S-H GDP GAP GEF Фосфатаза Киназа O -P -O GTP Trx АФК 4 S-O H
Молекулярные переключатели клетки -O-H S-H GDP GAP GEF Фосфатаза Киназа O -P -O GTP Trx АФК 4 S-O H
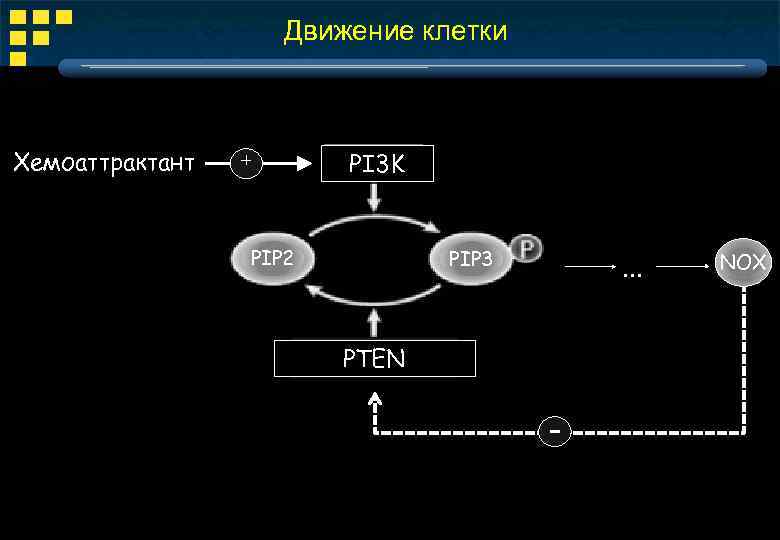 Движение клетки Хемоаттрактант + PI 3 K PIP 2 PIP 3 . . . PTEN - NOX Р
Движение клетки Хемоаттрактант + PI 3 K PIP 2 PIP 3 . . . PTEN - NOX Р


