8sistemy_ravn_t-d.pptx
- Количество слайдов: 15
 Формирование современной эволюционносинергетической парадигмы естествознания Идея постепенного развития – эволюции: -геология-XVIII век - Биология-XIX век -Космология- XX век Непрерывный процесс развития присущ явлениям различной природы и обеспечивается самопроизвольным направленным усложнением системной организации
Формирование современной эволюционносинергетической парадигмы естествознания Идея постепенного развития – эволюции: -геология-XVIII век - Биология-XIX век -Космология- XX век Непрерывный процесс развития присущ явлениям различной природы и обеспечивается самопроизвольным направленным усложнением системной организации
 Представление о равновесной термодинамике 1. 2. 3. 4. 5. 6. Системность Термодинамические системы Равновесное состояние Законы равновесной термодинамики Энтропия. Порядок и беспорядок. Гипотеза тепловой смерти Вселенной
Представление о равновесной термодинамике 1. 2. 3. 4. 5. 6. Системность Термодинамические системы Равновесное состояние Законы равновесной термодинамики Энтропия. Порядок и беспорядок. Гипотеза тепловой смерти Вселенной
 Системность как отражение единства мира • Система- совокупность некоторых элементов, объединённых внутренними связями и образующих качественно новое целое, взаимодействующее с окружающей средой посредством внешних связей. • Система характеризуется особенностями поведения , новыми свойствами и новыми параметрами, отсутствующими у её элементов. • «Система» и «элемент» - понятия относительные, природные системы иерархичны. • Симметрия и структура системы определяются внутренними связями элементов и являются устойчивыми в определённом интервале внешних условий. • По взаимодействию с внешней средой различают изолированные и открытые системы. • Все природные объекты- структурированные, упорядоченные, иерархически организованные системы. • Системный способ объединения элементов, благодаря иерархичности систем, обеспечивает единство всех систем живой и неживой природы, т. е. единство материального мира. Каждый элемент любой системы оказывается связан со всеми элементами всех возможных систем.
Системность как отражение единства мира • Система- совокупность некоторых элементов, объединённых внутренними связями и образующих качественно новое целое, взаимодействующее с окружающей средой посредством внешних связей. • Система характеризуется особенностями поведения , новыми свойствами и новыми параметрами, отсутствующими у её элементов. • «Система» и «элемент» - понятия относительные, природные системы иерархичны. • Симметрия и структура системы определяются внутренними связями элементов и являются устойчивыми в определённом интервале внешних условий. • По взаимодействию с внешней средой различают изолированные и открытые системы. • Все природные объекты- структурированные, упорядоченные, иерархически организованные системы. • Системный способ объединения элементов, благодаря иерархичности систем, обеспечивает единство всех систем живой и неживой природы, т. е. единство материального мира. Каждый элемент любой системы оказывается связан со всеми элементами всех возможных систем.
 Термодинамические системы. Равновесие. • Термодинамическая система- совокупность большого числа частиц, выделенная из окружающей среды (макроскопические тела- газы, жидкости, твёрдые тела). Обмен Новые свойства: температура, энтропия, Система Внешняя среда внутренняя энергия… • Система, не обменивающаяся с внешней средой ни веществом, ни энергией, называется изолированной. • Изолированная термодинамическая система самопроизвольно переходит в новое состояние, называемое равновесным, в котором свойства системы одинаковы во всех её частях и не изменяются со временем. • Особенности равновесного состояния: - Единственно -Устойчиво -Стационарно -Максимально симметрично -Склеротично
Термодинамические системы. Равновесие. • Термодинамическая система- совокупность большого числа частиц, выделенная из окружающей среды (макроскопические тела- газы, жидкости, твёрдые тела). Обмен Новые свойства: температура, энтропия, Система Внешняя среда внутренняя энергия… • Система, не обменивающаяся с внешней средой ни веществом, ни энергией, называется изолированной. • Изолированная термодинамическая система самопроизвольно переходит в новое состояние, называемое равновесным, в котором свойства системы одинаковы во всех её частях и не изменяются со временем. • Особенности равновесного состояния: - Единственно -Устойчиво -Стационарно -Максимально симметрично -Склеротично
 Равновесное состояние Исходные состояния Равновесное состояниестационарное состояние изолированной системы
Равновесное состояние Исходные состояния Равновесное состояниестационарное состояние изолированной системы
 Равновесная термодинамика и статистика • Свойства термодинамических систем изучаются методами термодинамики и молекулярной статистической теории. • В термодинамике состояние системы характеризуется макроскопическими параметрами: температура, давление, объём… Изолированные системы изучает равновесная термодинамика. • Изменение параметров состояния называется процессом. Для равновесных процессов термодинамика даёт их полное количественное описание, основываясь на системе опытных фундаментальных законов, называемых началами термодинамики. • Начала термодинамики являются обобщением экспериментальных исследований, имеют универсальный характер и не зависят от конкретной природы образующих термодинамическую систему тел. • В молекулярной статистике устанавливается связь макропараметров системы с характером молекулярного движения, т. е. с микропараметрами. Основываясь на модели внутренней структуры системы, состоящей из очень большого числа частиц, статистика позволяет определить параметры её состояния.
Равновесная термодинамика и статистика • Свойства термодинамических систем изучаются методами термодинамики и молекулярной статистической теории. • В термодинамике состояние системы характеризуется макроскопическими параметрами: температура, давление, объём… Изолированные системы изучает равновесная термодинамика. • Изменение параметров состояния называется процессом. Для равновесных процессов термодинамика даёт их полное количественное описание, основываясь на системе опытных фундаментальных законов, называемых началами термодинамики. • Начала термодинамики являются обобщением экспериментальных исследований, имеют универсальный характер и не зависят от конкретной природы образующих термодинамическую систему тел. • В молекулярной статистике устанавливается связь макропараметров системы с характером молекулярного движения, т. е. с микропараметрами. Основываясь на модели внутренней структуры системы, состоящей из очень большого числа частиц, статистика позволяет определить параметры её состояния.
 Первое начало термодинамики. Ю. Р. Майер, Дж. Джоуль, Г. Гельмгольц, 1842 - 1847 г. • Внутренняя энергия(U) - это функция состояния системы, равная энергии движения и взаимодействия составляющих систему частиц. • Первое начало термодинамики устанавливает два способа изменения внутренней энергии: теплопередачу и работу. • В процессе теплопередачи внутренняя энергия системы изменяется за счёт внутренней энергии других тел. Виды теплопередачи: теплопроводность, излучение, конвекция. Мерой энергии, переданной в процессе теплопередачи является количество теплоты ( теплота)- Q • В процессе совершения работы внутренняя (или другая) энергия изменяются за счёт энергии упорядоченного движения. Мерой энергии, переданной в этом процессе является работа- A. • Работа и теплота зависят от рода процесса и не являются функциями состояния системы.
Первое начало термодинамики. Ю. Р. Майер, Дж. Джоуль, Г. Гельмгольц, 1842 - 1847 г. • Внутренняя энергия(U) - это функция состояния системы, равная энергии движения и взаимодействия составляющих систему частиц. • Первое начало термодинамики устанавливает два способа изменения внутренней энергии: теплопередачу и работу. • В процессе теплопередачи внутренняя энергия системы изменяется за счёт внутренней энергии других тел. Виды теплопередачи: теплопроводность, излучение, конвекция. Мерой энергии, переданной в процессе теплопередачи является количество теплоты ( теплота)- Q • В процессе совершения работы внутренняя (или другая) энергия изменяются за счёт энергии упорядоченного движения. Мерой энергии, переданной в этом процессе является работа- A. • Работа и теплота зависят от рода процесса и не являются функциями состояния системы.
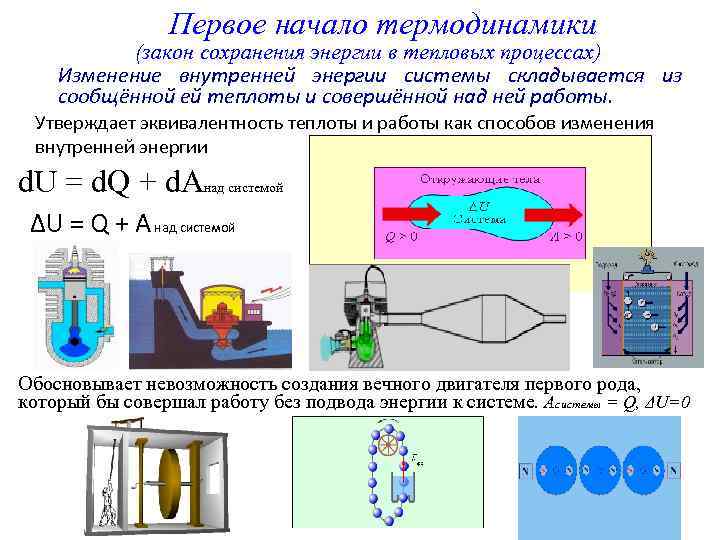 Первое начало термодинамики (закон сохранения энергии в тепловых процессах) Изменение внутренней энергии системы складывается из сообщённой ей теплоты и совершённой над ней работы. Утверждает эквивалентность теплоты и работы как способов изменения внутренней энергии d. U = d. Q + d. Aнад системой ΔU = Q + A над системой Обосновывает невозможность создания вечного двигателя первого рода, который бы совершал работу без подвода энергии к системе. Aсистемы = Q, ΔU=0
Первое начало термодинамики (закон сохранения энергии в тепловых процессах) Изменение внутренней энергии системы складывается из сообщённой ей теплоты и совершённой над ней работы. Утверждает эквивалентность теплоты и работы как способов изменения внутренней энергии d. U = d. Q + d. Aнад системой ΔU = Q + A над системой Обосновывает невозможность создания вечного двигателя первого рода, который бы совершал работу без подвода энергии к системе. Aсистемы = Q, ΔU=0
 1824 г. С. Карно Сади Карно (1796 – 1832)
1824 г. С. Карно Сади Карно (1796 – 1832)
 Второе начало термодинамики. С. Карно, Р. Клаузиус, У. Томсон • Второе начало термодинамики устанавливает направленность самопроизвольных процессов в изолированных системах. При количественной эквивалентности теплоты и работы, существуют качественные особенности. Превращение всех видов энергии упорядоченного движения в теплоту происходит полностью и самопроизвольно. Теплота превращается в работу лишь частично. • 1850 г. Р. Клаузиус. Невозможен процесс, в котором теплота бы самопроизвольно переходила от тел более холодных к телам более горячим. • 1851 г. , У. Томсон. Невозможно существование периодически действующей тепловой машины, которая бы всё тепло, полученное от нагревателя. превращала в эквивалентную ему работу. • Вечный двигатель второго рода невозможен
Второе начало термодинамики. С. Карно, Р. Клаузиус, У. Томсон • Второе начало термодинамики устанавливает направленность самопроизвольных процессов в изолированных системах. При количественной эквивалентности теплоты и работы, существуют качественные особенности. Превращение всех видов энергии упорядоченного движения в теплоту происходит полностью и самопроизвольно. Теплота превращается в работу лишь частично. • 1850 г. Р. Клаузиус. Невозможен процесс, в котором теплота бы самопроизвольно переходила от тел более холодных к телам более горячим. • 1851 г. , У. Томсон. Невозможно существование периодически действующей тепловой машины, которая бы всё тепло, полученное от нагревателя. превращала в эквивалентную ему работу. • Вечный двигатель второго рода невозможен
 Энтропия. Р. Клаузиус, 1865 г. • Энтропия (S)-функция состояния системы, являющаяся мерой беспорядка в ней. • Энтропия увеличивается с ростом беспорядка в расположении и движении частиц: при увеличении объёма, при нагревании, плавлении и т. д. • Энтропия системы может изменяться вследствие: теплообмена - d. Se необратимых процессов в системе – d. Si • Общее изменение энтропии системы d. S = d. Se + d. Si • Изменение энтропии при сообщении системе теплоты постоянной температуре
Энтропия. Р. Клаузиус, 1865 г. • Энтропия (S)-функция состояния системы, являющаяся мерой беспорядка в ней. • Энтропия увеличивается с ростом беспорядка в расположении и движении частиц: при увеличении объёма, при нагревании, плавлении и т. д. • Энтропия системы может изменяться вследствие: теплообмена - d. Se необратимых процессов в системе – d. Si • Общее изменение энтропии системы d. S = d. Se + d. Si • Изменение энтропии при сообщении системе теплоты постоянной температуре
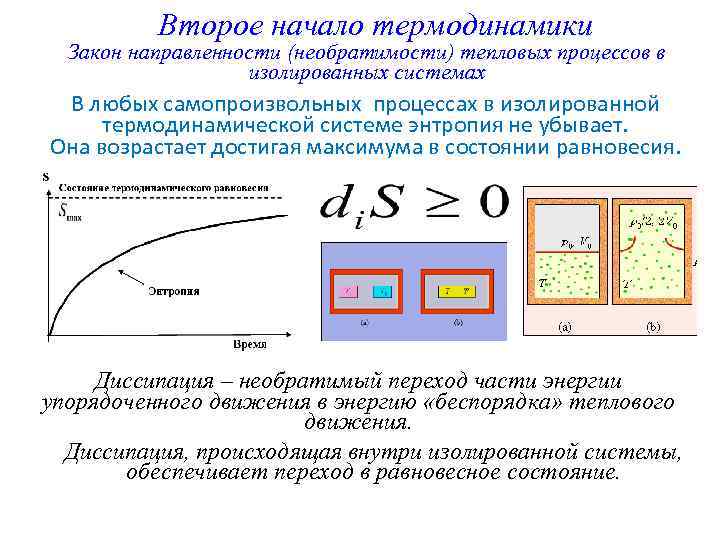 Второе начало термодинамики Закон направленности (необратимости) тепловых процессов в изолированных системах В любых самопроизвольных процессах в изолированной термодинамической системе энтропия не убывает. Она возрастает достигая максимума в состоянии равновесия. Диссипация – необратимый переход части энергии упорядоченного движения в энергию «беспорядка» теплового движения. Диссипация, происходящая внутри изолированной системы, обеспечивает переход в равновесное состояние.
Второе начало термодинамики Закон направленности (необратимости) тепловых процессов в изолированных системах В любых самопроизвольных процессах в изолированной термодинамической системе энтропия не убывает. Она возрастает достигая максимума в состоянии равновесия. Диссипация – необратимый переход части энергии упорядоченного движения в энергию «беспорядка» теплового движения. Диссипация, происходящая внутри изолированной системы, обеспечивает переход в равновесное состояние.
 МАКРО- И МИКРОСОСТОЯНИЯ СИСТЕМЫ. Термодинамическая вероятность Макросостояние - состояние системы с заданным распределением «безымянных» частиц. Микросостояние- состояние с распределением «известных» частиц по ячейкам системы. Термодинамической вероятностью макросостояния с определёнными макроскопическими параметрами называется количество микросостояний, которыми оно может быть реализовано. Все микросостояния равновероятны, поэтому, чем больше т. -д. вероятность, тем чаще возникает данное макросостояние.
МАКРО- И МИКРОСОСТОЯНИЯ СИСТЕМЫ. Термодинамическая вероятность Макросостояние - состояние системы с заданным распределением «безымянных» частиц. Микросостояние- состояние с распределением «известных» частиц по ячейкам системы. Термодинамической вероятностью макросостояния с определёнными макроскопическими параметрами называется количество микросостояний, которыми оно может быть реализовано. Все микросостояния равновероятны, поэтому, чем больше т. -д. вероятность, тем чаще возникает данное макросостояние.
 Энтропия- мера беспорядка в системе Людвиг Эдуард Больцман (1844 -1906) Энтропия –прямо пропорциональна термодинамической вероятности данного состояния. Постоянная Больцмана Термодинамическая вероятность и энтропия равновесного состояния максимальны, а во всех самопроизвольных процессах в изолированной термодинамической системе они возрастают.
Энтропия- мера беспорядка в системе Людвиг Эдуард Больцман (1844 -1906) Энтропия –прямо пропорциональна термодинамической вероятности данного состояния. Постоянная Больцмана Термодинамическая вероятность и энтропия равновесного состояния максимальны, а во всех самопроизвольных процессах в изолированной термодинамической системе они возрастают.
 Значение второго начала термодинамики • Необратимое возрастание энтропии можно рассматривать как проявление стремления макроскопической системы к молекулярному хаосу, стиранию любой начальной асимметрии. • Законы механики обратимы во времени, обратимы и элементарные молекулярные процессы. Естественное направление времени определяется направлением хода необратимых процессов в макросистеме, сопровождающихся ростом энтропии, рассеянием энергии. • Закон возрастания энтропии имеет статистически- вероятностный характер и отклонения от него ( флуктуации) возможны в микрообъёмах. • Гипотеза “тепловой смерти Вселенной “ противоречит современным экспериментальным фактам.
Значение второго начала термодинамики • Необратимое возрастание энтропии можно рассматривать как проявление стремления макроскопической системы к молекулярному хаосу, стиранию любой начальной асимметрии. • Законы механики обратимы во времени, обратимы и элементарные молекулярные процессы. Естественное направление времени определяется направлением хода необратимых процессов в макросистеме, сопровождающихся ростом энтропии, рассеянием энергии. • Закон возрастания энтропии имеет статистически- вероятностный характер и отклонения от него ( флуктуации) возможны в микрообъёмах. • Гипотеза “тепловой смерти Вселенной “ противоречит современным экспериментальным фактам.


