Фолдинг белка.ppt
- Количество слайдов: 175

Фолдинг и сортинг белков как необходимые условия реализации их функциональной активности Владимир Николаевич Кокряков доктор биологических наук, профессор кафедра биохимии СПб. ГУ
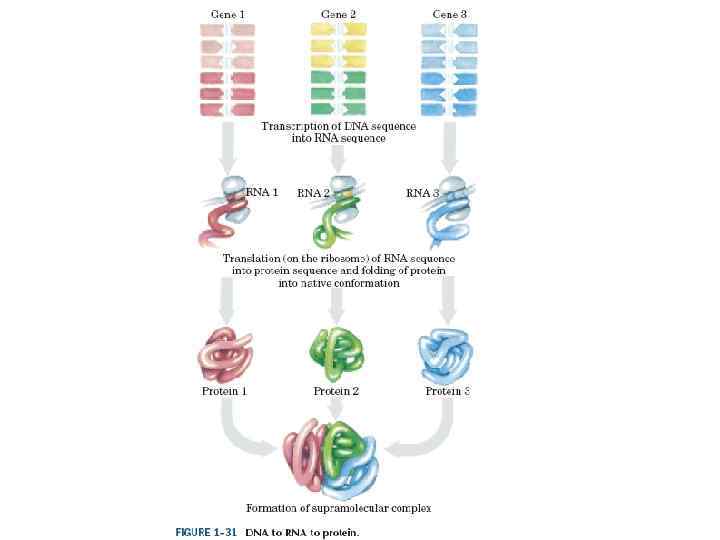
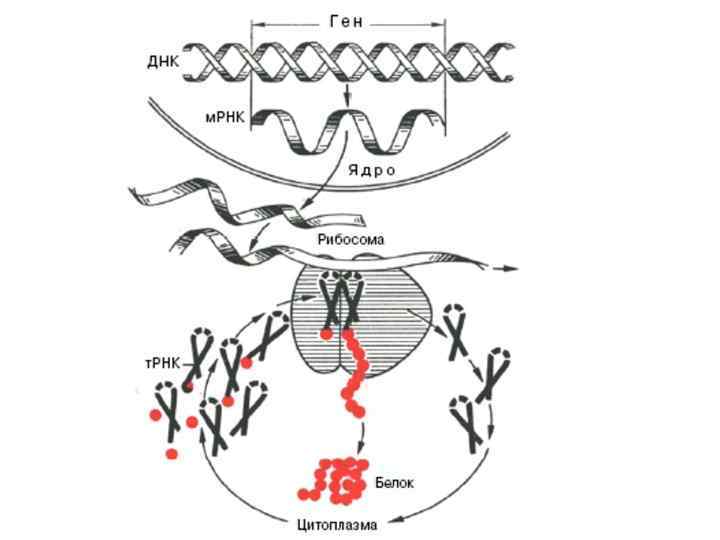
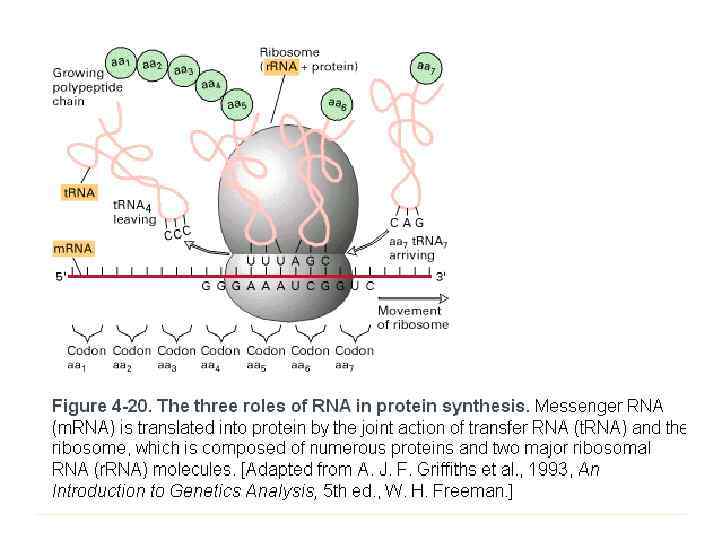
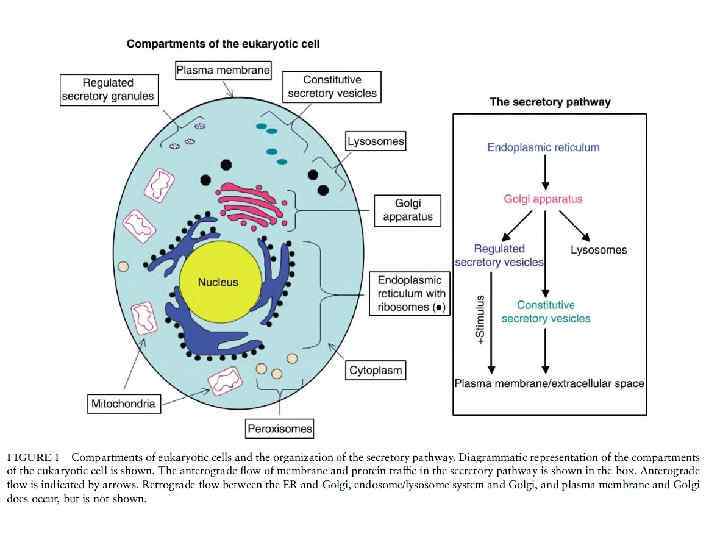

Гюнтер Блобель (нем. Günter Blobel; род. 21 мая 1936, Вальтерсдорф, Германия (ныне деревня Niegosławice (Польша)) — американский биолог немецкого происхождения, лауреат Нобелевской премии по физиологии и медицине 1999 года «за обнаружение в белковых молекулах сигнальных аминокислотных последовательностей, ответственных за адресный транспорт белков в клетке» . Профессор Рокфеллеровского университета.


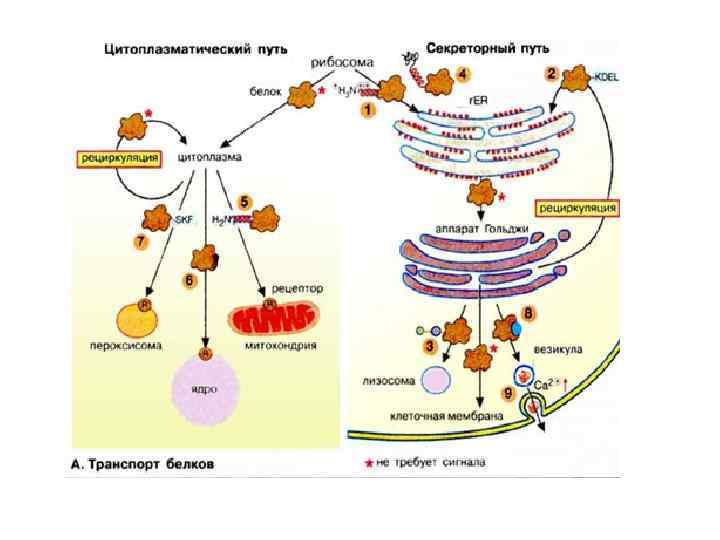
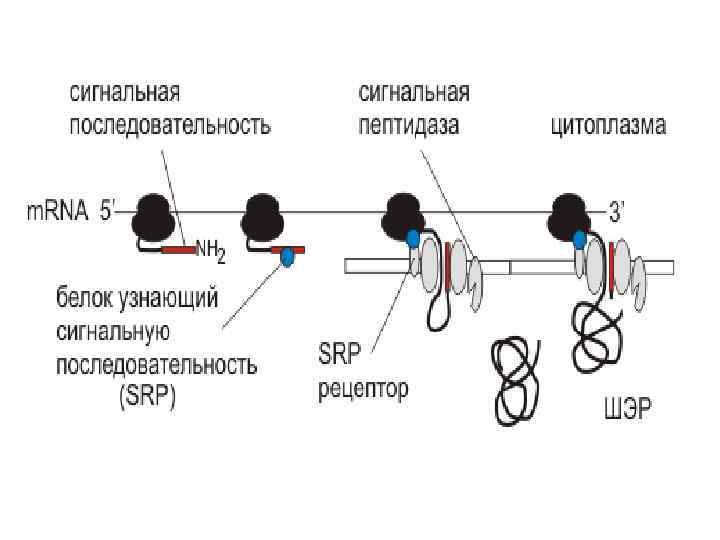
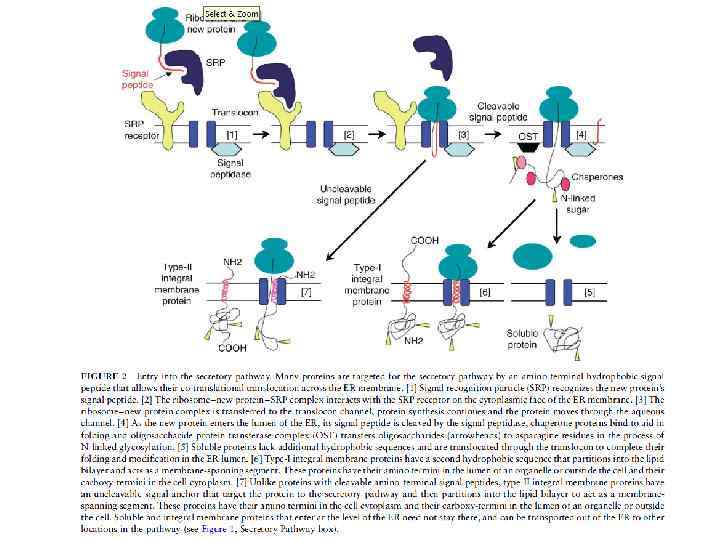
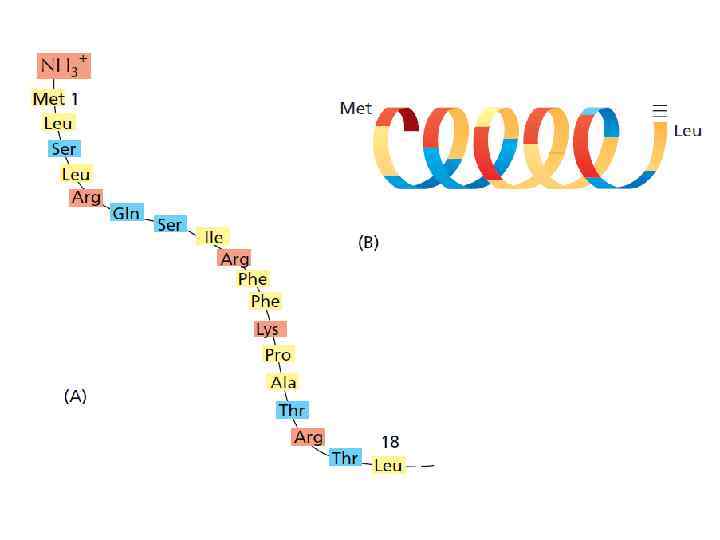
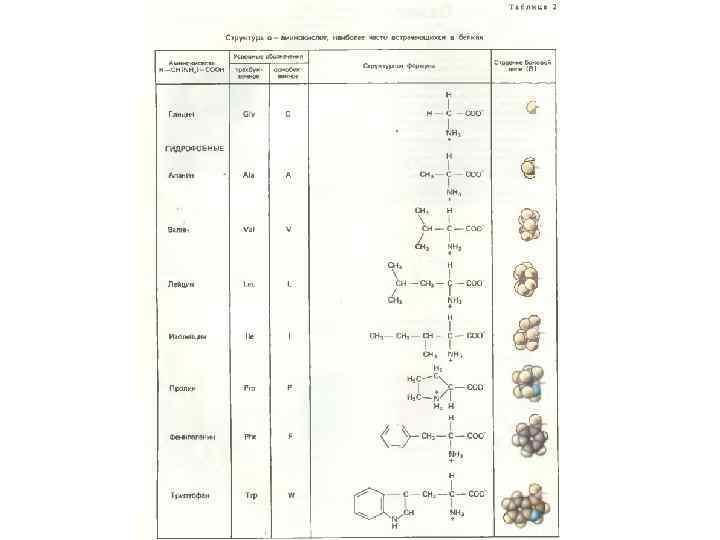
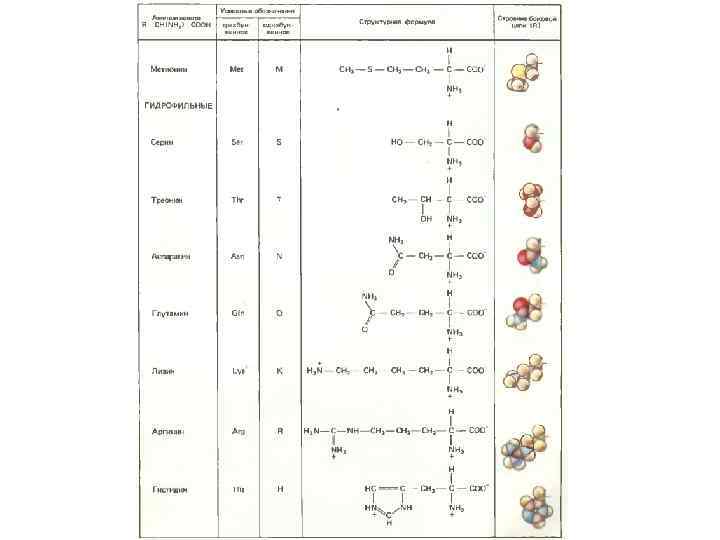
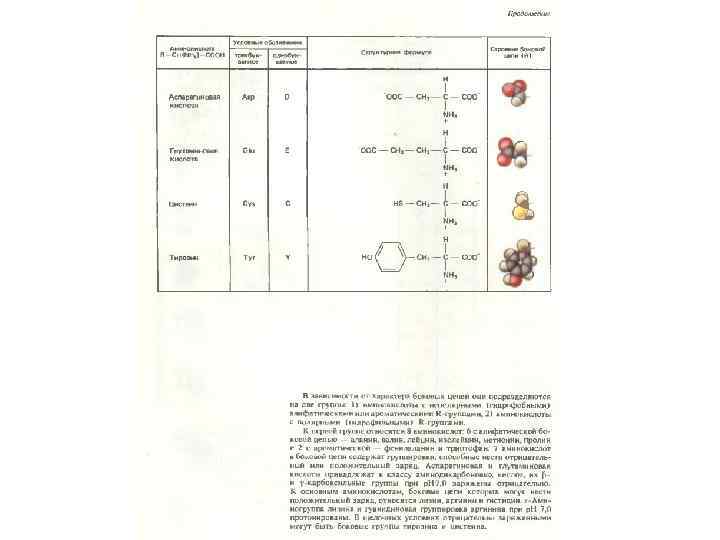
СИГНАЛЬНЫЙ ПЕПТИД Отщепляемая сигнальная последовательность (n – h – c): N-конец растущего полипептида, 15 – 30 аминокислотных остатков. Короткий «+» -участок (группа Lys, Arg, His) – – гидрофобный участок (7 - 13 остатков, Leu, Ile, Phe, Trp, Ala) – – консервативный участок (5 – 7 остатков, место расщепления). G. Blobel and D. D. Sabatini (1970) Controlled proteolysis of nascent polypeptides in rat liver cell fractions. J. Cell Biol. 45: 130 -145. G. Blobel and B. Dobberstein (1975) Transfer of proteins across membranes. J. Cell Biol. 67: 835 -851.

СИГНАЛЬНЫЙ ПЕПТИД Отщепляемая сигнальная последовательность (n – h – c): N-конец растущего полипептида, 15 – 30 аминокислотных остатков. Короткий «+» -участок (группа Lys, Arg, His) – – гидрофобный участок (7 - 13 остатков, Leu, Ile, Phe, Trp, Ala) – – консервативный участок (5 - 7 остатков, место расщепления). Не отщепляемая сигнальная последовательность: Внутренняя часть растущего полипептида. Группа «+» -аминокислот (Lys, Arg, His) – – гидрофобный участок (20 - 25 остатков).
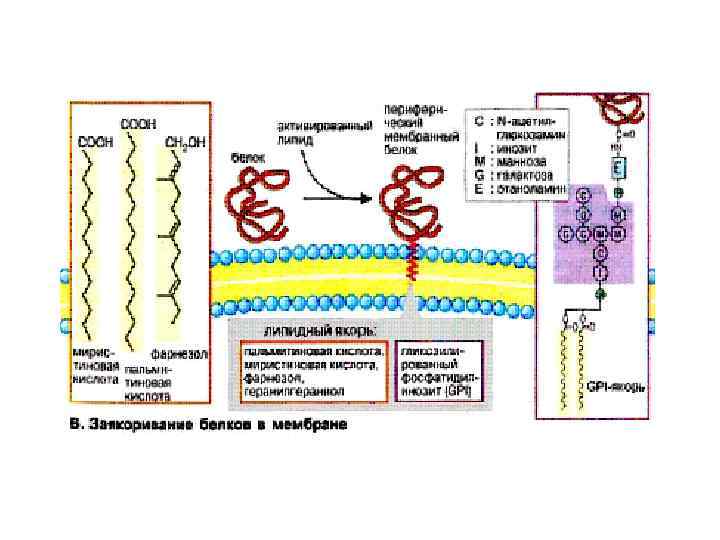
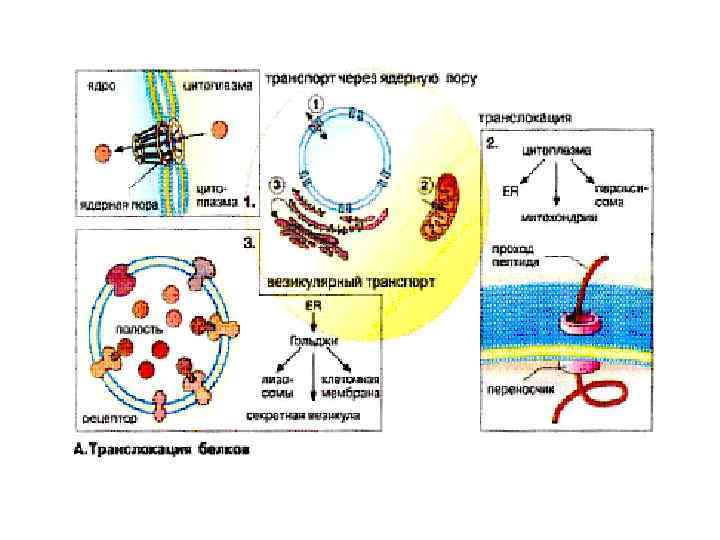
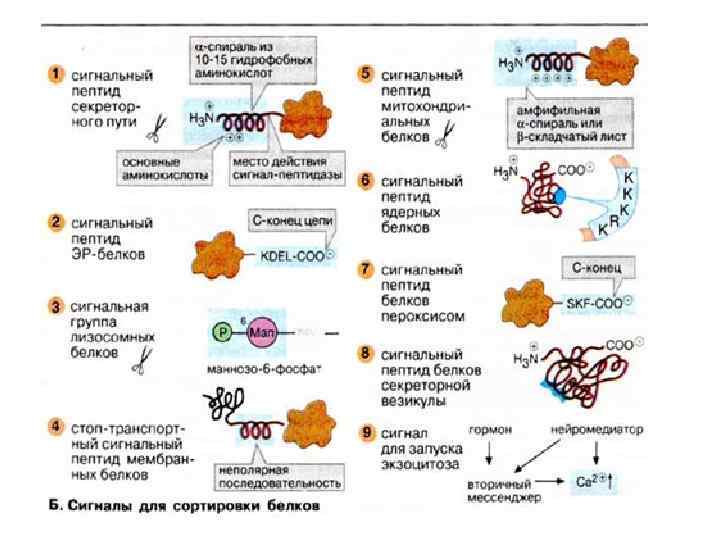

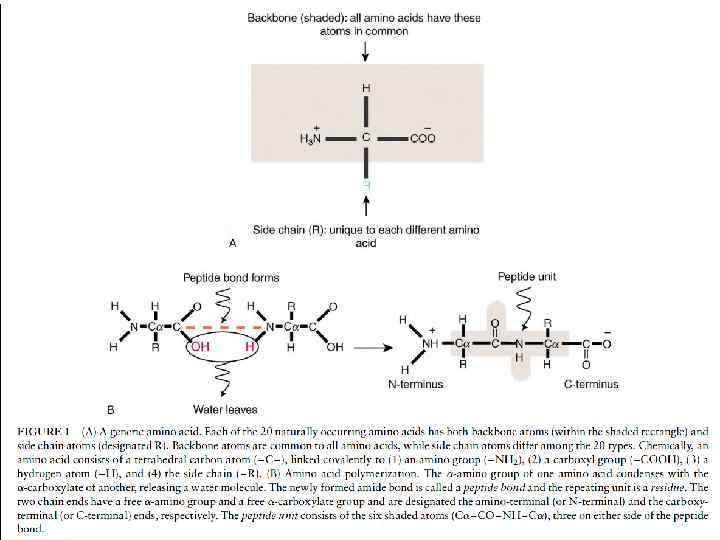
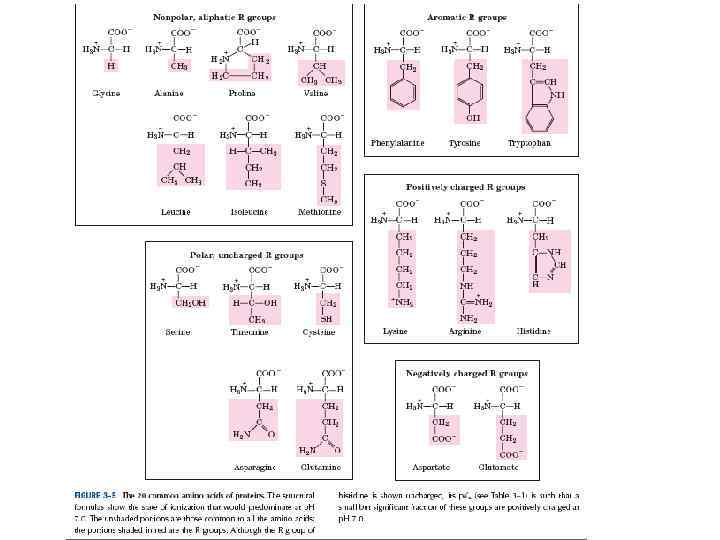
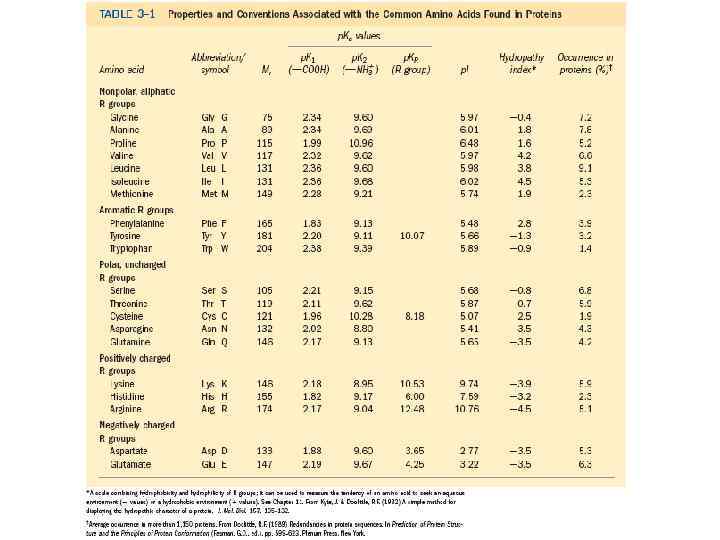
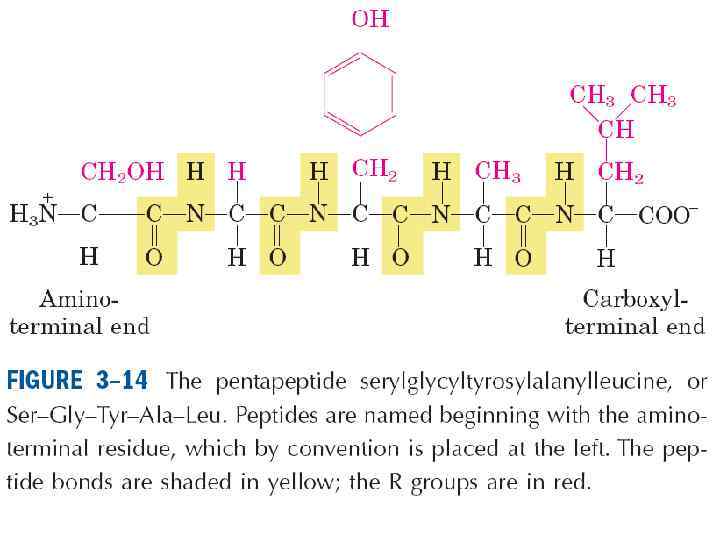
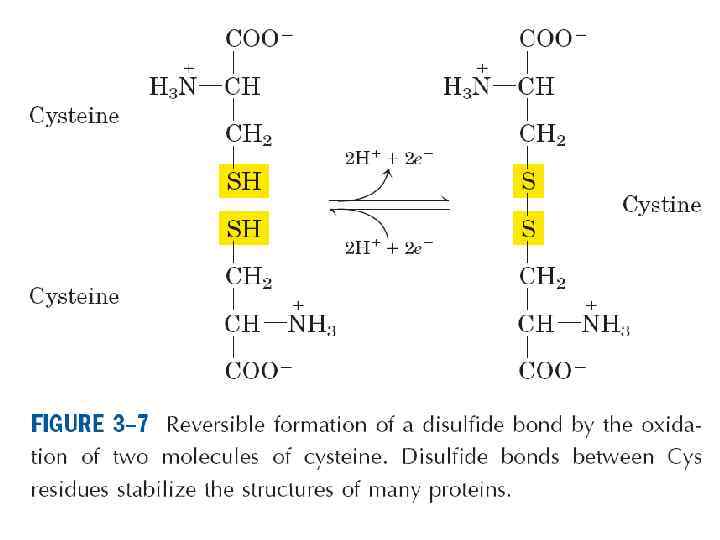

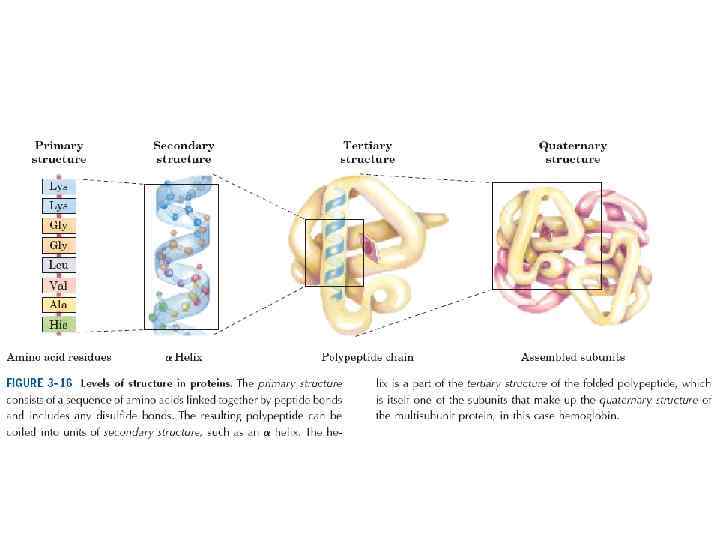
• По предложению датского исследователя К. У. Линдерстрёма-Ланга различают три уровня организации белковой молекулы: первичная, вторичная и третичная структуры. Джо Берналом введено представление о четвертичной структуре, характерной для олигомерных белков.
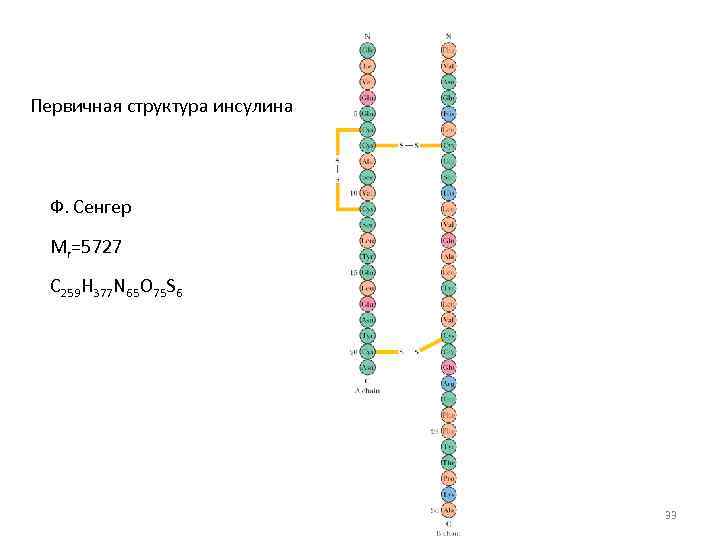
Первичная структура инсулина Ф. Сенгер Mr=5727 С 259 Н 377 N 65 O 75 S 6 33


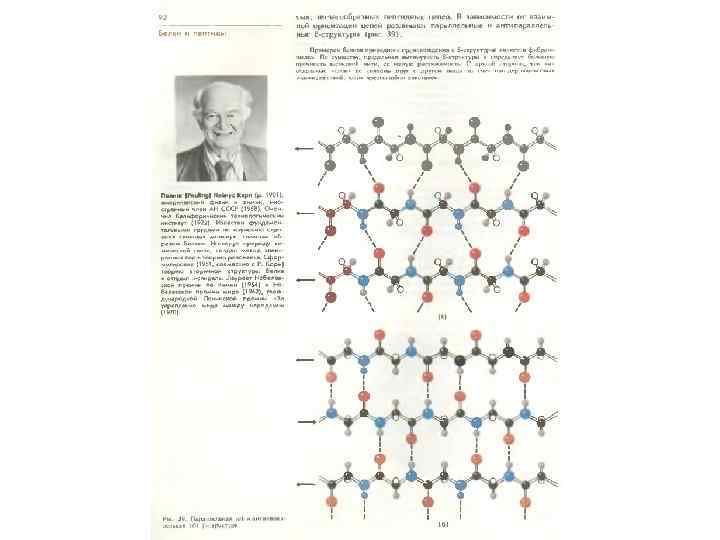
• Основные представления о характере вторичных структур белков были разработаны и введены в научный обиход благодаря исследованиям американских ученых Л. Полинга и Р. Кори.

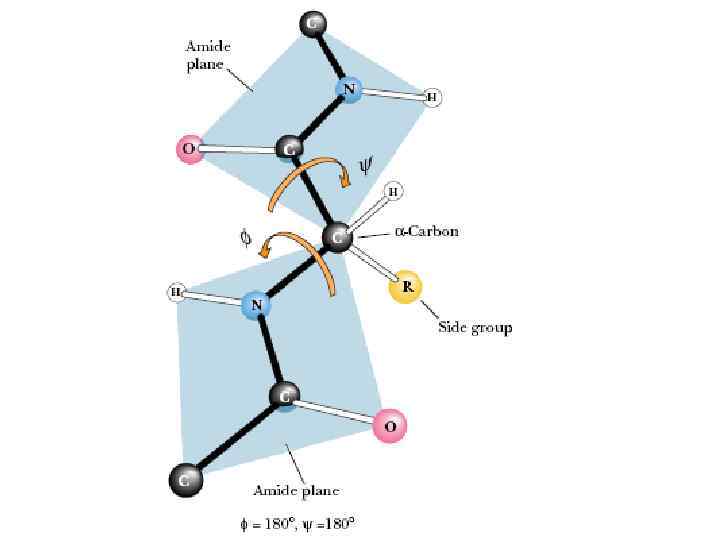
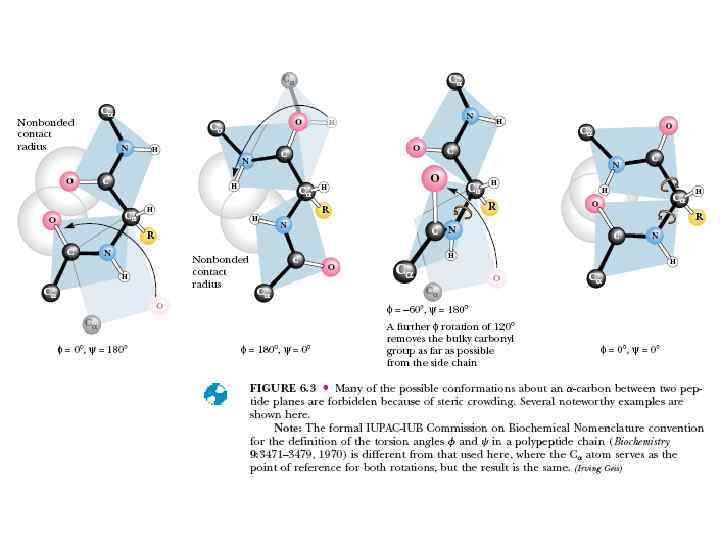
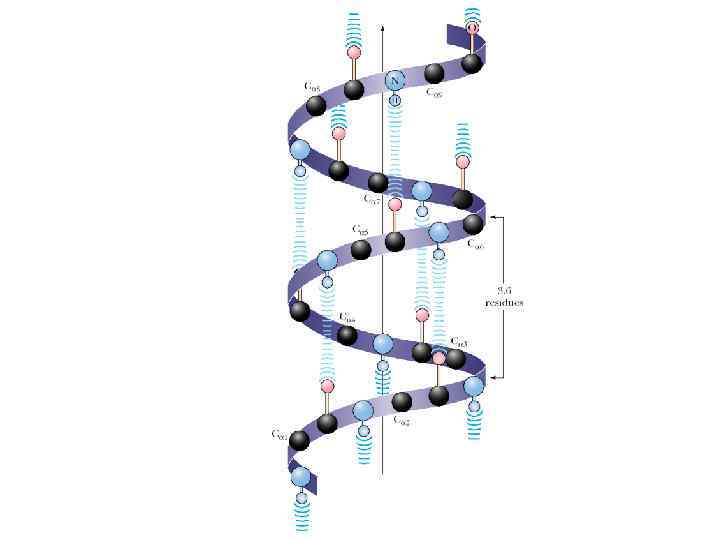

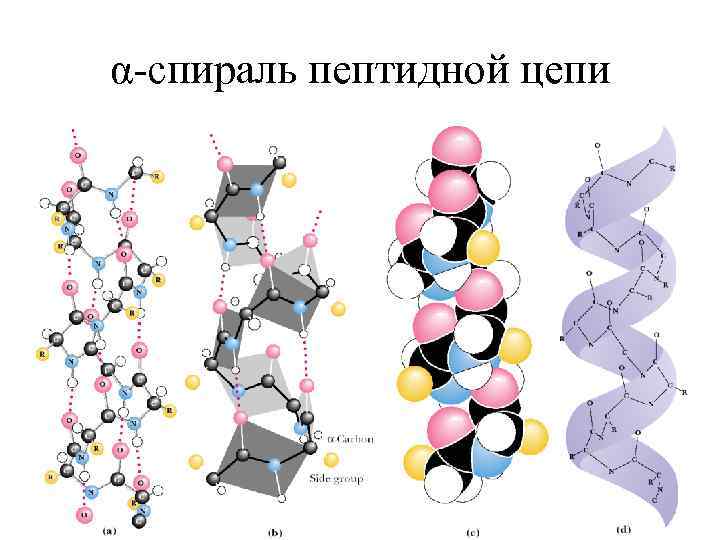
α-спираль пептидной цепи
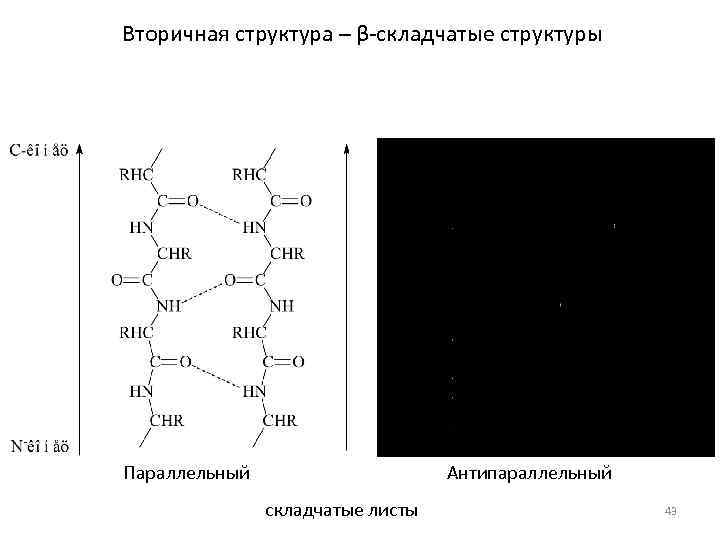
Вторичная структура – β-складчатые структуры Параллельный Антипараллельный складчатые листы 43
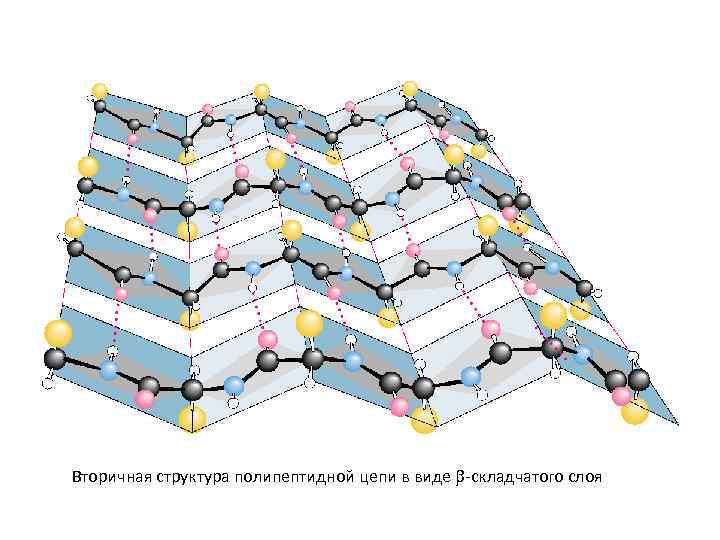
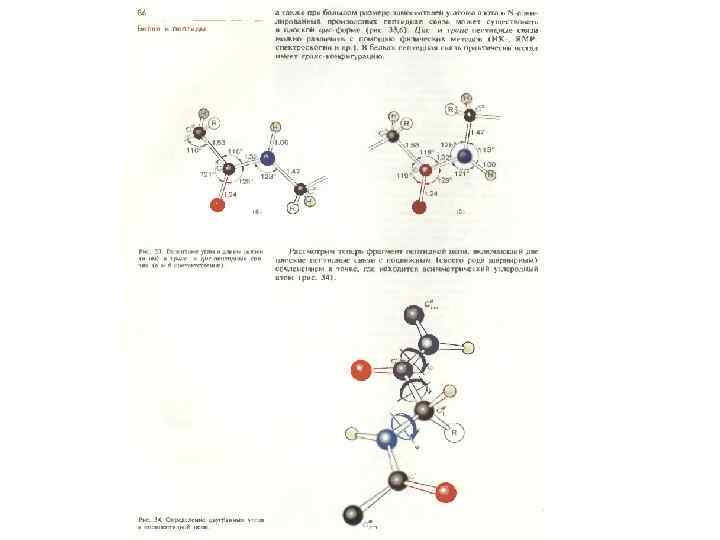
Вторичная структура полипептидной цепи в виде -складчатого слоя
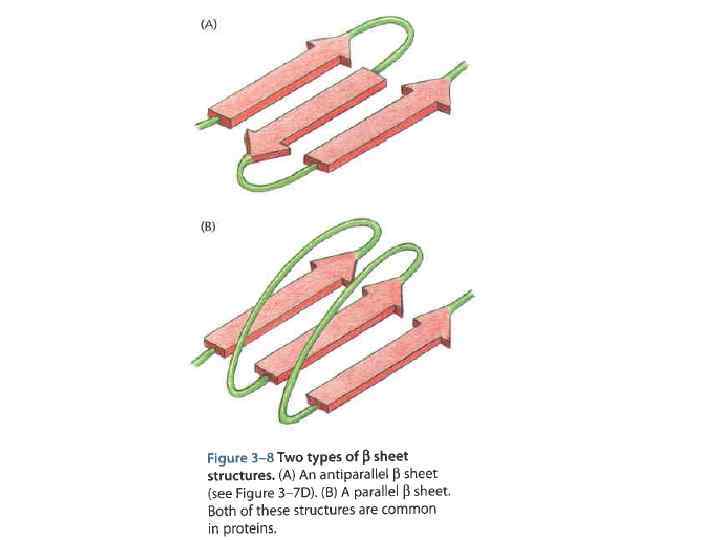
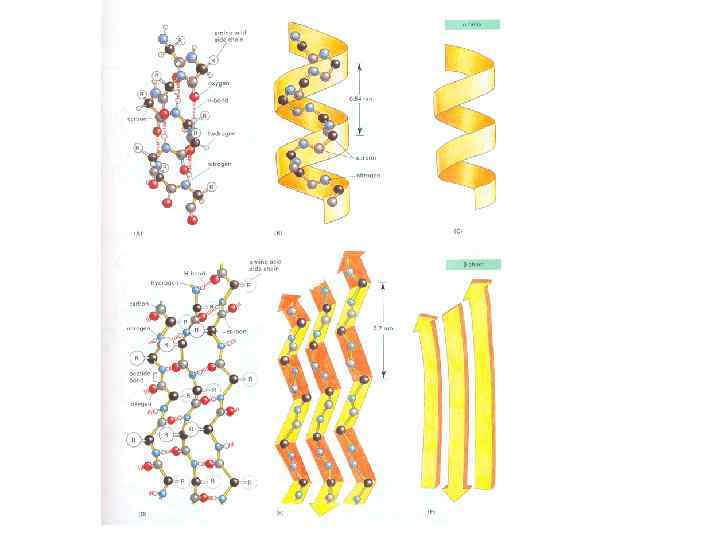

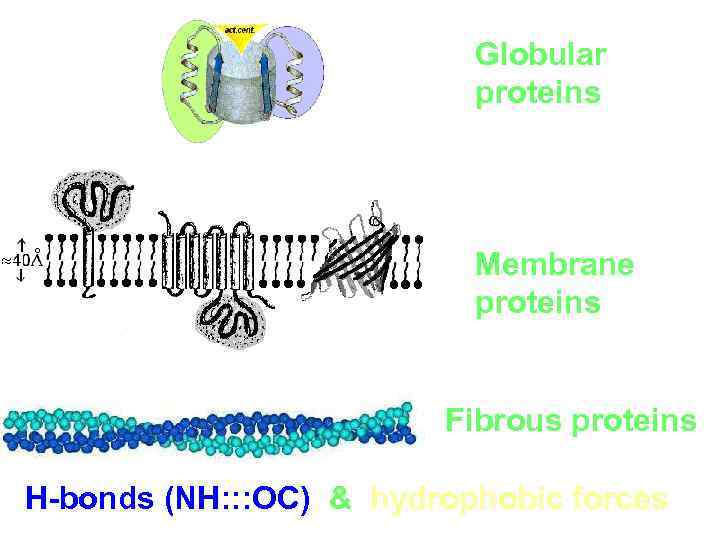
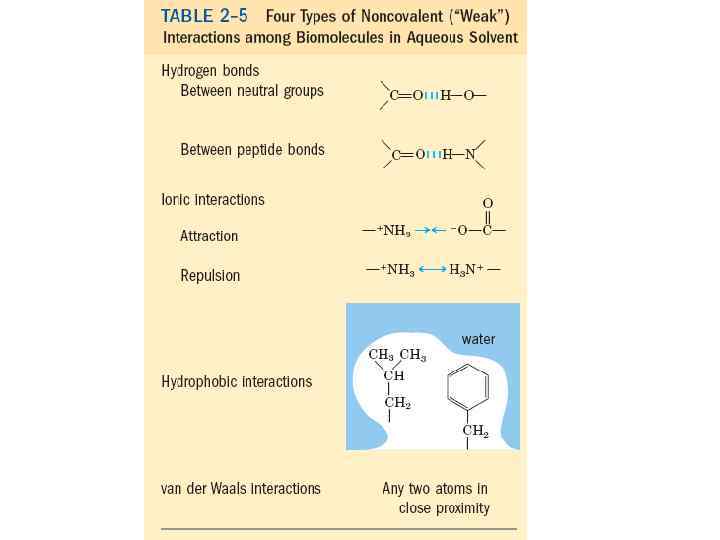
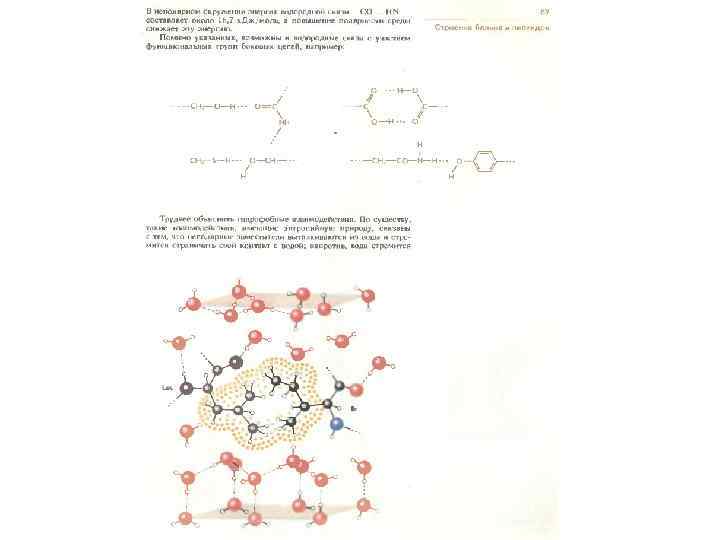
Globular proteins Membrane proteins Fibrous proteins H-bonds (NH: : : OC) & hydrophobic forces
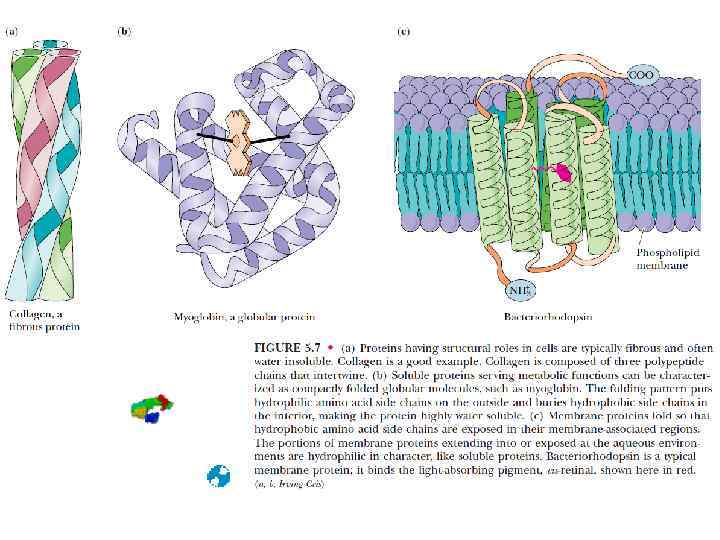
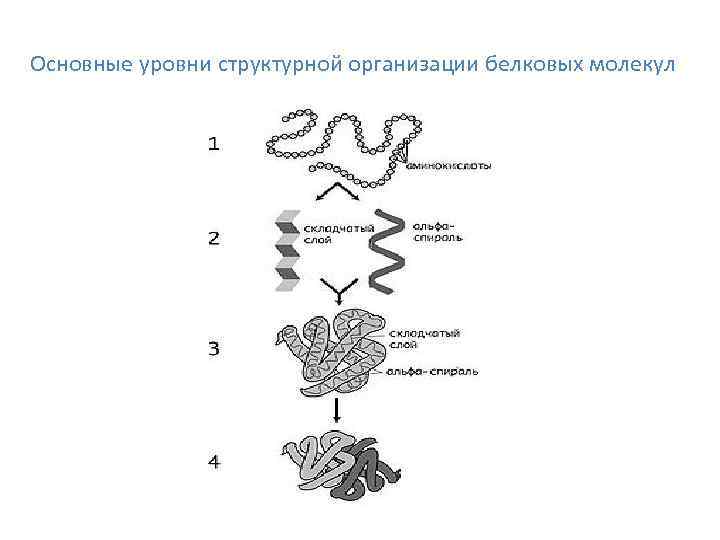
Основные уровни структурной организации белковых молекул
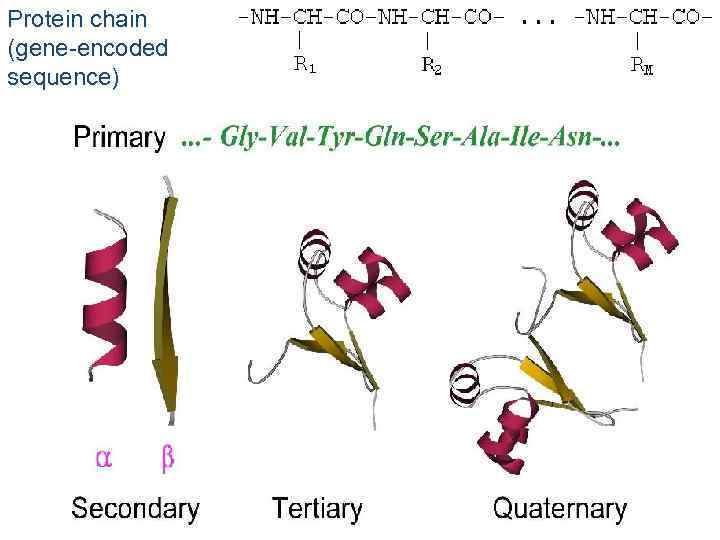
Protein chain (gene-encoded sequence)
PROTEIN CHAIN CAN FORM ITS UNIQUE 3 D STRUCTURE SPONTANEOUSLY IN VITRO (Anfinsen, 1961: Nobel Prize, 1972)

Кристиан Бемер Анфинсен Christian Boehmer Anfinsen Кристиан Бемер Анфинсен (англ. Dr. Christian Boehmer Anfinsen, Jr. ) (26 марта 1916, Монессен, штат Пенсильвания, США — 14 мая 1995) — американский биохимик, член Национальной АН США, Американской академии искусств и наук (1958), иностранный член Датского королевского общества (1964). Лауреат Нобелевской премии по химии (1972).
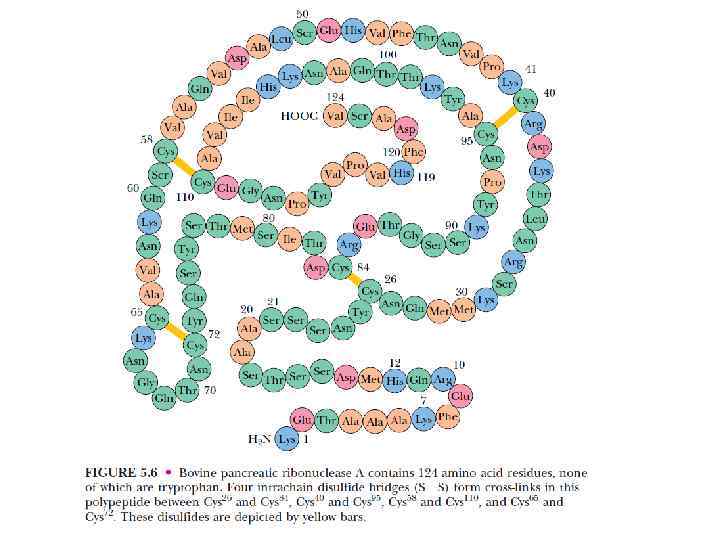
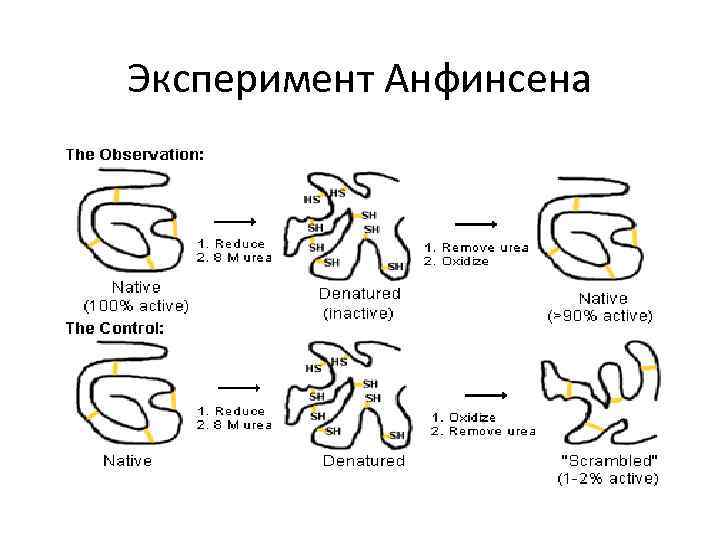
Эксперимент Анфинсена
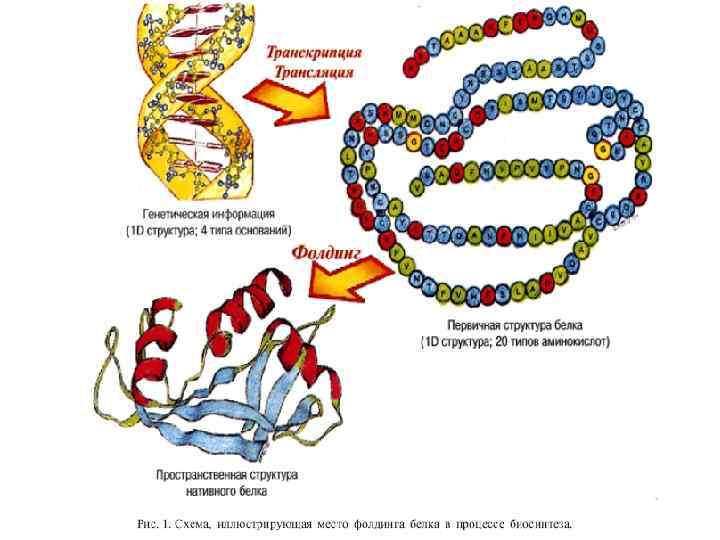
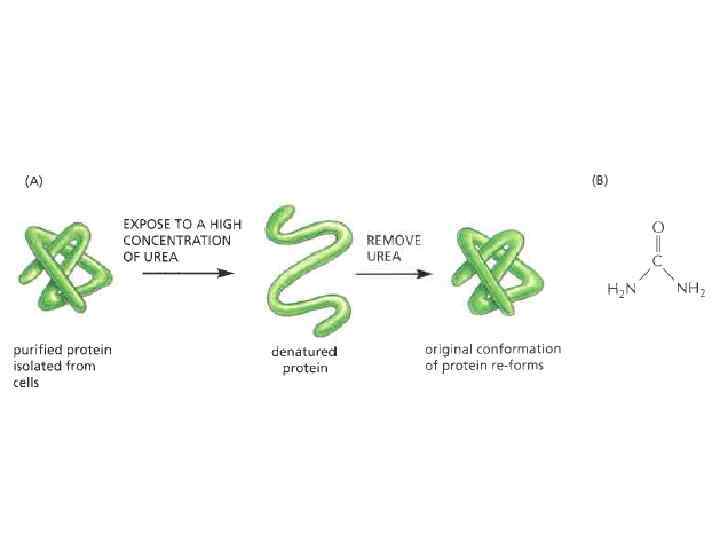
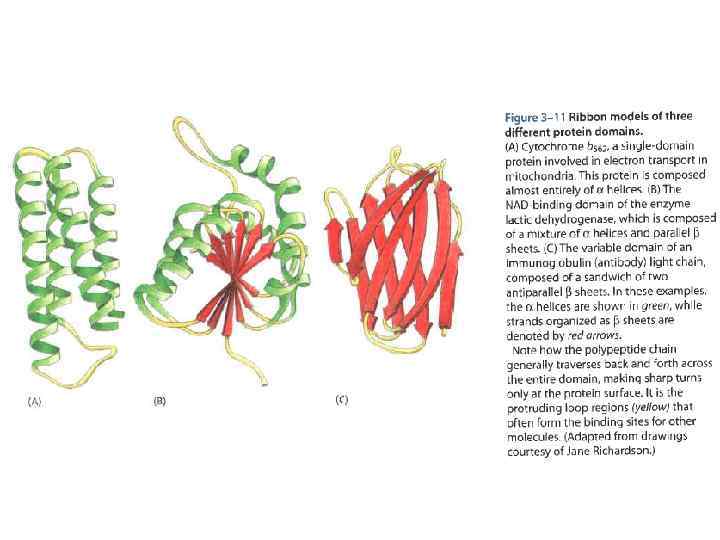
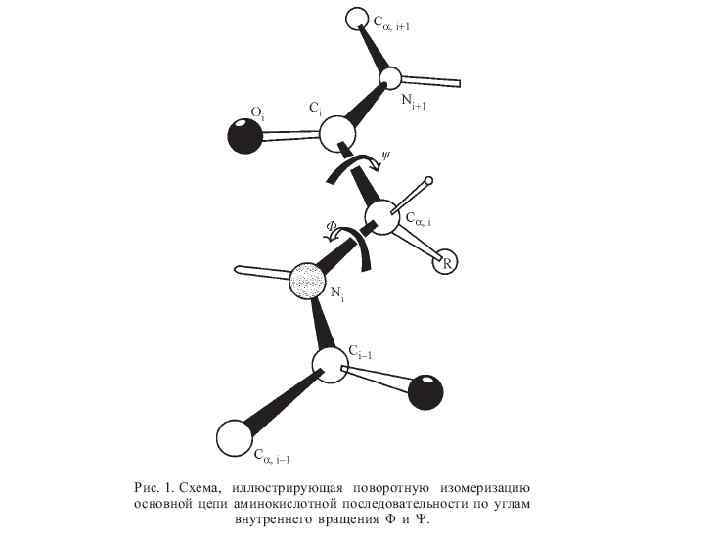
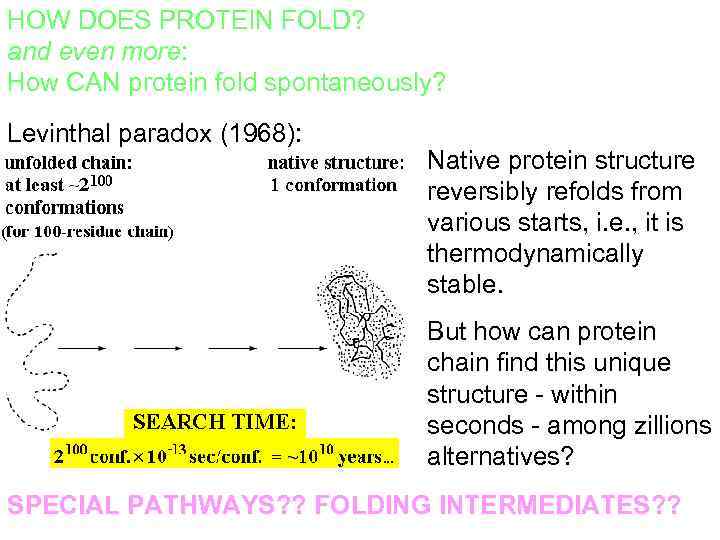
HOW DOES PROTEIN FOLD? and even more: How CAN protein fold spontaneously? Levinthal paradox (1968): Native protein structure reversibly refolds from various starts, i. e. , it is thermodynamically stable. But how can protein chain find this unique structure - within seconds - among zillions alternatives? SPECIAL PATHWAYS? ? FOLDING INTERMEDIATES? ?
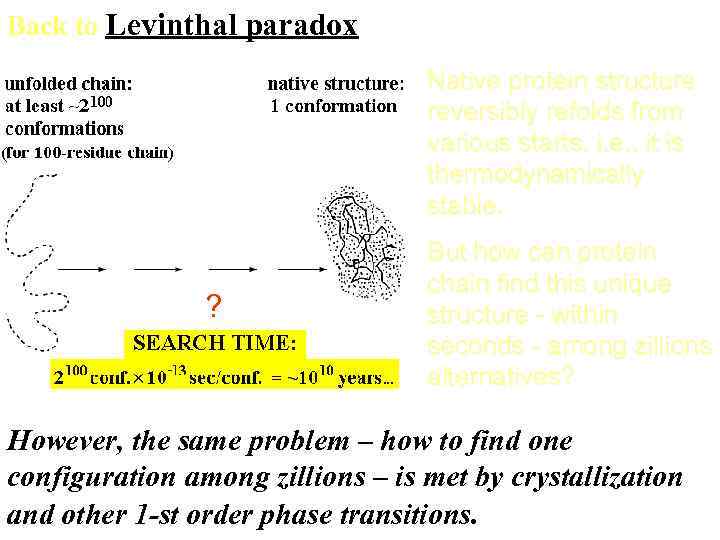
Back to Levinthal paradox Native protein structure reversibly refolds from various starts, i. e. , it is thermodynamically stable. ? But how can protein chain find this unique structure - within seconds - among zillions alternatives? However, the same problem – how to find one configuration among zillions – is met by crystallization and other 1 -st order phase transitions.
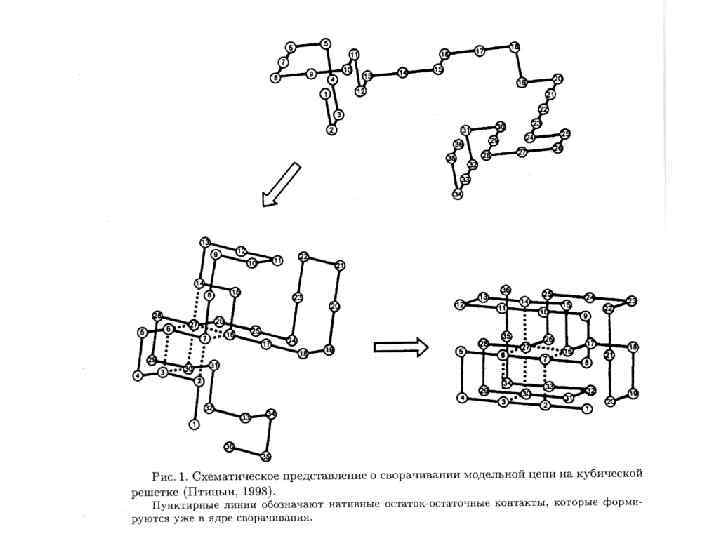
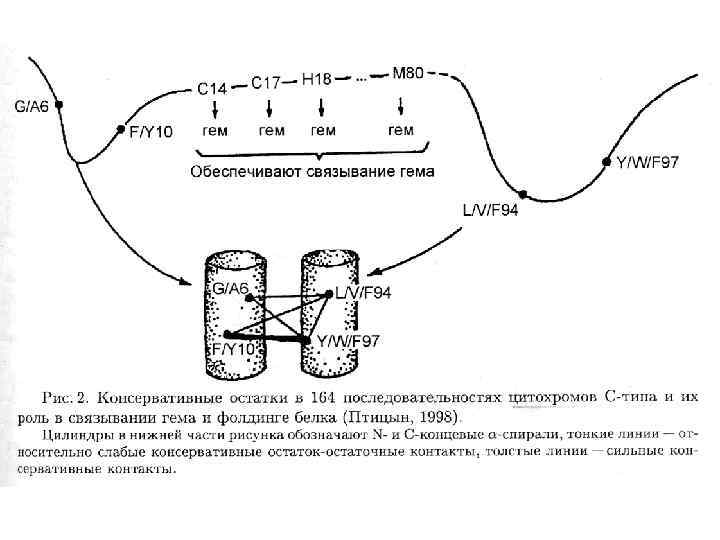
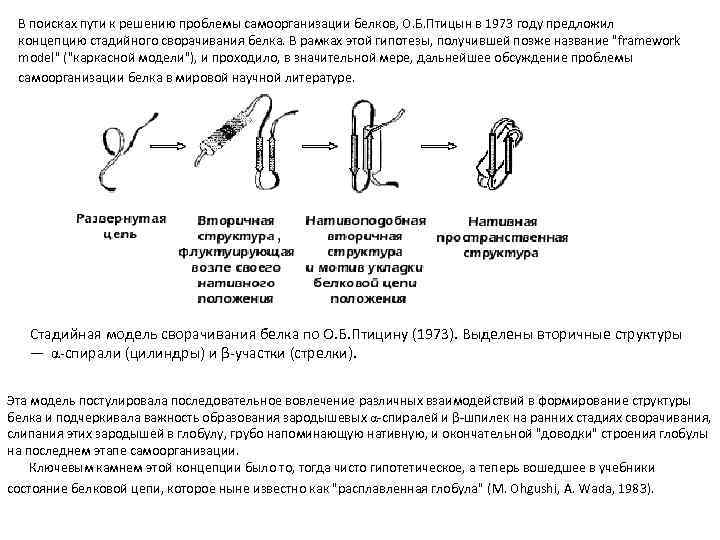
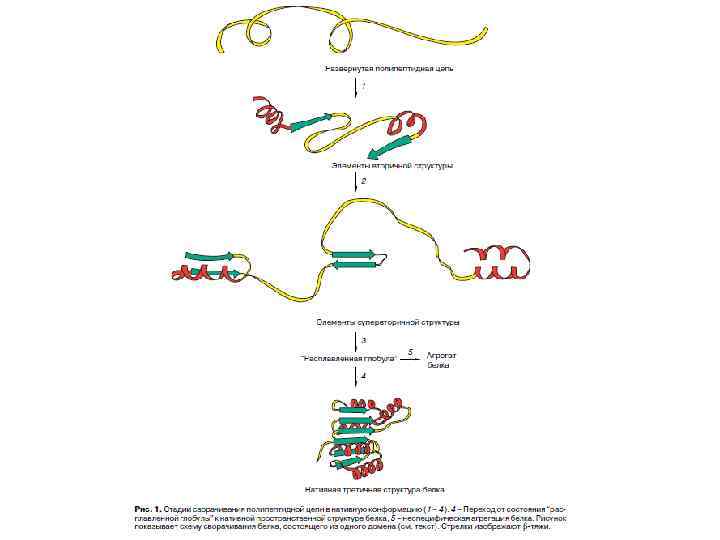
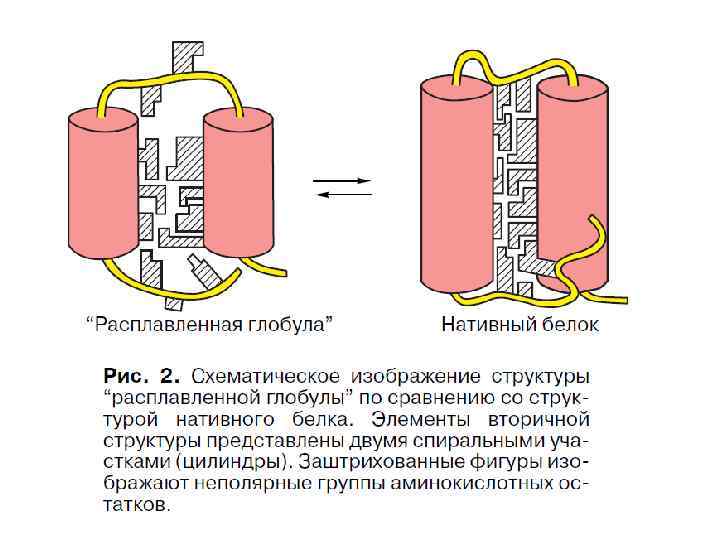
В поисках пути к решению проблемы самоорганизации белков, О. Б. Птицын в 1973 году предложил концепцию стадийного сворачивания белка. В рамках этой гипотезы, получившей позже название "framework model" ("каркасной модели"), и проходило, в значительной мере, дальнейшее обсуждение проблемы самоорганизации белка в мировой научной литературе. Стадийная модель сворачивания белка по О. Б. Птицину (1973). Выделены вторичные структуры — α-спирали (цилиндры) и β-участки (стрелки). Эта модель постулировала последовательное вовлечение различных взаимодействий в формирование структуры белка и подчеркивала важность образования зародышевых α-спиралей и β-шпилек на ранних стадиях сворачивания, слипания этих зародышей в глобулу, грубо напоминающую нативную, и окончательной "доводки" строения глобулы на последнем этапе самоорганизации. Ключевым камнем этой концепции было то, тогда чисто гипотетическое, а теперь вошедшее в учебники состояние белковой цепи, которое ныне известно как "расплавленная глобула" (M. Ohgushi, A. Wada, 1983).
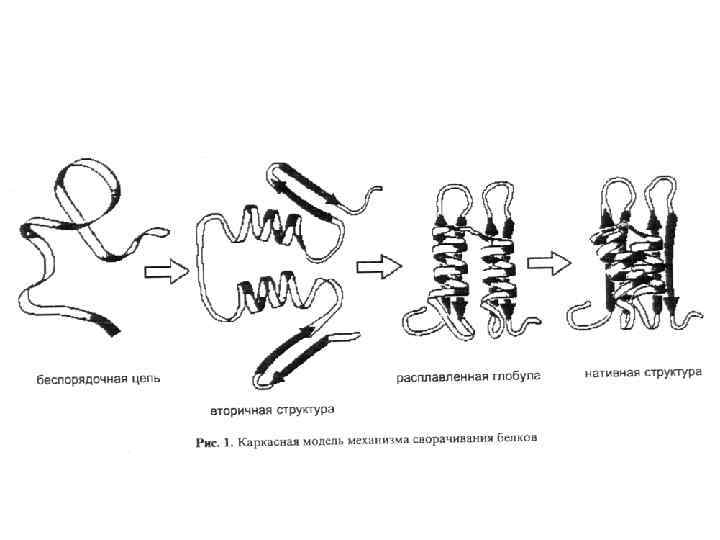
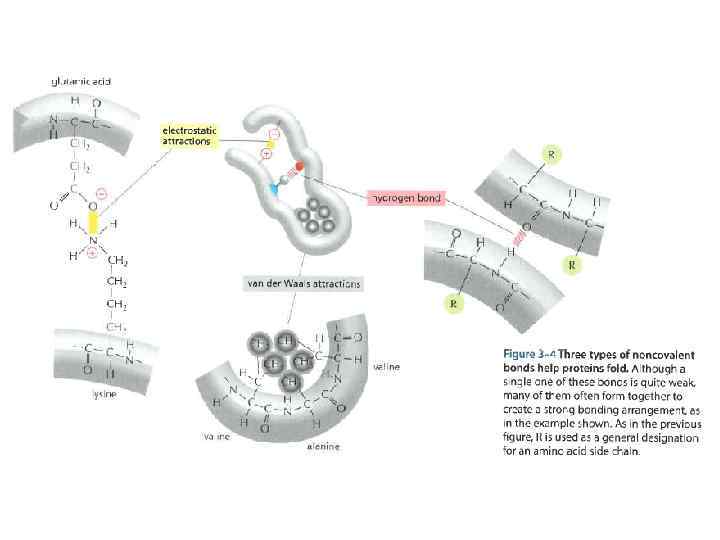
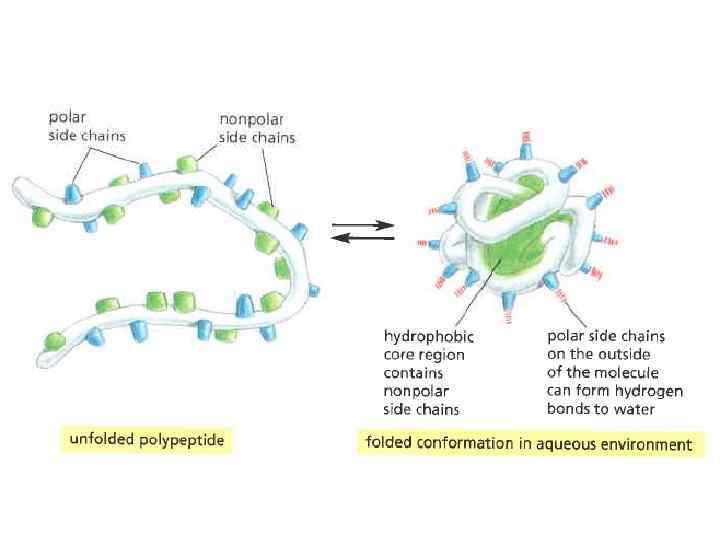
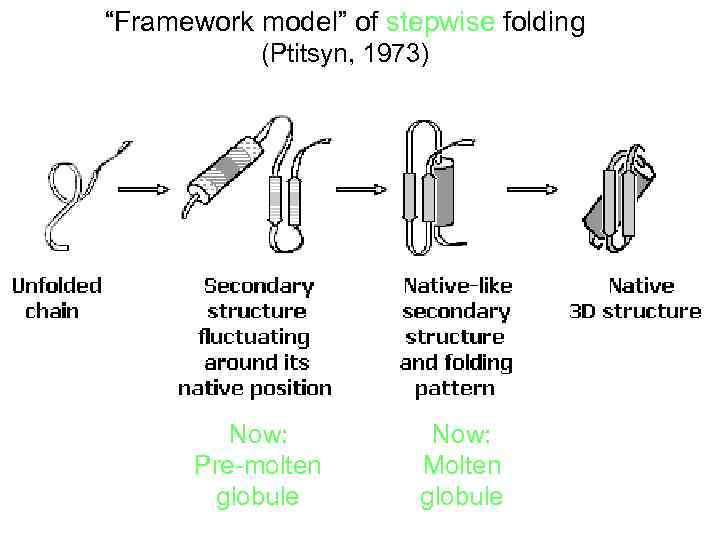
“Framework model” of stepwise folding (Ptitsyn, 1973) Now: Pre-molten globule Now: Molten globule
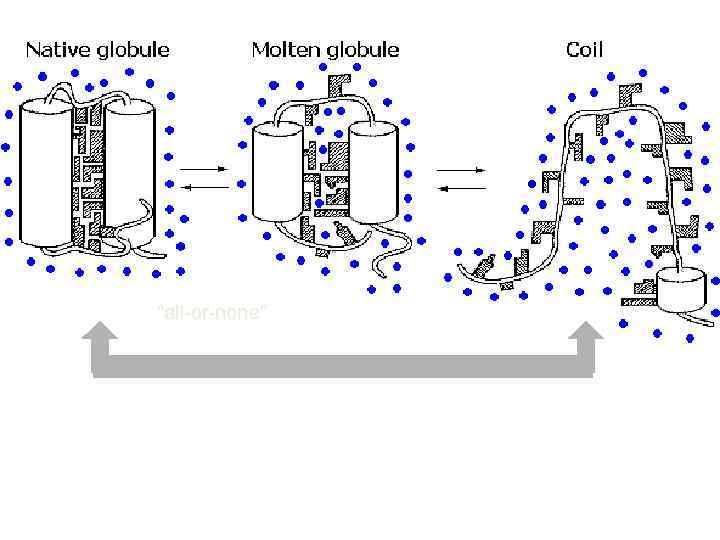
“all-or-none”
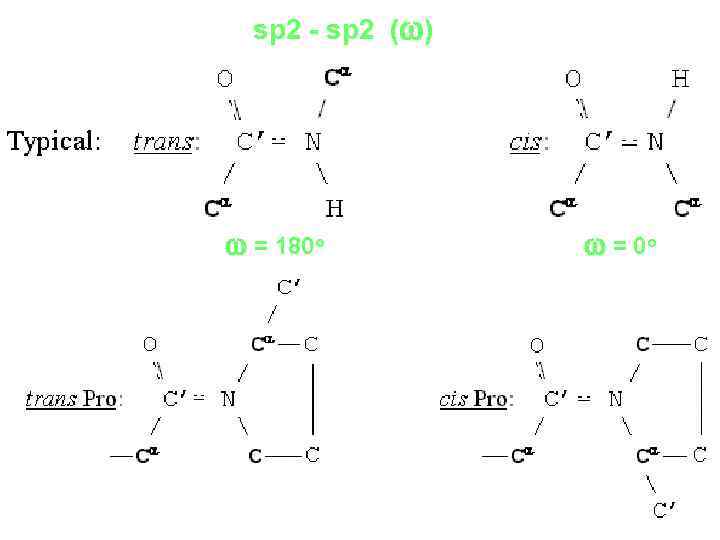
sp 2 - sp 2 (w) w = 180 o w = 0 o
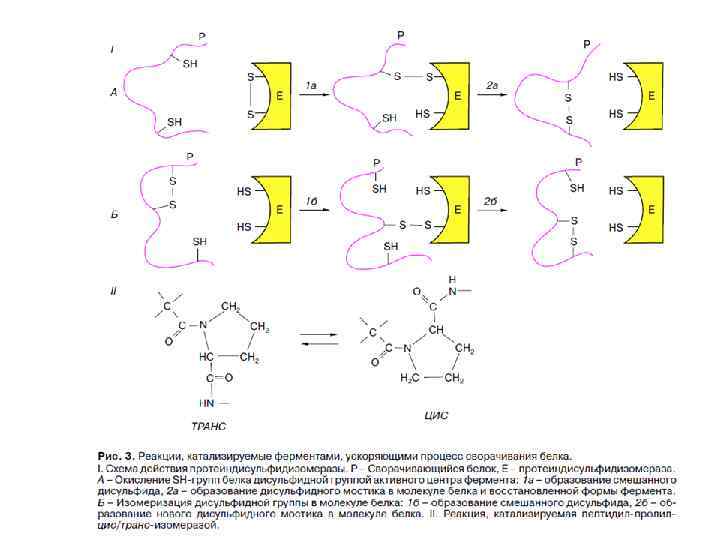
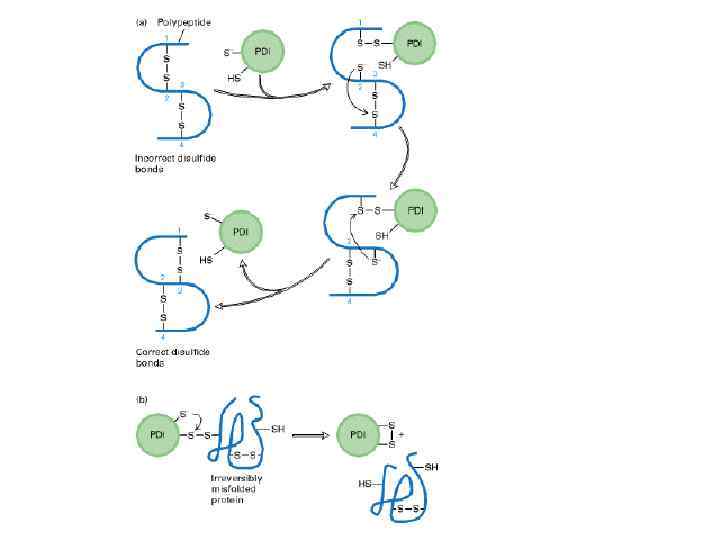
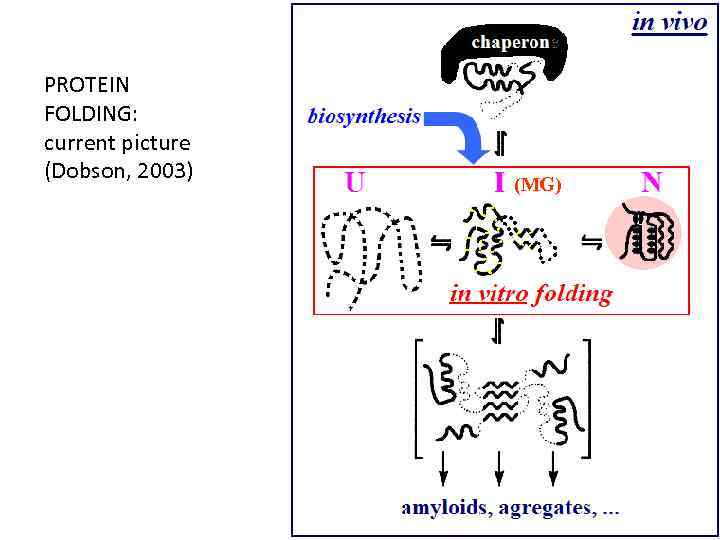
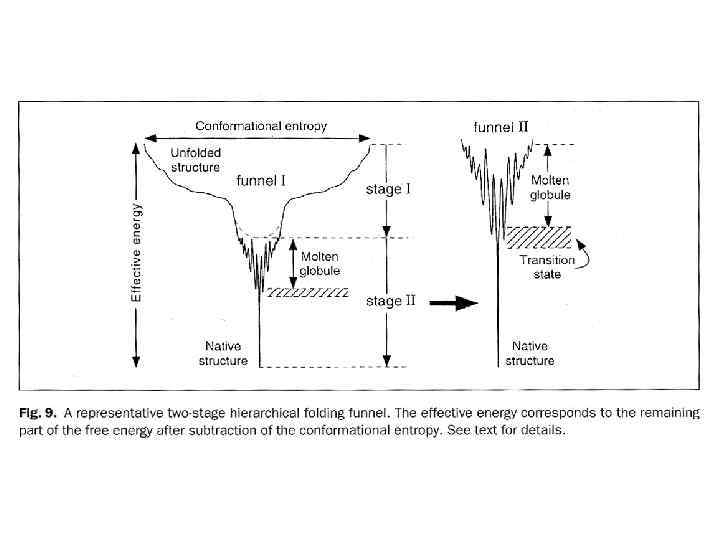
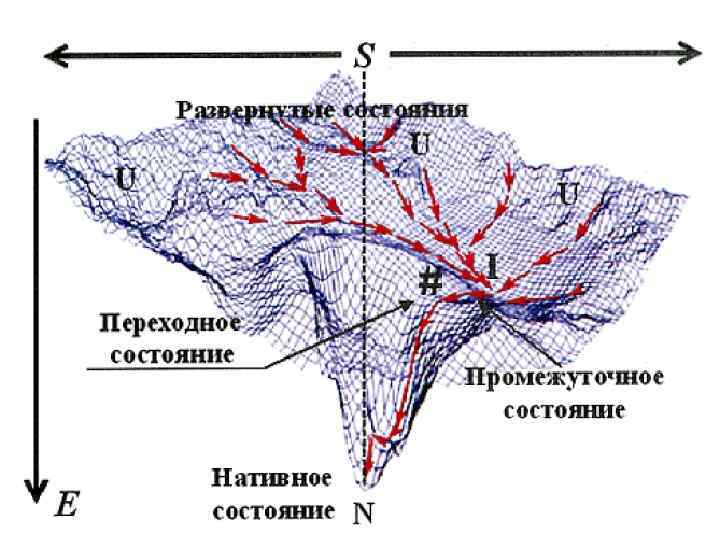
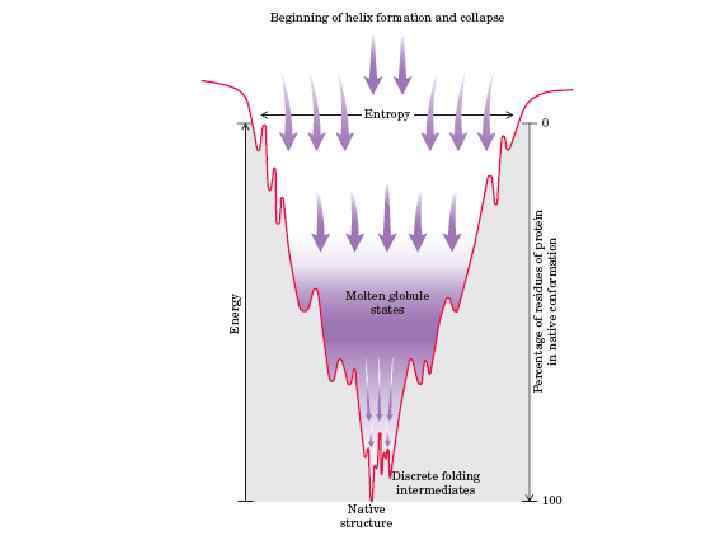
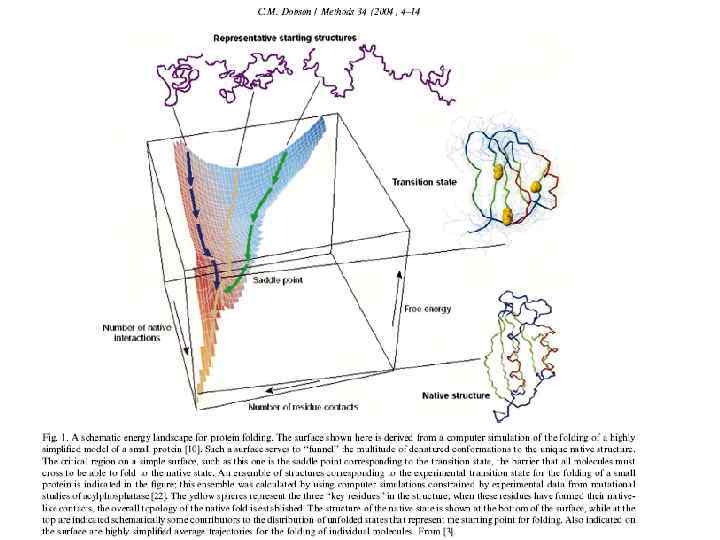
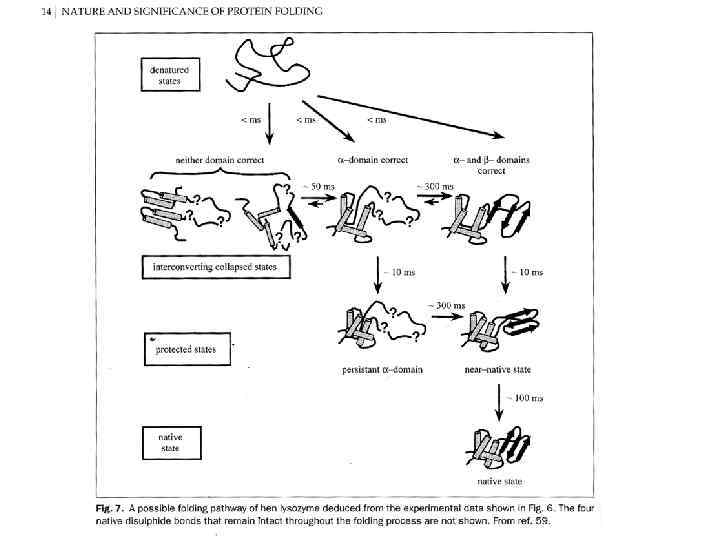
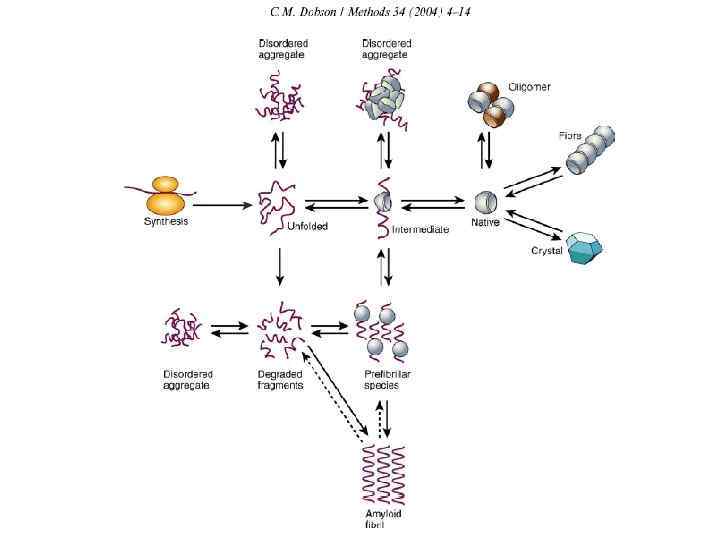
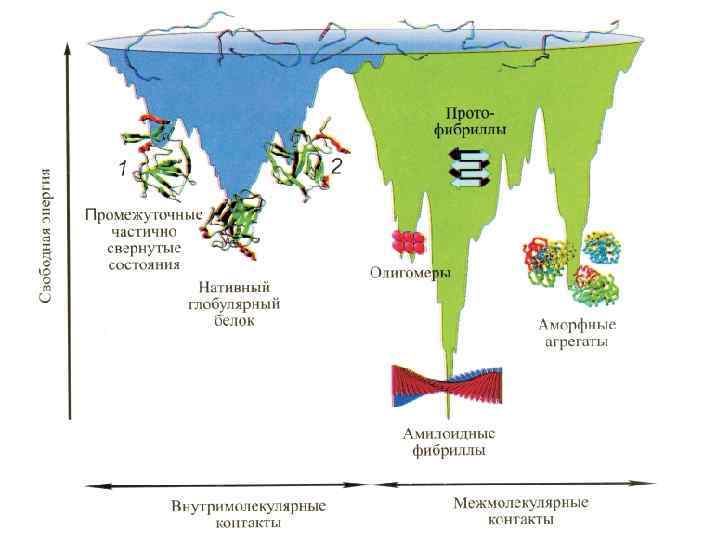
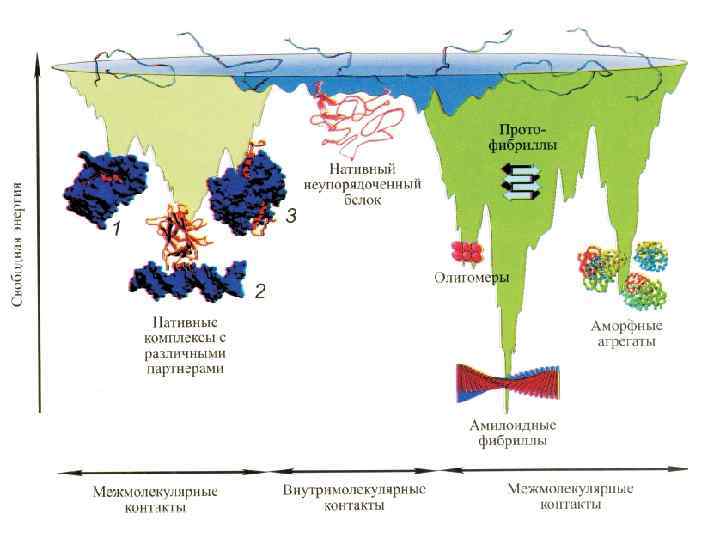
e PROTEIN FOLDING: current picture (Dobson, 2003) (MG)
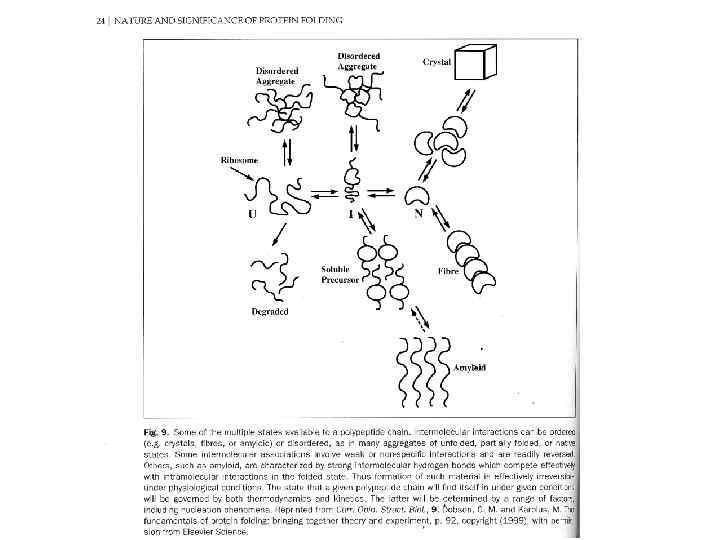
Патологии фолдинга • Многие болезни связаны с неправильным фолдингом. • Первой из таких болезней была описана куру в начале 1950 -х годов D. Carleton Gadjusek. Это неврологическое расстройство, встречающееся у аборигенов Новой Гвинеи. • Симптомы куру, что буквально означает "trembling with fear", подобны таковым для скрепи (болезнь овец) и болезни Крейцфельда-Якоба у людей.
Фолдинг белков и прионы • Причина куру, скрепи, болезни Крейцфельда-Якоба заключается в присутствии ненормальной формы нормального белка, называемой прионом. Таким образом мы можем рассматривать прионы как антишапероны. • Идея рассмотрения белков в качестве инфекционных агентов принадлежит Stan Prusiner.
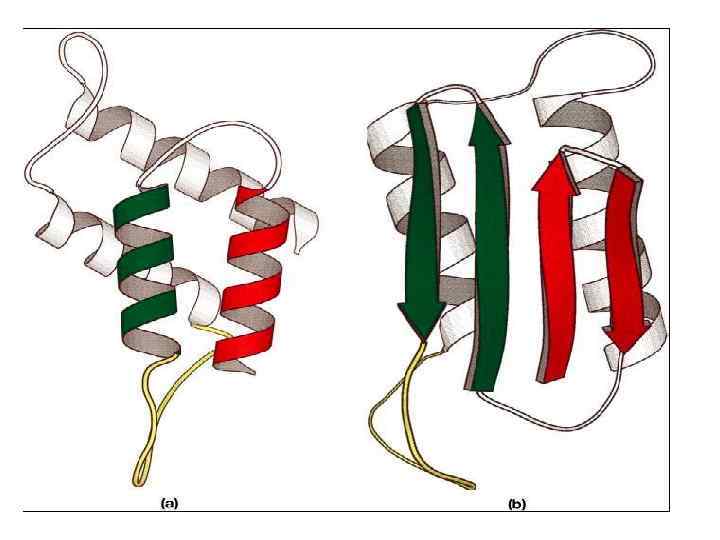
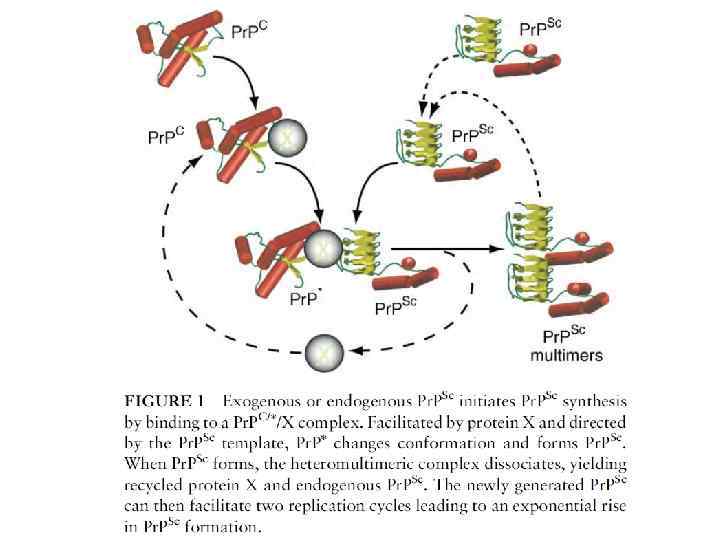
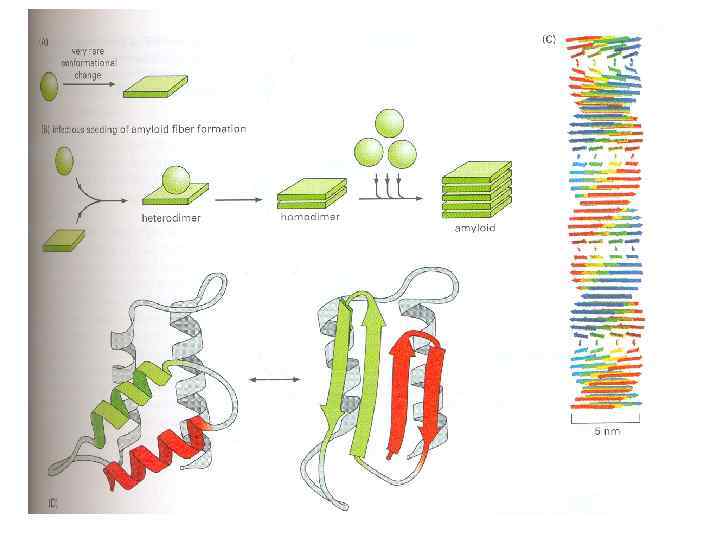
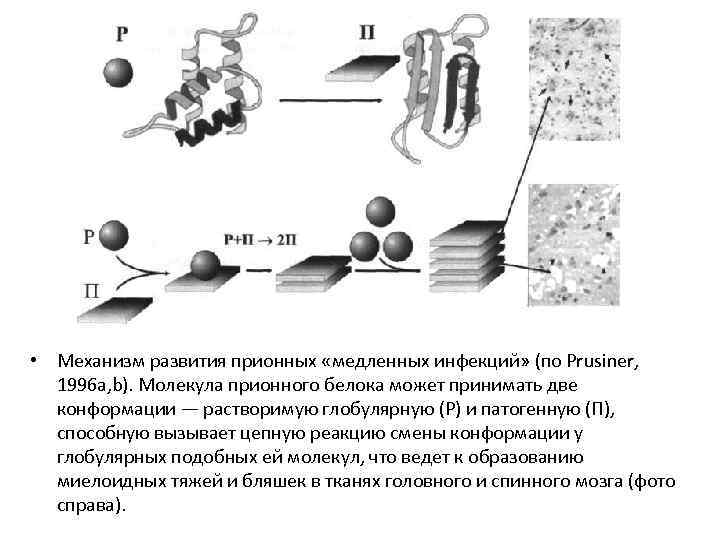
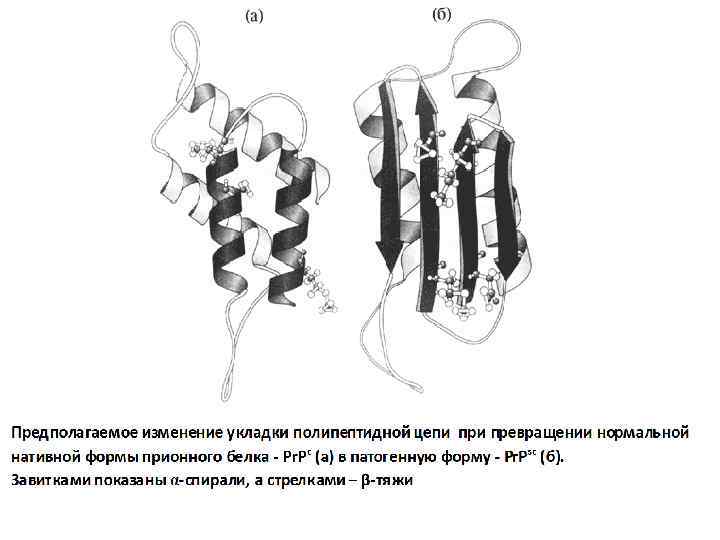
• Механизм развития прионных «медленных инфекций» (по Prusiner, 1996 a, b). Молекула прионного белока может принимать две конформации — растворимую глобулярную (Р) и патогенную (П), способную вызывает цепную реакцию смены конформации у глобулярных подобных ей молекул, что ведет к образованию миелоидных тяжей и бляшек в тканях головного и спинного мозга (фото справа).
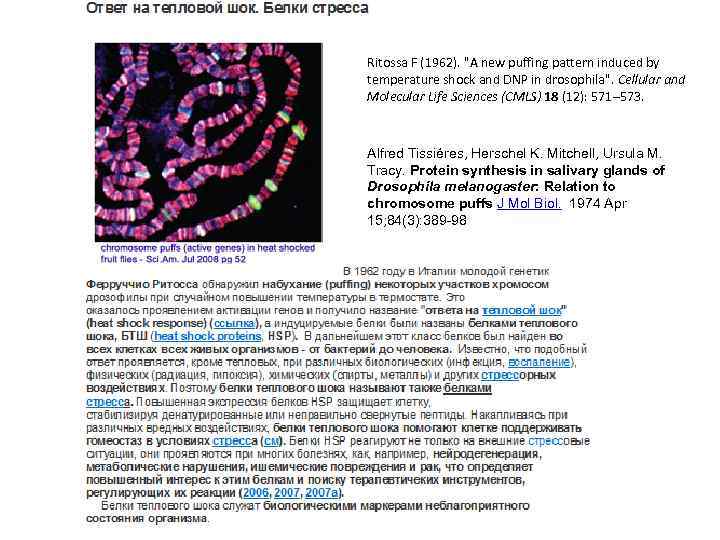
Ritossa F (1962). "A new puffing pattern induced by temperature shock and DNP in drosophila". Cellular and Molecular Life Sciences (CMLS) 18 (12): 571– 573. Alfred Tissiéres, Herschel K. Mitchell, Ursula M. Tracy. Protein synthesis in salivary glands of Drosophila melanogaster: Relation to chromosome puffs J Mol Biol. 1974 Apr 15; 84(3): 389 -98

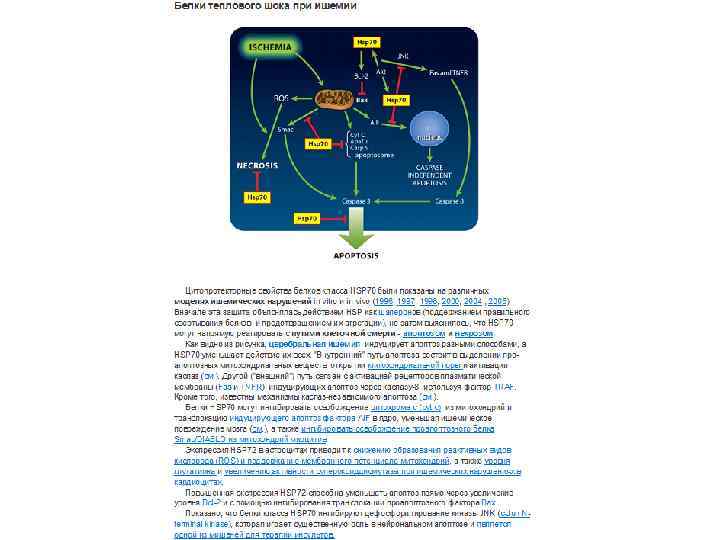

NEF
![Eukaryotes NAC Hsp 70 system prefoldin Archaea NAC [Hsp 70 system] prefoldin Bacteria Trigger Eukaryotes NAC Hsp 70 system prefoldin Archaea NAC [Hsp 70 system] prefoldin Bacteria Trigger](https://present5.com/presentation/182635565_172546575/image-96.jpg)
Eukaryotes NAC Hsp 70 system prefoldin Archaea NAC [Hsp 70 system] prefoldin Bacteria Trigger Factor Hsp 70 system - chaperonins (group II) (Hsp 60) chaperonins (group I) (Hsp 60) small Hsps [small Hsps] Hsp 90 AAA ATPases (Hsp 100) - [Hsp 90] AAA ATPases (Hsp 100) Sec. B [Pap. D/Fim. C] Hip, Hop, Bag, clusterin, cofactors A-E, calnexin, calreticulin, etc. - -

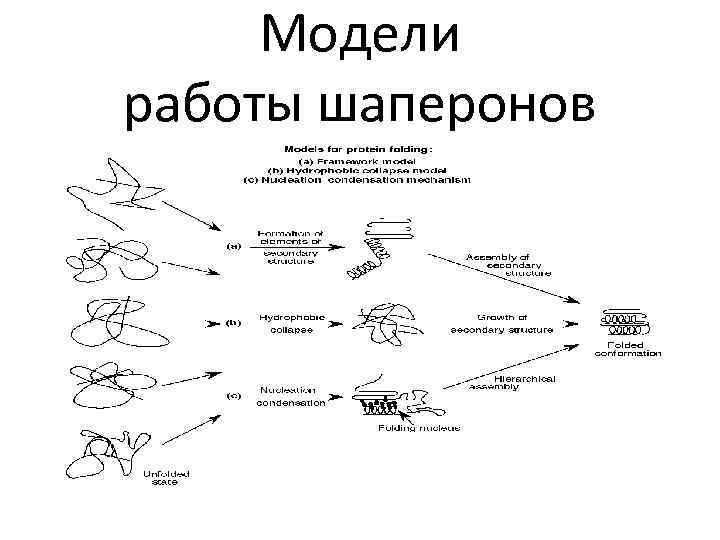
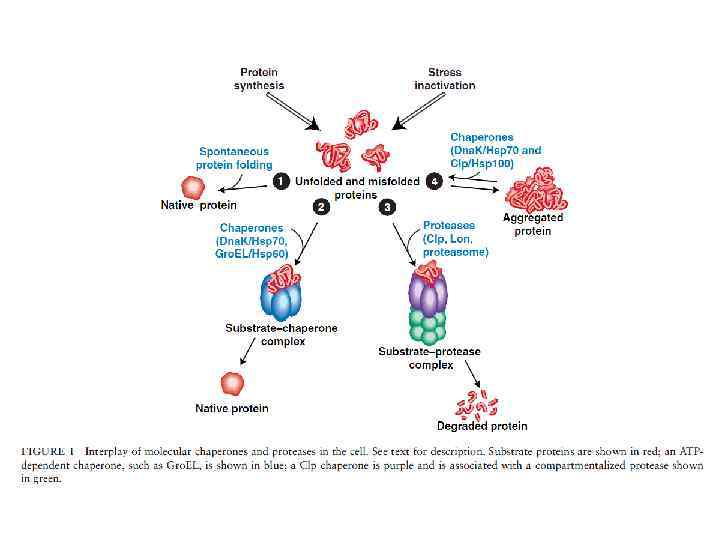
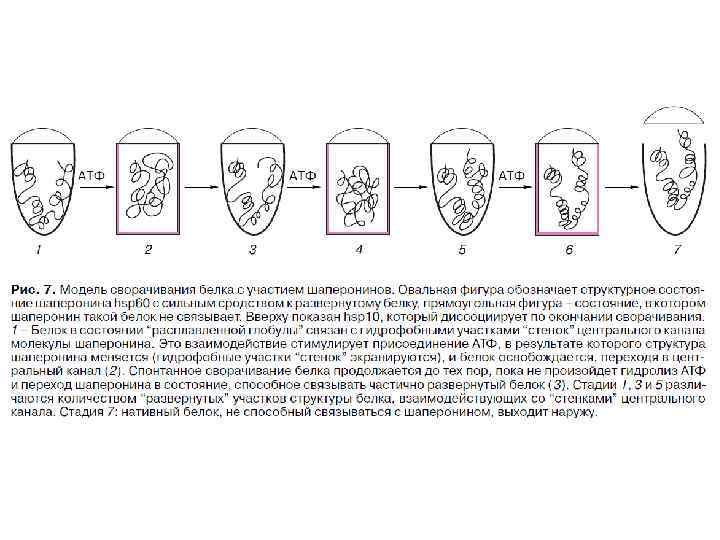
Модели работы шаперонов
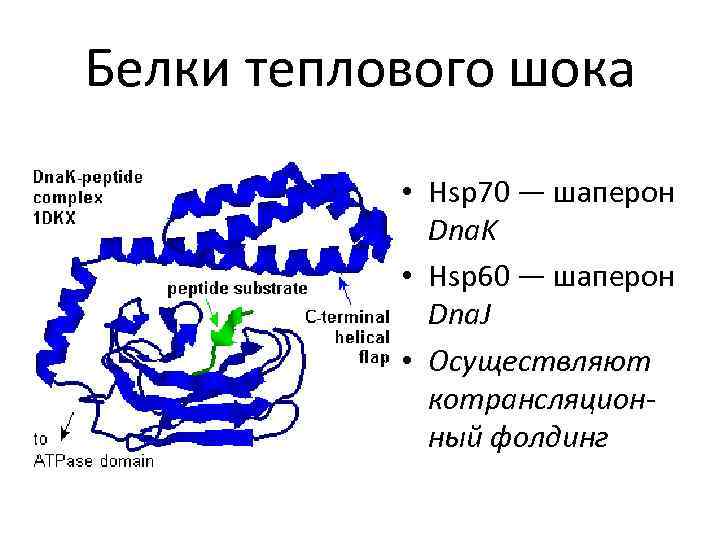
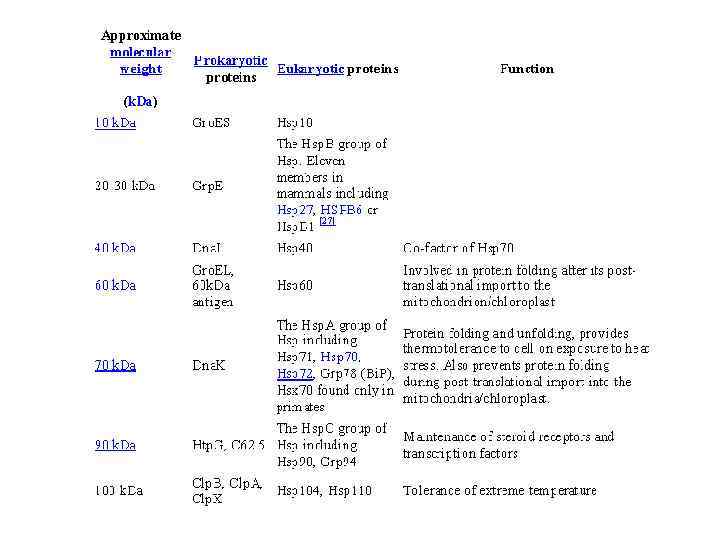
Белки теплового шока • Hsp 70 — шаперон Dna. K • Hsp 60 — шаперон Dna. J • Осуществляют котрансляционный фолдинг
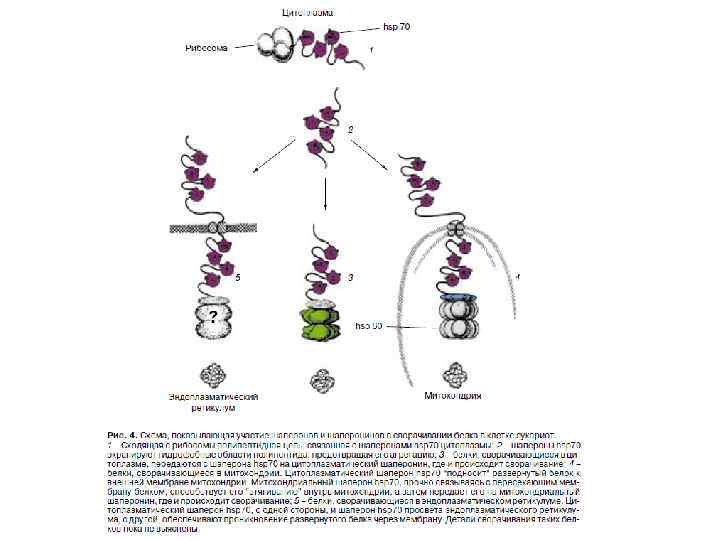
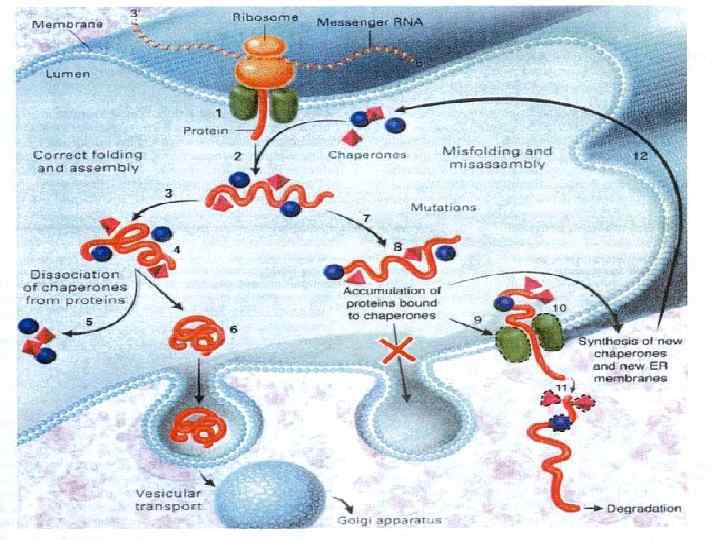
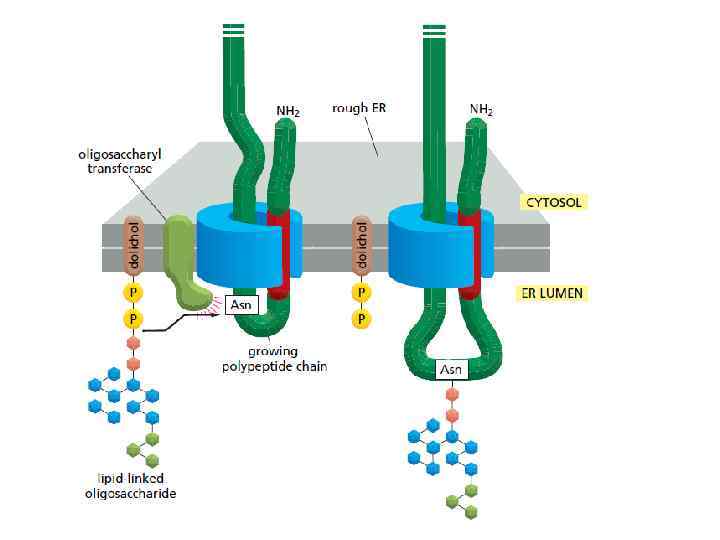
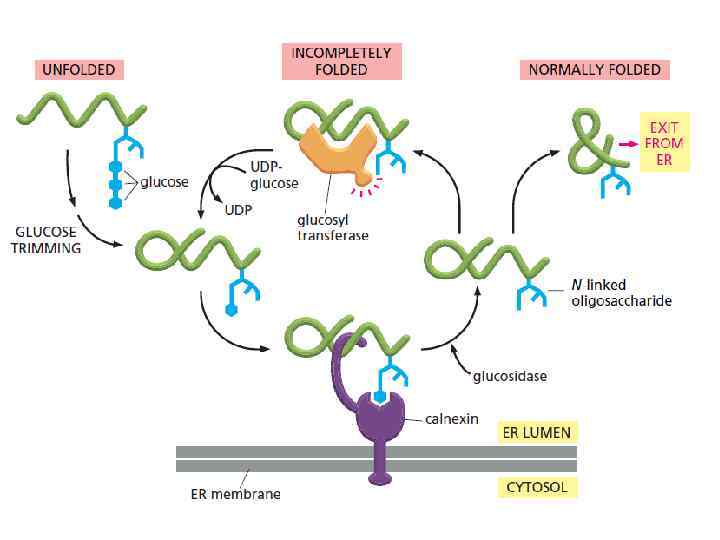
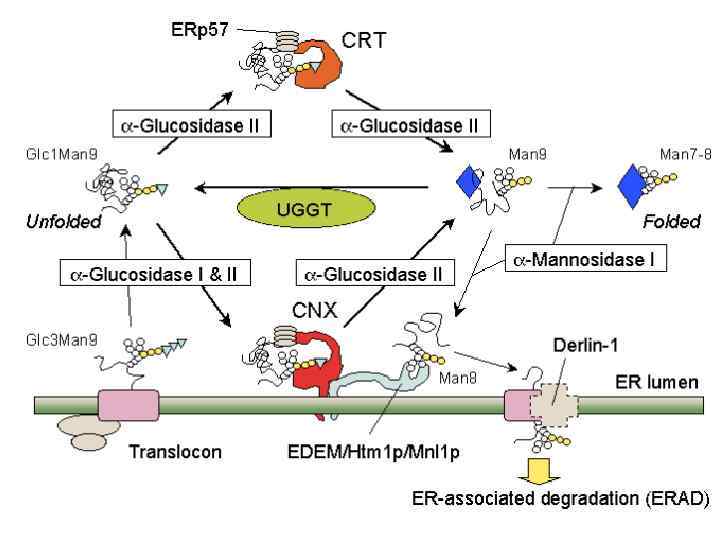
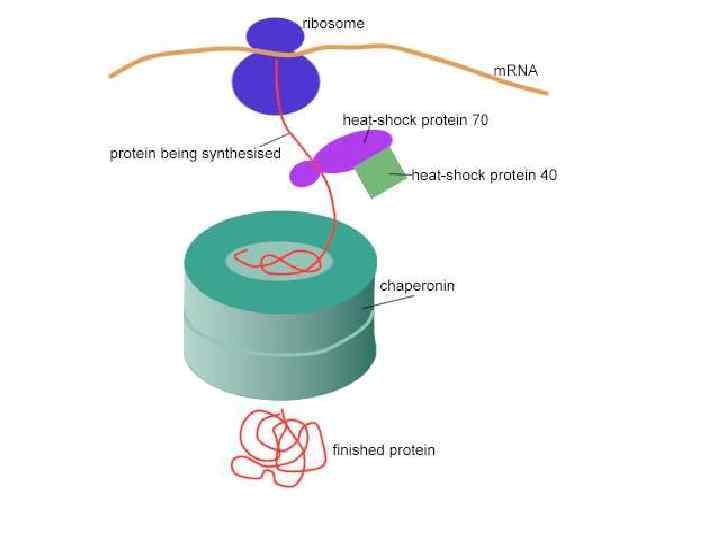
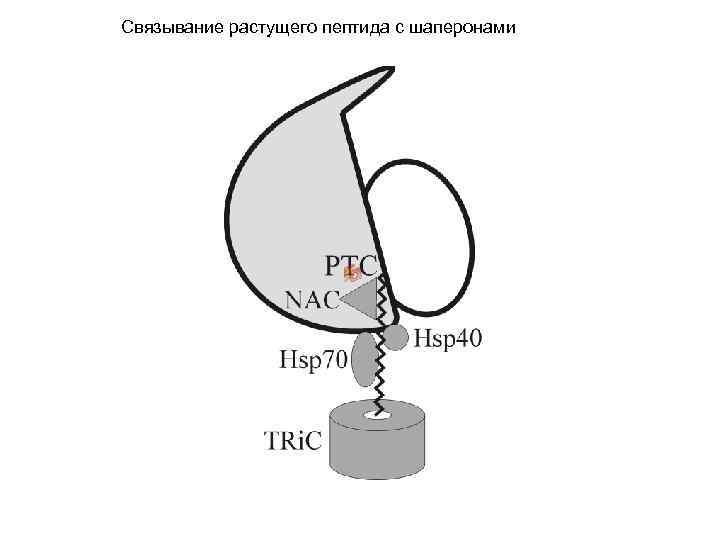
Связывание растущего пептида с шаперонами
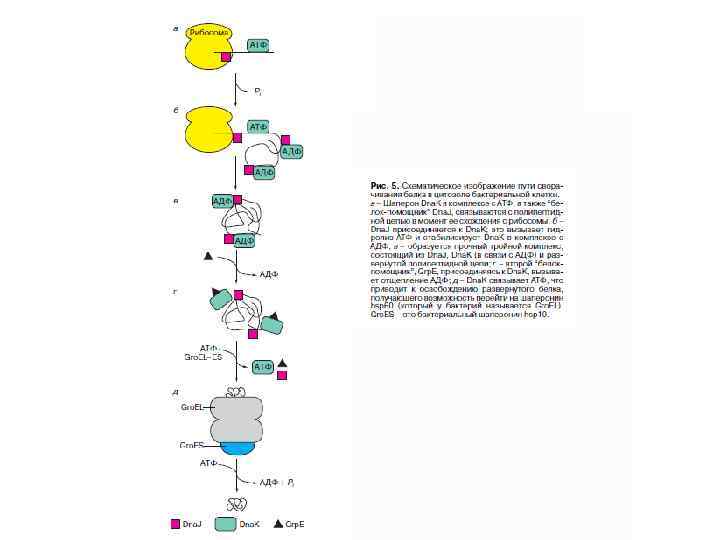
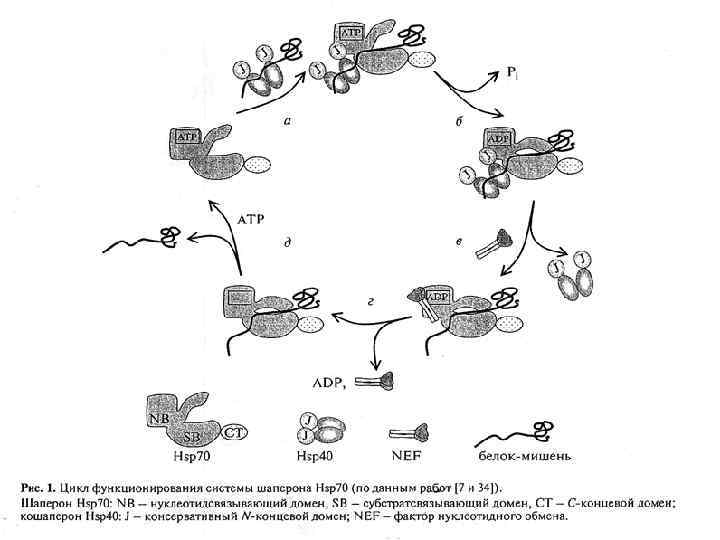
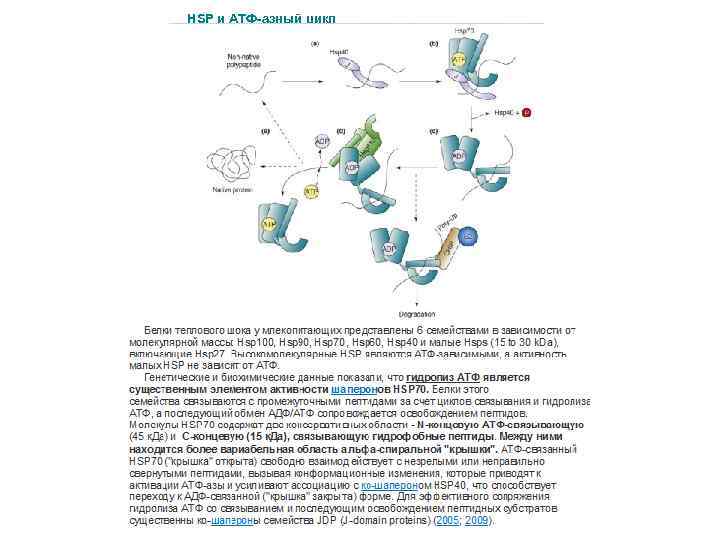
HSP и АТФ-азный цикл
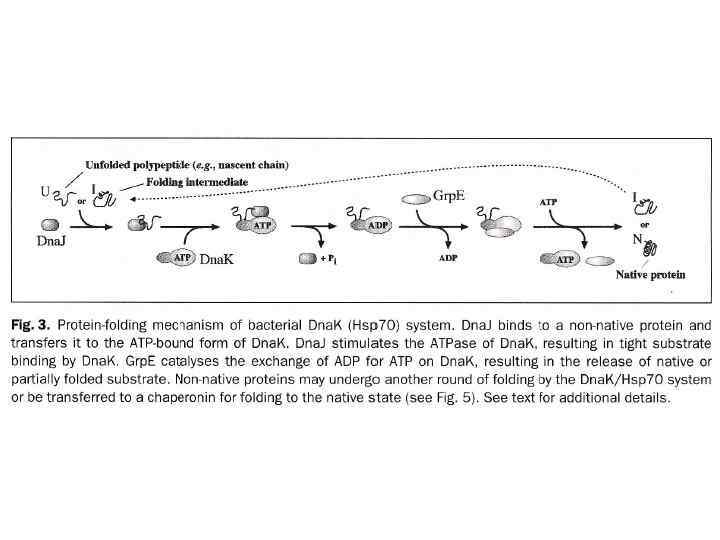
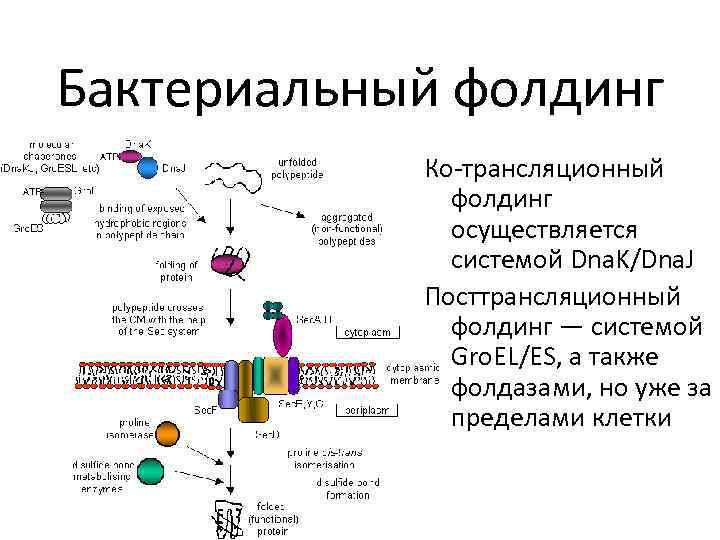
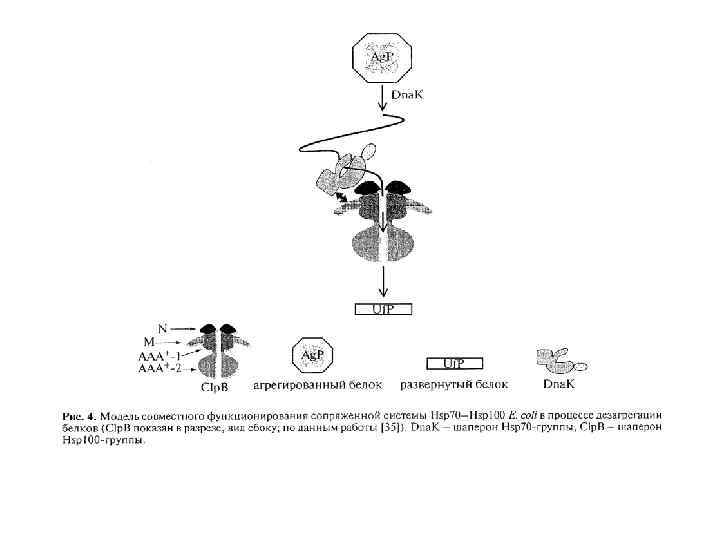
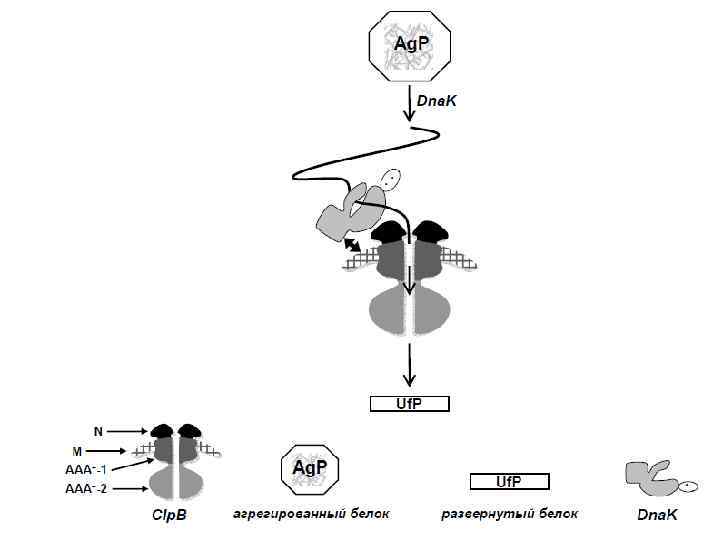
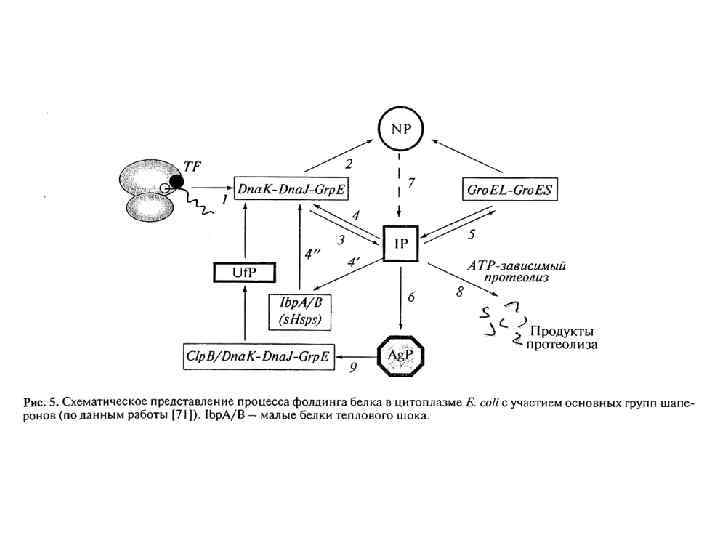
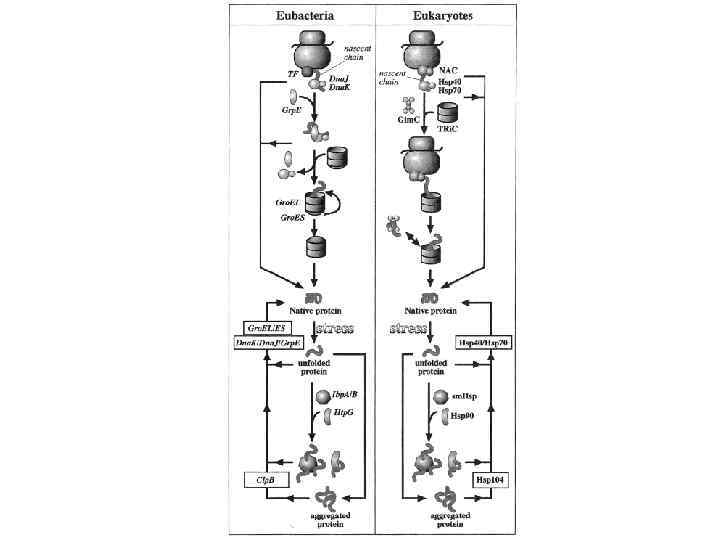
Бактериальный фолдинг Ко-трансляционный фолдинг осуществляется системой Dna. K/Dna. J Посттрансляционный фолдинг — системой Gro. EL/ES, а также фолдазами, но уже за пределами клетки
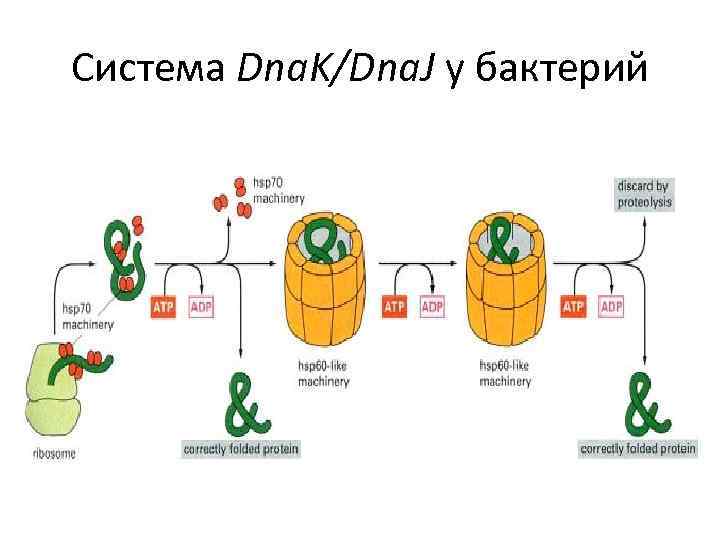
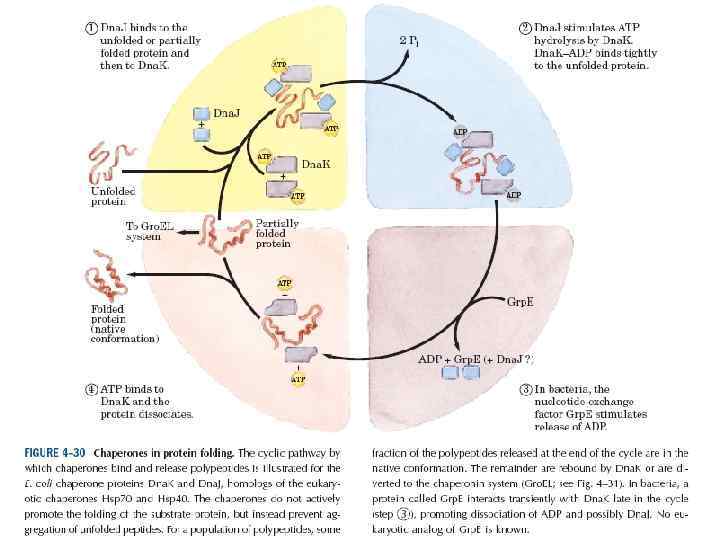
Система Dna. K/Dna. J у бактерий
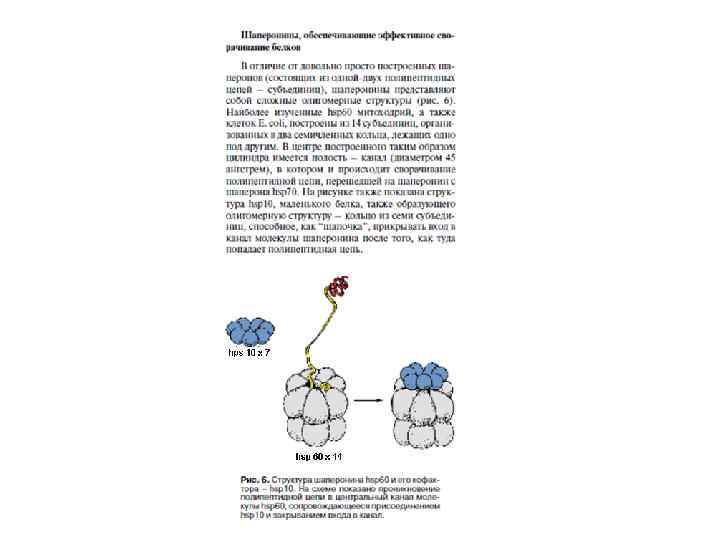
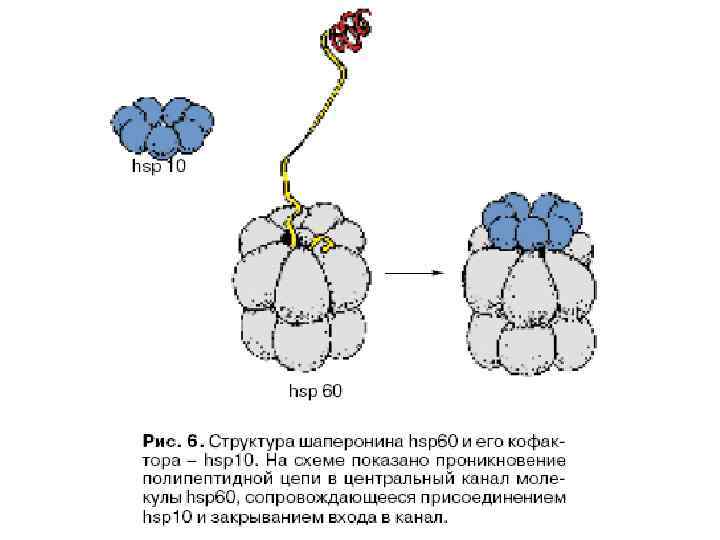
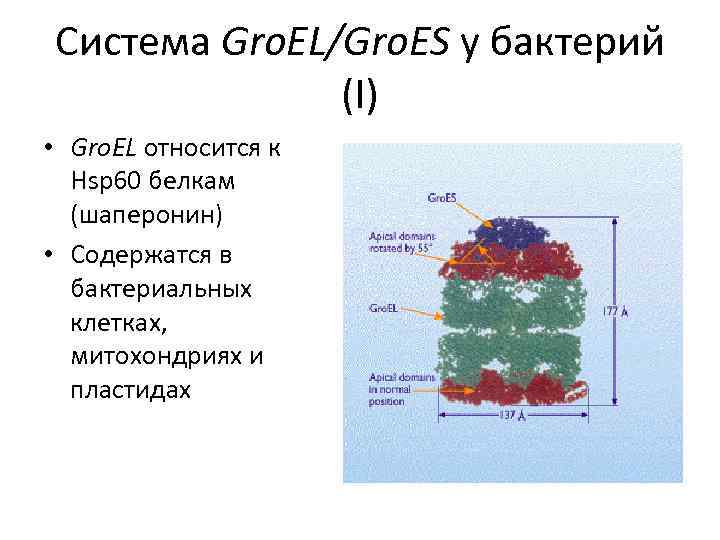
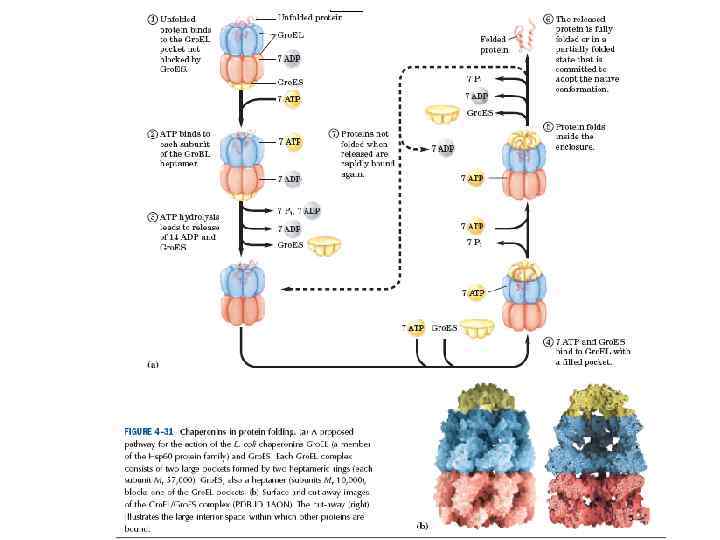
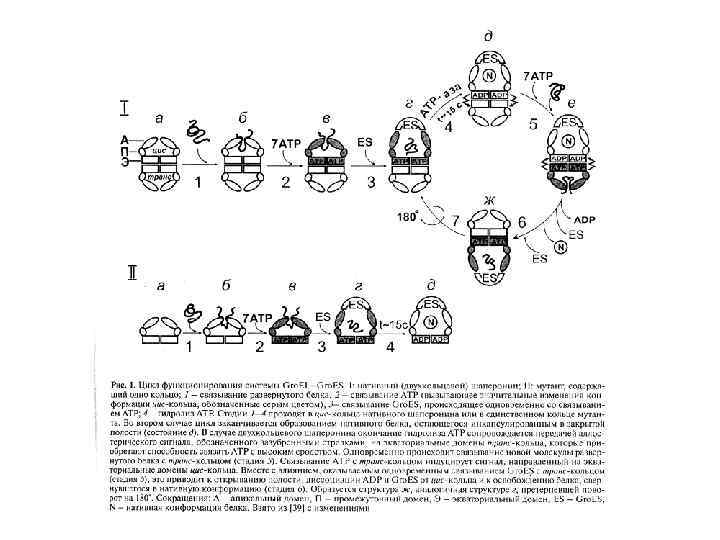
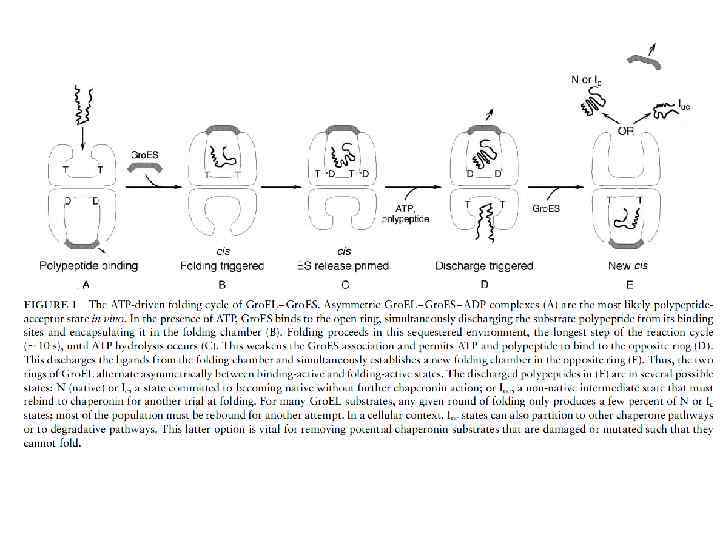
Система Gro. EL/Gro. ES у бактерий (І) • Gro. EL относится к Hsp 60 белкам (шаперонин) • Содержатся в бактериальных клетках, митохондриях и пластидах
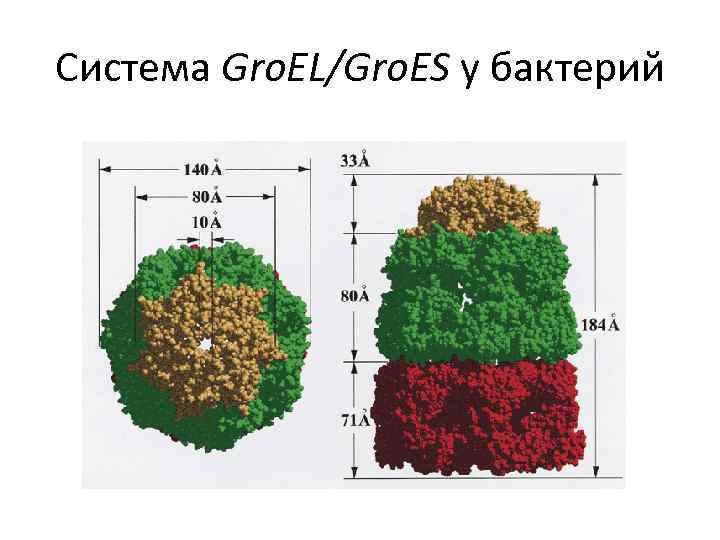
Система Gro. EL/Gro. ES у бактерий
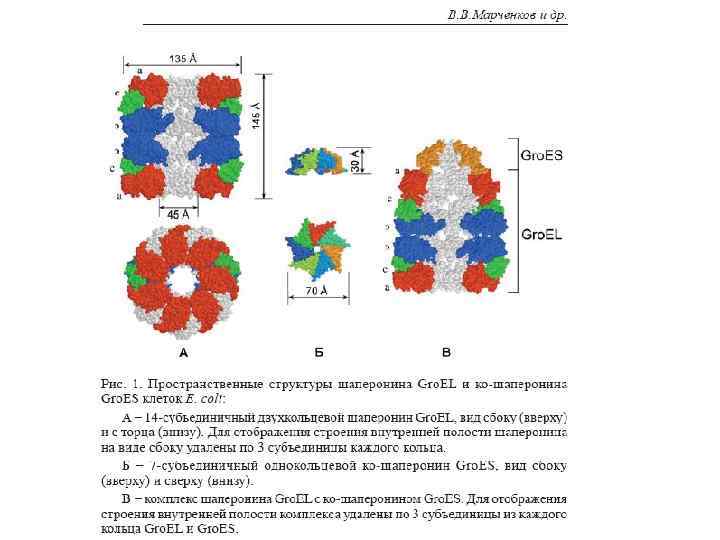
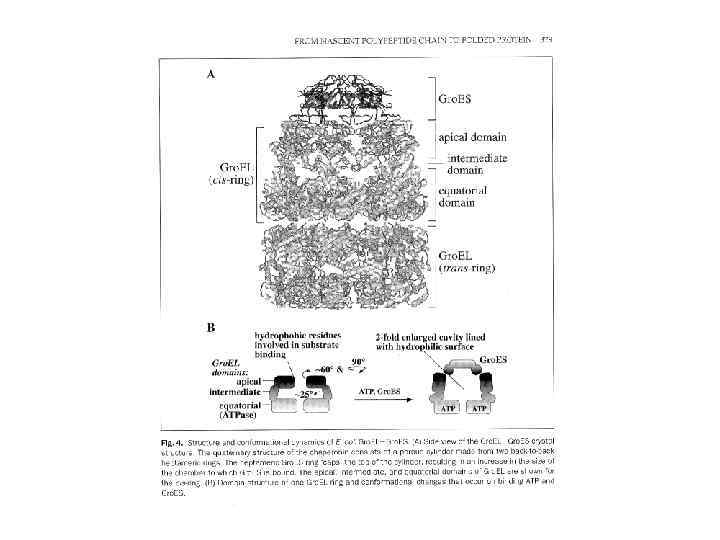
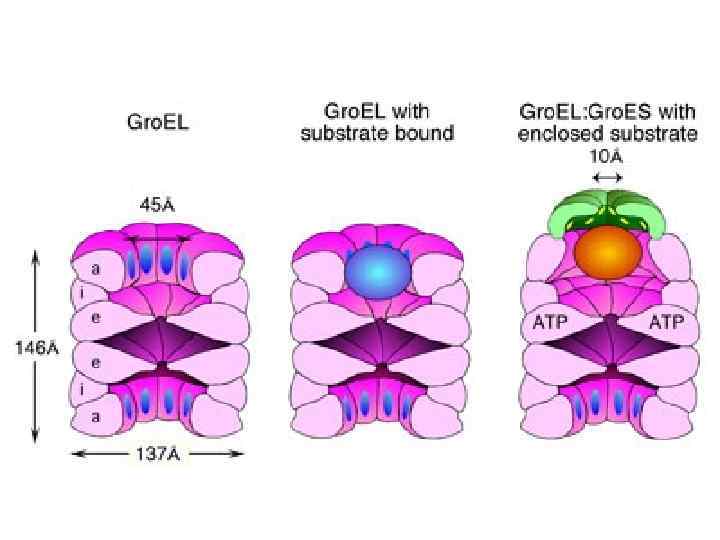
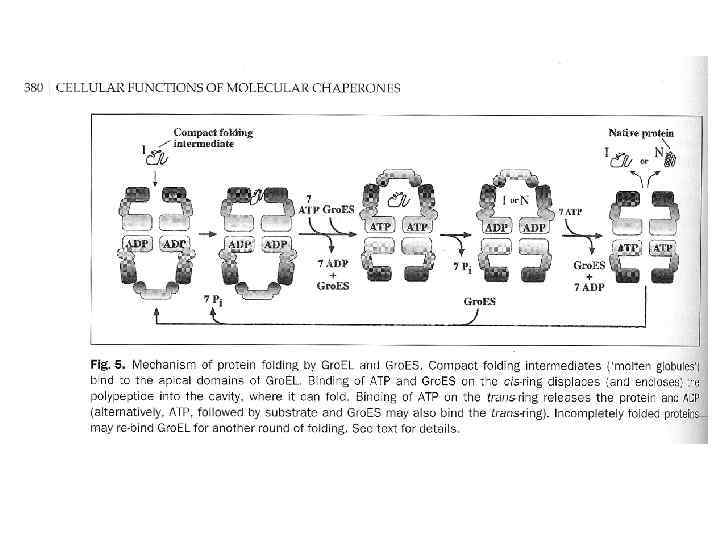
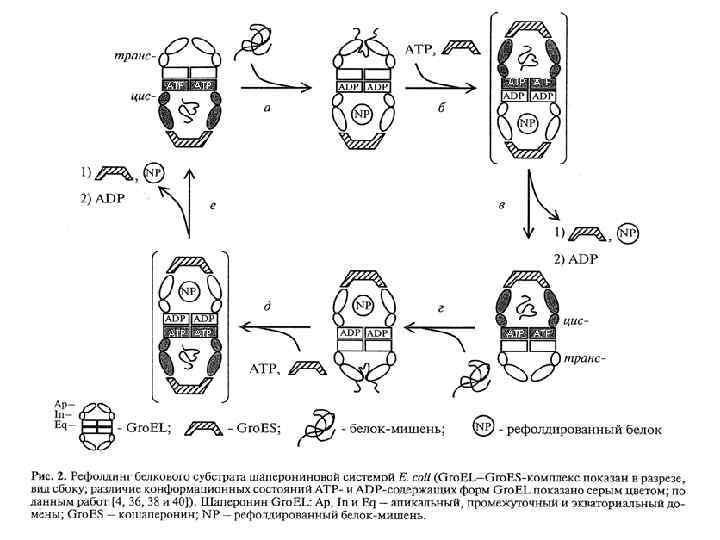
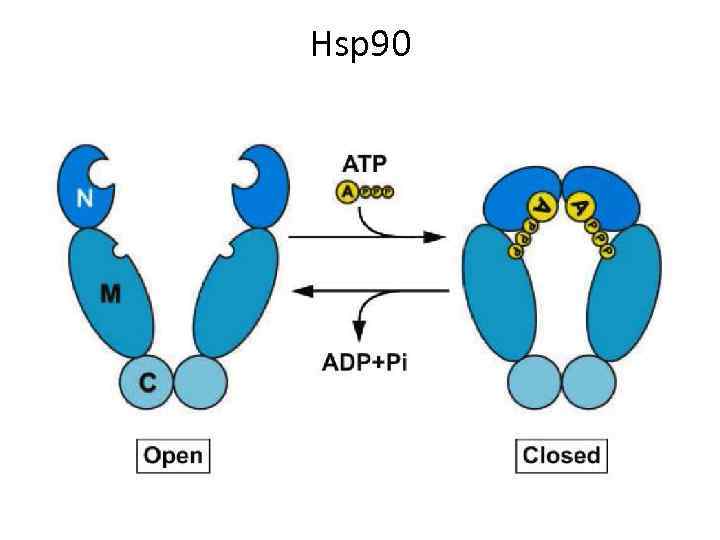
Hsp 90
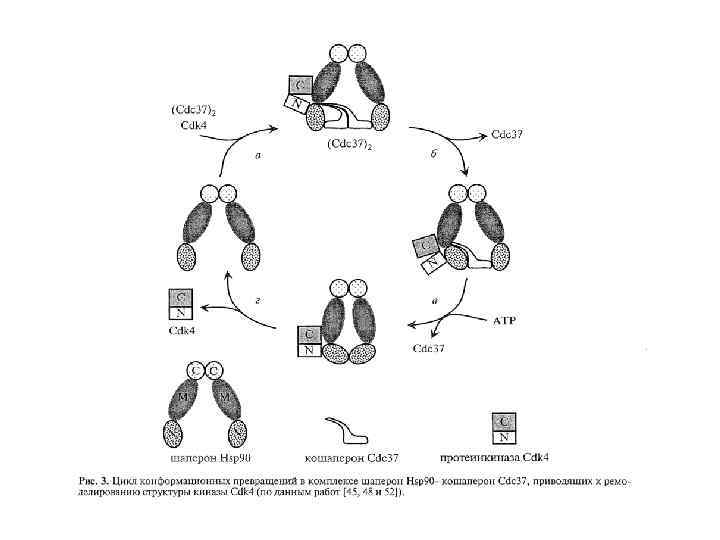
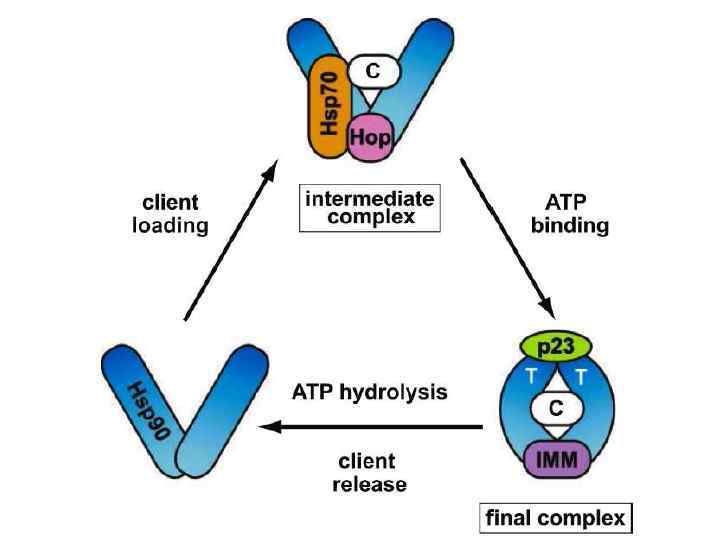
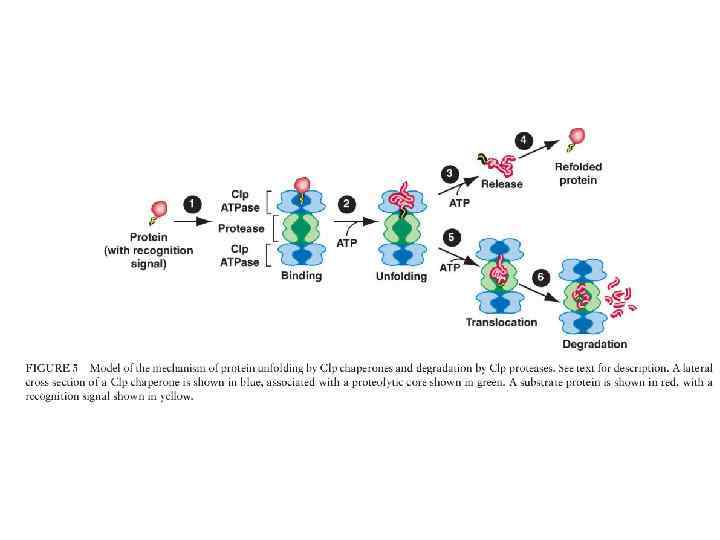

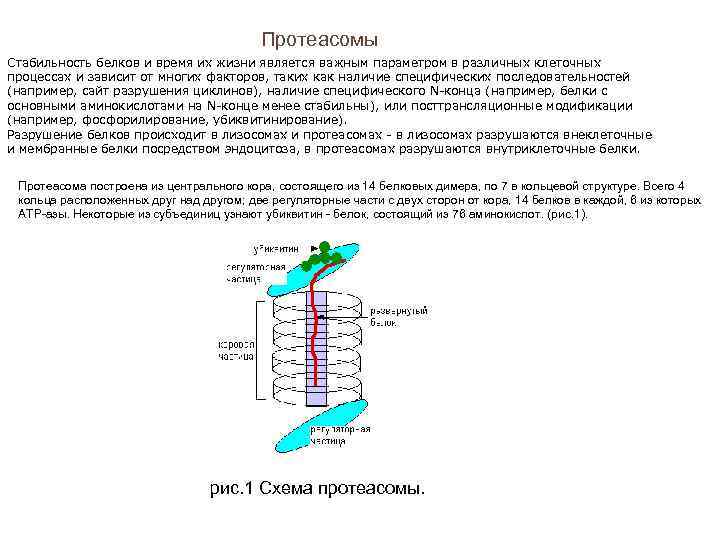
Протеасомы Стабильность белков и время их жизни является важным параметром в различных клеточных процессах и зависит от многих факторов, таких как наличие специфических последовательностей (например, сайт разрушения циклинов), наличие специфического N-конца (например, белки с основными аминокислотами на N-конце менее стабильны), или посттрансляционные модификации (например, фосфорилирование, убиквитинирование). Разрушение белков происходит в лизосомах и протеасомах - в лизосомах разрушаются внеклеточные и мембранные белки посредством эндоцитоза, в протеасомах разрушаются внутриклеточные белки. Протеасома построена из центрального кора, состоящего из 14 белковых димера, по 7 в кольцевой структуре. Всего 4 кольца расположенных друг над другом; две регуляторные части с двух сторон от кора, 14 белков в каждой, 6 из которых ATP-азы. Некоторые из субъединиц узнают убиквитин - белок, состоящий из 76 аминокислот. (рис. 1). рис. 1 Схема протеасомы.
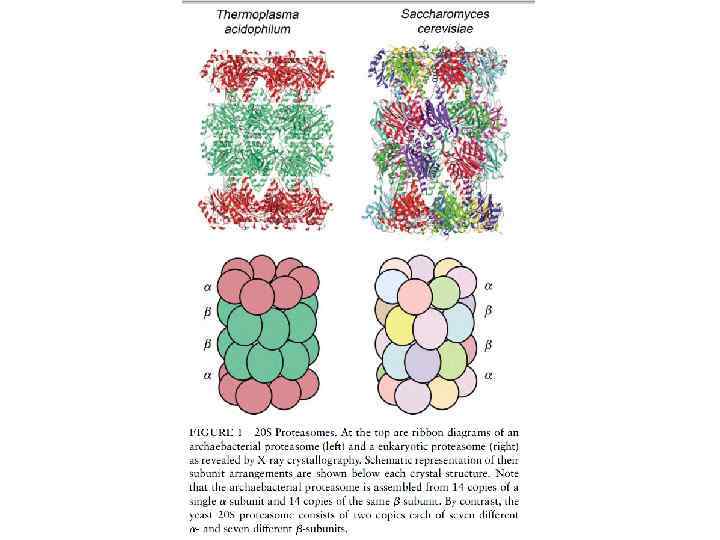
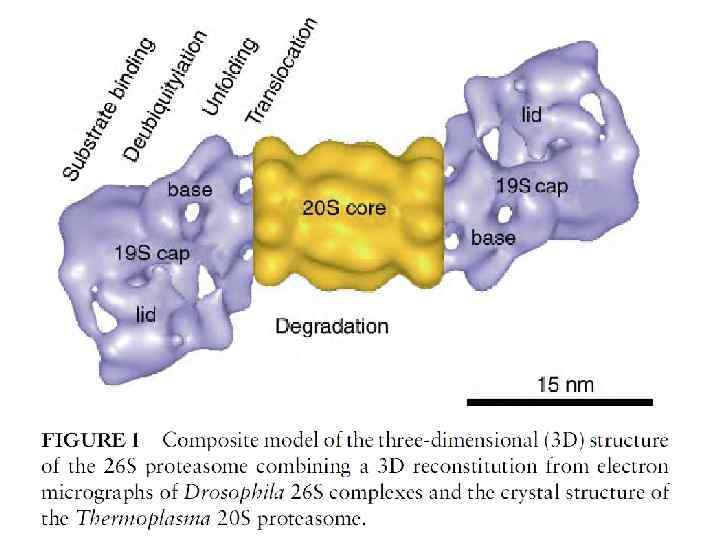
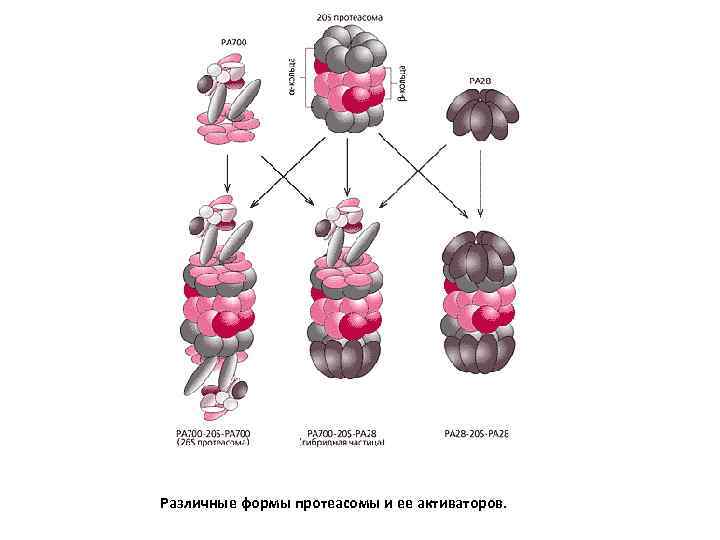
Различные формы протеасомы и ее активаторов.
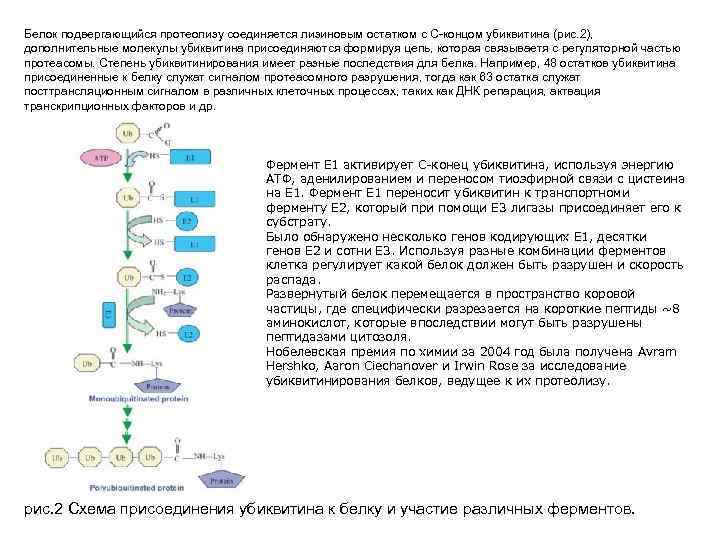
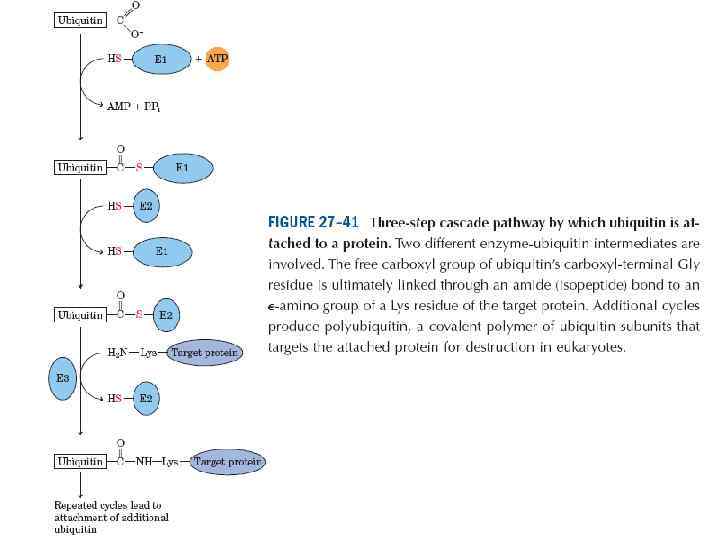
Белок подвергающийся протеолизу соединяется лизиновым остатком с С-концом убиквитина (рис. 2), дополнительные молекулы убиквитина присоединяются формируя цепь, которая связываетя с регуляторной частью протеасомы. Степень убиквитинирования имеет разные последствия для белка. Например, 48 остатков убиквитина присоединенные к белку служат сигналом протеасомного разрушения, тогда как 63 остатка служат посттрансляционным сигналом в различных клеточных процессах, таких как ДНК репарация, актвация транскрипционных факторов и др. Фермент Е 1 активирует С-конец убиквитина, используя энергию АТФ, аденилированием и переносом тиоэфирной связи с цистеина на E 1. Фермент Е 1 переносит убиквитин к транспортноми ферменту Е 2, который при помощи Е 3 лигазы присоединяет его к субстрату. Было обнаружено несколько генов кодирующих Е 1, десятки генов Е 2 и сотни Е 3. Используя разные комбинации ферментов клетка регулирует какой белок должен быть разрушен и скорость распада. Развернутый белок перемещается в пространство коровой частицы, где специфически разрезается на короткие пептиды ~8 аминокислот, которые впоследствии могут быть разрушены пептидазами цитозоля. Нобелевская премия по химии за 2004 год была получена Avram Hershko, Aaron Ciechanover и Irwin Rose за исследование убиквитинирования белков, ведущее к их протеолизу. рис. 2 Схема присоединения убиквитина к белку и участие различных ферментов.
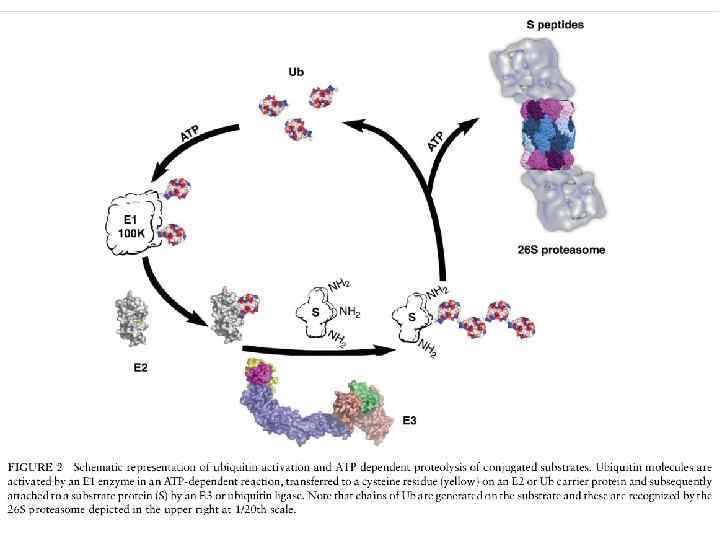
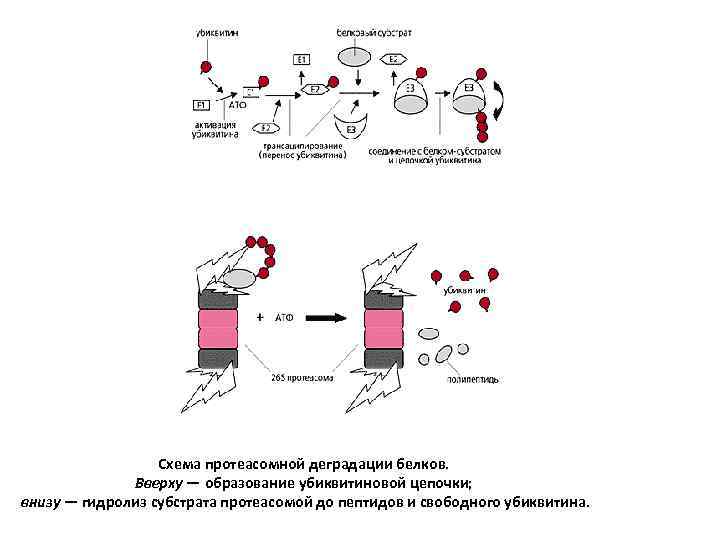
Схема протеасомной деградации белков. Вверху — образование убиквитиновой цепочки; внизу — гидролиз субстрата протеасомой до пептидов и свободного убиквитина.
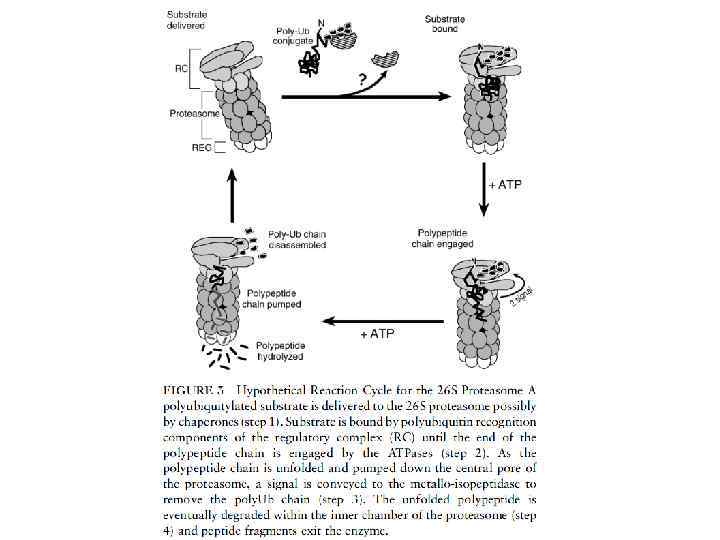
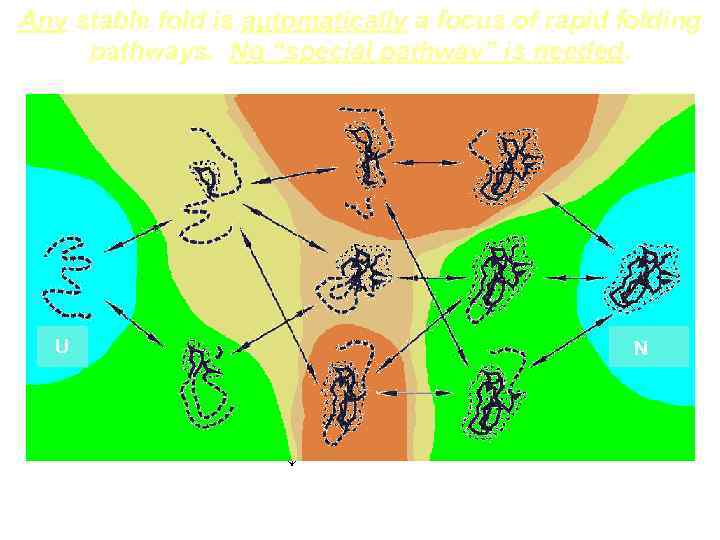
Any stable fold is automatically a focus of rapid folding pathways. No “special pathway” is needed. ΔFN ↓ U N ↓ ↓ ↓ ΔFN ↓ ↓
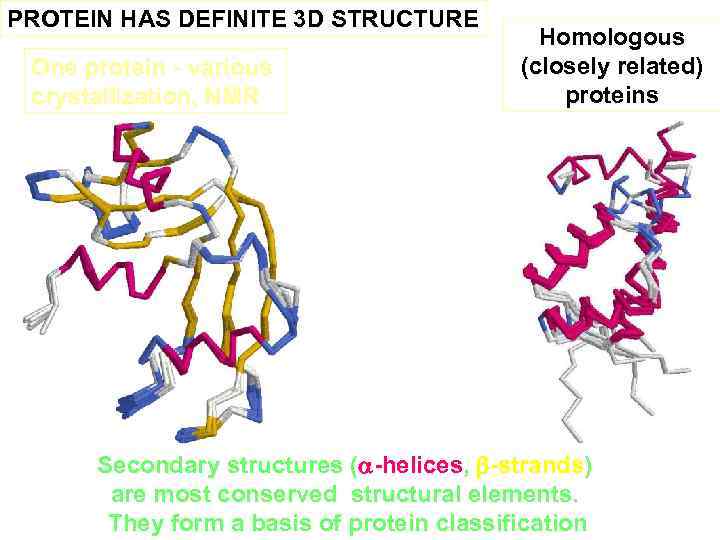
PROTEIN HAS DEFINITE 3 D STRUCTURE One protein - various crystallization, NMR Homologous (closely related) proteins Secondary structures (a-helices, b-strands) are most conserved structural elements. They form a basis of protein classification
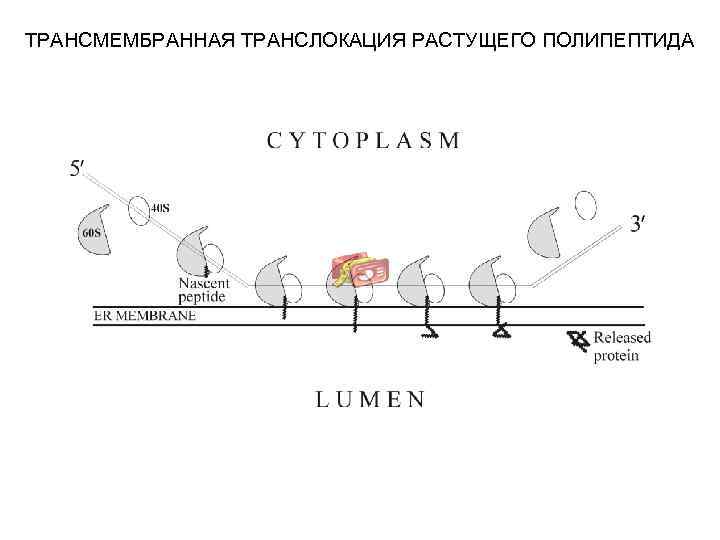
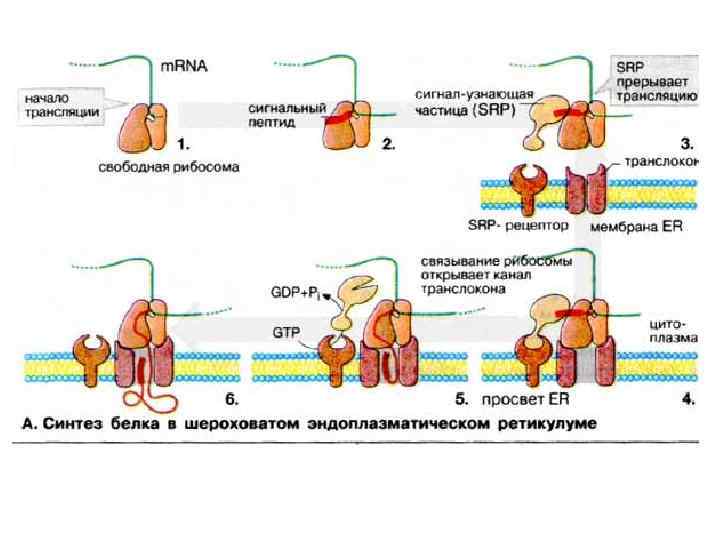
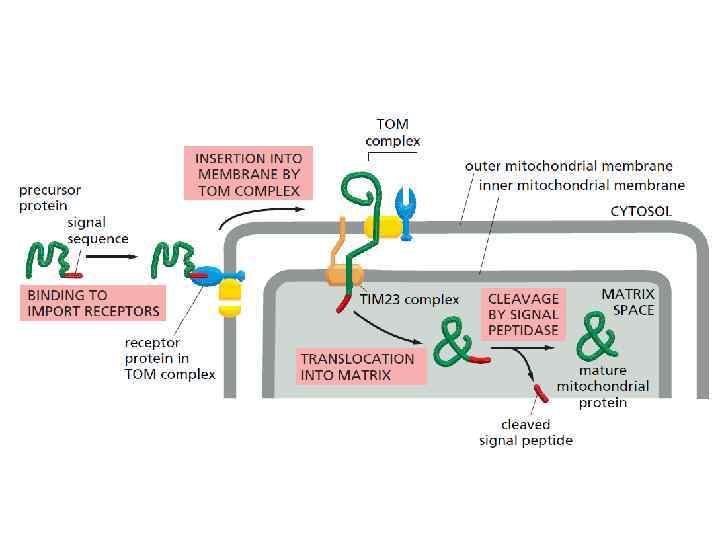
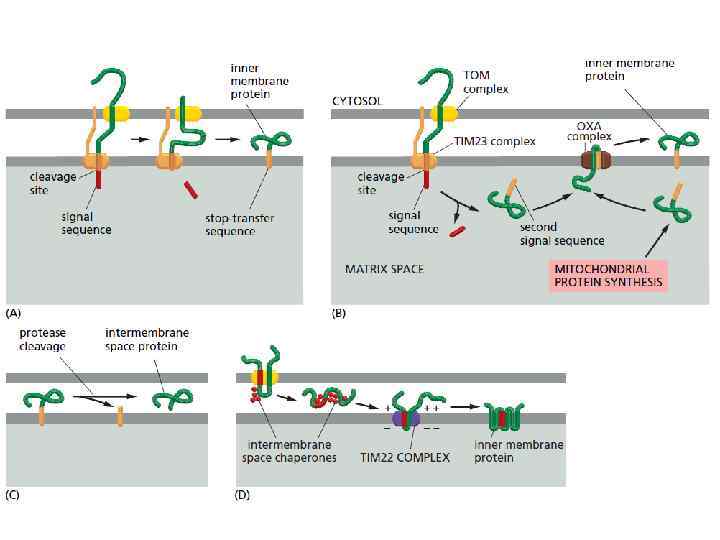
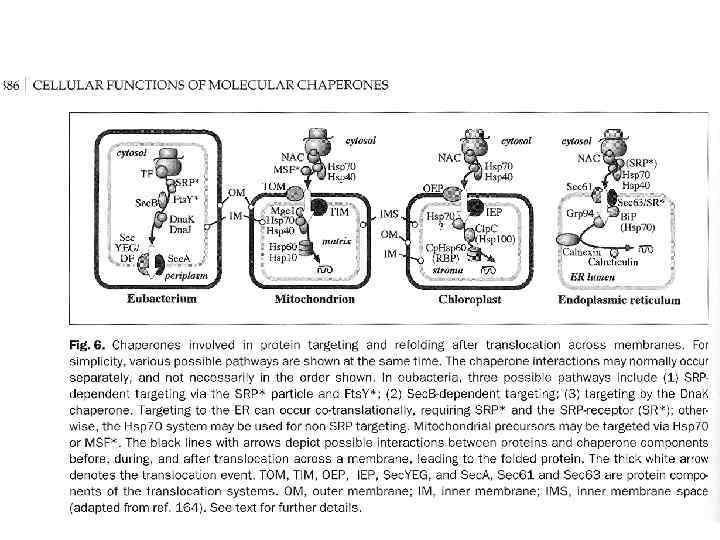
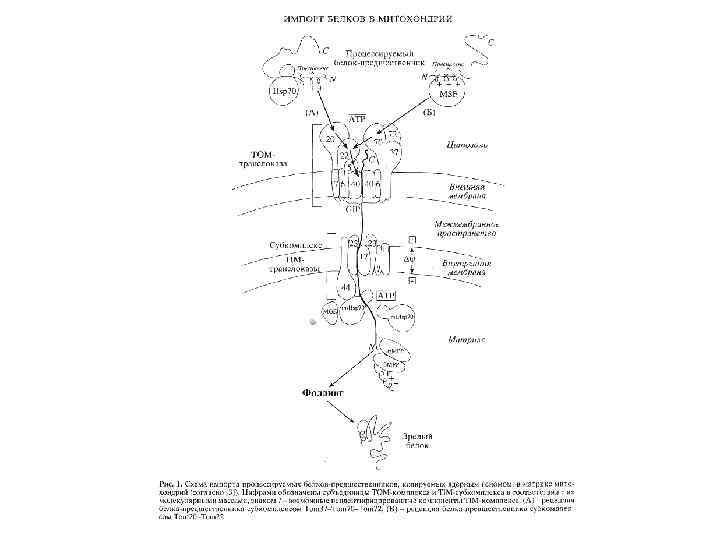
ТРАНСМЕМБРАННАЯ ТРАНСЛОКАЦИЯ РАСТУЩЕГО ПОЛИПЕПТИДА
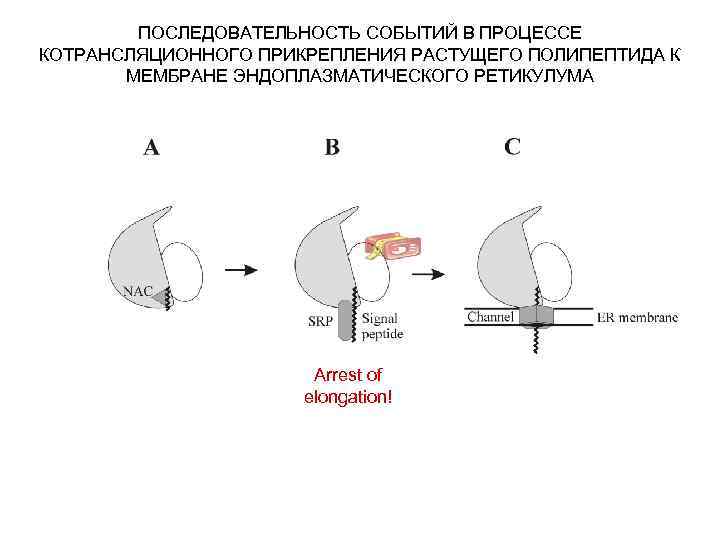
ПОСЛЕДОВАТЕЛЬНОСТЬ СОБЫТИЙ В ПРОЦЕССЕ КОТРАНСЛЯЦИОННОГО ПРИКРЕПЛЕНИЯ РАСТУЩЕГО ПОЛИПЕПТИДА К МЕМБРАНЕ ЭНДОПЛАЗМАТИЧЕСКОГО РЕТИКУЛУМА Arrest of elongation!
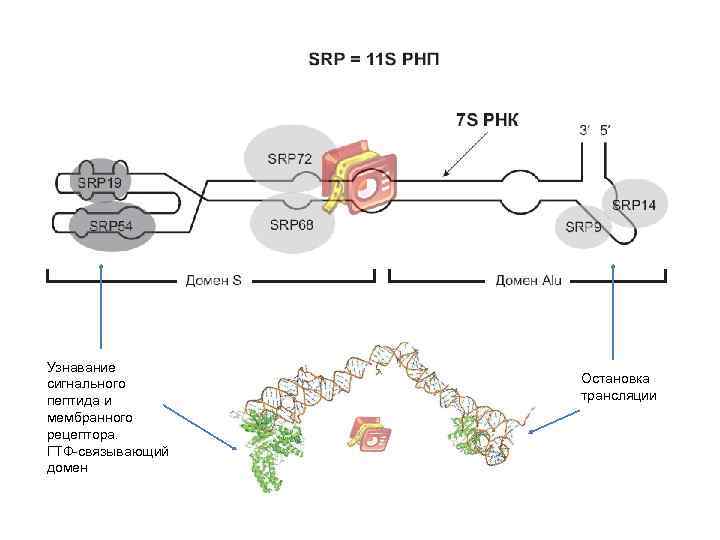
Узнавание сигнального пептида и мембранного рецептора. ГТФ-связывающий домен Остановка трансляции
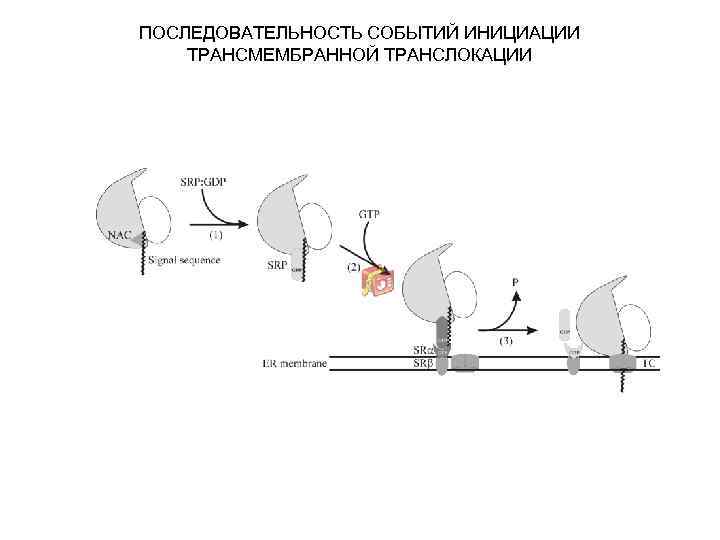
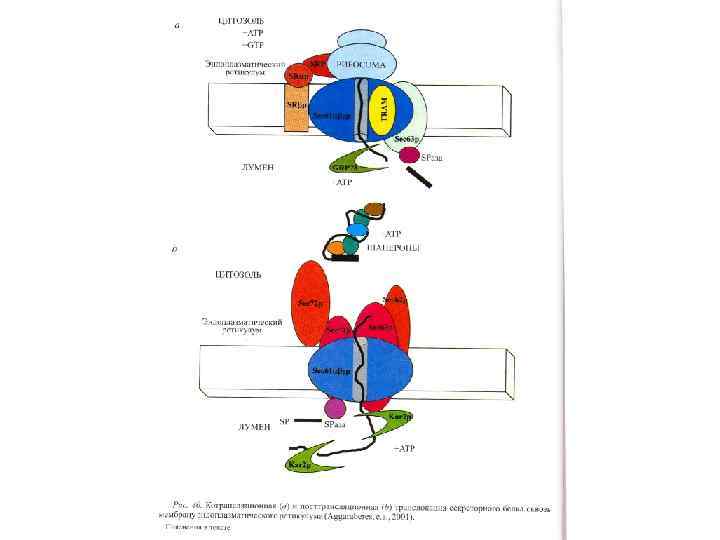
ПОСЛЕДОВАТЕЛЬНОСТЬ СОБЫТИЙ ИНИЦИАЦИИ ТРАНСМЕМБРАННОЙ ТРАНСЛОКАЦИИ
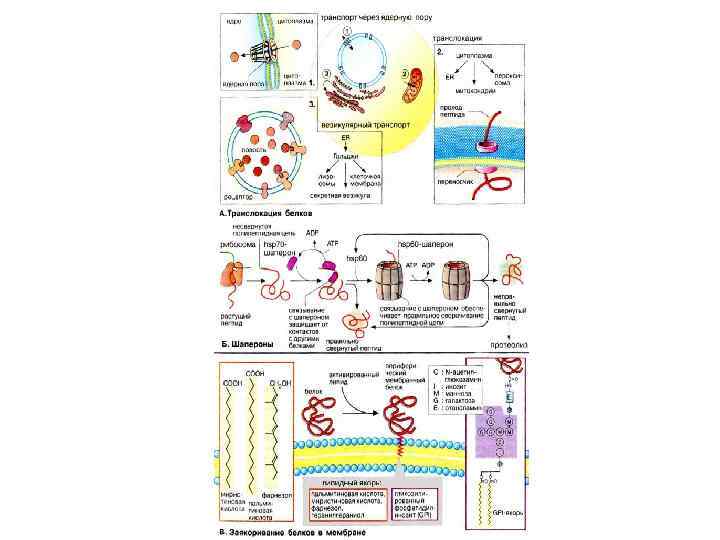


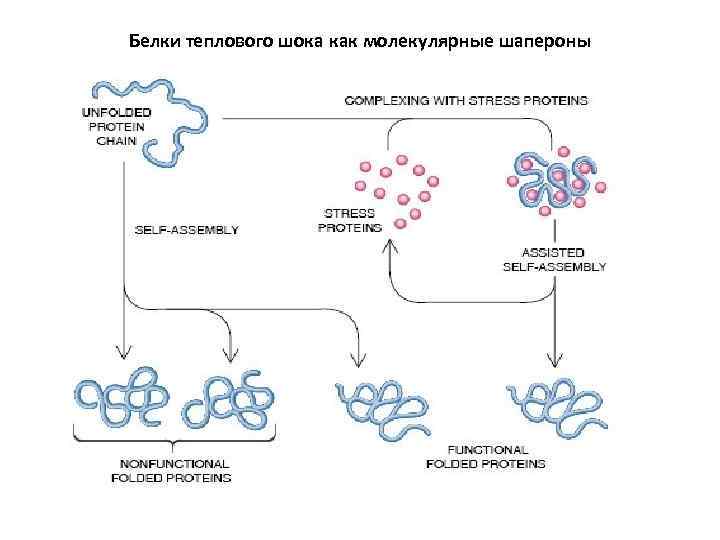
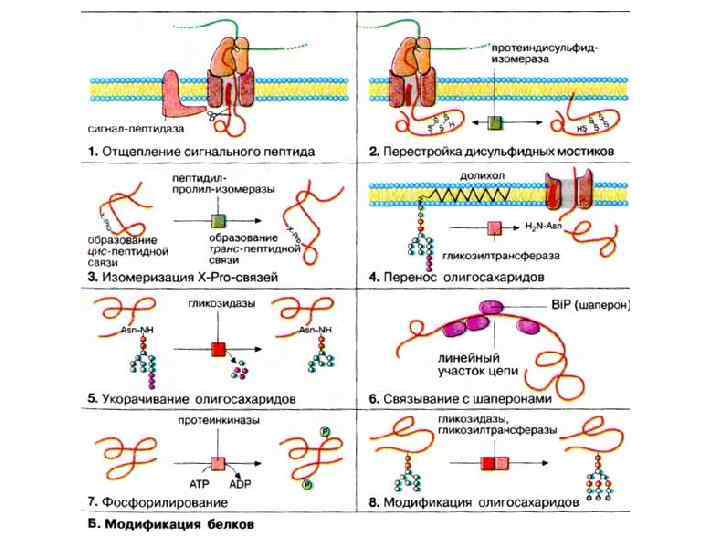
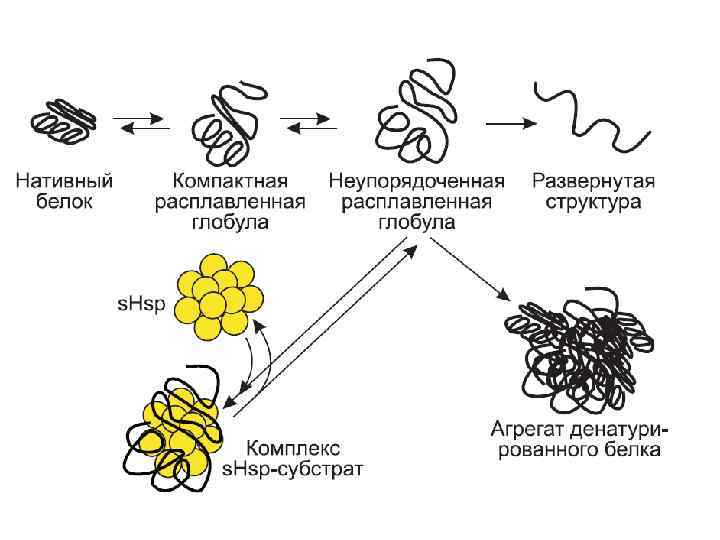
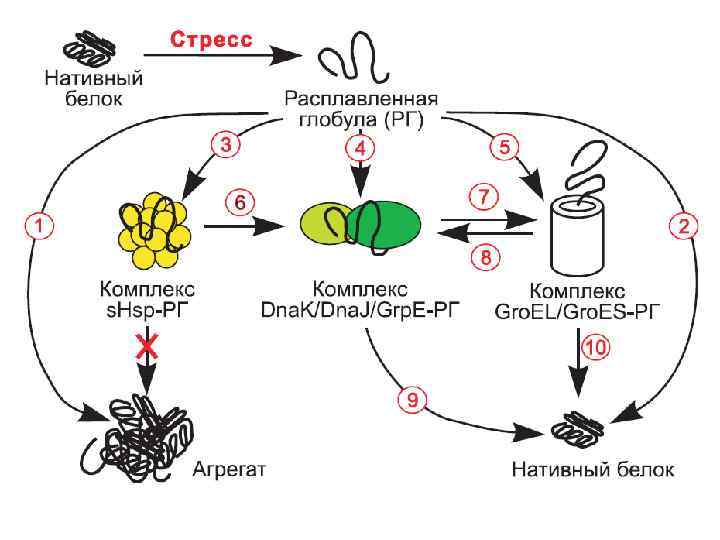
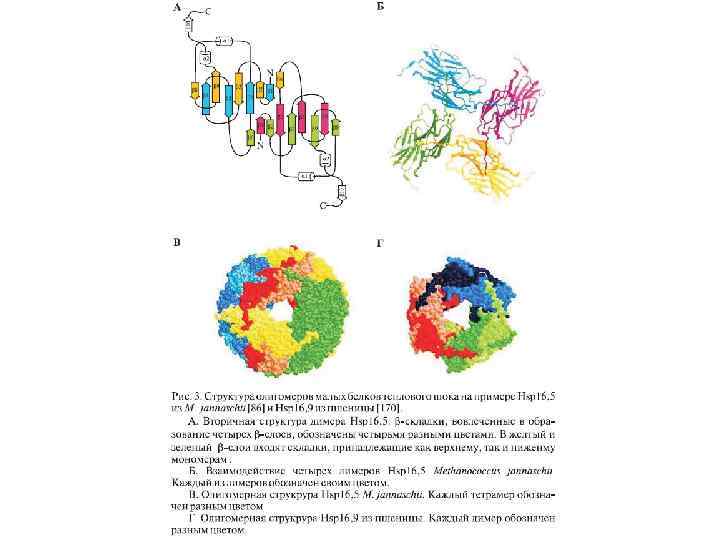
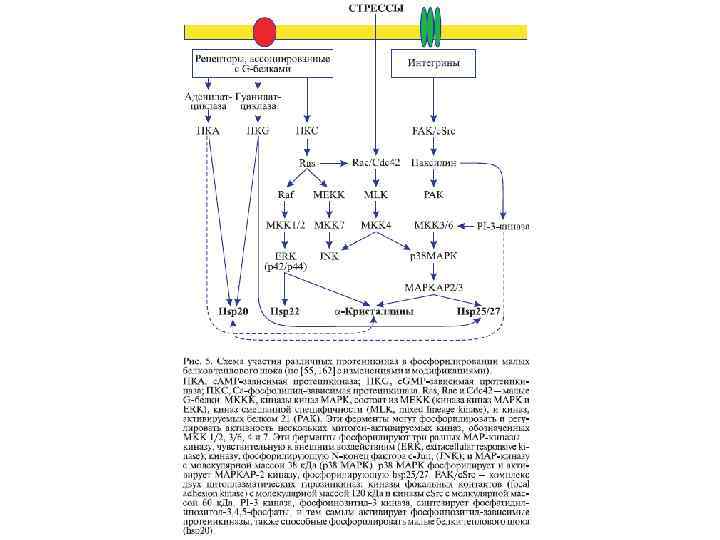
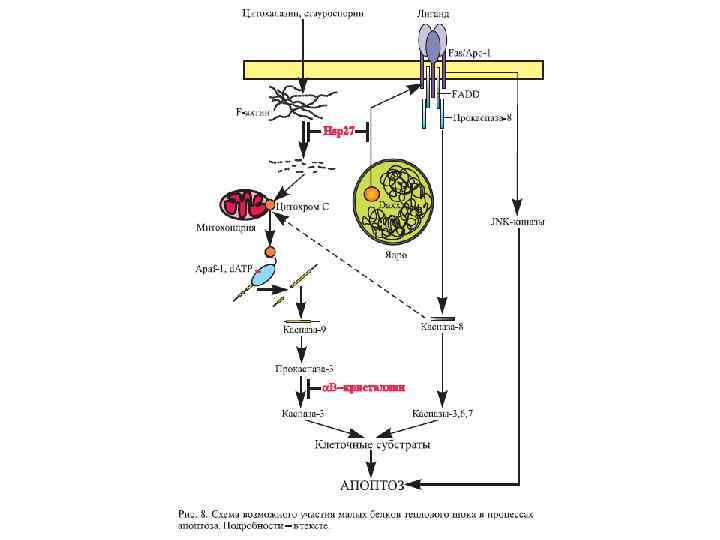
Белки теплового шока как молекулярные шапероны

Фолдинг белка.ppt