Физиология микроорганизмов.ppt
- Количество слайдов: 61

Физиология микроорганизмов. Бактериологический метод диагностики. профессор Т. А. Бажукова зав. каф. микробиологии, вирусологии и иммунологии

Питание бактерий I. Источник энергии: 1. Фототрофы (свет) 2. Хемотрофы (окислительновосстановительные реакции) а) литотрофы (неорганические доноры электронов) б) органотрофы (органиеческие соединения в качестве доноров электронов)

Питание бактерий II. Источник углерода 1. Аутотрофы (используют неорганический 2. Гетеротрофы (используют органический кислород) углерод) Микроорганизмы изучаемые медицинской микробиологией называют гетерохемоорганотрофы По степени гетеротрофности: 1. Сапрофиты 2. Паразиты (облигатные и факультативные)

Транспорт веществ в бактериальную клетку 1. Простая диффузия 2. Облегченная диффузия (с участием белка-переносчика) 3. Активный транспорт (с помощью пермеаз) выделяют 2 типа: а. активный транспорт б. транслокация радикалов (фосфорилирование сахаров в процессе переноса)
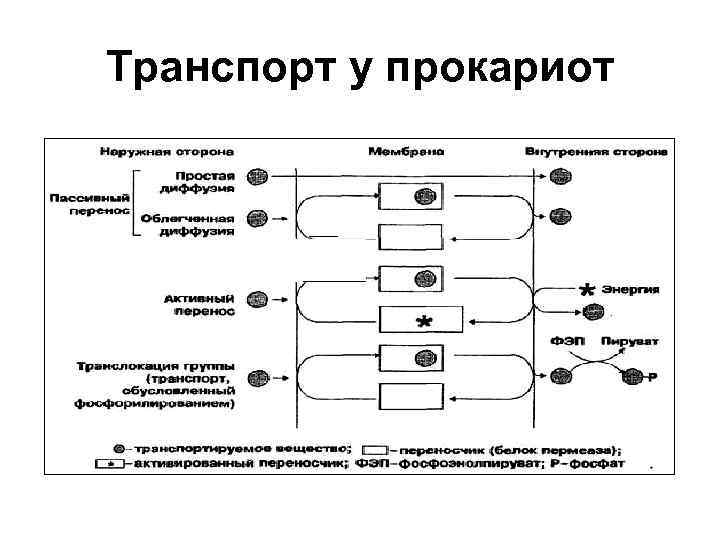
Транспорт у прокариот
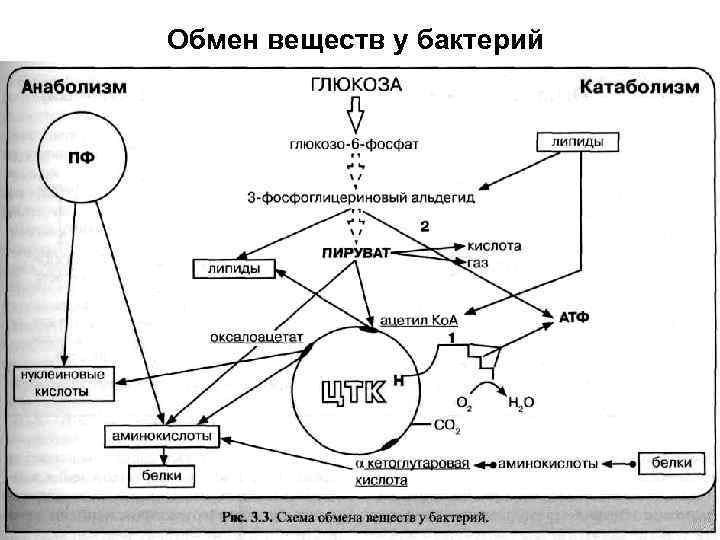
Обмен веществ у бактерий
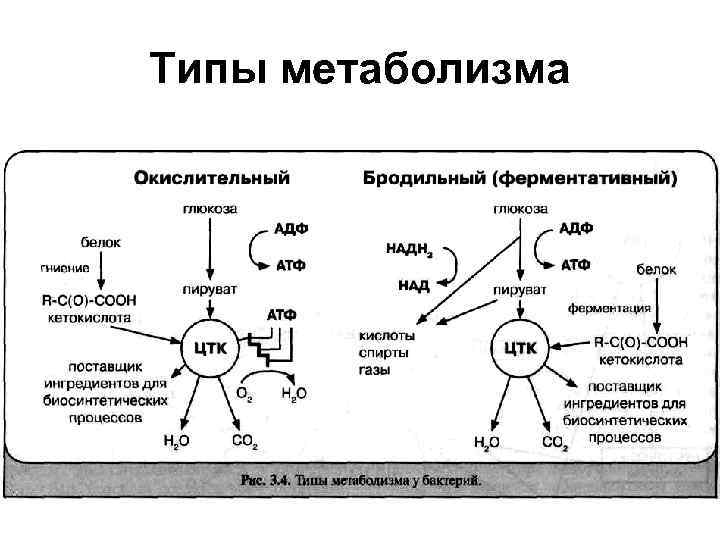
Типы метаболизма

Типы брожения 1. Спиртовое – этиловый спирт 2. Молочнокислое – молочная кислота) 3. Пропионовокислое (пропионовая кислота) 4. Маслянокислое (масляная кислота) 5. Муравьинокислое ( смешанное)

Типы дыхания 1. • • 2. • • 3. Аэробы: Облигатные Микроаэрофилы Анаэробы: Облигатные или строгие Аэротолерантные Факультативные анаэробы
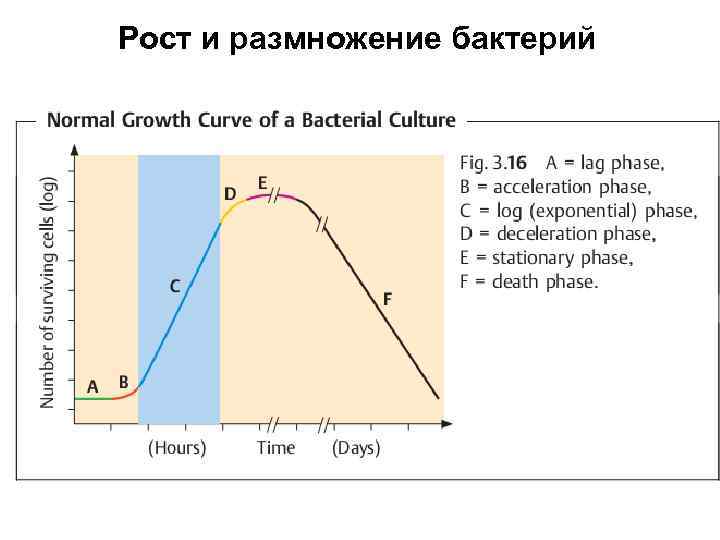
Рост и размножение бактерий
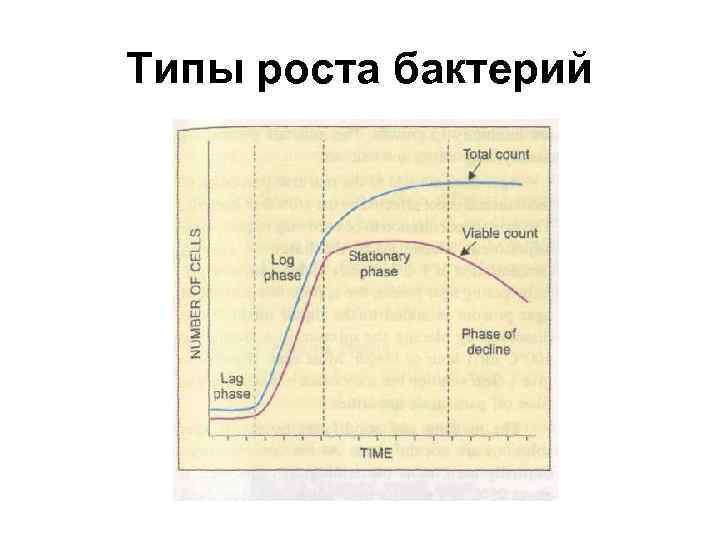
Типы роста бактерий

Условия культивирования бактерий 1. Питательная среда (р. Н) 2. Температура: мезофилы 20 - 40°С термофилы 40 - 60°С психрофилы 0 -2 0° 3. Атмосфера культивирования аэробы факультативные анаэробы облигатные анаэробы микроаэрофилы

Условия культивирования бактерий 4. Время культивирования 5. Освещение 6. Стерильность

Бактериологический метод I этап – Посев на питательные среды II этап – Выделение чистой культуры III этап - Идентификация
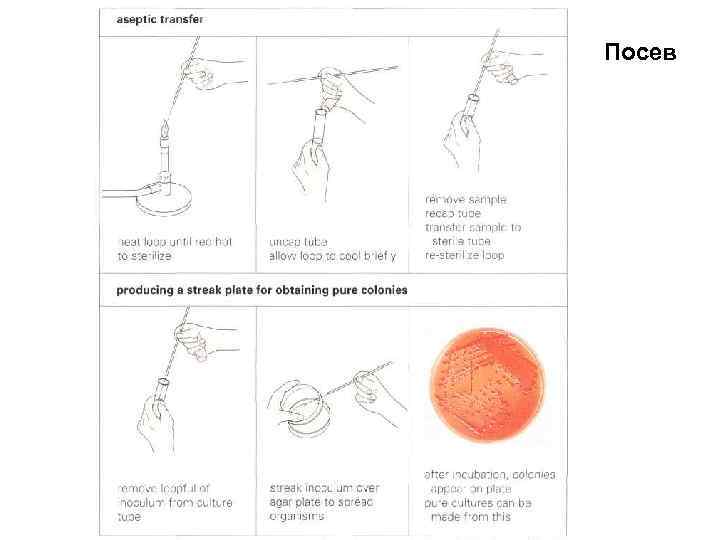
Посев
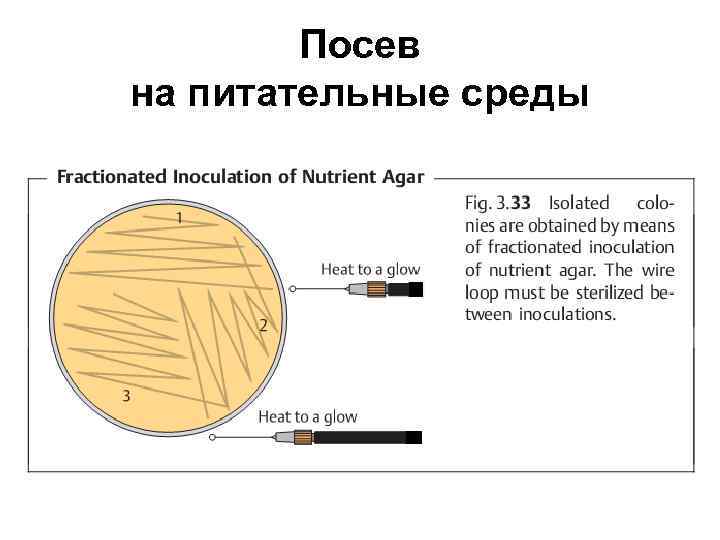
Посев на питательные среды

Выделение чистой культуры • Метод Дригальского – выделение изолированных колоний • Метод Коха – метод серийных разведений • Метод Шукевича – для роящихся культур на свежескошенном агаре.
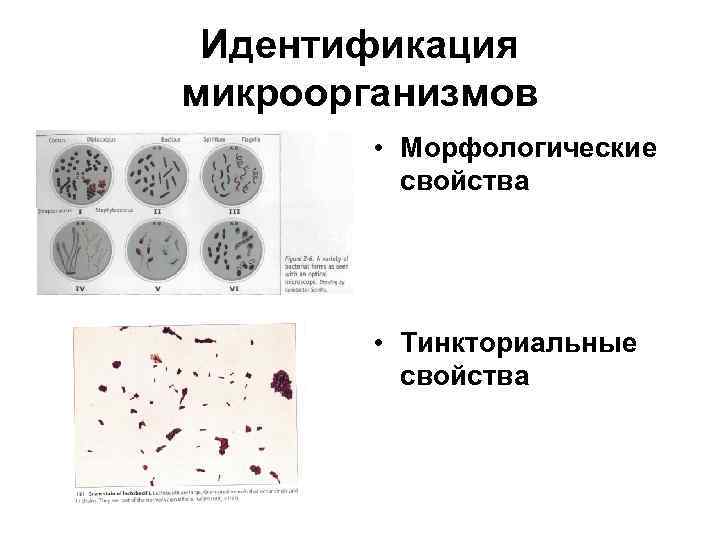
Идентификация микроорганизмов • Морфологические свойства • Тинкториальные свойства

Культуральные признаки
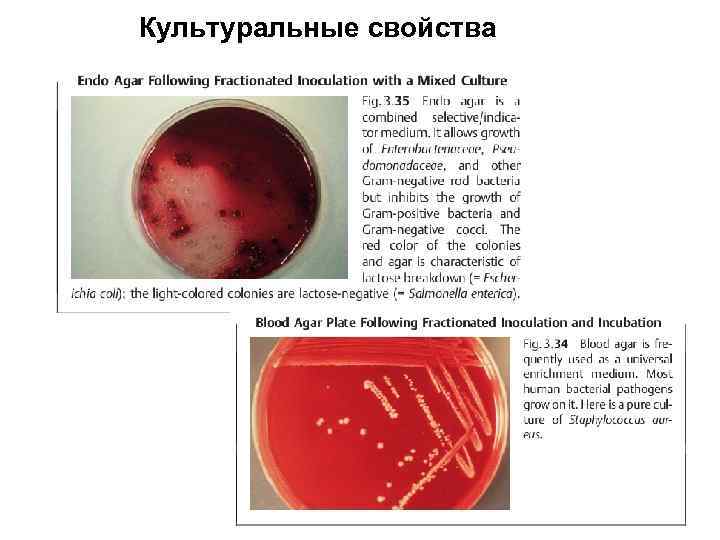
Культуральные свойства

Культуральные признаки
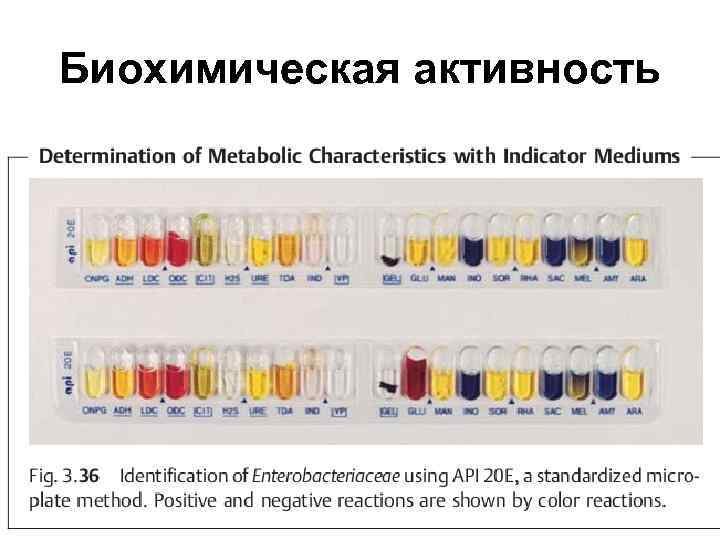
Биохимическая активность
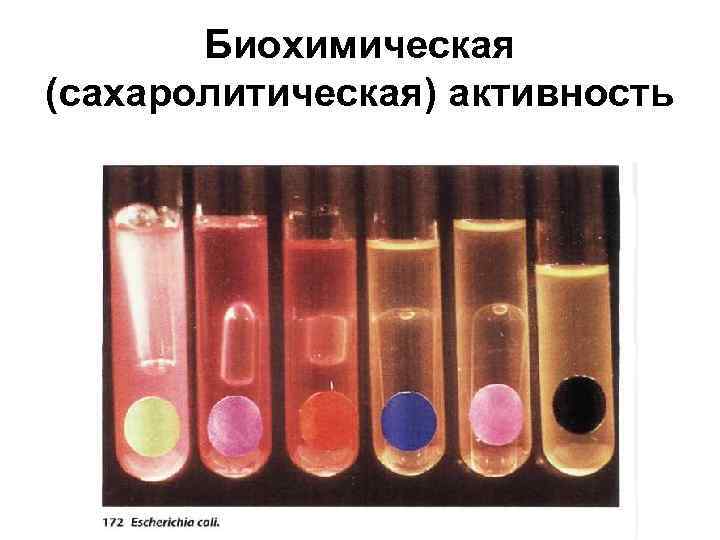
Биохимическая (сахаролитическая) активность

Продукция индола
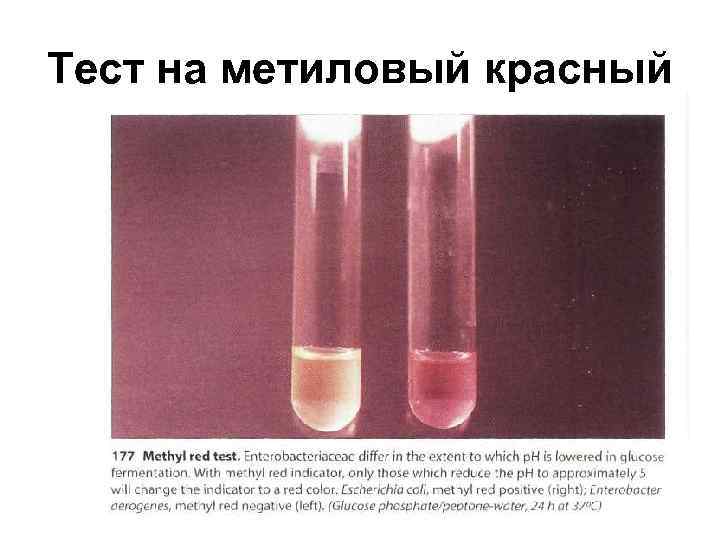
Тест на метиловый красный

Утилизация цитрата

Продукция сероводорода
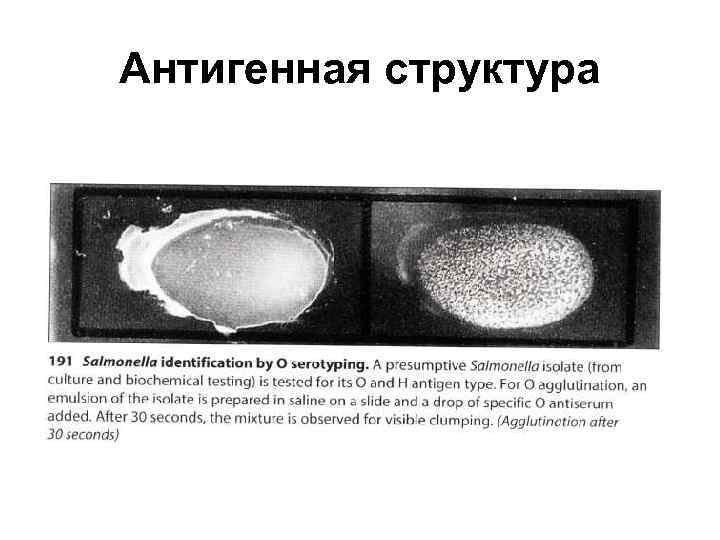
Антигенная структура
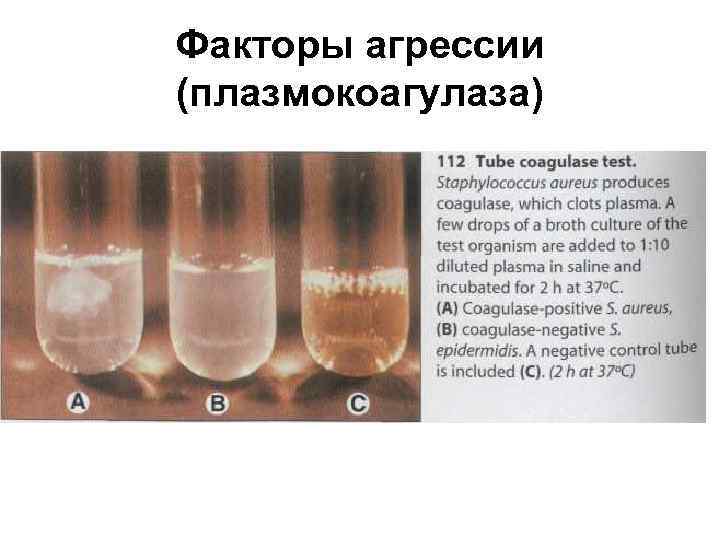
Факторы агрессии (плазмокоагулаза)
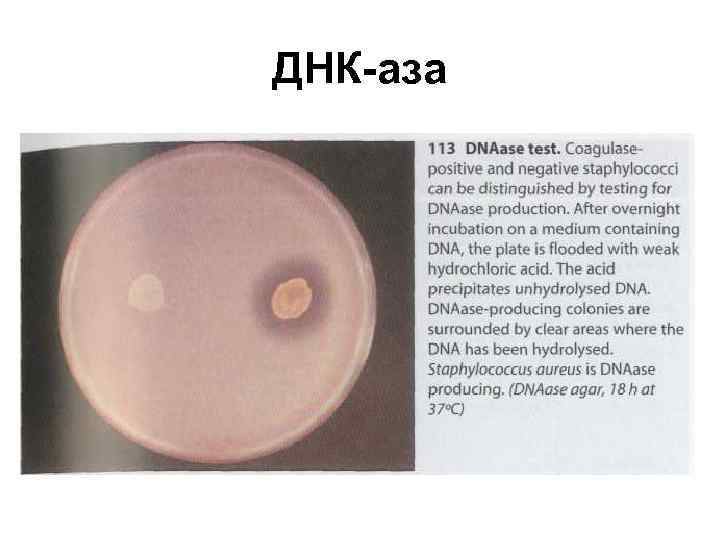
ДНК-аза
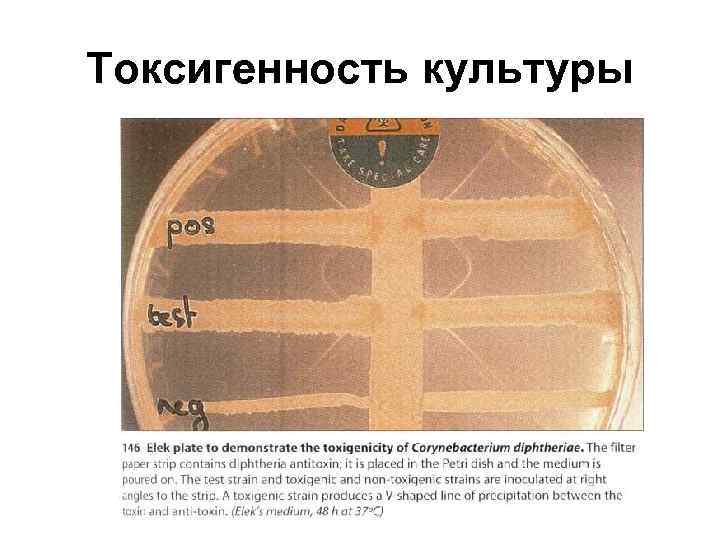
Токсигенность культуры
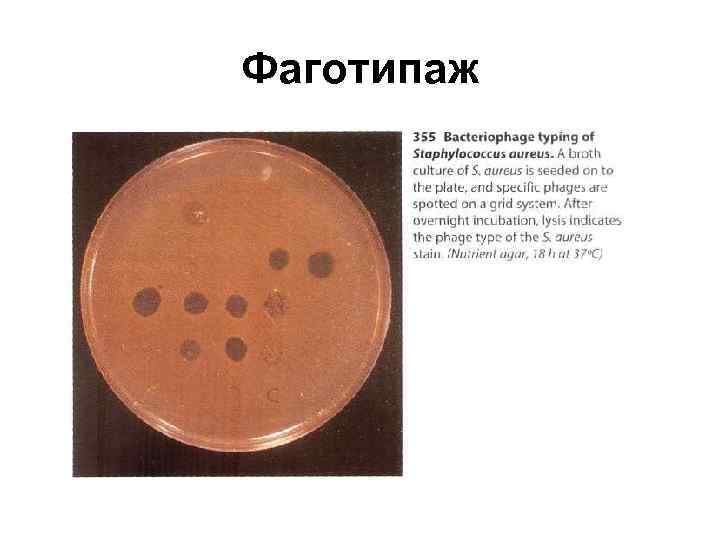
Фаготипаж

Определение чувствительности к антибиотикам Метод дисков

Основные этапы проведения тестирования на антибиотикочувствительность микроорганизмов. • приготовление питательных сред • приготовление суспензии исследуемых микроорганизмов (инокулюма) • инокуляция • инкубация • учет и интерпретация результатов, формулировка рекомендаций по лечению.
Приготовление инокулюма

Инокуляция с помощью тампона
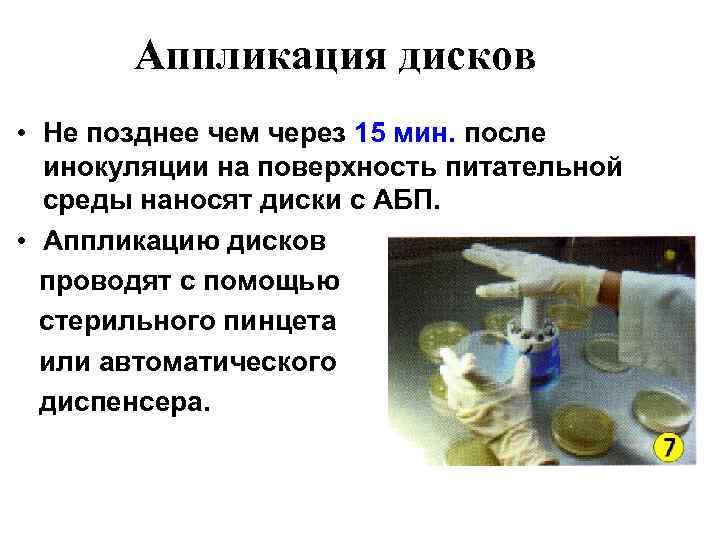
Аппликация дисков • Не позднее чем через 15 мин. после инокуляции на поверхность питательной среды наносят диски с АБП. • Аппликацию дисков проводят с помощью стерильного пинцета или автоматического диспенсера.

ДДМ

Учет результатов • После окончания инкубации чашки помещают кверху дном на темную матовую поверхность так, чтобы свет падал на них под углом в 45° (учет в отраженном свете). • Диаметр зон задержки роста измеряют с точностью до 1 мм, предпочтительнее пользоваться штангенциркулем или кронциркулем.

Учет результатов • При измерении зон задержки роста следует ориентироваться на зону полного подавления видимого роста. Не следует обращать внимания на очень мелкие колонии, выявляемые в пределах зоны задержки роста только при особых условиях освещения или увеличении, и едва заметный налет у края зоны. Исключение составляют случаи учета результатов определения чувствительности стафилококков к оксациллину, когда необходимо учитывать и самые мелкие колонии, выявляемые в пределах четкой зоны подавления роста.
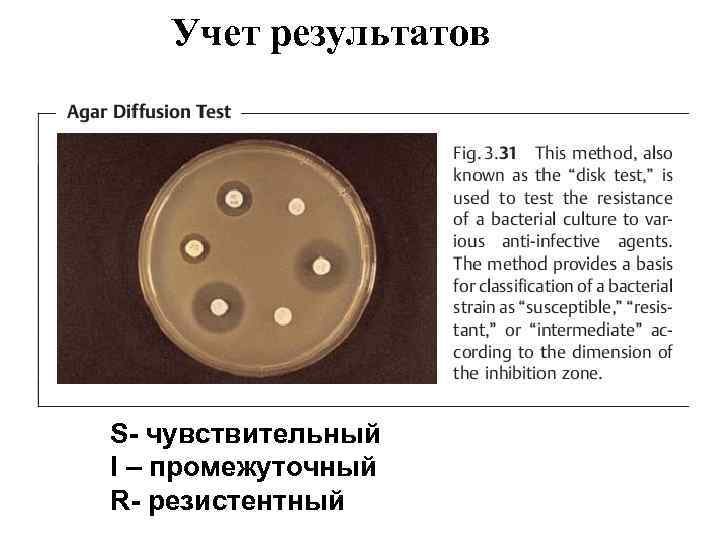
Учет результатов S- чувствительный I – промежуточный R- резистентный
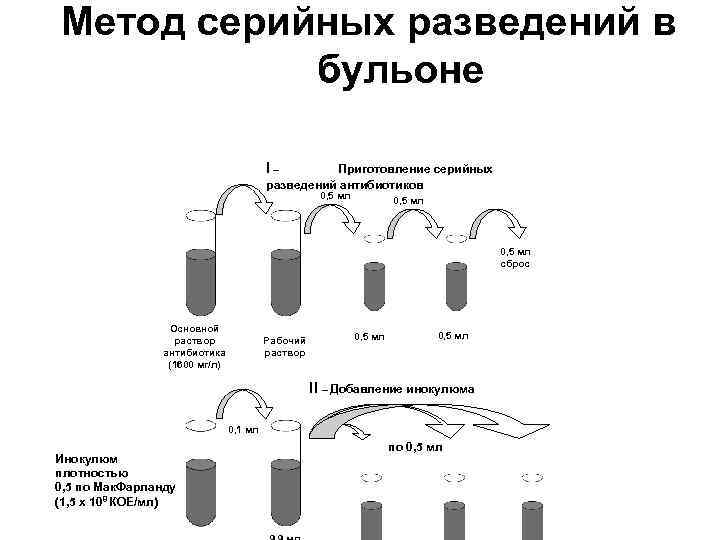
Метод серийных разведений в бульоне I– Приготовление серийных разведений антибиотиков 0, 5 мл сброс Основной раствор антибиотика (1600 мг/л) Рабочий раствор 0, 5 мл II – Добавление инокулюма 0, 1 мл Инокулюм плотностью 0, 5 по Мак. Фарланду (1, 5 х 108 КОЕ/мл) по 0, 5 мл
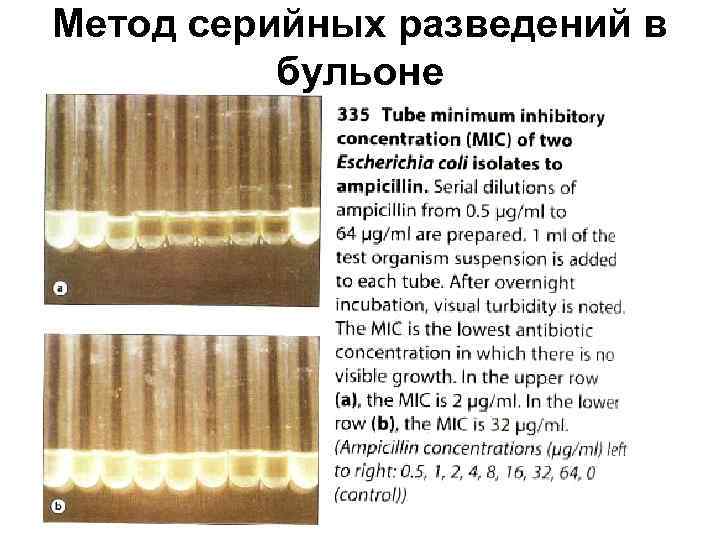
Метод серийных разведений в бульоне
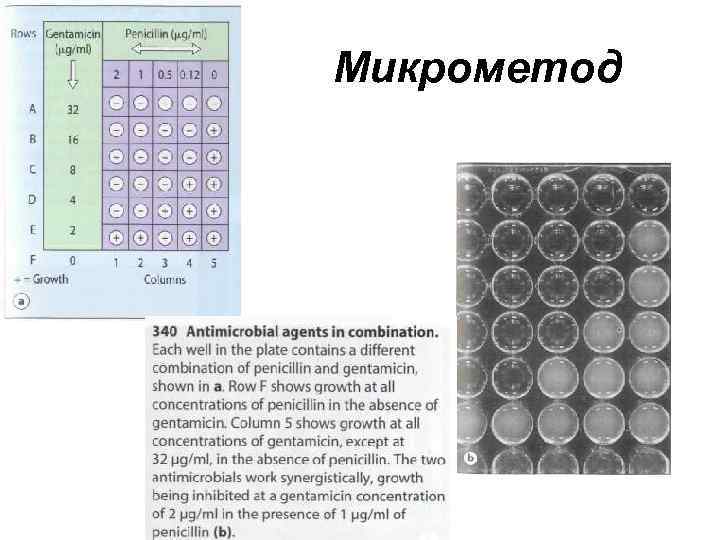
Микрометод
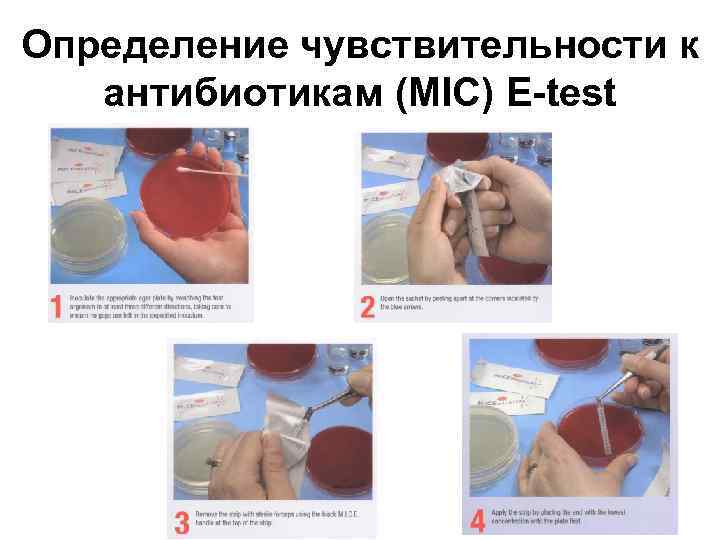
Определение чувствительности к антибиотикам (MIC) E-test
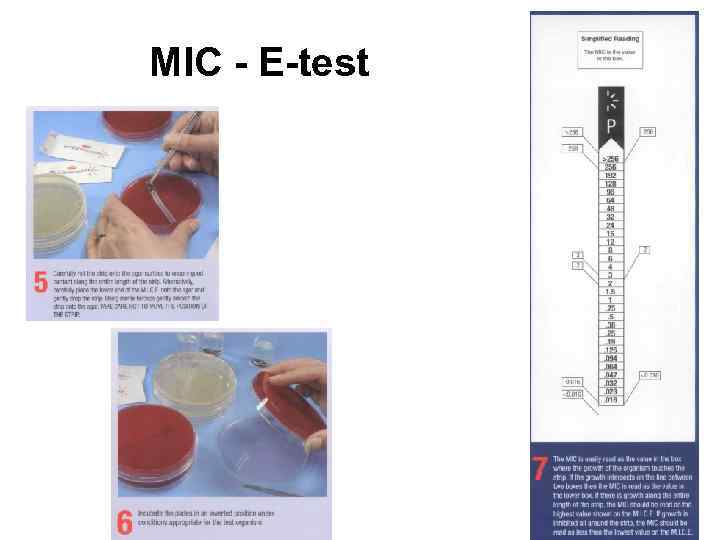
MIC - E-test

MIC - E-test 2 1 3 1. Если рост культуры пересекается на линии между двумя зонами, то МИК читаем по значению меньшей зоны. 2. Если рост культуры наблюдается на протяжении всей полоски, это раскениваем как высокий показатель МИК. 3. Если рост культуры ингибируется вокруг полоски, то МИК расцениваем как минимальную.
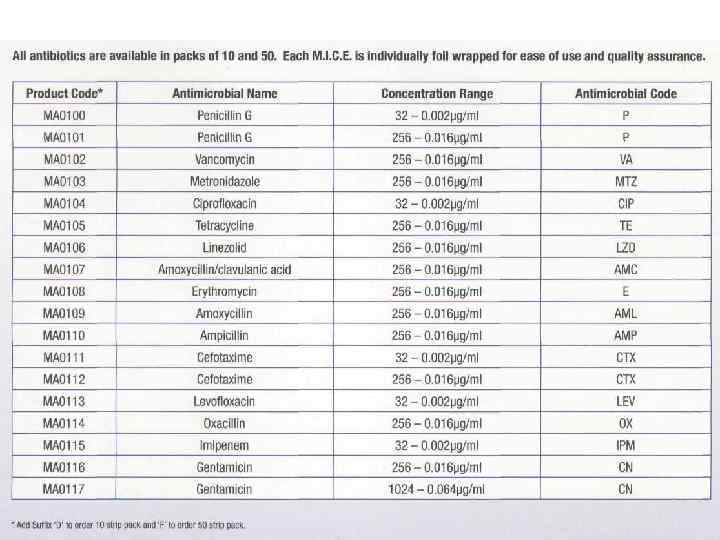

Минимальная ингибирующая концентрация (MIC) E-test

E-test

Культивирование анаэробов • Физический метод (анаэростат, в глубине агара, в эксикаторе) • Химический метод (поглотители кислорода) • Биологический метод Фортнера

Современные методы диагностики • • Полимеразно-цепная реакция (ПЦР) Секвенирование ДНК Саузернблоттинг Нозернблоттинг ДНК-гибридизация Риботипирование Рестрикционный анализ

Полимеразная цепная реакция (ПЦР • • • ПЦР заключается в амплификации, т. е. увеличении количества копий специфического (маркерного) гена возбудителя. Выделенную из исследуемого материала ДНК, «расплетают» при нагревании около 90 °С (денатурируют) Достраивают к расплетенным нитям ДНК новые комплементарные нити, снижая температуру до 50 °С ( «отжиг» ). Достраивание (при 70 °С) новых комплементарных нитей ДНК происходит при добавлении к искомым генам праймеров (затравки из коротких однонитевых ДНК, комплементарных 3'-концам ДНК искомого гена), ДНК-полимеразы и нуклеотидов. 3'-концы праймеров достраиваются добавлением термостабильной полимеразы ( «Taq-полимеразы» ). В результате достраивания комплементарных нитей ДНК из одного гена образуются два. Этот цикл копирования генов, состоящий из денатурации, ренатурации и элонгации многократно повторяется при заданных температурных режимах. Продукты ПЦР отделяют с помощью гель-электрофореза и выявляют с помощью добавления этидия бромида, который флюоресцирует при освещении ультрафиолетом.

Секвенирование ДНК • При идентификации микроорганизмов используют секвенирование ДНК для чего экстрагируют нуклеиновую кислоту, амплифицируют специфическую последовательность нуклеотидов методом ПЦР, определяют ее и проводят компьютерный подбор соответствующего «сиквенса» в базе данных. Обычно для секвенирования используют ДНК-копию гена 16 S р. РНК — наиболее стабильный компонент бактерий и ген белка теплового шока (HSP 65).
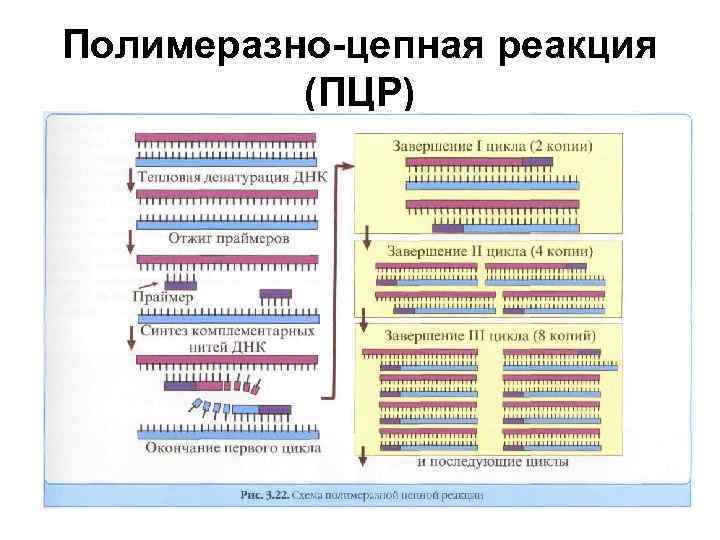
Полимеразно-цепная реакция (ПЦР)
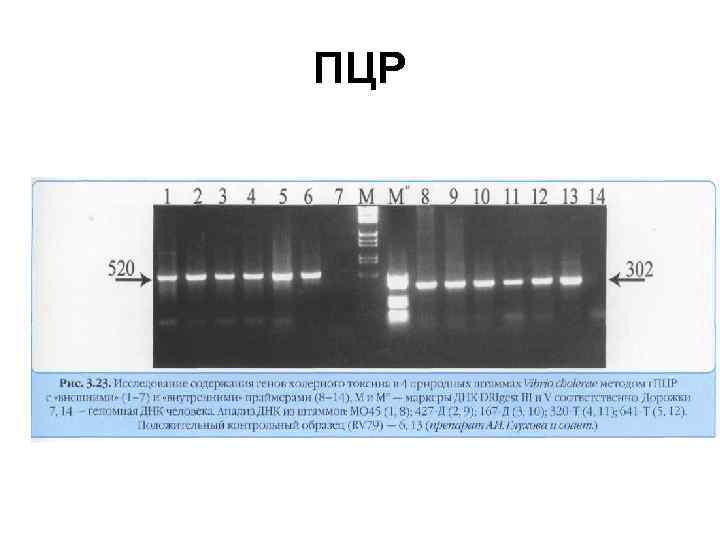
ПЦР

Саузернблоттинг • Разделение фрагментов ДНК (гель-электрофорез) • Перенос в щелочной раствор для получения однонитевых фрагментов ДНК. • Перенос на нитроцеллюлозную или нейлоновую мембрану • Гибридизация со специфической меченой пробой ДНК • Выявление полос меченого зонда ДНК путем экспонирования фильтра с рентгеновской пленкой (ауторадиография), • Зонды, меченые флюорохромом, выявляют при помощи люминесцентной микроскопии.

Нозернблоттинг • Применяют для выявления и гибридизации РНК (фрагментов РНК). • Размер и количество специфических молекул и. РНК определяется после обработки общей РНК или поли (А) РНК. • Молекулы РНК выделяют гель-электрофорезом и переносят на иммобилизованную мембрану. • Искомые последовательности РНК определяют гибридизацией с меченой пробой.

ДНК-гибридизация • Денатурация, т. е. разделениу двунитевой ДНК на отдельные нити в щелочной среде (90°С) • Восстановление (отжиг) двунитевой структуры с комплементарной меченой нитью ДНК (молекулярным зондом) (10 -37°С). • Гибридизацию проводят на фильтрах (блотгибридизация) или in situ. Молекулярный зонд с присоединенным биотином гибридизируется на ДНК мишени. • После отжига и промывки на образец наносят антибиотиновый конъюгат (стрептавидин, соединенный со щелочной фосфатазой) и проводят специфическое окрашивание клеток. • Стрептавидин с меткой избирательно связывается с биотином, что выявляется при микроскопии. Так выявляют локализацию микробов в ткани, хромосомные аномалии в клетках и т. д.

Риботипирование Выявление количественных различий по рибосомным оперонам и нуклеотидным последовательностям. • Проводят гидролиз ДНК, которую разделяют в агарозном геле и затем гибридизируют с ДНК-зондами на один или более генов, кодирующих 16 S-, 23 S-, 5 S-рибосомные РНК. • Бактерии можно типировать по серотипу, фаготипу и по риботипу. Методически сходно с риботипированием S-типирование: проводят сравнительный анализ числа копий S-элементов и рестрикционного разнообразия нуклеотидных последовательностей различных штаммов микробов.

Рестрикционный анализ • ДНК расщепляют с помощью рестриктаз (бактериальных эндонуклеаз)/ • Отдельные рестриктазы способствуют выделению строго определенных фрагментов ДНК. Размер полученных фрагментов ДНК можно определить путем электрофореза в агарозном или полиакриламидном геле. • После электрофореза каждый фрагмент ДНК располагается в определенном участке геля в виде дискретной полосы. Фрагменты ДНК выявляют путем обработки геля бромидом этидия, который связывается с ДНК. • Такие фрагменты ДНК высвечиваются при ультрафиолетовом облучении в красной области спектра. Длину каждого фрагмента можно выявить, сравнивая расстояние, пройденное фрагментом ДНК при электрофорезе, с расстоянием, пройденняым стандартным фрагментом ДНК известного размера.
Физиология микроорганизмов.ppt