Поверхностные явления.ppt
- Количество слайдов: 31

Физикохимия поверхностных явлений Адсорбция Лекция 9 Кафедра медицинской и биологической химии ХМГМА

План лекции n n Поверхностные явления и поверхностное натяжение жидкостей. Единицы измерения. Поверхностно-активные, поверхностноинактивные и поверхностно нейтральные вещества. Строение молекулы ПАВ. Изотерма поверхностного натяжения. Поверхностная активность. Явление адсорбции. Понятие адсорбента и адсорбтива. Особенности адсорбции на границе твердое тело-газ, твердое тело-жидкость. Применение адсорбции в медицине (гемосорбция, иониты).

Разделы фаз: n Подвижные границы Газ-жидкость (г-ж) Жидкость-жидкость (ж-ж) n Неподвижные границы Газ-твердое вещество (г-тв) Жидкость-твердое вещество (ж-тв)

n n Живые организмы – системы с очень развитыми поверхностями раздела. К ним относят кожные покровы, поверхность стенок кровеносных сосудов, слизистые оболочки, клеточные мембраны. Поверхность кожи взрослого человека составляет 3 м 2, площадь поверхности всех эритроцитов – 2500 м 2, площадь альвеол лёгкого – 1000 м 2.

n n Поверхностные явления – процессы, проходящие на поверхности раздела фаз и обусловленные особенностями состава и строения поверхностного слоя. Поверхностные явления связаны с тем, что состояние молекул вещества, расположенных на границе раздела двух фаз отличается от состояния молекул в объёме фаз.
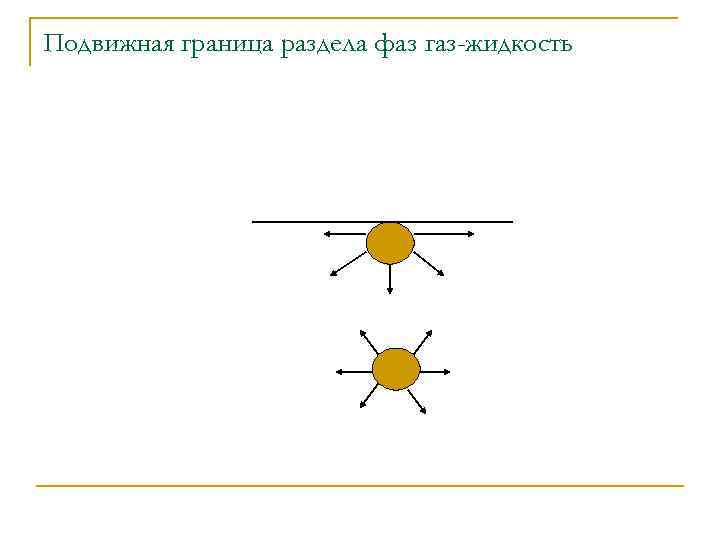
Подвижная граница раздела фаз газ-жидкость

n n Каждая молекула внутри жидкости окружена другими молекулами и силы, действующие на молекулу распределены симметрично: в результате все внутренние молекулы, как бы пребывают в состоянии внутреннего равновесия, равнодействующая сил равна нулю. В ином положении находятся молекулы на границе раздела фаз. Силы притяжения, действующие со стороны жидкости, не уравновешиваются силами, действующими со стороны газообразной фазы. Следовательно, действующая молекулярных сил не равна нулю. Эта действующая сила, перпендикулярная к поверхности жидкости, есть внутреннее давление. Она втягивает молекулы, расположенные на поверхности жидкости внутрь и тем самым стремится снизить поверхность до минимума (роса, слеза – шар).


n Сила, действующая на единицу длины границы раздела и обуславливающая сокращение поверхности жидкости – поверхностное натяжение – σ. σ = дин/см ; σ = Дж/м 2 = Н·м/м 2 = Н/м; Н/м = дин/см · 10 -3 σ (H 2 O) = 72, 8 Н/м, σ (C 2 H 5 OH ) = 15 Н/м, σ (крови)= 45, 5 Н/м, σ(ртути) = 436 Н/м.

n Величина поверхностной энергии – F – произведение поверхностного натяжения на величину всей поверхности. F = σ · S (Дж/м 2 · м 2 = Дж)

n n Способность растворённых веществ изменять поверхностное натяжение раствора – g – поверхностная активность, которая выражается: g = -dσ / dс = -∆σ / ∆c = - (σ1 - σ2)/(с1 -с2) При растворении веществ поверхностное натяжение может снижаться, повышаться, не изменяться

n n Поверхностное натяжение может снижаться, так как молекулы растворенного вещества будут подниматься наверх, и разрушать поверхностную плёнку, а поверхностная активность будет увеличиваться. Те вещества, которые уменьшают поверхностное натяжение называются поверхностно-активными веществами – ПАВ снижают взаимодействие молекул в поверхностном слое и это ведёт к снижению поверхностного натяжения.

n n Молекулы ПАВ состоят из двух частей: полярная часть ( «голова» ) : – OH, – COONa; и неполярная часть – R ( «хвост» ) : – C 17 H 35. R – COOH Полярная часть - голова гидрофильная ( «любит» воду), хвост – гидрофобный ( «боится» воды). ПАВ находится на границе раздела и ориентируется в поверхностном слое согласно своему строению (подобное растворяется в подобном).

n n Те вещества, которые увеличивают поверхностное натяжение называются поверхностно-инактивные вещества – ПИАВ, к ним относят: соли, щёлочи, кислоты, глицерин, α-аминокислоты. Молекулы стремятся внутрь жидкости, поверхностное натяжение возрастает. Растворенное вещество, не изменяющее поверхностное натяжение (при этом молекулы равномерно распределены между поверхностным слоем и объемом раствора) называются поверхностно-нейтральные вещества - ПНВ (сахар, глюкоза, углеводы).

n n Величина поверхностного натяжения зависит от концентрации этих веществ, а не только от их природы. График зависимости поверхностного натяжения от концентрации – изотерма поверхностного натяжения при постоянной температуре.
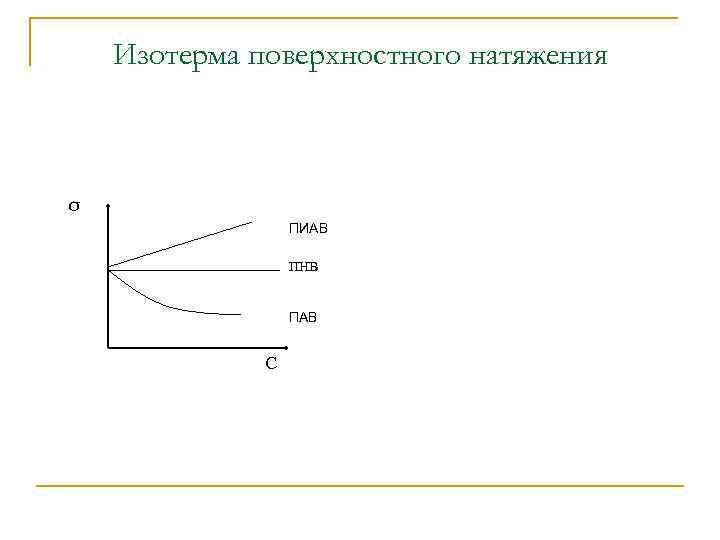
Изотерма поверхностного натяжения σ ПИАВ ПНВ ПАВ С

n n Всякая система стремится к минимуму энергии, то есть к снижению поверхностной энергии, которая может снизиться за счёт следующих факторов: За счёт снижения площади. За счёт снижения поверхностного натяжения. Для уменьшения величины поверхностного натяжения необходимо увеличить температуру, так как молекулы двигаются быстрее. Понизить поверхностное натяжение можно путём добавления ПАВ.

n На снижение поверхностного натяжения высокую роль играет природа ПАВ, а именно длина углеводородного радикала. Закономерность Дюкло-Траубе: поверхностная активность вещества одного гомогенного ряда (спирты) возрастает в 3 раза при удлинении углеводородной цепи на 1 звено метиленовой группы (CH 2).

АДСОРБЦИЯ Адсорбция – накопление, концентрирование одного вещества на поверхности раздела двух фаз одна из которых является обычно жидкостью или твёрдым веществом. n Вещества способные адсорбировать другие вещества на своей поверхности – адсорбенты, адсорбируемое вещество – адсорбтив или адсорбат. Адсорбцию выражают в моль/см 2, кмоль/м 2. n

Типы адсорбционных систем Адсорбент Адсорбат подвижные поверхности раздела сред Ж Г Ж Ж неподвижные поверхности раздела сред Тв Г Тв Ж n

Системы с подвижными поверхностями раздела Адсорбцию в данной системе определить непосредственно нельзя. Её рассчитывают по величине поверхностного натяжения, по уравнению Гиббса. Г = - dσ/d. С ∙ (С(ПАВ) /RT) , где С (ПАВ) – молярная концентрация ПАВ, Если σ↓, т. е. dσ/d. С < 0 → Г > 0 – положительная адсорбция (все вещества встали на границе раздела. Работают ПАВ Если σ↑, т. е. dσ/d. С > 0 → Г < 0 – отрицательная адсорбция (вещества находятся в объёме раствора). Работают ПИАВ. Если σ - const, т. е. dσ/d. С = 0 → Г = 0 – вещество распределено равномерно между поверхностью и объёмом.

Адсорбция на неподвижных поверхностях раздела К этому типу относится адсорбция на твёрдой поверхности. Адсорбцию рассчитывают по формуле: Г = n(х) / m(х), где Г – адсорбция, n(х) – количество молей адсорбированного вещества, m(х) – масса вещества на поверхности которого идёт адсорбция. В качестве адсорбента используются пористые вещества: активированный уголь, силикагель, крахмал, белая глина (Al 2 O 3·Si. O 2· 2 H 2 O), Al(OH)3.

n n Механизм адсорбции объяснил Лэнгмюр. Адсорбция идёт не на всей поверхности адсорбента, а только на активных центрах. Активными центрами служат узлы кристаллической решётки, выступы, шероховатости. Каждый активный центр адсорбирует только 1 молекулу. Адсорбтив располагается на поверхности адсорбента мономолекулярным слоем. На поверхности твердого вещества адсорбируются те газы, которые легко конденсируются на данной поверхности. Например: уголь хорошо адсорбирует аммиак, почти не адсорбирует угарный газ.
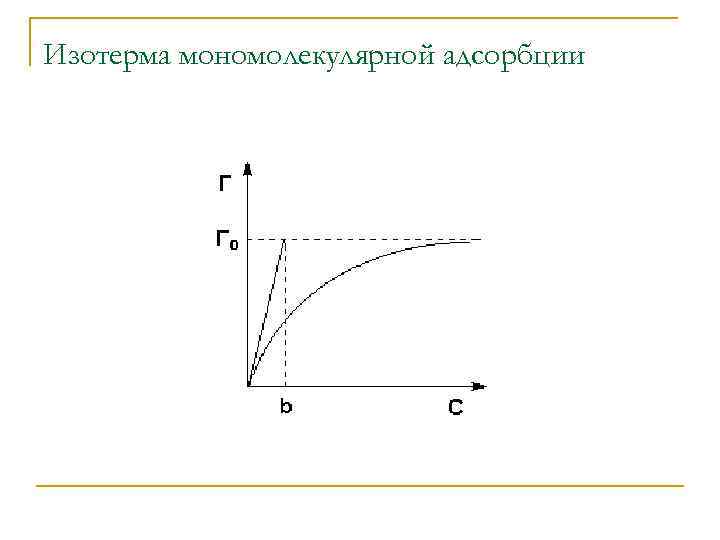
Изотерма мономолекулярной адсорбции

Адсорбция из растворов (молекулярная) n n В процессе адсорбции из растворов участвуют три вещества: адсорбат, адсорбент и растворитель. Процесс в этом случае осложняется тем, что на адсорбенте может адсорбироваться не только адсорбат, но и растворитель, тем самым, снижая адсорбцию адсорбата. Молекулярную адсорбцию изучал русский ученый П. А. Ребиндер. Он сформулировал правило выравнивания полярностей: на полярных адсорбентах лучше адсорбируется полярные адсорбаты, из малополярных растворителей, на неполярных адсорбентах лучше адсорбируется неполярные адсорбаты, из полярных растворителей. То есть подобное растворяется в подобном, но труднее из него адсорбируется. Все гидрофильные вещества (силикагель, глина, оксид магния, гидроксид алюминия) хорошо адсорбируют полярные вещества из неполярных жидкостей. Все гидрофобные вещества (уголь, графит, парафин, целлюлоза, крахмал) хорошо адсорбируют неполярные вещества из полярных жидкостей.

n Механизм молекулярной адсорбции лежит в основе одного из самых современных методов лечения – гемосорбции – очистки крови от токсических веществ с помощью различных адсорбентов. В медицине это называют гемоперфузией и используют при почечной и печеночной недостаточности, сильными отравлениями барбитуратами, фосфорорганическими и хлорсодержащими (дихлорэтан, тетрахлорметан ир др. ) соединениями.

Ионная адсорбция n Если на адсорбент действовать растворами электролитов, то будет происходить ионная адсорбция. Необходимым условием адсорбции ионов является наличие на поверхности адсорбента либо полярных молекул, либо ионов. Адсорбционная способность ионов на адсорбенте увеличивается с увеличением их заряда. При одинаковых зарядах адсорбционная способность увеличивается с увеличением их радиуса. В соответствии с этим правилом ионы располагаются в лиотропные ряды: Cs+ > Rb+ > K+ > Na+ > Li+; J- > Br- > Cl- >F-; K+ < Ca 2+ < Al 3+.

Различают несколько видов ионной адсорбции: n Избирательная адсорбция. Правило Фаянса: на поверхности кристалла адсорбируются те ионы, которые входят в состав кристаллической решетки адсорбента. Например: адсорбент – йодид серебра, адсорбат – йодид калия, адсорбироваться будут ионы йода. n Ионно-обменная адсорбция. В данном случае раствор электролита и адсорбент обмениваются в эквивалентных количествах одноименно заряженными ионами.

n Адсорбентами могут быть природные алюмосиликаты (цеолиты) или синтетические ионно-обменные смолы, которые представляют собой органические вещества, в состав которых входит Н+, тогда соединение называют катионит, ОН- - анионит, и Н+ и ОН- - амфолит. Эти вещества способны обменивать ионы водорода и гидроксид ионы на катионы и анионы, находящиеся в растворе.

n n n Амфолиты способны адсорбировать и катионы, и анионы. Это используется для устранения жесткости, которая обусловлена присутствием ионов кальция, магния, сульфатов, хлоридов, карбонатов. В качестве амфолитов используют пермутиты (соли алюминия). Ионно-обменные смолы можно регенерировать, пропуская через них ионы натрия. В медицине используют катиониты для консервирования крови. Кальций крови замещают на натрий катионита, процесс свертывания прекращается. Для снижения ацидоза крови используют замену ионов водорода крови на ионы натрия катионитов. Явление адсорбции лежит в основе многих физико-химических методов исследования, в том числе и хроматографии.

n n n n n Примеры адсорбентов как лекарственных препаратов (в гранулах, порошках, таблетках, пастах, гелях): На основе активированного угля (Карболен, Карболонг, Карбактин, Уголь активированный «КМ» , Ультра адсорб). На основе поливинилпирролидона ( Энтеродез, Энтеросорб). На основе кремнийорганических веществ ( Энтеросгель, Полисорб МП). На основе алюминия и магния ( Альмагель, Гастал, Фосфалюгель). На основе сукральфата ( Вентер). На основе лигнина и целлюлозы (Лигносорб, Полифепан, Фильрум-СТИ, Энтегнин). На основе медицинской глины ( Смекта и Неосмектин). Производные альгиновой кислоты (Альгисорб); анионообменные смолы – Колестирамин и Колестипол.
Поверхностные явления.ppt