Л 10. Дисперсные системы.ppt
- Количество слайдов: 53
 Физикохимия дисперсных систем и растворов ВМС Лекция 10 Кафедра медицинской и биологической химии ХМГМА
Физикохимия дисперсных систем и растворов ВМС Лекция 10 Кафедра медицинской и биологической химии ХМГМА
 План лекции p p p Классификация дисперсных систем по степени дисперсности; по силе межмолекулярного взаимодействия между дисперсной фазой и дисперсионной средой. Природа коллоидного состояния. Получение суспензий, эмульсий, коллоидных растворов. Диализ, электродиализ, ультрафильтрация. Физико-химические принципы функционирования искусственной почки. Молекулярно-кинетические, оптические и электрокинетические свойства коллоидно-дисперсных систем; устойчивость. Коллоидные ПАВ. Мицеллообразование в растворах ПАВ. Липосомы, применение в медицине. Свойства растворов ВМС. Особенности растворения ВМС, как следствие их структуры. Свойства растворов биополимеров.
План лекции p p p Классификация дисперсных систем по степени дисперсности; по силе межмолекулярного взаимодействия между дисперсной фазой и дисперсионной средой. Природа коллоидного состояния. Получение суспензий, эмульсий, коллоидных растворов. Диализ, электродиализ, ультрафильтрация. Физико-химические принципы функционирования искусственной почки. Молекулярно-кинетические, оптические и электрокинетические свойства коллоидно-дисперсных систем; устойчивость. Коллоидные ПАВ. Мицеллообразование в растворах ПАВ. Липосомы, применение в медицине. Свойства растворов ВМС. Особенности растворения ВМС, как следствие их структуры. Свойства растворов биополимеров.
 Дисперсные системы (ДСи) – многофазные системы, состоящие из дисперсной фазы (ДФ) и непрерывной дисперсионной среды(ДС). Дисперсная фаза раздробленных частиц. – это совокупность
Дисперсные системы (ДСи) – многофазные системы, состоящие из дисперсной фазы (ДФ) и непрерывной дисперсионной среды(ДС). Дисперсная фаза раздробленных частиц. – это совокупность
 Классификация дисперсных систем По степени дисперсности: = 1/d, d – диаметр частиц, м p Грубодисперсные (d 10 -7 м; 107 м-1). К ним относят суспензии, эмульсии. p Коллоидно-дисперсные (d = 10 -7 - 10 -9 м; = 107 - 109 м-1). Это коллоидные растворы. p Молекулярные ДСи (d 10 -9 м). К ним относят истинные растворы.
Классификация дисперсных систем По степени дисперсности: = 1/d, d – диаметр частиц, м p Грубодисперсные (d 10 -7 м; 107 м-1). К ним относят суспензии, эмульсии. p Коллоидно-дисперсные (d = 10 -7 - 10 -9 м; = 107 - 109 м-1). Это коллоидные растворы. p Молекулярные ДСи (d 10 -9 м). К ним относят истинные растворы.
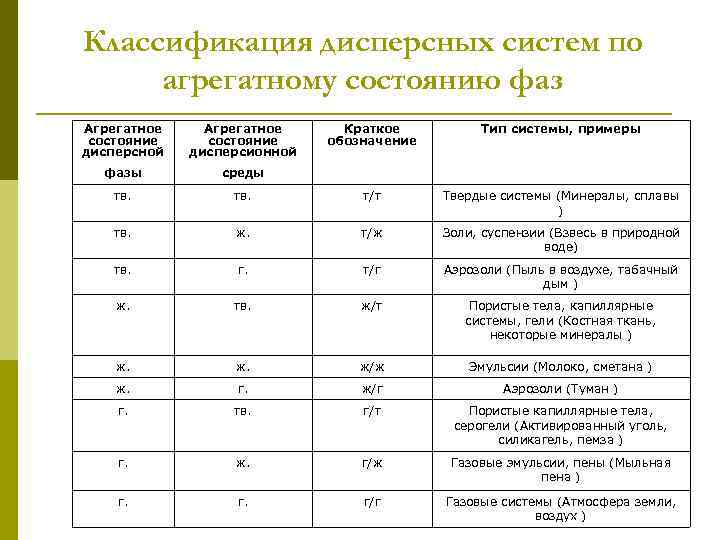 Классификация дисперсных систем по агрегатному состоянию фаз Агрегатное состояние дисперсной Агрегатное состояние дисперсионной Краткое обозначение Тип системы, примеры фазы среды тв. т/т Твердые системы (Минералы, сплавы ) тв. ж. т/ж Золи, суспензии (Взвесь в природной воде) тв. г. т/г Аэрозоли (Пыль в воздухе, табачный дым ) ж. тв. ж/т Пористые тела, капиллярные системы, гели (Костная ткань, некоторые минералы ) ж. ж/ж Эмульсии (Молоко, сметана ) ж. г. ж/г Аэрозоли (Туман ) г. тв. г/т Пористые капиллярные тела, серогели (Активированный уголь, силикагель, пемза ) г. ж. г/ж Газовые эмульсии, пены (Мыльная пена ) г. г/г Газовые системы (Атмосфера земли, воздух )
Классификация дисперсных систем по агрегатному состоянию фаз Агрегатное состояние дисперсной Агрегатное состояние дисперсионной Краткое обозначение Тип системы, примеры фазы среды тв. т/т Твердые системы (Минералы, сплавы ) тв. ж. т/ж Золи, суспензии (Взвесь в природной воде) тв. г. т/г Аэрозоли (Пыль в воздухе, табачный дым ) ж. тв. ж/т Пористые тела, капиллярные системы, гели (Костная ткань, некоторые минералы ) ж. ж/ж Эмульсии (Молоко, сметана ) ж. г. ж/г Аэрозоли (Туман ) г. тв. г/т Пористые капиллярные тела, серогели (Активированный уголь, силикагель, пемза ) г. ж. г/ж Газовые эмульсии, пены (Мыльная пена ) г. г/г Газовые системы (Атмосфера земли, воздух )
 Классификация дисперсных систем по характеру взаимодействия дисперсной фазы по отношению к дисперсионной среде: p p Лиофильные (гидрофильные) – сильное взаимодействие между фазами. Характеризуются высокой устойчивостью. Лиофобные (гидрофобные) – слабое взаимодействие между фазами. Характеризуются низкой устойчивостью. Свободнодисперсные – частицы дисперсной фазы могут независимо передвигаться в дисперсионной среде, обладают текучестью (суспензии, эмульсии, золи, аэрозоли) Связнодисперсные – частицы дисперсной фазы не могут независимо передвигаться в дисперсионной среде, не обладают текучестью (гели, пасты, порошки, концентрированные эмульсии) Переход связнодисперсных систем в свободнодисперсные и наоборот, называется тиксотропией.
Классификация дисперсных систем по характеру взаимодействия дисперсной фазы по отношению к дисперсионной среде: p p Лиофильные (гидрофильные) – сильное взаимодействие между фазами. Характеризуются высокой устойчивостью. Лиофобные (гидрофобные) – слабое взаимодействие между фазами. Характеризуются низкой устойчивостью. Свободнодисперсные – частицы дисперсной фазы могут независимо передвигаться в дисперсионной среде, обладают текучестью (суспензии, эмульсии, золи, аэрозоли) Связнодисперсные – частицы дисперсной фазы не могут независимо передвигаться в дисперсионной среде, не обладают текучестью (гели, пасты, порошки, концентрированные эмульсии) Переход связнодисперсных систем в свободнодисперсные и наоборот, называется тиксотропией.
 Методы получения коллоидных растворов Диспергационные: дробление - механическое; - ультразвуковое; - электрическое; - химическое. • Конденсационные: - физическая конденсация; - химическая конденсация •
Методы получения коллоидных растворов Диспергационные: дробление - механическое; - ультразвуковое; - электрическое; - химическое. • Конденсационные: - физическая конденсация; - химическая конденсация •
 Строение коллоидных частиц Ag. NO 3 + KJ Ag. J +KNO 3 При избытке Ag. NO 3: {m. Ag. J n. Ag+ (n-x)NO 3 -}x+ x. NO 3 - _______ агрегат _______ ядро _____________ гранула ____________________ мицелла n. Ag+ - потенциалопределяющие ионы; (n-x)NO 3 - - противоионы; x. NO 3 - - диффузный слой
Строение коллоидных частиц Ag. NO 3 + KJ Ag. J +KNO 3 При избытке Ag. NO 3: {m. Ag. J n. Ag+ (n-x)NO 3 -}x+ x. NO 3 - _______ агрегат _______ ядро _____________ гранула ____________________ мицелла n. Ag+ - потенциалопределяющие ионы; (n-x)NO 3 - - противоионы; x. NO 3 - - диффузный слой
 Строение коллоидных частиц При избытке KJ: {m. Ag. J n. J- (n-x)K+}x- x. K+ При равенстве концентраций KJ и Ag. NO 3: {m. Ag. J n. Ag+ n. NO 3 -}0, или {m. Ag. J n. Ag+ n. J-}0
Строение коллоидных частиц При избытке KJ: {m. Ag. J n. J- (n-x)K+}x- x. K+ При равенстве концентраций KJ и Ag. NO 3: {m. Ag. J n. Ag+ n. NO 3 -}0, или {m. Ag. J n. Ag+ n. J-}0
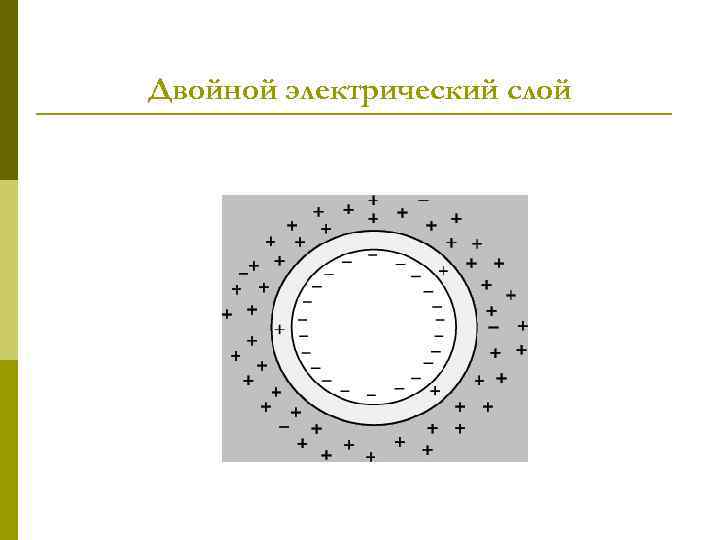 Двойной электрический слой
Двойной электрический слой
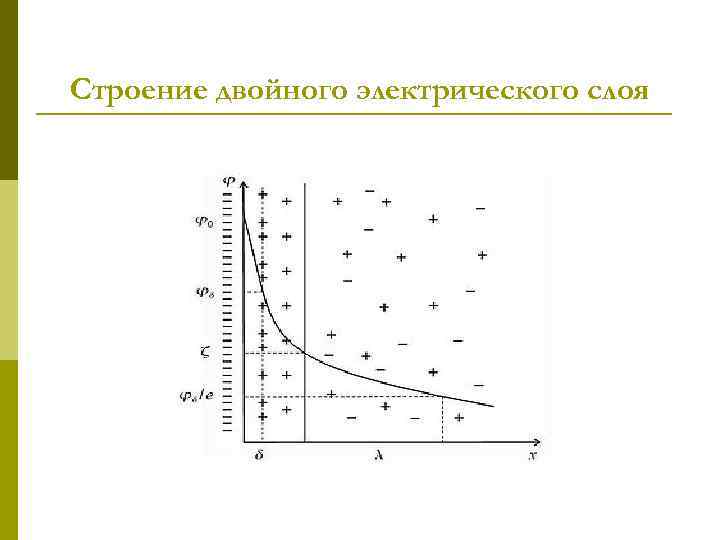 Строение двойного электрического слоя
Строение двойного электрического слоя
 Потенциалы двойного электрического слоя Слой Гельмгольца или адсорбционный слой, примыкающий непосредственно к межфазной поверхности. Этот слой имеет толщину δ, равную радиусу потенциалопределяющих ионов в не сольватированном состоянии. p Диффузный слой или слой Гуи, в котором находятся противоионы. Диффузный слой имеет толщину λ, которая зависит от свойств системы и может достигать больших значений. p
Потенциалы двойного электрического слоя Слой Гельмгольца или адсорбционный слой, примыкающий непосредственно к межфазной поверхности. Этот слой имеет толщину δ, равную радиусу потенциалопределяющих ионов в не сольватированном состоянии. p Диффузный слой или слой Гуи, в котором находятся противоионы. Диффузный слой имеет толщину λ, которая зависит от свойств системы и может достигать больших значений. p
 Потенциалы двойного электрического слоя Электрической характеристикой ДЭС является потенциал φ. Существует несколько характеристических потенциалов: - Потенциал диффузного слоя φδ, соответствующий границе адсорбционного и диффузного слоёв. - Потенциал φx = λ, меньший, чем φδ и характеризующий толщину диффузного слоя. - Электрокинетический потенциал или дзета-потенциал ζ. Этот потенциал соответствует плоскости скольжения и является частью потенциала диффузного слоя. Плоскость скольжения образуется в результате того, что при движении дисперсных частиц наиболее удаленная часть диффузного слоя не участвует в движении, а остается неподвижной. Поэтому появляется нескомпенсированность поверхностного заряда частицы и становятся возможными электрокинетические явления. Дзетапотенциал является одной из важнейших характеристик двойного электрического слоя.
Потенциалы двойного электрического слоя Электрической характеристикой ДЭС является потенциал φ. Существует несколько характеристических потенциалов: - Потенциал диффузного слоя φδ, соответствующий границе адсорбционного и диффузного слоёв. - Потенциал φx = λ, меньший, чем φδ и характеризующий толщину диффузного слоя. - Электрокинетический потенциал или дзета-потенциал ζ. Этот потенциал соответствует плоскости скольжения и является частью потенциала диффузного слоя. Плоскость скольжения образуется в результате того, что при движении дисперсных частиц наиболее удаленная часть диффузного слоя не участвует в движении, а остается неподвижной. Поэтому появляется нескомпенсированность поверхностного заряда частицы и становятся возможными электрокинетические явления. Дзетапотенциал является одной из важнейших характеристик двойного электрического слоя.
 Электрокинетические свойства дисперсных систем Электрокинетические явления: 1. перемещение дисперсной фазы или дисперсионной среды под действием внешнего электрического поля; 2. возникновение разности потенциалов при перемещении дисперсной фазы или дисперсионной среды при относительно друга
Электрокинетические свойства дисперсных систем Электрокинетические явления: 1. перемещение дисперсной фазы или дисперсионной среды под действием внешнего электрического поля; 2. возникновение разности потенциалов при перемещении дисперсной фазы или дисперсионной среды при относительно друга
 Электрокинетические свойства дисперсных систем Явления 1 рода: p Электрофорез – движение дисперсной фазы относительно неподвижной дисперсионной среды под действием электрического тока. p Электроосмос - движение дисперсионной среды относительно неподвижной дисперсной фазы под действием электрического тока. Явления 2 рода: p Потенциал седиментации - возникновение разности потенциалов при движении частиц дисперсной фазы в неподвижной дисперсионной среде. p Потенциал протекания - возникновение разности потенциалов при движении дисперсионной среды относительно неподвижной дисперсной фазы.
Электрокинетические свойства дисперсных систем Явления 1 рода: p Электрофорез – движение дисперсной фазы относительно неподвижной дисперсионной среды под действием электрического тока. p Электроосмос - движение дисперсионной среды относительно неподвижной дисперсной фазы под действием электрического тока. Явления 2 рода: p Потенциал седиментации - возникновение разности потенциалов при движении частиц дисперсной фазы в неподвижной дисперсионной среде. p Потенциал протекания - возникновение разности потенциалов при движении дисперсионной среды относительно неподвижной дисперсной фазы.
 Молекулярно-кинетические свойства коллоидных растворов Броуновское движение: x =√ k. B t T / 3 π r ή – уравнение Энштейна. Смолуховского p Диффузия p Осмотическое давление πосм. =3 m. Д k. B T/ 4 π r 3 ρ p Седиментация U = 2/9 g r 2 (ρ- ρ0)/ ή - закон Стокса p
Молекулярно-кинетические свойства коллоидных растворов Броуновское движение: x =√ k. B t T / 3 π r ή – уравнение Энштейна. Смолуховского p Диффузия p Осмотическое давление πосм. =3 m. Д k. B T/ 4 π r 3 ρ p Седиментация U = 2/9 g r 2 (ρ- ρ0)/ ή - закон Стокса p
 Оптические свойства дисперсных систем При попадании луча света на дисперсную систему могут наблюдаться: p Прохождение света через систему; p Преломление; p Рассеяние; p Отражение; p Абсорбция (поглощение).
Оптические свойства дисперсных систем При попадании луча света на дисперсную систему могут наблюдаться: p Прохождение света через систему; p Преломление; p Рассеяние; p Отражение; p Абсорбция (поглощение).
 Оптические свойства дисперсных систем Интенсивность рассеивания света зависит от природы дисперсной системы Закон Рэлея: J=Jo Kр (Сυ r 6/λ 4 ), где Jo – интенсивность падающего света, В/м 2; J – интенсивность рассеянного света, В/м 2; С υ – частичная концентрация; Kр – константа Рэлея, м 3; λ – длина волны падающего света, м; r – радиус частиц, м. p
Оптические свойства дисперсных систем Интенсивность рассеивания света зависит от природы дисперсной системы Закон Рэлея: J=Jo Kр (Сυ r 6/λ 4 ), где Jo – интенсивность падающего света, В/м 2; J – интенсивность рассеянного света, В/м 2; С υ – частичная концентрация; Kр – константа Рэлея, м 3; λ – длина волны падающего света, м; r – радиус частиц, м. p
 p Эффект Тиндаля - рассеяние света при прохождении светового пучка через оптически неоднородную среду. Обычно наблюдается в виде светящегося конуса (конус Тиндаля), видимого на тёмном фоне
p Эффект Тиндаля - рассеяние света при прохождении светового пучка через оптически неоднородную среду. Обычно наблюдается в виде светящегося конуса (конус Тиндаля), видимого на тёмном фоне

 Устойчивость и коагуляция дисперсных систем Устойчивость дисперсных систем характеризуется неизменностью во времени её основных параметров: степени дисперсности и равномерного распределения дисперсной фазы в дисперсионной среде. Устойчивость: - агрегативная - седиментационная (кинетическая);
Устойчивость и коагуляция дисперсных систем Устойчивость дисперсных систем характеризуется неизменностью во времени её основных параметров: степени дисперсности и равномерного распределения дисперсной фазы в дисперсионной среде. Устойчивость: - агрегативная - седиментационная (кинетическая);
 Факторы устойчивости дисперсных систем Термодинамические: - электростатический – за счет образования на поверхности частиц двойных электрических слоев с одноименно заряженными противоионами, что вызывает электростатическое отталкивание частиц; - адсорбционно-сольватный – за счет уменьшения поверхностного натяжения при взаимодействии частиц дисперсной фазы со средой либо за счет сольватации поверхности, либо адсорбции неэлектролитов, либо за счет поверхностной диссоциации - энтропийный – за счет броуновского движения, стремления частиц дисперсной фазы к равномерному распределению по объему системы под действием теплового движения p
Факторы устойчивости дисперсных систем Термодинамические: - электростатический – за счет образования на поверхности частиц двойных электрических слоев с одноименно заряженными противоионами, что вызывает электростатическое отталкивание частиц; - адсорбционно-сольватный – за счет уменьшения поверхностного натяжения при взаимодействии частиц дисперсной фазы со средой либо за счет сольватации поверхности, либо адсорбции неэлектролитов, либо за счет поверхностной диссоциации - энтропийный – за счет броуновского движения, стремления частиц дисперсной фазы к равномерному распределению по объему системы под действием теплового движения p
 Факторы устойчивости дисперсных систем Кинетические: - структурно-механический – за счет образования на поверхности частиц упругих и прочных пленок из вводимых в систему ПАВ или ВМС; - гидродинамический затрудняет сближение частиц вследствие увеличения вязкости и плотности прослоек среды между частицами. p
Факторы устойчивости дисперсных систем Кинетические: - структурно-механический – за счет образования на поверхности частиц упругих и прочных пленок из вводимых в систему ПАВ или ВМС; - гидродинамический затрудняет сближение частиц вследствие увеличения вязкости и плотности прослоек среды между частицами. p
 Коагуляция – процесс потери агрегативной устойчивости, сопровождающейся разделением фаз и разрушением дисперсной системы. При этом происходит соединение частиц, образование более крупных агрегатов. Коагуляция электролитами – правило Шульца-Гарди: «Коагулирующее действие вызывает тот ион, который несет заряд противоположный заряду гранулы» Коагулирующая способность ионов зависит от природы электролита: заряда иона и радиуса. Чем больше заряд и больше радиус иона, тем коагулирующая способность выше.
Коагуляция – процесс потери агрегативной устойчивости, сопровождающейся разделением фаз и разрушением дисперсной системы. При этом происходит соединение частиц, образование более крупных агрегатов. Коагуляция электролитами – правило Шульца-Гарди: «Коагулирующее действие вызывает тот ион, который несет заряд противоположный заряду гранулы» Коагулирующая способность ионов зависит от природы электролита: заряда иона и радиуса. Чем больше заряд и больше радиус иона, тем коагулирующая способность выше.
 Коагуляция может быть скрытой и явной. Минимальная концентрация электролита, по достижении которой начинается коагуляция, называется порогом коагуляции С(пор. ) = (С(эл) V(эл)/ V(общ)) 1000, ммоль/л; Коагулирующая способность электролита Vкс =1/ С(пор. ) При коагуляции смесями электролитов возможны: аддитивность, антагонизм, синергизм электролитов.
Коагуляция может быть скрытой и явной. Минимальная концентрация электролита, по достижении которой начинается коагуляция, называется порогом коагуляции С(пор. ) = (С(эл) V(эл)/ V(общ)) 1000, ммоль/л; Коагулирующая способность электролита Vкс =1/ С(пор. ) При коагуляции смесями электролитов возможны: аддитивность, антагонизм, синергизм электролитов.
 Пептизация- переход осадков, полученных при коагуляции дисперсных систем, в золи. p Коллоидная защита – повышение устойчивости золей от коагуляции электролитами при добавлении некоторых веществ (ПАВ, ВМС). p
Пептизация- переход осадков, полученных при коагуляции дисперсных систем, в золи. p Коллоидная защита – повышение устойчивости золей от коагуляции электролитами при добавлении некоторых веществ (ПАВ, ВМС). p
 Методы очистки коллоидных растворов p p p Фильтрация – основана на способности коллоидных частиц проходить через поры фильтров. Ультрафильтрация – метод фильтрации под давлением, позволяет очистить систему от низкомолекулярных веществ. Диализ – удаление с помощью мембран низкомолекулярных соединений из коллоидных растворов и растворов высокомолекулярных соединений. В качестве мембран для диализа применяют как естественные, так и искусственные материалы. Электродиализ – диализ с использованием постоянного электрического поля с падением потенциала. Компенсационный диализ - удаление с помощью мембран лишь части низкомолекулярных соединений из коллоидных растворов и растворов высокомолекулярных соединений. Принцип лежит в основе работы «искусственная почка» .
Методы очистки коллоидных растворов p p p Фильтрация – основана на способности коллоидных частиц проходить через поры фильтров. Ультрафильтрация – метод фильтрации под давлением, позволяет очистить систему от низкомолекулярных веществ. Диализ – удаление с помощью мембран низкомолекулярных соединений из коллоидных растворов и растворов высокомолекулярных соединений. В качестве мембран для диализа применяют как естественные, так и искусственные материалы. Электродиализ – диализ с использованием постоянного электрического поля с падением потенциала. Компенсационный диализ - удаление с помощью мембран лишь части низкомолекулярных соединений из коллоидных растворов и растворов высокомолекулярных соединений. Принцип лежит в основе работы «искусственная почка» .
 Липосомы, применение в медицине p Липосомы сферические мицеллы, образующиеся в системе вода-фосфолипид. Молекулы фосфолипидов образуют в липосомах бислойную мембрану, в которой полярные группы обращены к воде, неполярные- друг к другу. Липосомы являются моделью биологических мембран. Липосомы используют для направленной доставки лекарственных веществ.
Липосомы, применение в медицине p Липосомы сферические мицеллы, образующиеся в системе вода-фосфолипид. Молекулы фосфолипидов образуют в липосомах бислойную мембрану, в которой полярные группы обращены к воде, неполярные- друг к другу. Липосомы являются моделью биологических мембран. Липосомы используют для направленной доставки лекарственных веществ.

 Свойства растворов высокомолекулярных соединений (ВМС) К высокомолекулярным соединениям (ВМС) относят вещества с молекулярной массой 104 – 106 г/моль (Дальтон). ВМС состоят из ковалентно и молекулярно связанных мономерных звеньев. ВМС называют полимерами, а вещества биологического происхождения – биополимерами. Если звено полимерной цепи содержит ионогенную группу, полимер называют полиэлектролитом.
Свойства растворов высокомолекулярных соединений (ВМС) К высокомолекулярным соединениям (ВМС) относят вещества с молекулярной массой 104 – 106 г/моль (Дальтон). ВМС состоят из ковалентно и молекулярно связанных мономерных звеньев. ВМС называют полимерами, а вещества биологического происхождения – биополимерами. Если звено полимерной цепи содержит ионогенную группу, полимер называют полиэлектролитом.
 Классификация высокомолекулярных соединений По пространственной структуре: Линейные ( каучук, целлюлоза, желатин); p Разветвленные (амилопектин, гликоген); p Лестничные (искусственные волокна); p Сетчатые (фибрин, шерсть) p
Классификация высокомолекулярных соединений По пространственной структуре: Линейные ( каучук, целлюлоза, желатин); p Разветвленные (амилопектин, гликоген); p Лестничные (искусственные волокна); p Сетчатые (фибрин, шерсть) p
 По характеру мономеров: p Гомополимеры (один вид мономера); p Гетерополимеры (несколько видов мономеров); Гетерополимеры, с закономерным чередованием двух-трёх одних и тех же звеньев, называют сополимерами. По природе мономеров: p Неорганические; p Органические; p Элементорганические
По характеру мономеров: p Гомополимеры (один вид мономера); p Гетерополимеры (несколько видов мономеров); Гетерополимеры, с закономерным чередованием двух-трёх одних и тех же звеньев, называют сополимерами. По природе мономеров: p Неорганические; p Органические; p Элементорганические
 p p p По происхождению: Природные полимеры, синтезирующиеся клетками растений и животных: белки, нуклеиновые кислоты, полисахариды, латексы. Искусственные полимеры - продукты переработки природных полимеров: шелк, вискоза, каучуки. Синтетические полимеры - полученные химическим синтезом: полиэтилен, нейлон, капрон, лавсан, поливинилацетат.
p p p По происхождению: Природные полимеры, синтезирующиеся клетками растений и животных: белки, нуклеиновые кислоты, полисахариды, латексы. Искусственные полимеры - продукты переработки природных полимеров: шелк, вискоза, каучуки. Синтетические полимеры - полученные химическим синтезом: полиэтилен, нейлон, капрон, лавсан, поливинилацетат.
 Образование растворов ВМС образуют как молекулярные, так и коллоидные растворы. Если молекулы ВМС содержат в своей молекуле полярные группы, то образуют водные растворы. Неполярные полимеры образуют растворы с неполярными растворителями. Например, большинство белков легко растворяются в воде, но в этаноле они переходят в коллоидное состояние. Поливинилацетатный клей образует прозрачные молекулярные растворы в этаноле, но переходит в коллоидное состояние в воде. Растворению ВМС предшествует набухание
Образование растворов ВМС образуют как молекулярные, так и коллоидные растворы. Если молекулы ВМС содержат в своей молекуле полярные группы, то образуют водные растворы. Неполярные полимеры образуют растворы с неполярными растворителями. Например, большинство белков легко растворяются в воде, но в этаноле они переходят в коллоидное состояние. Поливинилацетатный клей образует прозрачные молекулярные растворы в этаноле, но переходит в коллоидное состояние в воде. Растворению ВМС предшествует набухание
 Набухание- это самопроизвольный процесс избирательного поглощения низкомолекулярного растворителя высокомолекулярным соединением за счет односторонней диффузии растворителя, сопровождающийся увеличением массы и объема полимера. Различают два типа набухания: - неограниченное набухание, которое заканчивается полным растворением полимера и образованием молекулярного раствора. Так набухают большинство белков и полисахаридов: желатин, гиалуроновая кислота, пектины и т. д. - ограниченное набухание идет до определенного момента и прекращается образованием студней и гелей, которые содержат пространственную сетку из цепей полимера, заполненную молекулами растворителя. Ограниченно набухают в воде большинство ионообменных смол, каучук в бензоле и т. д.
Набухание- это самопроизвольный процесс избирательного поглощения низкомолекулярного растворителя высокомолекулярным соединением за счет односторонней диффузии растворителя, сопровождающийся увеличением массы и объема полимера. Различают два типа набухания: - неограниченное набухание, которое заканчивается полным растворением полимера и образованием молекулярного раствора. Так набухают большинство белков и полисахаридов: желатин, гиалуроновая кислота, пектины и т. д. - ограниченное набухание идет до определенного момента и прекращается образованием студней и гелей, которые содержат пространственную сетку из цепей полимера, заполненную молекулами растворителя. Ограниченно набухают в воде большинство ионообменных смол, каучук в бензоле и т. д.
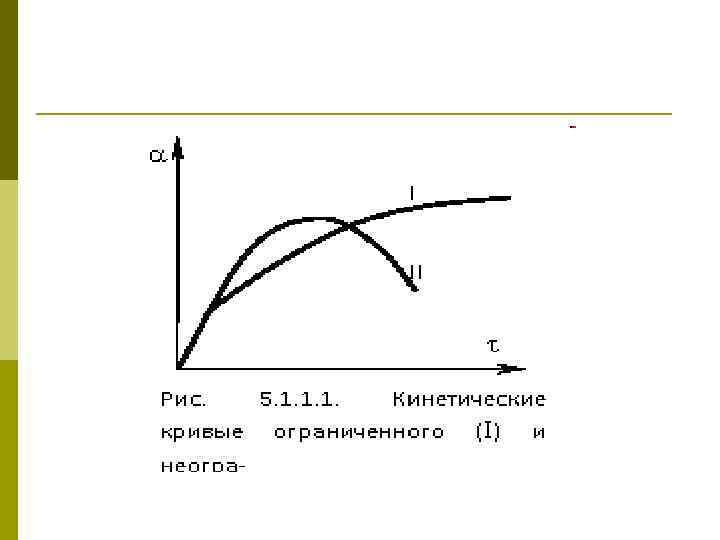
 Степень набухания (α) можно определить по разнице между массой полимера после набухания (m) и его начальной массой (mo): α% = (m – mo/mo) х 100 %, либо по разнице между объемом полимера после набухания (V) и его начальным объемом (Vo): α% = (V – Vo/Vo) х 100 %,
Степень набухания (α) можно определить по разнице между массой полимера после набухания (m) и его начальной массой (mo): α% = (m – mo/mo) х 100 %, либо по разнице между объемом полимера после набухания (V) и его начальным объемом (Vo): α% = (V – Vo/Vo) х 100 %,
 Механизм и термодинамика процесса набухания І стадия – сольватация(гидратация) полимера, при которой происходит диффузия растворителя в ВМС, связывание молекул растворителя с определенными группами макромолекул. Вода, образующая гидратные оболочки, называется «связанной» . ΔΗ< 0. ІІ стадия - связана с проникновением молекул растворителя между цепями полимера и заполнении пустот. Движущей силой является осмос. В этой стадии увеличивается объем и масса полимера. Δ S>0.
Механизм и термодинамика процесса набухания І стадия – сольватация(гидратация) полимера, при которой происходит диффузия растворителя в ВМС, связывание молекул растворителя с определенными группами макромолекул. Вода, образующая гидратные оболочки, называется «связанной» . ΔΗ< 0. ІІ стадия - связана с проникновением молекул растворителя между цепями полимера и заполнении пустот. Движущей силой является осмос. В этой стадии увеличивается объем и масса полимера. Δ S>0.
 Факторы, влияющие на процесс набухания полимеров: Природа ВМС – лучше набухают ВМС с гибкими анизодиаметрическими макромолекулами, в аморфном состоянии. р. Н - концентрация ионов водорода определяет степень ионизации заряженных групп в молекуле полимера и их способность связывать молекулы воды. Для полиамфолитов набухание минимально при р. Н = р. J. Присутствие электролитов, образующих большие гидратные оболочки снижает степень набухания полимера, поскольку они отвлекают молекулы воды на себя. В то же время ионы, слабо гидратирующиеся ускоряют набухание.
Факторы, влияющие на процесс набухания полимеров: Природа ВМС – лучше набухают ВМС с гибкими анизодиаметрическими макромолекулами, в аморфном состоянии. р. Н - концентрация ионов водорода определяет степень ионизации заряженных групп в молекуле полимера и их способность связывать молекулы воды. Для полиамфолитов набухание минимально при р. Н = р. J. Присутствие электролитов, образующих большие гидратные оболочки снижает степень набухания полимера, поскольку они отвлекают молекулы воды на себя. В то же время ионы, слабо гидратирующиеся ускоряют набухание.
 Факторы, влияющие на процесс набухания полимеров Повышение температуры ускоряет сольватацию полимера и может вызывать переход ограниченного набухания до неограниченного. Процессы набухания наблюдаются в живых системах, которые имеют значительное количество белков, нуклеиновых кислот, полисахаридов, способных связывать значительные количества воды. При снижении р. Н (например, при воспалительном процессе в тканях, укусах пчел и т. д. ) белки начинают связывать большее количество молекул воды, что проявляется припухлостью в участке воспаления. Для живых систем характерно антагонистическое набухание.
Факторы, влияющие на процесс набухания полимеров Повышение температуры ускоряет сольватацию полимера и может вызывать переход ограниченного набухания до неограниченного. Процессы набухания наблюдаются в живых системах, которые имеют значительное количество белков, нуклеиновых кислот, полисахаридов, способных связывать значительные количества воды. При снижении р. Н (например, при воспалительном процессе в тканях, укусах пчел и т. д. ) белки начинают связывать большее количество молекул воды, что проявляется припухлостью в участке воспаления. Для живых систем характерно антагонистическое набухание.
![Вязкость растворов ВМС описывается уравнением Штаудингера: [ή] =К·Мα где, К, α – экспериментальные константы, Вязкость растворов ВМС описывается уравнением Штаудингера: [ή] =К·Мα где, К, α – экспериментальные константы,](https://present5.com/presentation/3/-58532597_245939088.pdf-img/-58532597_245939088.pdf-41.jpg) Вязкость растворов ВМС описывается уравнением Штаудингера: [ή] =К·Мα где, К, α – экспериментальные константы, зависящие от формы молекул в растворе и от проницаемости молекул для растворителя; М - молекулярная масса полимера. По величине вязкости растворов ВМС можно рассчитать их среднюю молекулярную массу.
Вязкость растворов ВМС описывается уравнением Штаудингера: [ή] =К·Мα где, К, α – экспериментальные константы, зависящие от формы молекул в растворе и от проницаемости молекул для растворителя; М - молекулярная масса полимера. По величине вязкости растворов ВМС можно рассчитать их среднюю молекулярную массу.
 Осмотическое давление растворов биополимеров Осмотическое давление растворов коллоидов и ВМС меньше по величине, чем у ионных растворов (которые при той же массе растворенного вещества содержат больше частиц). Осмотическое давление растворов ВМС не электролитов можно рассчитать по формуле Галлера: π = (С·R · T/М) + β · С 2 где, С - массовая концентрация полимера, г/л; М - молекулярная масса полимера; R - газовая постоянная; Т - абсолютная температура; β – коэффициент, учитывающий гибкость и форму макромолекул в растворе.
Осмотическое давление растворов биополимеров Осмотическое давление растворов коллоидов и ВМС меньше по величине, чем у ионных растворов (которые при той же массе растворенного вещества содержат больше частиц). Осмотическое давление растворов ВМС не электролитов можно рассчитать по формуле Галлера: π = (С·R · T/М) + β · С 2 где, С - массовая концентрация полимера, г/л; М - молекулярная масса полимера; R - газовая постоянная; Т - абсолютная температура; β – коэффициент, учитывающий гибкость и форму макромолекул в растворе.
 Часть осмотического давления биологических жидкостей, создаваемого белками называется онкотическим давленим. Онкотическое давление составляет 0, 5% от общего осмотического давления плазмы крови (соответственно 0, 038 и 7, 7 атм. ). Значение - распределение воды и низкомолекулярных веществ между кровью и тканями.
Часть осмотического давления биологических жидкостей, создаваемого белками называется онкотическим давленим. Онкотическое давление составляет 0, 5% от общего осмотического давления плазмы крови (соответственно 0, 038 и 7, 7 атм. ). Значение - распределение воды и низкомолекулярных веществ между кровью и тканями.
 Устойчивость растворов высокомолекулярных соединений Основным фактором термодинамической устойчивости растворов ВМС и, непосредственно растворов белков, есть их высокая гидрофильность, обусловленная наличием полярных групп в боковых цепях, вокруг которых образуются мощные гидратные оболочки.
Устойчивость растворов высокомолекулярных соединений Основным фактором термодинамической устойчивости растворов ВМС и, непосредственно растворов белков, есть их высокая гидрофильность, обусловленная наличием полярных групп в боковых цепях, вокруг которых образуются мощные гидратные оболочки.
 Виды нарушения устойчивости растворов ВМС Коацервация (расслоение) – проявляется образованим в растворе изолированных друг от друга макроскопических капель второй жидкой фазы – коацервата. Коацерват состоит из микроскопических капелек, разделенных гидратными оболочками. В зависимости от вязкости среды, они могут сливаться (коалесценция), либо соединяться друг с другом, образуя флокулы(флокуляция). Коацервацию используют для микрокапсулирования лекарств.
Виды нарушения устойчивости растворов ВМС Коацервация (расслоение) – проявляется образованим в растворе изолированных друг от друга макроскопических капель второй жидкой фазы – коацервата. Коацерват состоит из микроскопических капелек, разделенных гидратными оболочками. В зависимости от вязкости среды, они могут сливаться (коалесценция), либо соединяться друг с другом, образуя флокулы(флокуляция). Коацервацию используют для микрокапсулирования лекарств.
 Высаливание – осаждение белков при введении в раствор больших количеств нейтральных электролитов. Прямой лиотропный ряд Гофмейстера C 2 O 42 - >SO 42 - >PO 43 - >CH 3 COO- >Cl- >NO 3 - >Br - >I- >CNSПолнота высаливания зависит от молекулярной массы белков: чем больше молекулярная масса, тем полнее и быстрее происходит осаждение.
Высаливание – осаждение белков при введении в раствор больших количеств нейтральных электролитов. Прямой лиотропный ряд Гофмейстера C 2 O 42 - >SO 42 - >PO 43 - >CH 3 COO- >Cl- >NO 3 - >Br - >I- >CNSПолнота высаливания зависит от молекулярной массы белков: чем больше молекулярная масса, тем полнее и быстрее происходит осаждение.
 q Денатурация – нарушение нативной пространственной структуры белка, приводящее к изменению его физикохимических и биологических свойств. Факторы, вызывающие денатурацию: - повышение температуры; - замораживание и оттаивание; - ультразвук; - высокое давление; - радиация; - кислоты и щелочи; - соли тяжелых металлов; - сильно гидратирующиеся соли; - органические растворители; - окислители и восстановители;
q Денатурация – нарушение нативной пространственной структуры белка, приводящее к изменению его физикохимических и биологических свойств. Факторы, вызывающие денатурацию: - повышение температуры; - замораживание и оттаивание; - ультразвук; - высокое давление; - радиация; - кислоты и щелочи; - соли тяжелых металлов; - сильно гидратирующиеся соли; - органические растворители; - окислители и восстановители;
 p Застудневание – процесс превращения растворов ВМС в студни. Студни – растворы ВМС, потерявшие текучесть в результате образования в них внутренних структур. В организме человека студнями являются мозговое вещество, цитоплазма клеток и др.
p Застудневание – процесс превращения растворов ВМС в студни. Студни – растворы ВМС, потерявшие текучесть в результате образования в них внутренних структур. В организме человека студнями являются мозговое вещество, цитоплазма клеток и др.
 Мембранное равновесие Доннана
Мембранное равновесие Доннана
 Мембранное равновесие Доннана связано с переносом некоторого количества вещества низкомолекулярного электролита внутрь пространства, содержащего полимер, и, вследствие этого, неравномерного распределения концентраций этого электролита по обе стороны полупроницаемой мембраны. p. В левой части сосуда, разделенного полупроницаемой мембраной, находится раствор полимера, который в результате диссоциации представлен поликатионом R(Z+) и противоионом Cl–, концентрации которых равны соответственно C 1 и ZC 1. p
Мембранное равновесие Доннана связано с переносом некоторого количества вещества низкомолекулярного электролита внутрь пространства, содержащего полимер, и, вследствие этого, неравномерного распределения концентраций этого электролита по обе стороны полупроницаемой мембраны. p. В левой части сосуда, разделенного полупроницаемой мембраной, находится раствор полимера, который в результате диссоциации представлен поликатионом R(Z+) и противоионом Cl–, концентрации которых равны соответственно C 1 и ZC 1. p
 p p В правой части – раствор низкомолекулярного электролита, например KCl, с концентрацией С 2, диссоциирующий на К+ и Cl–. При установлении равновесия вследствие диффузии в такой системе малые ионы K+ перемещаются преимущественно из правой части сосуда в левую. Макрокатионы R(Z+) не могут проникать через мембрану, поэтому для сохранения электронейтральности вместе с катионами K+ справа налево происходит перемещение избыточного числа анионов Cl–. В результате этих процессов концентрация низкомолекулярного электролита в растворе ВМС повышается.
p p В правой части – раствор низкомолекулярного электролита, например KCl, с концентрацией С 2, диссоциирующий на К+ и Cl–. При установлении равновесия вследствие диффузии в такой системе малые ионы K+ перемещаются преимущественно из правой части сосуда в левую. Макрокатионы R(Z+) не могут проникать через мембрану, поэтому для сохранения электронейтральности вместе с катионами K+ справа налево происходит перемещение избыточного числа анионов Cl–. В результате этих процессов концентрация низкомолекулярного электролита в растворе ВМС повышается.
 Условием равновесия является равенство произведений концентраций электролитов в левой и правой части сосуда, разделенного полупроницаемой мембраной: [K+]внутр. [Cl–]внутр. = [K+]внеш. [Cl–]внеш. Подставляя обозначения, имеем уравнение: X (ZC 1 + X) = (C 2 – X)2 X = C 22/ ZC 1 + 2 C 2
Условием равновесия является равенство произведений концентраций электролитов в левой и правой части сосуда, разделенного полупроницаемой мембраной: [K+]внутр. [Cl–]внутр. = [K+]внеш. [Cl–]внеш. Подставляя обозначения, имеем уравнение: X (ZC 1 + X) = (C 2 – X)2 X = C 22/ ZC 1 + 2 C 2
 p Уравнение Доннана показывает количество низкомолекулярного вещества, переносимого в фазу ВМС через полупроницаемую мембрану. Из него следует вывод, что низкомолекулярный электролит распределяется неравномерно по обе стороны мембраны. Перенос вещества всегда существует из внешнего раствора во внутренний, в результате чего во внутреннем растворе наблюдается более высокая концентрация переносимых электролитов по сравнению с внешним раствором. Этим же объясняется некоторый избыток осмотического давления в растворах, содержащих ВМС и электролиты.
p Уравнение Доннана показывает количество низкомолекулярного вещества, переносимого в фазу ВМС через полупроницаемую мембрану. Из него следует вывод, что низкомолекулярный электролит распределяется неравномерно по обе стороны мембраны. Перенос вещества всегда существует из внешнего раствора во внутренний, в результате чего во внутреннем растворе наблюдается более высокая концентрация переносимых электролитов по сравнению с внешним раствором. Этим же объясняется некоторый избыток осмотического давления в растворах, содержащих ВМС и электролиты.


