¡ ФИЗИКОХИМИЯ ДИСПЕРСНЫХ СИСТЕМ ¡ Дисперсная система























![n Золотое число — это количество мг сухого полимера [например, желатины], защищающего 10 n Золотое число — это количество мг сухого полимера [например, желатины], защищающего 10](https://present5.com/presentation/3/44900853_24936417.pdf-img/44900853_24936417.pdf-35.jpg)








дисперсные системы.ppt
- Количество слайдов: 36
 ¡ ФИЗИКОХИМИЯ ДИСПЕРСНЫХ СИСТЕМ ¡ Дисперсная система – гетерогенная система, в которой мелкие частицы (дисперсная фаза) равномерно распределены в объеме другой фазы (дисперсионная среда).
¡ ФИЗИКОХИМИЯ ДИСПЕРСНЫХ СИСТЕМ ¡ Дисперсная система – гетерогенная система, в которой мелкие частицы (дисперсная фаза) равномерно распределены в объеме другой фазы (дисперсионная среда).
 l ЛИОФОБНЫЕ КОЛЛОИДНЫЕ РАСТВОРЫ - золи. ¡ Получение золей ¡. А. Дисперсионный метод. ¡ а/ Механические методы - дроблением, ¡ измельчением, истиранием ¡ б/ Ультразвуковой метод - под действием сжатий ¡ и расширений системы в/ Метод пептизации –перевод свежеприготовленных осадков при добавлении электролита (пептизатора) в коллоидный раствор; лечение тромбофлебита гепарином ¡ г/ Распыление под водой в вольтовой дуге ¡ благородных металлов с последующей ¡ конденсацией паров металла при охлаждении ¡ [метод Бредига)
l ЛИОФОБНЫЕ КОЛЛОИДНЫЕ РАСТВОРЫ - золи. ¡ Получение золей ¡. А. Дисперсионный метод. ¡ а/ Механические методы - дроблением, ¡ измельчением, истиранием ¡ б/ Ультразвуковой метод - под действием сжатий ¡ и расширений системы в/ Метод пептизации –перевод свежеприготовленных осадков при добавлении электролита (пептизатора) в коллоидный раствор; лечение тромбофлебита гепарином ¡ г/ Распыление под водой в вольтовой дуге ¡ благородных металлов с последующей ¡ конденсацией паров металла при охлаждении ¡ [метод Бредига)
 ¡ Б. Конденсационный метод. ¡ -на переводе веществ в нерастворимое ¡ состояние при помощи химических реакций ¡ а/ Метод окисления. ¡ 2 H 2 S + SO 2 3 S + 2 H 2 O ¡ б/ Метод восстановления. ¡ Ag 2 O + H 2 2 Ag + H 2 O [так образуется ¡ золь серебра] ¡ в/ Реакция двойного обмена с образованием труднорастворимого вещества: ¡ Ba. Cl 2 + K 2 SO 4 Ba. SO 4 + 2 KCl ¡ [золь сульфата бария] ¡ г / метод гидролиза. ¡ Fe. Cl 3 + 3 H 2 O Fe(OH)3 + 3 HCl ¡ д/ метод замены растворителя.
¡ Б. Конденсационный метод. ¡ -на переводе веществ в нерастворимое ¡ состояние при помощи химических реакций ¡ а/ Метод окисления. ¡ 2 H 2 S + SO 2 3 S + 2 H 2 O ¡ б/ Метод восстановления. ¡ Ag 2 O + H 2 2 Ag + H 2 O [так образуется ¡ золь серебра] ¡ в/ Реакция двойного обмена с образованием труднорастворимого вещества: ¡ Ba. Cl 2 + K 2 SO 4 Ba. SO 4 + 2 KCl ¡ [золь сульфата бария] ¡ г / метод гидролиза. ¡ Fe. Cl 3 + 3 H 2 O Fe(OH)3 + 3 HCl ¡ д/ метод замены растворителя.
 ¡ Очистка коллоидных растворов ¡ Диализ. –метод очистки коллоидных растворов от ионов и молекул низкомолекулярных примесей в результате их диффузии в чистый растворитель через полупроницаемую мемрану. ¡ Электродиализ – диализ в условиях постоянного тока ( ускоренный диализ)
¡ Очистка коллоидных растворов ¡ Диализ. –метод очистки коллоидных растворов от ионов и молекул низкомолекулярных примесей в результате их диффузии в чистый растворитель через полупроницаемую мемрану. ¡ Электродиализ – диализ в условиях постоянного тока ( ускоренный диализ)
 ¡ Вивидиализ ( гемодиализ): биологическая жидкость омывается не чистым ¡ растворителем, а изотоническими ¡ растворами электролитов. Для повышения ¡ эффективности диализа при острых ¡ отравлениях используются ¡ гипертонические растворы (0, 35 -0, 85 ¡ осмоль/л. ¡ Ультрафильтрация — это отделение дисперсной ¡ фазы от дисперсионной среды путем фильтрования ¡ через мембраны под давлением или в вакууме. ¡ Аппарат «искусственная почка» - сочетание ¡ диализа и ультрафильтрации. ¡ Гельфильтрация. В поры декстринового гель низко- молекулярные соединения входят , а ВМС (белки) ¡ нет. При элюировании сначала появится фракция ¡ ВМС, а затем НМС
¡ Вивидиализ ( гемодиализ): биологическая жидкость омывается не чистым ¡ растворителем, а изотоническими ¡ растворами электролитов. Для повышения ¡ эффективности диализа при острых ¡ отравлениях используются ¡ гипертонические растворы (0, 35 -0, 85 ¡ осмоль/л. ¡ Ультрафильтрация — это отделение дисперсной ¡ фазы от дисперсионной среды путем фильтрования ¡ через мембраны под давлением или в вакууме. ¡ Аппарат «искусственная почка» - сочетание ¡ диализа и ультрафильтрации. ¡ Гельфильтрация. В поры декстринового гель низко- молекулярные соединения входят , а ВМС (белки) ¡ нет. При элюировании сначала появится фракция ¡ ВМС, а затем НМС
 ¡ Молекулярно-кинетические свойства коллоидных систем ¡ 1. Броуновское движение для коллодных частиц замедленно и зависит: ¡ от температуры – скорость движения возрастает ¡ от вязкости дисперсионной среды, внутреннего трения. ¡ от коэффициента диффузии ¡ 2. Диффузия коллоидных систем замедленна, т. к. крупные частицы. ¡ 3. Росм коллоидных растворов значительно ниже Росм истинных растворов вследствие большого размера частиц и малых концентраций ¡ 4. Способность дисперсной системы сохранять по всему объёму распределение частиц называется седиментационной или кинетической устойчивостью. ¡ . Ультрацентрифугирование. Оседание коллоидов под действием центробежной силы. А. В. Думанский в 1913 г. , Сведберг (ультрацентрифуга)
¡ Молекулярно-кинетические свойства коллоидных систем ¡ 1. Броуновское движение для коллодных частиц замедленно и зависит: ¡ от температуры – скорость движения возрастает ¡ от вязкости дисперсионной среды, внутреннего трения. ¡ от коэффициента диффузии ¡ 2. Диффузия коллоидных систем замедленна, т. к. крупные частицы. ¡ 3. Росм коллоидных растворов значительно ниже Росм истинных растворов вследствие большого размера частиц и малых концентраций ¡ 4. Способность дисперсной системы сохранять по всему объёму распределение частиц называется седиментационной или кинетической устойчивостью. ¡ . Ультрацентрифугирование. Оседание коллоидов под действием центробежной силы. А. В. Думанский в 1913 г. , Сведберг (ультрацентрифуга)
 Оптические свойства ¡ Рассеяние света. ……. Дифракционное рассеивание света в результате огибания частиц световой волной- (конус. Тиндаля ). Формула Рэлея [1871 г. ]: где I — интенсивность рассеяния света; I 0 — интенсивность падающего света; К — константа, зависящая от показателей преломления дисперсионной среды и дисперсной фазы частиц; n — число частиц; V — объём частиц; — длина волны падающего света.
Оптические свойства ¡ Рассеяние света. ……. Дифракционное рассеивание света в результате огибания частиц световой волной- (конус. Тиндаля ). Формула Рэлея [1871 г. ]: где I — интенсивность рассеяния света; I 0 — интенсивность падающего света; К — константа, зависящая от показателей преломления дисперсионной среды и дисперсной фазы частиц; n — число частиц; V — объём частиц; — длина волны падающего света.
 n Окраска золей n связана с избирательным поглощением световых лучей. n Если золь только рассеивает, а не поглощает световые лучи — он бесцветен. n Опалесценция-изменение окраски бесцветного коллоидного раствора в проходящем (розовая) и отраженном (голубая) свете n Дихроизм— наложение опалесценции на собственную окраску золя. n Грубодисперсные имеют синюю окраску, высокодисперсные –красную.
n Окраска золей n связана с избирательным поглощением световых лучей. n Если золь только рассеивает, а не поглощает световые лучи — он бесцветен. n Опалесценция-изменение окраски бесцветного коллоидного раствора в проходящем (розовая) и отраженном (голубая) свете n Дихроизм— наложение опалесценции на собственную окраску золя. n Грубодисперсные имеют синюю окраску, высокодисперсные –красную.
 n СТРОЕНИЕ МИЦЕЛЛ n Мицелла - гетерогенная микросистема, n Ядро мицеллы - микрокристалл малорастворимого вещества, на поверхности которого адсорбированы, потенциалопределяющие ионы, сообщающие заряд ядру мицеллы.
n СТРОЕНИЕ МИЦЕЛЛ n Мицелла - гетерогенная микросистема, n Ядро мицеллы - микрокристалл малорастворимого вещества, на поверхности которого адсорбированы, потенциалопределяющие ионы, сообщающие заряд ядру мицеллы.
 • Межфазным потенциалом – (электродинамическим)(фи) - потенциал на границе раздела между твердой и жидкой фазами в мицелле (на схемах мицеллы - граница АА). • Электрокинетическим потенциалом (дзета) называется потенциал на границе скольжения между адсорбционной и диффузионной частями мицеллы
• Межфазным потенциалом – (электродинамическим)(фи) - потенциал на границе раздела между твердой и жидкой фазами в мицелле (на схемах мицеллы - граница АА). • Электрокинетическим потенциалом (дзета) называется потенциал на границе скольжения между адсорбционной и диффузионной частями мицеллы
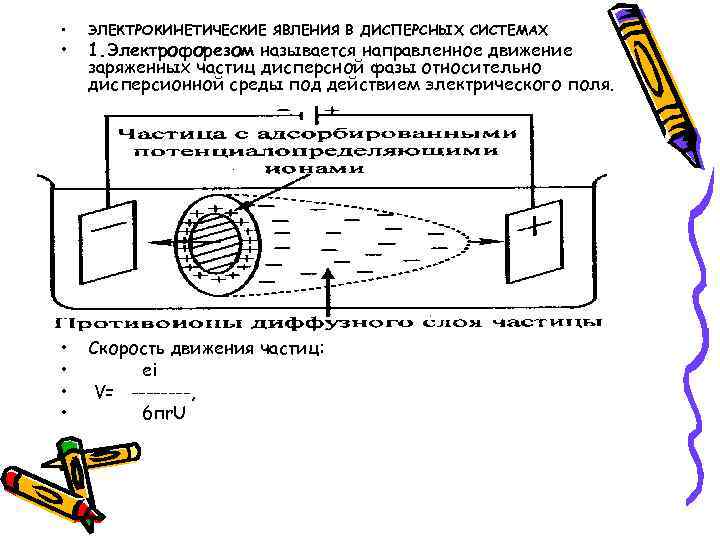
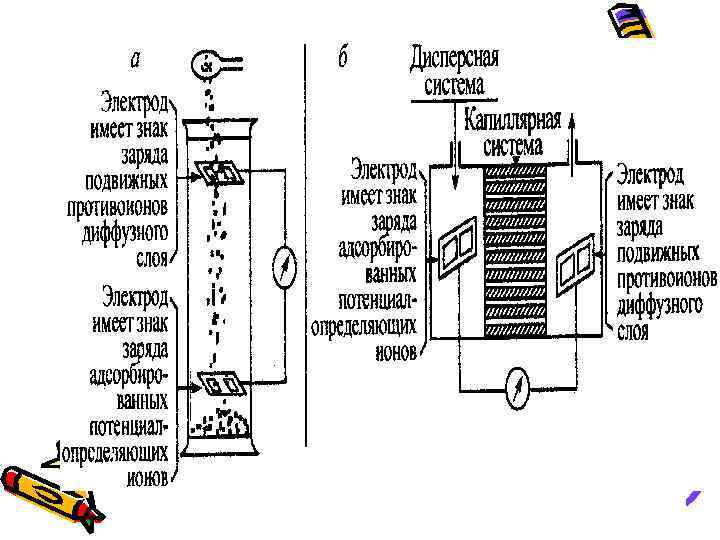
 • ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ В ДИСПЕРСНЫХ СИСТЕМАХ • 1. Электрофорезом называется направленное движение заряженных частиц дисперсной фазы относительно дисперсионной среды под действием электрического поля. • Скорость движения частиц: • ei • V= ----, • 6 пr. U
• ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ В ДИСПЕРСНЫХ СИСТЕМАХ • 1. Электрофорезом называется направленное движение заряженных частиц дисперсной фазы относительно дисперсионной среды под действием электрического поля. • Скорость движения частиц: • ei • V= ----, • 6 пr. U
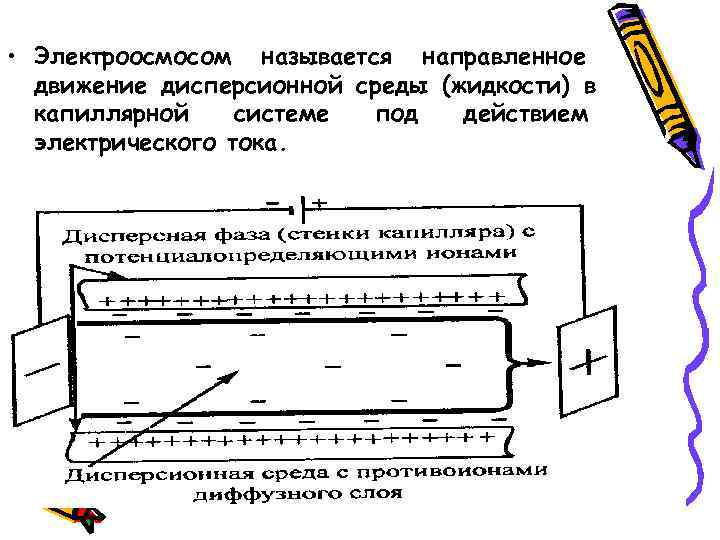
 • Электроосмосом называется направленное движение дисперсионной среды (жидкости) в капиллярной системе под действием электрического тока.
• Электроосмосом называется направленное движение дисперсионной среды (жидкости) в капиллярной системе под действием электрического тока.
 • . 3. Потенциалом седиментации (Дорна) называется разность потенциалов, возникающая при оседании частиц дисперсной фазы в жидкой дисперсионной среде. • 4. Потенциалом течения (Квинке) называется разность потенциалов, возникающая при протекании через систему жидкой дисперсионной среды.
• . 3. Потенциалом седиментации (Дорна) называется разность потенциалов, возникающая при оседании частиц дисперсной фазы в жидкой дисперсионной среде. • 4. Потенциалом течения (Квинке) называется разность потенциалов, возникающая при протекании через систему жидкой дисперсионной среды.
 •
•
 • Потенциалы течения и оседания - механизмы возникновения биотоков при движении крови по сосудам. Зубец Q на электрокардиограмме обусловлен течением крови в коронарной системе.
• Потенциалы течения и оседания - механизмы возникновения биотоков при движении крови по сосудам. Зубец Q на электрокардиограмме обусловлен течением крови в коронарной системе.
 • Устойчивость коллоидных растворов – способность дисперсной фазы сохранять состояние равномерного распределения частиц дисперсной фазы во всем объеме дисперсионной среды – седиментационное равновесие.
• Устойчивость коллоидных растворов – способность дисперсной фазы сохранять состояние равномерного распределения частиц дисперсной фазы во всем объеме дисперсионной среды – седиментационное равновесие.
 • Агрегативная устойчивость –способность дисперсной фазы противостоять их агрегации. Причина – наличие заряда и сольватной оболочки частиц. • Кинетическая – способность частиц оставаться во взвешанном состоянии. Причина – броуновское движение частиц. • Теория Дерягина-Ландау –теория расклинивающего действия воды – гидратные оболочки противоионов диффузного слоя обладают упругими свойствами. Гидратные оболочки препятствуют сближению частиц.
• Агрегативная устойчивость –способность дисперсной фазы противостоять их агрегации. Причина – наличие заряда и сольватной оболочки частиц. • Кинетическая – способность частиц оставаться во взвешанном состоянии. Причина – броуновское движение частиц. • Теория Дерягина-Ландау –теория расклинивающего действия воды – гидратные оболочки противоионов диффузного слоя обладают упругими свойствами. Гидратные оболочки препятствуют сближению частиц.
 • Коагуляция – • процесс слипания коллоидных частиц с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной устойчивости • Коагуляцию можно вызвать воздействиями: • -добавлением электролита, • -концентрированием коллоидного раствора, • -изменением температуры, • -действием ультразвука, • -электромагнитного поля и др.
• Коагуляция – • процесс слипания коллоидных частиц с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной устойчивости • Коагуляцию можно вызвать воздействиями: • -добавлением электролита, • -концентрированием коллоидного раствора, • -изменением температуры, • -действием ультразвука, • -электромагнитного поля и др.
 n Коагуляция под действием электролитов. n Для каждого электролита необходима своя минимальная концентрация, называемая порогом коагуляции (спк). n Порогом коагуляции называется минимальное количество электролита, которое надо добавить к коллоидному раствору, чтобы вызвать явную коагуляцию n где с. ПК — исходная концентрация раствора электролита; VЭЛ — объем раствора электролита, добавленного к коллоидному раствору; VКР - объем коллоидного раствора.
n Коагуляция под действием электролитов. n Для каждого электролита необходима своя минимальная концентрация, называемая порогом коагуляции (спк). n Порогом коагуляции называется минимальное количество электролита, которое надо добавить к коллоидному раствору, чтобы вызвать явную коагуляцию n где с. ПК — исходная концентрация раствора электролита; VЭЛ — объем раствора электролита, добавленного к коллоидному раствору; VКР - объем коллоидного раствора.
 n Коагулирующее действие n электролитов подчиняется правилу Шульце — Гарди: n 1. коагуляцию вызывают любые ионы, которые имеют знак заряда, противоположный заряду гранул. n 2. Коагулирующее действие ионов (у) тем сильнее, чем выше заряд иона- коагулянта - прямо пропорционально заряду в шестой степени: n у = f(z 6).
n Коагулирующее действие n электролитов подчиняется правилу Шульце — Гарди: n 1. коагуляцию вызывают любые ионы, которые имеют знак заряда, противоположный заряду гранул. n 2. Коагулирующее действие ионов (у) тем сильнее, чем выше заряд иона- коагулянта - прямо пропорционально заряду в шестой степени: n у = f(z 6).
 • ……. Примеры: ---коагуляция золя Agl с по- тенциалопределяющими ионами - анионы I-); y(Na+) : у(Са 2+ ) : y. Аl 3+ ) = 1 : 64 : 729.
• ……. Примеры: ---коагуляция золя Agl с по- тенциалопределяющими ионами - анионы I-); y(Na+) : у(Са 2+ ) : y. Аl 3+ ) = 1 : 64 : 729.
 n Механизм коагуляции. n Роль электролитов при коагуляции заключается в уменьшении расклинивающего давления между сближающимися коллоидными частицами. Это может происходить двумя путями: n -за счет уменьшения заряда поверхности ядра, т. е. за счет снижения межфазного потенциала n - за счет уменьшения толщины (сжатия) ионных атмосфер мицелл
n Механизм коагуляции. n Роль электролитов при коагуляции заключается в уменьшении расклинивающего давления между сближающимися коллоидными частицами. Это может происходить двумя путями: n -за счет уменьшения заряда поверхности ядра, т. е. за счет снижения межфазного потенциала n - за счет уменьшения толщины (сжатия) ионных атмосфер мицелл
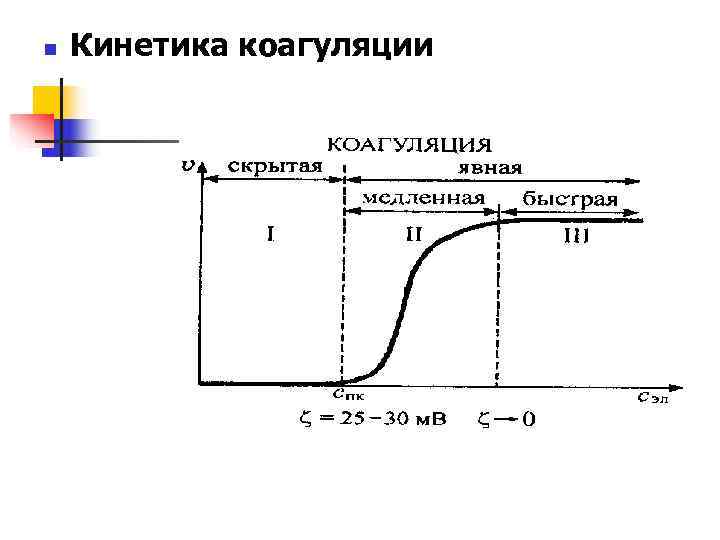
 n Кинетика коагуляции
n Кинетика коагуляции
 n Взаимная коагуляция — слипание разноименно заряженных гранул коллоидных растворов. . n Привыкание золя - при медленном добавлении электролита коагуляция может не наступить, а если этот же электролит добавлять быстро, то коагуляция наступит.
n Взаимная коагуляция — слипание разноименно заряженных гранул коллоидных растворов. . n Привыкание золя - при медленном добавлении электролита коагуляция может не наступить, а если этот же электролит добавлять быстро, то коагуляция наступит.
 n Явление коагуляции имеет большую роль в живом организме, т. к. коллоидные растворы клеток в биологических жидкостях находятся при соприкосновении с электролитами. Поэтому при введении элетролитов в организм необходимо учитывать не только его концентрацию , но и заряд ионов. При введении внутривенно смеси электролитов для предотвращения коагуляции белков необходимо: n медленно вводить растворы электролитов n учитывать не только заряд ионов, но и их синергизм.
n Явление коагуляции имеет большую роль в живом организме, т. к. коллоидные растворы клеток в биологических жидкостях находятся при соприкосновении с электролитами. Поэтому при введении элетролитов в организм необходимо учитывать не только его концентрацию , но и заряд ионов. При введении внутривенно смеси электролитов для предотвращения коагуляции белков необходимо: n медленно вводить растворы электролитов n учитывать не только заряд ионов, но и их синергизм.
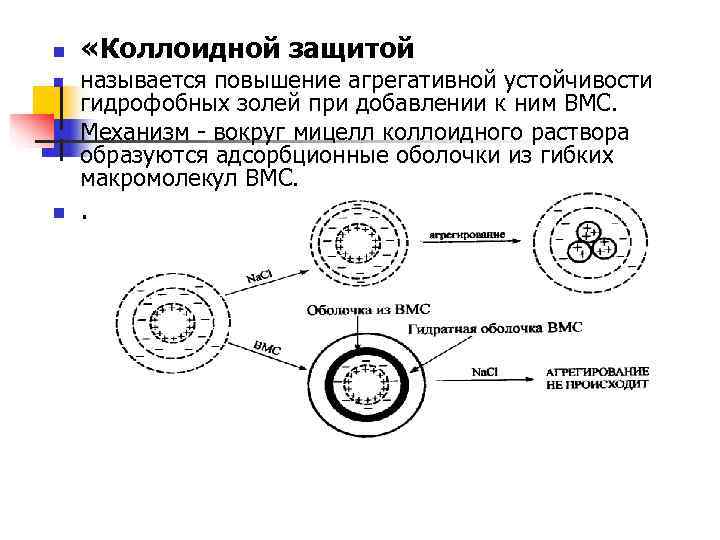
 n «Коллоидной защитой n называется повышение агрегативной устойчивости гидрофобных золей при добавлении к ним ВМС. n Механизм - вокруг мицелл коллоидного раствора образуются адсорбционные оболочки из гибких макромолекул ВМС. n .
n «Коллоидной защитой n называется повышение агрегативной устойчивости гидрофобных золей при добавлении к ним ВМС. n Механизм - вокруг мицелл коллоидного раствора образуются адсорбционные оболочки из гибких макромолекул ВМС. n .
 n Основными условиями защитного действия являются: n — хорошая растворимость ВМС в дисперсионной среде коллоидного раствора; n —хорошая адсорбируемость молекул ВМС на коллоидных частицах; n минимальная концентрация ВМС, образующего мономолекулярный слой на поверхности мицеллы n минимальное защитное число ВМС n одинаковый заряд ВМС и золя
n Основными условиями защитного действия являются: n — хорошая растворимость ВМС в дисперсионной среде коллоидного раствора; n —хорошая адсорбируемость молекул ВМС на коллоидных частицах; n минимальная концентрация ВМС, образующего мономолекулярный слой на поверхности мицеллы n минимальное защитное число ВМС n одинаковый заряд ВМС и золя
![>n Золотое число — это количество мг сухого полимера [например, желатины], защищающего 10 >n Золотое число — это количество мг сухого полимера [например, желатины], защищающего 10](https://present5.com/presentation/3/44900853_24936417.pdf-img/44900853_24936417.pdf-35.jpg) n Золотое число — это количество мг сухого полимера [например, желатины], защищающего 10 мл красного гидрозоля золота от коагуляции 1 мл 10% раствора поваренной соли. n Эту величину [0, 01 мг] Зигмонди назвал «золотым числом» желатины.
n Золотое число — это количество мг сухого полимера [например, желатины], защищающего 10 мл красного гидрозоля золота от коагуляции 1 мл 10% раствора поваренной соли. n Эту величину [0, 01 мг] Зигмонди назвал «золотым числом» желатины.
 n Значение биологической защиты ВМС n Кровь – дисперсная система: дисперсионная среда – плазма, дисперсная фаза – форменные элементы крови, плохо растворимые вещества: ураты, липиды, фосфаты. карбонаты и др. n Белки крови защищают и препятствуют осаждению плохо растворимых соединений и образованию камней в почках и печени, развитию атеросклероза ( отложение холестерина на поверхности сосудов).
n Значение биологической защиты ВМС n Кровь – дисперсная система: дисперсионная среда – плазма, дисперсная фаза – форменные элементы крови, плохо растворимые вещества: ураты, липиды, фосфаты. карбонаты и др. n Белки крови защищают и препятствуют осаждению плохо растворимых соединений и образованию камней в почках и печени, развитию атеросклероза ( отложение холестерина на поверхности сосудов).
 n В условиях in vivo кровь является агрегативно и седиментационно устойчивой дисперсной системой. n Агрегативная устойчивость крови обеспечивается мощными гидратными оболочками на поверхности клеточных мембран, препятствующих слипанию. n Изменение конформации белков при патологии приводит к уменьшению стуктурированной воды на поверхности клеток, а следовательно нарушается агрегативная устойчивость.
n В условиях in vivo кровь является агрегативно и седиментационно устойчивой дисперсной системой. n Агрегативная устойчивость крови обеспечивается мощными гидратными оболочками на поверхности клеточных мембран, препятствующих слипанию. n Изменение конформации белков при патологии приводит к уменьшению стуктурированной воды на поверхности клеток, а следовательно нарушается агрегативная устойчивость.
 n Вторым фактором агрегативной устойчивостью является заряд поверхности клетки. Изменение конформации белков при патологии приводит к уменьшению стуктурированной воды на поверхности клеток, а следовательно нарушается агрегативная устойчивость.
n Вторым фактором агрегативной устойчивостью является заряд поверхности клетки. Изменение конформации белков при патологии приводит к уменьшению стуктурированной воды на поверхности клеток, а следовательно нарушается агрегативная устойчивость.
 n Седиментационная устойчивость крови связана с непрерывным движением крови. При отсутствии движения кровь теряет устойчивость и происходит оседание форменных элементов.
n Седиментационная устойчивость крови связана с непрерывным движением крови. При отсутствии движения кровь теряет устойчивость и происходит оседание форменных элементов.
 n Лекарственные препараты – дисперсные системы – препараты серебра: протаргол (7, 8 -8, 3%) и колларгол (70%) устойчивость приобретают благодаря защитному действию ВМС. n Определение золотого защитного числа спинно-мозговой жидкости используется при диагностике менингита ( защитное число при этом снижается) n Проба Ланге –измерение защитной способности белков. К нескольким разведениям спинно-мозговой жидкости добавляют одинаковый объем коллоидного раствора золота. При отрицательной реакции красно-вишневая окраска остается без изменений.
n Лекарственные препараты – дисперсные системы – препараты серебра: протаргол (7, 8 -8, 3%) и колларгол (70%) устойчивость приобретают благодаря защитному действию ВМС. n Определение золотого защитного числа спинно-мозговой жидкости используется при диагностике менингита ( защитное число при этом снижается) n Проба Ланге –измерение защитной способности белков. К нескольким разведениям спинно-мозговой жидкости добавляют одинаковый объем коллоидного раствора золота. При отрицательной реакции красно-вишневая окраска остается без изменений.
 n Следовательно белки плазмы обеспечивают стабильность золя золота. n При патологических состояниях некоторые разведения теряют защитную способность и наступает коагуляция. Интенсивность коагуляции оценивается по изменению окраски: от красно- фиолетового через фиолетовую и голубую до ее исчезновения. Патологический процесс определяется по кривым зависимости интенсивности коагуляции от разведения.
n Следовательно белки плазмы обеспечивают стабильность золя золота. n При патологических состояниях некоторые разведения теряют защитную способность и наступает коагуляция. Интенсивность коагуляции оценивается по изменению окраски: от красно- фиолетового через фиолетовую и голубую до ее исчезновения. Патологический процесс определяется по кривым зависимости интенсивности коагуляции от разведения.
 n Аэрозоли: дисперсные системы, в которых дисперсионная среда – газ, дисперсная фаза – твердые или жидкие частицы с размером 10 -7 -10 -4 м. n Два вида устойчивости: седиментационная ( основная) за счет броуновского движения и агрегативная. n Использование аэрозолей в медицине для ингаляций лекарственных препаратов: n лекарственные аэрозоли с размером частиц 5. 10 -6 м осаждаются в носоглотке; n с размером частиц 2. 10 -6 м –попадают в легкие и бронхи; n 10 -6 м – проникают в альвеолы легких.
n Аэрозоли: дисперсные системы, в которых дисперсионная среда – газ, дисперсная фаза – твердые или жидкие частицы с размером 10 -7 -10 -4 м. n Два вида устойчивости: седиментационная ( основная) за счет броуновского движения и агрегативная. n Использование аэрозолей в медицине для ингаляций лекарственных препаратов: n лекарственные аэрозоли с размером частиц 5. 10 -6 м осаждаются в носоглотке; n с размером частиц 2. 10 -6 м –попадают в легкие и бронхи; n 10 -6 м – проникают в альвеолы легких.
 n Болезни, вызываемые действием различных пылей на легкие: n силикоз (кварцевая пыль); n антракоз (угольная пыль); n асбестоз (асбестовая пыль) n аэрозоли металлов и их оксидов проникают сквозь клеточные мембраны и нарушают жизнедеятельность клеток; n аэрозоли, содержащие цветочную пыльцу, вызывают аллергию; n аэрозоли, содержащие вирусы, различные микроорганизмы вызывают соответствующие заболевания
n Болезни, вызываемые действием различных пылей на легкие: n силикоз (кварцевая пыль); n антракоз (угольная пыль); n асбестоз (асбестовая пыль) n аэрозоли металлов и их оксидов проникают сквозь клеточные мембраны и нарушают жизнедеятельность клеток; n аэрозоли, содержащие цветочную пыльцу, вызывают аллергию; n аэрозоли, содержащие вирусы, различные микроорганизмы вызывают соответствующие заболевания

