POLYMERASES(19.09.14).ppt
- Количество слайдов: 81
ФИЗИКО-ХИМИЧЕСКИЕ ЗАКОНОМЕРНОСТИ БИОСИНТЕЗА НУКЛЕИНОВЫХ КИСЛОТ. С. Н. Кочетков Институт молекулярной биологии им. В. А. Энгельгардта РАН и Химический факультет МГУ им. М. В. Ломоносова
РЕПЛИКАЦИЯ РЕПАРАЦИЯ ТРАНСКРИПЦИЯ

ФЕРМЕНТЫ

§ФЕРМЕНТЫ §МЕХАНИЗМ КАТАЛИЗА §СПЕЦИФИЧНОСТЬ В ОТНОШЕНИИ NTP §СПЕЦИФИЧНОСТЬ В ОТНОШЕНИИ МАТРИЦЫ/ПРАЙМЕРА §ПРОЦЕССИВНОСТЬ § 3’-5’-ЭКЗОНУКЛЕАЗНАЯ АКТИВНОСТЬ
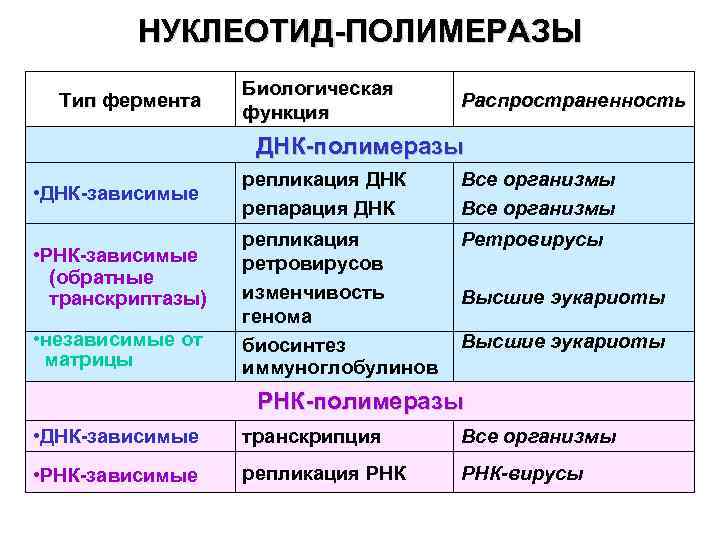
НУКЛЕОТИД-ПОЛИМЕРАЗЫ Тип фермента Биологическая функция Распространенность ДНК-полимеразы • ДНК-зависимые • РНК-зависимые (обратные транскриптазы) • независимые от матрицы репликация ДНК репарация ДНК Все организмы репликация ретровирусов изменчивость генома биосинтез иммуноглобулинов Ретровирусы Высшие эукариоты РНК-полимеразы • ДНК-зависимые транскрипция Все организмы • РНК-зависимые репликация РНК-вирусы

НУКЛЕОТИД-ПОЛИМЕРАЗЫ ДНК-зависимые ДНК-полимеразы d. NTP РНК- зависимые ДНК-полимеразы (обратные транскриптазы) d. NTP DNA RNA DNA/RNA РНК- зависимые ДНК-полимеразы r. NTP xn РНК- зависимые ДНК-полимеразы (РНК-репликазы) r. NTP xn
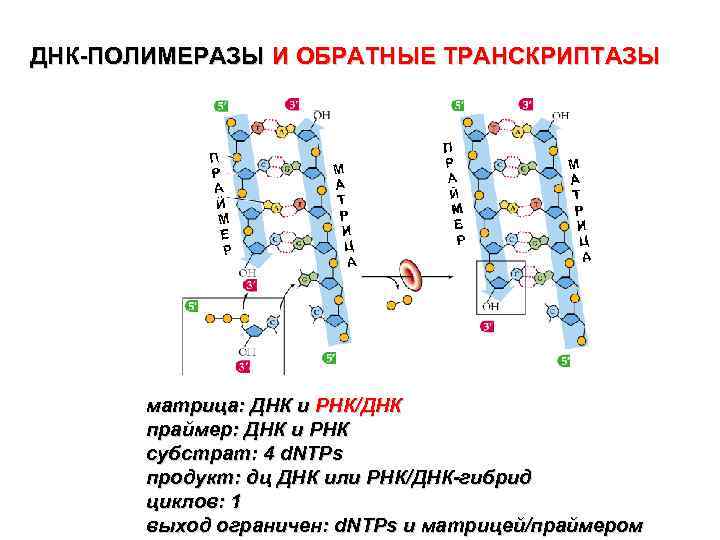
ДНК-ПОЛИМЕРАЗЫ И ОБРАТНЫЕ ТРАНСКРИПТАЗЫ матрица: ДНК и РНК/ДНК праймер: ДНК и РНК субстрат: 4 d. NTPs продукт: дц ДНК или РНК/ДНК-гибрид циклов: 1 выход ограничен: d. NTPs и матрицей/праймером
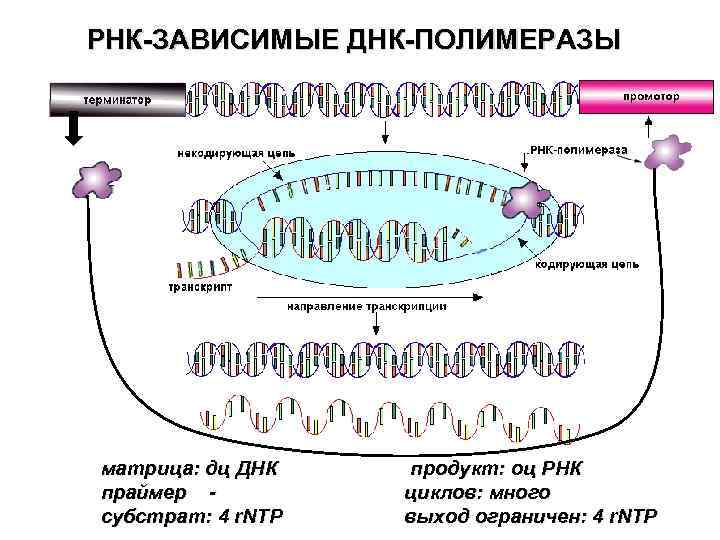
РНК-ЗАВИСИМЫЕ ДНК-ПОЛИМЕРАЗЫ матрица: дц ДНК праймер субстрат: 4 r. NTP продукт: оц РНК циклов: много выход ограничен: 4 r. NTP
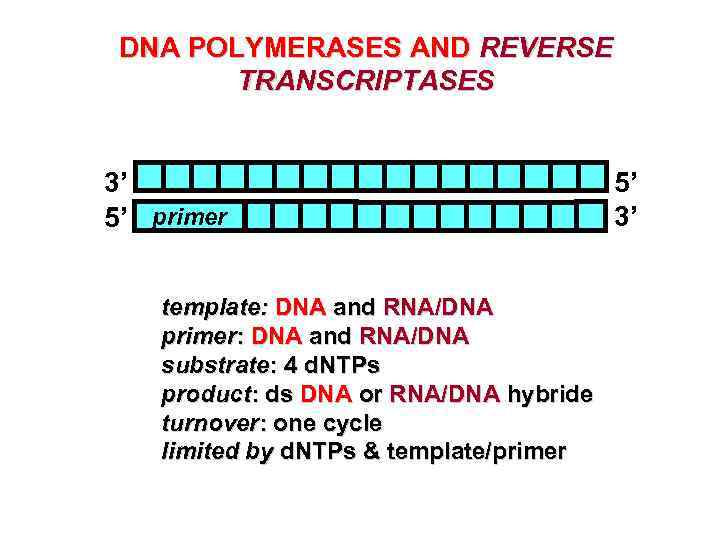
DNA POLYMERASES AND REVERSE TRANSCRIPTASES 3’ 5’ primer template: DNA and RNA/DNA primer: DNA and RNA/DNA substrate: 4 d. NTPs product: ds DNA or RNA/DNA hybride turnover: one cycle limited by d. NTPs & template/primer 5’ 3’
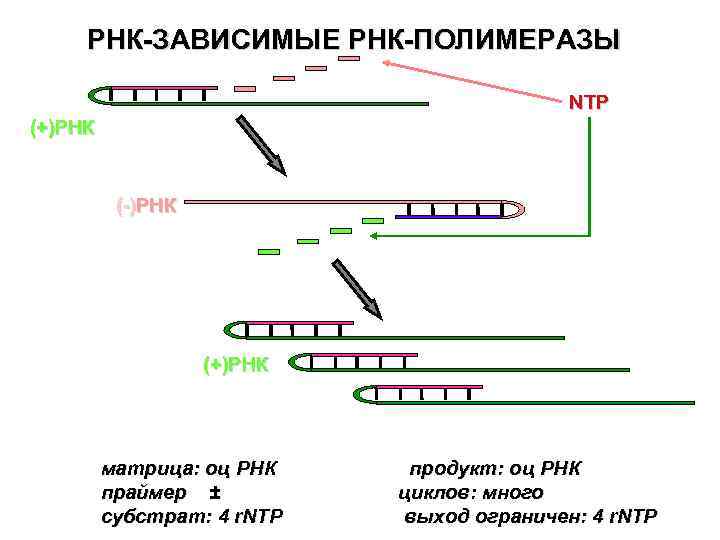
РНК-ЗАВИСИМЫЕ РНК-ПОЛИМЕРАЗЫ NTP (+)РНК (-)РНК (+)РНК матрица: оц РНК праймер ± субстрат: 4 r. NTP продукт: оц РНК циклов: много выход ограничен: 4 r. NTP
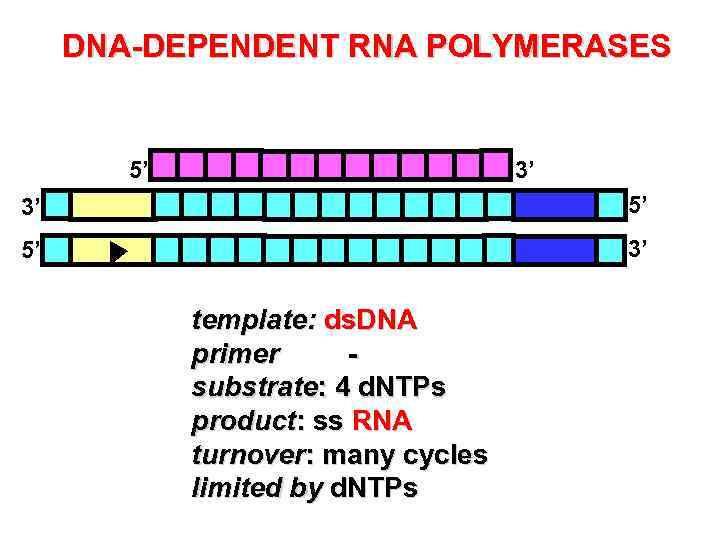
DNA-DEPENDENT RNA POLYMERASES 5’ 3’ 3’ 5’ 5’ 3’ template: ds. DNA primer substrate: 4 d. NTPs product: ss RNA turnover: many cycles limited by d. NTPs
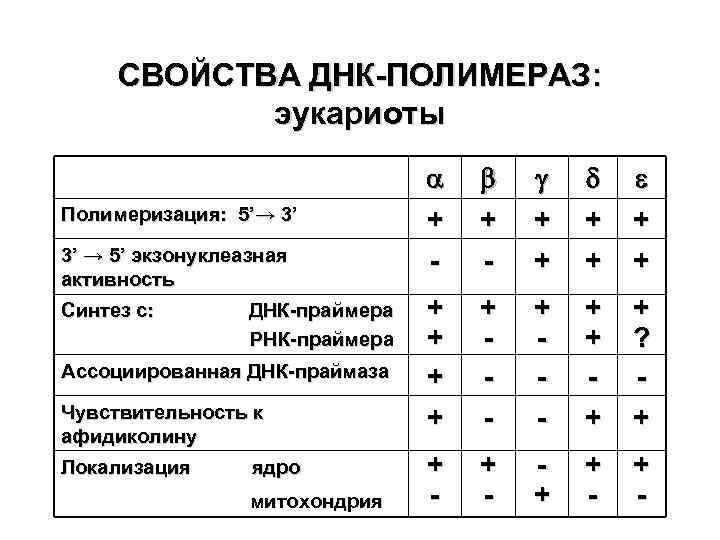
СВОЙСТВА ДНК-ПОЛИМЕРАЗ: эукариоты Полимеризация: 5’→ 3’ 3’ → 5’ экзонуклеазная активность Синтез с: ДНК-праймера РНК-праймера Ассоциированная ДНК-праймаза Чувствительность к афидиколину Локализация ядро митохондрия a + - g + + d + + e + + + + - + + ? + + - + -
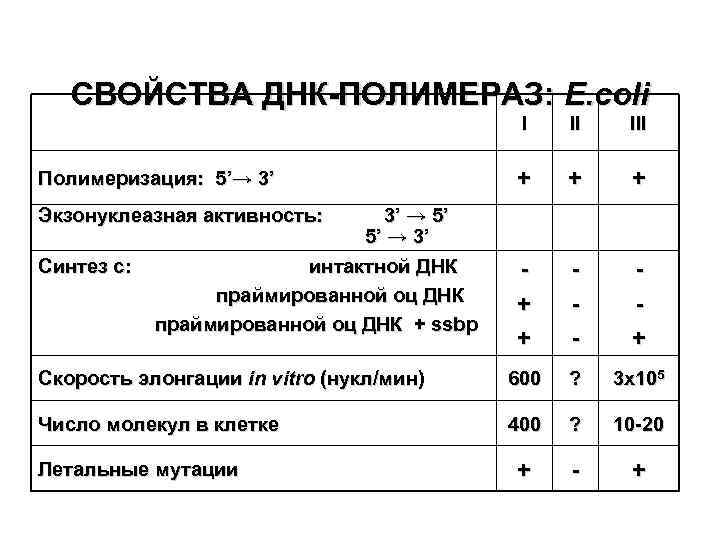
СВОЙСТВА ДНК-ПОЛИМЕРАЗ: E. coli I II III + + + - + Скорость элонгации in vitro (нукл/мин) 600 ? 3 x 105 Число молекул в клетке 400 ? 10 -20 + - + Полимеризация: 5’→ 3’ Экзонуклеазная активность: Синтез с: 3’ → 5 ’ 5’ → 3 ’ интактной ДНК праймированной оц ДНК + ssbp Летальные мутации
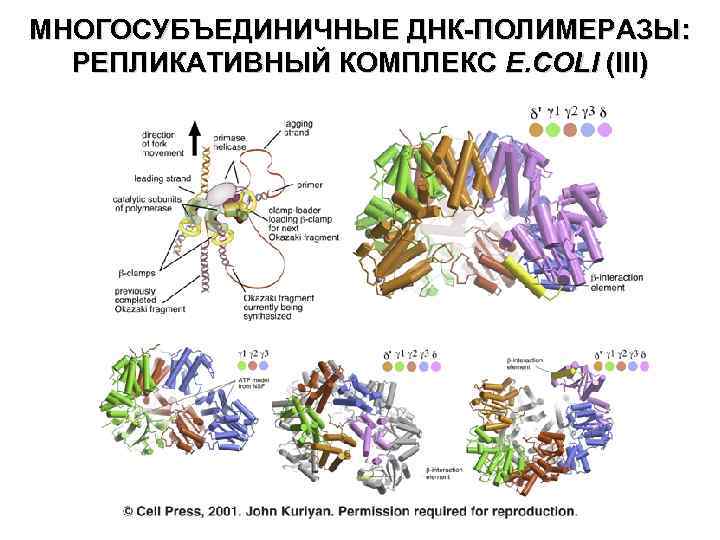
МНОГОСУБЪЕДИНИЧНЫЕ ДНК-ПОЛИМЕРАЗЫ: РЕПЛИКАТИВНЫЙ КОМПЛЕКС E. COLI (III)
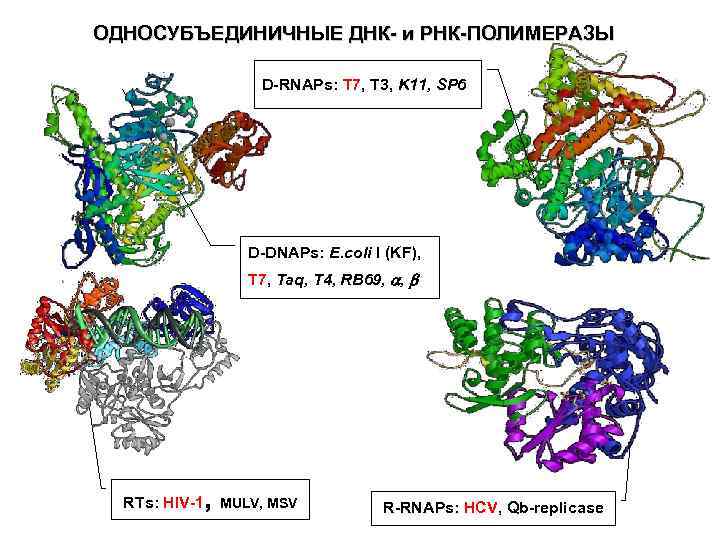
ОДНОСУБЪЕДИНИЧНЫЕ ДНК- и РНК-ПОЛИМЕРАЗЫ D-RNAPs: T 7, T 3, K 11, SP 6 D-DNAPs: E. coli I (KF), T 7, Taq, T 4, RB 69, a, b , RTs: HIV-1 MULV, MSV R-RNAPs: HCV, Qb-replicase

ТРЕХМЕРНЫЕ СТРУКТУРЫ ОДНОСУБЪЕДИНИЧНЫХ НУКЛЕОТИДПОЛИМЕРАЗ 1 324 411 565 784 fingers thumb palm 883
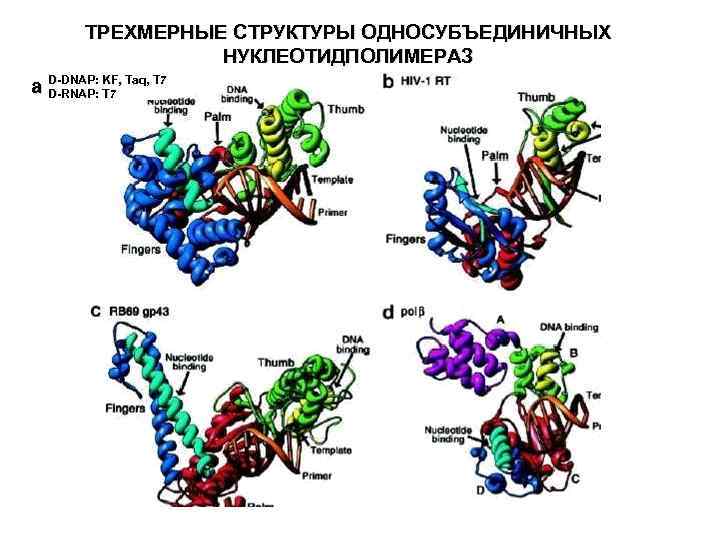
ТРЕХМЕРНЫЕ СТРУКТУРЫ ОДНОСУБЪЕДИНИЧНЫХ НУКЛЕОТИДПОЛИМЕРАЗ a D-DNAP: KF, Taq, T 7 D-RNAP: T 7
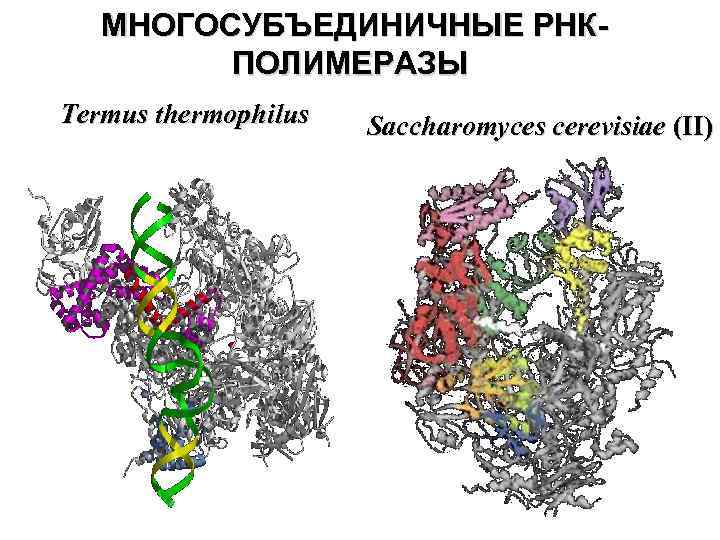
МНОГОСУБЪЕДИНИЧНЫЕ РНКПОЛИМЕРАЗЫ Termus thermophilus Saccharomyces cerevisiae (II)
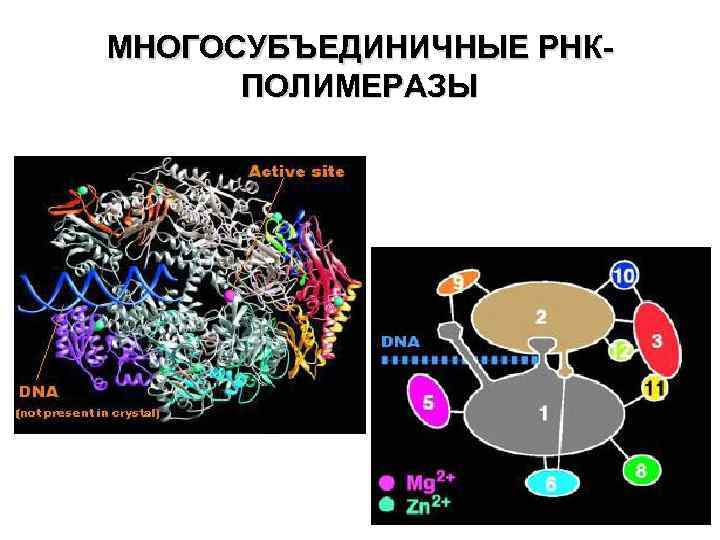
МНОГОСУБЪЕДИНИЧНЫЕ РНКПОЛИМЕРАЗЫ

МЕХАНИЗМ КАТАЛИЗА
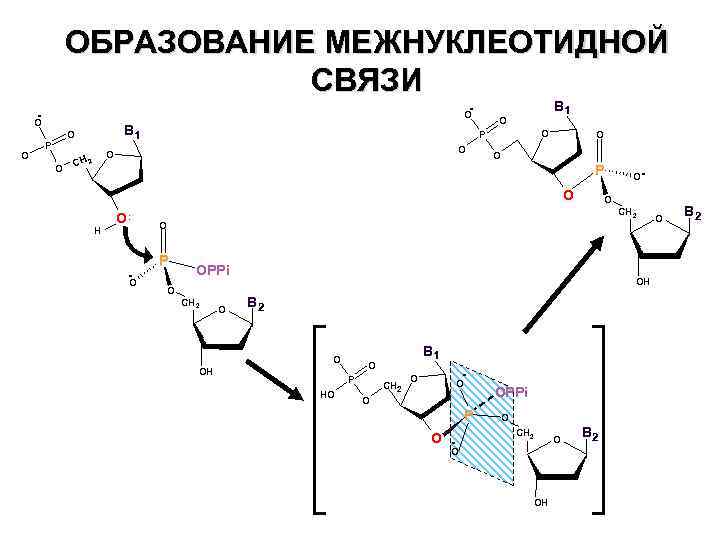
ОБРАЗОВАНИЕ МЕЖНУКЛЕОТИДНОЙ СВЯЗИ O O O B 1 - - B 1 O P O O CH 2 O O O P O H O: - O O- O CH 2 O P OPPi O CH 2 O OH B 2 O OH O P HO B 1 CH 2 - O O O P O - OPPi O CH 2 O OH O B 2
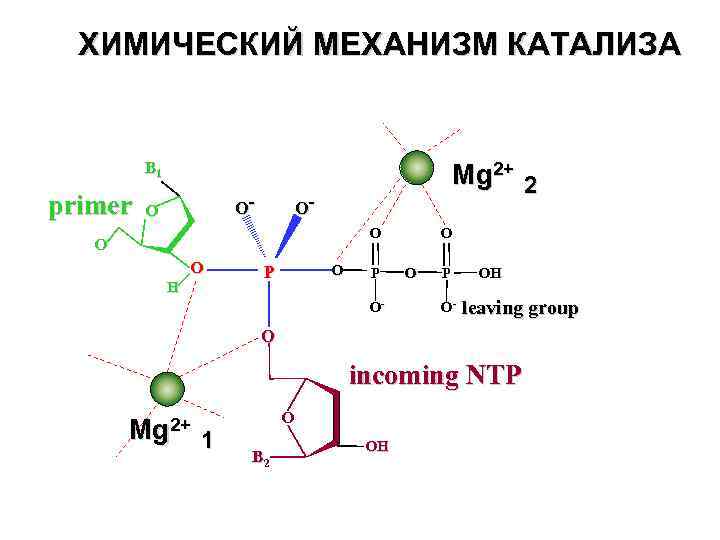
ХИМИЧЕСКИЙ МЕХАНИЗМ КАТАЛИЗА B 1 primer O- O Mg 2+ 2 OO O O H P O- O O P O- OH leaving group O incoming NTP Mg 2+ 1 O B 2 OH
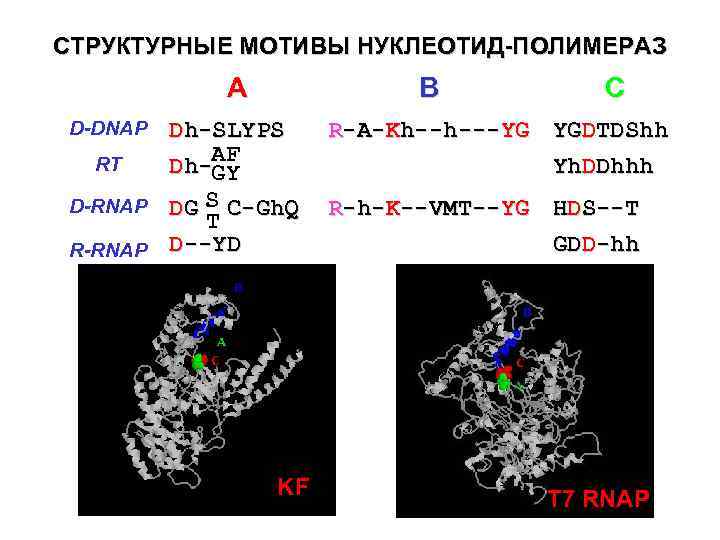
СТРУКТУРНЫЕ МОТИВЫ НУКЛЕОТИД-ПОЛИМЕРАЗ A B Dh-SLYPS RT Dh-AF GY D-RNAP DG S C-Gh. Q T R-RNAP D--YD D-DNAP KF C R-A-Kh--h---YG YGDTDShh Yh. DDhhh R-h-K--VMT--YG HDS--T GDD-hh T 7 RNAP
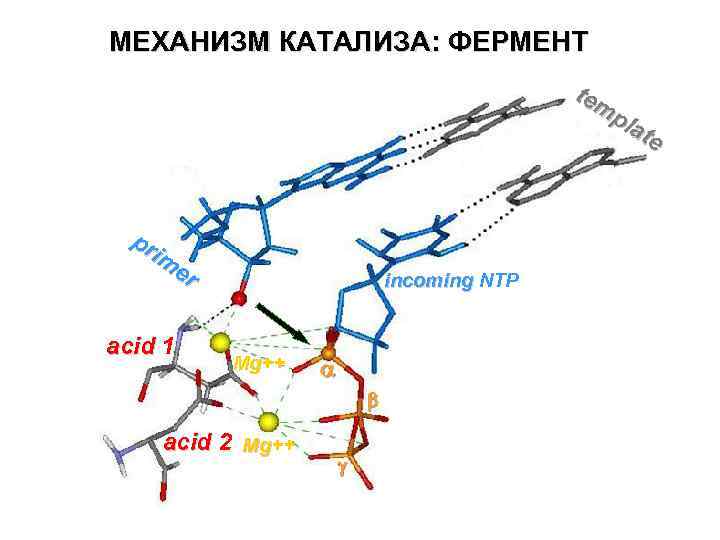
МЕХАНИЗМ КАТАЛИЗА: ФЕРМЕНТ tem pla te pr im er acid 1 incoming NTP Mg++ Mg a acid 2 Mg++ Mg g
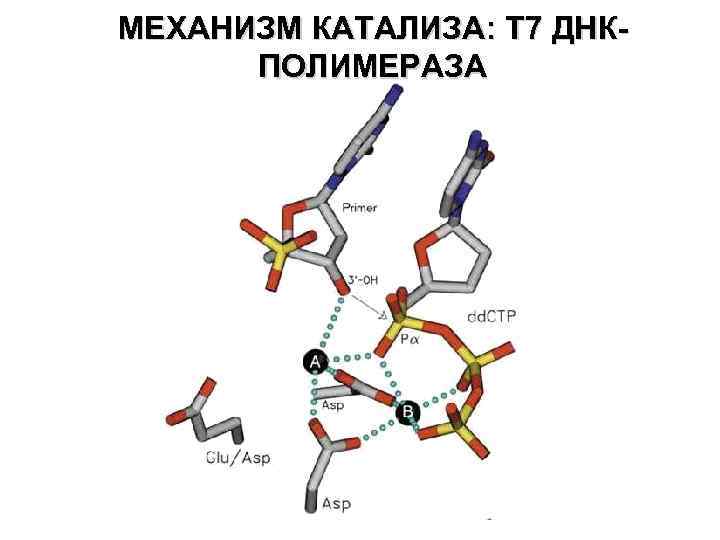
МЕХАНИЗМ КАТАЛИЗА: T 7 ДНКПОЛИМЕРАЗА
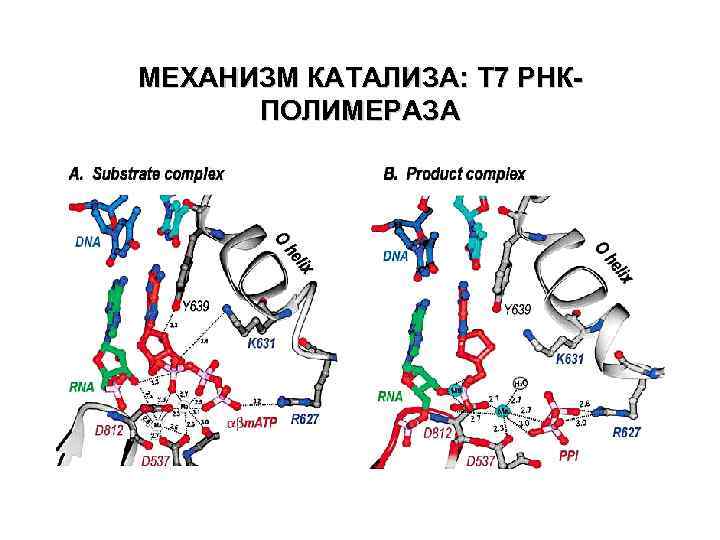
МЕХАНИЗМ КАТАЛИЗА: T 7 РНКПОЛИМЕРАЗА
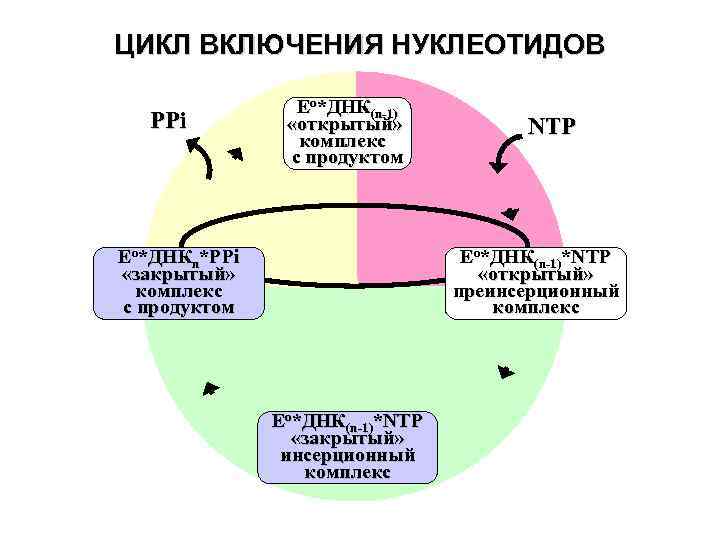
ЦИКЛ ВКЛЮЧЕНИЯ НУКЛЕОТИДОВ РРi Eо*ДНК(n-1) «открытый» комплекс с продуктом NTP Eо*ДНК(n-1)*NTP «открытый» преинсерционный комплекс Eо*ДНКn*РРi «закрытый» комплекс с продуктом Eо*ДНК(n-1)*NTP «закрытый» инсерционный комплекс
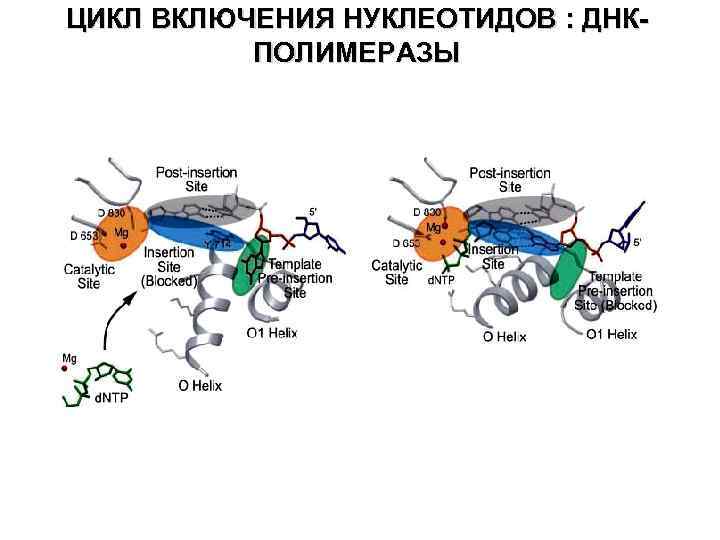
ЦИКЛ ВКЛЮЧЕНИЯ НУКЛЕОТИДОВ : ДНКПОЛИМЕРАЗЫ
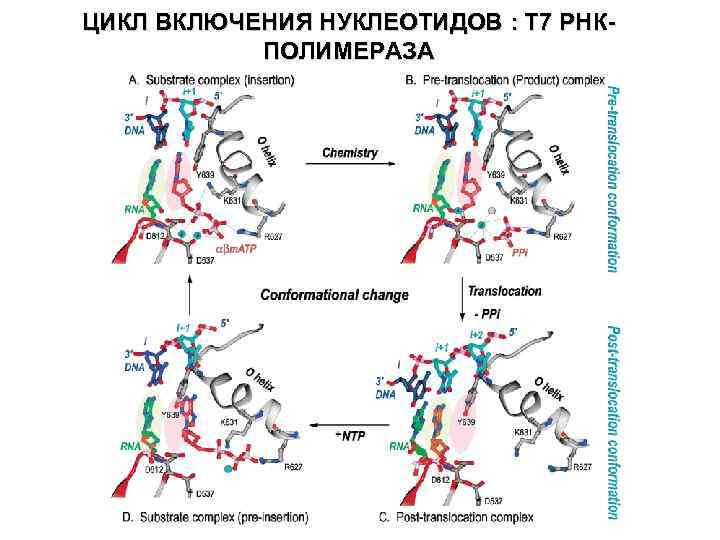
ЦИКЛ ВКЛЮЧЕНИЯ НУКЛЕОТИДОВ : T 7 PНКПОЛИМЕРАЗA
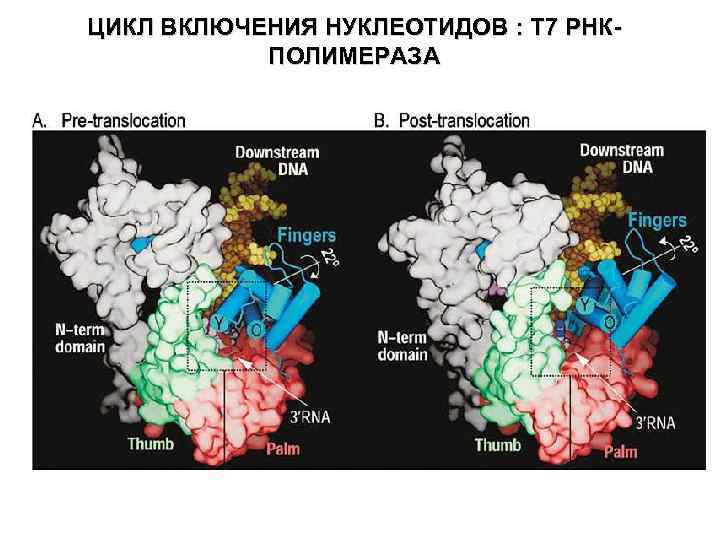
ЦИКЛ ВКЛЮЧЕНИЯ НУКЛЕОТИДОВ : T 7 PНКПОЛИМЕРАЗA
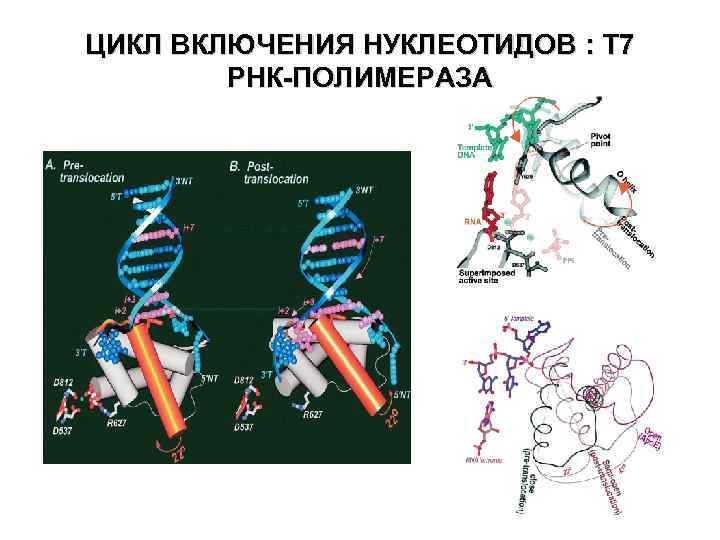
ЦИКЛ ВКЛЮЧЕНИЯ НУКЛЕОТИДОВ : T 7 PНК-ПОЛИМЕРАЗA

ПРОЦЕССИВНОСТЬ
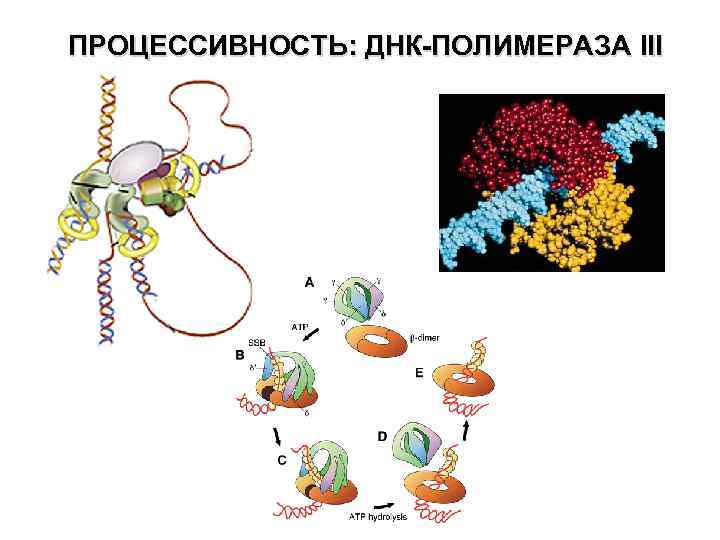
ПРОЦЕССИВНОСТЬ: ДНК-ПОЛИМЕРАЗА III
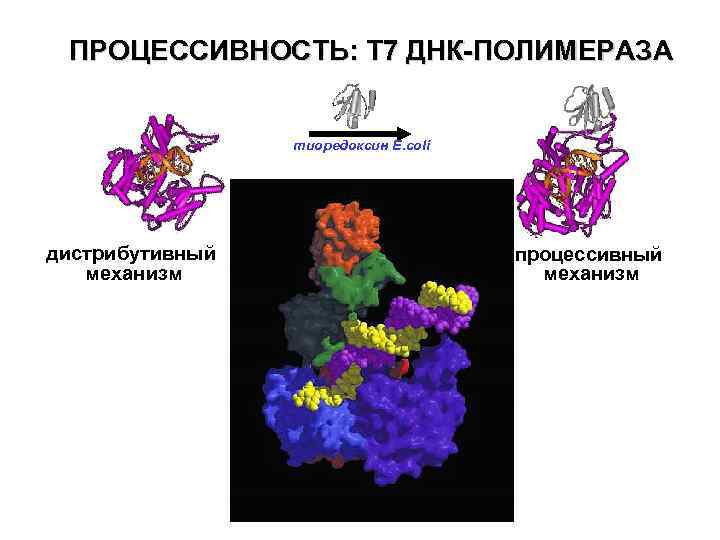
ПРОЦЕССИВНОСТЬ: Т 7 ДНК-ПОЛИМЕРАЗА тиоредоксин E. coli дистрибутивный механизм процессивный механизм
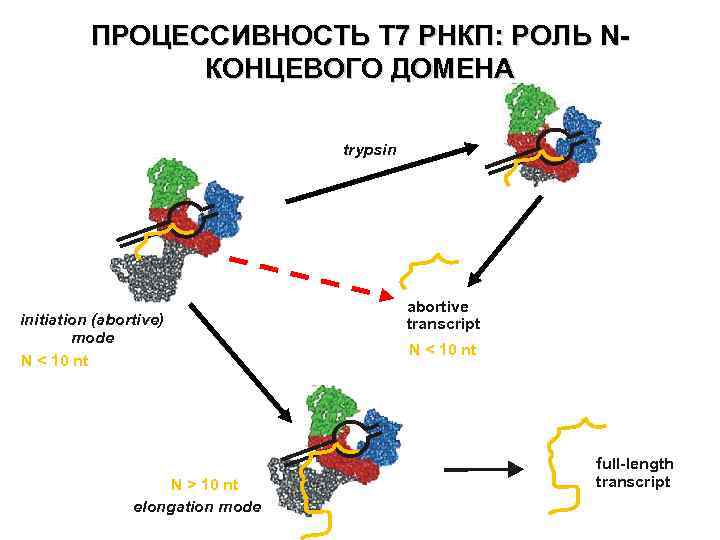
ПРОЦЕССИВНОСТЬ Т 7 РНКП: РОЛЬ NКОНЦЕВОГО ДОМЕНА trypsin initiation (abortive) mode N < 10 nt N > 10 nt elongation mode abortive transcript N < 10 nt full-length transcript
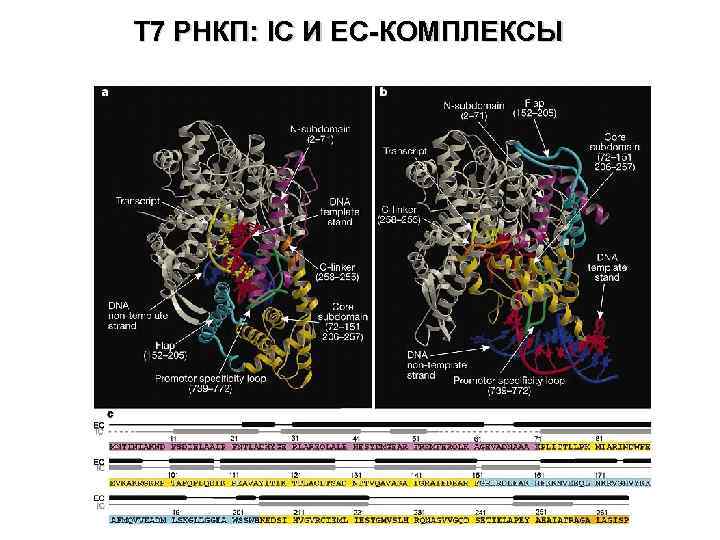
Т 7 РНКП: IC И EC-КОМПЛЕКСЫ
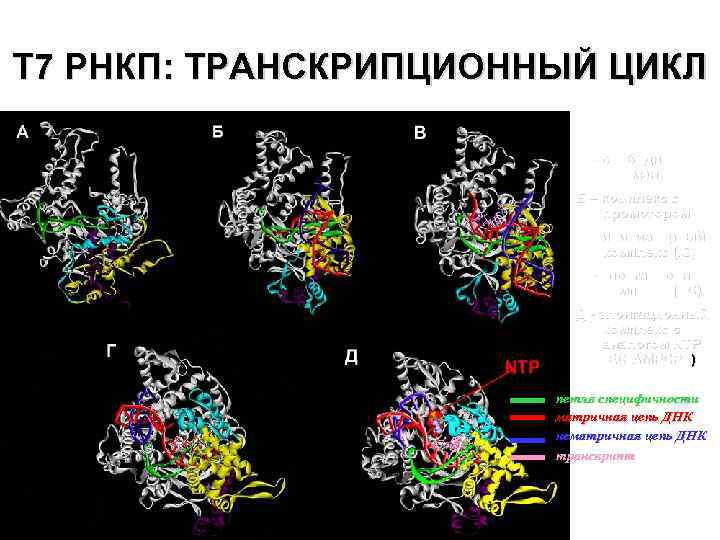
Т 7 РНКП: ТРАНСКРИПЦИОННЫЙ ЦИКЛ А – свободный фермент Б – комплекс с промотором В – инициаторный комплекс (IC) Г - элонгационный комплекс (ЕС) Д - элонгационный комплекс с аналогом NTP (ЕС-AMPCPP) петля специфичности матричная цепь ДНК нематричная цепь ДНК транскрипт
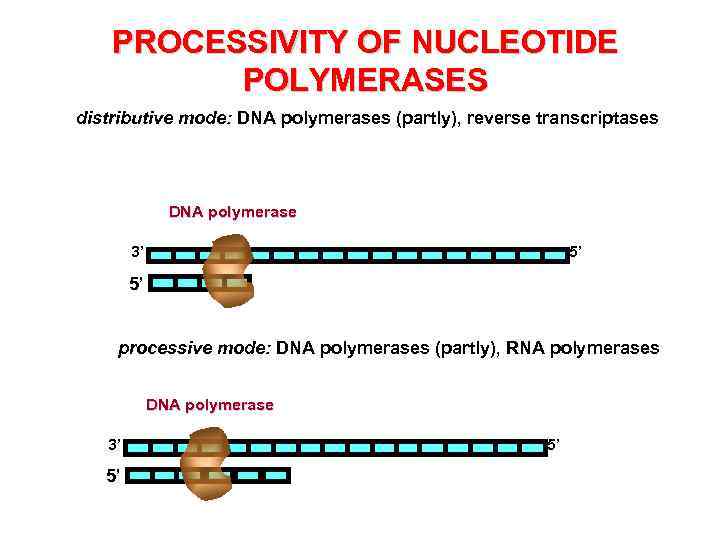
PROCESSIVITY OF NUCLEOTIDE POLYMERASES distributive mode: DNA polymerases (partly), reverse transcriptases DNA polymerase 3’ 5’ 5’ processive mode: DNA polymerases (partly), RNA polymerases DNA polymerase 3’ 5’ 5’

СПЕЦИФИЧНОСТЬ В ОТНОШЕНИИ NTP
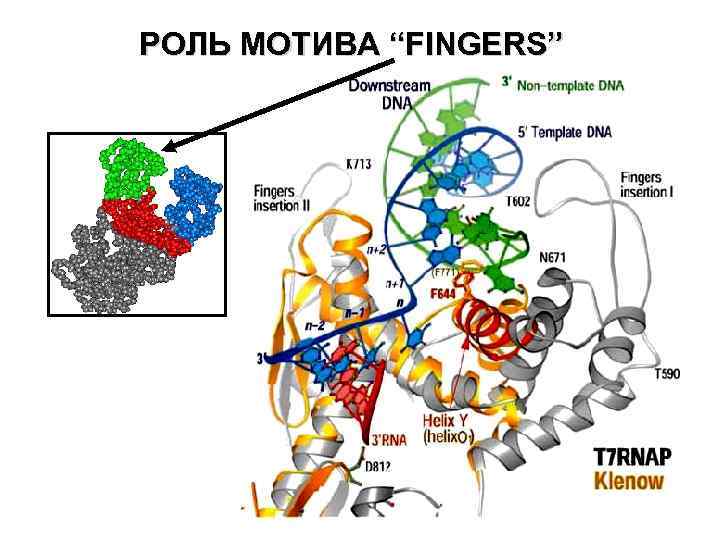
РОЛЬ МОТИВА “FINGERS”
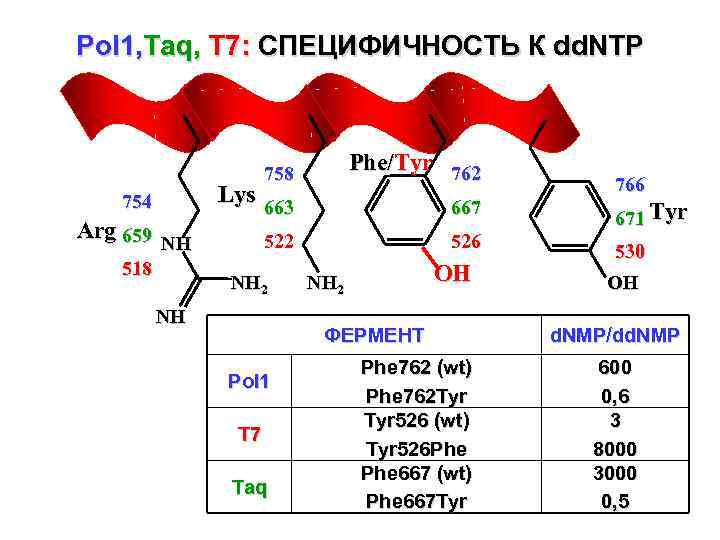
Pol 1, Taq, T 7: СПЕЦИФИЧНОСТЬ К dd. NTP 758 754 Arg 659 NH 518 Phe/Tyr 762 663 667 522 526 Lys 663 NH 2 NH OH NH 2 ФЕРМЕНТ Pol 1 T 7 Taq Phe 762 (wt) Phe 762 Tyr 526 (wt) Tyr 526 Phe 667 (wt) Phe 667 Tyr 766 671 Tyr 530 OH d. NMP/dd. NMP 600 0, 6 3 8000 3000 0, 5
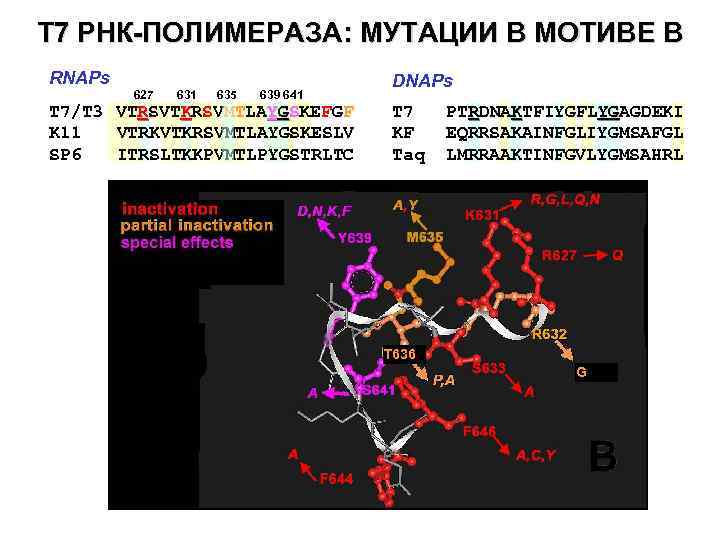
T 7 РНК-ПОЛИМЕРАЗА: МУТАЦИИ В МОТИВЕ В RNAPs 627 631 635 639 641 Т 7/Т 3 VTRSVTKRSVMTLAYGSKEFGF K 11 VTRKVTKRSVMTLAYGSKESLV SP 6 ITRSLTKKPVMTLPYGSTRLTC DNAPs Т 7 KF Taq PTRDNAKTFIYGFLYGAGDEKI YG EQRRSAKAINFGLIYGMSAFGL LMRRAAKTINFGVLYGMSAHRL T 636 G
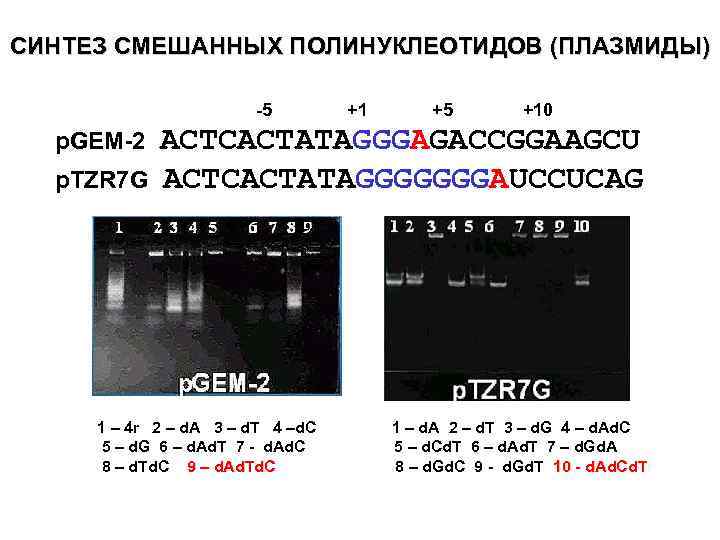
СИНТЕЗ СМЕШАННЫХ ПОЛИНУКЛЕОТИДОВ (ПЛАЗМИДЫ) -5 p. GEM-2 p. TZR 7 G +1 +5 +10 ACTCACTATAGGGAGACCGGAAGCU ACTCACTATAGGGGGGGAUCCUCAG 1 – 4 r 2 – d. A 3 – d. T 4 –d. C 5 – d. G 6 – d. Ad. T 7 - d. Ad. C 8 – d. Td. C 9 – d. Ad. Td. C 1 – d. A 2 – d. T 3 – d. G 4 – d. Ad. C 5 – d. Cd. T 6 – d. Ad. T 7 – d. Gd. A 8 – d. Gd. C 9 - d. Gd. T 10 - d. Ad. Cd. T
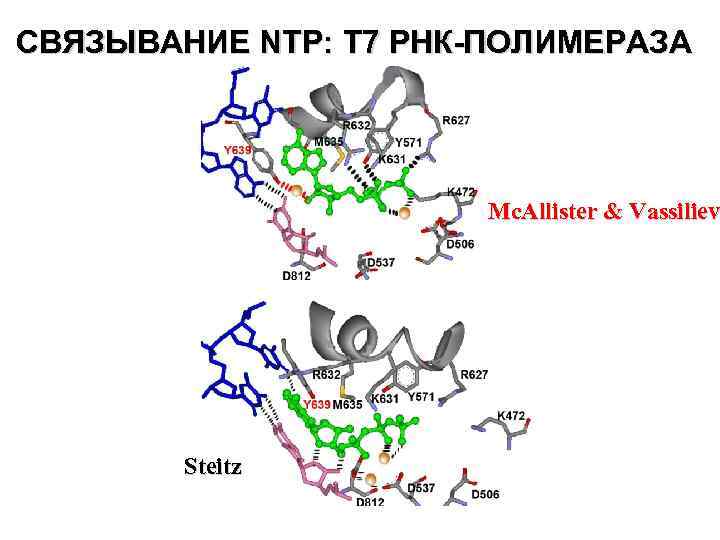
СВЯЗЫВАНИЕ NTP: Т 7 РНК-ПОЛИМЕРАЗА Mc. Allister & Vassiliev Steitz

Taq DNAP : КАРМАН СПЕЦИФИЧНОСТИ
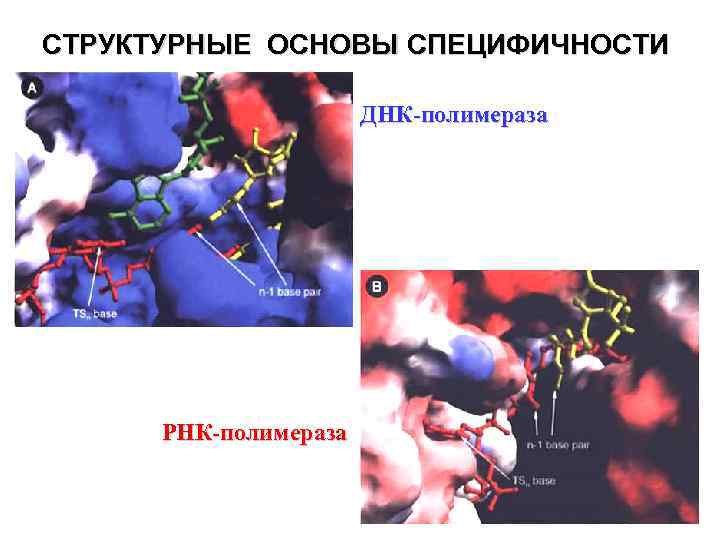
СТРУКТУРНЫЕ ОСНОВЫ СПЕЦИФИЧНОСТИ ДНК-полимераза РНК-полимераза
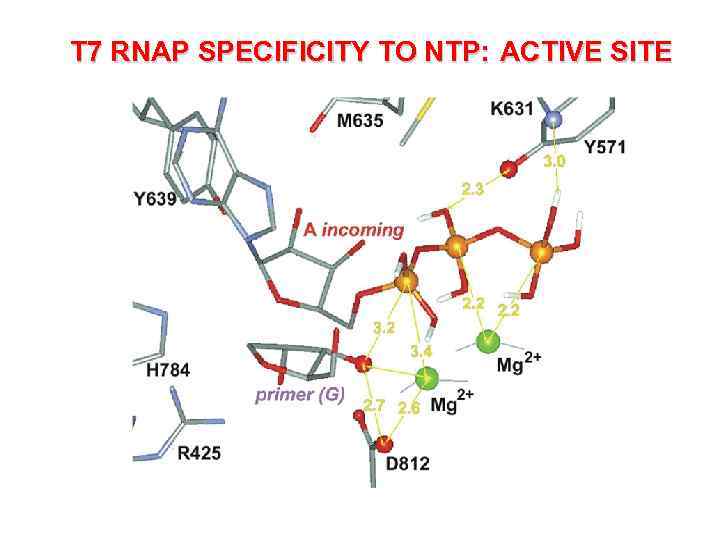
T 7 RNAP SPECIFICITY TO NTP: ACTIVE SITE
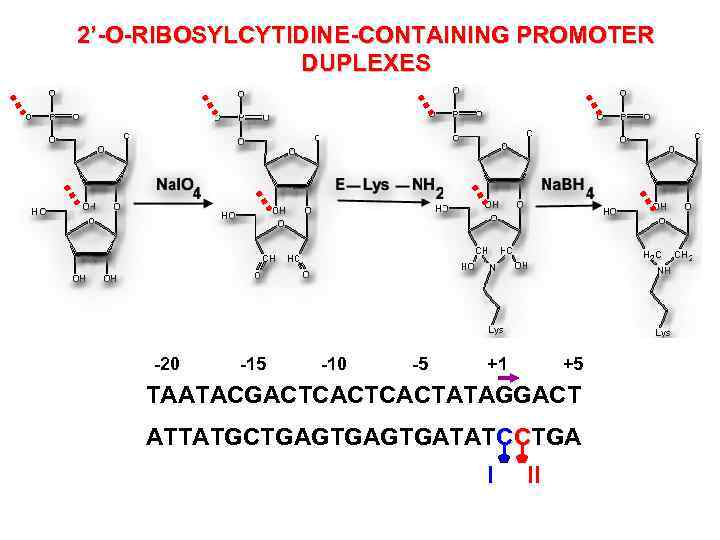
2’-O-RIBOSYLCYTIDINE-CONTAINING PROMOTER DUPLEXES -20 -15 -10 -5 +1 +5 TAATACGACTCACTATAGGACT ATTATGCTGAGTGATATCCTGA I II
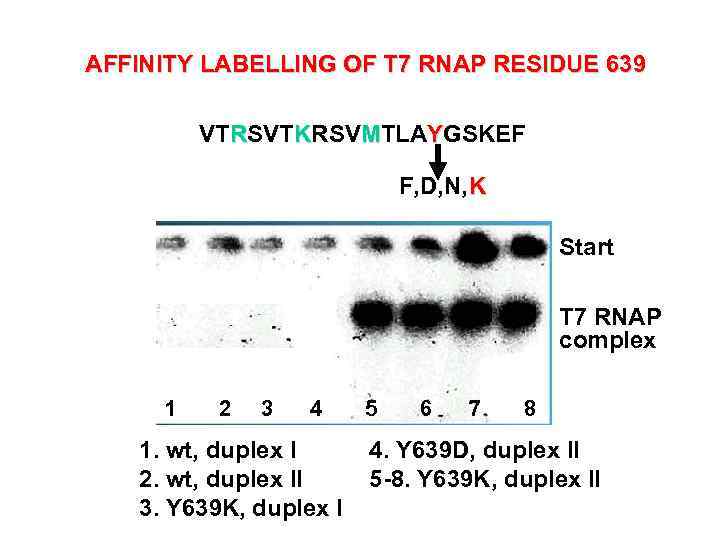
AFFINITY LABELLING OF T 7 RNAP RESIDUE 639 VTRSVTKRSVMTLAYGSKEF F, D, N, K Start T 7 RNAP complex 1 2 3 4 1. wt, duplex I 2. wt, duplex II 3. Y 639 K, duplex I 5 6 7 8 4. Y 639 D, duplex II 5 -8. Y 639 K, duplex II
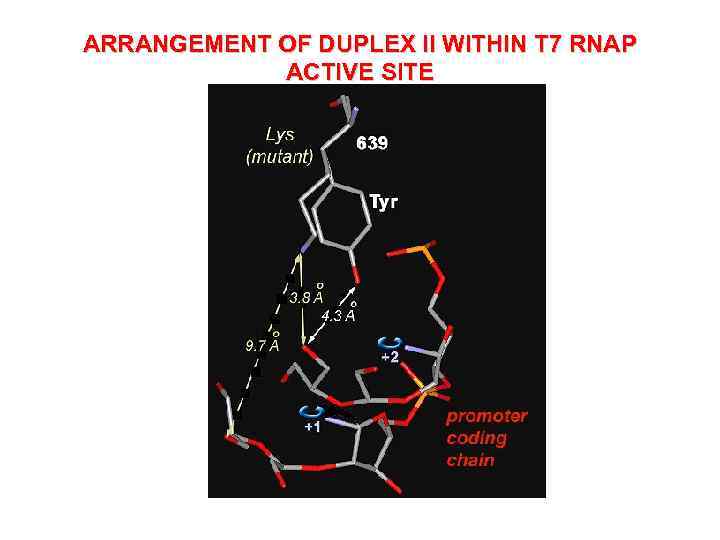
ARRANGEMENT OF DUPLEX II WITHIN T 7 RNAP ACTIVE SITE
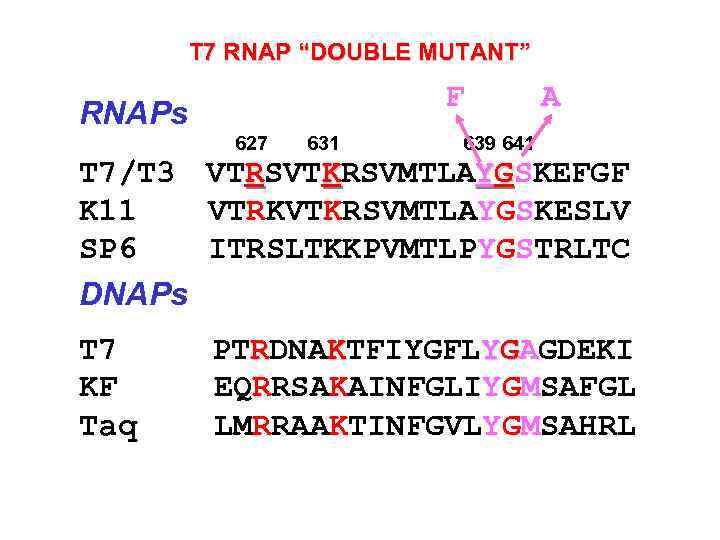
T 7 RNAP “DOUBLE MUTANT” F RNAPs 627 631 A 639 641 Т 7/Т 3 VTRSVTKRSVMTLAYGSKEFGF K 11 VTRKVTKRSVMTLAYGSKESLV SP 6 ITRSLTKKPVMTLPYGSTRLTC DNAPs Т 7 KF Taq PTRDNAKTFIYGFLYGAGDEKI EQRRSAKAINFGLIYGMSAFGL LMRRAAKTINFGVLYGMSAHRL
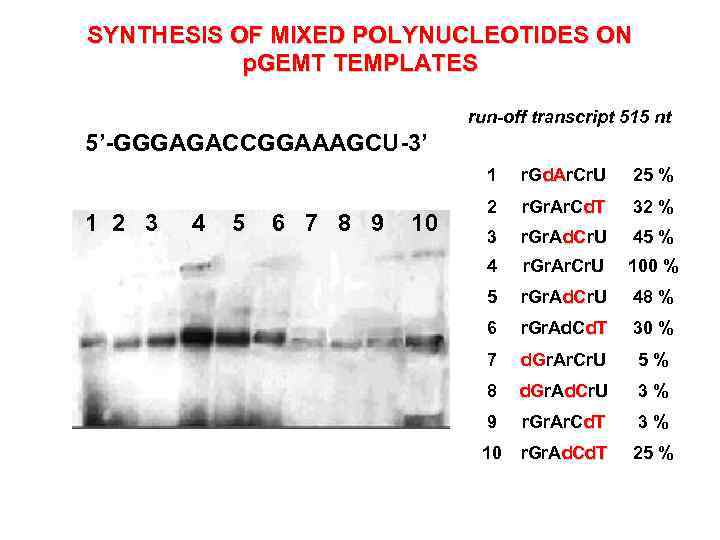
SYNTHESIS OF MIXED POLYNUCLEOTIDES ON p. GEMT TEMPLATES run-off transcript 515 nt 5’-GGGAGACCGGAAAGCU-3’ 1 1 2 3 4 5 6 7 8 9 10 r. Gd. Ar. Cr. U d. A 25 % 2 r. Gr. Ar. Cd. T 32 % 3 r. Gr. Ad. Cr. U d. C 45 % 4 r. Gr. Ar. Cr. U 100 % 5 r. Gr. Ad. Cr. U d. C 48 % 6 r. Gr. Ad. Cd. T 30 % 7 d. Gr. Ar. Cr. U 5% 8 d. Gr. Ad. Cr. U d. G d. C 3% 9 r. Gr. Ar. Cd. T 3% 10 r. Gr. Ad. Cd. T 25 %
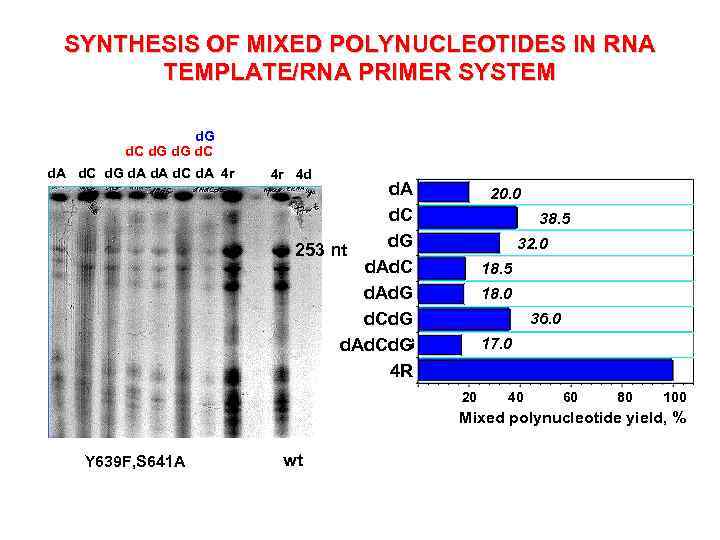
SYNTHESIS OF MIXED POLYNUCLEOTIDES IN RNA TEMPLATE/RNA PRIMER SYSTEM d. G d. C d. A d. C d. G d. A d. C d. A 4 r 4 r 4 d d. A d. C d. G 253 nt d. Ad. C d. Ad. G d. Cd. G d. Ad. Cd. G 4 R 20. 0 38. 5 32. 0 18. 5 18. 0 36. 0 17. 0 20 40 60 80 100 Mixed polynucleotide yield, % Y 639 F, S 641 A wt
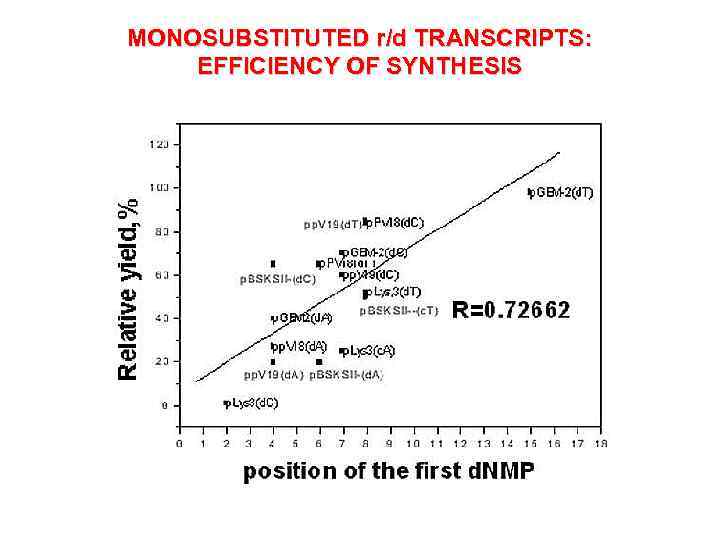
MONOSUBSTITUTED r/d TRANSCRIPTS: EFFICIENCY OF SYNTHESIS
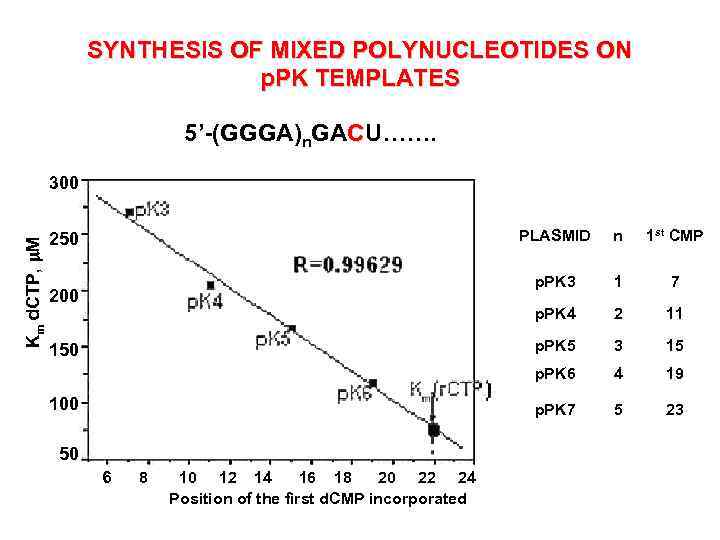
SYNTHESIS OF MIXED POLYNUCLEOTIDES ON p. PK TEMPLATES 5’-(GGGA)n. GACU……. Km d. CTP, m. M 300 PLASMID 6 8 10 12 14 16 18 20 22 24 Position of the first d. CMP incorporated 2 11 3 15 4 19 p. PK 7 50 7 p. PK 6 100 1 p. PK 5 150 1 st CMP p. PK 4 200 n p. PK 3 250 5 23
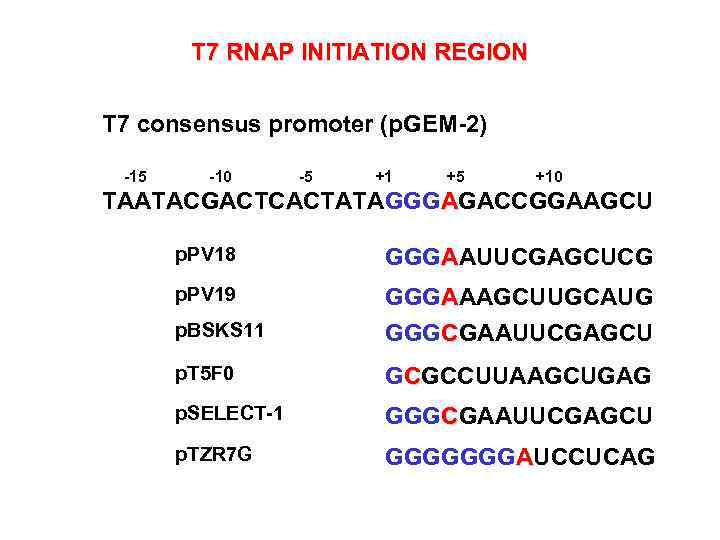
T 7 RNAP INITIATION REGION T 7 consensus promoter (p. GEM-2) -15 -10 -5 +1 +5 +10 TAATACGACTCACTATAGGGAGACCGGAAGCU p. PV 18 GGGAAUUCGAGCUCG p. PV 19 p. BSKS 11 GGGAAAGCUUGCAUG GGGCGAAUUCGAGCU p. T 5 F 0 GCGCCUUAAGCUGAG p. SELECT-1 GGGCGAAUUCGAGCU p. TZR 7 G GGGGGGGAUCCUCAG
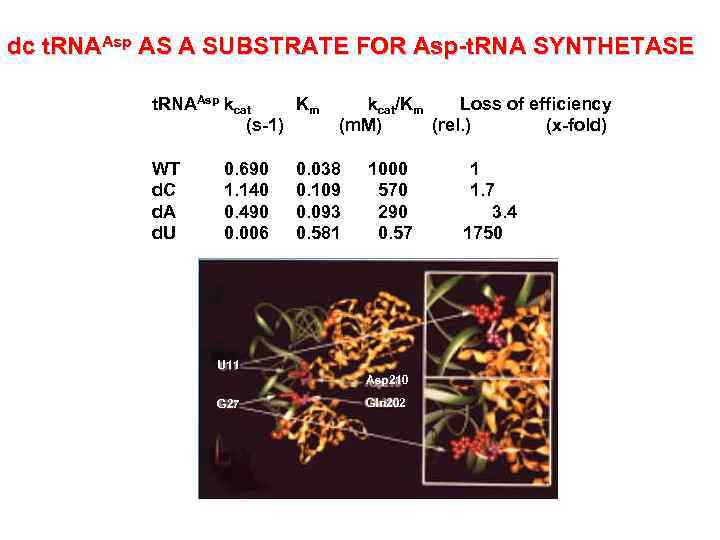
dc t. RNAAsp AS A SUBSTRATE FOR Asp-t. RNA SYNTHETASE t. RNAAsp kcat Km (s-1) WT d. C d. A d. U 0. 690 1. 140 0. 490 0. 006 kcat/Km Loss of efficiency (m. M) (rel. ) (x-fold) 0. 038 0. 109 0. 093 0. 581 1000 570 290 0. 57 U 11 Asp 210 G 27 Gln 202 1 1. 7 3. 4 1750

СПЕЦИФИЧНОСТЬ В ОТНОШЕНИИ МАТРИЦЫ/ПРАЙМЕРА
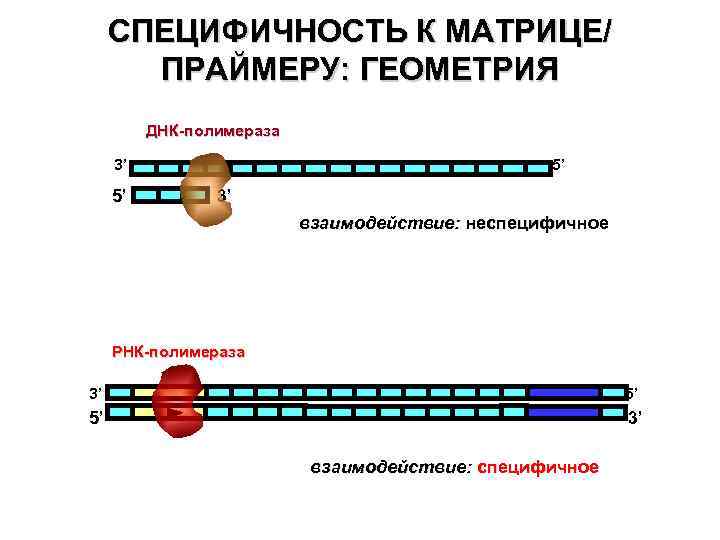
СПЕЦИФИЧНОСТЬ К МАТРИЦЕ/ ПРАЙМЕРУ: ГЕОМЕТРИЯ ДНК-полимераза 3’ 5’ 5’ 3’ взаимодействие: неспецифичное РНК-полимераза 3’ 5’ 5’ 3’ взаимодействие: специфичное
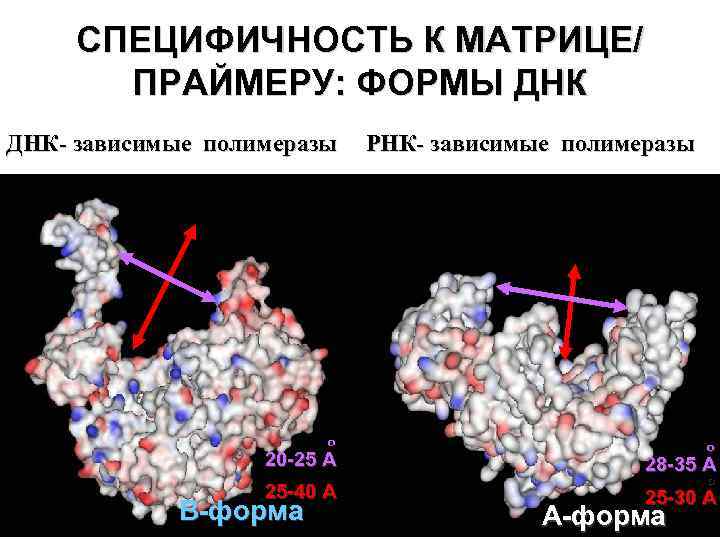
СПЕЦИФИЧНОСТЬ К МАТРИЦЕ/ ПРАЙМЕРУ: ФОРМЫ ДНК- зависимые полимеразы РНК- зависимые полимеразы o 20 -25 A o 25 -40 A В-форма o 2 8 -3 5 A o 25 -30 A А-форма
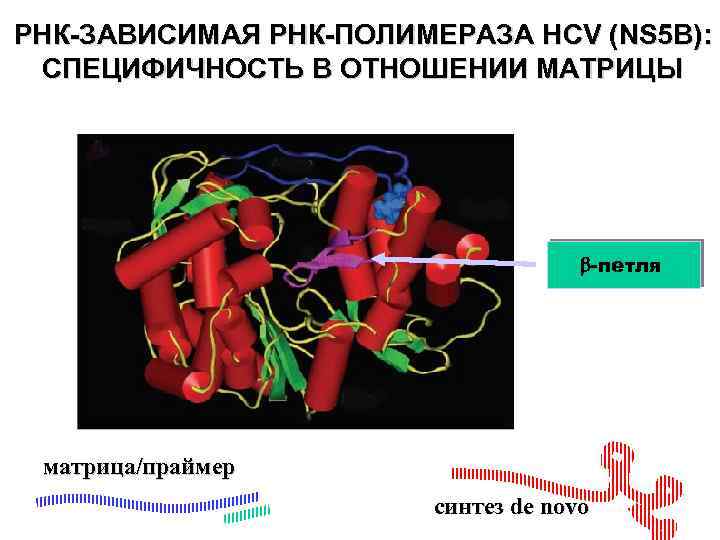
РНК-ЗАВИСИМАЯ РНК-ПОЛИМЕРАЗА HCV (NS 5 B): СПЕЦИФИЧНОСТЬ В ОТНОШЕНИИ МАТРИЦЫ -петля матрица/праймер синтез de novo
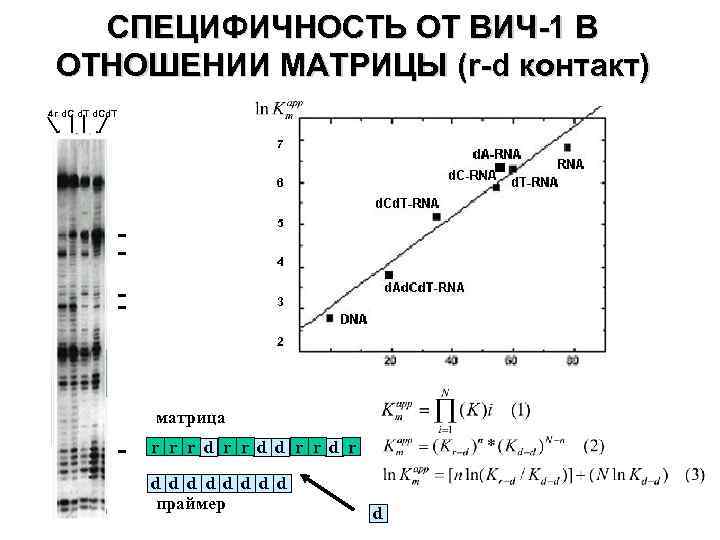
СПЕЦИФИЧНОСТЬ ОТ ВИЧ-1 В ОТНОШЕНИИ МАТРИЦЫ (r-d контакт) 4 r d. C d. T d. Cd. T 7 6 5 4 3 2 матрица r r r d d d d d праймер d
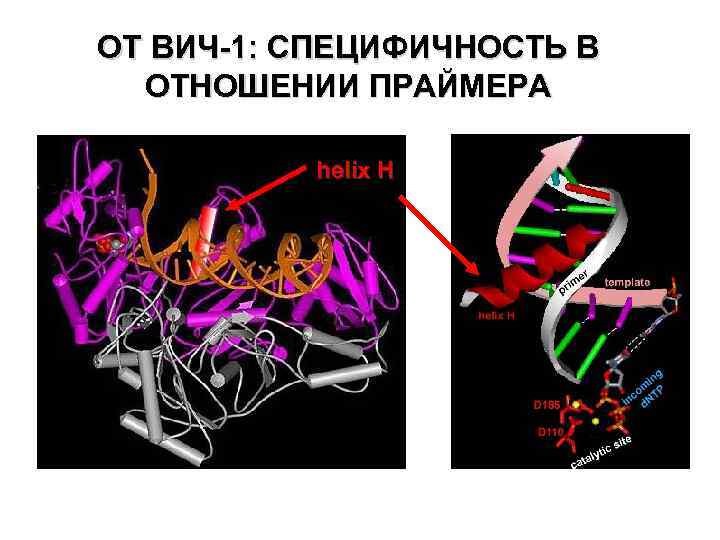
ОТ ВИЧ-1: СПЕЦИФИЧНОСТЬ В ОТНОШЕНИИ ПРАЙМЕРА helix H
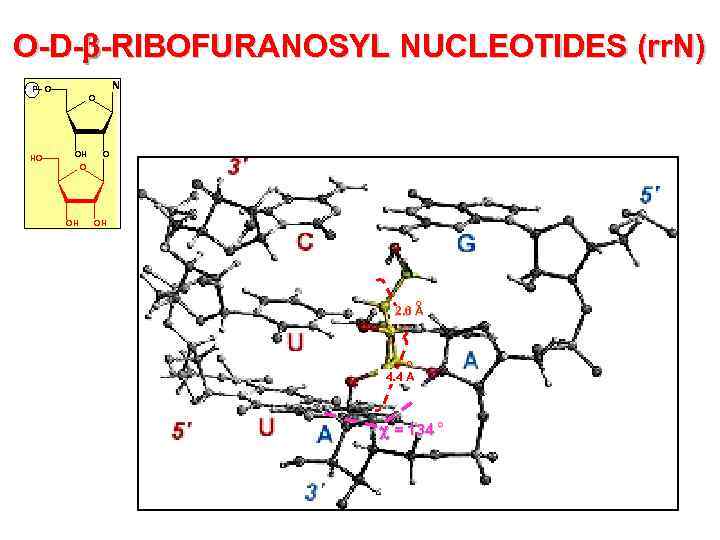
O-D- -RIBOFURANOSYL NUCLEOTIDES (rr. N) N P O HO O OH OH o 2. 6 A o 4. 4 A = 134 o
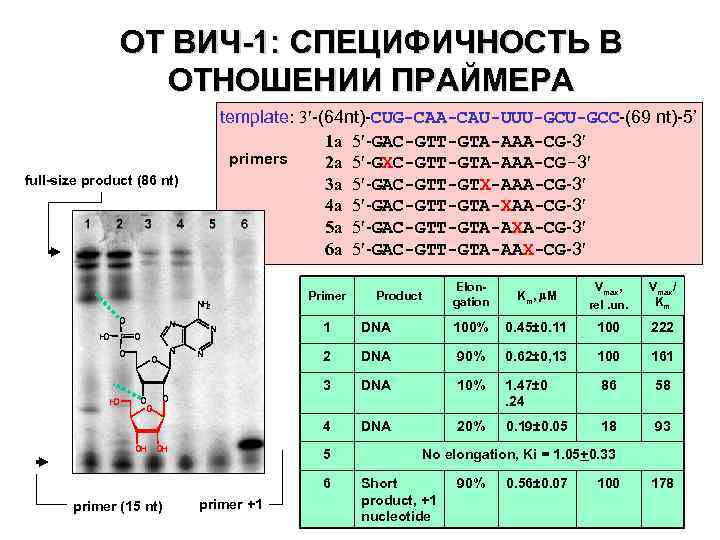
ОТ ВИЧ-1: СПЕЦИФИЧНОСТЬ В ОТНОШЕНИИ ПРАЙМЕРА template: 3 -(64 nt)-CUG-CAA-CAU-UUU-GCC-(69 nt)-5’ 1 a 5 -GAC-GTT-GTA-AAA-CG-3 primers 2 a 5 -GXC-GTT-GTA-AAA-CG-3 3 a 5 -GAC-GTT-GTX-AAA-CG-3 4 a 5 -GAC-GTT-GTA-XAA-CG-3 5 a 5 -GAC-GTT-GTA-AXA-CG-3 6 a 5 -GAC-GTT-GTA-AAX-CG-3 full-size product (86 nt) Primer N 2 H O N Elongation Product Km, m. М Vmax, rel. un. Vmax/ Km O H O N O O O N DNA 100% 0. 45± 0. 11 100 222 2 DNA 90% 0. 62± 0, 13 100 161 DNA 10% 1. 47± 0. 24 86 58 4 N P O 1 3 H O DNA 20% 0. 19± 0. 05 18 93 O OH OH 5 6 primer (15 nt) primer +1 No elongation, Ki = 1. 05+0. 33 Short product, +1 nucleotide 90% 0. 56± 0. 07 100 178
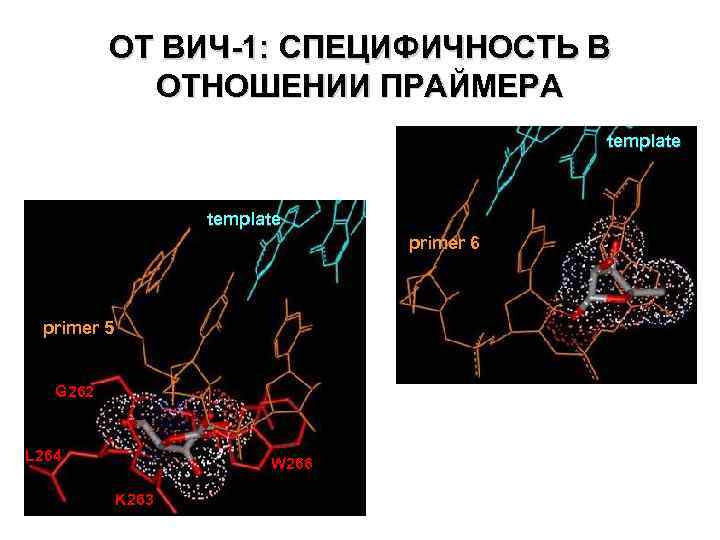
ОТ ВИЧ-1: СПЕЦИФИЧНОСТЬ В ОТНОШЕНИИ ПРАЙМЕРА template primer 6 primer 5 G 262 L 264 W 266 K 263
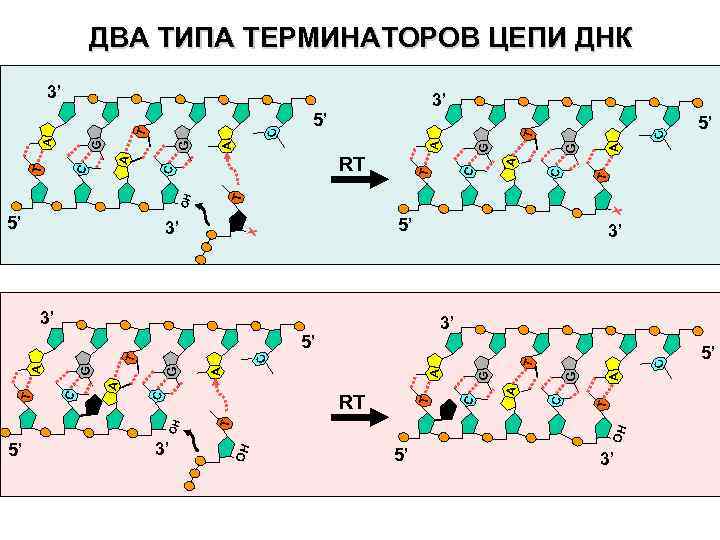
ДВА ТИПА ТЕРМИНАТОРОВ ЦЕПИ ДНК 3’ C G T C A OH OH T C A C T T OH C RT 3’ G G A A A G T T G C T C 3’ 5’ 5’ A T A C 3’ 3’ A G A T 5’ X 3’ X OH 5’ 5’ T C C T A RT 5’ C 5’ A G G A T C 3’ 5’ 3’
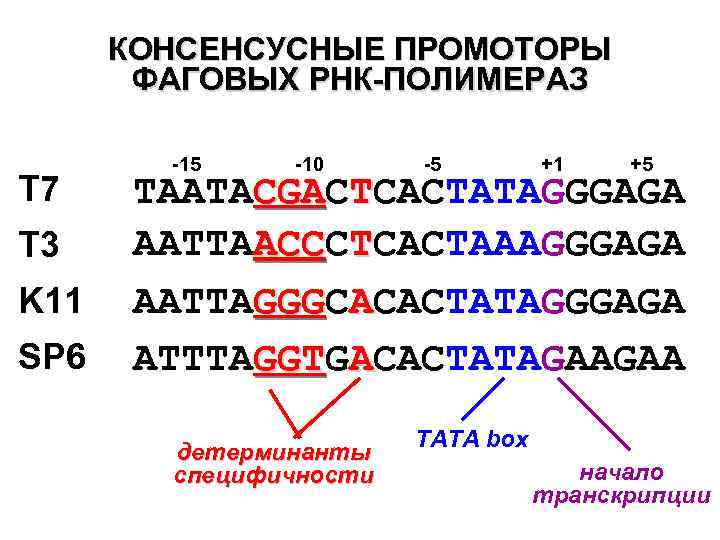
КОНСЕНСУСНЫЕ ПРОМОТОРЫ ФАГОВЫХ РНК-ПОЛИМЕРАЗ T 7 T 3 K 11 SP 6 -15 -10 -5 +1 +5 TAATACGACTCACTATAGGGAGA CGA AATTAACCCTCACTAAAGGGAGA ACC AATTAGGGCACACTATAGGGAGA GGG ATTTAGGTGACACTATAGAAGAA GGT детерминанты специфичности TATA box начало транскрипции
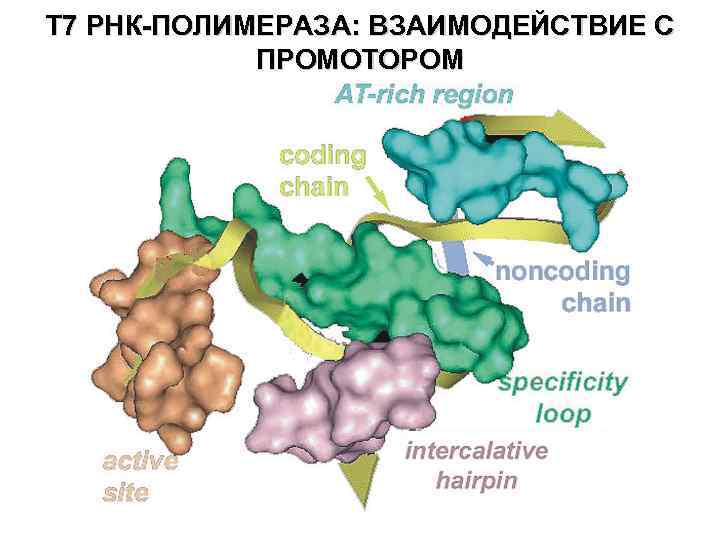
T 7 РНК-ПОЛИМЕРАЗА: ВЗАИМОДЕЙСТВИЕ С ПРОМОТОРОМ
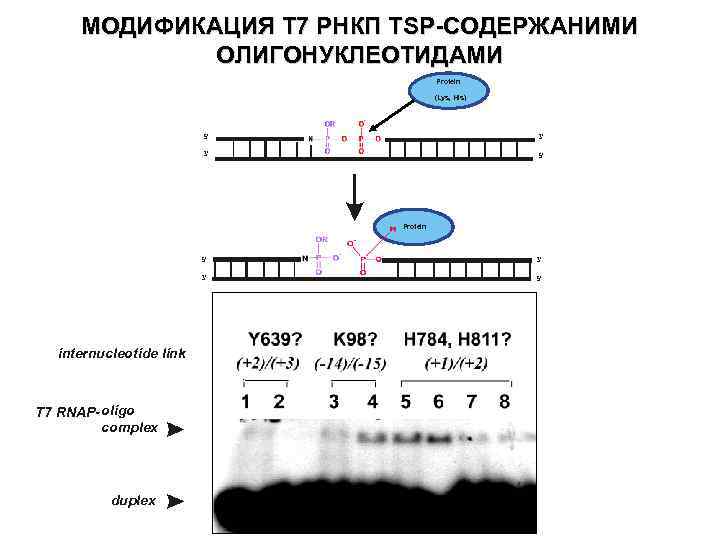
МОДИФИКАЦИЯ Т 7 РНКП TSP-СОДЕРЖАНИМИ ОЛИГОНУКЛЕОТИДАМИ Protein (Lys, His) 5’ 3’ 3’ 5’ Protein 5’ 3’ internucleotide link T 7 RNAP- oligo complex duplex 3’ 5’

T 7 RNAP MODIFICATION WITH TSP-CONTAINING OLIGOS Protein (Lys, His) 5’ 3’ 3’ 5’ Protein 5’ 3’ CODING 3’ 5’ E 421 R 298 W 422 T 299 R 423 H 300 N 131 Q 135 R 425 E 421 R 298 Q 135 R 231 Y 739 W 422 T 299 S 139 D 240 K 773 Y 427 W 422 K 206 E 242 G 777 Q 737 W 736 Q 744 V 237 R 746 Y 639 N 781 E 738 Q 737 T 760 D 240 Q 758 G 777 H 784 Y 739 E 738 K 206 I 761 Q 744 R 759 P 780 H 811 Y 739 W 201 N 762 T 760 R 231 E 242 R 746 E 755 R 756 E 755 I 757 R 756 Q 758 R 756 K 93 R 96 K 95 G 97 R 96 K 98 R 99 5' T G G A G T C C T A G T G A G T C G T A T T A 3' +8 +7 +6 +5 +4 +3 +2 +1 - 2 - 3 - 4 - 5 - 6 - 7 - 8 - 9 - 10 - 11 - 12 - 13 - 14 - 15 - 16 - 17 3' A C C T C A G G A T C A C T C A G C A T A A T 5' NONCODING
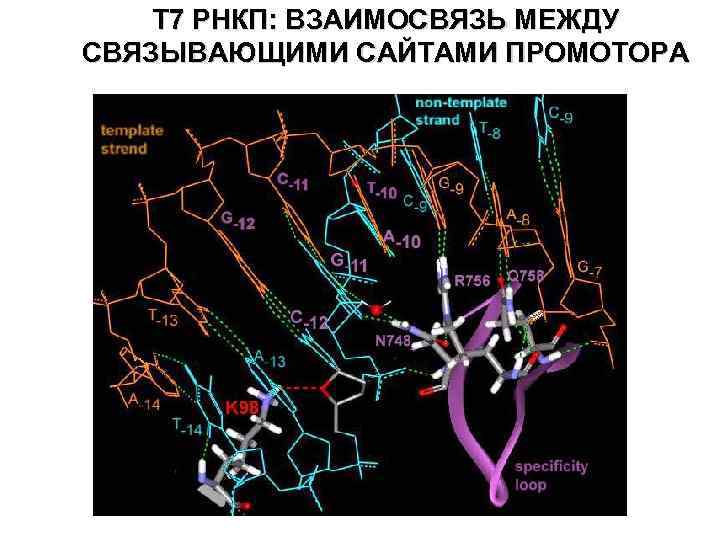
T 7 РНКП: ВЗАИМОСВЯЗЬ МЕЖДУ СВЯЗЫВАЮЩИМИ САЙТАМИ ПРОМОТОРА
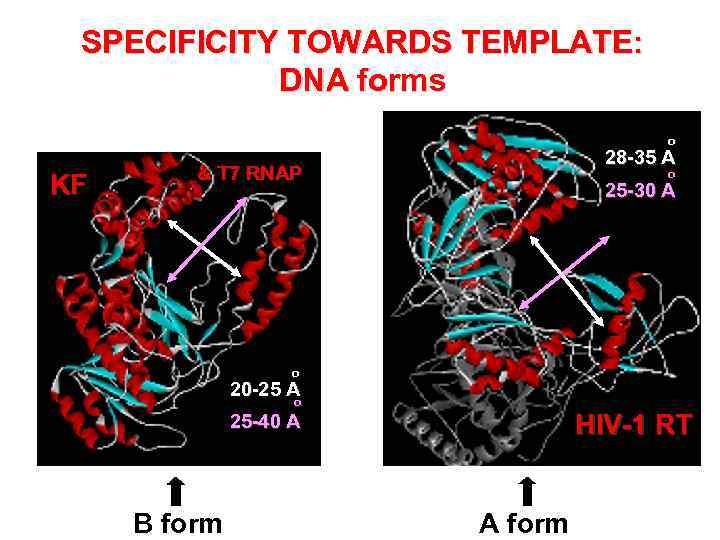
SPECIFICITY TOWARDS TEMPLATE: DNA forms o KF 28 -35 A & T 7 RNAP o 25 -30 A o 20 -25 A o o HIV-1 RT 25 -40 A B form A form
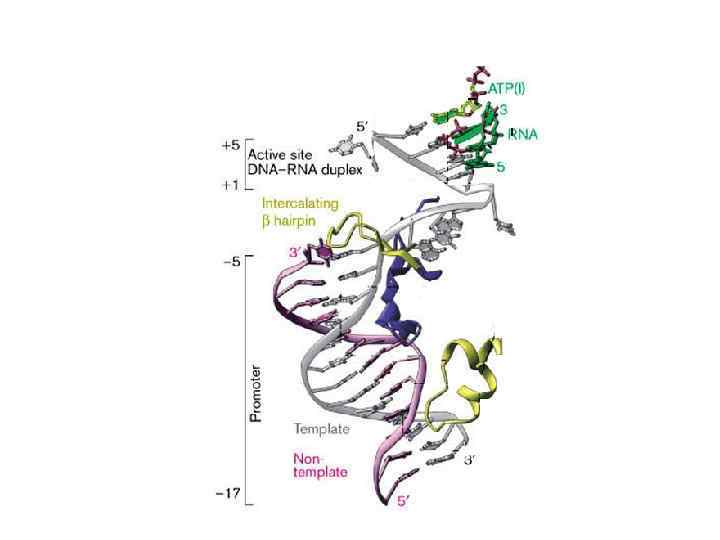
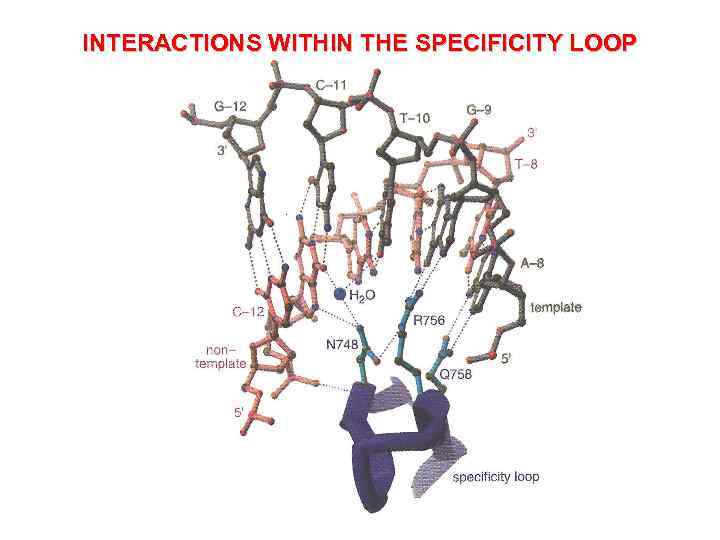
INTERACTIONS WITHIN THE SPECIFICITY LOOP
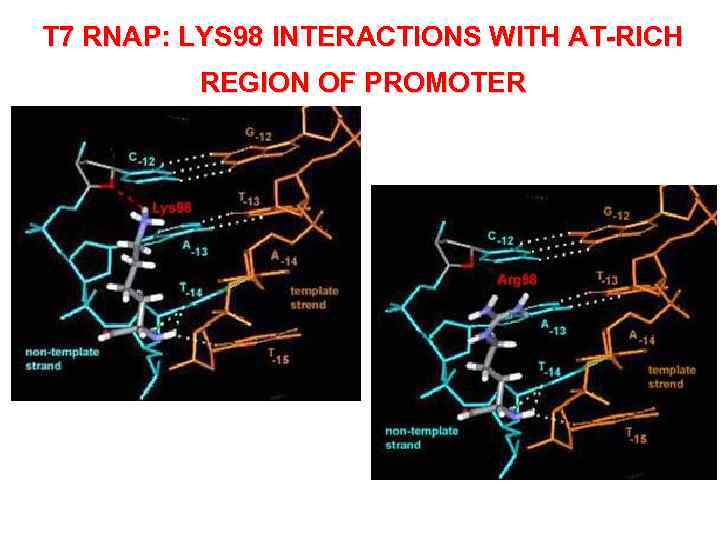
T 7 RNAP: LYS 98 INTERACTIONS WITH AT-RICH REGION OF PROMOTER

3’-5’-ЭКЗОНУКЛЕАЗНАЯ АКТИВНОСТЬ
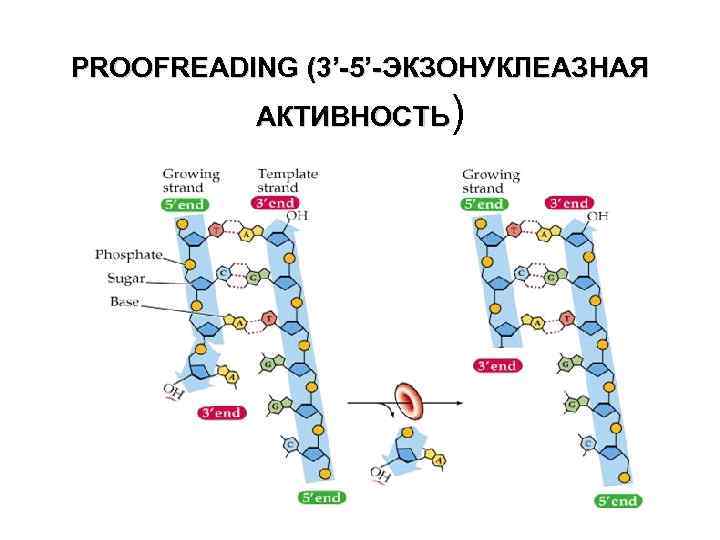
PROOFREADING (3’-5’-ЭКЗОНУКЛЕАЗНАЯ АКТИВНОСТЬ)
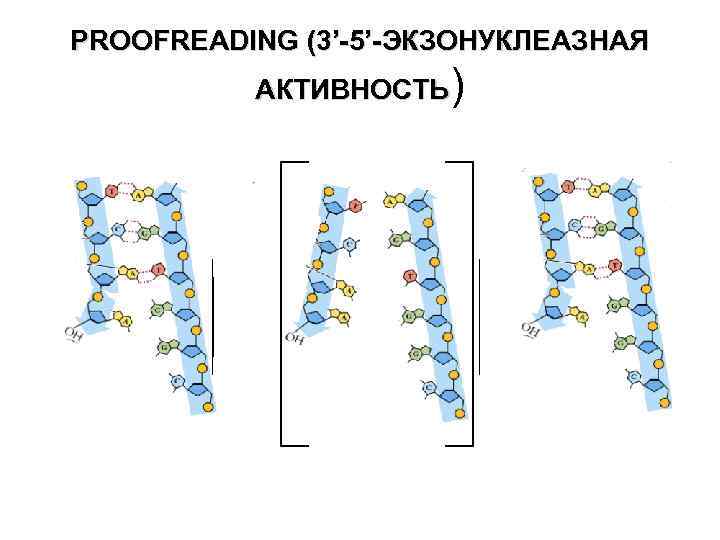
PROOFREADING (3’-5’-ЭКЗОНУКЛЕАЗНАЯ АКТИВНОСТЬ)
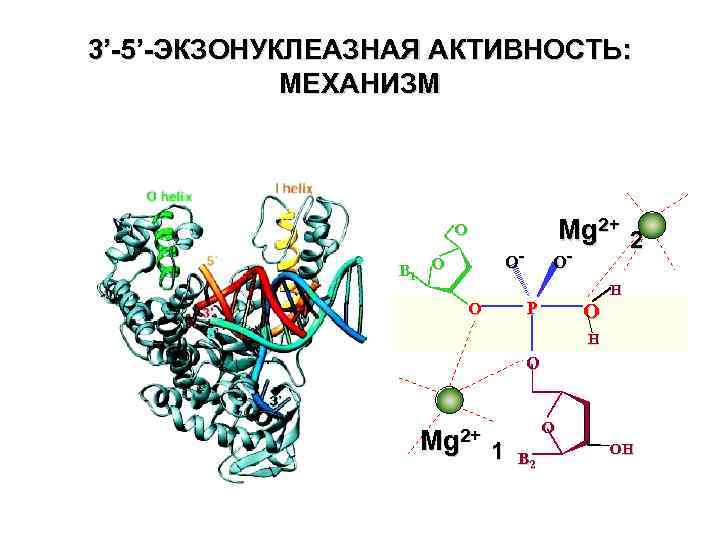
3’-5’-ЭКЗОНУКЛЕАЗНАЯ АКТИВНОСТЬ: МЕХАНИЗМ Mg 2+ 2 - O O- B 1 O O H P O O H O Mg 2+ O 1 B 2 OH
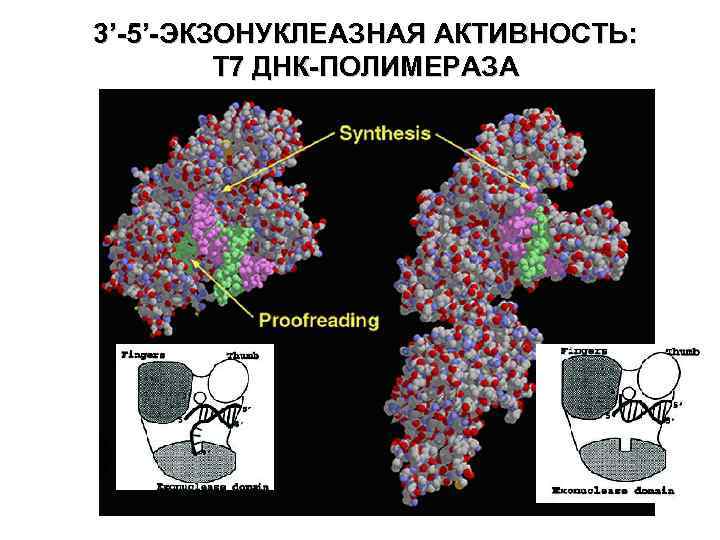
3’-5’-ЭКЗОНУКЛЕАЗНАЯ АКТИВНОСТЬ: Т 7 ДНК-ПОЛИМЕРАЗА
POLYMERASES(19.09.14).ppt