1Физико-химические свойства мочи.ppt
- Количество слайдов: 42
 Физико-химические свойства мочи
Физико-химические свойства мочи
 Преаналитика n n n Для исследования собирают всю порцию утренней мочи после тщательного туалета половых органов. Мочу необходимо собирать в совершенно чистую, сухую посуду; хранить до исследования можно не более 1, 5 часа в холодном месте. Применение консерви-рующих веществ нежелательно, но допускается в виде исключения. Лучшие результаты наблюдения при обработке мочи тимолом (кристаллик тимола на 100 -150 мл мочи).
Преаналитика n n n Для исследования собирают всю порцию утренней мочи после тщательного туалета половых органов. Мочу необходимо собирать в совершенно чистую, сухую посуду; хранить до исследования можно не более 1, 5 часа в холодном месте. Применение консерви-рующих веществ нежелательно, но допускается в виде исключения. Лучшие результаты наблюдения при обработке мочи тимолом (кристаллик тимола на 100 -150 мл мочи).
 ФИЗИЧЕСКИЕ СВОЙСТВА МОЧИ
ФИЗИЧЕСКИЕ СВОЙСТВА МОЧИ
 Количество n Измерение объёма утренней мочи целесообразно для интерпретации её относительной плотности
Количество n Измерение объёма утренней мочи целесообразно для интерпретации её относительной плотности
 Цвет n n n Нормальная моча окрашена в жёлтый цвет ( от соломенного до янтарно-жёлтого). Окраска может меняться приёме лекарств (амидопирина, салицилатов и др. ) или употреблении некоторых пищевых продуктов (ревеня, свеклы, черники). Патологические изменённая окраска мочи бывает при гематурии (вид мясных помоев), при билирубинурии (оранжево-красный).
Цвет n n n Нормальная моча окрашена в жёлтый цвет ( от соломенного до янтарно-жёлтого). Окраска может меняться приёме лекарств (амидопирина, салицилатов и др. ) или употреблении некоторых пищевых продуктов (ревеня, свеклы, черники). Патологические изменённая окраска мочи бывает при гематурии (вид мясных помоев), при билирубинурии (оранжево-красный).
 Прозрачность, запах Свежевыделенная моча здорового человека обычно прозрачна. Однако при длительном стоянии в ней образуется небольшое помутнение в виде облачка, состоящего из мукоида (слизь из мочевых путей) и фосфатов. Значительное помутнение мочи и снижение ее прозрачности бывает обусловлено выделением большого количества слизи, лейкоцитов и эритроцитов, бактерий, эпителиальных клеток, капель жира, солей (особенно фосфатов и уратов). Свежая моча имеет слабый ароматический запах. При длительном стоянии, особенно в теплом помещении, в результате процессов брожения она приобретает запах аммиака. У больных сахарным диабетом, осложненным гипергликемической комой, моча имеет запах гнилых яблок в связи с наличием в ней ацетона. Неприятный специфический запах мочи отмечается после обильного употребления кофе, хрена, чеснока.
Прозрачность, запах Свежевыделенная моча здорового человека обычно прозрачна. Однако при длительном стоянии в ней образуется небольшое помутнение в виде облачка, состоящего из мукоида (слизь из мочевых путей) и фосфатов. Значительное помутнение мочи и снижение ее прозрачности бывает обусловлено выделением большого количества слизи, лейкоцитов и эритроцитов, бактерий, эпителиальных клеток, капель жира, солей (особенно фосфатов и уратов). Свежая моча имеет слабый ароматический запах. При длительном стоянии, особенно в теплом помещении, в результате процессов брожения она приобретает запах аммиака. У больных сахарным диабетом, осложненным гипергликемической комой, моча имеет запах гнилых яблок в связи с наличием в ней ацетона. Неприятный специфический запах мочи отмечается после обильного употребления кофе, хрена, чеснока.
 Реакция мочи n n Определение p. H при помощи лакмусовой бумаги следует проводить одновременно синей и красной: 1) синяя лакмусовая бумага краснеет, красная не изменяет цвет – кислая реакция, 2) красная лакмусовая бумага синеет, синяя не изменяет цвет – щелочная реакция, 3) оба вида бумаги не меняют цвет – нейтральная реакция.
Реакция мочи n n Определение p. H при помощи лакмусовой бумаги следует проводить одновременно синей и красной: 1) синяя лакмусовая бумага краснеет, красная не изменяет цвет – кислая реакция, 2) красная лакмусовая бумага синеет, синяя не изменяет цвет – щелочная реакция, 3) оба вида бумаги не меняют цвет – нейтральная реакция.
 Реакция мочи (р. Н) обусловлена концентрацией в ней свободных ионов водорода (Н+). В норме при смешанной пище реакция мочи кислая или нейтральная р. Н 5, 5 -7, 0, но чаще значения р. Н составляют 5 -6. Кислотность определяется в свежевыпущенной моче, т. к. при стоянии выделяется углекислота и р. Н сдвигается в щелочную сторону. На величину р. Н мочи влияет характер пищи. При употреблении преимущественно мясной пищи моча имеет более кислую реакцию, при овощной диете реакция мочи щелочная. Кислая реакция мочи у человека зависит от присутствия в ней главным образом однозамещенных фосфатов (например, КН 2 РО 4 или Na. H 2 PO 4). В щелочной моче преобладают двузамещенные фосфаты или бикарбонаты калия либо натрия. При длительном хранении р. Н мочи становится щелочной в результате роста бактерий, поэтому теряется его диагностическое значение.
Реакция мочи (р. Н) обусловлена концентрацией в ней свободных ионов водорода (Н+). В норме при смешанной пище реакция мочи кислая или нейтральная р. Н 5, 5 -7, 0, но чаще значения р. Н составляют 5 -6. Кислотность определяется в свежевыпущенной моче, т. к. при стоянии выделяется углекислота и р. Н сдвигается в щелочную сторону. На величину р. Н мочи влияет характер пищи. При употреблении преимущественно мясной пищи моча имеет более кислую реакцию, при овощной диете реакция мочи щелочная. Кислая реакция мочи у человека зависит от присутствия в ней главным образом однозамещенных фосфатов (например, КН 2 РО 4 или Na. H 2 PO 4). В щелочной моче преобладают двузамещенные фосфаты или бикарбонаты калия либо натрия. При длительном хранении р. Н мочи становится щелочной в результате роста бактерий, поэтому теряется его диагностическое значение.
 Относительная плотность n n Относительная плотность мочи (ОПН) колеблется от 1, 001 до 1, 040 у взрослого человека. ОПН зависит от: Количества выпитой жидкости Концентрации в моче белка, глюкозы, кальция и т. д. Определение относительной плотности мочи имеет большое клиническое значение, так как дает представление о концентрации растворенных в ней веществ (мочевины, мочевой кислоты, солей) и отражает способность почек к концентрированию и разведению.
Относительная плотность n n Относительная плотность мочи (ОПН) колеблется от 1, 001 до 1, 040 у взрослого человека. ОПН зависит от: Количества выпитой жидкости Концентрации в моче белка, глюкозы, кальция и т. д. Определение относительной плотности мочи имеет большое клиническое значение, так как дает представление о концентрации растворенных в ней веществ (мочевины, мочевой кислоты, солей) и отражает способность почек к концентрированию и разведению.
 Высокая ОПН: В утренних порциях мочи у здоровых лиц, особенно в летний период года У лихорадящих больных в связи с повышенным выделением мочевины, мочевой кислоты, креатинина в уменьшенном количестве мочи При амилойдном и липойдном нефрозах Сахарном диабете Пищевой глюкозурии «Застойной почке» Низкая ОПН: При выведении больших количеств мочи (полиурия) Органических поражениях почек
Высокая ОПН: В утренних порциях мочи у здоровых лиц, особенно в летний период года У лихорадящих больных в связи с повышенным выделением мочевины, мочевой кислоты, креатинина в уменьшенном количестве мочи При амилойдном и липойдном нефрозах Сахарном диабете Пищевой глюкозурии «Застойной почке» Низкая ОПН: При выведении больших количеств мочи (полиурия) Органических поражениях почек
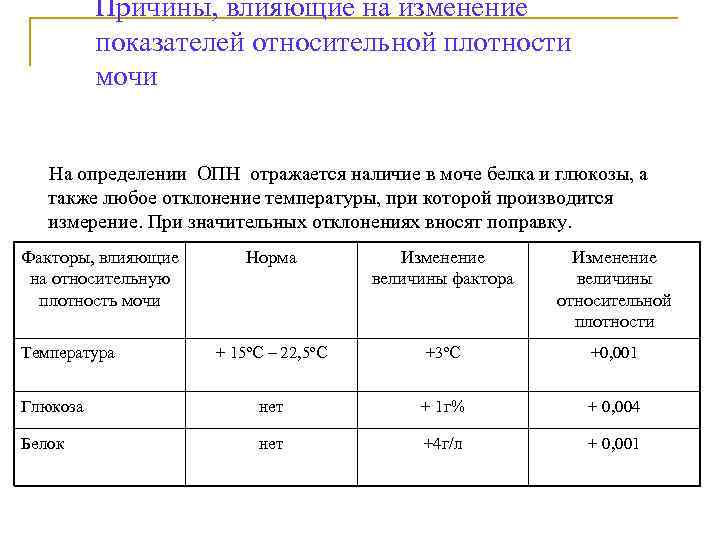 Причины, влияющие на изменение показателей относительной плотности мочи На определении ОПН отражается наличие в моче белка и глюкозы, а также любое отклонение температуры, при которой производится измерение. При значительных отклонениях вносят поправку. Факторы, влияющие на относительную плотность мочи Норма Изменение величины фактора Изменение величины относительной плотности + 15ºС – 22, 5ºС +3ºС +0, 001 Глюкоза нет + 1 г% + 0, 004 Белок нет +4 г/л + 0, 001 Температура
Причины, влияющие на изменение показателей относительной плотности мочи На определении ОПН отражается наличие в моче белка и глюкозы, а также любое отклонение температуры, при которой производится измерение. При значительных отклонениях вносят поправку. Факторы, влияющие на относительную плотность мочи Норма Изменение величины фактора Изменение величины относительной плотности + 15ºС – 22, 5ºС +3ºС +0, 001 Глюкоза нет + 1 г% + 0, 004 Белок нет +4 г/л + 0, 001 Температура
 Определение относительной плотности мочи Относительную плотность мочи определяют с помощью урометра. Мочи должно быть не менее 40 мл (лучше 60 -100 мл). Если невозможно получить большее количество мочи, относительную плотность находят путем разведения мочи дистиллированной водой в 2 -3 раза и более. При этом две последние цифры полученной плотности умножают на показатель степени разведения мочи. Например, при получении 30 мл мочу разводят дистиллированной водой до 60 мл, т. е. в 2 раза, после чего урометром определяют относительную плотность разведенной мочи. Если она равна 1010, то истинная плотность мочи составит 1020.
Определение относительной плотности мочи Относительную плотность мочи определяют с помощью урометра. Мочи должно быть не менее 40 мл (лучше 60 -100 мл). Если невозможно получить большее количество мочи, относительную плотность находят путем разведения мочи дистиллированной водой в 2 -3 раза и более. При этом две последние цифры полученной плотности умножают на показатель степени разведения мочи. Например, при получении 30 мл мочу разводят дистиллированной водой до 60 мл, т. е. в 2 раза, после чего урометром определяют относительную плотность разведенной мочи. Если она равна 1010, то истинная плотность мочи составит 1020.
 Метод Тода, Санфорда и Уэлльса Удельный вес незначительных количеств мочи (например, несколько капель, полученных катетером) можно определить с помощью смеси жидкостей. В цилиндр наливают смесь хлороформа и бензола и добавляют в нее каплю исследуемой мочи. Если капля идет ко дну, то удельный вес мочи выше удельного веса смеси; если капля остается на поверхности, то ниже. Прибавлением хлороформа (если капля идет ко дну) или бензола (если капля остается на поверхности) регулируют смесь, чтобы капля осталась посередине жидкости. В таком случае удельный вес мочи равен удельному весу смеси, который определяют урометром.
Метод Тода, Санфорда и Уэлльса Удельный вес незначительных количеств мочи (например, несколько капель, полученных катетером) можно определить с помощью смеси жидкостей. В цилиндр наливают смесь хлороформа и бензола и добавляют в нее каплю исследуемой мочи. Если капля идет ко дну, то удельный вес мочи выше удельного веса смеси; если капля остается на поверхности, то ниже. Прибавлением хлороформа (если капля идет ко дну) или бензола (если капля остается на поверхности) регулируют смесь, чтобы капля осталась посередине жидкости. В таком случае удельный вес мочи равен удельному весу смеси, который определяют урометром.
 n Изостенури я (isosthenuria; греч. isos равный, одинаковый + sthenos сила, вес + uron моча) выделение мочи с монотонно низким осмотическим давлением, близким к осмотическому давлению плазмы крови при почечной недостаточности; признак глубокого нарушения почечных процессов концентрирования и разведения мочи; относительная плотность мочи при этом устойчиво снижена до 1010 и не изменяется в зависимости от содержания в пище жидкости и белка n Гипоизостенурия (от греч. hypo - снизу, под, isos - одинаковый, равный, sthenos - сила и uron - моча) - качественное изменение мочи, характеризующееся низким и монотонным в течение суток удельным весом. Развитие гипоизостенурии связано с поражением почечных канальцев и потерей их способности концентрировать клубочковый фильтрат.
n Изостенури я (isosthenuria; греч. isos равный, одинаковый + sthenos сила, вес + uron моча) выделение мочи с монотонно низким осмотическим давлением, близким к осмотическому давлению плазмы крови при почечной недостаточности; признак глубокого нарушения почечных процессов концентрирования и разведения мочи; относительная плотность мочи при этом устойчиво снижена до 1010 и не изменяется в зависимости от содержания в пище жидкости и белка n Гипоизостенурия (от греч. hypo - снизу, под, isos - одинаковый, равный, sthenos - сила и uron - моча) - качественное изменение мочи, характеризующееся низким и монотонным в течение суток удельным весом. Развитие гипоизостенурии связано с поражением почечных канальцев и потерей их способности концентрировать клубочковый фильтрат.
 Химические свойства мочи
Химические свойства мочи
 Белок в моче n Методы определения белка в моче основаны на его коагуляции в объёме мочи или на границе сред (моча и кислота); если есть способ измерить интенсивность коагуляции, то проба – количественная.
Белок в моче n Методы определения белка в моче основаны на его коагуляции в объёме мочи или на границе сред (моча и кислота); если есть способ измерить интенсивность коагуляции, то проба – количественная.
 Унифицированная проба с сульфосалициловой кислотой (1972) n n Реактив. 20% раствор сульфосалициловой кислоты. Ход определения. В 2 пробирки наливают по 3 мл профильтрован-ной мочи. В опытную пробирку добавляют 6 -8 капель реактива. На тёмном фоне сравнивают контрольную пробирку с опытной. Примечание. Если реакция мочи щелочная, то её подкисляют 2 -3 каплями 10% раствора уксусной кислоты.
Унифицированная проба с сульфосалициловой кислотой (1972) n n Реактив. 20% раствор сульфосалициловой кислоты. Ход определения. В 2 пробирки наливают по 3 мл профильтрован-ной мочи. В опытную пробирку добавляют 6 -8 капель реактива. На тёмном фоне сравнивают контрольную пробирку с опытной. Примечание. Если реакция мочи щелочная, то её подкисляют 2 -3 каплями 10% раствора уксусной кислоты.
 Унифицированный метод Брандберга. Робертса-Стольникова(1972) n n n Реактивы. 30% раствор азотной кислоты (относительная плотность 1, 2) или реактив Ларионовой. Реактив Ларионовой: 20 -30 г хлорида натрия растворяют при нагревании в 100 мл дистиллированной воды, остудить, профильтровать. К 99 мл фильтрата прилить 1 мл концентрированной азотной кислоты. Ход определения. В пробирку наливают 1 -2 мл азотной кислоты (или реактива Ларионовой) и осторожно, по стенке пробирки, наслаивают такое же количество профильтрованной мочи. Появление тонкого белого кольца на границе жидкостей на 2 - 3 минуте указывает на наличие белка в концентрации примерно 0, 033 г/л. Если кольцо появляется раньше 2 минут, мочу следует развести водой и провести повторное определение. Степень разведения подбирают в зависимости от вида, ширины, времени появления кольца. Примечание. Иногда белое кольцо получается при наличии больших количеств уратов. Отличие: уратное кольцо появляется немного выше границы между жидкостями и растворяется при лёгком нагревании.
Унифицированный метод Брандберга. Робертса-Стольникова(1972) n n n Реактивы. 30% раствор азотной кислоты (относительная плотность 1, 2) или реактив Ларионовой. Реактив Ларионовой: 20 -30 г хлорида натрия растворяют при нагревании в 100 мл дистиллированной воды, остудить, профильтровать. К 99 мл фильтрата прилить 1 мл концентрированной азотной кислоты. Ход определения. В пробирку наливают 1 -2 мл азотной кислоты (или реактива Ларионовой) и осторожно, по стенке пробирки, наслаивают такое же количество профильтрованной мочи. Появление тонкого белого кольца на границе жидкостей на 2 - 3 минуте указывает на наличие белка в концентрации примерно 0, 033 г/л. Если кольцо появляется раньше 2 минут, мочу следует развести водой и провести повторное определение. Степень разведения подбирают в зависимости от вида, ширины, времени появления кольца. Примечание. Иногда белое кольцо получается при наличии больших количеств уратов. Отличие: уратное кольцо появляется немного выше границы между жидкостями и растворяется при лёгком нагревании.
 Количественное определение белка в моче по помутнению, образующемуся при добавлении сульфосалициловой кислоты (1972) n n n Принцип. Интенсивность помутнения при коагуляции белка сульфосалициловой кислотой пропорциональна его концентрации. Реактивы. 1. 3% раствор сульфосалициловой к-ты. 2. 0, 9% раствор хлорида натрия. 3. Стандартный 1% раствор альбумина. Оборудование: фотоэлектроколориметр. Ход определения. В пробирку вносят 1, 25 мл профильтрованной мочи, доливают до 5 мл 3% раствором сульфосалициловой к-ты, перемешивают. Через 5 мин измеряют на фотоэлектроколори--метре при длине волны 590 -650 нм против контроля в кювете 5 мм. Контролем служит пробирка, в которой к 1, 25 мл мочи долили до 5 мл 0, 9% раствор хлорида натрия. Расчёт ведут по калибровочному графику, для построения которого из стандартного раствора готовят разведения и обрабатывают, как опытные пробы. Примечание. Прямолинейная зависимость при построении графика сохраняется до 1 г/л. При более высоких концентрациях пробу следует разводить и учитывать разведение при расчёте. Ложноположительные результаты могут получиться при наличии в моче контрастных веществ, содержащих органический йод (тест нельзя использовать у лиц, принимающих препараты йода). Ложноположительный тест может быть также приёме сульфа-ниламидных препаратов, больших доз пенициллина, при высоком содержании мочевой кислоты.
Количественное определение белка в моче по помутнению, образующемуся при добавлении сульфосалициловой кислоты (1972) n n n Принцип. Интенсивность помутнения при коагуляции белка сульфосалициловой кислотой пропорциональна его концентрации. Реактивы. 1. 3% раствор сульфосалициловой к-ты. 2. 0, 9% раствор хлорида натрия. 3. Стандартный 1% раствор альбумина. Оборудование: фотоэлектроколориметр. Ход определения. В пробирку вносят 1, 25 мл профильтрованной мочи, доливают до 5 мл 3% раствором сульфосалициловой к-ты, перемешивают. Через 5 мин измеряют на фотоэлектроколори--метре при длине волны 590 -650 нм против контроля в кювете 5 мм. Контролем служит пробирка, в которой к 1, 25 мл мочи долили до 5 мл 0, 9% раствор хлорида натрия. Расчёт ведут по калибровочному графику, для построения которого из стандартного раствора готовят разведения и обрабатывают, как опытные пробы. Примечание. Прямолинейная зависимость при построении графика сохраняется до 1 г/л. При более высоких концентрациях пробу следует разводить и учитывать разведение при расчёте. Ложноположительные результаты могут получиться при наличии в моче контрастных веществ, содержащих органический йод (тест нельзя использовать у лиц, принимающих препараты йода). Ложноположительный тест может быть также приёме сульфа-ниламидных препаратов, больших доз пенициллина, при высоком содержании мочевой кислоты.
 Биуретовый метод n n n Принцип. Пептидные связи белка с солями меди в щелочной среде образуют комплекс фиолетового цвета. Белки предварительно осаждают трихлоруксусной к-той. Реактивы. 1. 10% раствор трихлоруксусной к-ты. 2. 20% раствор Cu. SO 4*5 H 2 O. 3. 3% раствор Na. OH. Ход определения. К 5 мл мочи из суточного количества прибавляют 3 мл раствора трихлоруксусной к-ты, центрифугируют до постоян-ного объёма осадка. Надосадочную жидкость отсасывают пипеткой, осадок растворяют в 5 мл раствора Na. OH. К раствору добавляют 0, 25 мл Cu. SO 4, смесь перемешивают и центрифугируют. Надосадок фотометрируют при длине волны 540 нм в кювете 10 мм против воды. Концентрацию белка рассчитывают по калибровочной кривой. По полученной концентрации рассчитывают суточную потерю белка с мочой.
Биуретовый метод n n n Принцип. Пептидные связи белка с солями меди в щелочной среде образуют комплекс фиолетового цвета. Белки предварительно осаждают трихлоруксусной к-той. Реактивы. 1. 10% раствор трихлоруксусной к-ты. 2. 20% раствор Cu. SO 4*5 H 2 O. 3. 3% раствор Na. OH. Ход определения. К 5 мл мочи из суточного количества прибавляют 3 мл раствора трихлоруксусной к-ты, центрифугируют до постоян-ного объёма осадка. Надосадочную жидкость отсасывают пипеткой, осадок растворяют в 5 мл раствора Na. OH. К раствору добавляют 0, 25 мл Cu. SO 4, смесь перемешивают и центрифугируют. Надосадок фотометрируют при длине волны 540 нм в кювете 10 мм против воды. Концентрацию белка рассчитывают по калибровочной кривой. По полученной концентрации рассчитывают суточную потерю белка с мочой.
 Норма белка в моче n n n Небольшое количество белка в суточной моче обнаруживается у здоровых лиц, но такие концентрации не выявляют в разовых порциях. Приблизительно 70% белков мочи здорового человека приходится на уромукоид – белок, являющийся продуктом почечной ткани. Доля гломерулярного белка в моче здорового человека ничтожно мала. Протеинурия в норме составляет 50 -150 мг/сут. Большинство белков мочи идентично сывороточным.
Норма белка в моче n n n Небольшое количество белка в суточной моче обнаруживается у здоровых лиц, но такие концентрации не выявляют в разовых порциях. Приблизительно 70% белков мочи здорового человека приходится на уромукоид – белок, являющийся продуктом почечной ткани. Доля гломерулярного белка в моче здорового человека ничтожно мала. Протеинурия в норме составляет 50 -150 мг/сут. Большинство белков мочи идентично сывороточным.
 Клиническое значение n n n Принято различать следующие формы протеинурии в зависимости от места возникновения: преренальная – связана с усиленным распадом белка тканей, выраженным гемолизом; ренальная – обусловлена патологией почек, делят на клубочкловую и канальцевую; постренальная – связана с патологией мочевыводящих путей и чаще обусловлена воспалительной экссудацией. В зависимости от длительности выделяют протеинурию постоян-ную, существующую в течение многих недель (лет), и преходящую, появляющуюся периодически, например, при лихорадке и выраженной интоксикации.
Клиническое значение n n n Принято различать следующие формы протеинурии в зависимости от места возникновения: преренальная – связана с усиленным распадом белка тканей, выраженным гемолизом; ренальная – обусловлена патологией почек, делят на клубочкловую и канальцевую; постренальная – связана с патологией мочевыводящих путей и чаще обусловлена воспалительной экссудацией. В зависимости от длительности выделяют протеинурию постоян-ную, существующую в течение многих недель (лет), и преходящую, появляющуюся периодически, например, при лихорадке и выраженной интоксикации.
 Вариабельность протеинурии n n умеренная – при суточной потере белка до 1 г, средняя – при потере от 1 до 3 г, выраженная – при потере более 3 г. Обнаружение в моче белков с большой молекулярной массой свидетельствует об отсутствии избирательного почечного фильтра и выраженном его повреждении. В этих случаях говорят о низкой селективности протеинурии.
Вариабельность протеинурии n n умеренная – при суточной потере белка до 1 г, средняя – при потере от 1 до 3 г, выраженная – при потере более 3 г. Обнаружение в моче белков с большой молекулярной массой свидетельствует об отсутствии избирательного почечного фильтра и выраженном его повреждении. В этих случаях говорят о низкой селективности протеинурии.
 Обнаружение белка Бенс-Джонса n n n Целесообразно проводить только при положительной пробе с сульфосалициловой к-той. Принцип. Реакция термопреципитации. Наиболее достоверно выявление этого парапротеина осаждением при температуре 40 -60 градусов, но и тогда осаждение может не произойти при p. H<3, 0 -3, 5 или p. H>6, 5; при низкой относительной плотности мочи и при низкой концентрации белка Бенс-Джонса. Реактив. 2 М ацетатный буфер р. Н 4, 9. Ход исследования. 4 мл профильтрованной мочи смешивают с 1 мл буфера и согревают 15 мин на водяной бане при температуре 56 градусов. При наличии белка Бенс-Джонса уже в течение 2 мин появляется выраженный осадок, если парапротеина менее 3 г/л проба может быть отрицательной. С полной достоверностью белок Бенс-Джонса может быть обнаружен иммуноэлектрофорезом при использовании специфических сывороток против тяжёлых и лёгких цепей иммуноглобулинов. Клиническое значение. Белок Бенс-Джонса может выделяться при миеломной болезни, при макроглобулинемии Вальдестрема.
Обнаружение белка Бенс-Джонса n n n Целесообразно проводить только при положительной пробе с сульфосалициловой к-той. Принцип. Реакция термопреципитации. Наиболее достоверно выявление этого парапротеина осаждением при температуре 40 -60 градусов, но и тогда осаждение может не произойти при p. H<3, 0 -3, 5 или p. H>6, 5; при низкой относительной плотности мочи и при низкой концентрации белка Бенс-Джонса. Реактив. 2 М ацетатный буфер р. Н 4, 9. Ход исследования. 4 мл профильтрованной мочи смешивают с 1 мл буфера и согревают 15 мин на водяной бане при температуре 56 градусов. При наличии белка Бенс-Джонса уже в течение 2 мин появляется выраженный осадок, если парапротеина менее 3 г/л проба может быть отрицательной. С полной достоверностью белок Бенс-Джонса может быть обнаружен иммуноэлектрофорезом при использовании специфических сывороток против тяжёлых и лёгких цепей иммуноглобулинов. Клиническое значение. Белок Бенс-Джонса может выделяться при миеломной болезни, при макроглобулинемии Вальдестрема.
 Определение глюкозы в моче
Определение глюкозы в моче
 Унифицированный метод определения с помощью индикаторных полосок (1972) n n Ход определения. Бумагу «Глюкотест» погружают в исследуемую мочу так, чтобы полоса с реактивами оказалась смоченной, после этого немедленно извлекают и на 2 мин оставляют на пластмассо-вой пластинке. Сразу через 2 мин сравнивают окраску цветной полосы со шкалой, имеющейся в комплекте. Примечания. 1. Хранить полоски при +8 - +18 гр. Избегать прикосно-вений до реакционной полосы, попадания солнечных лучей. 2. Исследуют свежую мочу. 3. При содержании глюкозы более 20 г/л интенсивность окраски становится предельной - далее не меняется.
Унифицированный метод определения с помощью индикаторных полосок (1972) n n Ход определения. Бумагу «Глюкотест» погружают в исследуемую мочу так, чтобы полоса с реактивами оказалась смоченной, после этого немедленно извлекают и на 2 мин оставляют на пластмассо-вой пластинке. Сразу через 2 мин сравнивают окраску цветной полосы со шкалой, имеющейся в комплекте. Примечания. 1. Хранить полоски при +8 - +18 гр. Избегать прикосно-вений до реакционной полосы, попадания солнечных лучей. 2. Исследуют свежую мочу. 3. При содержании глюкозы более 20 г/л интенсивность окраски становится предельной - далее не меняется.
 Унифицированные методы обнаружения глюкозы в моче. Проба Гайнеса. n n n Принцип. Основан на способности глюкозы восстанавливать в щелочной среде при нагревании гидрат окиси меди (синего цвета) в гидрат закиси меди (жёлтого цвета) и закись меди (красного цвета). Чтобы из гидрата окиси меди при нагревании не образовал-ся чёрный осадок, к реактиву добавляют глицерин, гидроксильные группы которого связывают гидрат окиси меди. Реактивы. Реактив Гайнеса: 1) 13, 3 г кристаллического сульфата меди х. ч. (Cu. SO 4*H 2 O) растворяют в 400 мл дистиллированной воды; 2) 50 г Na. OH растворяют в 400 мл дист. воды; 3) 15 г глицерина ч. д. а. растворяют в 200 мл дист. воды. Смешивают растворы 1 и 2 и тотчас приливают раствор 3. Реактив стоек. Ход определения. К 6 - 8 мл мочи прибавляют 20 капель реактива до появления голубоватой окраски, смешивают и нагревают верхнюю часть пробирки до начала кипения. Нижняя часть пробирки – контроль. При наличии глюкозы в верхней части пробирки появляется жёлтая окраска.
Унифицированные методы обнаружения глюкозы в моче. Проба Гайнеса. n n n Принцип. Основан на способности глюкозы восстанавливать в щелочной среде при нагревании гидрат окиси меди (синего цвета) в гидрат закиси меди (жёлтого цвета) и закись меди (красного цвета). Чтобы из гидрата окиси меди при нагревании не образовал-ся чёрный осадок, к реактиву добавляют глицерин, гидроксильные группы которого связывают гидрат окиси меди. Реактивы. Реактив Гайнеса: 1) 13, 3 г кристаллического сульфата меди х. ч. (Cu. SO 4*H 2 O) растворяют в 400 мл дистиллированной воды; 2) 50 г Na. OH растворяют в 400 мл дист. воды; 3) 15 г глицерина ч. д. а. растворяют в 200 мл дист. воды. Смешивают растворы 1 и 2 и тотчас приливают раствор 3. Реактив стоек. Ход определения. К 6 - 8 мл мочи прибавляют 20 капель реактива до появления голубоватой окраски, смешивают и нагревают верхнюю часть пробирки до начала кипения. Нижняя часть пробирки – контроль. При наличии глюкозы в верхней части пробирки появляется жёлтая окраска.
 Трактовка глюкозы в моче n n n Примечание. При бактериурии глюкоза мочи быстро разлагается. Нормальную концентрацию глюкозы до 0, 2 г/л обычными пробами не обнаруживают. Появление глюкозы в моче может быть результатом физиологической гликемии ( алиментарной, эмоциональной, лекарственной). Клиническое значение. Появление глюкозы в моче зависит от концентрации её в крови, от процесса фильтрации в клубочках (гломерулярных клиренсов) и от реабсорбции глюкозы в канальцах нефрона. Патологические глюкозурии делятся на панкреатогенные и внепанкреатогенные. Важнейшая из панкреатогенных – диабетическая глюкозурия. Внепанкреатические глюкозурии наблюдаются при раздражении ЦНС, гипертиреозе, синдроме Иценко-Кушинга, патологии печени, почек. Для оценки степени глюкозурии необходимо рассчитывать суточную потерю глюкозы с мочей.
Трактовка глюкозы в моче n n n Примечание. При бактериурии глюкоза мочи быстро разлагается. Нормальную концентрацию глюкозы до 0, 2 г/л обычными пробами не обнаруживают. Появление глюкозы в моче может быть результатом физиологической гликемии ( алиментарной, эмоциональной, лекарственной). Клиническое значение. Появление глюкозы в моче зависит от концентрации её в крови, от процесса фильтрации в клубочках (гломерулярных клиренсов) и от реабсорбции глюкозы в канальцах нефрона. Патологические глюкозурии делятся на панкреатогенные и внепанкреатогенные. Важнейшая из панкреатогенных – диабетическая глюкозурия. Внепанкреатические глюкозурии наблюдаются при раздражении ЦНС, гипертиреозе, синдроме Иценко-Кушинга, патологии печени, почек. Для оценки степени глюкозурии необходимо рассчитывать суточную потерю глюкозы с мочей.
 КЕТОНОВЫЕ ТЕЛА. Унифицированная проба Ланге (1979). n n n Принцип. Нитропруссид натрия в щелочной среде реагирует с кетоновыми телами (ацетоуксусной к-той, ацетоном, бетаоксимасляной к-той) с образованием комплекса краснофиолетового цвета. Реактивы. 1. Натрия нитропруссид, раствор 50 г/л, готовят перед употреблением. 2. Уксусная кислота концентрированная. 3. Аммик водный (NH 4 OH) – 25 % раствор. Ход определения. Исследуют мочу в первые 3 ч после мочеиспу-скания. В пробирку к 3– 5 мл мочи приливают 5 - 10 капель раствора натрия нитропруссида и 0, 5 мл уксусной кислоты, смешивают, затем осторожно по стенке пробирки пипеткой наслаивают 2– 3 мл водного раствора аммиака. Пробу считают положительной, если в течение 3 мин на границе сред образуется красно-фиолетовое кольцо.
КЕТОНОВЫЕ ТЕЛА. Унифицированная проба Ланге (1979). n n n Принцип. Нитропруссид натрия в щелочной среде реагирует с кетоновыми телами (ацетоуксусной к-той, ацетоном, бетаоксимасляной к-той) с образованием комплекса краснофиолетового цвета. Реактивы. 1. Натрия нитропруссид, раствор 50 г/л, готовят перед употреблением. 2. Уксусная кислота концентрированная. 3. Аммик водный (NH 4 OH) – 25 % раствор. Ход определения. Исследуют мочу в первые 3 ч после мочеиспу-скания. В пробирку к 3– 5 мл мочи приливают 5 - 10 капель раствора натрия нитропруссида и 0, 5 мл уксусной кислоты, смешивают, затем осторожно по стенке пробирки пипеткой наслаивают 2– 3 мл водного раствора аммиака. Пробу считают положительной, если в течение 3 мин на границе сред образуется красно-фиолетовое кольцо.
 Модифицированная проба Ротеры (1979). n n Реактивы. 1. Натрия нитропруссид, раствор 50 г/л, готовят перед употреблением. 2. Аммония сульфат. 3. Аммиак водный 25 % раствор. Ход определения. Приблизительно 200 мг сухого сульфата аммония, 5 капель мочи и 2 капли раствора натрия нитропруссида тщательно перемешивают в пробирке, затем на эту смесь осторож-но наслаивают 10– 15 капель раствора водного аммика. При наличии кетоновых тел на границе сред в течение 3– 5 мин образуется красно-фиолетовое кольцо, интенсивность окраски которого позволяет ориентировочно судить о концентрации кетоновых тел в моче. При незначительной концентрации кетоно-вых тел слабое кольцо может появиться на 8– 10 минуте.
Модифицированная проба Ротеры (1979). n n Реактивы. 1. Натрия нитропруссид, раствор 50 г/л, готовят перед употреблением. 2. Аммония сульфат. 3. Аммиак водный 25 % раствор. Ход определения. Приблизительно 200 мг сухого сульфата аммония, 5 капель мочи и 2 капли раствора натрия нитропруссида тщательно перемешивают в пробирке, затем на эту смесь осторож-но наслаивают 10– 15 капель раствора водного аммика. При наличии кетоновых тел на границе сред в течение 3– 5 мин образуется красно-фиолетовое кольцо, интенсивность окраски которого позволяет ориентировочно судить о концентрации кетоновых тел в моче. При незначительной концентрации кетоно-вых тел слабое кольцо может появиться на 8– 10 минуте.
 n n Нормальные величины. В норме с мочой выделяется 20– 50 мг кетоновых тел за 24 ч. Клиническое значение. Чаще всего кетонурия наблюдается при диабете, что является критерием правильности подбора пищевого режима: если количество вводимых не соответствует количеству усваиваемых углеводов, то увеличивается выделение кетоновых тел. При уменьшении введения углеводов (лечение без инсулина) при обычном количестве жиров начинает выделяться ацетон; при лечении инсулином уничтожение глюкозурии достигается лучшим усвоением углеводов и не сопровождается кетонурией. Таким образом, обнаружение кетоновых тел в моче больных диабетом необходимо для регулирования диеты.
n n Нормальные величины. В норме с мочой выделяется 20– 50 мг кетоновых тел за 24 ч. Клиническое значение. Чаще всего кетонурия наблюдается при диабете, что является критерием правильности подбора пищевого режима: если количество вводимых не соответствует количеству усваиваемых углеводов, то увеличивается выделение кетоновых тел. При уменьшении введения углеводов (лечение без инсулина) при обычном количестве жиров начинает выделяться ацетон; при лечении инсулином уничтожение глюкозурии достигается лучшим усвоением углеводов и не сопровождается кетонурией. Таким образом, обнаружение кетоновых тел в моче больных диабетом необходимо для регулирования диеты.
 ЖЕЛЧНЫЕ ПИГМЕНТЫ. БИЛИРУБИН n Большинство качественных проб для обнаружения билирубина в моче основано на его превращении под действием окислителя в зелёный биливердин или пурпурно-красные билипурпурины, которые, примешиваясь к биливердину, дают синее окрашивание.
ЖЕЛЧНЫЕ ПИГМЕНТЫ. БИЛИРУБИН n Большинство качественных проб для обнаружения билирубина в моче основано на его превращении под действием окислителя в зелёный биливердин или пурпурно-красные билипурпурины, которые, примешиваясь к биливердину, дают синее окрашивание.
 Унифицированная проба Фуше (1972). n n Реактивы. 1. 15% раствор хлорида бария. 2. Реактив Фуше: 25 г трихлоруксусной к-ты растворяют в 100 мл дист. воды и приливают 10 мл 10% раствора хлорного железа (Fe. Cl 3). Ход определения. К 10 мл мочи прибавляют 5 мл 15% раствора хлорида бария. Смешивают, фильтруют. На вынутый из воронки и расправленный на дне чашки Петри фильтр наносят 2 капли реак-тива Фуше. Появление на фильтре сине-зелёных пятен говорит о присутствии билирубина. Если реакция мочи щелочная, то её необходимо подкислить её несколькими каплями уксусной к-ты.
Унифицированная проба Фуше (1972). n n Реактивы. 1. 15% раствор хлорида бария. 2. Реактив Фуше: 25 г трихлоруксусной к-ты растворяют в 100 мл дист. воды и приливают 10 мл 10% раствора хлорного железа (Fe. Cl 3). Ход определения. К 10 мл мочи прибавляют 5 мл 15% раствора хлорида бария. Смешивают, фильтруют. На вынутый из воронки и расправленный на дне чашки Петри фильтр наносят 2 капли реак-тива Фуше. Появление на фильтре сине-зелёных пятен говорит о присутствии билирубина. Если реакция мочи щелочная, то её необходимо подкислить её несколькими каплями уксусной к-ты.
 Унифицированная проба Розина (1972). n n Реактив: 1% спиртовой раствор йода. Ход определения. В пробирку наливают 4– 5 мл мочи и осторожно по стенке пробирки наслаивают раствор йода. Появление на границе сред зелёного кольца говорит о присутствии билирубина.
Унифицированная проба Розина (1972). n n Реактив: 1% спиртовой раствор йода. Ход определения. В пробирку наливают 4– 5 мл мочи и осторожно по стенке пробирки наслаивают раствор йода. Появление на границе сред зелёного кольца говорит о присутствии билирубина.
 Проба Готфрида. n n n Принцип: билирубина глюкуронид (холебили-рубин) при соединении с диазотированной сульфаниловой к-той даёт розовую окраску за счёт образования билирубина. Реактивы. 1. 10% раствор сульфида бария. 2. Диазореактив: а) диазо-раствор 1: 5 г сульфаниловой к-ты растворяют в небольшом количе-стве воды, прибавляют 15 мл концентрированной HCl и доливают до 1000 мл дист. водой; б) диазораствор 2: 0, 5% раствор нитрата натрия. Непосредственно перед определением смешивают 10 мл диазораствора 1 и 0, 25% диазораствора 2. 3. Спирт этиловый 96%. 4. 6% раствор двузамещённого фосфата натрия. Ход определения. К 10 мл мочи, подкисленной несколькими кап. уксусной к-той, прибавляют 5 мл 10% раствора хлорида бария, перемешивают, фильтруют через бумажный фильтр. Фильтр раскладывают на дне чашки Петри и на осадок, содержащий билирубин, капают 1– 2 капли свежеприготовленной диазосмеси, 4 капли спирта и 1 каплю двузамещённого фосфата натрия. При положительной пробе получается красно-фиолетовая окраска.
Проба Готфрида. n n n Принцип: билирубина глюкуронид (холебили-рубин) при соединении с диазотированной сульфаниловой к-той даёт розовую окраску за счёт образования билирубина. Реактивы. 1. 10% раствор сульфида бария. 2. Диазореактив: а) диазо-раствор 1: 5 г сульфаниловой к-ты растворяют в небольшом количе-стве воды, прибавляют 15 мл концентрированной HCl и доливают до 1000 мл дист. водой; б) диазораствор 2: 0, 5% раствор нитрата натрия. Непосредственно перед определением смешивают 10 мл диазораствора 1 и 0, 25% диазораствора 2. 3. Спирт этиловый 96%. 4. 6% раствор двузамещённого фосфата натрия. Ход определения. К 10 мл мочи, подкисленной несколькими кап. уксусной к-той, прибавляют 5 мл 10% раствора хлорида бария, перемешивают, фильтруют через бумажный фильтр. Фильтр раскладывают на дне чашки Петри и на осадок, содержащий билирубин, капают 1– 2 капли свежеприготовленной диазосмеси, 4 капли спирта и 1 каплю двузамещённого фосфата натрия. При положительной пробе получается красно-фиолетовая окраска.
 n n Нормальные значения. Моча здоровых людей содержит мини-мальные количества билирубина, которые не могут быть обнару-жены качественными пробами, применяемыми в практической медицине. С мочой выделяется только билирубина глюкуронид (прямой билирубин), концентрация которого в норме в крови незначительна. Клиническое значение. Билирубинурию наблюдают при пораже-ниях паренхимы печени (паренхиматозные желтухе) и нарушении оттока желчи (обтурационные желтухи). Для гемолитической желтухи билирубинурия нехарактерна, так как гемобилирубин (непрямой билирубин) не проходит через почечный фильтр.
n n Нормальные значения. Моча здоровых людей содержит мини-мальные количества билирубина, которые не могут быть обнару-жены качественными пробами, применяемыми в практической медицине. С мочой выделяется только билирубина глюкуронид (прямой билирубин), концентрация которого в норме в крови незначительна. Клиническое значение. Билирубинурию наблюдают при пораже-ниях паренхимы печени (паренхиматозные желтухе) и нарушении оттока желчи (обтурационные желтухи). Для гемолитической желтухи билирубинурия нехарактерна, так как гемобилирубин (непрямой билирубин) не проходит через почечный фильтр.
 УРОБИЛИНОИДЫ. Унифицированная проба Флоранса (1979). n n n Принцип. С HCl уробилин образует соединение, окрашенное в красный цвет. Реактивы. 1. Серная к-та концентр. 2. Диэтиловый эфир. 3. Соляная к-та концентр. Ход определения. В пробирке 8– 10 мл мочи подкисляют 8– 10 кап. серной концентр. к-ты, перемешивают, затем приливают 2– 3 мл эфира. Закрыв пробирку пробкой, несколько раз осторожно пропускают эфир через слой мочи для экстрагирования уробилина. Затем эфирную вытяжку мочи наслаивают, лучше пастеровской пипеткой, на 2– 3 мл концентр. к-ты, налитой в другую пробирку. При наличии уробилина на границе жидкостей образуется розовое кольцо. Интенсивность окраски пропорциональна количеству уробилина. Оценка результата. Проба настолько чувствительна, что даже в норме на границе между двумя жидкостями видно лёгкое розовое окрашивание. Этой пробой можно установить полное отсутстствие уробилинов в моче.
УРОБИЛИНОИДЫ. Унифицированная проба Флоранса (1979). n n n Принцип. С HCl уробилин образует соединение, окрашенное в красный цвет. Реактивы. 1. Серная к-та концентр. 2. Диэтиловый эфир. 3. Соляная к-та концентр. Ход определения. В пробирке 8– 10 мл мочи подкисляют 8– 10 кап. серной концентр. к-ты, перемешивают, затем приливают 2– 3 мл эфира. Закрыв пробирку пробкой, несколько раз осторожно пропускают эфир через слой мочи для экстрагирования уробилина. Затем эфирную вытяжку мочи наслаивают, лучше пастеровской пипеткой, на 2– 3 мл концентр. к-ты, налитой в другую пробирку. При наличии уробилина на границе жидкостей образуется розовое кольцо. Интенсивность окраски пропорциональна количеству уробилина. Оценка результата. Проба настолько чувствительна, что даже в норме на границе между двумя жидкостями видно лёгкое розовое окрашивание. Этой пробой можно установить полное отсутстствие уробилинов в моче.
 Унифицированный метод с парадиметиламинобензальдегидом (1979). n n Принцип. Уробилиноген с парадиметиламинобензальде-гидом образует комплекс, окрашенный в красный цвет; интенсив-ность окраски пропорциональна содержанию уробилиногена. Для восстановле-ния уробилина в уробилиноген используют аскорбиновую к-ту и гидрат окиси железа. Для увеличения специфичности реакции добавляют ацетат натрия. Реактивы. 1. Диметиламинобензальдегид. 2. НСl концентр. х. ч. 3. Реактив Эрлиха; 0, 7 г пара-диметиламинобензальдегида раство-ряют в 150 мл концентр. НСl, приливают к 100 мл дистил. воды и смешивают. Раствор должен быть бесцветным или слегка желто-ватым. Реактив стабилен, хранят в посуде из тёмного стекла. 4. Натрия ацетат ч. д. а. , х. ч. , насыщенный раствор: 375 г СН 3 СООNa*3 H 2 O растворяют в 250 мл тёплой дистилл. охлаждают до комнатной температуры. Хранят при температуре 20 градусов. Раствор должен быть бесцветным или прозрачным. 5. Аскорбиновая к-та. 6. Бария хлорид, раствор 100 г/л. 8. Фенолсуль-фофталеин (феноловый красный). Используют для приготовления калибровочного раствора. 9. Основной калибровочный раствор: 20 мг фенолсульфофталеина растворяют в 100 мл 0, 5 г/л раствора ед-кого натра. Стабилен. Рабочий калибровочный раствор готовят разведением основного раствора 0, 5 г/л раствором едкого натра в 100 раз. Стабилен в течении недели при 20 градусах. Рабочий раствор содержит 0, 2 мг фенолсульфофталеина в 100 мл и эквивалентен по окраске раствору уробилиногена – 0, 345 мг/100 мл. Точность приго-товления можно проверить на спектрофотометре: при длине волны 542 нм оптическая плотность раствора должна быть 0, 38 – 0, 39.
Унифицированный метод с парадиметиламинобензальдегидом (1979). n n Принцип. Уробилиноген с парадиметиламинобензальде-гидом образует комплекс, окрашенный в красный цвет; интенсив-ность окраски пропорциональна содержанию уробилиногена. Для восстановле-ния уробилина в уробилиноген используют аскорбиновую к-ту и гидрат окиси железа. Для увеличения специфичности реакции добавляют ацетат натрия. Реактивы. 1. Диметиламинобензальдегид. 2. НСl концентр. х. ч. 3. Реактив Эрлиха; 0, 7 г пара-диметиламинобензальдегида раство-ряют в 150 мл концентр. НСl, приливают к 100 мл дистил. воды и смешивают. Раствор должен быть бесцветным или слегка желто-ватым. Реактив стабилен, хранят в посуде из тёмного стекла. 4. Натрия ацетат ч. д. а. , х. ч. , насыщенный раствор: 375 г СН 3 СООNa*3 H 2 O растворяют в 250 мл тёплой дистилл. охлаждают до комнатной температуры. Хранят при температуре 20 градусов. Раствор должен быть бесцветным или прозрачным. 5. Аскорбиновая к-та. 6. Бария хлорид, раствор 100 г/л. 8. Фенолсуль-фофталеин (феноловый красный). Используют для приготовления калибровочного раствора. 9. Основной калибровочный раствор: 20 мг фенолсульфофталеина растворяют в 100 мл 0, 5 г/л раствора ед-кого натра. Стабилен. Рабочий калибровочный раствор готовят разведением основного раствора 0, 5 г/л раствором едкого натра в 100 раз. Стабилен в течении недели при 20 градусах. Рабочий раствор содержит 0, 2 мг фенолсульфофталеина в 100 мл и эквивалентен по окраске раствору уробилиногена – 0, 345 мг/100 мл. Точность приго-товления можно проверить на спектрофотометре: при длине волны 542 нм оптическая плотность раствора должна быть 0, 38 – 0, 39.
 n n Специальное оборудование. ФЭК или спектрофотометр. Подготовка образца. Исследование проводят в первые 2– 3 ч после мочеиспускания. При наличии мутности мочу фильтруют, затем проводят качественное определение билирубина. Если его обнаруживают, то 8 мл мочи смешивают с 2 мл 100 г/л раствора хлорида бария и фильтруют через бумажный фильтр. Конечный результат умножают на 1, 25 (поправка на разведение). Ход определения. 100 мг аскорбиновой к-ты растворяют в 10 мл исследуемой мочи и помещают по 1, 5 мл в 2 пробирки для опытной и холостой пробы В пробирку с холостой пробой приливают 4, 5 мл свежеприготовленной смеси 1 объёма раствора Эрлиха и двух объёмов насыщенного раствора ацетата натрия. В пробирку с опыт -ной пробой прибавляют 1, 5 мл раствора Эрлиха и немедленно при -ливают 3 мл насыщенного раствора ацетата натрия. Через 5 мин измеряют экстинкцию обеих проб против воды на ФЭК при длине волны 500– 590 нм в кювете 1 см; на спектрофотометре при 562 нм. Рабочий калибровочный раствор измеряют при тех же условиях, что опытную пробу. Примечания. 1. Рекомендуется собирать мочу в посуду из тёмного стекла, так как при дневном свете окисление уробилиногена происходит значительно быстрее. 2. Для расчёта выделения уробилиногена за определённое время для исследования надо брать мочу из всего собранного за это время объёма.
n n Специальное оборудование. ФЭК или спектрофотометр. Подготовка образца. Исследование проводят в первые 2– 3 ч после мочеиспускания. При наличии мутности мочу фильтруют, затем проводят качественное определение билирубина. Если его обнаруживают, то 8 мл мочи смешивают с 2 мл 100 г/л раствора хлорида бария и фильтруют через бумажный фильтр. Конечный результат умножают на 1, 25 (поправка на разведение). Ход определения. 100 мг аскорбиновой к-ты растворяют в 10 мл исследуемой мочи и помещают по 1, 5 мл в 2 пробирки для опытной и холостой пробы В пробирку с холостой пробой приливают 4, 5 мл свежеприготовленной смеси 1 объёма раствора Эрлиха и двух объёмов насыщенного раствора ацетата натрия. В пробирку с опыт -ной пробой прибавляют 1, 5 мл раствора Эрлиха и немедленно при -ливают 3 мл насыщенного раствора ацетата натрия. Через 5 мин измеряют экстинкцию обеих проб против воды на ФЭК при длине волны 500– 590 нм в кювете 1 см; на спектрофотометре при 562 нм. Рабочий калибровочный раствор измеряют при тех же условиях, что опытную пробу. Примечания. 1. Рекомендуется собирать мочу в посуду из тёмного стекла, так как при дневном свете окисление уробилиногена происходит значительно быстрее. 2. Для расчёта выделения уробилиногена за определённое время для исследования надо брать мочу из всего собранного за это время объёма.
 n n Нормальные величины. В моче здорового человека содержаться следы уробилиногена, а за сутки выделяются не больше 6 мг, у детей – не более 2 мг. Клиническое значение. В свежевыпущенной моче содержится уро-билиноген, который при стоянии окисляется в уробилины. Все эти вещества являются производными билирубина и называются уро-билиноидами. Уробилиноиды образуются под действием фермен-тов бактерий и клеток слизистой оболочки кишечника из билируби-на, выделившегося с желчью. Уробилиноидурия является одним из характерных симптомов поражения паренхимы печени (гепатиты, циррозы), гемолитических состояний и заболеваний кишечника (энтериты, наклонность к запорам, кишечная непроходимость). Полное отсутствие уробилиноидов говорит о полном нарушении поступления желчи в кишечник.
n n Нормальные величины. В моче здорового человека содержаться следы уробилиногена, а за сутки выделяются не больше 6 мг, у детей – не более 2 мг. Клиническое значение. В свежевыпущенной моче содержится уро-билиноген, который при стоянии окисляется в уробилины. Все эти вещества являются производными билирубина и называются уро-билиноидами. Уробилиноиды образуются под действием фермен-тов бактерий и клеток слизистой оболочки кишечника из билируби-на, выделившегося с желчью. Уробилиноидурия является одним из характерных симптомов поражения паренхимы печени (гепатиты, циррозы), гемолитических состояний и заболеваний кишечника (энтериты, наклонность к запорам, кишечная непроходимость). Полное отсутствие уробилиноидов говорит о полном нарушении поступления желчи в кишечник.
 Определение кальция (проба Сулковича). n n n Принцип. Ионы кальция с щавелевой к-той образуют нерастворимую щавелевокислую соль. Реактивы. 1. Щавеливая к-та. 2. Аммония оксалат. 3. Уксусная к-та ледяная. 4. Реактив Сулковича: в 50 мл дистиллированной воды растворяют по 2, 5 мл щавелевой к-ты и оксалата аммония, добавляют 5 мл ледяной уксусной к-ты и доводят объём до 150 мл. Ход определения. Смешивают по 2, 5 мл мочи и реактива Сулковича. Через 1– 2 мин оценивают степень помутнения. Оценка результатов. Степень помутнения оценивают визуально: 1 – слабое, 2 – умеренное, 3 – значительное, 4 – значительное помут -нение. О повышенном содержании кальция в моче свидетельствует 3 -я и 4 -я степень помутнения. Клиническое значение. Высокое содержание кальция в моче может быть при гипервитаминозе D и гиперпаратиреозе. После выявления положительных результатов описанных выше тестов больной ребёнок нуждается в тщательном обследовании с помощью точных количественных методов (аминокислотный анализатор, высоковольтный электрофорез с последующей хроматографией на бумаге, исследование гормонального профиля и др. ) в специализированных учреждениях.
Определение кальция (проба Сулковича). n n n Принцип. Ионы кальция с щавелевой к-той образуют нерастворимую щавелевокислую соль. Реактивы. 1. Щавеливая к-та. 2. Аммония оксалат. 3. Уксусная к-та ледяная. 4. Реактив Сулковича: в 50 мл дистиллированной воды растворяют по 2, 5 мл щавелевой к-ты и оксалата аммония, добавляют 5 мл ледяной уксусной к-ты и доводят объём до 150 мл. Ход определения. Смешивают по 2, 5 мл мочи и реактива Сулковича. Через 1– 2 мин оценивают степень помутнения. Оценка результатов. Степень помутнения оценивают визуально: 1 – слабое, 2 – умеренное, 3 – значительное, 4 – значительное помут -нение. О повышенном содержании кальция в моче свидетельствует 3 -я и 4 -я степень помутнения. Клиническое значение. Высокое содержание кальция в моче может быть при гипервитаминозе D и гиперпаратиреозе. После выявления положительных результатов описанных выше тестов больной ребёнок нуждается в тщательном обследовании с помощью точных количественных методов (аминокислотный анализатор, высоковольтный электрофорез с последующей хроматографией на бумаге, исследование гормонального профиля и др. ) в специализированных учреждениях.
 БЛАГОДАРЮ ЗА ВНИМАНИЕ!
БЛАГОДАРЮ ЗА ВНИМАНИЕ!


