02 БФ Аминокислоты.Заряд.ppt
- Количество слайдов: 14
 Физико-химические свойства аминокислот и пептидов Часть 1. Заряды © 2012 Ю. А. Владимиров (ФФМ МГУ)
Физико-химические свойства аминокислот и пептидов Часть 1. Заряды © 2012 Ю. А. Владимиров (ФФМ МГУ)
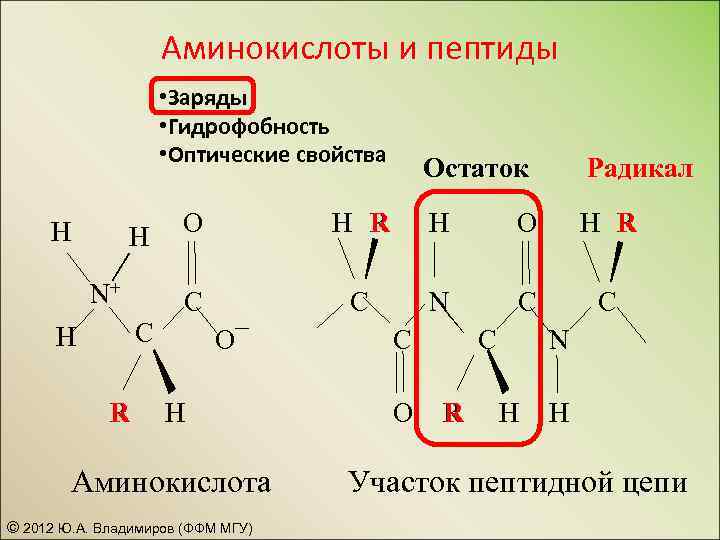 Аминокислоты и пептиды • Заряды • Гидрофобность • Оптические свойства H H N+ C H R Остаток Радикал O H R H O H R C C N C C O¯ O H Аминокислота © 2012 Ю. А. Владимиров (ФФМ МГУ) C O C R N H H Участок пептидной цепи
Аминокислоты и пептиды • Заряды • Гидрофобность • Оптические свойства H H N+ C H R Остаток Радикал O H R H O H R C C N C C O¯ O H Аминокислота © 2012 Ю. А. Владимиров (ФФМ МГУ) C O C R N H H Участок пептидной цепи
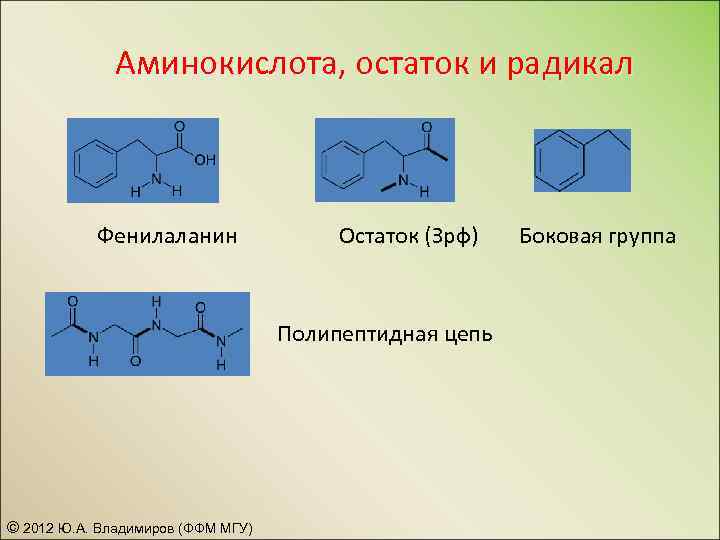 Аминокислота, остаток и радикал Фенилаланин Остаток (Зрф) Полипептидная цепь © 2012 Ю. А. Владимиров (ФФМ МГУ) Боковая группа
Аминокислота, остаток и радикал Фенилаланин Остаток (Зрф) Полипептидная цепь © 2012 Ю. А. Владимиров (ФФМ МГУ) Боковая группа
 Таб. 02. Скелетные структуры аминокислотных остатков Неполярные Полярные Ala Asn Cys* Gln Gly Ser Ile Pro*** Leu Thr Pro Заряженные Phe Asp Trp** Arg Тyr* Glu Met** Lys Промежуточный His © 2012 Ю. А. Владимиров (ФФМ МГУ)
Таб. 02. Скелетные структуры аминокислотных остатков Неполярные Полярные Ala Asn Cys* Gln Gly Ser Ile Pro*** Leu Thr Pro Заряженные Phe Asp Trp** Arg Тyr* Glu Met** Lys Промежуточный His © 2012 Ю. А. Владимиров (ФФМ МГУ)
 Последовательность аминокислотных остатков цитохрома с Последовательность аминокислот в полипептидной цепи данного белка называется его первичной структурой. Например, первичная структура цитохрома с выглядит следующим образом (читаем строчка за строчкой сверху вниз). Найти первичную структуру белка можно в его молекулярном файле в белковой базе данных PDB. © 2012 Ю. А. Владимиров (ФФМ МГУ)
Последовательность аминокислотных остатков цитохрома с Последовательность аминокислот в полипептидной цепи данного белка называется его первичной структурой. Например, первичная структура цитохрома с выглядит следующим образом (читаем строчка за строчкой сверху вниз). Найти первичную структуру белка можно в его молекулярном файле в белковой базе данных PDB. © 2012 Ю. А. Владимиров (ФФМ МГУ)
 Свойства аминокислотных остатков • Заряды • Гидрофобность • Оптические свойства При включении в полипептидную цепь заряды аминной и карбоксильной группы исчезают, и аминокислотные остатки имеют заряд, которым обладают боковые группы R. Заряд могут иметь лишь те боковые группы, которые способны при определенной величине р. Н присоединять протон (и приобретать положительный заряд) или терять его (приобретая отрицательный заряд). © 2012 Ю. А. Владимиров (ФФМ МГУ)
Свойства аминокислотных остатков • Заряды • Гидрофобность • Оптические свойства При включении в полипептидную цепь заряды аминной и карбоксильной группы исчезают, и аминокислотные остатки имеют заряд, которым обладают боковые группы R. Заряд могут иметь лишь те боковые группы, которые способны при определенной величине р. Н присоединять протон (и приобретать положительный заряд) или терять его (приобретая отрицательный заряд). © 2012 Ю. А. Владимиров (ФФМ МГУ)
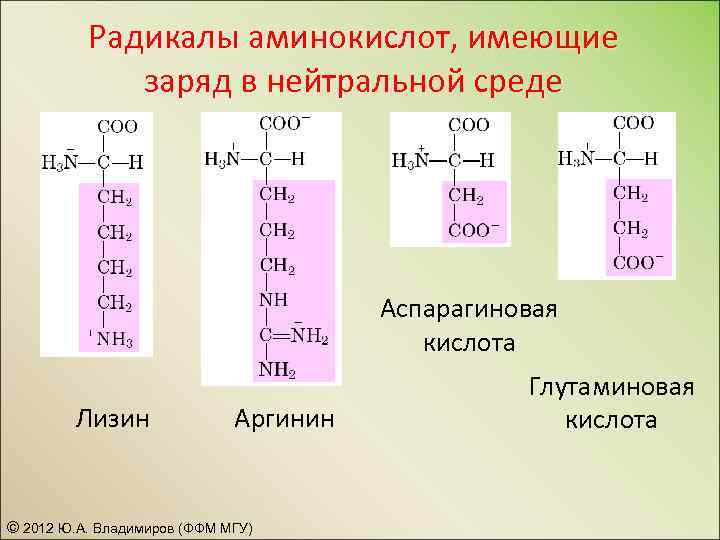 Радикалы аминокислот, имеющие заряд в нейтральной среде Аспарагиновая кислота Лизин Аргинин © 2012 Ю. А. Владимиров (ФФМ МГУ) Глутаминовая кислота
Радикалы аминокислот, имеющие заряд в нейтральной среде Аспарагиновая кислота Лизин Аргинин © 2012 Ю. А. Владимиров (ФФМ МГУ) Глутаминовая кислота
 Константа диссоциации Реакция ионизации HA H+ + A¯ характеризуется константой диссоциации Введем величину р. Kа по тому же уравнению, по которому вводилось понятие р. Н: р. Н При р. Н = р. Ка , [Н+] = [НА] Т. е. кислота ионизована наполовину. © 2012 Ю. А. Владимиров (ФФМ МГУ)
Константа диссоциации Реакция ионизации HA H+ + A¯ характеризуется константой диссоциации Введем величину р. Kа по тому же уравнению, по которому вводилось понятие р. Н: р. Н При р. Н = р. Ка , [Н+] = [НА] Т. е. кислота ионизована наполовину. © 2012 Ю. А. Владимиров (ФФМ МГУ)
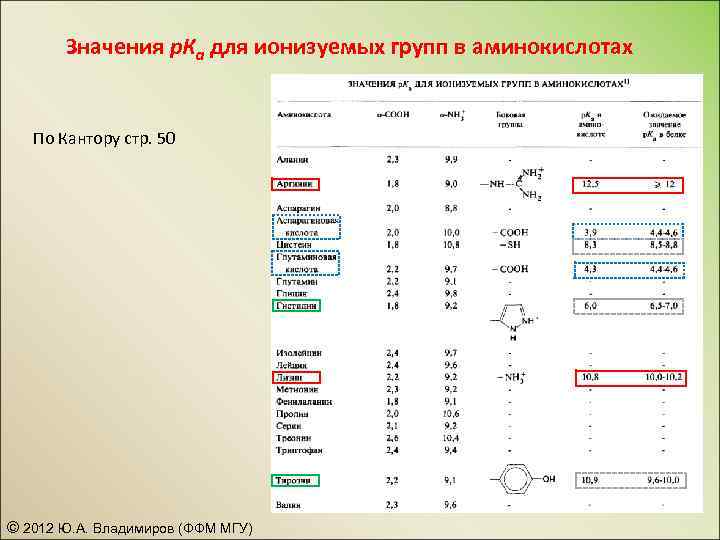 Значения р. Ка для ионизуемых групп в аминокислотах По Кантору стр. 50 © 2012 Ю. А. Владимиров (ФФМ МГУ)
Значения р. Ка для ионизуемых групп в аминокислотах По Кантору стр. 50 © 2012 Ю. А. Владимиров (ФФМ МГУ)
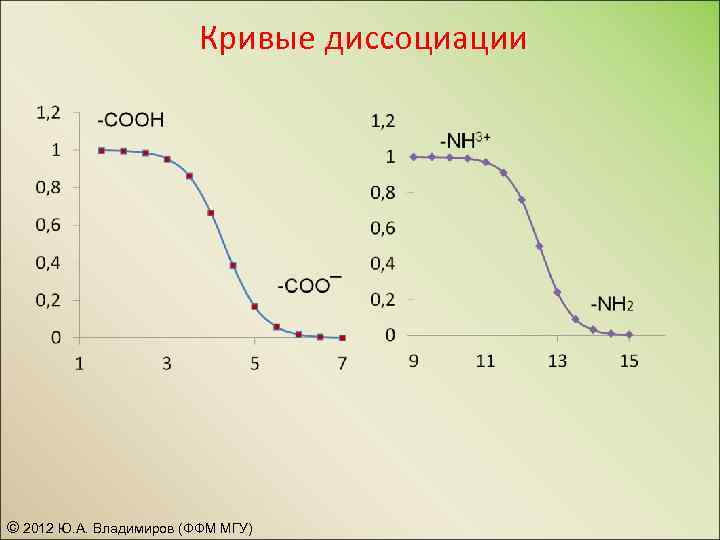 Кривые диссоциации © 2012 Ю. А. Владимиров (ФФМ МГУ)
Кривые диссоциации © 2012 Ю. А. Владимиров (ФФМ МГУ)
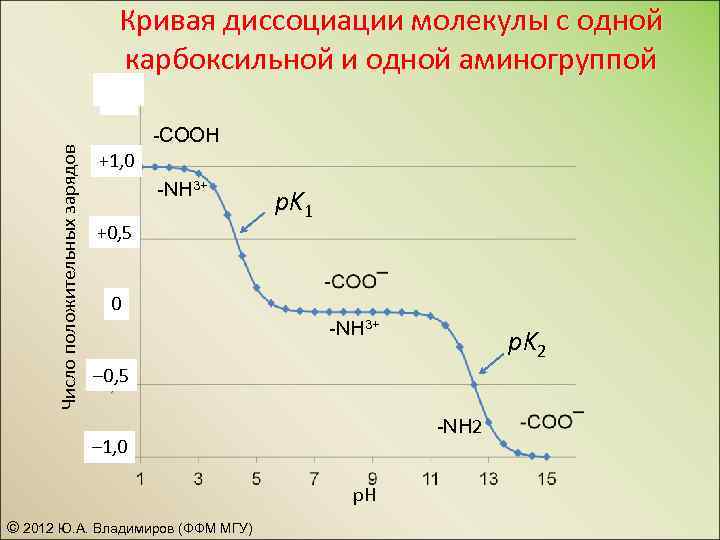 Кривая диссоциации молекулы с одной карбоксильной и одной аминогруппой Число положительных зарядов – 1, 0 -COOH +1, 0 -NH 3+ +0, 5 p. K 1 0 -NH 3+ p. K 2 – 0, 5 -NH 2 – 1, 0 p. H © 2012 Ю. А. Владимиров (ФФМ МГУ)
Кривая диссоциации молекулы с одной карбоксильной и одной аминогруппой Число положительных зарядов – 1, 0 -COOH +1, 0 -NH 3+ +0, 5 p. K 1 0 -NH 3+ p. K 2 – 0, 5 -NH 2 – 1, 0 p. H © 2012 Ю. А. Владимиров (ФФМ МГУ)
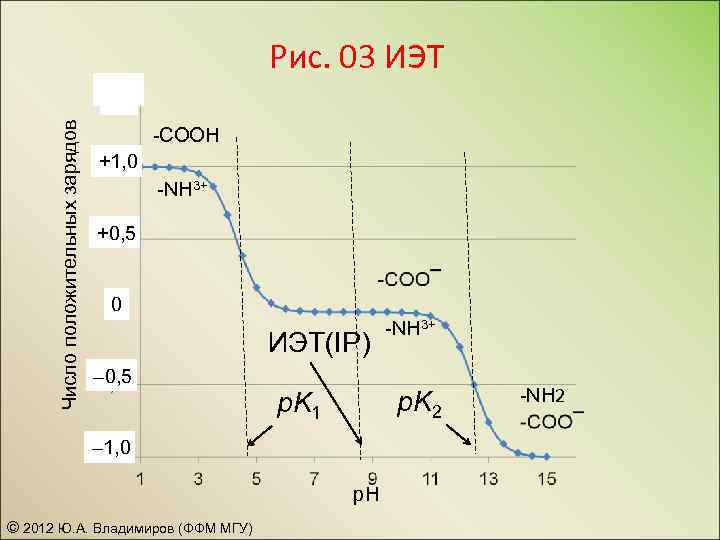 Рис. 03 ИЭТ Число положительных зарядов – 1, 0 -COOH +1, 0 -NH 3+ +0, 5 0 ИЭТ(IP) – 0, 5 p. K 2 p. K 1 – 1, 0 p. H © 2012 Ю. А. Владимиров (ФФМ МГУ) -NH 3+ -NH 2
Рис. 03 ИЭТ Число положительных зарядов – 1, 0 -COOH +1, 0 -NH 3+ +0, 5 0 ИЭТ(IP) – 0, 5 p. K 2 p. K 1 – 1, 0 p. H © 2012 Ю. А. Владимиров (ФФМ МГУ) -NH 3+ -NH 2
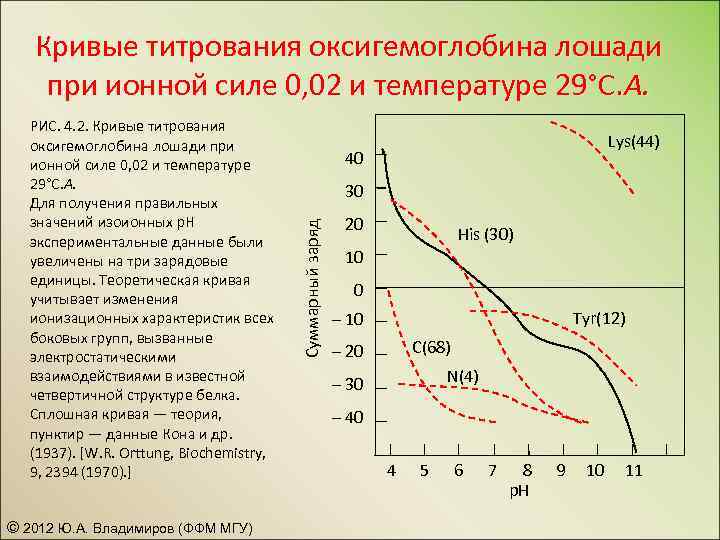 Кривые титрования оксигемоглобина лошади при ионной силе 0, 02 и температуре 29°С. А. © 2012 Ю. А. Владимиров (ФФМ МГУ) Lys(44) 40 30 Суммарный заряд РИС. 4. 2. Кривые титрования оксигемоглобина лошади при ионной силе 0, 02 и температуре 29°С. А. Для получения правильных значений изоионных р. Н экспериментальные данные были увеличены на три зарядовые единицы. Теоретическая кривая учитывает изменения ионизационных характеристик всех боковых групп, вызванные электростатическими взаимодействиями в известной четвертичной структуре белка. Сплошная кривая — теория, пунктир — данные Кона и др. (1937). [W. R. Orttung, Biochemistry, 9, 2394 (1970). ] 20 His (30) 10 0 Tyr(12) – 10 С(68) – 20 N(4) – 30 – 40 4 5 6 7 8 р. Н 9 10 11
Кривые титрования оксигемоглобина лошади при ионной силе 0, 02 и температуре 29°С. А. © 2012 Ю. А. Владимиров (ФФМ МГУ) Lys(44) 40 30 Суммарный заряд РИС. 4. 2. Кривые титрования оксигемоглобина лошади при ионной силе 0, 02 и температуре 29°С. А. Для получения правильных значений изоионных р. Н экспериментальные данные были увеличены на три зарядовые единицы. Теоретическая кривая учитывает изменения ионизационных характеристик всех боковых групп, вызванные электростатическими взаимодействиями в известной четвертичной структуре белка. Сплошная кривая — теория, пунктир — данные Кона и др. (1937). [W. R. Orttung, Biochemistry, 9, 2394 (1970). ] 20 His (30) 10 0 Tyr(12) – 10 С(68) – 20 N(4) – 30 – 40 4 5 6 7 8 р. Н 9 10 11
 Вопросы для зачета 1. Нарисуйте химическую структуру участка полипептидной цепи. Укажите основные группы полипептидной цепи (пептидная связь, Nконец и т. д. ) 2. Название и свойства заряженных аминокислотных остатков. Химические формулы или основные функциональные группы положительно и отрицательно заряженных остатков 3. Что такое константа диссоциации кислоты? p. H и p. K. 4. Нарисуйте и объясните кривую диссоциации аминокислоты в водном растворе 5. Что такое кривая диссоциации белка. Изоэлектрическая точка. © 2012 Ю. А. Владимиров (ФФМ МГУ)
Вопросы для зачета 1. Нарисуйте химическую структуру участка полипептидной цепи. Укажите основные группы полипептидной цепи (пептидная связь, Nконец и т. д. ) 2. Название и свойства заряженных аминокислотных остатков. Химические формулы или основные функциональные группы положительно и отрицательно заряженных остатков 3. Что такое константа диссоциации кислоты? p. H и p. K. 4. Нарисуйте и объясните кривую диссоциации аминокислоты в водном растворе 5. Что такое кривая диссоциации белка. Изоэлектрическая точка. © 2012 Ю. А. Владимиров (ФФМ МГУ)


