Физико-химические свойства аминокислот.ppt
- Количество слайдов: 21
 Физико-химические свойства аминокислот Гомельский государственный медицинский университет Кафедра биохимии Доцент, к. б. н. А. Н. Коваль А. Н. , 2006 (C)
Физико-химические свойства аминокислот Гомельский государственный медицинский университет Кафедра биохимии Доцент, к. б. н. А. Н. Коваль А. Н. , 2006 (C)
 Общие свойства Аминокислоты (АК) обычно содержат 1. 2. 3. 4. 5. 6. 2/17/2018 карбоксильную группу (COOH), аминогруппу (NH 2), боковой радикал, Эти группы соединены с атомом углерода в αположении. Природные АК обычно L-конфигурации. При физиологических p. H NH 2 -группы АК заряжены «+» , COOH-группы – «-» , Боковые радикалы содержат различные химические группы. Между собой АМК соединены пептидными связями. Коваль А. Н. , 2006 (C) 2
Общие свойства Аминокислоты (АК) обычно содержат 1. 2. 3. 4. 5. 6. 2/17/2018 карбоксильную группу (COOH), аминогруппу (NH 2), боковой радикал, Эти группы соединены с атомом углерода в αположении. Природные АК обычно L-конфигурации. При физиологических p. H NH 2 -группы АК заряжены «+» , COOH-группы – «-» , Боковые радикалы содержат различные химические группы. Между собой АМК соединены пептидными связями. Коваль А. Н. , 2006 (C) 2
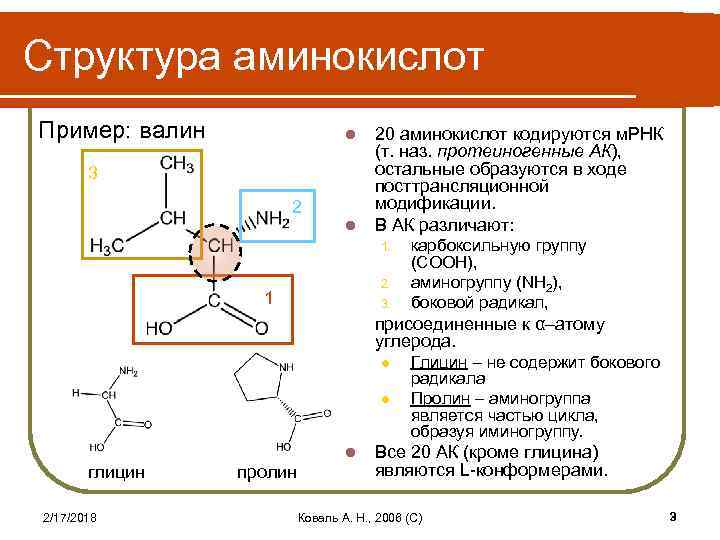 Структура аминокислот Пример: валин l 3 2 l 20 аминокислот кодируются м. РНК (т. наз. протеиногенные АК), остальные образуются в ходе посттрансляционной модификации. В АК различают: 1. 2. 1 3. карбоксильную группу (COOH), аминогруппу (NH 2), боковой радикал, присоединенные к α–атому углерода. l l l глицин 2/17/2018 пролин Глицин – не содержит бокового радикала Пролин – аминогруппа является частью цикла, образуя иминогруппу. Все 20 АК (кроме глицина) являются L-конформерами. Коваль А. Н. , 2006 (C) 3
Структура аминокислот Пример: валин l 3 2 l 20 аминокислот кодируются м. РНК (т. наз. протеиногенные АК), остальные образуются в ходе посттрансляционной модификации. В АК различают: 1. 2. 1 3. карбоксильную группу (COOH), аминогруппу (NH 2), боковой радикал, присоединенные к α–атому углерода. l l l глицин 2/17/2018 пролин Глицин – не содержит бокового радикала Пролин – аминогруппа является частью цикла, образуя иминогруппу. Все 20 АК (кроме глицина) являются L-конформерами. Коваль А. Н. , 2006 (C) 3
 Классификация аминокислот l По боковому радикалу: 1. Гидрофобные АК – способны к гидрофобным взаимодействиям 1. 2. 3. Содержащие гидроксильные группы (серин и треонин) – могут образовывать водородные связи Серосодержащие (цистеин и метионин) 1. 4. 5. 6. 2/17/2018 Алифатические группы (валин, лейцин и изолейцин); Ароматические группы (фенилаланин, тирозин и триптофан). Сульфгидрильные (-SH) группы 2 -х цистеинов могут образовать дисульфидную связь. Ионизирующиеся группы – у 7 АК. В зависимости от p. H могут нести заряды. В таком виде способны к электростатическим взаимодействиям Амиды – у аспарагина и глутамина. Боковой радикал пролина образует кольцо с азотом, присоединенным к α–атому. Коваль А. Н. , 2006 (C) 4
Классификация аминокислот l По боковому радикалу: 1. Гидрофобные АК – способны к гидрофобным взаимодействиям 1. 2. 3. Содержащие гидроксильные группы (серин и треонин) – могут образовывать водородные связи Серосодержащие (цистеин и метионин) 1. 4. 5. 6. 2/17/2018 Алифатические группы (валин, лейцин и изолейцин); Ароматические группы (фенилаланин, тирозин и триптофан). Сульфгидрильные (-SH) группы 2 -х цистеинов могут образовать дисульфидную связь. Ионизирующиеся группы – у 7 АК. В зависимости от p. H могут нести заряды. В таком виде способны к электростатическим взаимодействиям Амиды – у аспарагина и глутамина. Боковой радикал пролина образует кольцо с азотом, присоединенным к α–атому. Коваль А. Н. , 2006 (C) 4
 Заряды аминокислот l Заряды α–аминогрупп и α– карбоксильных групп l Заряды боковых радикалов Положительные l Отрицательные l l Изоэлектрическая 2/17/2018 точка (p. I) Коваль А. Н. , 2006 (C) 5
Заряды аминокислот l Заряды α–аминогрупп и α– карбоксильных групп l Заряды боковых радикалов Положительные l Отрицательные l l Изоэлектрическая 2/17/2018 точка (p. I) Коваль А. Н. , 2006 (C) 5
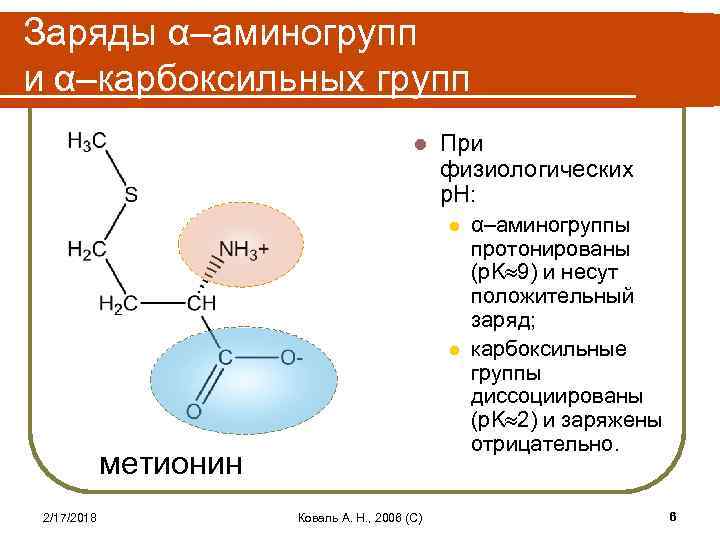 Заряды α–аминогрупп и α–карбоксильных групп l При физиологических p. H: l l метионин 2/17/2018 Коваль А. Н. , 2006 (C) α–аминогруппы протонированы (p. K 9) и несут положительный заряд; карбоксильные группы диссоциированы (p. K 2) и заряжены отрицательно. 6
Заряды α–аминогрупп и α–карбоксильных групп l При физиологических p. H: l l метионин 2/17/2018 Коваль А. Н. , 2006 (C) α–аминогруппы протонированы (p. K 9) и несут положительный заряд; карбоксильные группы диссоциированы (p. K 2) и заряжены отрицательно. 6
 Заряды боковых радикалов l Положительные l заряды Боковые радикалы основных аминокислот – аргинина, лизина и гистидина заряжены положительно при p. H 7. Для гуанидиновой группы аргинина p. K=12. 5 l ε-аминогруппа лизина имеет p. K=10. 5 l Имидазольная группа гистидина – p. K=6. 5 l 2/17/2018 Коваль А. Н. , 2006 (C) 7
Заряды боковых радикалов l Положительные l заряды Боковые радикалы основных аминокислот – аргинина, лизина и гистидина заряжены положительно при p. H 7. Для гуанидиновой группы аргинина p. K=12. 5 l ε-аминогруппа лизина имеет p. K=10. 5 l Имидазольная группа гистидина – p. K=6. 5 l 2/17/2018 Коваль А. Н. , 2006 (C) 7
 Заряды боковых радикалов l Отрицательные заряды l l 2/17/2018 Боковые радикалы кислых АК - аспарагиновой и глутаминовой кислот (аспартата и глутамата) несут отрицательный заряд при p. H 7 (p. Kасп = 3, 9, p. Kглу = 4, 1); Тирозин (p. K=10, 1) и цистеин (p. K=8, 2) могут отдавать протоны и заряжаться отрицательно при повышении кислотности (не при физиологических p. H). Коваль А. Н. , 2006 (C) 8
Заряды боковых радикалов l Отрицательные заряды l l 2/17/2018 Боковые радикалы кислых АК - аспарагиновой и глутаминовой кислот (аспартата и глутамата) несут отрицательный заряд при p. H 7 (p. Kасп = 3, 9, p. Kглу = 4, 1); Тирозин (p. K=10, 1) и цистеин (p. K=8, 2) могут отдавать протоны и заряжаться отрицательно при повышении кислотности (не при физиологических p. H). Коваль А. Н. , 2006 (C) 8
 Изоэлектрическая точка (p. I) l Изоэлектрическая точка (p. I) – это значение p. H, при котором число положительных зарядов равно числу отрицательных (в аминокислоте или пептиде). 2/17/2018 Коваль А. Н. , 2006 (C) 9
Изоэлектрическая точка (p. I) l Изоэлектрическая точка (p. I) – это значение p. H, при котором число положительных зарядов равно числу отрицательных (в аминокислоте или пептиде). 2/17/2018 Коваль А. Н. , 2006 (C) 9
 Определение заряда пептидов при различных p. H l Особенности пептидов: l В них обязательно присутствуют концевые α –амино и α–карбоксигруппы (p. K соответственно 2, 5 и 9, 0); l Боковые радикалы 7 АК могут приобретать заряды: l Отрицательный: l асп (p. K=3, 9), глу (p. K=4, 1), цис (p. K=8, 2), тир (p. K=10, 1); 2/17/2018 Коваль А. Н. , 2006 (C) Положительный: арг (p. K=12, 5), лиз (p. K=10, 5), гис (p. K=6, 5). 10
Определение заряда пептидов при различных p. H l Особенности пептидов: l В них обязательно присутствуют концевые α –амино и α–карбоксигруппы (p. K соответственно 2, 5 и 9, 0); l Боковые радикалы 7 АК могут приобретать заряды: l Отрицательный: l асп (p. K=3, 9), глу (p. K=4, 1), цис (p. K=8, 2), тир (p. K=10, 1); 2/17/2018 Коваль А. Н. , 2006 (C) Положительный: арг (p. K=12, 5), лиз (p. K=10, 5), гис (p. K=6, 5). 10
 Пример расчета зарядов пептида при различных p. H Коваль А. Н. , 2006 (C)
Пример расчета зарядов пептида при различных p. H Коваль А. Н. , 2006 (C)
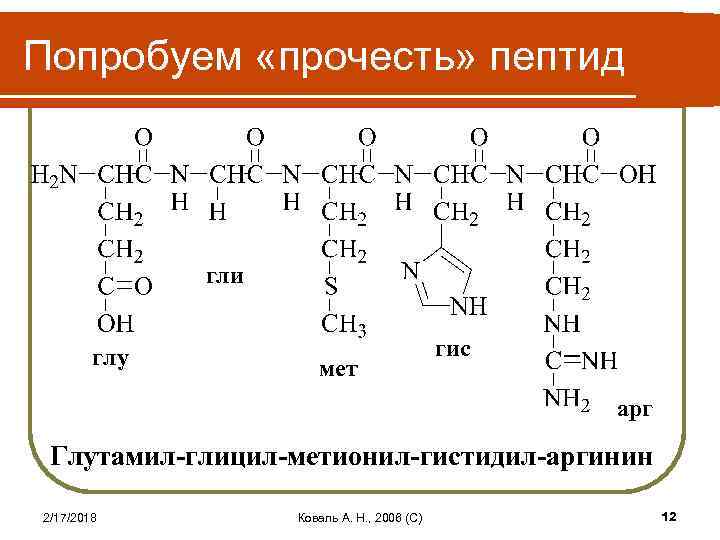 Попробуем «прочесть» пептид гли глу мет гис арг Глутамил-глицил-метионил-гистидил-аргинин 2/17/2018 Коваль А. Н. , 2006 (C) 12
Попробуем «прочесть» пептид гли глу мет гис арг Глутамил-глицил-метионил-гистидил-аргинин 2/17/2018 Коваль А. Н. , 2006 (C) 12
 Изменение заряда пептида при увеличении p. H от 0 до 14 + - 3+ 2+ 0 2, 5 1 2/17/2018 2 + 0 4, 1 3 4 6, 5 5 6 2 - 9, 0 7 8 Коваль А. Н. , 2006 (C) 9 12, 5 10 11 12 14 13 13
Изменение заряда пептида при увеличении p. H от 0 до 14 + - 3+ 2+ 0 2, 5 1 2/17/2018 2 + 0 4, 1 3 4 6, 5 5 6 2 - 9, 0 7 8 Коваль А. Н. , 2006 (C) 9 12, 5 10 11 12 14 13 13
 2/17/2018 Коваль А. Н. , 2006 (C) 14
2/17/2018 Коваль А. Н. , 2006 (C) 14
 2/17/2018 Коваль А. Н. , 2006 (C) 15
2/17/2018 Коваль А. Н. , 2006 (C) 15
 2/17/2018 Коваль А. Н. , 2006 (C) 16
2/17/2018 Коваль А. Н. , 2006 (C) 16
 2/17/2018 Коваль А. Н. , 2006 (C) 17
2/17/2018 Коваль А. Н. , 2006 (C) 17
 2/17/2018 Коваль А. Н. , 2006 (C) 18
2/17/2018 Коваль А. Н. , 2006 (C) 18
 2/17/2018 Коваль А. Н. , 2006 (C) 19
2/17/2018 Коваль А. Н. , 2006 (C) 19
 2/17/2018 Коваль А. Н. , 2006 (C) 20
2/17/2018 Коваль А. Н. , 2006 (C) 20
 2/17/2018 Коваль А. Н. , 2006 (C) 21
2/17/2018 Коваль А. Н. , 2006 (C) 21


