ФИЗИКО-ХИМИЧЕСКИЕ ПРОЦЕССЫ В ГИДРОСФЕРЕ.pptx
- Количество слайдов: 55
 ФИЗИКО-ХИМИЧЕСКИЕ ПРОЦЕССЫ В ГИДРОСФЕРЕ
ФИЗИКО-ХИМИЧЕСКИЕ ПРОЦЕССЫ В ГИДРОСФЕРЕ
 ГИДРОСФЕРА это прерывистая водная оболочка Земли, расположенная между атмосферой и твердой земной корой (литосферой), представляющая собой совокупность океанов, морей и поверхностных вод суши. В более широком смысле гидросфера понимается как непрерывная оболочка системы лед – вода – водяной пар, включающая всю воду, находящуюся на Земле в трех агрегатных состояниях, в том числе атмосферную воду, подземные воды, льды и снежный покров, а также воду, содержащуюся в живых организмах, и воду, входящую в состав химических соединений.
ГИДРОСФЕРА это прерывистая водная оболочка Земли, расположенная между атмосферой и твердой земной корой (литосферой), представляющая собой совокупность океанов, морей и поверхностных вод суши. В более широком смысле гидросфера понимается как непрерывная оболочка системы лед – вода – водяной пар, включающая всю воду, находящуюся на Земле в трех агрегатных состояниях, в том числе атмосферную воду, подземные воды, льды и снежный покров, а также воду, содержащуюся в живых организмах, и воду, входящую в состав химических соединений.
 Для гидросферы в целом характерен постоянный обмен веществом и энергией с литосферой и атмосферой. С термодинамической точки зрения, гидросфера представляет собой открытую термодинамическую систему. Исключение – отдельные ограниченные объемы подземных вод
Для гидросферы в целом характерен постоянный обмен веществом и энергией с литосферой и атмосферой. С термодинамической точки зрения, гидросфера представляет собой открытую термодинамическую систему. Исключение – отдельные ограниченные объемы подземных вод
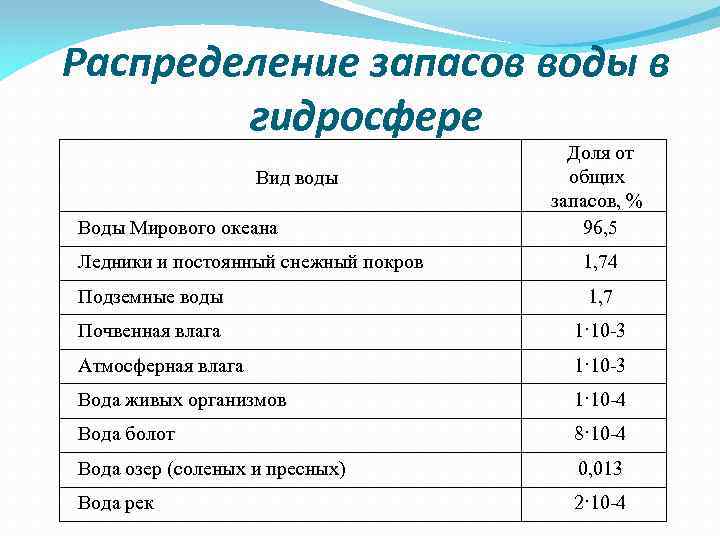 Распределение запасов воды в гидросфере Вид воды Воды Мирового океана Доля от общих запасов, % 96, 5 Ледники и постоянный снежный покров 1, 74 Подземные воды 1, 7 Почвенная влага 1·10 -3 Атмосферная влага 1·10 -3 Вода живых организмов 1·10 -4 Вода болот 8·10 -4 Вода озер (соленых и пресных) 0, 013 Вода рек 2·10 -4
Распределение запасов воды в гидросфере Вид воды Воды Мирового океана Доля от общих запасов, % 96, 5 Ледники и постоянный снежный покров 1, 74 Подземные воды 1, 7 Почвенная влага 1·10 -3 Атмосферная влага 1·10 -3 Вода живых организмов 1·10 -4 Вода болот 8·10 -4 Вода озер (соленых и пресных) 0, 013 Вода рек 2·10 -4
 1. Особенности физикохимических свойств воды и их значение для биосферы
1. Особенности физикохимических свойств воды и их значение для биосферы
 При реально существующих на Земле диапазонах атмосферного давления и температуры вода может находиться в разных агрегатных состояниях. Вода имеет необыкновенно высокие температуры кипения и замерзания, что и определяет возможность существования воды на Земле, как в жидком, так и в газообразном и твердом состоянии. Температура кипения и замерзания воды зависит от давления. При нормальном атмосферном давлении (101, 3 к. Па) точки кипения и замерзания соответствуют 100°С и 0°С. Температура кипения снижается с уменьшением давления
При реально существующих на Земле диапазонах атмосферного давления и температуры вода может находиться в разных агрегатных состояниях. Вода имеет необыкновенно высокие температуры кипения и замерзания, что и определяет возможность существования воды на Земле, как в жидком, так и в газообразном и твердом состоянии. Температура кипения и замерзания воды зависит от давления. При нормальном атмосферном давлении (101, 3 к. Па) точки кипения и замерзания соответствуют 100°С и 0°С. Температура кипения снижается с уменьшением давления
 Температурная зависимость плотности воды характеризуется максимумом плотности при температуре 4 °С. Особенности изменения плотности воды связаны с перестройкой молекулярной структуры воды. Гидрологическое значение: лед из-за более низкой плотности остается на поверхности воды; водоемы не промерзают до дна, так как охлажденная до температуры ниже 4°С вода становится менее плотной и поэтому остается в поверхностном слое.
Температурная зависимость плотности воды характеризуется максимумом плотности при температуре 4 °С. Особенности изменения плотности воды связаны с перестройкой молекулярной структуры воды. Гидрологическое значение: лед из-за более низкой плотности остается на поверхности воды; водоемы не промерзают до дна, так как охлажденная до температуры ниже 4°С вода становится менее плотной и поэтому остается в поверхностном слое.
 Плотность воды изменяется в зависимости от содержания в ней растворенных веществ и увеличивается с ростом солености. Увеличение солености приводит к понижению температуры наибольшей плотности. Соотношения между температурой наибольшей плотности и температурой замерзания влияют на характер процесса охлаждения воды и вертикальной конвекции – перемешивания, обусловленного различиями в плотности. Охлаждение воды в результате теплообмена с воздухом приводит к увеличению плотности воды и опусканию вниз более плотной воды, на место которой поднимаются более теплые и менее плотные воды.
Плотность воды изменяется в зависимости от содержания в ней растворенных веществ и увеличивается с ростом солености. Увеличение солености приводит к понижению температуры наибольшей плотности. Соотношения между температурой наибольшей плотности и температурой замерзания влияют на характер процесса охлаждения воды и вертикальной конвекции – перемешивания, обусловленного различиями в плотности. Охлаждение воды в результате теплообмена с воздухом приводит к увеличению плотности воды и опусканию вниз более плотной воды, на место которой поднимаются более теплые и менее плотные воды.
 Удельная теплоемкость воды – 4190 Дж/(кг. К) выше, чем почти у всех твердых и жидких веществ. Благодаря огромной теплоемкости Мировой океан сглаживает колебания температуры, и перепад температур от экватора до полюса составляет всего около 30°. Теплота плавления твердой воды (льда) составляет 6, 012 к. Дж/моль, что значительно выше соответствующих значений для других веществ. Фазовые переходы (таяние снега и льда, замерзание воды) сопровождаются соответственно значительным поглощением и выделением энергии (при замерзании 1 м 3 воды выделяется тепла примерно столько же, что и при сжигании 10 кг угля). Благодаря высокой теплоте плавления на Земле растягиваются во времени и сглаживаются сезонные переходы.
Удельная теплоемкость воды – 4190 Дж/(кг. К) выше, чем почти у всех твердых и жидких веществ. Благодаря огромной теплоемкости Мировой океан сглаживает колебания температуры, и перепад температур от экватора до полюса составляет всего около 30°. Теплота плавления твердой воды (льда) составляет 6, 012 к. Дж/моль, что значительно выше соответствующих значений для других веществ. Фазовые переходы (таяние снега и льда, замерзание воды) сопровождаются соответственно значительным поглощением и выделением энергии (при замерзании 1 м 3 воды выделяется тепла примерно столько же, что и при сжигании 10 кг угля). Благодаря высокой теплоте плавления на Земле растягиваются во времени и сглаживаются сезонные переходы.
 Теплота испарения воды (при 0°С – 2, 5· 103 к. Дж/кг, при 100°С – 2, 26· 103 к. Дж/кг) также имеет аномально высокое значение. Большая часть солнечной энергии, достигающей Земли, расходуется на испарение воды, тем самым препятствуя перегреву земной поверхности. Конденсация паров воды в атмосфере сопровождается выделением тепла. Изменение температуры воздуха является причиной атмосферных циркуляций.
Теплота испарения воды (при 0°С – 2, 5· 103 к. Дж/кг, при 100°С – 2, 26· 103 к. Дж/кг) также имеет аномально высокое значение. Большая часть солнечной энергии, достигающей Земли, расходуется на испарение воды, тем самым препятствуя перегреву земной поверхности. Конденсация паров воды в атмосфере сопровождается выделением тепла. Изменение температуры воздуха является причиной атмосферных циркуляций.
 Поверхностное натяжение воды максимально среди жидких веществ (за исключением ртути). Высокое значение поверхностного натяжения приводит к появлению на водной поверхности ряби и волн уже при слабом ветре, в результате чего сильно возрастает площадь контакта с атмосферой и интенсифицируются процессы теплопередачи и газообмена. С высоким поверхностным натяжением воды связано и действие капиллярных сил, благодаря которым вода может подниматься на высоту до 10 – 12 м от уровня грунтовых вод.
Поверхностное натяжение воды максимально среди жидких веществ (за исключением ртути). Высокое значение поверхностного натяжения приводит к появлению на водной поверхности ряби и волн уже при слабом ветре, в результате чего сильно возрастает площадь контакта с атмосферой и интенсифицируются процессы теплопередачи и газообмена. С высоким поверхностным натяжением воды связано и действие капиллярных сил, благодаря которым вода может подниматься на высоту до 10 – 12 м от уровня грунтовых вод.
 Диэлектрическая проницаемость воды имеет аномально высокое значение. Это определяет самую большую растворяющую способность воды по отношению к веществам с полярной и ионной структурой. Поэтому в природе нет химически чистой воды, человек всегда имеет дело с растворами. Даже самые чистые атмосферные осадки содержат до 5 мг/л растворенных солей.
Диэлектрическая проницаемость воды имеет аномально высокое значение. Это определяет самую большую растворяющую способность воды по отношению к веществам с полярной и ионной структурой. Поэтому в природе нет химически чистой воды, человек всегда имеет дело с растворами. Даже самые чистые атмосферные осадки содержат до 5 мг/л растворенных солей.
 Компоненты химического состава природных вод 1. Главные ионы, или макрокомпоненты. катионы K+, Na+, Mg 2+, Ca 2+ анионы Cl¯, SO 42 -, HCO 3¯, (CO 32 -) Ионный состав природных вод определяется растворением таких минералов галит (Na. Cl), гипс (Ca. SO 4· 2 H 2 O), кальцит (Ca. CO 3), доломит (Ca. CO 3 *Mg. CO 3).
Компоненты химического состава природных вод 1. Главные ионы, или макрокомпоненты. катионы K+, Na+, Mg 2+, Ca 2+ анионы Cl¯, SO 42 -, HCO 3¯, (CO 32 -) Ионный состав природных вод определяется растворением таких минералов галит (Na. Cl), гипс (Ca. SO 4· 2 H 2 O), кальцит (Ca. CO 3), доломит (Ca. CO 3 *Mg. CO 3).
 Ионы, преобладающие в воде Мирового океана (в порядке убывания концентрации): Na+ > Mg 2+ > Ca 2+ > K+ >> другие катионы. Cl- > SO 42 - > HCO 3 - > Br- > F- >> другие анионы. В речной воде среди ионов наиболее распространены: Ca 2+> Na+ > Mg 2+ > K+ >> другие катионы, HCO 3 - > SO 42 - >Cl- >> другие анионы. Для среднего состава дождевой воды преобладающим катионом является Na+, а анионом SO 42 -.
Ионы, преобладающие в воде Мирового океана (в порядке убывания концентрации): Na+ > Mg 2+ > Ca 2+ > K+ >> другие катионы. Cl- > SO 42 - > HCO 3 - > Br- > F- >> другие анионы. В речной воде среди ионов наиболее распространены: Ca 2+> Na+ > Mg 2+ > K+ >> другие катионы, HCO 3 - > SO 42 - >Cl- >> другие анионы. Для среднего состава дождевой воды преобладающим катионом является Na+, а анионом SO 42 -.
 2. Растворенные газы. О 2, CO 2, N 2, H 2 S, CH 4 и др Важнейшими газами, растворенными в воде, являются кислород и диоксид углерода.
2. Растворенные газы. О 2, CO 2, N 2, H 2 S, CH 4 и др Важнейшими газами, растворенными в воде, являются кислород и диоксид углерода.
 Кислород находится в воде в виде растворенных молекул. На содержание кислорода в воде влияют две группы процессов: – процессы, обогащающие воду кислородом, – источники кислорода (абсорбция O 2 из атмосферы и выделение водной растительностью в процессе фотосинтеза); – процессы, уменьшающие содержание кислорода в воде, стоки кислорода (потребление O 2 на окисление органических и неорганических веществ и десорбция в атмосферу).
Кислород находится в воде в виде растворенных молекул. На содержание кислорода в воде влияют две группы процессов: – процессы, обогащающие воду кислородом, – источники кислорода (абсорбция O 2 из атмосферы и выделение водной растительностью в процессе фотосинтеза); – процессы, уменьшающие содержание кислорода в воде, стоки кислорода (потребление O 2 на окисление органических и неорганических веществ и десорбция в атмосферу).
 Обогащение воды кислородом при абсорбции может происходить только в том случае, если вода не насыщена им, т. е. содержание кислорода в ней меньше, чем должно быть при данной температуре и давлении при установлении термодинамического равновесия. Этот процесс может происходить только на поверхности водоема.
Обогащение воды кислородом при абсорбции может происходить только в том случае, если вода не насыщена им, т. е. содержание кислорода в ней меньше, чем должно быть при данной температуре и давлении при установлении термодинамического равновесия. Этот процесс может происходить только на поверхности водоема.
 Десорбция кислорода может происходить только в том случае, если вода при данной температуре и давлении окажется пересыщенной кислородом. Выделение кислорода из воды может происходить только в поверхностных слоях, тогда как потребление кислорода протекает на различных глубинах, хотя и не с одинаковой интенсивностью.
Десорбция кислорода может происходить только в том случае, если вода при данной температуре и давлении окажется пересыщенной кислородом. Выделение кислорода из воды может происходить только в поверхностных слоях, тогда как потребление кислорода протекает на различных глубинах, хотя и не с одинаковой интенсивностью.
 Диоксид углерода находится в воде главным образом в виде растворенных молекул СО 2 (р-р). Около 1% молекул вступает во взаимодействие с водой, образуя угольную кислоту СО 2 (г) ↔ СО 2 (р-р) + Н 2 О ↔ Н 2 СО 3
Диоксид углерода находится в воде главным образом в виде растворенных молекул СО 2 (р-р). Около 1% молекул вступает во взаимодействие с водой, образуя угольную кислоту СО 2 (г) ↔ СО 2 (р-р) + Н 2 О ↔ Н 2 СО 3
 источники диоксида углерода: процессы окисления органических веществ, происходящие с выделением СО 2 (непосредственно в воде, в почвах и илах, с которыми соприкасается вода); дыхание водных организмов; вулканические газы, выделяющиеся из недр Земли (дегазация мантии, процессы метаморфизации осадочных пород, протекающие в глубинах под действием высоких температур).
источники диоксида углерода: процессы окисления органических веществ, происходящие с выделением СО 2 (непосредственно в воде, в почвах и илах, с которыми соприкасается вода); дыхание водных организмов; вулканические газы, выделяющиеся из недр Земли (дегазация мантии, процессы метаморфизации осадочных пород, протекающие в глубинах под действием высоких температур).
 уменьшение содержания СО 2 происходит: при фотосинтезе 2 HCO 3 - ↔ СО 2 + CO 32 - + H 2 O при растворении карбонатов: Ca. CO 3 + CO 2 + H 2 O ↔ Ca(HCO 3)2 при химическом выветривании алюмосиликатов Na 2 O·Al 2 O 3· 6 Si. O 2 + CO 2 + 2 H 2 O = Al 2 O 3· 2 Si. O 2· 2 H 2 O + 4 Si. O 2 + Na 2 CO 3
уменьшение содержания СО 2 происходит: при фотосинтезе 2 HCO 3 - ↔ СО 2 + CO 32 - + H 2 O при растворении карбонатов: Ca. CO 3 + CO 2 + H 2 O ↔ Ca(HCO 3)2 при химическом выветривании алюмосиликатов Na 2 O·Al 2 O 3· 6 Si. O 2 + CO 2 + 2 H 2 O = Al 2 O 3· 2 Si. O 2· 2 H 2 O + 4 Si. O 2 + Na 2 CO 3
 3. Биогенные вещества Соединения: азота (нитраты, аммонийный азот); фосфора (фосфаты и гидрофосфаты); кремния (коллоидные или истинно растворенные формы кремниевой и поликремниевых кислот); железа (гидроксид (+3) и комплексы железа (+3) c органическими кислотами). источники - внутриводоемные процессы и поступление с поверхностным стоком, атмосферными осадками и сточными водами.
3. Биогенные вещества Соединения: азота (нитраты, аммонийный азот); фосфора (фосфаты и гидрофосфаты); кремния (коллоидные или истинно растворенные формы кремниевой и поликремниевых кислот); железа (гидроксид (+3) и комплексы железа (+3) c органическими кислотами). источники - внутриводоемные процессы и поступление с поверхностным стоком, атмосферными осадками и сточными водами.
 Соединения азота Неорганические соединения – ионы аммония NH 4+, нитрит-ионы NO 2 - и нитрат-ионы NO 3 -. В органических соединениях азот находится главным образом в составе белка тканей организмов и продуктов его распада, образующихся как при отмирании самих организмов, так и при распаде продуктов их жизнедеятельности.
Соединения азота Неорганические соединения – ионы аммония NH 4+, нитрит-ионы NO 2 - и нитрат-ионы NO 3 -. В органических соединениях азот находится главным образом в составе белка тканей организмов и продуктов его распада, образующихся как при отмирании самих организмов, так и при распаде продуктов их жизнедеятельности.
 Источники связанного азота : поступление нитратов с дождевой водой, процесс связывания азота азотфиксирующими бактериями (Clostridium Pasteurianum, Azotobacter), денитрификация 4 NO 3 - + 5 C + 2 H 2 O = 2 N 2 + CO 2 + 4 HCO 3 -. антропогенное поступление соединений азота с промышленными и особенно бытовыми сточными водами.
Источники связанного азота : поступление нитратов с дождевой водой, процесс связывания азота азотфиксирующими бактериями (Clostridium Pasteurianum, Azotobacter), денитрификация 4 NO 3 - + 5 C + 2 H 2 O = 2 N 2 + CO 2 + 4 HCO 3 -. антропогенное поступление соединений азота с промышленными и особенно бытовыми сточными водами.
 Конечным неорганическим продуктом сложного процесса минерализации азотсодержащих органических веществ является аммиак. Ионы аммония усваиваются растениями при фотосинтезе и могут быть окислены в нитриты и нитраты.
Конечным неорганическим продуктом сложного процесса минерализации азотсодержащих органических веществ является аммиак. Ионы аммония усваиваются растениями при фотосинтезе и могут быть окислены в нитриты и нитраты.
 Первая стадия – переход NH 4+ в NO 2 - – осуществляется под действием бактерий- нитрификаторов (семейство Bacteriaceae род Nitrosomonas) по схеме: NH 4+ + 2 O 2 = NO 2 - + 2 H 2 O. Вторая стадия – окисление нитритионов в нитрат-ионы под воздействием других бактерий (род Nitrobacter Win. ): 2 NO 2 - + O 2 = 2 NO 3 -.
Первая стадия – переход NH 4+ в NO 2 - – осуществляется под действием бактерий- нитрификаторов (семейство Bacteriaceae род Nitrosomonas) по схеме: NH 4+ + 2 O 2 = NO 2 - + 2 H 2 O. Вторая стадия – окисление нитритионов в нитрат-ионы под воздействием других бактерий (род Nitrobacter Win. ): 2 NO 2 - + O 2 = 2 NO 3 -.
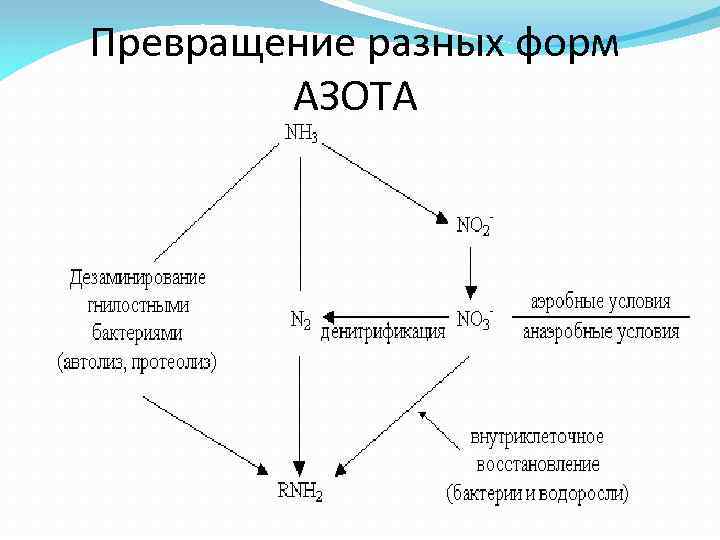 Превращение разных форм АЗОТА
Превращение разных форм АЗОТА
 Соединения фосфора. Неорганический фосфор находится преимущественно в виде производных ортофосфорной кислоты H 3 PO 4 ↔ H+ + H 2 PO 4 - ↔ H+ + HPO 42 - ↔ H+ + PO 43 Кроме того, фосфор находится в воде виде взвесей также неорганического (взвеси, содержащие апатиты, фосфориты и др. ) и органического (остатки организмов) происхождения.
Соединения фосфора. Неорганический фосфор находится преимущественно в виде производных ортофосфорной кислоты H 3 PO 4 ↔ H+ + H 2 PO 4 - ↔ H+ + HPO 42 - ↔ H+ + PO 43 Кроме того, фосфор находится в воде виде взвесей также неорганического (взвеси, содержащие апатиты, фосфориты и др. ) и органического (остатки организмов) происхождения.
 Стоком фосфатов является потребление их водными растениями, фитопланктоном и фитобентосом. Большая часть фосфатов, использованных водными растениями и животными, возвращается обратно в воду в процессе жизнедеятельности организмов или при минерализации их остатков, и лишь некоторая часть попадает на дно водоемов с остатками организмов
Стоком фосфатов является потребление их водными растениями, фитопланктоном и фитобентосом. Большая часть фосфатов, использованных водными растениями и животными, возвращается обратно в воду в процессе жизнедеятельности организмов или при минерализации их остатков, и лишь некоторая часть попадает на дно водоемов с остатками организмов
 Кремний. постоянный компонент состава природных вод. Этому способствует повсеместная распространенность соединений кремния в горных породах, малая растворимость последних объясняет малое содержание кремния в воде. Основные формы соединений кремния в природных водах ортокремниевая H 4 Si. O 4 и поликремниевая кислоты : H 4 Si. O 4 ↔ H+ + H 3 Si. O 4 -.
Кремний. постоянный компонент состава природных вод. Этому способствует повсеместная распространенность соединений кремния в горных породах, малая растворимость последних объясняет малое содержание кремния в воде. Основные формы соединений кремния в природных водах ортокремниевая H 4 Si. O 4 и поликремниевая кислоты : H 4 Si. O 4 ↔ H+ + H 3 Si. O 4 -.
 Железо. В подземных водах при повышенном содержании угольной кислоты и отсутствии кислорода оно находится в виде гидрокарбоната железа (II). При выходе на поверхность и достаточной аэрации гидрокарбонат железа (II) гидролизуется и малорастворимый гидроксид железа (II) окисляется в гидроксид железа (III): Fe 2+ + 2 HCO 3 - ↔ Fe(OH)2 + CO 2 + H 2 O 4 Fe(OH)2 + O 2 + 2 H 2 O → 4 Fe(OH)3 В равновесии с Fe(OH)3 присутствует еще ряд других форм: [Fe. OH]2+, [Fe(OH)2]+, [Fe 2(OH)2]4+.
Железо. В подземных водах при повышенном содержании угольной кислоты и отсутствии кислорода оно находится в виде гидрокарбоната железа (II). При выходе на поверхность и достаточной аэрации гидрокарбонат железа (II) гидролизуется и малорастворимый гидроксид железа (II) окисляется в гидроксид железа (III): Fe 2+ + 2 HCO 3 - ↔ Fe(OH)2 + CO 2 + H 2 O 4 Fe(OH)2 + O 2 + 2 H 2 O → 4 Fe(OH)3 В равновесии с Fe(OH)3 присутствует еще ряд других форм: [Fe. OH]2+, [Fe(OH)2]+, [Fe 2(OH)2]4+.
 Повышенное содержание железа (свыше 1 мг/дм 3) ухудшает качество воды и возможность ее использования для питьевых и технических целей
Повышенное содержание железа (свыше 1 мг/дм 3) ухудшает качество воды и возможность ее использования для питьевых и технических целей
 4. Микроэлементы. относятся все катионы металлов, кроме главных ионов и железа, такие как Cu 2+, Mn 2+ и другие, а также анионы, встречающиеся в водоемах в малых концентрациях (Вr¯, F¯, I¯и др. )
4. Микроэлементы. относятся все катионы металлов, кроме главных ионов и железа, такие как Cu 2+, Mn 2+ и другие, а также анионы, встречающиеся в водоемах в малых концентрациях (Вr¯, F¯, I¯и др. )
 группа веществ включает различные органические соединения: органические кислоты, спирты, альдегиды и кетоны, сложные эфиры, в том числе липиды, фенолы, гуминовые вещества, ароматические соединения, углеводы, азотсодержащие соединения (амины, аминокислоты, белки) и т. д.
группа веществ включает различные органические соединения: органические кислоты, спирты, альдегиды и кетоны, сложные эфиры, в том числе липиды, фенолы, гуминовые вещества, ароматические соединения, углеводы, азотсодержащие соединения (амины, аминокислоты, белки) и т. д.
 По происхождению органические вещества делят на две группы: продукты метаболизма и биохимического распада остатков организмов (1 группа) характерны для вод морей, озер и водохранилищ вещества, поступающие с поверхностными стоками, атмосферными осадками и сточными водами (2 группа). характерны для речных вод.
По происхождению органические вещества делят на две группы: продукты метаболизма и биохимического распада остатков организмов (1 группа) характерны для вод морей, озер и водохранилищ вещества, поступающие с поверхностными стоками, атмосферными осадками и сточными водами (2 группа). характерны для речных вод.
 Ввиду сложности определения индивидуальных органических веществ, их многообразия и малых природных концентраций для оценки содержания РОВ используют косвенные показатели: общее содержание Сорг, Nорг. , Рорг. , перманганатную окисляемость воды(ПО), ХПК и БПК
Ввиду сложности определения индивидуальных органических веществ, их многообразия и малых природных концентраций для оценки содержания РОВ используют косвенные показатели: общее содержание Сорг, Nорг. , Рорг. , перманганатную окисляемость воды(ПО), ХПК и БПК
 ПО – число миллиграммов атомарного кислорода, эквивалентное количеству перманганата калия, необходимого для окисления РОВ, содержащихся в 1 дм 3 воды. ХПК (химическое потребление кислорода) – число миллиграммов атомарного кислорода, эквивалентное количеству дихромата калия, необходимого для окисления РОВ, содержащихся в 1 дм 3 воды. БПК (биохимическое потребление кислорода) – число миллиграммов атомарного кислорода, необходимого для окисления РОВ, содержащихся в 1 дм 3 воды, с участием микроорганизмов.
ПО – число миллиграммов атомарного кислорода, эквивалентное количеству перманганата калия, необходимого для окисления РОВ, содержащихся в 1 дм 3 воды. ХПК (химическое потребление кислорода) – число миллиграммов атомарного кислорода, эквивалентное количеству дихромата калия, необходимого для окисления РОВ, содержащихся в 1 дм 3 воды. БПК (биохимическое потребление кислорода) – число миллиграммов атомарного кислорода, необходимого для окисления РОВ, содержащихся в 1 дм 3 воды, с участием микроорганизмов.
 Первичное органическое вещество создается фотосинтезирующими растениями и хемосинтезирующими бактериями. На основе этого вещества различные организмы, потребляя его в пищу, создают более сложные виды органической материи. Образуется пищевая цепь: растения → растениеядный зоопланктон и зообентос → хищный зоопланктон и зообентос → рыбы → крупные хищные рыбы
Первичное органическое вещество создается фотосинтезирующими растениями и хемосинтезирующими бактериями. На основе этого вещества различные организмы, потребляя его в пищу, создают более сложные виды органической материи. Образуется пищевая цепь: растения → растениеядный зоопланктон и зообентос → хищный зоопланктон и зообентос → рыбы → крупные хищные рыбы
 6. Токсичные загрязняющие вещества, попадающие в воду из антропогенных источников. соединения тяжелых металлов, нефтепродукты, хлорорганические соединения, СПАВ, различные органические соединения. Источники - атмосферные осадки, поверхностные стоки и производственные и коммунально-бытовые СВ.
6. Токсичные загрязняющие вещества, попадающие в воду из антропогенных источников. соединения тяжелых металлов, нефтепродукты, хлорорганические соединения, СПАВ, различные органические соединения. Источники - атмосферные осадки, поверхностные стоки и производственные и коммунально-бытовые СВ.
 приоритетные загрязнители (около 180 соединений, объединенные в 13 групп): ароматические углеводороды, полиядерные ароматические углеводороды (ПАУ), пестициды (4 группы), летучие и малолетучие хлорорганические соединения, хлорфенолы, хлоранилины и хлорнитроароматические соединения, полихлорированные и полибромированные бифенилы, металлорганические соединения и другие. Источники - атмосферные осадки, поверхностные стоки и производственные и коммунально-бытовые СВ.
приоритетные загрязнители (около 180 соединений, объединенные в 13 групп): ароматические углеводороды, полиядерные ароматические углеводороды (ПАУ), пестициды (4 группы), летучие и малолетучие хлорорганические соединения, хлорфенолы, хлоранилины и хлорнитроароматические соединения, полихлорированные и полибромированные бифенилы, металлорганические соединения и другие. Источники - атмосферные осадки, поверхностные стоки и производственные и коммунально-бытовые СВ.
 Таким образом, природная вода представляет собой многофазную (гетерогенную) систему открытого типа, обменивающуюся веществами и энергией с сопредельными средами (водными объектами, атмосферой, донными отложениями) и с биологической составляющей.
Таким образом, природная вода представляет собой многофазную (гетерогенную) систему открытого типа, обменивающуюся веществами и энергией с сопредельными средами (водными объектами, атмосферой, донными отложениями) и с биологической составляющей.
 2. Классификация природных вод
2. Классификация природных вод
 ОСНОВНЫЕ ПРОЦЕССЫ ФОРМИРОВАНИЯ ХИМИЧЕСКОГО СОСТАВА ПРИРОДНЫХ ВОД При формировании химического состава природных вод принято выделять прямые и косвенные факторы, влияющие на содержание в них растворенных компонентов.
ОСНОВНЫЕ ПРОЦЕССЫ ФОРМИРОВАНИЯ ХИМИЧЕСКОГО СОСТАВА ПРИРОДНЫХ ВОД При формировании химического состава природных вод принято выделять прямые и косвенные факторы, влияющие на содержание в них растворенных компонентов.
 Прямыми называют факторы, которые оказываю непосредственное влияние на химический состав воды и связаны с химическим составом контактирующих с данной природной водой веществ (минералов, горных пород, веществ почвы). Косвенные факторы оказывают влияние на состав природных вод через посредство прямых факторов; к ним относятся температура, давление и др. Главные факторы определяют содержание главных анионов и катионов (т. е. класс и тип воды по классификации О. А. Алесина). Второстепенные факторы вызывают появление некоторых особенностей данной воды (цвета, запаха и др. ), но не влияют на ее класс и тип.
Прямыми называют факторы, которые оказываю непосредственное влияние на химический состав воды и связаны с химическим составом контактирующих с данной природной водой веществ (минералов, горных пород, веществ почвы). Косвенные факторы оказывают влияние на состав природных вод через посредство прямых факторов; к ним относятся температура, давление и др. Главные факторы определяют содержание главных анионов и катионов (т. е. класс и тип воды по классификации О. А. Алесина). Второстепенные факторы вызывают появление некоторых особенностей данной воды (цвета, запаха и др. ), но не влияют на ее класс и тип.
 По характеру воздействия на формирование состава природных вод все факторы делят на 5 групп: 1) физико-географические (рельеф, климат…); 2) геологические (вид горных пород, гидрогеологические условия и т. п. ); 3) биологические (деятельность живых организмов); 4) антропогенные (состав сточных вод, состав твердых отходов и т. п. ); 5) физико-химические (химические свойства соединений, кислотно-основные и окислительно-восстановительные условия).
По характеру воздействия на формирование состава природных вод все факторы делят на 5 групп: 1) физико-географические (рельеф, климат…); 2) геологические (вид горных пород, гидрогеологические условия и т. п. ); 3) биологические (деятельность живых организмов); 4) антропогенные (состав сточных вод, состав твердых отходов и т. п. ); 5) физико-химические (химические свойства соединений, кислотно-основные и окислительно-восстановительные условия).
 По величине общей жесткости природные воды принято делить на ряд групп: Общая жесткость, моль/м 3 Меньше 1, 5 – 3, 0 – 5, 4 – 10, 7 Больше 10, 7 Вода Очень мягкая Мягкая Средней жесткости Жесткая Очень жесткая Жесткость воды – свойство, обусловленное содержанием в воде катионов двухвалентных металлов, прежде всего кальция и магния, в меньшей степени железа.
По величине общей жесткости природные воды принято делить на ряд групп: Общая жесткость, моль/м 3 Меньше 1, 5 – 3, 0 – 5, 4 – 10, 7 Больше 10, 7 Вода Очень мягкая Мягкая Средней жесткости Жесткая Очень жесткая Жесткость воды – свойство, обусловленное содержанием в воде катионов двухвалентных металлов, прежде всего кальция и магния, в меньшей степени железа.
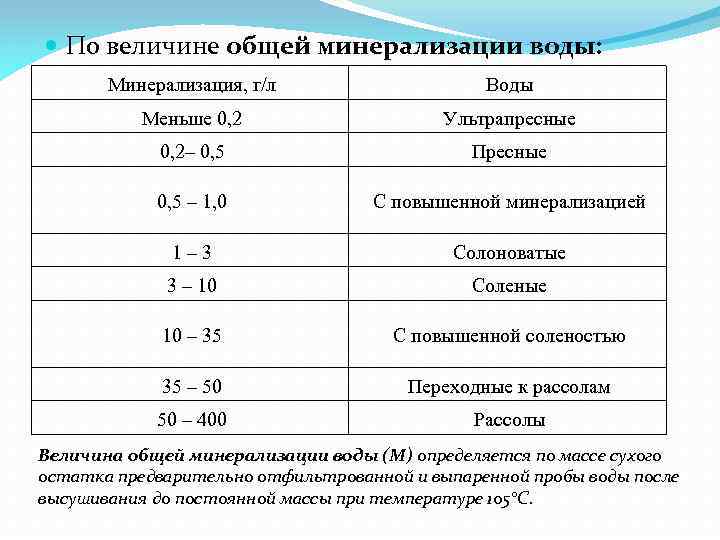 По величине общей минерализации воды: Минерализация, г/л Воды Меньше 0, 2 Ультрапресные 0, 2– 0, 5 Пресные 0, 5 – 1, 0 С повышенной минерализацией 1– 3 Солоноватые 3 – 10 Соленые 10 – 35 С повышенной соленостью 35 – 50 Переходные к рассолам 50 – 400 Рассолы Величина общей минерализации воды (М) определяется по массе сухого остатка предварительно отфильтрованной и выпаренной пробы воды после высушивания до постоянной массы при температуре 105°С.
По величине общей минерализации воды: Минерализация, г/л Воды Меньше 0, 2 Ультрапресные 0, 2– 0, 5 Пресные 0, 5 – 1, 0 С повышенной минерализацией 1– 3 Солоноватые 3 – 10 Соленые 10 – 35 С повышенной соленостью 35 – 50 Переходные к рассолам 50 – 400 Рассолы Величина общей минерализации воды (М) определяется по массе сухого остатка предварительно отфильтрованной и выпаренной пробы воды после высушивания до постоянной массы при температуре 105°С.
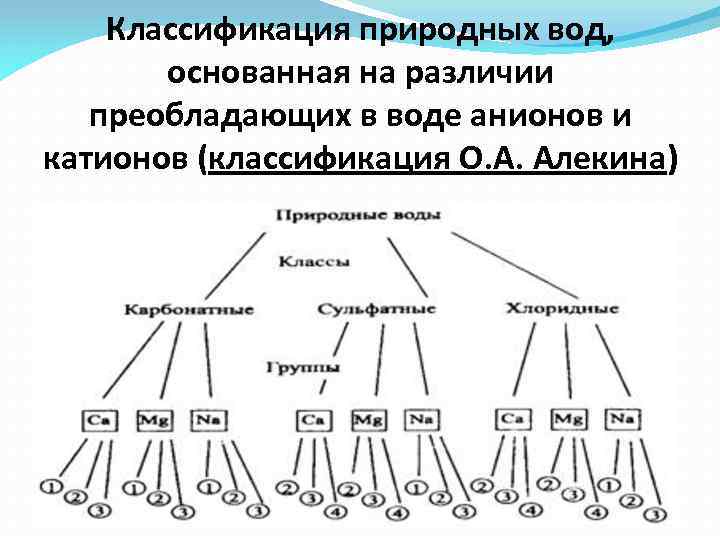 Классификация природных вод, основанная на различии преобладающих в воде анионов и катионов (классификация О. А. Алекина)
Классификация природных вод, основанная на различии преобладающих в воде анионов и катионов (классификация О. А. Алекина)
 геохимическая классификация вод природных ландшафтов А. И. Перельмана 1. По окислительновосстановительным условиям в ландшафтах выделяются воды с окислительной и восстановительной обстановкой.
геохимическая классификация вод природных ландшафтов А. И. Перельмана 1. По окислительновосстановительным условиям в ландшафтах выделяются воды с окислительной и восстановительной обстановкой.
 2. По щелочно-кислотным условиям в классификации А. И. Перельмана выделяются воды «сильнокислые» (р. Н < 3 – 4); «кислые и слабокислые» (р. Н от 3 – 4 до 6, 5); «нейтральные и слабощелочные» (р. Н от 6, 5 до 8, 5) и «сильнощелочные» (р. Н > 8, 5).
2. По щелочно-кислотным условиям в классификации А. И. Перельмана выделяются воды «сильнокислые» (р. Н < 3 – 4); «кислые и слабокислые» (р. Н от 3 – 4 до 6, 5); «нейтральные и слабощелочные» (р. Н от 6, 5 до 8, 5) и «сильнощелочные» (р. Н > 8, 5).
 По содержанию солей вода делится на пресную (менее 1 г/л), засоленную (до 25 г/л), соленую (более 25 г/л).
По содержанию солей вода делится на пресную (менее 1 г/л), засоленную (до 25 г/л), соленую (более 25 г/л).
 Лекция 2
Лекция 2
 1. Кислотно-основные равновесия в природных водах В соответствии с ионным составом кислотноосновные равновесия в природных водах определяются, в основном, присутствием ионов HCO 3¯ и CO 32 - вследствие протолитических равновесий HCO 3¯ + Н 2 О → H 2 CO 3 + OH¯ CO 32 - + Н 2 О → HCO 3¯ + OH¯ Остальные ионы, присутствующие в воде в заметных количествах (Na+, K+, Ca 2+, Cl¯, SO 42 -, NO 3 -), на р. Н раствора влияния не оказывают.
1. Кислотно-основные равновесия в природных водах В соответствии с ионным составом кислотноосновные равновесия в природных водах определяются, в основном, присутствием ионов HCO 3¯ и CO 32 - вследствие протолитических равновесий HCO 3¯ + Н 2 О → H 2 CO 3 + OH¯ CO 32 - + Н 2 О → HCO 3¯ + OH¯ Остальные ионы, присутствующие в воде в заметных количествах (Na+, K+, Ca 2+, Cl¯, SO 42 -, NO 3 -), на р. Н раствора влияния не оказывают.
 Серьезные проблемы, связанные с хозяйственной деятельностью человека, встают и перед более крупными водными объектами: проблема Каспия; проблема Азовского моря; проблема озера Байкал.
Серьезные проблемы, связанные с хозяйственной деятельностью человека, встают и перед более крупными водными объектами: проблема Каспия; проблема Азовского моря; проблема озера Байкал.



