01 Физико-химические основы жизни.pptx
- Количество слайдов: 108

Физико-химические основы жизни Михаил Пантелеев
Проблема. В каком фазовом состоянии должны быть живые организмы? Решение. Жидкость

Бонусы от воды: Water has a large liquidity range, which means that can be found in a liquid form in many different conditions. Water is extremely common in the universe (in fact, it's the most common chemical compound). Ice is less dense than liquid water. That allows ice to float and insulate the water below, preventing a whole ocean to freeze. Water is a polar solvent: that allows it to carry dissolved salts. Moreover, it can dissolve proteins, sugars, DNA and oxygen. Water is transparent to visible light, permitting the development of submarine photosynthetical ecologies. Water has a high specific heat and heat of vaporization, which allows it to absorb large quantities of heat, therefore regulating temperature differences. Water is amphoteric: it can work both as an acid and as a base, and is therefore able to participate in a large array of reactions, as a solvent, a reactant or a product. Alternatives: NH 3, HF, HCN, CH 4(? )

Часть 1. 1 Немедленные последствия выбора воды

Выбор воды и его последствия Особенности: 1. Малое расстояние диффузии 2. Полярность 3. Способность к маленькой, слабой диссоциации
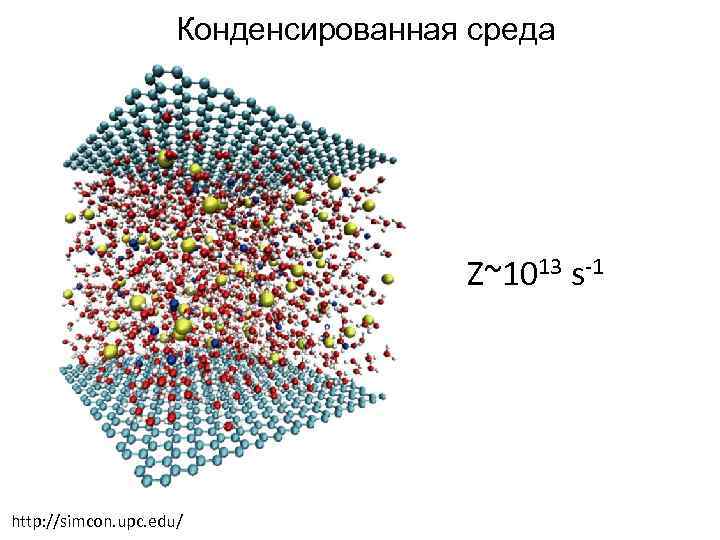
Конденсированная среда Z~1013 s-1 http: //simcon. upc. edu/

Проблема. Малое расстояние диффузии в воде Dметаболита~1000 мкм 2 с-1 Dбелка~100 мкм 2 с-1 http: //leavingbio. net/OSMOSIS%20 AND%20 DIFFUSION. htm

Решение. Нужна клетка Размер клетки определяется характерными расстояниями диффузии. Точнее, скорость химических реакций в растворах задает характерные времена, а комбинация этих времен и скоростей диффузии - задает характерные расстояния.
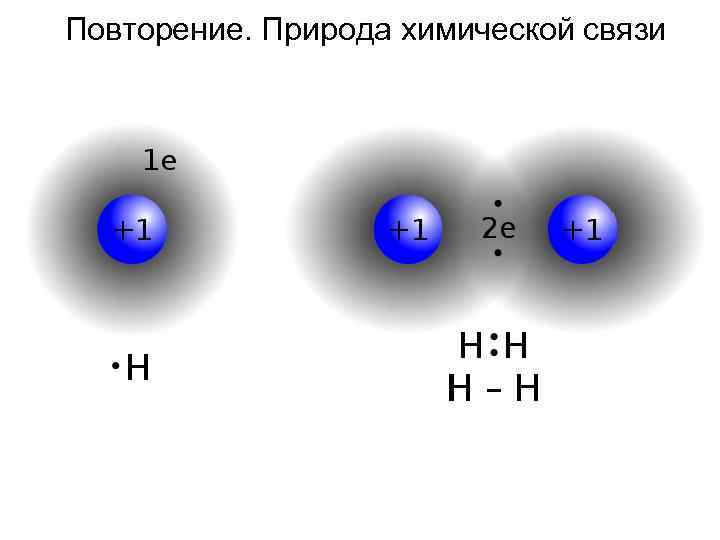
Повторение. Природа химической связи
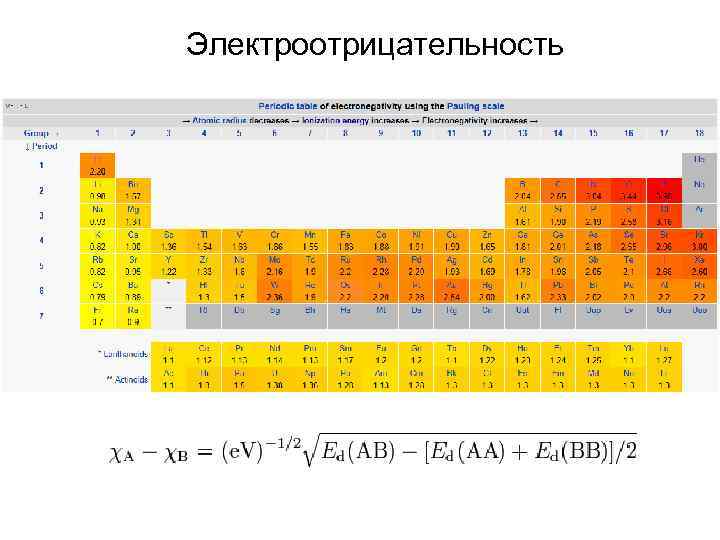
Электроотрицательность
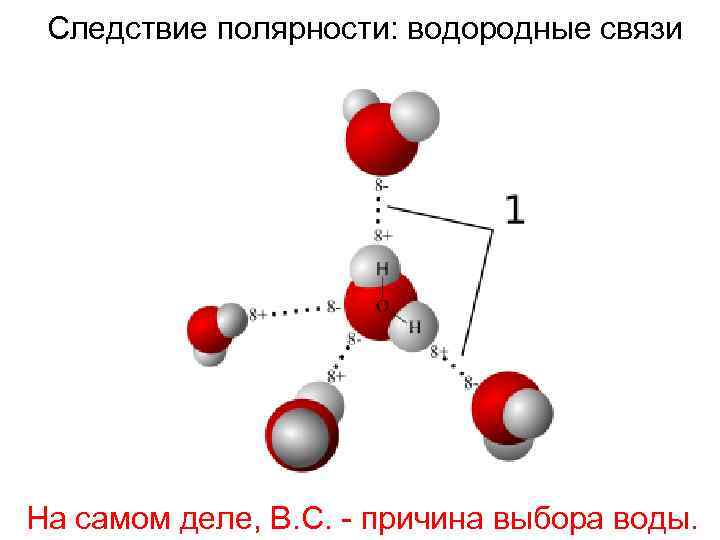
Следствие полярности: водородные связи На самом деле, В. С. - причина выбора воды.
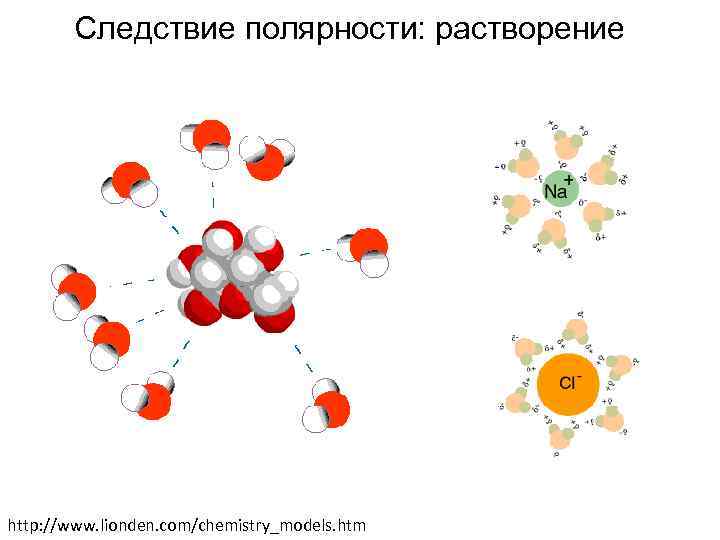
Следствие полярности: растворение http: //www. lionden. com/chemistry_models. htm
Выигрыш от полярности. Структура и взаимодействия Прочность материалов на макроскопическом уровне также определяется водородными связями.

Проблема: клеточная стенка 1. Стенка должна быть гибкой, прочной, избирательно проницаемой, легко увеличиваться при росте и легко рваться при делении, в идеале - самозатягивающейся 2. Если она будет нерастворимой (полиэтиленовый пакет или резиновая оболочка или кристалл) - не получится. Надо из динамически взаимодействующих молекул. 3. Если она будет из полярных молекул - то растворится 4. Если из неполярных, то они соберутся в капли. 5. Как быть?
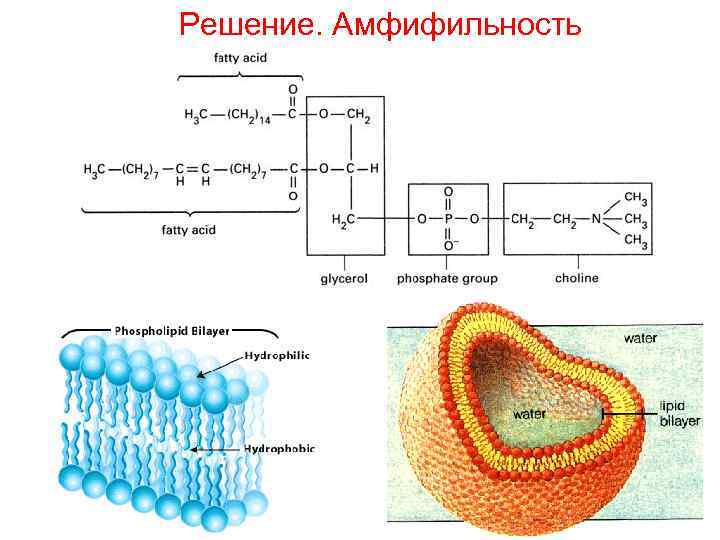
Решение. Амфифильность
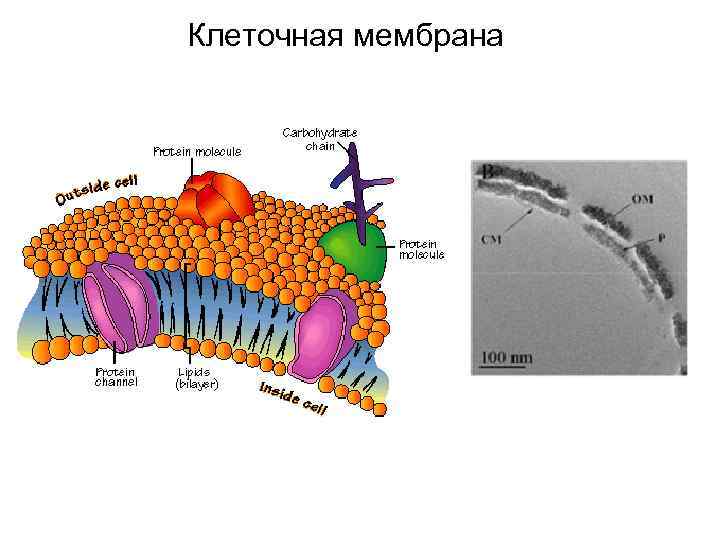
Клеточная мембрана

Проблема. Осмос
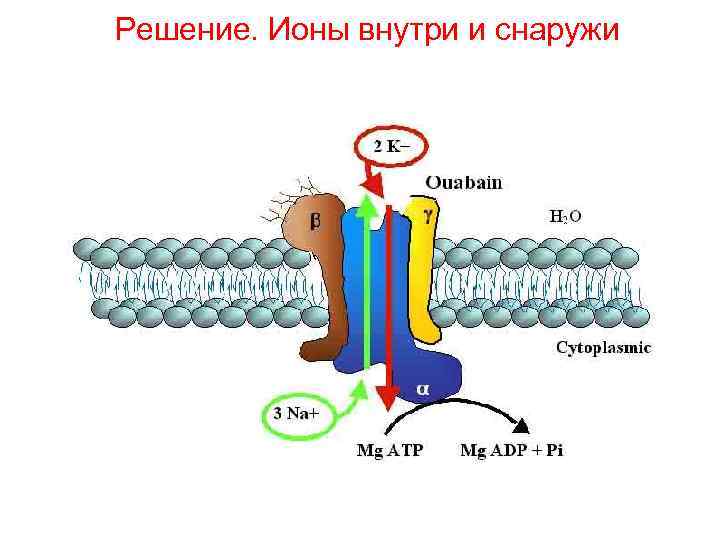
Решение. Ионы внутри и снаружи

Проблема. Долгосрочное хранение энергии

Решение. Гидрофильные нераствормые глобулы и гидрофобные капли

Феномен диссоциации воды

Выигрыш. Можно делать электростатику. Проблема. Стабильность условий The solvent accessible surface of calcineurin with the bound RII peptide, showing the electrostatic potential energy values calculated for the total protein. The center area is strongly positively charged (blue), surrounded by an area of neutral charge (white), and areas of negative charge (red).
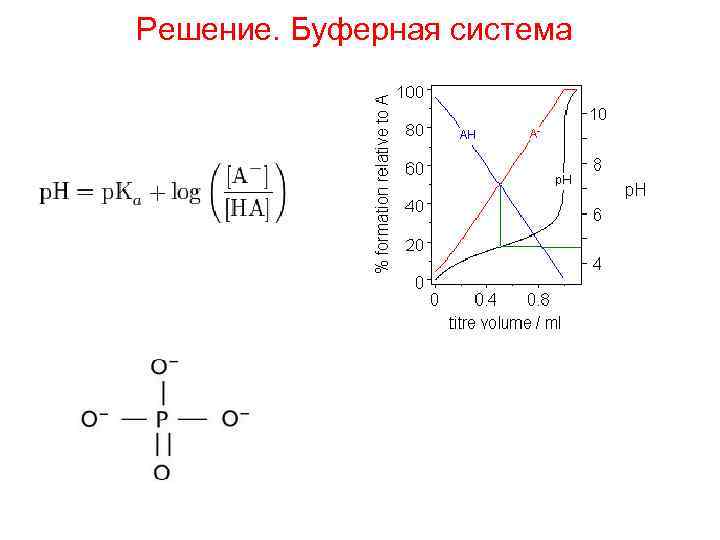
Решение. Буферная система

Проблема и решение. Оперативное хранение энергии

Итого по воде: 1. Стабильность и динамика ===> жидкость (т. е. конденсированная среда) 2. Конденсированная среда ===> ограниченность диффузии (т. е. клетки) 3. Нужда в связях ===> необходимость полярной жидкости 4. Полярность жидкости ===> полярность биомолекул 5. Полярность жидкости ===> бислойные амфифильные стенки клетки 6. Амфифильные динамические стенки ===> проблема осмоса 7. Проблема осмоса ===> ионный баланс 8. Проблема осмоса ===> углеводные глобулы и жиры 9. Диссоциация жидкости ===> возможность игр с зарядом биомолекул 10. Изменения заряда от p. H ===> необходимость в буферной системе 11. Буферная система ===> инструмент для оперативного хранения энергии Заметьте: мы даже еще не сказали, что жизнь на основе углерода, а уже можем столько всего предсказать на основе воды.

Дальнейшее развитие 1. Высокая концентрация ионов ===> близкодействие (в доли нм) и проблемы организации 2. Наличие ионов ===> солевые мостики, потенциал мембраны (ориентация белков положительным зарядом внутрь и возбудимость) 3. Диэлектрическая проницаемость ===> ослабление связей (на порядок) и проблема стабильности 4. Высокая температура, конденсированная среда ===> высокая частота столкновений (1013 -1014 в сек) и проблема стабильности 5. Как ускорять реакции и одновременно хранить данные ? ===> белки и ДНК 6. Как сделать систему так, чтобы она могла развиваться? ===> модульность и иерархия

Часть 1. 2 Химические элементы в живых системах

Какие требования к элементам? 1. Химические элементы должны уметь образовывать сложные биомолекулы 2. Биомолекулы должны быть стабильными и прочными 3. Но при этом активными, реакционно способными и динамическими, хотя бы кусками 4. Они должны быть полярными, а часто заряженными 5. Причем уметь образовывать заряды разного знака 6. Но при этом иногда гидрофобными, полностью или частично 7. И желательно быть доступными

Базовые понятия 1. Термодинамика против кинетики 2. Атака: нуклеофильность, электрофильность, радикалы 3. Как ускорять и изменять направление реакции: в принципе и в деталях 4. Энергия ионизации, сродство к электрону, электроотрицательность, редокс-потенциал
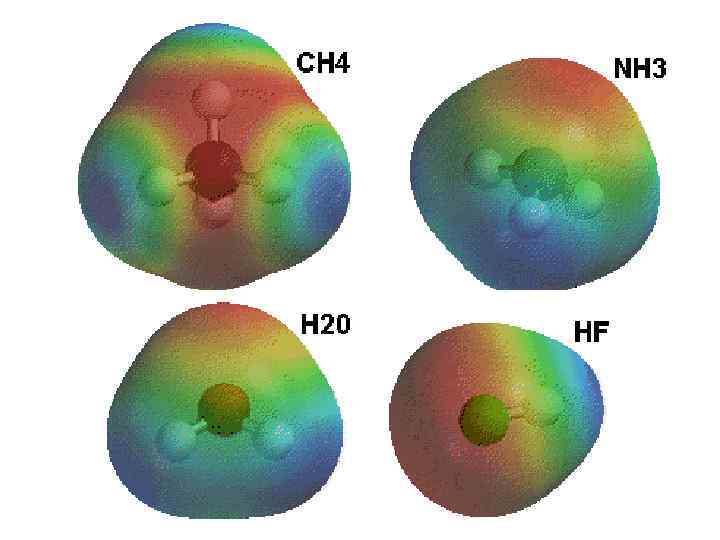


Категория 1: "Большая шестерка" 1. H, C, O, N, P, S 2. Вопрос на двойку: почему в ее составе нет благородных газов? 3. На тройку: а металлов? 4. На четверку: а галогенов? 5. На пятерку: а селен?
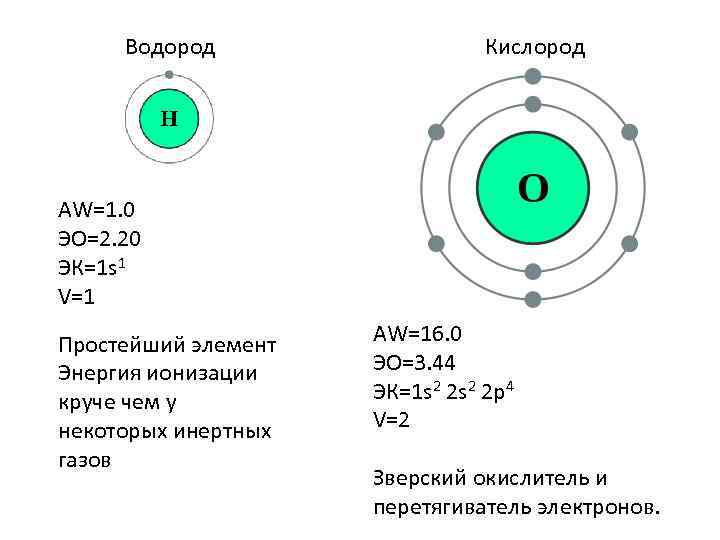
Водород Кислород AW=1. 0 ЭО=2. 20 ЭК=1 s 1 V=1 Простейший элемент Энергия ионизации круче чем у некоторых инертных газов AW=16. 0 ЭО=3. 44 ЭК=1 s 2 2 p 4 V=2 Зверский окислитель и перетягиватель электронов.

Углерод AW=12. 0 ЭО=2. 55 ЭК=1 s 2 2 p 2 V=4 Идеален для сложных структур, включая: цепочки, разветвления, двойные связи Неполярные соединения с водородом, полярные с кислородом Валентность равна координационному числу => экранирование Образует ковалентные связи со всеми.
Силикаты

Что можно сделать из H, O, C? 1. Углеводороды: простые, двойные связи, циклы, ароматика, сопряжение 2. Гидроксилы => спирты 3. Карбонилы => карбоновые кислоты 4. Альдегиды и кетоны => углеводы => энергетика и прочность 5. Эфиры и сложные эфиры => полисахариды и липиды

Азот AW=14. 0 ЭО=3. 04 ЭК=1 s 2 2 p 3 V=3
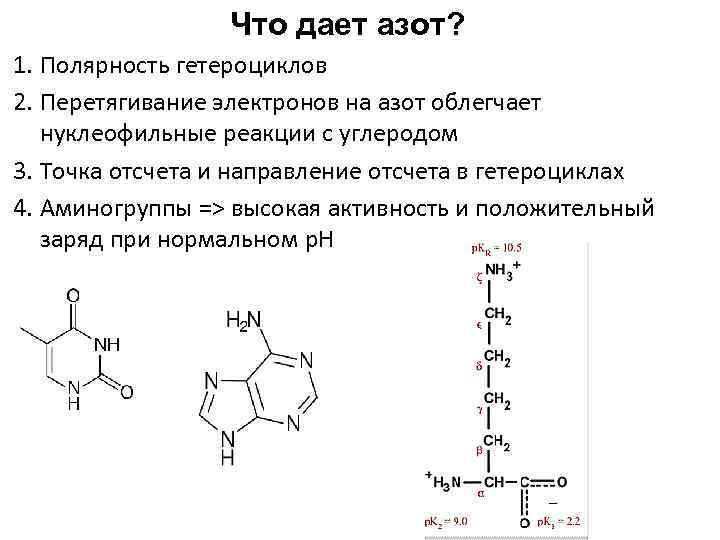
Что дает азот? 1. Полярность гетероциклов 2. Перетягивание электронов на азот облегчает нуклеофильные реакции с углеродом 3. Точка отсчета и направление отсчета в гетероциклах 4. Аминогруппы => высокая активность и положительный заряд при нормальном p. H

Сера AW=32. 0 ЭО=2. 58 ЭК=3 s 2 3 p 4 V=2

Что дает сера? 1. Двухвалентная молекула типа кислорода, только без его гадких свойств: связи слабее, полярность меньше, хилый окислитель 2. Сульфгидрильная группа: подвижный водород (просто оторвать), перенос ацетилов и метилов, серные мостики и другие окислительно-восстановительные вещи 3. Встречается в циклах.
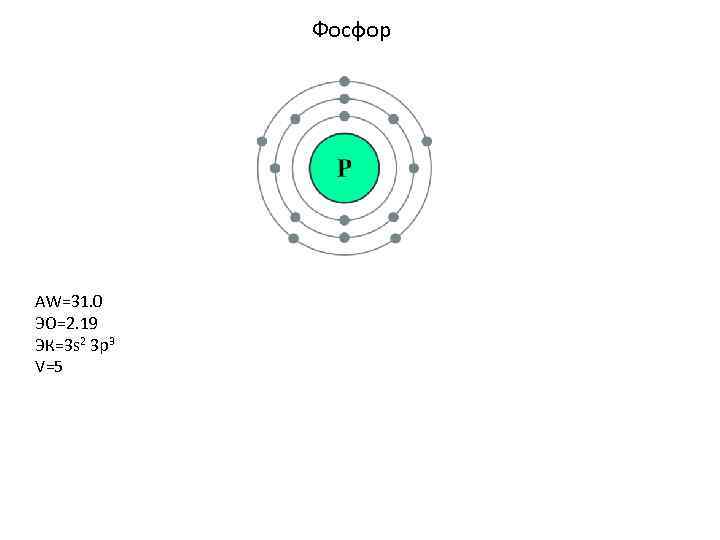
Фосфор AW=31. 0 ЭО=2. 19 ЭК=3 s 2 3 p 3 V=5

Что дает фосфор? 1. В отличие от азота, чаще пятивалентен. Обожает кислород и нестабилен в его присутствии. 2. Фосфаты со зверским зарядом => самый главный буфер, энергетика, регулятор, кости и мембраны 3. А почему не мышьяк?

Категория 2: Ионы Na+, K+, Cl-, Ca++, Mg++, Zn++ Зачем ионы? Почему металлы и как пролез хлор?

Что делают: 1. 2. 3. 4. 5. 6. Осмос (Na, K, Cl, Ca) Динамические мостики (Ca) Прочные комплексы (Ca, Mg) Сигнализация (Ca) Катализ (Mg, Zn) Регуляция p. H (Сl)
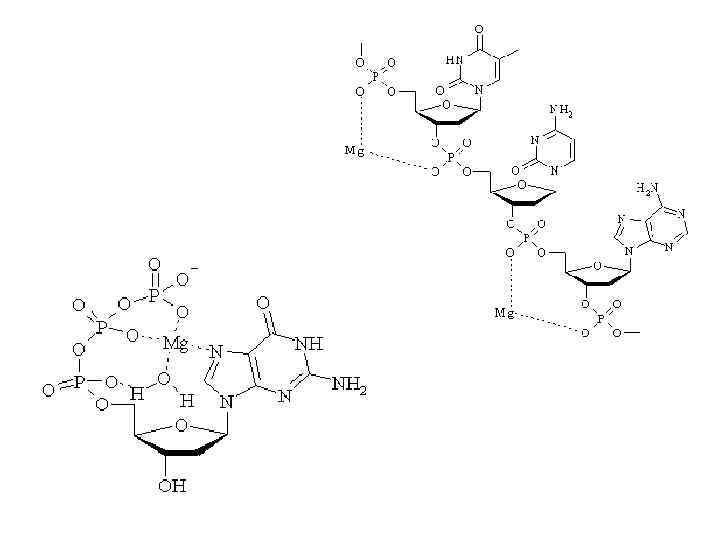
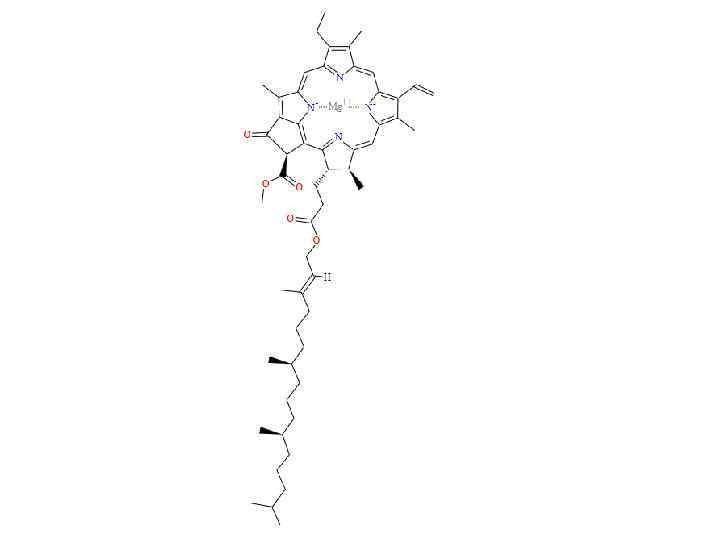

Категория 3: По мелочам Se - структуры, аналог серы и кислорода Fe - гемоглобин, цитохром, каталаза, азотфиксация и многие другие Cu - также транспорт и преобразование кислорода Co - витамин B-12, катализ Mo - катализ (азотфиксация); сложные отношения с О 2 Mn - катализ I - гормоны, что странно F - зубы
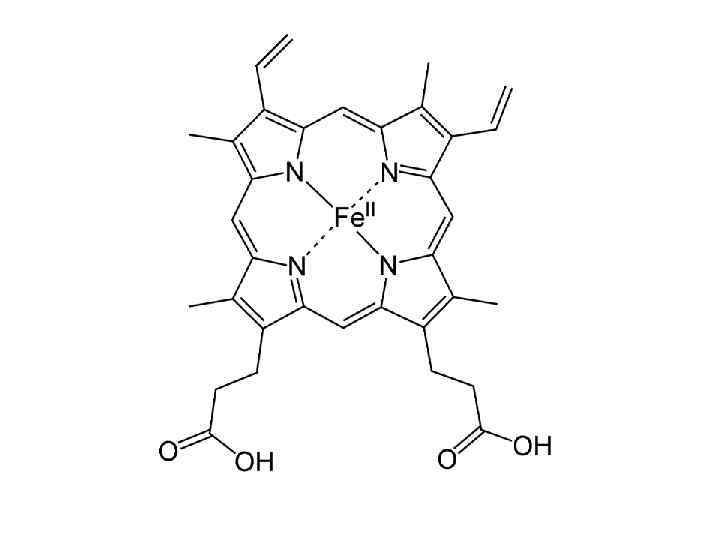


Категория 4: Раритеты As - энергетический метаболизм W - катализ Vd - замена железа и молибдена при азотфиксации, прочая экзотика Cd - замена цинку Br - экзотика Si - скелеты, прочая роль неясна Ni - катализ (уреаза)

Подводим итоги

Подводим итоги

Часть 1. 3 Активные группы и неактивные скелеты в биохимии

C-H связь 1. Неполярная: C=2. 55, H=2. 2 2. Сила связи: ~100 ккал/моль (103 для метана)=~400 к. Дж/моль (всего на 20% слабее тефлона, в 2 раза слабее азота) 3. Экранирована 4. Чем пробить?

http: //csi. chemie. tu-darmstadt. de/ak/immel/script/redirect. cgi? filename=http: //csi. chemie. tudarmstadt. de/ak/immel/tutorials/orbitals/molecular/methane. html


C-C связь 1. Неполярная, если только нет радикалов 2. Сила разрыва: ~85 ккал/моль или ~350 к. Дж/моль (при нагреве рвется раньше)

C=C связь 1. Неполярные 2. Формально прочнее: 611 к. Дж/моль против 350 3. Жесткие: структуры, фазовое состояние 4. Уязвимы к электрофильной атаке 5. Сопряженность: пигменты и транспорт электронов 6. Ароматика: структуры, связывание с гидрофобными 7. В чистом виде не бывает, как и предыдущие связи
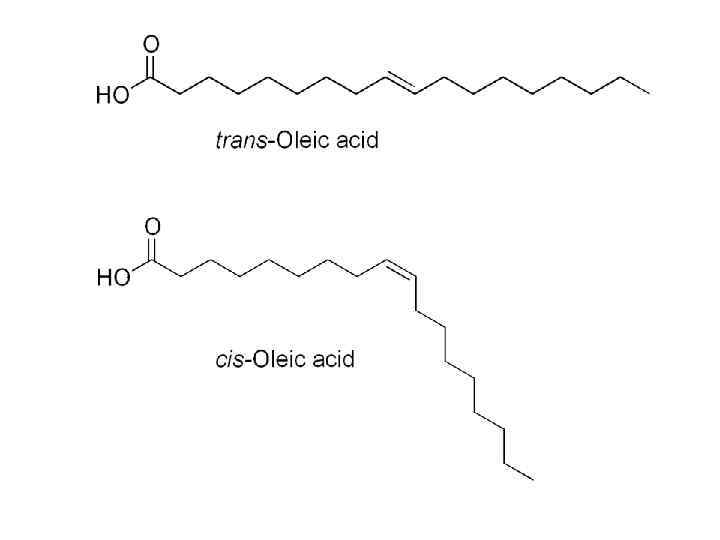
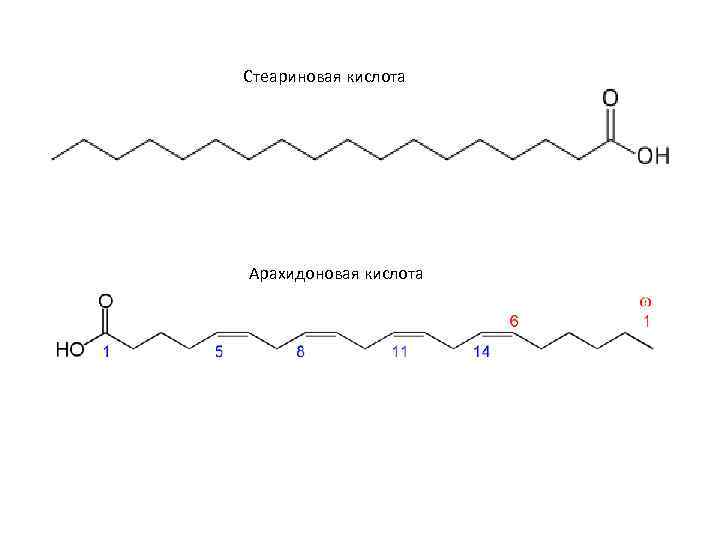
Стеариновая кислота Арахидоновая кислота


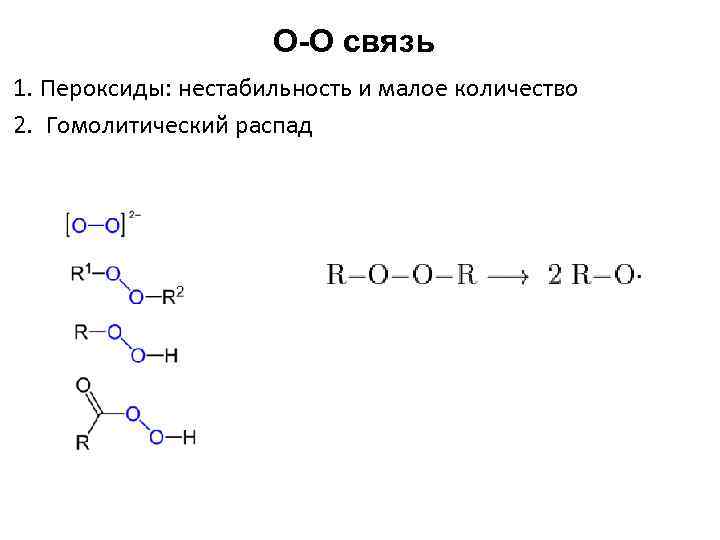
O-O связь 1. Пероксиды: нестабильность и малое количество 2. Гомолитический распад

O-H связь 1. Сила разрыва: ~110 ккал/моль или ~460 к. Дж/моль 2. Полярная: гидрофильность, депротонирование и фосфорилирование, протонирование и дегидратация в эфиры, окисление (дегидрогенация) в альдегиды и кетоны 3. Первые молекулы в нашем списке, которые реально есть в биологии: этанол, глицерин, ретинол 4. Составные части углеводов, аминокислот, витаминов, липидов
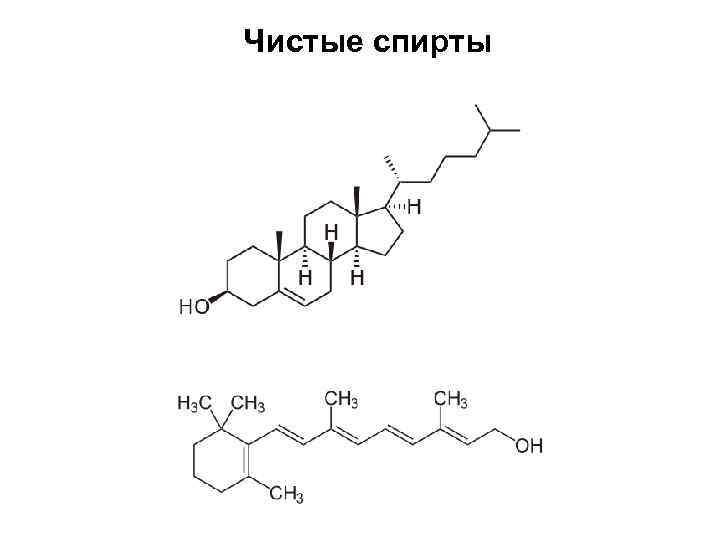
Чистые спирты
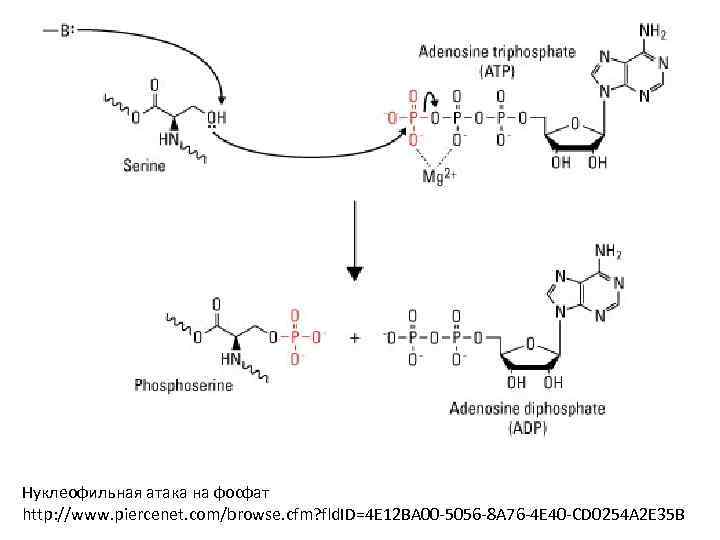
Нуклеофильная атака на фосфат http: //www. piercenet. com/browse. cfm? fld. ID=4 E 12 BA 00 -5056 -8 A 76 -4 E 40 -CD 0254 A 2 E 35 B

C=O связь 1. Сильно полярная 2. Плоская и потому уязвимая 3. Углерод особенно подвержен нуклеофильной атаке, а кислород - электрофильной 4. Углерод можно атаковать серой от цистеина, оторвать водород, затем атаковать водой и окислить в кислоту 5. Сшивки => эфиры 6. Сшивки => шиффовы основания
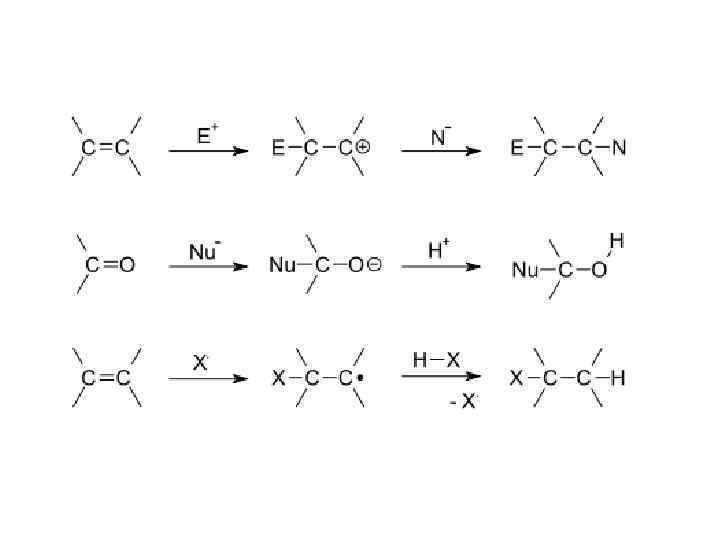

Альдегиды: углеводы Комбинация гидроксилов и карбонилов: растворимость, прочность, реактивность


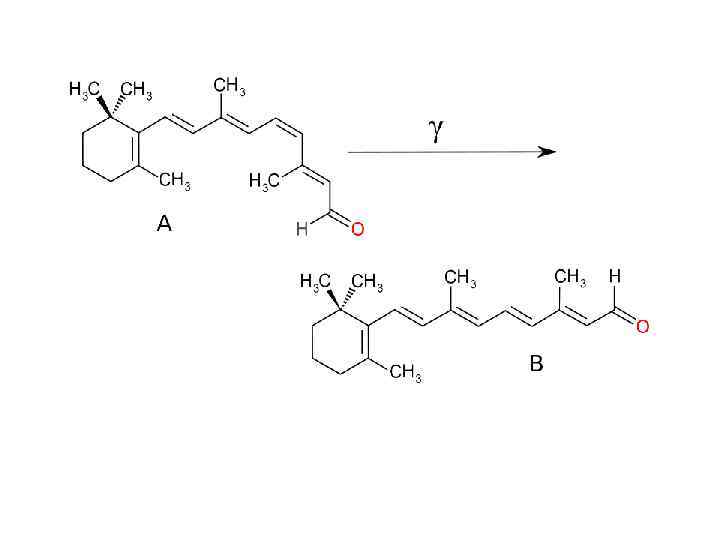

C-O связь 1. Резко полярная: C=2. 55, О=3. 44 2. Сила разрыва: ~87 -91 ккал/моль

Эфир 1. Эфиры реактивнее алканов, но вообще довольно инертны. 2. Зато полярны. 3. Поэтому в чистом виде типа C-O-C они нужны только для крепких связей (это была одна из причин привлечь азот для гетероколец). Например, хитин или лактоза или ДНК

Сложный эфир Эфиры можно "исправить" или точнее испортить, резко перекособочив электронную плотность около одного углерода. Сложные эфиры охотно поддаются нуклеофильной атаке.
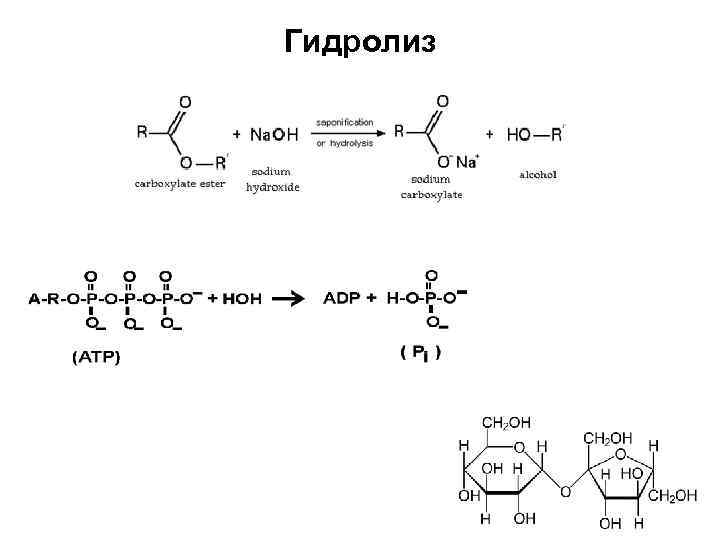
Гидролиз

Гидролиз амидной связи

Аминогруппа 1. Заряд 2. Нуклеофильность => присоединение ацилов (пептидная связь) 3. Ацетилирование, карбоксилирование, метилирование

Фосфат 1. Фосфор - электрофил 2. Буферные свойства 3. Заряд 4. Соли: зубы, кости и хитин
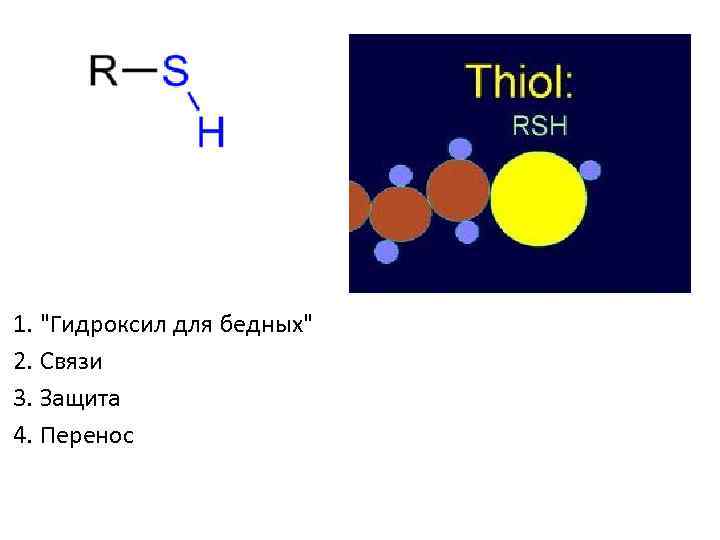
1. "Гидроксил для бедных" 2. Связи 3. Защита 4. Перенос

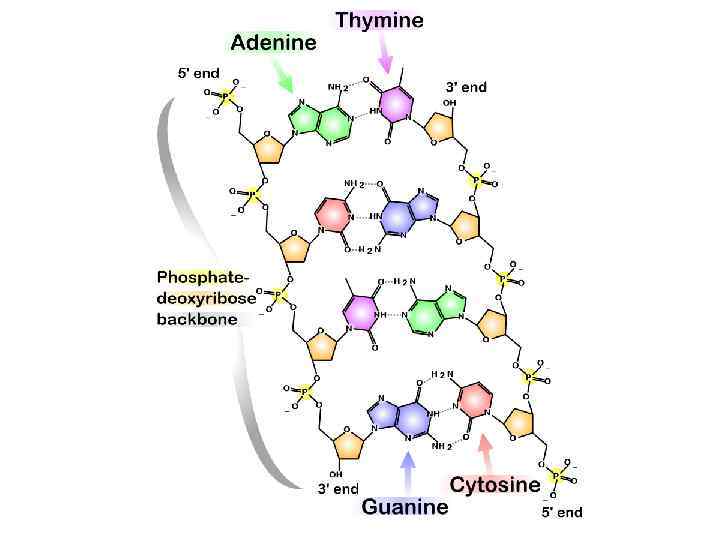

Упражнения


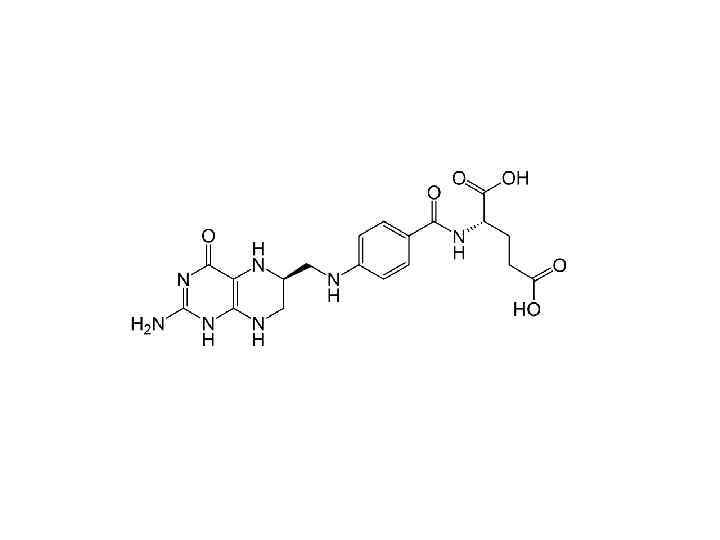

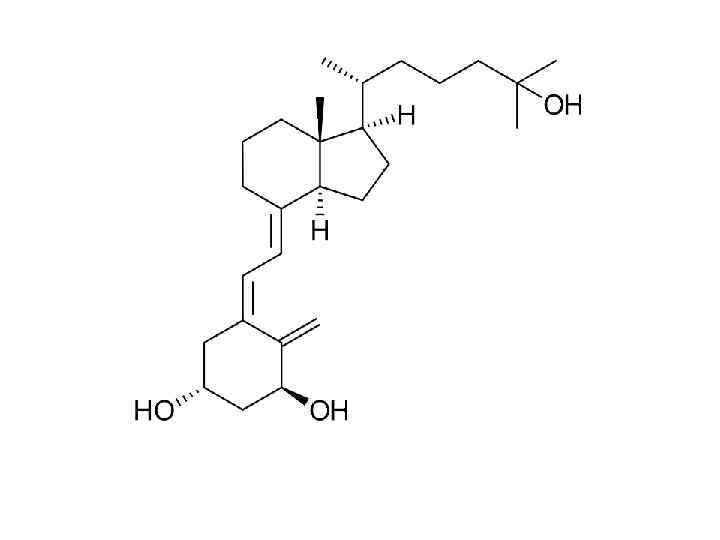

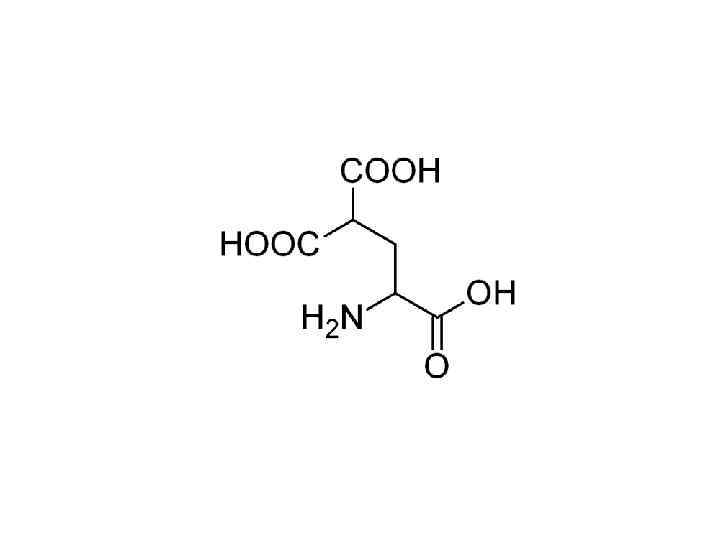
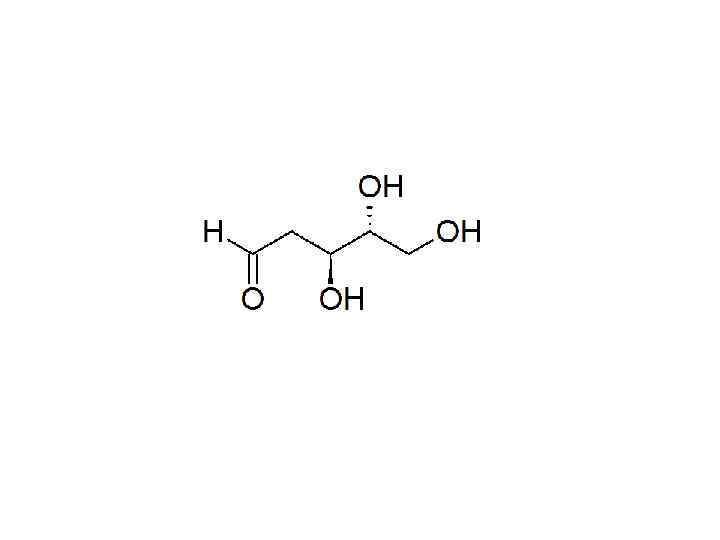


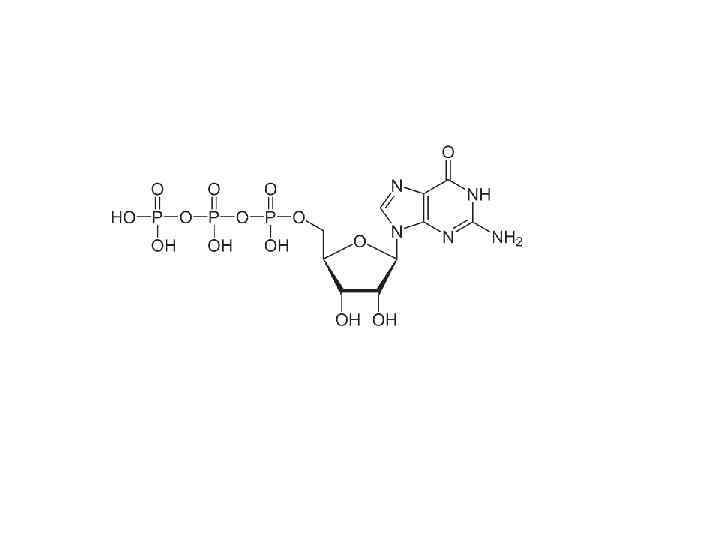

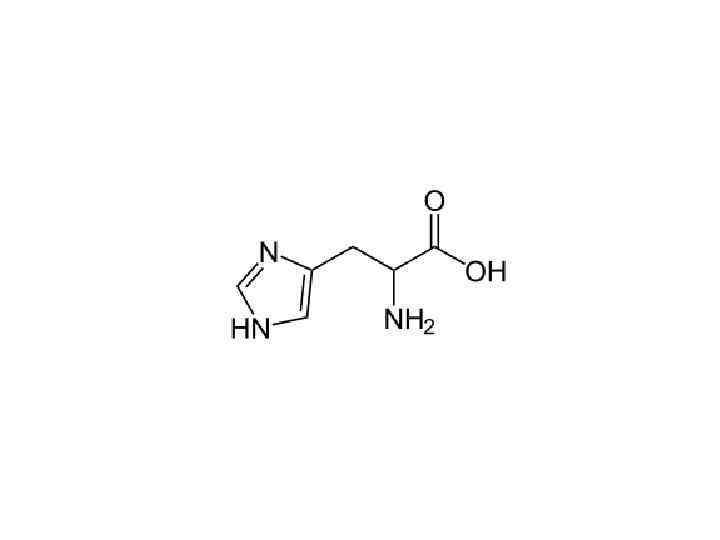


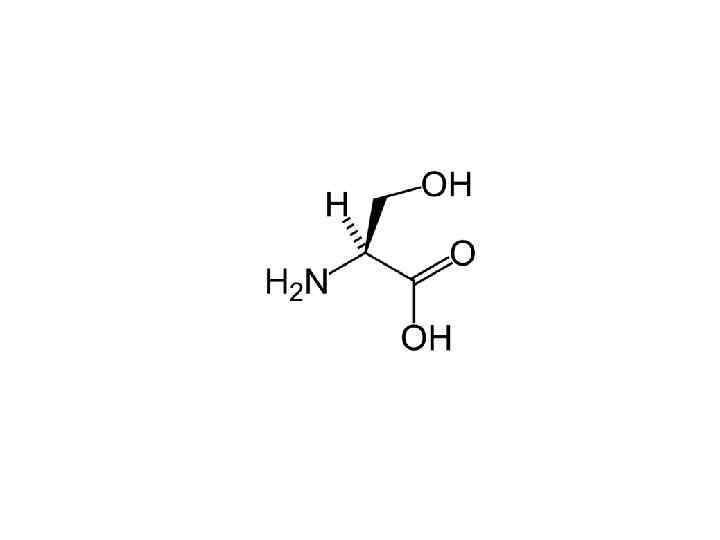
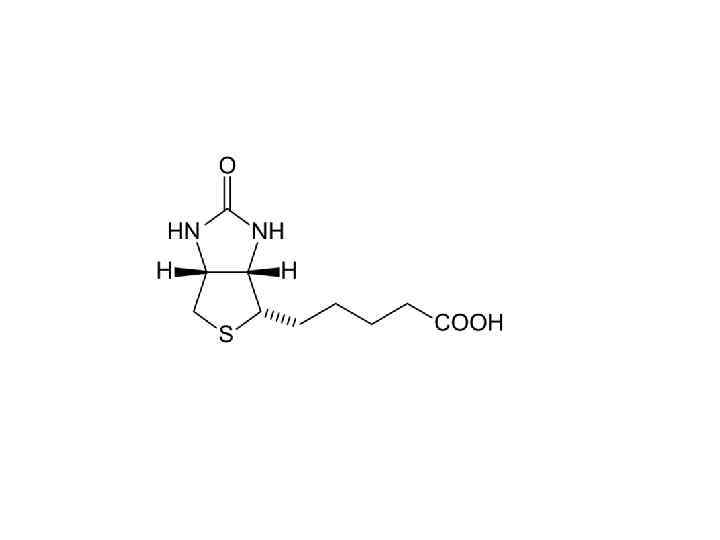


Комментарии 1 • Эти лекции делятся на три части и ориентировочно должны занимать 3 пары. • Нельзя знать биохимию, если имеешь проблемы с теорией валентности, физической химией воды или химической термодинамикой. • Темы валентной связи и молекулярных орбиталей, гибридизации, двойной связи , структуры атомов, вандерваальсовых и прочих взаимодействий, окислениявосстановления и т. п. в лекциях не раскрыты. • Если бы кто-то доверил мне создать жизнь на Земле, я бы тоже делал ее на водной основе. Вот за ее пределами возможны варианты. • Скорость химических реакций задает временной масштаб в биологии. Вместе со скоростью диффузии они задают пространственный масштаб клетки. • Углеводы крайне похожи на углеводороды. Если бы не проблема с полярностью, можно было бы пить бензин. • Кремний не подходит для создания жизни в присутствии кислорода и высоких температур. Вот на спутнике Юпитера, в океане ледяного аммиака вместо воды, можно было бы получить жизнь. Сероводород тоже сгодится, но он встречается реже; и диапазон температур для обоих уже (от -77 до -33 аммиак, от -80 до -60 сероводород). • Соединения мышьяка не заменяют фосфор из-за той же нестабильности. • А вообще тема углеродного и водного шовинизма не раскрыта

Комментарии 2 • Тема классификации химических реакций и групп не раскрыта до конца. В идеале, лекция (с возможным семинаром) должна быть доведена до такого состояния, что студент должен достаточно свободно оценивать из данных по полярности и общих соображений, как проходят атаки разными нуклеофилами-электрофилами-радикалами на любые типы атомов в молекуле, и что в итоге получится. • Тем не менее, какие-то элементарные вещи (типа того, что полярную молекулу логично атаковать нуклеофилом на положительный атом, а неполярную логично атаковать электрофильно) должны отложиться. • Тема окислительно-восстановительных процессов не раскрыта. • Биохимики гораздо меньше заморачиваются насчет механизмов реакций, чем органики. Во-первых, они их не знают, и в силу сложности ферментов вряд ли скоро узнают. Во-вторых, какая разница какой был порог реакции, если фермент его обходит и может посадить любую группу на любой атом? Но и совсем пренебрегать механизмами нельзя. • Вся органика неустойчива термодинамически. Но ее это не колышет. • Свободная энергия Гиббса должна быть тщательно описана и связана с энтропией, энтальпией, внутренней энергией и прочими смыслами. • Что определяет направление реакции? Две распространенные ошибки - стремление к минимуму энергии или к максимуму энтропии. Первое бессмысленно из-за закона сохранения (свечка в термосе будет гореть), второе бессмысленно для изолированной системы (лед в термосе не будет плавиться). Смысл Гиббса - как раз потенциал для реальной системы. Из нее видно, почему при низких температурах синтез, а при высоких распад

• В алканах атом углерода отлично экранирован, отсюда проблемы. Пробить можно только галогенами или радикалами. Фторуглероды еще круче. • Двойные связи не разобраны в плане электронной структуры. • Ароматику можно нарисовать на примере фенилаланина, а потом его переделать в тирозин (кислород великое дело), и на нем показать фосфорилирование d. Sw=d. Si+d. So>0 For isothermic: d. Si+Qo/T=d. Si-Qi/T>0 For Isobaric: Q=d. U+pd. V From this: Td. S-d. U-pd. V>0 Change of U+p. V-TS<0 Но в принципе Яковенко и Шведов должны это читать, надо узнать когда. • Группы и реакции готовились в спешке, стоит тщательно просмотреть на предмет упущенного. Так, аминогруппы разобраны, а поведение азота в гетероцикле и двойных связях нет (хотя есть дублирование с описанием элемента).

Комментарии 4 • Практически все витамины - это извращенные молекулы, необходимые для работы с неудобными группами и связями. Предшественники коферментов. ТГФ - метилы, Ко. А ацетат, Вит. К - карбоксил на углерод, Биотин - СО 2. Исключения тоже есть, та же аскорбинка не делается только от лени, а витамин Д - от идиотизма. • Упускаю разбор важных крупных групп: фенилы, разные гетероциклы, имидазолы, имины. Компенсировать при следующей итерации. • Разобраться с синглетным кислородом, супероксид-радикалом и механизмами его наработки • В конце стоит сделать упражнение: порисовать молекулы и пообсуждать их свойства. Варианты: липоевая кислота (все идеально выводится из формулы). • "Косяки эволюции" - йод-содержащие гормоны и витамин Д. Бессмысленно так извращаться с сигнальными молекулами. А все из-за принципа "я тебя слепила из того, что было". • Дружба и гидролиз амина и карбонила стоит раскрыть подробнее, особенно в плане когда там нужна и не нужна АТФ (амиды против шиффовых оснований), и для чего. • Тема макроэргичности: не только АТФ, но и карбамоилфосфат, и креатинфосфат. Механизмы: разрыв, неравновесность, резонансные структуры, буферные свойства.

Типичные группы в биохимии и их реакции
01 Физико-химические основы жизни.pptx