Химическая коррозия металлов Лекция 2.ppt
- Количество слайдов: 16
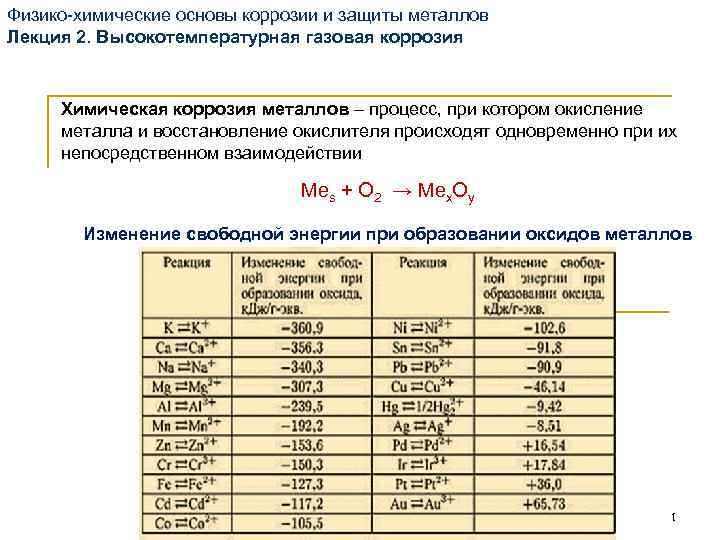 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Химическая коррозия металлов – процесс, при котором окисление металла и восстановление окислителя происходят одновременно при их непосредственном взаимодействии Mes + O 2 → Mex. Oy Изменение свободной энергии при образовании оксидов металлов 1
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Химическая коррозия металлов – процесс, при котором окисление металла и восстановление окислителя происходят одновременно при их непосредственном взаимодействии Mes + O 2 → Mex. Oy Изменение свободной энергии при образовании оксидов металлов 1
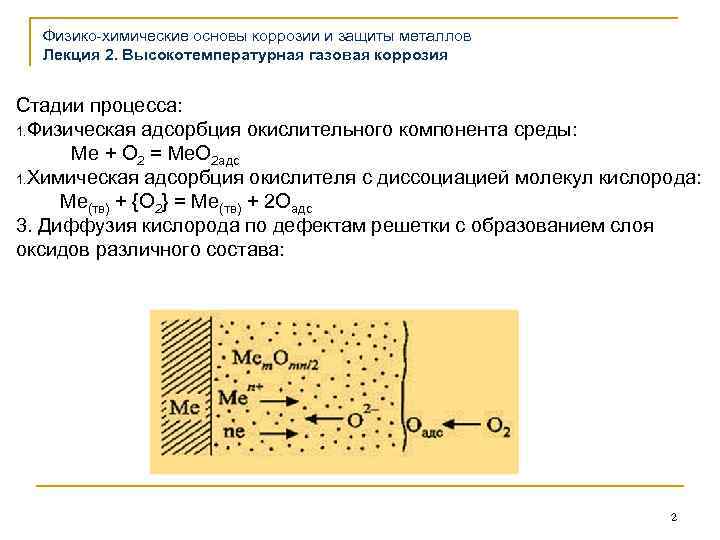 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Стадии процесса: 1. Физическая адсорбция окислительного компонента среды: Me + O 2 = Me. O 2 адс 1. Химическая адсорбция окислителя с диссоциацией молекул кислорода: Me(тв) + {O 2} = Me(тв) + 2 Oадс 3. Диффузия кислорода по дефектам решетки с образованием слоя оксидов различного состава: 2
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Стадии процесса: 1. Физическая адсорбция окислительного компонента среды: Me + O 2 = Me. O 2 адс 1. Химическая адсорбция окислителя с диссоциацией молекул кислорода: Me(тв) + {O 2} = Me(тв) + 2 Oадс 3. Диффузия кислорода по дефектам решетки с образованием слоя оксидов различного состава: 2
 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Оксидные слои на железе: 3
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Оксидные слои на железе: 3
 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Характеристики оксидов железа: Fe. O – вюстит – черный порошок, не обладает защитными свойствами. При высокотемпературной газовой коррозии образуется Fe 0, 8 -0, 9 O, по вакансиям кристаллической решетки кислород проникает под слой оксида. Fe 2 O 3 – гематит – желто-коричневого цвета. Существует в широком интервале температур, но выше 1100 ° С частично диссоциирует, используется в качестве пигмента. Fe. O • Fe 2 O 3 или Fe 3 O 4 – магнетит, обладает магнитными свойствами и электронной проводимостью, дефекты в структуре оксида обеспечивает легкость перехода электрона от одного катионного узла к другому. Магнетит устойчив во всем интервале температур от комнатной до точки плавления железа (1538 °С). Обладает высокими защитными свойствами. 4
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Характеристики оксидов железа: Fe. O – вюстит – черный порошок, не обладает защитными свойствами. При высокотемпературной газовой коррозии образуется Fe 0, 8 -0, 9 O, по вакансиям кристаллической решетки кислород проникает под слой оксида. Fe 2 O 3 – гематит – желто-коричневого цвета. Существует в широком интервале температур, но выше 1100 ° С частично диссоциирует, используется в качестве пигмента. Fe. O • Fe 2 O 3 или Fe 3 O 4 – магнетит, обладает магнитными свойствами и электронной проводимостью, дефекты в структуре оксида обеспечивает легкость перехода электрона от одного катионного узла к другому. Магнетит устойчив во всем интервале температур от комнатной до точки плавления железа (1538 °С). Обладает высокими защитными свойствами. 4
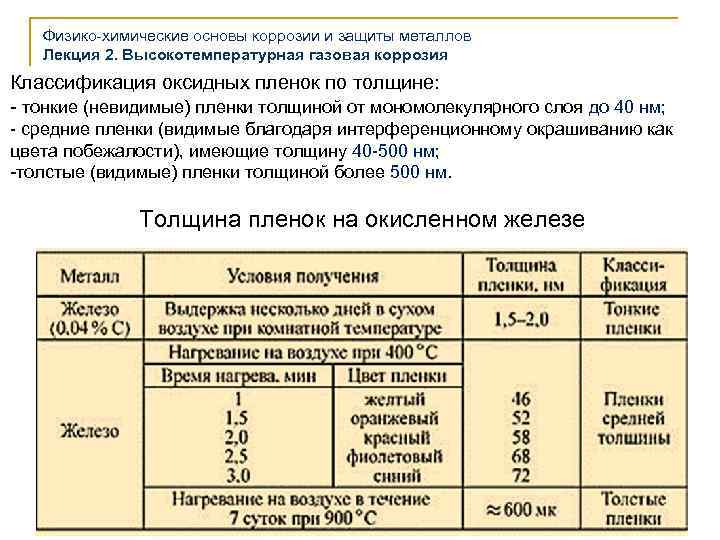 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Классификация оксидных пленок по толщине: - тонкие (невидимые) пленки толщиной от мономолекулярного слоя до 40 нм; - средние пленки (видимые благодаря интерференционному окрашиванию как цвета побежалости), имеющие толщину 40 -500 нм; -толстые (видимые) пленки толщиной более 500 нм. Толщина пленок на окисленном железе 5
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Классификация оксидных пленок по толщине: - тонкие (невидимые) пленки толщиной от мономолекулярного слоя до 40 нм; - средние пленки (видимые благодаря интерференционному окрашиванию как цвета побежалости), имеющие толщину 40 -500 нм; -толстые (видимые) пленки толщиной более 500 нм. Толщина пленок на окисленном железе 5
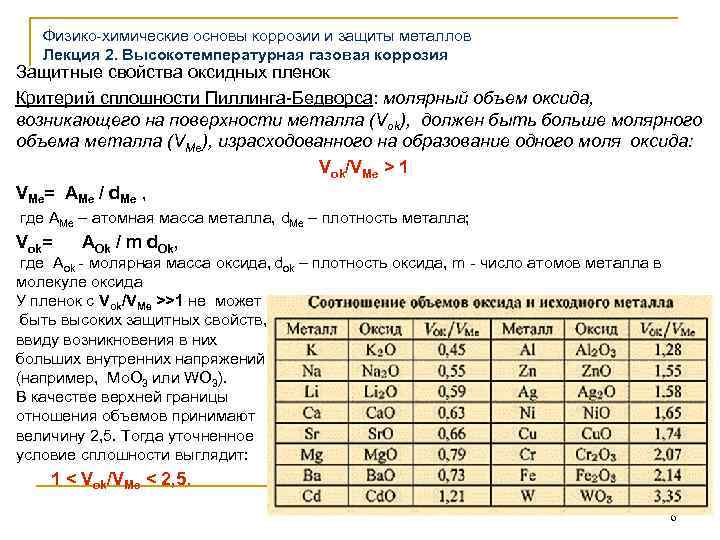 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Защитные свойства оксидных пленок Критерий сплошности Пиллинга-Бедворса: молярный объем оксида, возникающего на поверхности металла (Vok), должен быть больше молярного объема металла (VMe), израсходованного на образование одного моля оксида: Vok/VMe > 1 VMe= AMe / d. Me , где AMe – атомная масса металла, d. Me – плотность металла; Vok= AOk / m d. Ok, где Aok - молярная масса оксида, dok – плотность оксида, m - число атомов металла в молекуле оксида У пленок с Vok/VMe >>1 не может быть высоких защитных свойств, ввиду возникновения в них больших внутренних напряжений (например, Mo. O 3 или WO 3). В качестве верхней границы отношения объемов принимают величину 2, 5. Тогда уточненное условие сплошности выглядит: 1 < Vok/VMe < 2, 5. 6
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Защитные свойства оксидных пленок Критерий сплошности Пиллинга-Бедворса: молярный объем оксида, возникающего на поверхности металла (Vok), должен быть больше молярного объема металла (VMe), израсходованного на образование одного моля оксида: Vok/VMe > 1 VMe= AMe / d. Me , где AMe – атомная масса металла, d. Me – плотность металла; Vok= AOk / m d. Ok, где Aok - молярная масса оксида, dok – плотность оксида, m - число атомов металла в молекуле оксида У пленок с Vok/VMe >>1 не может быть высоких защитных свойств, ввиду возникновения в них больших внутренних напряжений (например, Mo. O 3 или WO 3). В качестве верхней границы отношения объемов принимают величину 2, 5. Тогда уточненное условие сплошности выглядит: 1 < Vok/VMe < 2, 5. 6
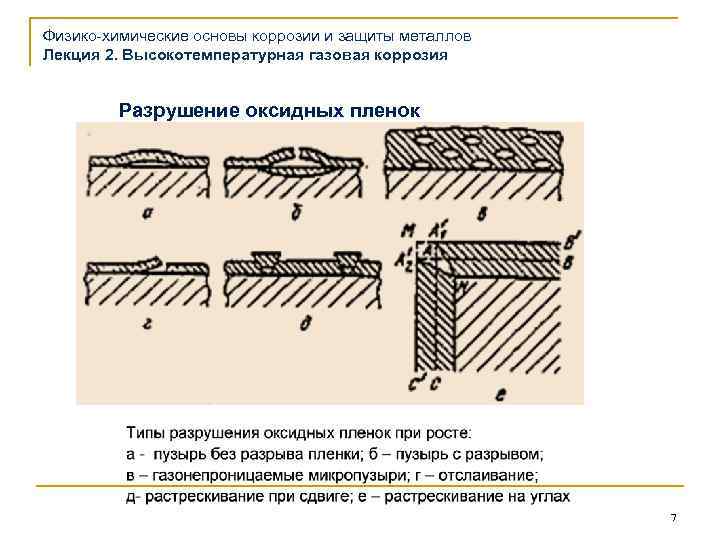 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Разрушение оксидных пленок 7
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Разрушение оксидных пленок 7
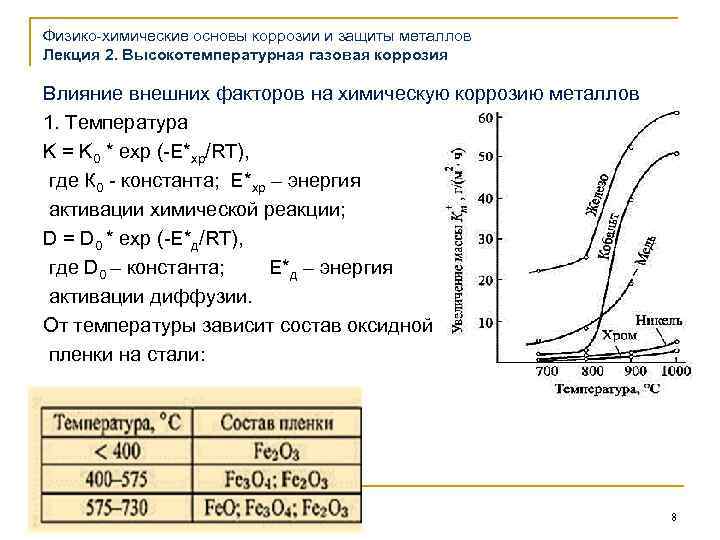 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внешних факторов на химическую коррозию металлов 1. Температура K = K 0 * exp (-E*хp/RT), где К 0 - константа; Е*хp – энергия активации химической реакции; D = D 0 * exp (-E*д/RT), где D 0 – константа; Е*д – энергия активации диффузии. От температуры зависит состав оксидной пленки на стали: 8
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внешних факторов на химическую коррозию металлов 1. Температура K = K 0 * exp (-E*хp/RT), где К 0 - константа; Е*хp – энергия активации химической реакции; D = D 0 * exp (-E*д/RT), где D 0 – константа; Е*д – энергия активации диффузии. От температуры зависит состав оксидной пленки на стали: 8
 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внешних факторов на химическую коррозию металлов 2. Состав газовой фазы Важнейшие окислители металлов при высоких температурах – О 2, СО 2, Н 2 О(пар), SO 2: 2 Me + O 2 → 2 Me. O, Me + CO 2 → Me. O + CO, Me + H 2 O → Me. O + H 2, 3 Me + SO 2 → 2 Me. O + Me. S, В атмосферах, содержащих O 2, CO 2 и Н 2 О, может происходить обезуглероживание (декарбонизация): Fe 3 C + 1/2 O 2 → 3 Fe + CO, Fe 3 C + CO 2 → 3 Fe + 2 CO, Fe 3 C + H 2 O → 3 Fe + CO + H 2 V 2 O 5 способен офлюсовывать (переводить в жидкое состояние) химические соединения золы и окалины: 4 Fe + 3 V 2 O 5 = 2 Fe 2 O 3 + V 2 O 3, V 2 O 3 + O 2 = V 2 O 5, V 2 O 5 + Fe 2 O 3 = 2 Fe. VO 4. 9
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внешних факторов на химическую коррозию металлов 2. Состав газовой фазы Важнейшие окислители металлов при высоких температурах – О 2, СО 2, Н 2 О(пар), SO 2: 2 Me + O 2 → 2 Me. O, Me + CO 2 → Me. O + CO, Me + H 2 O → Me. O + H 2, 3 Me + SO 2 → 2 Me. O + Me. S, В атмосферах, содержащих O 2, CO 2 и Н 2 О, может происходить обезуглероживание (декарбонизация): Fe 3 C + 1/2 O 2 → 3 Fe + CO, Fe 3 C + CO 2 → 3 Fe + 2 CO, Fe 3 C + H 2 O → 3 Fe + CO + H 2 V 2 O 5 способен офлюсовывать (переводить в жидкое состояние) химические соединения золы и окалины: 4 Fe + 3 V 2 O 5 = 2 Fe 2 O 3 + V 2 O 3, V 2 O 3 + O 2 = V 2 O 5, V 2 O 5 + Fe 2 O 3 = 2 Fe. VO 4. 9
 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внешних факторов на химическую коррозию металлов 3. Давление окислителя Так как поверхность металла покрыта слоем оксида, то зависимость скорости окисления от величины парциального давления окисляющей газа может быть различной в зависимости от строения защитной пленки. Например, при окислении железа при 700 -950 о. С скорость окисления не зависит от Po 2. 4. Скорость движения газовой фазы Окисление, как гетерогенный процесс, определяется скоростью подвода и отвода реагентов в зону реакции. Поэтому, чем больше скорость движения потока газа, тем больше и скорость окисления металла. 5. Режим нагрева металла Влияние режима нагрева металла может быть рассмотрено в контексте влияния колебаний температуры. То есть переменные нагрев и охлаждение увеличивают скорость окисления ввиду нарушения сохранности защитной пленки. 10
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внешних факторов на химическую коррозию металлов 3. Давление окислителя Так как поверхность металла покрыта слоем оксида, то зависимость скорости окисления от величины парциального давления окисляющей газа может быть различной в зависимости от строения защитной пленки. Например, при окислении железа при 700 -950 о. С скорость окисления не зависит от Po 2. 4. Скорость движения газовой фазы Окисление, как гетерогенный процесс, определяется скоростью подвода и отвода реагентов в зону реакции. Поэтому, чем больше скорость движения потока газа, тем больше и скорость окисления металла. 5. Режим нагрева металла Влияние режима нагрева металла может быть рассмотрено в контексте влияния колебаний температуры. То есть переменные нагрев и охлаждение увеличивают скорость окисления ввиду нарушения сохранности защитной пленки. 10
 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внутренних факторов на химическую коррозию металлов 1. Состав сплава При высоких температурах (более 800 о. С) с увеличением содержания C в стали скорость ее окисления и обезуглероживания уменьшается вследствие более активного образования СО, что снижает окислительный потенциал газовой фазы. S, P, Ni, Mn практически не влияют на скорость окисления железа. Ti, Cu, Co, Be заметно снижают скорость окисления железа. Cr, Al, Si сильно замедляют окисление железа. V, W и Mo могут значительно ускорить окисление стали, которое иногда носит катастрофический характер. 11
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внутренних факторов на химическую коррозию металлов 1. Состав сплава При высоких температурах (более 800 о. С) с увеличением содержания C в стали скорость ее окисления и обезуглероживания уменьшается вследствие более активного образования СО, что снижает окислительный потенциал газовой фазы. S, P, Ni, Mn практически не влияют на скорость окисления железа. Ti, Cu, Co, Be заметно снижают скорость окисления железа. Cr, Al, Si сильно замедляют окисление железа. V, W и Mo могут значительно ускорить окисление стали, которое иногда носит катастрофический характер. 11
 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внутренних факторов на химическую коррозию металлов 2. Структура сплава Чем меньше в сплаве структурных составляющих, тем выше его жаростойкость. Применительно к сплавам железо – углерод, наиболее устойчивой является аустенитная структура, обладающая более плотной упаковкой. Стали с двухфазной аустенитно – ферритной структурой менее устойчивы против окисления. Их меньшая жаростойкость связывается с большей неоднородностью образующейся защитной пленки, что приводит к ее разрушению при росте (неоднородность возникающих внутренних напряжений). Хромо - никелевые стали с однофазной аустенитной структурой более устойчивы против окисления, чем двухфазные: Х 12 Н 12 М 2 Т, Х 12 Н 9 Т ведут себя лучше, чем ОХ 21 Н 5 МД 2 Т, 1 Х 21 Н 5 Т. Чугуны с шаровидной форме графита более стойкие, чем с пластинчатой. 12
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Влияние внутренних факторов на химическую коррозию металлов 2. Структура сплава Чем меньше в сплаве структурных составляющих, тем выше его жаростойкость. Применительно к сплавам железо – углерод, наиболее устойчивой является аустенитная структура, обладающая более плотной упаковкой. Стали с двухфазной аустенитно – ферритной структурой менее устойчивы против окисления. Их меньшая жаростойкость связывается с большей неоднородностью образующейся защитной пленки, что приводит к ее разрушению при росте (неоднородность возникающих внутренних напряжений). Хромо - никелевые стали с однофазной аустенитной структурой более устойчивы против окисления, чем двухфазные: Х 12 Н 12 М 2 Т, Х 12 Н 9 Т ведут себя лучше, чем ОХ 21 Н 5 МД 2 Т, 1 Х 21 Н 5 Т. Чугуны с шаровидной форме графита более стойкие, чем с пластинчатой. 12
 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Методы защиты от газовой коррозии 1. Контролируемые и защитные атмосферы газовые среды из технически чистого азота, гелия, аргона и других инертных газов; азот и влажный водород(N 2+H 2/H 2 O); эту газовую смесь получают диссоциацией аммиака и дожиганием образовавшегося при диссоциации водорода; азот, моно- и диоксид углерода(N 2+СO/CO 2); данную газовую смесь получают в древесноугольных генераторах; азот, влажный водород, моно – и диоксид углерода (N 2+H 2/H 2 O+СO/CO 2): эта атмосфера - продукт неполного сгорания углеводородов; азот, моно- и диоксид углерода, метан, водород (N 2, СO/CO 2, CH 4/H 2); эта науглероживающая атмосфера, выполняющая кроме защитных функций и роль науглероживающей. 13
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Методы защиты от газовой коррозии 1. Контролируемые и защитные атмосферы газовые среды из технически чистого азота, гелия, аргона и других инертных газов; азот и влажный водород(N 2+H 2/H 2 O); эту газовую смесь получают диссоциацией аммиака и дожиганием образовавшегося при диссоциации водорода; азот, моно- и диоксид углерода(N 2+СO/CO 2); данную газовую смесь получают в древесноугольных генераторах; азот, влажный водород, моно – и диоксид углерода (N 2+H 2/H 2 O+СO/CO 2): эта атмосфера - продукт неполного сгорания углеводородов; азот, моно- и диоксид углерода, метан, водород (N 2, СO/CO 2, CH 4/H 2); эта науглероживающая атмосфера, выполняющая кроме защитных функций и роль науглероживающей. 13
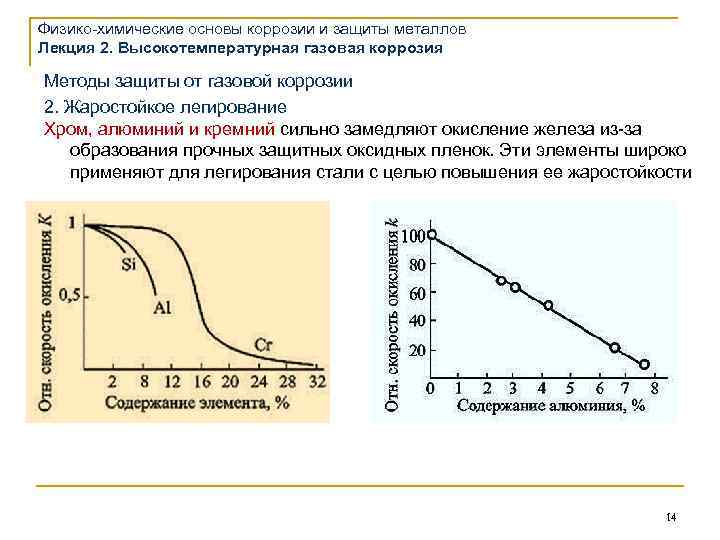 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Методы защиты от газовой коррозии 2. Жаростойкое легирование Хром, алюминий и кремний сильно замедляют окисление железа из-за образования прочных защитных оксидных пленок. Эти элементы широко применяют для легирования стали с целью повышения ее жаростойкости 14
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Методы защиты от газовой коррозии 2. Жаростойкое легирование Хром, алюминий и кремний сильно замедляют окисление железа из-за образования прочных защитных оксидных пленок. Эти элементы широко применяют для легирования стали с целью повышения ее жаростойкости 14
 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Методы защиты от газовой коррозии 3. Поверхностное легирование – термодиффузионное насыщение легирующим элементом поверхности защищаемого металла. 3. 1. Алитирование - процесс насыщения поверхностного слоя защищаемого материала алюминием. Покрываемый металл загружают в реактор, засыпают реакционной смесью (50%Al-порошка , 45 -48% Al 2 O 3 и 2 -5% NH 4 Cl) и помещают в нагревательное устройство (печь). Время выдержки 3 -4 часа, температура 950 -1000 о. С. 3. 2. Термохромирование - процесс насыщения поверхностного слоя защищаемого материала хромом. Покрываемый металл засыпают реакционной смесью (Crпорошка , каолина (Al 2 O 3 • 2 Si. O 2 • 2 H 2 O) и NH 4 Cl) и нагревают при температуре 1000 -1500 о. С. Процесс продолжается 8— 16 часов. За это время получают слой толщиной 50 -200 мкм. Содержание хрома во внешнем слое покрытия превышает 50 % и состав слоя представляет собой твердый раствор Fe-Cr. 15
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Методы защиты от газовой коррозии 3. Поверхностное легирование – термодиффузионное насыщение легирующим элементом поверхности защищаемого металла. 3. 1. Алитирование - процесс насыщения поверхностного слоя защищаемого материала алюминием. Покрываемый металл загружают в реактор, засыпают реакционной смесью (50%Al-порошка , 45 -48% Al 2 O 3 и 2 -5% NH 4 Cl) и помещают в нагревательное устройство (печь). Время выдержки 3 -4 часа, температура 950 -1000 о. С. 3. 2. Термохромирование - процесс насыщения поверхностного слоя защищаемого материала хромом. Покрываемый металл засыпают реакционной смесью (Crпорошка , каолина (Al 2 O 3 • 2 Si. O 2 • 2 H 2 O) и NH 4 Cl) и нагревают при температуре 1000 -1500 о. С. Процесс продолжается 8— 16 часов. За это время получают слой толщиной 50 -200 мкм. Содержание хрома во внешнем слое покрытия превышает 50 % и состав слоя представляет собой твердый раствор Fe-Cr. 15
 Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Методы защиты от газовой коррозии 3. Поверхностное легирование 3. 3. Силицирование - процесс насыщения поверхностного слоя защищаемого материала кремнием. Силицирование осуществляется при температуре 1000 -1200 о. С. Активная среда – смесь порошкообразного кремния или ферросилиция с NH 4 Cl. Силицирование – надежный способ предохранения от газовой коррозии тугоплавких металлов (Nb, W, Mo, Ta и др. ). Стойкость образующегося покрытия объясняется образованием плотных силицидных покрытий (WSi 2, Mo. Si 2), обладающих эффектом самозалечивания. 4. Неорганические металлические покрытия Из неметаллических неорганических покрытий для защиты стали и чугуна особенно большое значение имеет эмаль. Современные легкоплавкие эмали пригодны также для алюминия и иногда их используют в строительстве для деталей фасадов. Эмаль - это силикатное стекло с добавками оксидов металлов. Ее наносят на очищенную поверхность материала в виде порошка или взвеси и обжигают при 1000 °С. Температура плавления эмали для алюминия, содержащей много свинца, около 500 °С. Для хорошего прилипания, а значит, и устойчивости покрытий важно сблизить коэффициенты объемного расширения основного материала и покрытия. В последнее время получают развития ситалловые защитные покрытия, а также керамические на основе оксидной (Al 2 O 3 , Zn. O 2) или бескислородной керамики (Si. C, BN, Mo. Si 2). 16
Физико-химические основы коррозии и защиты металлов Лекция 2. Высокотемпературная газовая коррозия Методы защиты от газовой коррозии 3. Поверхностное легирование 3. 3. Силицирование - процесс насыщения поверхностного слоя защищаемого материала кремнием. Силицирование осуществляется при температуре 1000 -1200 о. С. Активная среда – смесь порошкообразного кремния или ферросилиция с NH 4 Cl. Силицирование – надежный способ предохранения от газовой коррозии тугоплавких металлов (Nb, W, Mo, Ta и др. ). Стойкость образующегося покрытия объясняется образованием плотных силицидных покрытий (WSi 2, Mo. Si 2), обладающих эффектом самозалечивания. 4. Неорганические металлические покрытия Из неметаллических неорганических покрытий для защиты стали и чугуна особенно большое значение имеет эмаль. Современные легкоплавкие эмали пригодны также для алюминия и иногда их используют в строительстве для деталей фасадов. Эмаль - это силикатное стекло с добавками оксидов металлов. Ее наносят на очищенную поверхность материала в виде порошка или взвеси и обжигают при 1000 °С. Температура плавления эмали для алюминия, содержащей много свинца, около 500 °С. Для хорошего прилипания, а значит, и устойчивости покрытий важно сблизить коэффициенты объемного расширения основного материала и покрытия. В последнее время получают развития ситалловые защитные покрытия, а также керамические на основе оксидной (Al 2 O 3 , Zn. O 2) или бескислородной керамики (Si. C, BN, Mo. Si 2). 16


