946a68b49c88e007603de05fd778b10a.ppt
- Количество слайдов: 25

Физико-химические методы исследования биологически активных веществ

Введение • Цель изучения дисциплины: формирование знаний, умений, навыков и • Структура курса: компетенций в области использования современных физико-химических методов для анализа медицинских препаратов на подлинность и количественного определения действующего вещества в препарате. Лекции 24 ч Лабораторные занятия 24 ч Самостоятельная работа 84 ч Экзамен Методическое обеспечение курса: • • • Сильверстейн Р. , Вебетер Ф. , Кимл Д. Спектрометрическая идентификация органических соединений. - М. : БИНОМ. Лаборатория знаний, - 2011. – 520 с. Преч Э. , Бюльманн Ф. , Аффольтер К. Определение строения органических соединений. М. : Мир. -2006. -439 с. (сетевые образовательные ресурсы в Web. CT каф. ОХОС). Беккер Ю. Хроматография. Инструментальная аналитика: методы хроматографии и капиллярного электрофореза. –М. : ТЕХНОСИЛА. 2009. -470 с. Краснокутская Е. А. Физико-химические методы анализа биологически активных веществ. Томск: -2005. -142 с. 5. Лебедев, А. Т. Масс-спектрометрия в органической химии. — М. : БИНОМ. Лаборатория знаний, 2003. — 493 с. (сетевые образовательные ресурсы в Web. CT каф. ОХОС). Персональный сайт Е. А. Краснокутской http: //portal. tpu. ru: 7777/SHARED/e/EAK

Лекция № 1 Спектральные методы исследования БАВ • Область применения спектральных методов • Электромагнитный спектр • Электронная, или УФ-спектроскопия – Возбуждение и релаксация
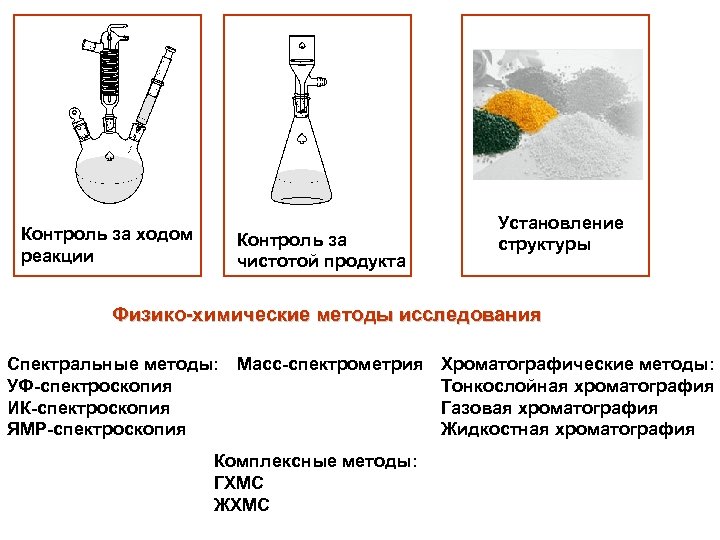
Контроль за ходом реакции Контроль за чистотой продукта Установление структуры Физико-химические методы исследования Спектральные методы: Масс-спектрометрия Хроматографические методы: УФ-спектроскопия Тонкослойная хроматография ИК-спектроскопия Газовая хроматография ЯМР-спектроскопия Жидкостная хроматография Комплексные методы: ГХМС ЖХМС
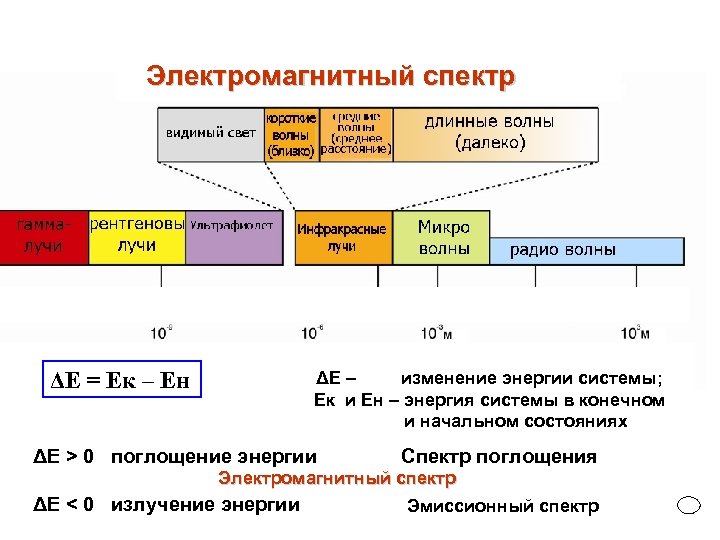
Электромагнитный спектр ΔЕ = Ек – Ен ΔЕ – изменение энергии системы; Ек и Ен – энергия системы в конечном и начальном состояниях ΔЕ > 0 поглощение энергии Спектр поглощения Электромагнитный спектр ΔЕ < 0 излучение энергии Эмиссионный спектр
![Электромагнитный спектр с= n с – скорость света [см/с] – длина волны [см], n Электромагнитный спектр с= n с – скорость света [см/с] – длина волны [см], n](https://present5.com/presentation/946a68b49c88e007603de05fd778b10a/image-6.jpg)
Электромагнитный спектр с= n с – скорость света [см/с] – длина волны [см], n – частота(в циклах за секунду [с-1], или в герцах [Гц]). Размерность , n С увеличением частоты излучения длина волны уменьшается Е=hn h – постоянная Планка, (9. 534∙ 10 -14 ккал·с/моль), n – частота [Гц]. С увеличением частоты излучения возрастает и его энергия, с увеличением длины волны излучения его энергия падает
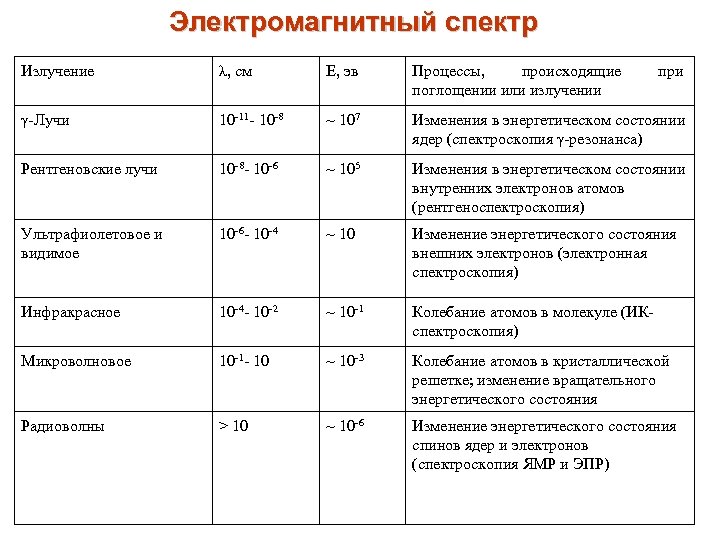
Электромагнитный спектр Излучение λ, см Е, эв Процессы, происходящие поглощении или излучении при γ-Лучи 10 -11 - 10 -8 ~ 107 Изменения в энергетическом состоянии ядер (спектроскопия γ-резонанса) Рентгеновские лучи 10 -8 - 10 -6 ~ 105 Изменения в энергетическом состоянии внутренних электронов атомов (рентгеноспектроскопия) Ультрафиолетовое и видимое 10 -6 - 10 -4 ~ 10 Изменение энергетического состояния внешних электронов (электронная спектроскопия) Инфракрасное 10 -4 - 10 -2 ~ 10 -1 Колебание атомов в молекуле (ИКспектроскопия) Микроволновое 10 -1 - 10 ~ 10 -3 Колебание атомов в кристаллической решетке; изменение вращательного энергетического состояния Радиоволны > 10 ~ 10 -6 Изменение энергетического состояния спинов ядер и электронов (спектроскопия ЯМР и ЭПР)
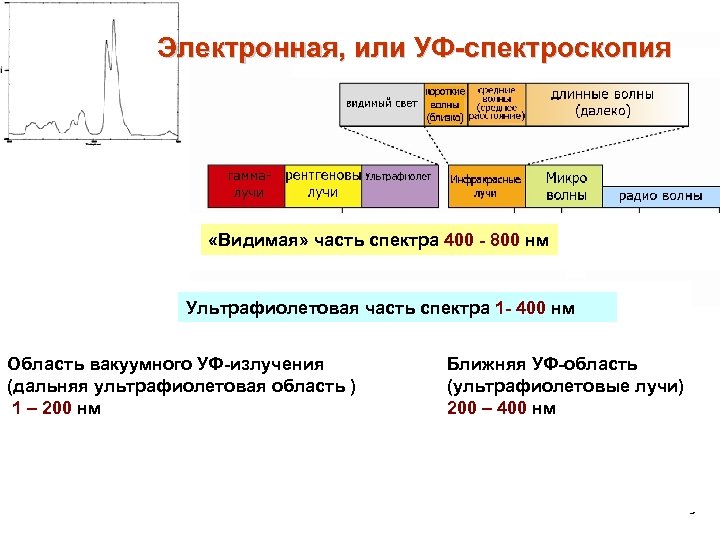
Электронная, или УФ-спектроскопия «Видимая» часть спектра 400 - 800 нм Ультрафиолетовая часть спектра 1 - 400 нм Область вакуумного УФ-излучения (дальняя ультрафиолетовая область ) 1 – 200 нм Ближняя УФ-область (ультрафиолетовые лучи) 200 – 400 нм
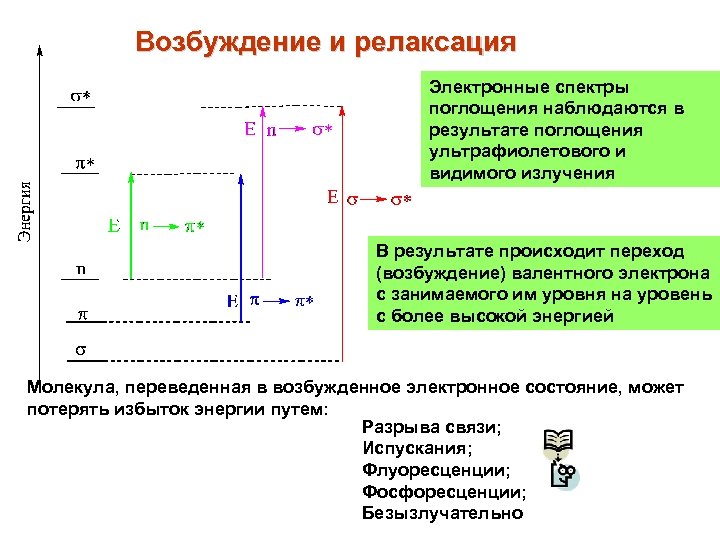
Возбуждение и релаксация Электронные спектры поглощения наблюдаются в результате поглощения ультрафиолетового и видимого излучения В результате происходит переход (возбуждение) валентного электрона с занимаемого им уровня на уровень с более высокой энергией Молекула, переведенная в возбужденное электронное состояние, может потерять избыток энергии путем: Разрыва связи; Испускания; Флуоресценции; Фосфоресценции; Безызлучательно

Закон Бера-Бугера-Ламберта Экспериментально открыт П. Бугером (1729), теоретически выведен И. Г. Ламбертом (1760), для растворов исследован А. Бером (1852) lg (I 0/I) = alc А = lc П. Бугер И. Г. Ламберт а - коэффициент поглощения, константа, зависящая от , но не зависящая от концентрации; l - длина оптического пути; c - концентрация При с [моль/л], b[см] , a = - молярный коэффициент поглощения Величина молярного коэффициента поглощения пропорциональна вероятности определенного перехода А = lg (I 0/ I) Т = I/I 0 А = - lg. Т А – погашение (оптическая плотность D) Т - пропускание
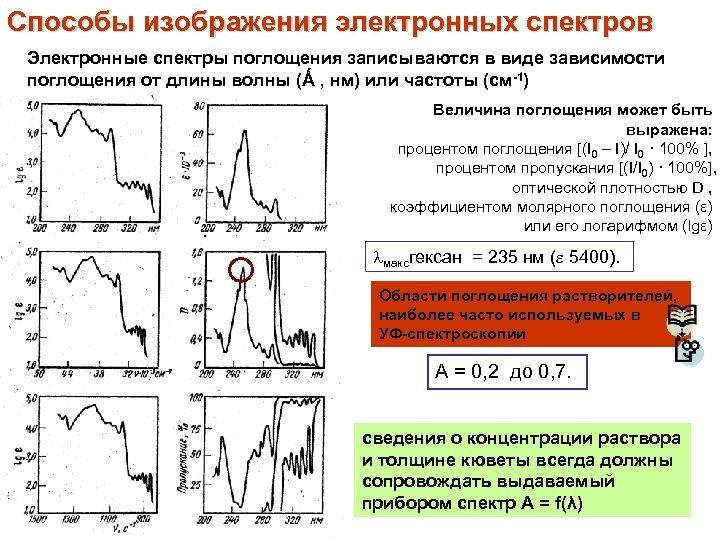
Способы изображения электронных спектров Электронные спектры поглощения записываются в виде зависимости поглощения от длины волны (Ǻ , нм) или частоты (см-1) Величина поглощения может быть выражена: процентом поглощения [(I 0 – I)/ I 0 · 100% ], процентом пропускания [(I/I 0) · 100%], оптической плотностью D , коэффициентом молярного поглощения (ε) или его логарифмом (lgε) максгексан = 235 нм ( 5400). Области поглощения растворителей, наиболее часто используемых в УФ-спектроскопии А = 0, 2 до 0, 7. сведения о концентрации раствора и толщине кюветы всегда должны сопровождать выдаваемый прибором спектр А = f(λ)
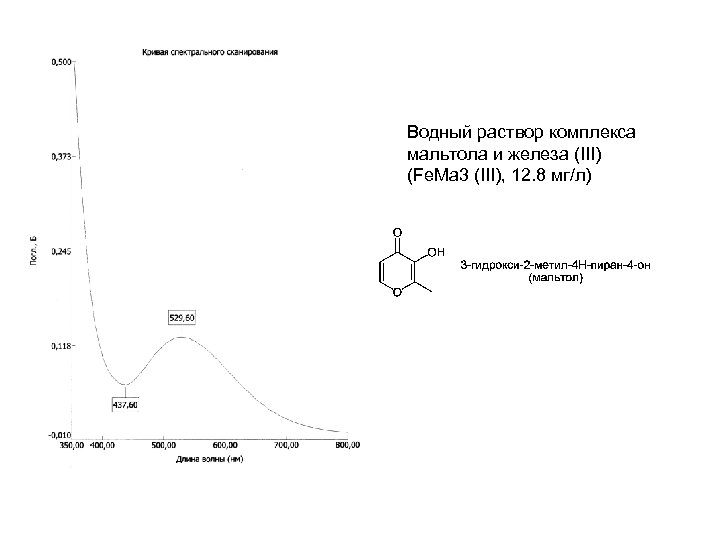
Водный раствор комплекса мальтола и железа (III) (Fe. Ma 3 (III), 12. 8 мг/л)

Взаимосвязь электронных спектров и структуры органических молекул Для характеристики спектральных изменений, вызванных модификацией структуры, введены специальные термины: гипсохромный сдвиг (синий сдвиг) – для смещения полос поглощения в коротковолновую область спектра; батохромный сдвиг (красный сдвиг) – для смещения полос поглощения в область длинных волн; гиперхромный эффект – увеличение интенсивности поглощения; гипохромный эффект – уменьшение интенсивности поглощения.
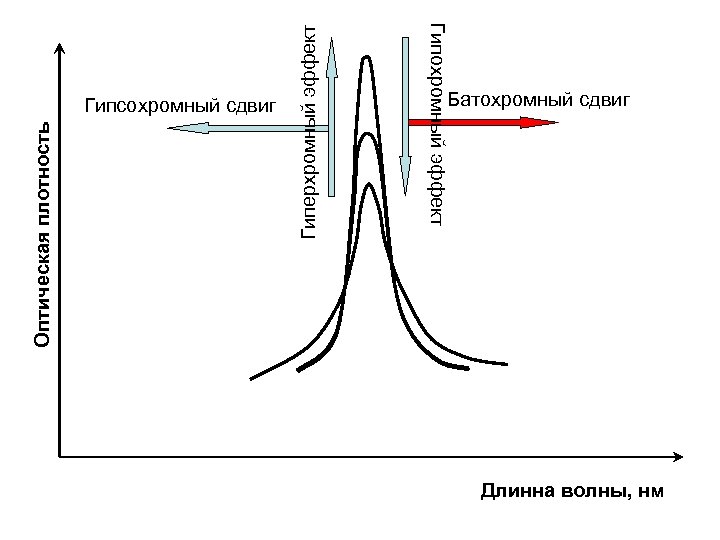
Гиперхромный эффект Оптическая плотность Гипохромный эффект Гипсохромный сдвиг Батохромный сдвиг Длинна волны, нм
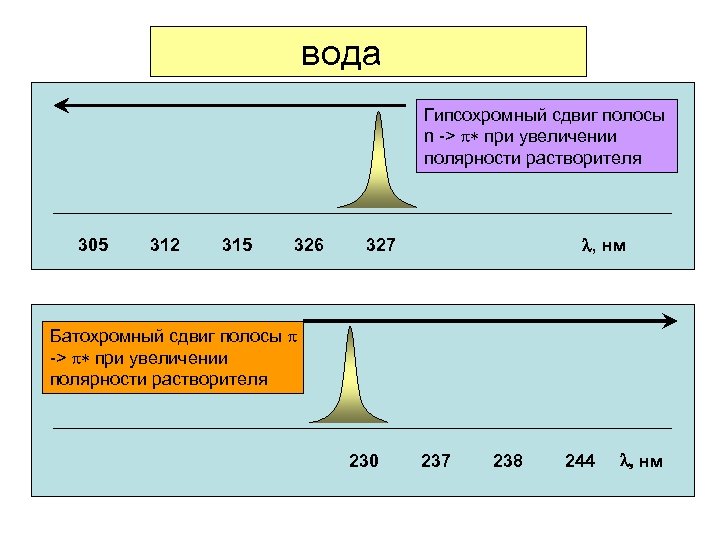
диэтиловый эфир вода метанол этанол гексан Гипсохромный сдвиг полосы n -> p* при увеличении полярности растворителя 305 312 315 326 , нм 327 Батохромный сдвиг полосы p -> p* при увеличении полярности растворителя 230 237 238 244 , нм

Взаимосвязь электронных спектров и структуры органических молекул Хромофоры Хромофор -простая функциональная группа, ответственная за поглощение с характеристическими величинами и X--Y спектр соединения - сумма спектральных характеристик индивидуальных хромофоров X и Y X-Y новый, хромофор с новыми спектральными характеристиками Ауксохром – функциональная группа, которая сама по себе не поглощает в близком ультрафиолете, но может влиять на поведение сопряженного с ней хромофора Типичные ауксохромы: -SH, -NH 2 , -OH
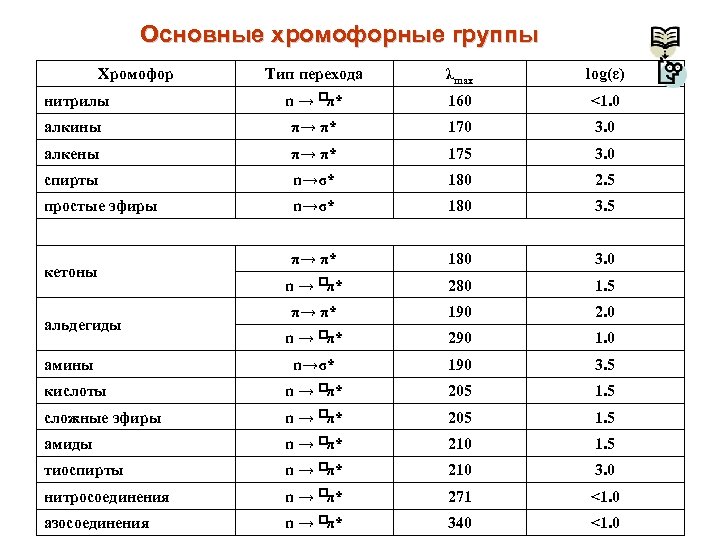
Основные хромофорные группы Хромофор Тип перехода λmax log(ε) нитрилы n → π* 160 <1. 0 алкины π→ π* 170 3. 0 алкены π→ π* 175 3. 0 спирты n→σ* 180 2. 5 простые эфиры n→σ* 180 3. 5 π→ π* 180 3. 0 n → π* 280 1. 5 π→ π* 190 2. 0 n → π* 290 1. 0 n→σ* 190 3. 5 кислоты n → π* 205 1. 5 сложные эфиры n → π* 205 1. 5 амиды n → π* 210 1. 5 тиоспирты n → π* 210 3. 0 нитросоединения n → π* 271 <1. 0 азосоединения n → π* 340 <1. 0 кетоны альдегиды амины

Электронные спектры поглощения основных классов органических соединений s → s* переходы Предельные углеводороды Соответствующие им полосы поглощения лежат в далеком ультрафиолете: · метан – 122 нм · этан – 135 нм · алканы - < 150 нм Насыщенные углеводороды с гетероатомами (О, S, N, галогены) s → s* и n → s* переходы соединение s → s*, нм n→ s*, нм CH 3 OH 150 177 CH 3 NH 2 170 215 CH 3 Cl 150 173 В области 200 – 800 нм большинство углеводородов и их производных «прозрачны» , что позволяет использовать их в качестве растворителей. Для функциональных производных эта область чуть уже: 250 – 800 нм.

Электронные спектры поглощения основных классов органических соединений Этилены s → s* p → p* (lmax =165 нм, emax > 104) переходы Алкильные заместители в этилене смещают p → p* полосу поглощения в красную область, и с ростом числа алкильных заместителей величина батохромного сдвига увеличивается. Соединения с сопряженными двойными связями Сопряжение проявляется в УФ-спектрах батохромным сдвигом для полосы p →p* перехода Структура Фрагмента Величина инкремента, нм Диеновая система в одном кольце 36 Дополнительное сопряжение, двойная связь 30 Экзоциклическая двойная связь (двойная связь вне цикла) 5 Заместители: · алкил · -OR · -OCOR · SR · -NR 2 · -Cl, -Br 5 6 0 30 60 5
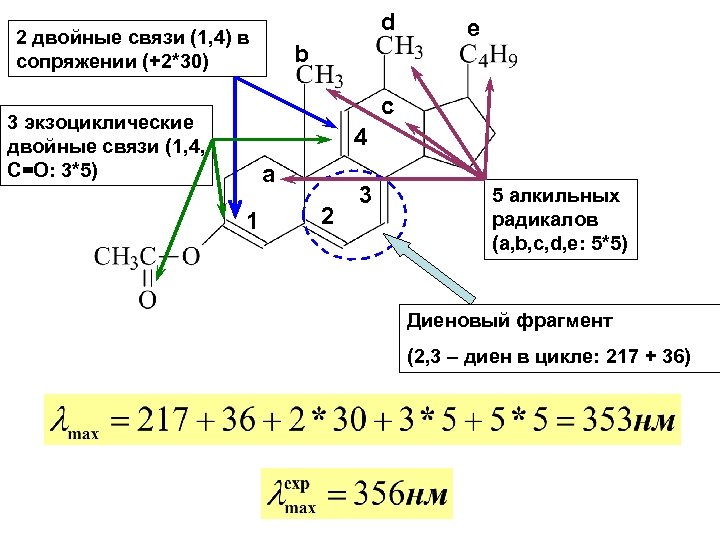
d 2 двойные связи (1, 4) в сопряжении (+2*30) b e c 3 экзоциклические двойные связи (1, 4, С=О: 3*5) 4 a 1 2 3 5 алкильных радикалов (a, b, c, d, e: 5*5) Диеновый фрагмент (2, 3 – диен в цикле: 217 + 36)

Электронные спектры поглощения основных классов органических соединений Карбонилсодержащие соединения n → p* n → s* p → p* переходы Обнаруживается в УФ-спектре по полосе n → p* перехода. Положение чувствительно к полярности растворителя и характеру заместителей X, Y. В полярных растворителях (особенно склонных к образованию водородных связей) эта полоса смещается гипсохромно. Замена Н-атома другими заместителями X, Y также приводит к гипсохромному сдвигу.

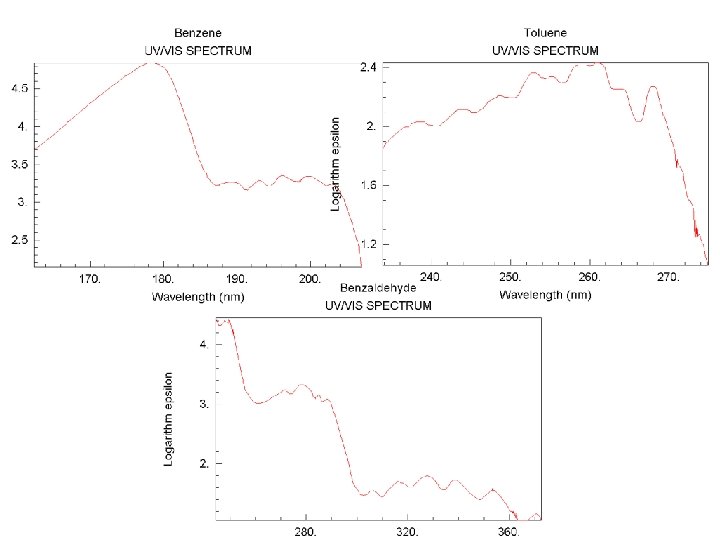
Электронные спектры поглощения основных классов органических соединений Ароматические соединения λ, нм ε, л/моль см 180 6 104 203 8 103 230 -260 200 В бензоле p → p * переходы Полоса бензольного поглощения На положение полосы в области 200 – 300 нм значительное влияние оказывают заместители и растворители Влияния заместителей на положение полосы поглощения ароматическим кольцом определяется характером заместителя. Заместители с I-эффектом практически не меняют вид спектра
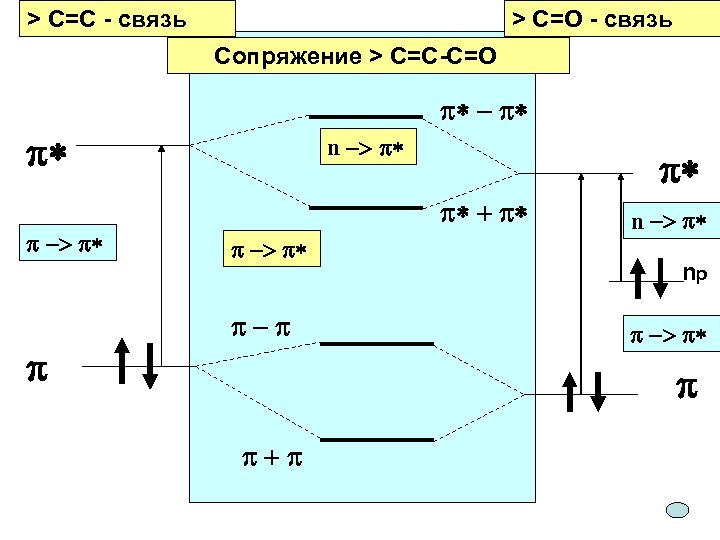
> C=C - связь > C=O - связь Сопряжение > C=C-C=O p* - p* p* p -> p* p n -> p* p* p* + p* p -> p* p-p n -> p* np p -> p* p p+p
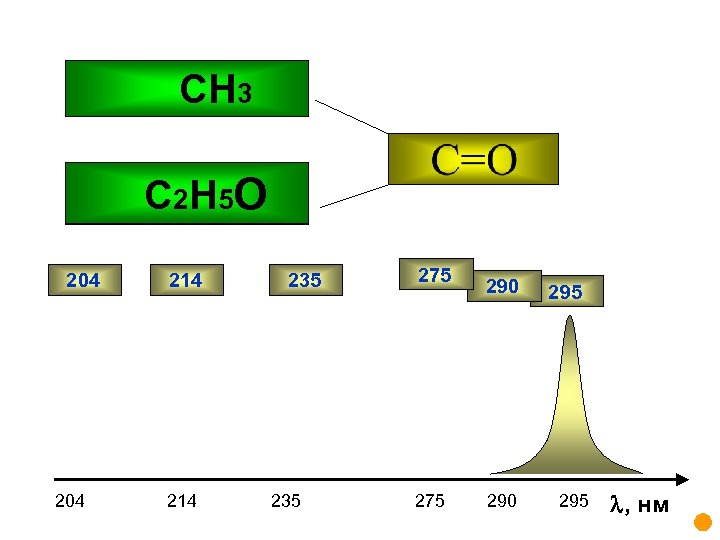
CH H 3 C 2 H 3 H 5 O Cl NH 2 CH 204 214 235 275 290 295 , нм
946a68b49c88e007603de05fd778b10a.ppt