ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ ИДЕНТИФИКАЦИИ СОЕДИНЕНИЙ




















Идентификация органических соединений.ppt
- Количество слайдов: 30
 ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ ИДЕНТИФИКАЦИИ СОЕДИНЕНИЙ Органическая химия
ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ ИДЕНТИФИКАЦИИ СОЕДИНЕНИЙ Органическая химия
 Спектральные методы анализа органических веществ: • Электронная, или ультрафиолетовая спектроскопия УФ • Инфракрасная спектроскопия ИК • Спектроскопия ядерного магнитного резонанса ЯМР • Масс-спектрометрия 2
Спектральные методы анализа органических веществ: • Электронная, или ультрафиолетовая спектроскопия УФ • Инфракрасная спектроскопия ИК • Спектроскопия ядерного магнитного резонанса ЯМР • Масс-спектрометрия 2
 Среди многообразных физических методов, которые применяются при исследовании строения органических молекул, наибольший интерес представляет взаимодействие вещества с электромагнитным излучением в широком интервале частот, начиная с радиоволн и кончая γ-лучами, т. е. по всему электромагнитному спектру. При этом происходит изменение энергии молекул, которое определяется соотношением Бора: ΔЕ = Ек – Ен =hv • ΔЕ – изменение энергии системы • Ек – энергия системы в конечном состоянии • Ен - энергия системы в начальном состоянии • h- постоянная Планка ( 6. 5· 10 -27 эрг/сек) • v - частота излучения или волновое число (см-1) или в герцах (Гц). – число волн, приходящееся на 1 см длины светового луча Ек > Ен ΔЕ > 0 поглощение энергии спектры поглощения Ек < Ен ΔЕ <0 излучение энергии эмиссионные спектры
Среди многообразных физических методов, которые применяются при исследовании строения органических молекул, наибольший интерес представляет взаимодействие вещества с электромагнитным излучением в широком интервале частот, начиная с радиоволн и кончая γ-лучами, т. е. по всему электромагнитному спектру. При этом происходит изменение энергии молекул, которое определяется соотношением Бора: ΔЕ = Ек – Ен =hv • ΔЕ – изменение энергии системы • Ек – энергия системы в конечном состоянии • Ен - энергия системы в начальном состоянии • h- постоянная Планка ( 6. 5· 10 -27 эрг/сек) • v - частота излучения или волновое число (см-1) или в герцах (Гц). – число волн, приходящееся на 1 см длины светового луча Ек > Ен ΔЕ > 0 поглощение энергии спектры поглощения Ек < Ен ΔЕ <0 излучение энергии эмиссионные спектры
 Поглощение электромагнитного излучения связано с определенными изменениями в молекуле вещества, точнее, с ее переходом на более высокий энергетический уровень. Внутренняя энергия молекулы квантована. В связи с этим количество поглощаемой энергии может иметь только строго опреде- ленные значения, т. е. поглощается излучение только определенной частоты. Поглощение излучения, а, следовательно, и энергии происходит в том слу- чае, если квант излучения соответствует разности между двумя энергетиче- скими уровнями облучаемого вещества. Переходами между уровнями энер- гии Е к и Е н «управляют» правила отбора. Это означает, что не все переходы возможны с = λ ν ΔЕ = Ек – Ен =hv с – скорость света (3∙ 1010 см/с), λ – длина волны (см) v – частота в циклах за секунду (-1 см) или (Гц) ν = с/ λ энергия электромагнитного излучения находится в прямой зависимости от его частоты
Поглощение электромагнитного излучения связано с определенными изменениями в молекуле вещества, точнее, с ее переходом на более высокий энергетический уровень. Внутренняя энергия молекулы квантована. В связи с этим количество поглощаемой энергии может иметь только строго опреде- ленные значения, т. е. поглощается излучение только определенной частоты. Поглощение излучения, а, следовательно, и энергии происходит в том слу- чае, если квант излучения соответствует разности между двумя энергетиче- скими уровнями облучаемого вещества. Переходами между уровнями энер- гии Е к и Е н «управляют» правила отбора. Это означает, что не все переходы возможны с = λ ν ΔЕ = Ек – Ен =hv с – скорость света (3∙ 1010 см/с), λ – длина волны (см) v – частота в циклах за секунду (-1 см) или (Гц) ν = с/ λ энергия электромагнитного излучения находится в прямой зависимости от его частоты
 Излучения, соответствующие различным областям электромагнитного спектра, характеризуются разными длинами волн (и частотами). Поэтому эти излучения должны иметь разные энергии. Область интенсивного поглощения излучения - полоса Совокупность полос - спектр поглощения Каждый тип изменений энергетических уровней молекулы происходит в определенной области частот колебаний. 1. Наибольшая энергия требуется для возбуждения электронов. Эта энергия соответствует излучению в ультрафиолетовой и видимой области (электронная спектроскопия) УФ 2. Меньшие затраты энергии необходимы для изменения длин связей и углов между атомами в инфракрасной области ИК 3. Еще меньше энергии необходимо для переориентации спинов ядер спектроскопия ядерного магнитного резонанса ЯМР
Излучения, соответствующие различным областям электромагнитного спектра, характеризуются разными длинами волн (и частотами). Поэтому эти излучения должны иметь разные энергии. Область интенсивного поглощения излучения - полоса Совокупность полос - спектр поглощения Каждый тип изменений энергетических уровней молекулы происходит в определенной области частот колебаний. 1. Наибольшая энергия требуется для возбуждения электронов. Эта энергия соответствует излучению в ультрафиолетовой и видимой области (электронная спектроскопия) УФ 2. Меньшие затраты энергии необходимы для изменения длин связей и углов между атомами в инфракрасной области ИК 3. Еще меньше энергии необходимо для переориентации спинов ядер спектроскопия ядерного магнитного резонанса ЯМР
 Спектроскопия в ультрафиолетовой и видимой области 6
Спектроскопия в ультрафиолетовой и видимой области 6
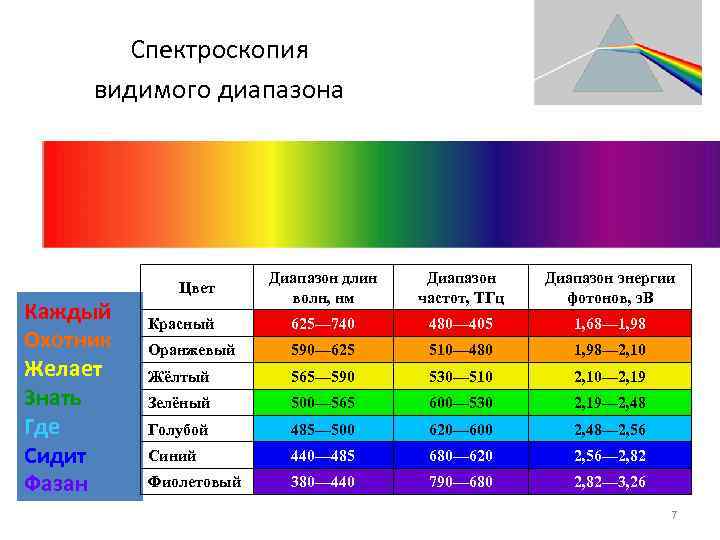
 Спектроскопия видимого диапазона Диапазон длин Диапазон энергии Цвет волн, нм частот, ТГц фотонов, э. В Каждый Красный 625— 740 480— 405 1, 68— 1, 98 Охотник Оранжевый 590— 625 510— 480 1, 98— 2, 10 Желает Жёлтый 565— 590 530— 510 2, 10— 2, 19 Знать Зелёный 500— 565 600— 530 2, 19— 2, 48 Где Голубой 485— 500 620— 600 2, 48— 2, 56 Сидит Синий 440— 485 680— 620 2, 56— 2, 82 Фазан Фиолетовый 380— 440 790— 680 2, 82— 3, 26 7
Спектроскопия видимого диапазона Диапазон длин Диапазон энергии Цвет волн, нм частот, ТГц фотонов, э. В Каждый Красный 625— 740 480— 405 1, 68— 1, 98 Охотник Оранжевый 590— 625 510— 480 1, 98— 2, 10 Желает Жёлтый 565— 590 530— 510 2, 10— 2, 19 Знать Зелёный 500— 565 600— 530 2, 19— 2, 48 Где Голубой 485— 500 620— 600 2, 48— 2, 56 Сидит Синий 440— 485 680— 620 2, 56— 2, 82 Фазан Фиолетовый 380— 440 790— 680 2, 82— 3, 26 7
 УФ-спектроскопия Метод стал фармакопейным с 1968 года Cпектры наблюдаются в результате поглощения УФ излучения; при этом происходит переход валентного электрона в возбужденное состояние
УФ-спектроскопия Метод стал фармакопейным с 1968 года Cпектры наблюдаются в результате поглощения УФ излучения; при этом происходит переход валентного электрона в возбужденное состояние
 • Е max - для возбуждения электронов σ связи (алкананы) • Е меньше - переход π – σ* полосы поглощения - в области 200 -300 нм. • Е min для перехода на разрыхляющую π* орбиталь Переходы π – σ* и π – π* (соединений с сопряженными связями, ароматические соединени => кратная связь и неподеленная электронная пара • их наличие, многочисленные сочетания в молекулах с разнообразными заместителями объясняет совокупность УФ органических соединений. Группировки, содержащие в своем составе сопряженные двойные связи и неподеленные пары электронов, называются хромофорами • Хромофор – группировка, вызывающая избирательное поглощение электромагнитного колебания в УФ-области.
• Е max - для возбуждения электронов σ связи (алкананы) • Е меньше - переход π – σ* полосы поглощения - в области 200 -300 нм. • Е min для перехода на разрыхляющую π* орбиталь Переходы π – σ* и π – π* (соединений с сопряженными связями, ароматические соединени => кратная связь и неподеленная электронная пара • их наличие, многочисленные сочетания в молекулах с разнообразными заместителями объясняет совокупность УФ органических соединений. Группировки, содержащие в своем составе сопряженные двойные связи и неподеленные пары электронов, называются хромофорами • Хромофор – группировка, вызывающая избирательное поглощение электромагнитного колебания в УФ-области.
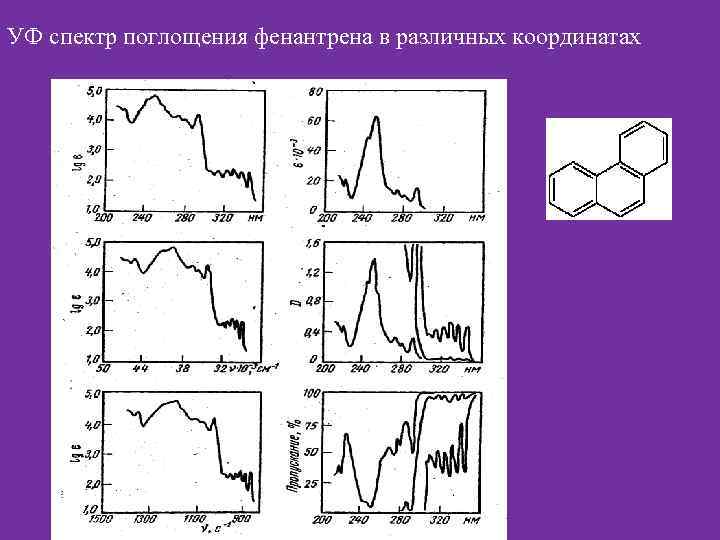
 УФ спектр поглощения фенантрена в различных координатах
УФ спектр поглощения фенантрена в различных координатах
 • Природа полос поглощения в УФ связана главным образом с числом и расположением электронов в поглощающих молекулах и ионах. • Определенные полосы поглощения в спектре указывают на наличие в структуре функциональных групп (хромофоров). Этим объясняется сходство спектров веществ, содержащих, например, фенильный радикал: эфедрин, димедрол, атропин, бензилпенициллин. • Лекарственные вещества, содержащие замещенный ароматический радикал (адреналин, морфин, эстрадиол, левомицетин и др. ) имеют в спектре один максимум около 280 нм, сопряженную еноновую систему
• Природа полос поглощения в УФ связана главным образом с числом и расположением электронов в поглощающих молекулах и ионах. • Определенные полосы поглощения в спектре указывают на наличие в структуре функциональных групп (хромофоров). Этим объясняется сходство спектров веществ, содержащих, например, фенильный радикал: эфедрин, димедрол, атропин, бензилпенициллин. • Лекарственные вещества, содержащие замещенный ароматический радикал (адреналин, морфин, эстрадиол, левомицетин и др. ) имеют в спектре один максимум около 280 нм, сопряженную еноновую систему
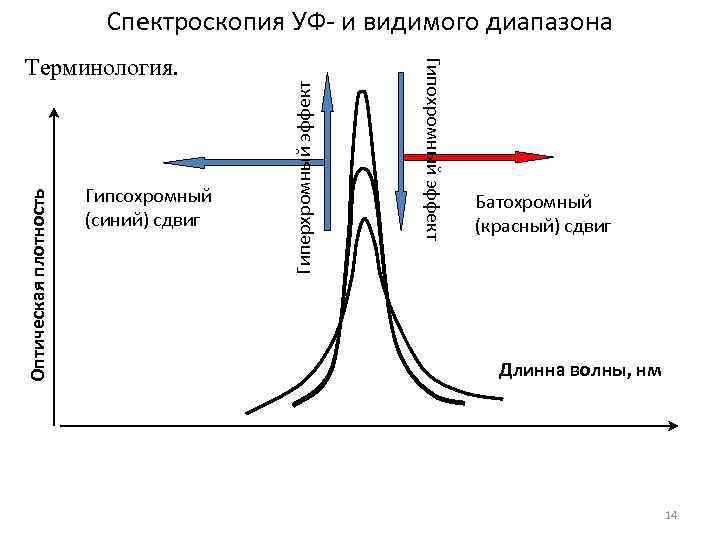
 Один и тот же хромофор проявляется практически одинаково, как в простых, так и в сложных молекулах. В зависимости от окружения, положение максимума поглощения может несколько изменятся. Сдвиг по максимуму поглощения в сторону более длинных волн вследствие замещения или влияния растворителя - батохромный сдвиг (красный сдвиг) Сдвиг в сторону более коротких волн – гипсохромный(синий сдвиг). Гиперхромный эффект – увеличение интенсивности поглощения. Гипохромный эффект – уменьшение интенсивности поглощения.
Один и тот же хромофор проявляется практически одинаково, как в простых, так и в сложных молекулах. В зависимости от окружения, положение максимума поглощения может несколько изменятся. Сдвиг по максимуму поглощения в сторону более длинных волн вследствие замещения или влияния растворителя - батохромный сдвиг (красный сдвиг) Сдвиг в сторону более коротких волн – гипсохромный(синий сдвиг). Гиперхромный эффект – увеличение интенсивности поглощения. Гипохромный эффект – уменьшение интенсивности поглощения.
 Спектроскопия УФ- и видимого диапазона Терминология. Гипохромный эффект Гиперхромный эффект Гипсохромный Батохромный Оптическая плотность (синий) сдвиг (красный) сдвиг Длинна волны, нм 14
Спектроскопия УФ- и видимого диапазона Терминология. Гипохромный эффект Гиперхромный эффект Гипсохромный Батохромный Оптическая плотность (синий) сдвиг (красный) сдвиг Длинна волны, нм 14
 Видеофильм УФ – 5 мин
Видеофильм УФ – 5 мин
 Инфракрасная спектроскопия ИК
Инфракрасная спектроскопия ИК
 Явление взаимодействия веществ с ИК -излучением было открыто Эбни и И. Фестингом в 1861 г. В настоящие время ИК – спектроскопия стала одним из основных методов исследования веществ различной химической природы, в том числе и лекарственных соединений. ν Впервые метод стал фармакопейным с 1968 г, где он рекомендовался для контроля качества трех лекарственных веществ. Наряду с ультрафиолетовой ИК включена во все современные фармакопеи. Так, Международная фармакопея (Женева)рекомендует этот метод практически в анализе половины описанных в ней лекарственных веществ. Получать ИК-спектры можно не только для субстанций, но и в ряде случаев для готовых препаратов. Для этого необходимо, чтобы вспомогательные вещества, входящие в состав препарата (например, таблеток), не подавляли спектр действующего вещества.
Явление взаимодействия веществ с ИК -излучением было открыто Эбни и И. Фестингом в 1861 г. В настоящие время ИК – спектроскопия стала одним из основных методов исследования веществ различной химической природы, в том числе и лекарственных соединений. ν Впервые метод стал фармакопейным с 1968 г, где он рекомендовался для контроля качества трех лекарственных веществ. Наряду с ультрафиолетовой ИК включена во все современные фармакопеи. Так, Международная фармакопея (Женева)рекомендует этот метод практически в анализе половины описанных в ней лекарственных веществ. Получать ИК-спектры можно не только для субстанций, но и в ряде случаев для готовых препаратов. Для этого необходимо, чтобы вспомогательные вещества, входящие в состав препарата (например, таблеток), не подавляли спектр действующего вещества.
 ИК-спектрометрия используется: • при установлении структуры новых БАВ, получаемых путем химического синтеза или выделяемых из природных объектов (животное или растительное сырье, продукты жизнедеятельности микроорганизмов); • изучении строения метаболитов; • при испытании на подлинность лекарственных веществ; • количественном анализе; • контроле технологического процесса в промышленном производстве фармацевтических препаратов.
ИК-спектрометрия используется: • при установлении структуры новых БАВ, получаемых путем химического синтеза или выделяемых из природных объектов (животное или растительное сырье, продукты жизнедеятельности микроорганизмов); • изучении строения метаболитов; • при испытании на подлинность лекарственных веществ; • количественном анализе; • контроле технологического процесса в промышленном производстве фармацевтических препаратов.
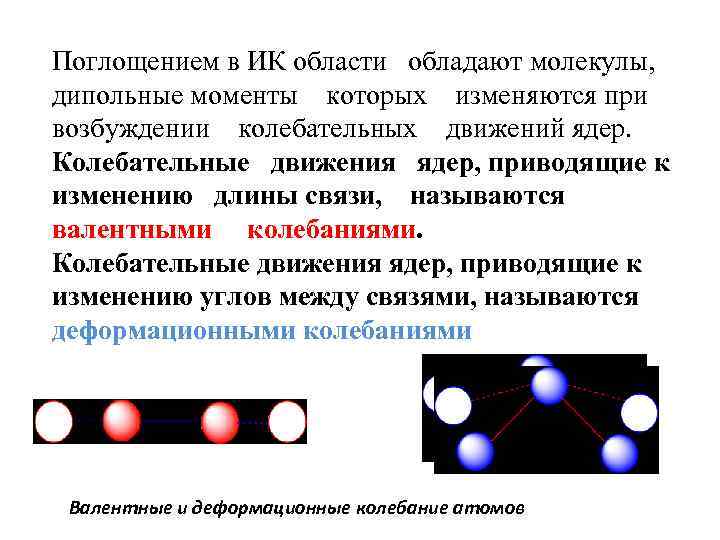
 Поглощением в ИК области обладают молекулы, дипольные моменты которых изменяются при возбуждении колебательных движений ядер. Колебательные движения ядер, приводящие к изменению длины связи, называются валентными колебаниями. Колебательные движения ядер, приводящие к изменению углов между связями, называются деформационными колебаниями Валентные и деформационные колебание атомов
Поглощением в ИК области обладают молекулы, дипольные моменты которых изменяются при возбуждении колебательных движений ядер. Колебательные движения ядер, приводящие к изменению длины связи, называются валентными колебаниями. Колебательные движения ядер, приводящие к изменению углов между связями, называются деформационными колебаниями Валентные и деформационные колебание атомов
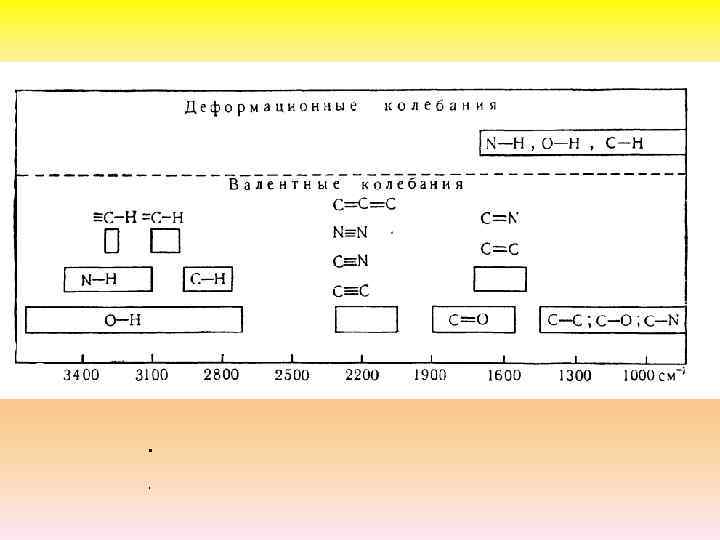
 Энергия деформационных колебаний δ значительно меньше, чем энергия валентных колебаний ν Деформационные колебания наблюдаются при больших длинах волн (низких волновых числах). Частота валентных колебаний связана с прочностью соответствующих связей: тройные связи (поглощение при 2300 -2000 см -1 ) прочнее двойных (поглощение при 1900 -1500 см -1 ), которые, в свою очередь, прочнее одинарных (связи С-С, С-N, С-О поглощают при 1300 -800 см -1 Наиболее интенсивными в ИК-спектре являются пики, отвечающие валентным колебаниям
Энергия деформационных колебаний δ значительно меньше, чем энергия валентных колебаний ν Деформационные колебания наблюдаются при больших длинах волн (низких волновых числах). Частота валентных колебаний связана с прочностью соответствующих связей: тройные связи (поглощение при 2300 -2000 см -1 ) прочнее двойных (поглощение при 1900 -1500 см -1 ), которые, в свою очередь, прочнее одинарных (связи С-С, С-N, С-О поглощают при 1300 -800 см -1 Наиболее интенсивными в ИК-спектре являются пики, отвечающие валентным колебаниям
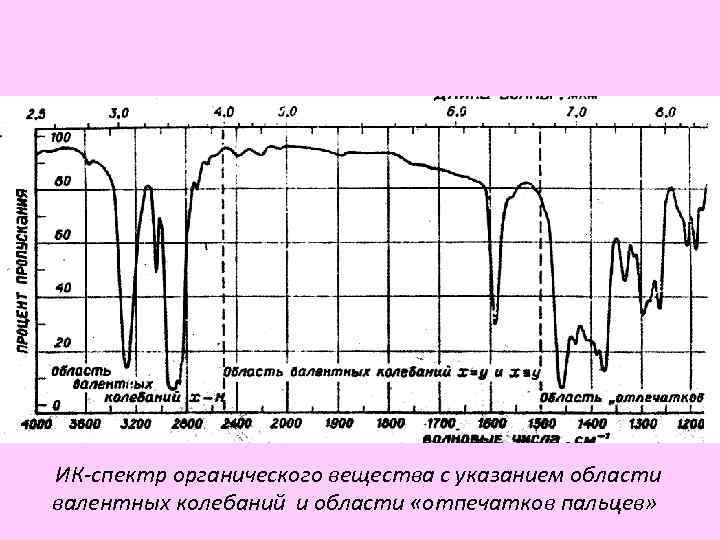
 ИК-спектр органического вещества с указанием области валентных колебаний и области «отпечатков пальцев»
ИК-спектр органического вещества с указанием области валентных колебаний и области «отпечатков пальцев»
 . .
. .
 Характеристические полосы (частоты) поглощения Многие атомные группы такие как -ОН, - NH 2, -NO, >СО, а также определенные связи, такие как С-Н, С- С, С=О, характеризуются определенными частотами, которые мало отличаются в различных соединениях. Такие частоты получили название характеристических. Валентные колебания связи С-Н ( С sp 3 -Н) алкильных фрагментов обнаруживаются в области 2962 -2853 см-1 ν СН 3 2962 -2853 см-1 Феформационные δ CH 3 1485 -1340 см-1
Характеристические полосы (частоты) поглощения Многие атомные группы такие как -ОН, - NH 2, -NO, >СО, а также определенные связи, такие как С-Н, С- С, С=О, характеризуются определенными частотами, которые мало отличаются в различных соединениях. Такие частоты получили название характеристических. Валентные колебания связи С-Н ( С sp 3 -Н) алкильных фрагментов обнаруживаются в области 2962 -2853 см-1 ν СН 3 2962 -2853 см-1 Феформационные δ CH 3 1485 -1340 см-1
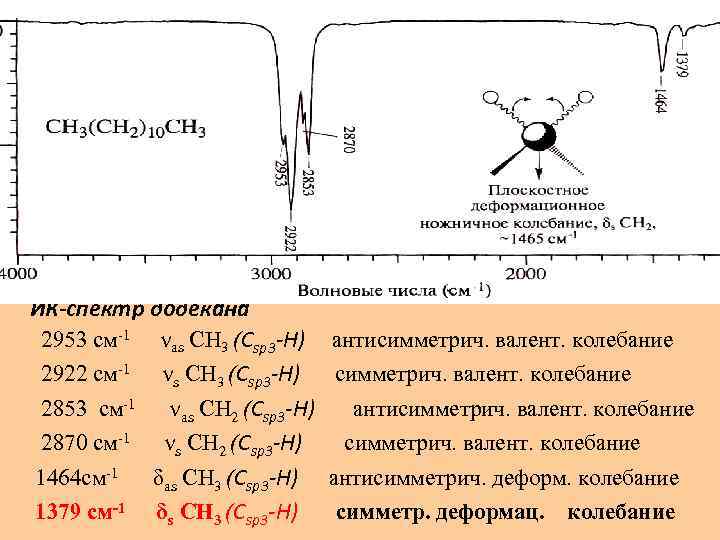
 ИК-спектр додекана 2953 см-1 νas CH 3 (Сsp 3 -Н) антисимметрич. валент. колебание 2922 см-1 νs CH 3 (Сsp 3 -Н) симметрич. валент. колебание 2853 см-1 νas CH 2 (Сsp 3 -Н) антисимметрич. валент. колебание 2870 см-1 νs CH 2 (Сsp 3 -Н) симметрич. валент. колебание 1464 см-1 δas CH 3 (Сsp 3 -Н) антисимметрич. деформ. колебание 1379 см-1 δs CH 3 (Сsp 3 -Н) симметр. деформац. колебание
ИК-спектр додекана 2953 см-1 νas CH 3 (Сsp 3 -Н) антисимметрич. валент. колебание 2922 см-1 νs CH 3 (Сsp 3 -Н) симметрич. валент. колебание 2853 см-1 νas CH 2 (Сsp 3 -Н) антисимметрич. валент. колебание 2870 см-1 νs CH 2 (Сsp 3 -Н) симметрич. валент. колебание 1464 см-1 δas CH 3 (Сsp 3 -Н) антисимметрич. деформ. колебание 1379 см-1 δs CH 3 (Сsp 3 -Н) симметр. деформац. колебание
 . групп (СН ) наблюдаются в Валентные колебания метильных 3 виде двух полос поглощения при 2953 и 2872 см-1. νas 2953 см-1 CH 3 результат антисимметричного (as) валентного колебания, в котором две связи С-Н метильной группы растягиваются, в то время как третья сжимается (νas CH 3). νs 2922 см-1 CH 3 симметричными (s) валентными колебаниями ( когда все три связи С-Н растягиваются или сжимаются в фазе. Валентные колебания метиленовых групп (СН 2 )также наблюдаются в виде двух полос поглощения, обусловленных антисимметричными (ν as CH 2 ) и симметричными (ν s CH 2 ) валентными колебаниями. Наличие нескольких метильных групп приводит к увеличению интенсивности соответствующих полос.
. групп (СН ) наблюдаются в Валентные колебания метильных 3 виде двух полос поглощения при 2953 и 2872 см-1. νas 2953 см-1 CH 3 результат антисимметричного (as) валентного колебания, в котором две связи С-Н метильной группы растягиваются, в то время как третья сжимается (νas CH 3). νs 2922 см-1 CH 3 симметричными (s) валентными колебаниями ( когда все три связи С-Н растягиваются или сжимаются в фазе. Валентные колебания метиленовых групп (СН 2 )также наблюдаются в виде двух полос поглощения, обусловленных антисимметричными (ν as CH 2 ) и симметричными (ν s CH 2 ) валентными колебаниями. Наличие нескольких метильных групп приводит к увеличению интенсивности соответствующих полос.
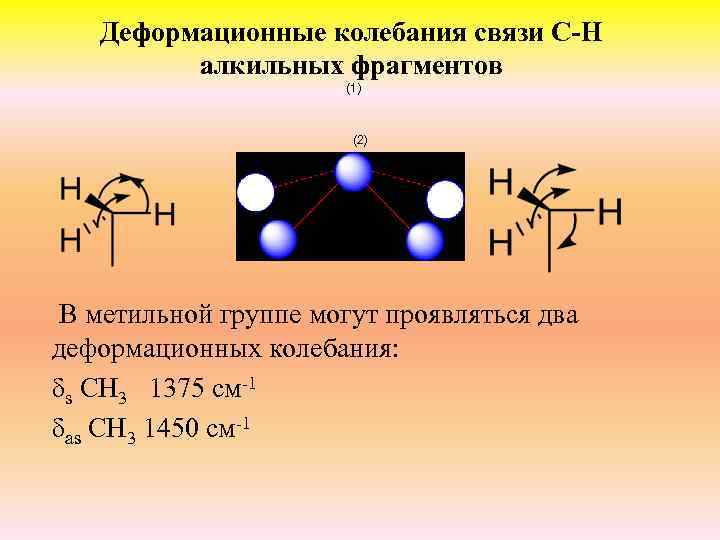
 Деформационные колебания связи С-Н алкильных фрагментов (1) (2) В метильной группе могут проявляться два деформационных колебания: δs CH 3 1375 см-1 δas CH 3 1450 см-1
Деформационные колебания связи С-Н алкильных фрагментов (1) (2) В метильной группе могут проявляться два деформационных колебания: δs CH 3 1375 см-1 δas CH 3 1450 см-1
 Видеофильм ИК-1 .
Видеофильм ИК-1 .
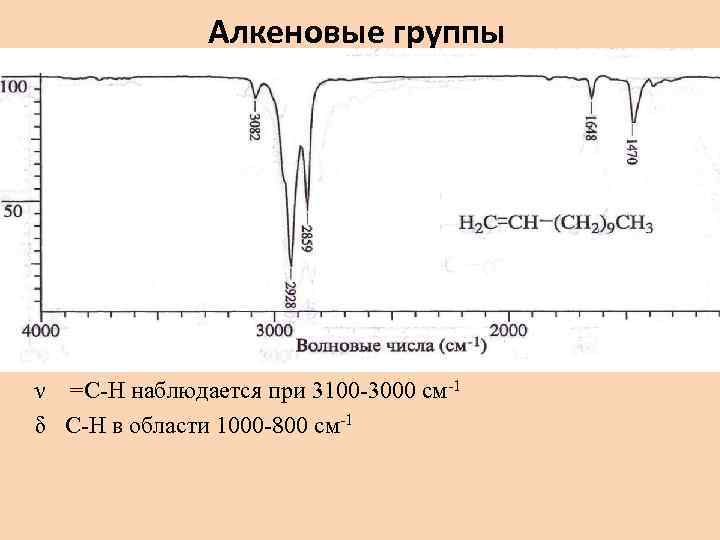
 Алкеновые группы ν =С-Н наблюдается при 3100 -3000 см-1 δ С-Н в области 1000 -800 см-1
Алкеновые группы ν =С-Н наблюдается при 3100 -3000 см-1 δ С-Н в области 1000 -800 см-1
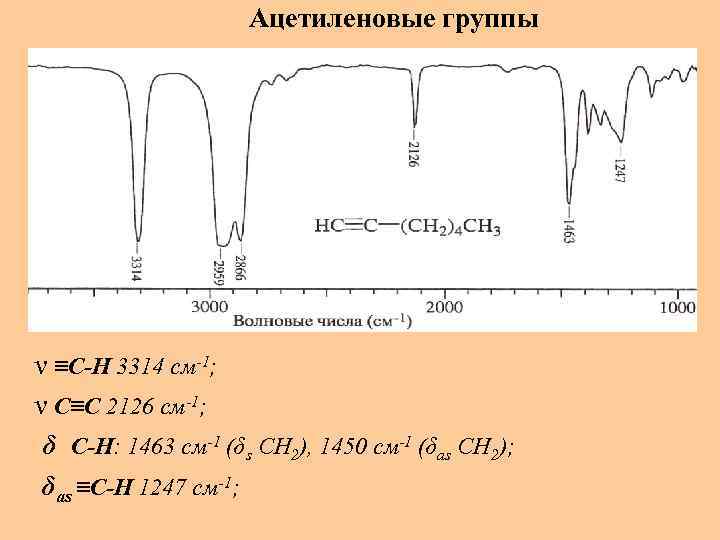
 Ацетиленовые группы ν ≡С-Н 3314 см-1; ν С≡С 2126 см-1; δ С-Н: 1463 см-1 (δs CH 2), 1450 см-1 (δas CH 2); δas ≡С-Н 1247 см-1;
Ацетиленовые группы ν ≡С-Н 3314 см-1; ν С≡С 2126 см-1; δ С-Н: 1463 см-1 (δs CH 2), 1450 см-1 (δas CH 2); δas ≡С-Н 1247 см-1;
 Видеофильм ИК-2 • .
Видеофильм ИК-2 • .
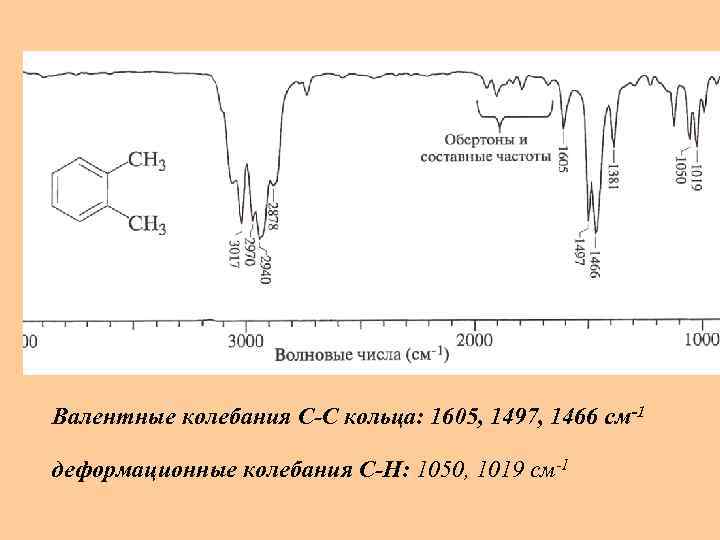
 Валентные колебания С-С кольца: 1605, 1497, 1466 см-1 деформационные колебания С-Н: 1050, 1019 см-1
Валентные колебания С-С кольца: 1605, 1497, 1466 см-1 деформационные колебания С-Н: 1050, 1019 см-1

