Spectroscopy_FPK.ppt
- Количество слайдов: 47
 ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
 Классификация ФХМА Спектральные (оптические) Атомная спектроскопия Молекулярная спектроскопия Электрохимические (электроаналитические) Методы разделения и концентрирования Радиохимические методы Термические методы
Классификация ФХМА Спектральные (оптические) Атомная спектроскопия Молекулярная спектроскопия Электрохимические (электроаналитические) Методы разделения и концентрирования Радиохимические методы Термические методы
 КАК ВЫБРАТЬ МЕТОД? Какую информацию дает метод? Какие достоинства и недостатки метода по отношению к другим методам? Какова правильность и воспроизводимость метода? Каковы границы определяемых концентраций анализируемого вещества? Сколько образца нужно для анализа? Какие образцы могут быть использованы для анализа? Какие компоненты образца могут оказывать мешающее влияние? Прочие факторы: скорость анализа, простота, бюджет, наличие приборов и квалификация персонала
КАК ВЫБРАТЬ МЕТОД? Какую информацию дает метод? Какие достоинства и недостатки метода по отношению к другим методам? Какова правильность и воспроизводимость метода? Каковы границы определяемых концентраций анализируемого вещества? Сколько образца нужно для анализа? Какие образцы могут быть использованы для анализа? Какие компоненты образца могут оказывать мешающее влияние? Прочие факторы: скорость анализа, простота, бюджет, наличие приборов и квалификация персонала
 Характеристики метода: Правильность, точность Характеристики систематической погрешности Абсолютная погрешность Относительная погрешность ПРОБЛЕМА: не знаем истиного значения РЕШЕНИЕ: -анализ стандартных образцов -анализ другим методом -анализ холостой пробы -“round robin” алгоритм эксперимента
Характеристики метода: Правильность, точность Характеристики систематической погрешности Абсолютная погрешность Относительная погрешность ПРОБЛЕМА: не знаем истиного значения РЕШЕНИЕ: -анализ стандартных образцов -анализ другим методом -анализ холостой пробы -“round robin” алгоритм эксперимента
 Характеристики метода: Прецизионность, воспроизводимость, повторяемость (сходимость) Характеристики случайной погрешности Стандартное отклонение S = Относительное стандартное отклонение SR = Стандартная ошибка SX = Дисперсия V = Размах варьирования w= Доверительный интервал =
Характеристики метода: Прецизионность, воспроизводимость, повторяемость (сходимость) Характеристики случайной погрешности Стандартное отклонение S = Относительное стандартное отклонение SR = Стандартная ошибка SX = Дисперсия V = Размах варьирования w= Доверительный интервал =
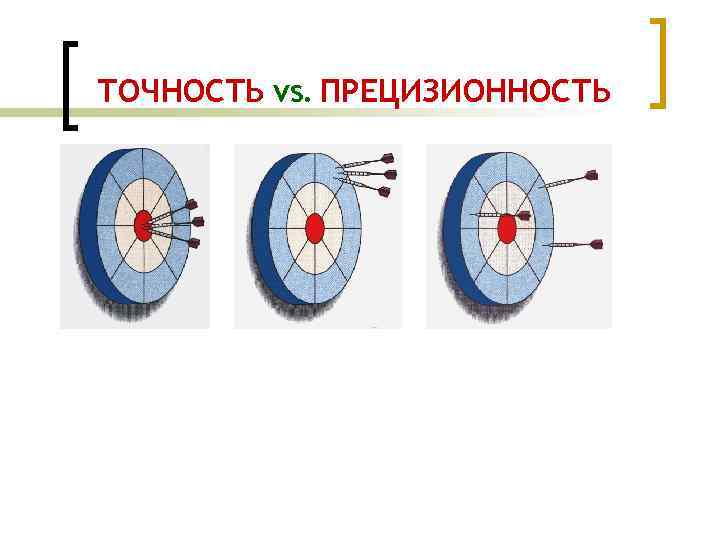 ТОЧНОСТЬ vs. ПРЕЦИЗИОННОСТЬ
ТОЧНОСТЬ vs. ПРЕЦИЗИОННОСТЬ
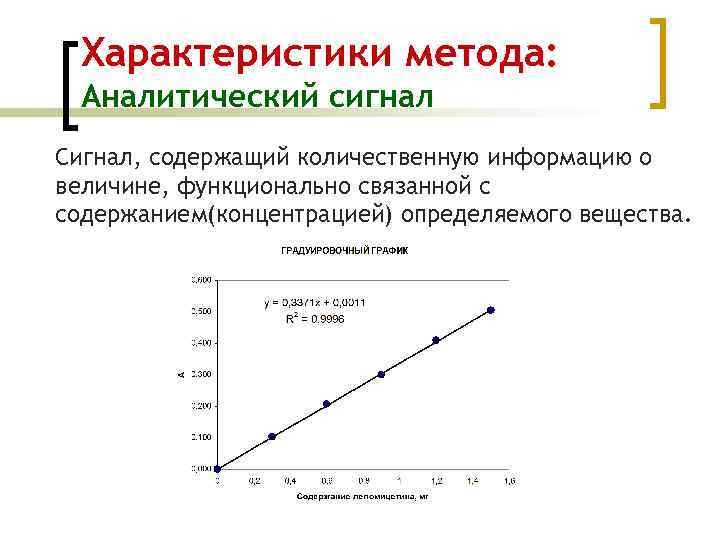 Характеристики метода: Аналитический сигнал Сигнал, содержащий количественную информацию о величине, функционально связанной с содержанием(концентрацией) определяемого вещества.
Характеристики метода: Аналитический сигнал Сигнал, содержащий количественную информацию о величине, функционально связанной с содержанием(концентрацией) определяемого вещества.
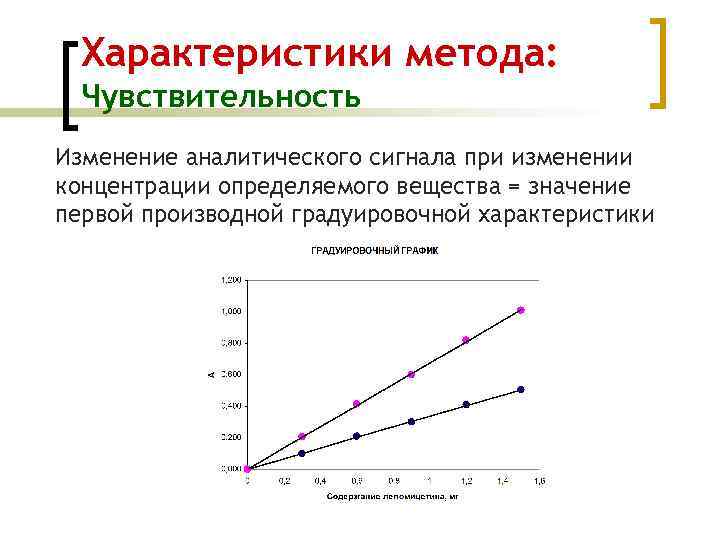 Характеристики метода: Чувствительность Изменение аналитического сигнала при изменении концентрации определяемого вещества = значение первой производной градуировочной характеристики
Характеристики метода: Чувствительность Изменение аналитического сигнала при изменении концентрации определяемого вещества = значение первой производной градуировочной характеристики
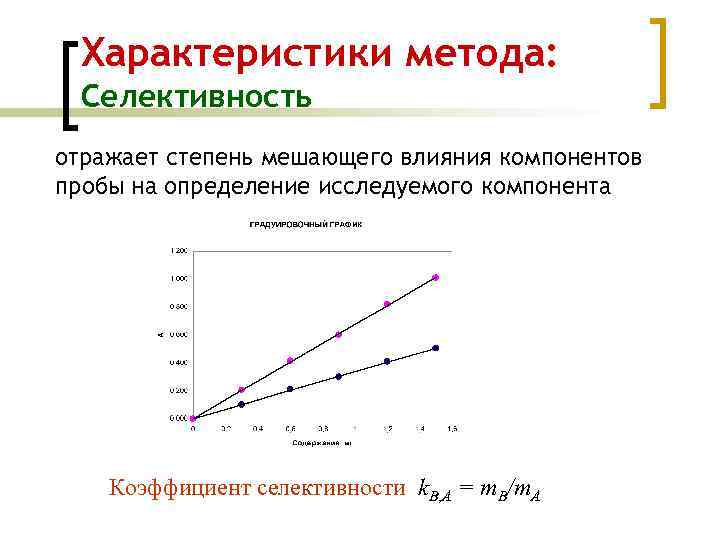 Характеристики метода: Селективность отражает степень мешающего влияния компонентов пробы на определение исследуемого компонента Коэффициент селективности k. B, A = m. B/m. A
Характеристики метода: Селективность отражает степень мешающего влияния компонентов пробы на определение исследуемого компонента Коэффициент селективности k. B, A = m. B/m. A
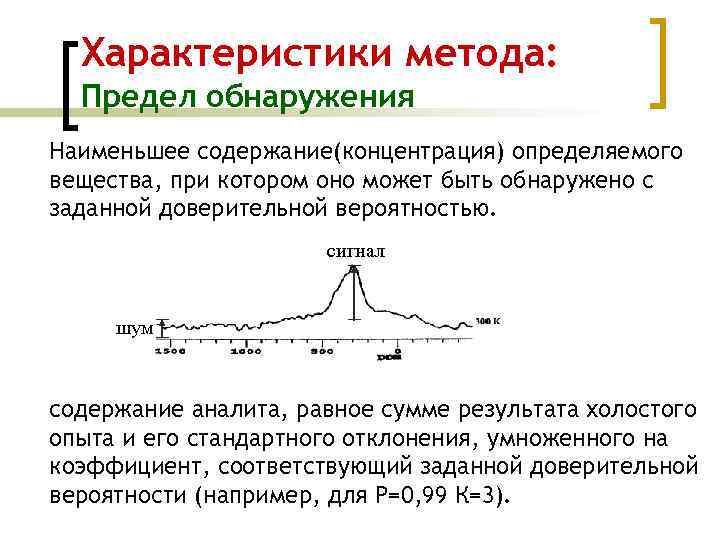 Характеристики метода: Предел обнаружения Наименьшее содержание(концентрация) определяемого вещества, при котором оно может быть обнаружено с заданной доверительной вероятностью. сигнал шум содержание аналита, равное сумме результата холостого опыта и его стандартного отклонения, умноженного на коэффициент, соответствующий заданной доверительной вероятности (например, для Р=0, 99 К=3).
Характеристики метода: Предел обнаружения Наименьшее содержание(концентрация) определяемого вещества, при котором оно может быть обнаружено с заданной доверительной вероятностью. сигнал шум содержание аналита, равное сумме результата холостого опыта и его стандартного отклонения, умноженного на коэффициент, соответствующий заданной доверительной вероятности (например, для Р=0, 99 К=3).
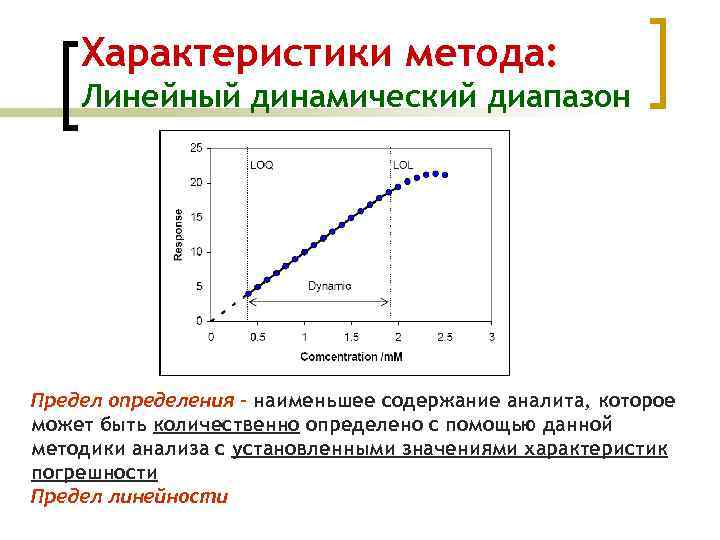 Характеристики метода: Линейный динамический диапазон Предел определения - наименьшее содержание аналита, которое может быть количественно определено с помощью данной методики анализа с установленными значениями характеристик погрешности Предел линейности
Характеристики метода: Линейный динамический диапазон Предел определения - наименьшее содержание аналита, которое может быть количественно определено с помощью данной методики анализа с установленными значениями характеристик погрешности Предел линейности
 ОПТИЧЕСКИЕ (СПЕКТРАЛЬНЫЕ) МЕТОДЫ АНАЛИЗА: Основы методов
ОПТИЧЕСКИЕ (СПЕКТРАЛЬНЫЕ) МЕТОДЫ АНАЛИЗА: Основы методов
 Спектроскопия раздел физики и аналитической химии, посвященный изучению взаимодействия электромагнитного излучения и материи Что такое электромагнитное излучение?
Спектроскопия раздел физики и аналитической химии, посвященный изучению взаимодействия электромагнитного излучения и материи Что такое электромагнитное излучение?
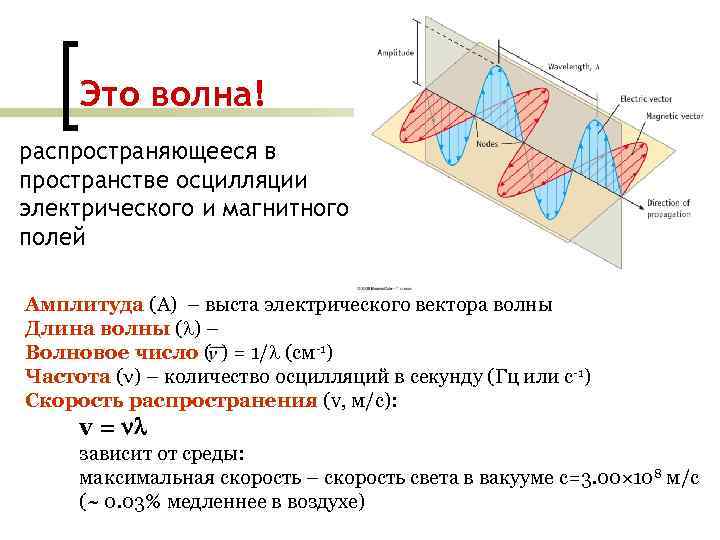 Это волна! распространяющееся в пространстве осцилляции электрического и магнитного полей Амплитуда (A) – выста электрического вектора волны Длина волны ( ) – Волновое число ( ) = 1/ (см-1) Частота ( ) – количество осцилляций в секунду (Гц или с-1) Скорость распространения (v, м/c): v = зависит от среды: максимальная скорость – скорость света в вакууме c=3. 00 108 м/с (~ 0. 03% медленнее в воздухе)
Это волна! распространяющееся в пространстве осцилляции электрического и магнитного полей Амплитуда (A) – выста электрического вектора волны Длина волны ( ) – Волновое число ( ) = 1/ (см-1) Частота ( ) – количество осцилляций в секунду (Гц или с-1) Скорость распространения (v, м/c): v = зависит от среды: максимальная скорость – скорость света в вакууме c=3. 00 108 м/с (~ 0. 03% медленнее в воздухе)
 Электромагнитная волна
Электромагнитная волна
 Это поток частиц! Как и другие частицы, свет может рассеиваться n. Количество частиц можно посчитать n n Фотон=частица энергии Энергия, которую несет фотон, пропорциональна его частоте: n h = 6. 626· 10 -34 Дж·с
Это поток частиц! Как и другие частицы, свет может рассеиваться n. Количество частиц можно посчитать n n Фотон=частица энергии Энергия, которую несет фотон, пропорциональна его частоте: n h = 6. 626· 10 -34 Дж·с
![Электромагнитный спектр [диапазон или ЭМИ] Электромагнитный спектр [диапазон или ЭМИ]](https://present5.com/presentation/131495341_437366963/image-17.jpg) Электромагнитный спектр [диапазон или ЭМИ]
Электромагнитный спектр [диапазон или ЭМИ]
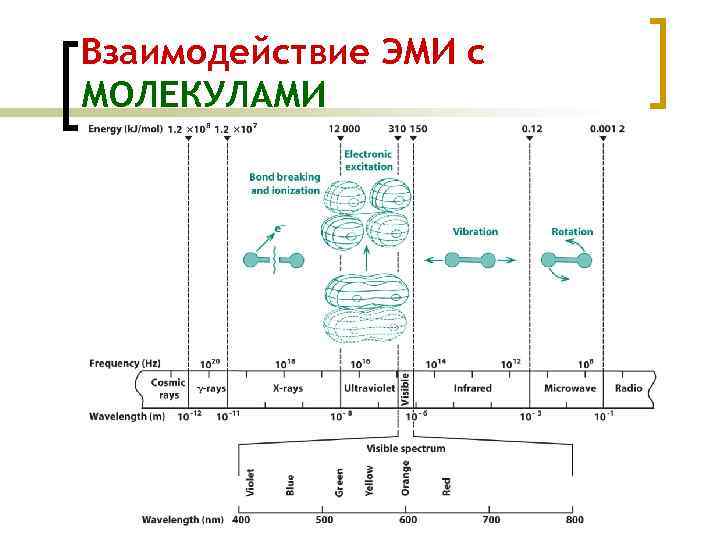 Взаимодействие ЭМИ с МОЛЕКУЛАМИ
Взаимодействие ЭМИ с МОЛЕКУЛАМИ
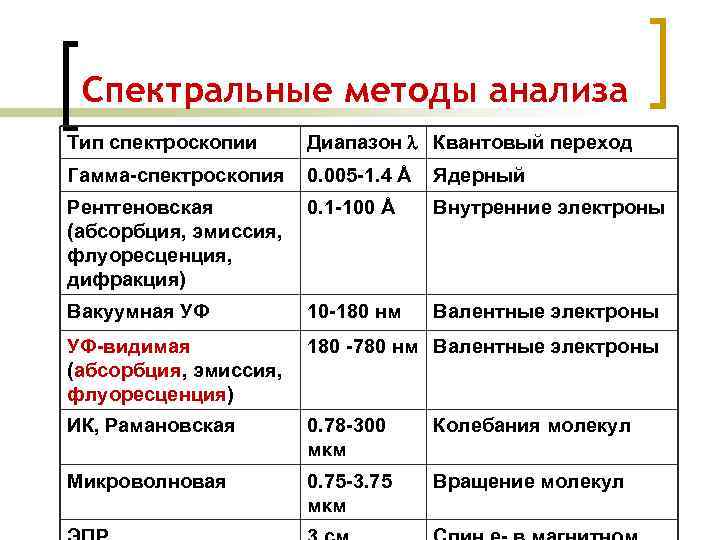 Спектральные методы анализа Тип спектроскопии Диапазон Квантовый переход Гамма-спектроскопия 0. 005 -1. 4 Å Ядерный Рентгеновская (абсорбция, эмиссия, флуоресценция, дифракция) 0. 1 -100 Å Внутренние электроны Вакуумная УФ 10 -180 нм Валентные электроны УФ-видимая (абсорбция, эмиссия, флуоресценция) 180 -780 нм Валентные электроны ИК, Рамановская 0. 78 -300 мкм Колебания молекул Микроволновая 0. 75 -3. 75 мкм Вращение молекул
Спектральные методы анализа Тип спектроскопии Диапазон Квантовый переход Гамма-спектроскопия 0. 005 -1. 4 Å Ядерный Рентгеновская (абсорбция, эмиссия, флуоресценция, дифракция) 0. 1 -100 Å Внутренние электроны Вакуумная УФ 10 -180 нм Валентные электроны УФ-видимая (абсорбция, эмиссия, флуоресценция) 180 -780 нм Валентные электроны ИК, Рамановская 0. 78 -300 мкм Колебания молекул Микроволновая 0. 75 -3. 75 мкм Вращение молекул
 ФОТОМЕТРИЯ Абсорбционная фотометрия - метод, основанный на измерении светопоглощения анализируемым объектом Фотоколориметрия (видимая область, низкая монохроматичность) Спектрофотометрия (УФ и видимая область, высокая монохроматичность)
ФОТОМЕТРИЯ Абсорбционная фотометрия - метод, основанный на измерении светопоглощения анализируемым объектом Фотоколориметрия (видимая область, низкая монохроматичность) Спектрофотометрия (УФ и видимая область, высокая монохроматичность)
 ПРИБОРЫ Колориметр vs Спектрофотометр Разрешающая способность Спектральный диапазон Стабильность источника излучения Точность установки длины волны Диапазон фотометрирования Скорость съемки спектра ЦЕНА
ПРИБОРЫ Колориметр vs Спектрофотометр Разрешающая способность Спектральный диапазон Стабильность источника излучения Точность установки длины волны Диапазон фотометрирования Скорость съемки спектра ЦЕНА
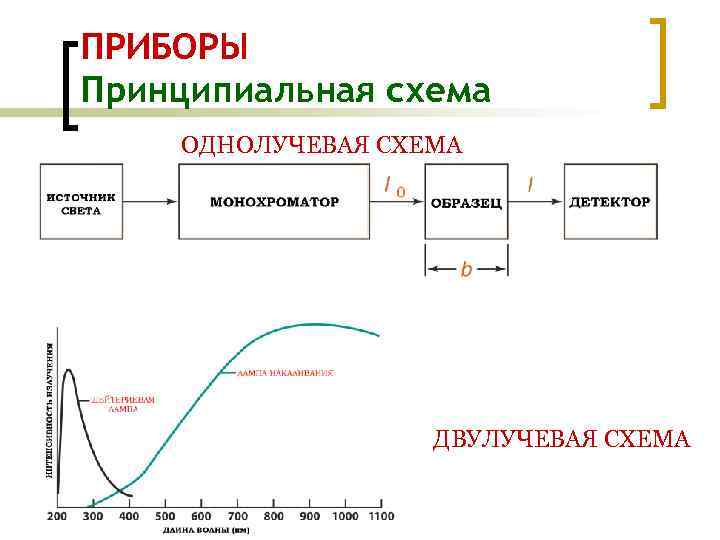 ПРИБОРЫ Принципиальная схема ОДНОЛУЧЕВАЯ СХЕМА ДВУЛУЧЕВАЯ СХЕМА
ПРИБОРЫ Принципиальная схема ОДНОЛУЧЕВАЯ СХЕМА ДВУЛУЧЕВАЯ СХЕМА
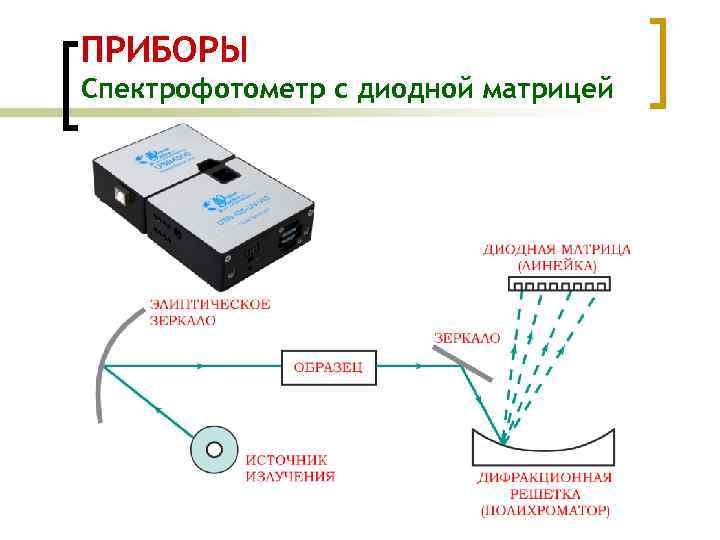 ПРИБОРЫ Спектрофотометр с диодной матрицей
ПРИБОРЫ Спектрофотометр с диодной матрицей
 Закон Бера (Бугера–Ламберта–Бера) Возбужденное состояние Основное состояние Светопоглощение при определенной длине волны описывается законом Бера:
Закон Бера (Бугера–Ламберта–Бера) Возбужденное состояние Основное состояние Светопоглощение при определенной длине волны описывается законом Бера:
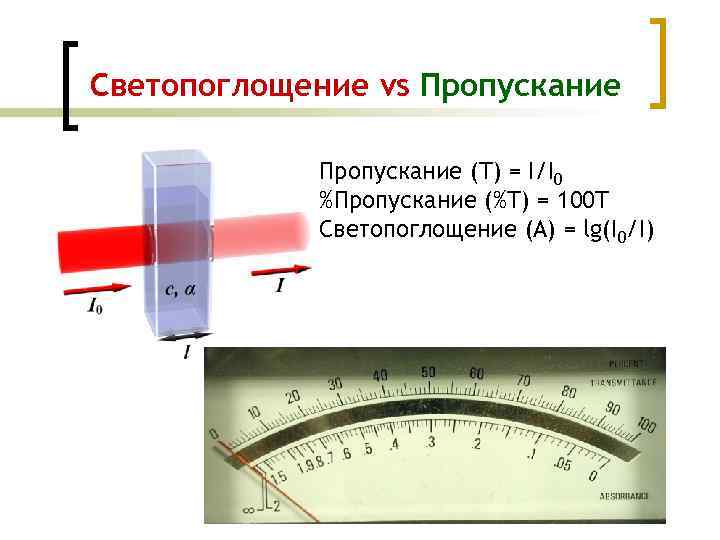 Светопоглощение vs Пропускание (T) = I/I 0 %Пропускание (%T) = 100 T Светопоглощение (A) = lg(I 0/I)
Светопоглощение vs Пропускание (T) = I/I 0 %Пропускание (%T) = 100 T Светопоглощение (A) = lg(I 0/I)
 Закон АДДИТИВНОСТИ светопоглощение смеси веществ равно сумме светопоглощения отдельных компонентов (!!! при отсутствии взаимодействия между ними)
Закон АДДИТИВНОСТИ светопоглощение смеси веществ равно сумме светопоглощения отдельных компонентов (!!! при отсутствии взаимодействия между ними)
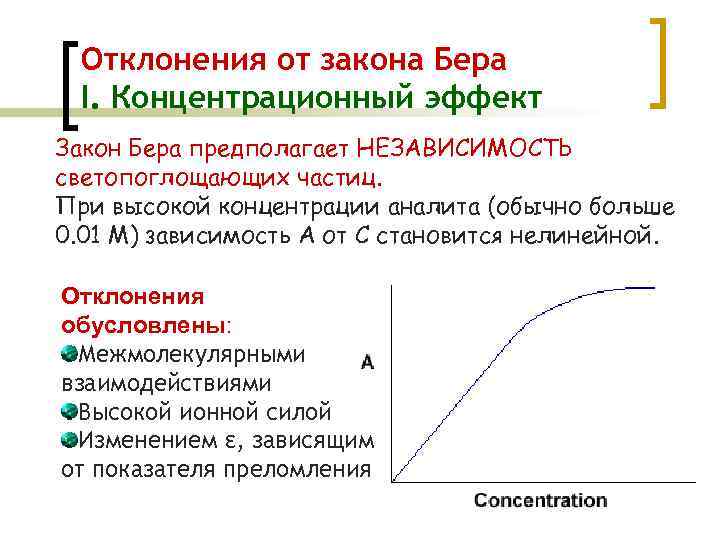 Отклонения от закона Бера I. Концентрационный эффект Закон Бера предполагает НЕЗАВИСИМОСТЬ светопоглощающих частиц. При высокой концентрации аналита (обычно больше 0. 01 М) зависимость А от С становится нелинейной. Отклонения обусловлены: Межмолекулярными взаимодействиями Высокой ионной силой Изменением ε, зависящим от показателя преломления
Отклонения от закона Бера I. Концентрационный эффект Закон Бера предполагает НЕЗАВИСИМОСТЬ светопоглощающих частиц. При высокой концентрации аналита (обычно больше 0. 01 М) зависимость А от С становится нелинейной. Отклонения обусловлены: Межмолекулярными взаимодействиями Высокой ионной силой Изменением ε, зависящим от показателя преломления
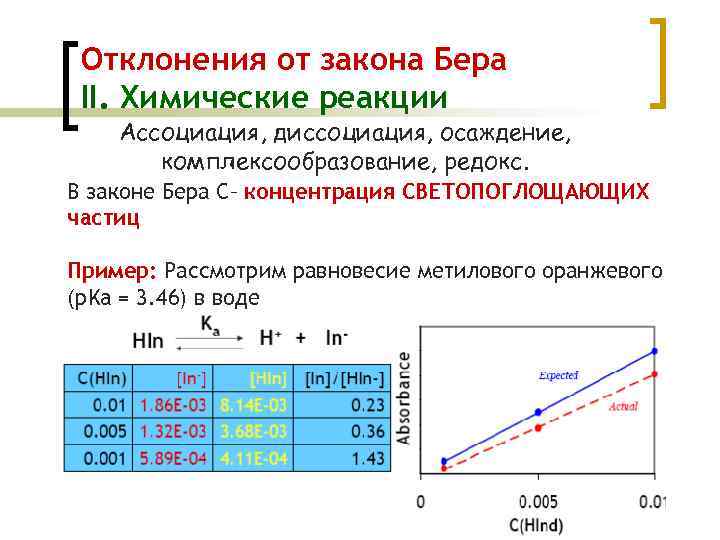 Отклонения от закона Бера II. Химические реакции Ассоциация, диссоциация, осаждение, комплексообразование, редокс. В законе Бера C– концентрация СВЕТОПОГЛОЩАЮЩИХ частиц Пример: Рассмотрим равновесие метилового оранжевого (p. Ka = 3. 46) в воде
Отклонения от закона Бера II. Химические реакции Ассоциация, диссоциация, осаждение, комплексообразование, редокс. В законе Бера C– концентрация СВЕТОПОГЛОЩАЮЩИХ частиц Пример: Рассмотрим равновесие метилового оранжевого (p. Ka = 3. 46) в воде
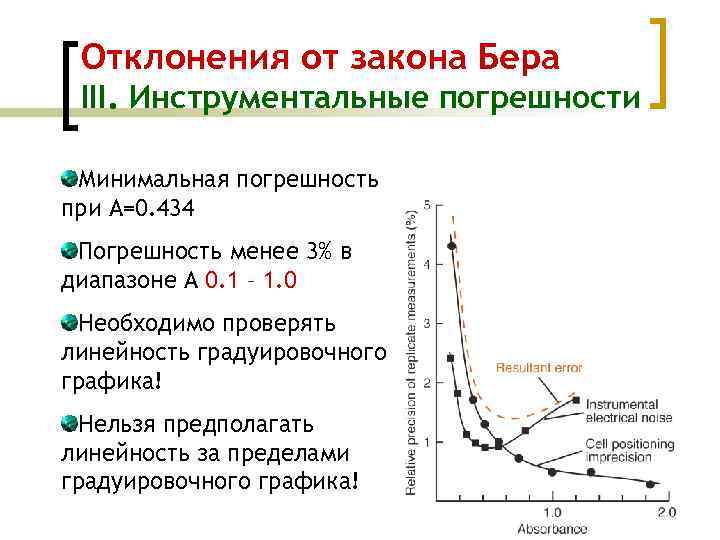 Отклонения от закона Бера III. Инструментальные погрешности Минимальная погрешность при А=0. 434 Погрешность менее 3% в диапазоне A 0. 1 – 1. 0 Необходимо проверять линейность градуировочного графика! Нельзя предполагать линейность за пределами градуировочного графика!
Отклонения от закона Бера III. Инструментальные погрешности Минимальная погрешность при А=0. 434 Погрешность менее 3% в диапазоне A 0. 1 – 1. 0 Необходимо проверять линейность градуировочного графика! Нельзя предполагать линейность за пределами градуировочного графика!
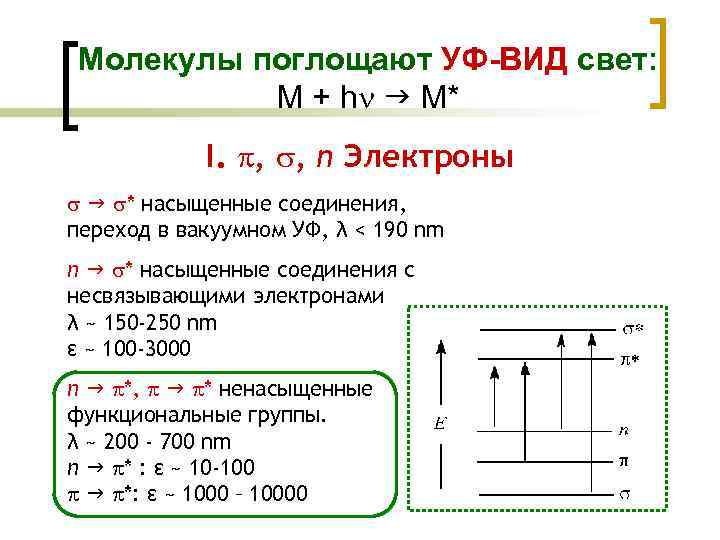 Молекулы поглощают УФ-ВИД свет: M + h M* I. , , n Электроны * насыщенные соединения, переход в вакуумном УФ, λ < 190 nm n * насыщенные соединения с несвязывающими электронами λ ~ 150 -250 nm ε ~ 100 -3000 n *, * ненасыщенные функциональные группы. λ ~ 200 - 700 nm n * : ε ~ 10 -100 *: ε ~ 1000 – 10000
Молекулы поглощают УФ-ВИД свет: M + h M* I. , , n Электроны * насыщенные соединения, переход в вакуумном УФ, λ < 190 nm n * насыщенные соединения с несвязывающими электронами λ ~ 150 -250 nm ε ~ 100 -3000 n *, * ненасыщенные функциональные группы. λ ~ 200 - 700 nm n * : ε ~ 10 -100 *: ε ~ 1000 – 10000
 Молекулы поглощают УФ-ВИД свет. . . II. d d* и f f* Переходы (комплексы ионов переходных металлов)
Молекулы поглощают УФ-ВИД свет. . . II. d d* и f f* Переходы (комплексы ионов переходных металлов)
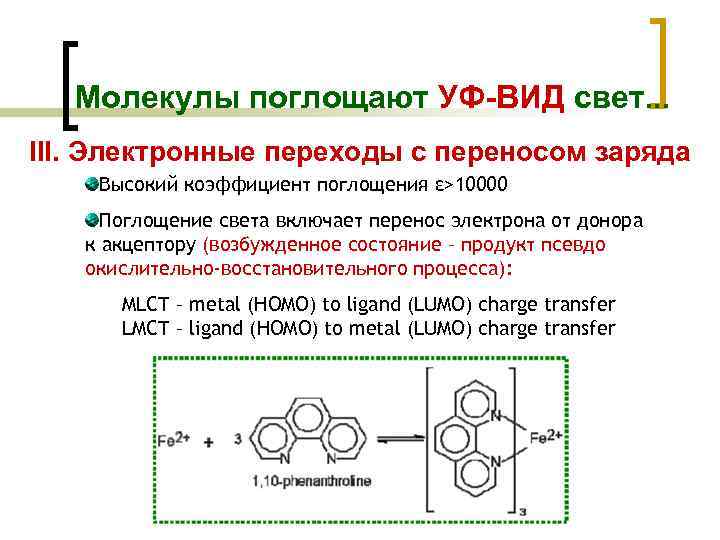 Молекулы поглощают УФ-ВИД свет. . . III. Электронные переходы с переносом заряда Высокий коэффициент поглощения ε>10000 Поглощение света включает перенос электрона от донора к акцептору (возбужденное состояние – продукт псевдо окислительно-восстановительного процесса): MLCT – metal (HOMO) to ligand (LUMO) charge transfer LMCT – ligand (HOMO) to metal (LUMO) charge transfer
Молекулы поглощают УФ-ВИД свет. . . III. Электронные переходы с переносом заряда Высокий коэффициент поглощения ε>10000 Поглощение света включает перенос электрона от донора к акцептору (возбужденное состояние – продукт псевдо окислительно-восстановительного процесса): MLCT – metal (HOMO) to ligand (LUMO) charge transfer LMCT – ligand (HOMO) to metal (LUMO) charge transfer
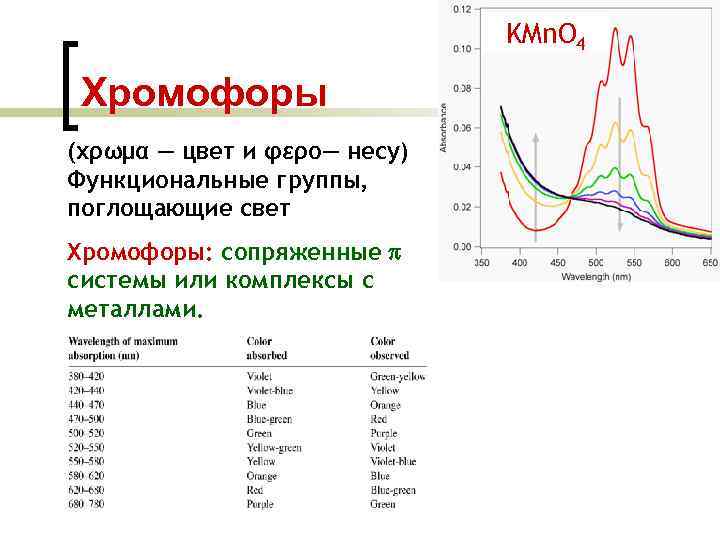 KMn. O 4 Хромофоры (χρωμα — цвет и φερο— несу) Функциональные группы, поглощающие свет Хромофоры: сопряженные системы или комплексы с металлами.
KMn. O 4 Хромофоры (χρωμα — цвет и φερο— несу) Функциональные группы, поглощающие свет Хромофоры: сопряженные системы или комплексы с металлами.
 Что происходит с поглощенной энергией? Безызлучательные переходы (внутренняя, интеркомбинационная конверсия) – энергия переносится через столкновения на молеклы растворителя без излучения фотона M* M + тепло (10 -9― 10 -8 с) Люминесценция – излучение света, происходящее после поглощения веществом энергии возбуждения. M* M + hν* (флуоресценция 10 -8― 10 -4 с и фосфоресценция 10 -4― 10 -2 с) Фотохимическая реакция: M* N (10 -8― 10 -9 s)
Что происходит с поглощенной энергией? Безызлучательные переходы (внутренняя, интеркомбинационная конверсия) – энергия переносится через столкновения на молеклы растворителя без излучения фотона M* M + тепло (10 -9― 10 -8 с) Люминесценция – излучение света, происходящее после поглощения веществом энергии возбуждения. M* M + hν* (флуоресценция 10 -8― 10 -4 с и фосфоресценция 10 -4― 10 -2 с) Фотохимическая реакция: M* N (10 -8― 10 -9 s)
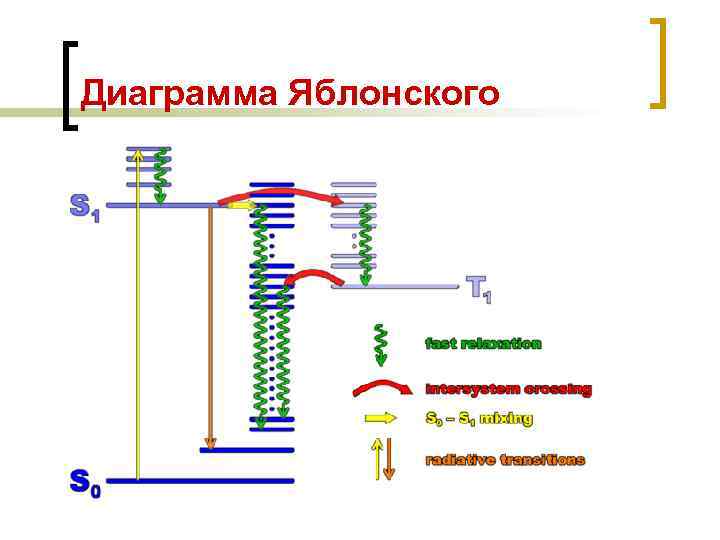 Диаграмма Яблонского
Диаграмма Яблонского
![УФ-ВИД терминология В изобестической точке: A = εl([HIn] + [In-]) УФ-ВИД терминология В изобестической точке: A = εl([HIn] + [In-])](https://present5.com/presentation/131495341_437366963/image-36.jpg) УФ-ВИД терминология В изобестической точке: A = εl([HIn] + [In-])
УФ-ВИД терминология В изобестической точке: A = εl([HIn] + [In-])
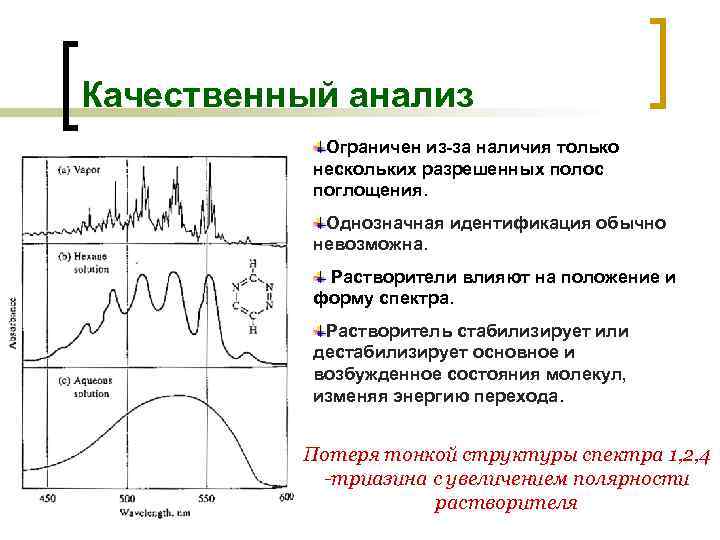 Качественный анализ Ограничен из-за наличия только нескольких разрешенных полос поглощения. Однозначная идентификация обычно невозможна. Растворители влияют на положение и форму спектра. Растворитель стабилизирует или дестабилизирует основное и возбужденное состояния молекул, изменяя энергию перехода. Потеря тонкой структуры спектра 1, 2, 4 -триазина с увеличением полярности растворителя
Качественный анализ Ограничен из-за наличия только нескольких разрешенных полос поглощения. Однозначная идентификация обычно невозможна. Растворители влияют на положение и форму спектра. Растворитель стабилизирует или дестабилизирует основное и возбужденное состояния молекул, изменяя энергию перехода. Потеря тонкой структуры спектра 1, 2, 4 -триазина с увеличением полярности растворителя
 Количественный анализ Широкий круг определяемых соединений (органических и неорганических) Обладает средней селективностью (зачастую требуется отделение, маскирование, селективная реакция) Предел обнаружения 10 -4 - 10 -7 M Прецизионность 1 -5 отн. % Относительно недорогой метод (при использовании колориметров) ПРЯМАЯ и ДИФФЕРЕНЦИАЛЬНАЯ ФОТОМЕТРИЯ основана на установлении зависимости А от С аналита (закон Бера) Метод градуировочного графика Метод стандартных растворов Метод добавок ФОТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Количественный анализ Широкий круг определяемых соединений (органических и неорганических) Обладает средней селективностью (зачастую требуется отделение, маскирование, селективная реакция) Предел обнаружения 10 -4 - 10 -7 M Прецизионность 1 -5 отн. % Относительно недорогой метод (при использовании колориметров) ПРЯМАЯ и ДИФФЕРЕНЦИАЛЬНАЯ ФОТОМЕТРИЯ основана на установлении зависимости А от С аналита (закон Бера) Метод градуировочного графика Метод стандартных растворов Метод добавок ФОТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
![Задача 1: Градуировочный график Определение железа в питьевой воде в виде [Fe(phen)3]2+ Какой массовый Задача 1: Градуировочный график Определение железа в питьевой воде в виде [Fe(phen)3]2+ Какой массовый](https://present5.com/presentation/131495341_437366963/image-39.jpg) Задача 1: Градуировочный график Определение железа в питьевой воде в виде [Fe(phen)3]2+ Какой массовый коэффициент поглощения? Молярный коэффициент поглощения? Как вы оцениваете чувствительность метода? Какой электронный переход осуществляется при 508 нм? Какой цвет этого соединения? Найдите концентрацию железа (ppm) в воде, если A(508 нм)=1. 235
Задача 1: Градуировочный график Определение железа в питьевой воде в виде [Fe(phen)3]2+ Какой массовый коэффициент поглощения? Молярный коэффициент поглощения? Как вы оцениваете чувствительность метода? Какой электронный переход осуществляется при 508 нм? Какой цвет этого соединения? Найдите концентрацию железа (ppm) в воде, если A(508 нм)=1. 235
 Задача 2: Метод стандарта Оптическая плотность раствора стандартного образца кофе, содержащего 1, 00 мг кофеина в 100, 0 мл 0, 005 М H 2 SO 4, равна 0, 510 при 272 нм в кювете с l=1, 00 см. Навеску растворимого кофе массой 2, 5000 г растворили в воде и разбавили до 500, 0 мл. Аликвоту 25, 00 мл полученного раствора поместили в мерную колбу 500, 0 мл, добавили 25 мл 0, 1 М H 2 SO 4, осветлили и разбавили раствор до метки. Оптическая плотность полученного раствора, измеренная в тех жу условиях, равна 0, 415. Рассчитайте массу кофеина в 100 г растворимого кофе.
Задача 2: Метод стандарта Оптическая плотность раствора стандартного образца кофе, содержащего 1, 00 мг кофеина в 100, 0 мл 0, 005 М H 2 SO 4, равна 0, 510 при 272 нм в кювете с l=1, 00 см. Навеску растворимого кофе массой 2, 5000 г растворили в воде и разбавили до 500, 0 мл. Аликвоту 25, 00 мл полученного раствора поместили в мерную колбу 500, 0 мл, добавили 25 мл 0, 1 М H 2 SO 4, осветлили и разбавили раствор до метки. Оптическая плотность полученного раствора, измеренная в тех жу условиях, равна 0, 415. Рассчитайте массу кофеина в 100 г растворимого кофе.
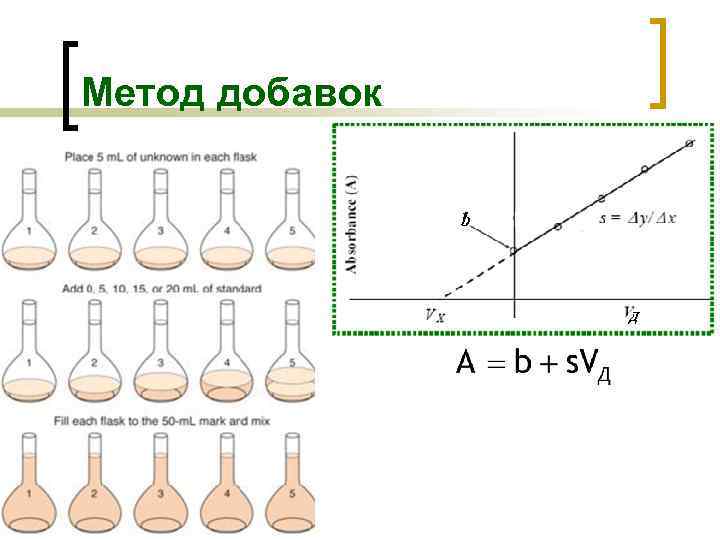 Метод добавок
Метод добавок
 Задача 3: Метод добавок Концентрацию фосфата в моче определяли спектрофотометрически по образованию молибденовой сини. Избыток молибдата добавили к 1. 0 мл образца мочи. Образец разбавили до 5. 0 мл и провели спектрофотометрический анализ. Оптическая плотность, измеренная при 710 нм, составила 0. 139. К 1. 0 мл 5. 0 мг/л раствора фосфата добавили аликвотную часть 1. 0 мл образца мочи, и избыток молибдата аммония. Образец разбавили до 5. 0 мл и измерили светопоглощение. Какова концентрация фосфата в моче (мг/л), если оптическая плотность этого раствора при 710 нм составила 0. 836?
Задача 3: Метод добавок Концентрацию фосфата в моче определяли спектрофотометрически по образованию молибденовой сини. Избыток молибдата добавили к 1. 0 мл образца мочи. Образец разбавили до 5. 0 мл и провели спектрофотометрический анализ. Оптическая плотность, измеренная при 710 нм, составила 0. 139. К 1. 0 мл 5. 0 мг/л раствора фосфата добавили аликвотную часть 1. 0 мл образца мочи, и избыток молибдата аммония. Образец разбавили до 5. 0 мл и измерили светопоглощение. Какова концентрация фосфата в моче (мг/л), если оптическая плотность этого раствора при 710 нм составила 0. 836?
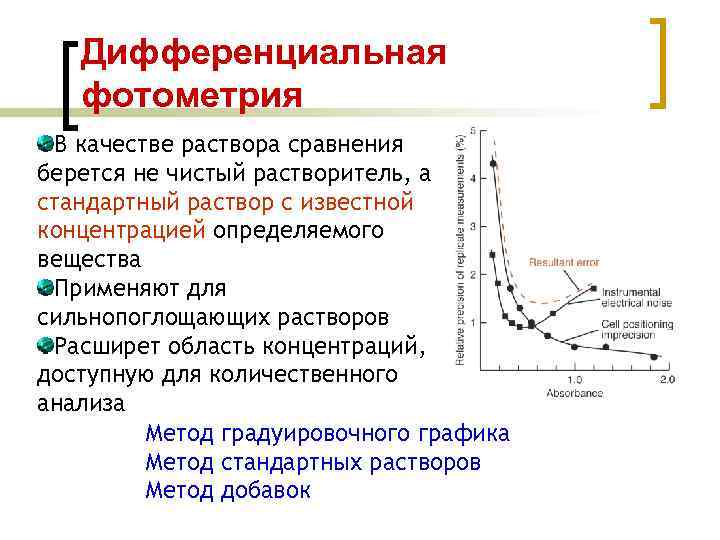 Дифференциальная фотометрия В качестве раствора сравнения берется не чистый растворитель, а стандартный раствор с известной концентрацией определяемого вещества Применяют для сильнопоглощающих растворов Расширет область концентраций, доступную для количественного анализа Метод градуировочного графика Метод стандартных растворов Метод добавок
Дифференциальная фотометрия В качестве раствора сравнения берется не чистый растворитель, а стандартный раствор с известной концентрацией определяемого вещества Применяют для сильнопоглощающих растворов Расширет область концентраций, доступную для количественного анализа Метод градуировочного графика Метод стандартных растворов Метод добавок
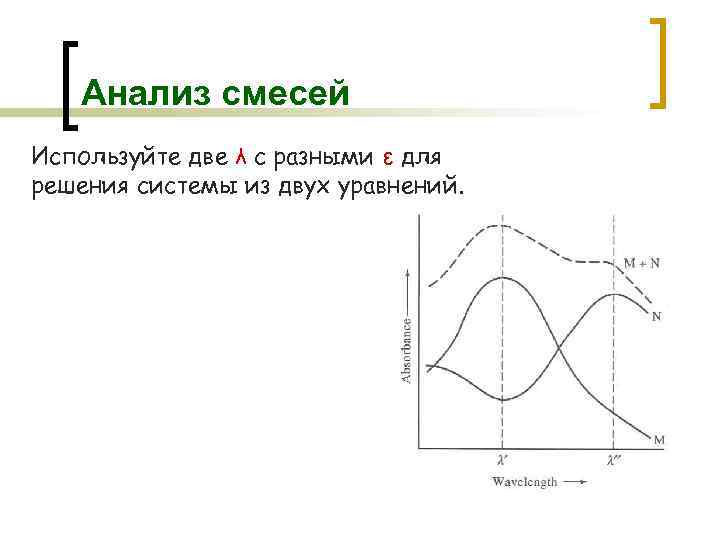 Анализ смесей Используйте две λ с разными ε для решения системы из двух уравнений.
Анализ смесей Используйте две λ с разными ε для решения системы из двух уравнений.
 Задача 4: Анализ смеси Одновременное определение кобальта и никеля можно провести по поглощению их комплексов с 8 -оксихинолином. Известны молярные коэффициенты сооветствующих комплексов в максимумах их светопоглощения: Молярные коэффициенты светопоглощения (M-1 см-1) 365 нм 700 нм Co Ni 3529 3228 428. 9 10. 2 По следующим данным вычислите молярную концентрацию никеля и кобальта в фотометрируемом растворе: Оптическая плотность (1. 00 -см кювета) 365 нм 700 нм Раствор A 0. 598 0. 039
Задача 4: Анализ смеси Одновременное определение кобальта и никеля можно провести по поглощению их комплексов с 8 -оксихинолином. Известны молярные коэффициенты сооветствующих комплексов в максимумах их светопоглощения: Молярные коэффициенты светопоглощения (M-1 см-1) 365 нм 700 нм Co Ni 3529 3228 428. 9 10. 2 По следующим данным вычислите молярную концентрацию никеля и кобальта в фотометрируемом растворе: Оптическая плотность (1. 00 -см кювета) 365 нм 700 нм Раствор A 0. 598 0. 039
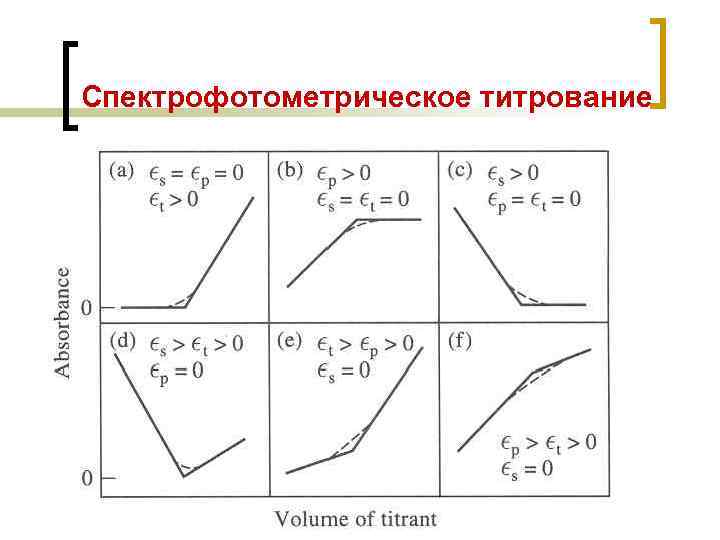 Спектрофотометрическое титрование
Спектрофотометрическое титрование
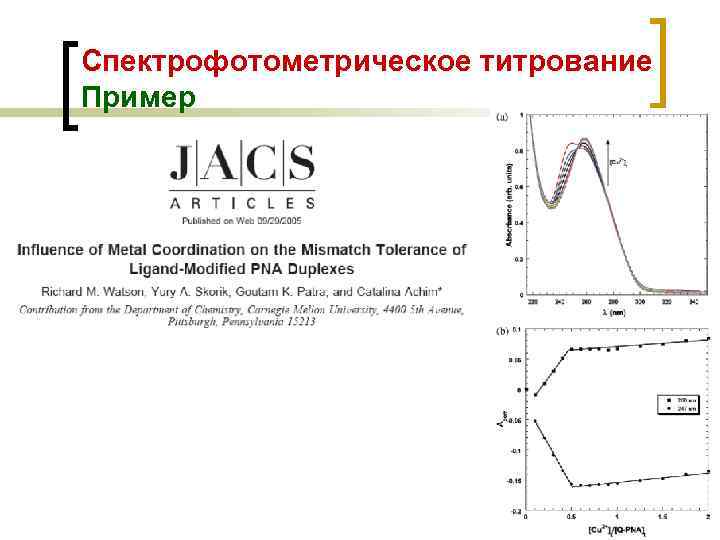 Спектрофотометрическое титрование Пример
Спектрофотометрическое титрование Пример


