Физико-химические методы анализа.pptx
- Количество слайдов: 16

Физико-химические методы анализа.

Инструментальные. Общая характеристика: 1. требуют серьёзного аппаратурного оформления; 2. трудоёмкие; 3. практически все имеют большую погрешность измерения, чем классические; 4. имеют гораздо большую селективность и чувствительность; 5. возможность автоматизации анализа; 6. некоторые из методов экспрессны (выполняются быстро). При гравиметрии 10 -4 г – чувствительность титриметрии 10 -3 -10 -4 г Физ-хим. методы: пико 10 -12 г фемто 10 -15 г.

Классификация 1. Сепарационные (разделительные) : 2. Оптические (рефрактометрия) и спектральные (МАСС) ИКА – спектральные и оптические. - хроматография; - электрофорез. 3. Электрохимические. 4. Прочие: - термогравиметрия; - радиометрические; - физико-химический анализ (исследование зависимости физических свойств от хим. свойств).

Электрохимические методы анализа. 1. Кулонометрия и электрогравиметрия. Кулонометрия основана на измерении количества электричества, требующегося для превращения электроактивного вещества. Q Кл Проводятся в варианте: - прямой кулонометрии; - кулонометрического титрования; - потенциостатической кулонометрии (потенциал = const); - гальваностатической кулонометрии (при I=const). 1)Электрогравиметрия – измерение массы вещества, выделившегося при электролизе. 2)Кондуктометрия – измерение сопротивления (R) или проводимость (i=1/R). 3)Потенциометрия – измеряется потенциал электрода (ЭДС между электродами). 4)Вольтамперометрия – измеряется зависимость I=f(U).
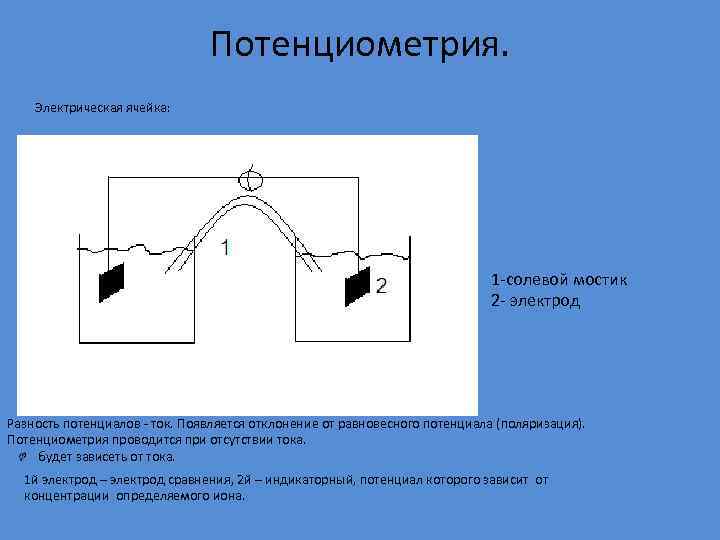
Потенциометрия. Электрическая ячейка: 1 -солевой мостик 2 - электрод Разность потенциалов - ток. Появляется отклонение от равновесного потенциала (поляризация). Потенциометрия проводится при отсутствии тока. будет зависеть от тока. 1 й электрод – электрод сравнения, 2 й – индикаторный, потенциал которого зависит от концентрации определяемого иона.

В качестве электрода сравнения чаще всего используется хлорсеребряный и каломельный электроды. Также водородный, но он не удобен. Потенциал индикаторного электрода также определяется уравнением Нернста:

• 1. Энертные электроды. В случае их использования материал электрода не участвует в процессе, переноса вещества нет. Платиновый, угольный, графитовый и другие, благородные металлы. • 2. Активные электроды. Материалы электрода участвуют в переносе вещества и заряда. Простейшие – электроды 1 го рода (металлы, погруженные в соль этого металла). Ag+/Ag 0; Zn 2+/Zn 0 Электроды 2 го рода (потенциал определяется ионом, который вместе с металлом образует соль). Мембранные электроды: C 6 H 4 O 2+2 H++2 Cl- = C 6 H 6 O 2

Для инертного электрода с редокс-потенциалом: Для мембранного электрода: В зависимости от состава мембраны Для активного электрода: U=E 1 -E 2+Eg E 2 – потенциал электрода сравнения; Eg - диффузный потенциал ( возникает на границе раздела растворов 1 вещества разных концентраций или растворов разных веществ за счёт различной подвижности ионов).
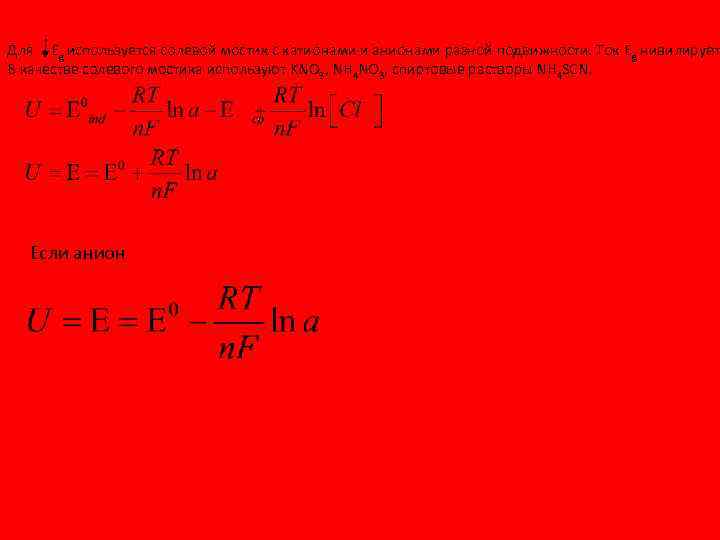
Для Eg используется солевой мостик с катионами и анионами разной подвижности. Ток Eg нивилирует В качестве солевого мостика используют KNO 3, NH 4 NO 3, спиртовые растворы NH 4 SCN. Если анион

Потенциал – функция логарифма активности: Величина, равная tg наклона градуировочной характеристики является показателем качества работы электрода. Может быть употреблён термин электродная функция

Мембранные электроды. 1. Электроды с твердой мембраной (стеклянный p. H – электрод). 2. Электроды со стеклообразной мембраной. 3. Электроды с монокристаллической мембраной. 4. Электроды с поликристаллической мембраной. 5. Электроды с гетерогенной мембраной. 1. p. H – электрод. - потенциал стеклянного электрода, определяется экспериментально.

2. Электроды с жидкой мембраной. Мембрана представляет собой гидрофобную пористую пластинку, пропитанную несмешивающейся с водой жидкостью, содержащей соли металла. Чувствительны к солям кальция и другим двухвалентным металлам. Коэффициент селективности – отношение концентрации целевого иона к концентрации мешающего иона , при которой он даёт такую же величину сигнала. Ион – селективные электроды – электроды, чувствительные к определённому катиону или аниону (1 го, 2 го рода и мембранные, чаще всего мембранные).

Практические приложения потенциометрического анализа. Прямая потенциометрии основана на прямом измерении потенциала и нахождении активности иона в растворе. • Преимущества: • - высокая скорость анализа; • - минимальная пробоподготовка; • -достаточно высокая селективность; • - возможность анализа дисперсных систем и окрашенных систем; • - чувствительный метод.

Недостаток - сравнительно высокая погрешность анализа. определение погрешности косвенного измерения - погрешность ЭДС Если ЭДС измерять в м. В, а погрешность в %, то

Количественное определение в прямой потенциометрии: - по градуировочному графику; - методом стандартной добавки; - метод концентрационного элемента. Электроды: - сравнения (насыщенные хлорсеребряные); • - индикаторные (p. H-электроды). • • •

Потенциометрическое титрование. Точность как у классических методов титрования, селективность отсутствует. Преимущество по сравнению с индикаторным титрованием: - возможность более тонкого фиксированного скачка титрования; - возможность титрования вещества с менее ярко выраженными ионно-основными свойствами; - возможность титрования смеси; - возможность автоматизации. Применение: - кислотно-основное титрование (стеклянный электрод); - осадительное (индикаторный серебряный электрод); - определение галогенидов и их солей; - комплексометрическое титрование; - окислительно – восстановительное титрование(инертные редокс – электроды: платиновые, графитовые). Определение точки эквивалентности: графическое (построение кривых титрования: интегральные, дифференциальные, бидифференциальные). расчётные (метод Грана).
Физико-химические методы анализа.pptx