Lecture 06.ppt
- Количество слайдов: 24
 Физика твердого тела Курс лекций 1 ВОЛНОВОЕ УРАВНЕНИЕ 2. Решение уравнения Шрёдингера для одномерного потенциального ящика 3. Решение уравнения Шрёдингера для трёхмерного потенциального ящика
Физика твердого тела Курс лекций 1 ВОЛНОВОЕ УРАВНЕНИЕ 2. Решение уравнения Шрёдингера для одномерного потенциального ящика 3. Решение уравнения Шрёдингера для трёхмерного потенциального ящика
 ВОЛНОВОЕ УРАВНЕНИЕ Для описания состояния физического объекта требуется указать E – энергию тела, р – импульс, [x, y, z] –координаты. Описание состояния твердого тела сводится к описанию состояния составляющих его микрочастиц: атомов, ионов, электронов. Атомы, ионы и электроны это – микрочастицы, находящиеся в микрообъеме. Из-за присущего им свойства, описываемого соотношением Гейзенберга (ΔрΔх h), возникает проблема точного «механического» описания их состояния. Австрийский физик Э. Шредингер (1926) предложил описывать состояние микрочастиц волновой функцией, являющейся решением волнового уравнения. Простейшее волновое уравнение имеет вид:
ВОЛНОВОЕ УРАВНЕНИЕ Для описания состояния физического объекта требуется указать E – энергию тела, р – импульс, [x, y, z] –координаты. Описание состояния твердого тела сводится к описанию состояния составляющих его микрочастиц: атомов, ионов, электронов. Атомы, ионы и электроны это – микрочастицы, находящиеся в микрообъеме. Из-за присущего им свойства, описываемого соотношением Гейзенберга (ΔрΔх h), возникает проблема точного «механического» описания их состояния. Австрийский физик Э. Шредингер (1926) предложил описывать состояние микрочастиц волновой функцией, являющейся решением волнового уравнения. Простейшее волновое уравнение имеет вид:
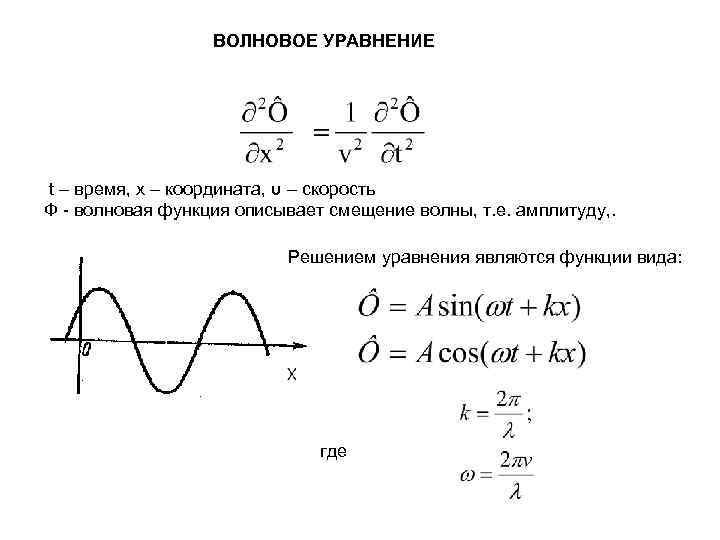 ВОЛНОВОЕ УРАВНЕНИЕ t – время, х – координата, υ – скорость Ф - волновая функция описывает смещение волны, т. е. амплитуду, . Решением уравнения являются функции вида: где
ВОЛНОВОЕ УРАВНЕНИЕ t – время, х – координата, υ – скорость Ф - волновая функция описывает смещение волны, т. е. амплитуду, . Решением уравнения являются функции вида: где
 Для 3 -х мерного случая волновое уравнение имеет вид: Запись: Называется оператором Лапласа и является оператором кинетической энергии частицы. Тогда волновое уравнение записывается как:
Для 3 -х мерного случая волновое уравнение имеет вид: Запись: Называется оператором Лапласа и является оператором кинетической энергии частицы. Тогда волновое уравнение записывается как:
 Шредингер преобразовал волновое уравнение для описания состояния микрочастиц. Для этого он добавил в уравнение (а)член учитывающий потенциальную энергию для стационарных систем, (б) убрал член, описывающий изменение энергии во времени. В результате получилось Уравнение известное как уравнение Шредингера: m – масса частицы - Волновая функция U –потенциальная энергия E – полная энергия частицы. Уравнение Шредингера является уравнением сохранения Энергии. Первый член описывает кинетическую энергию, Второй член - описывает кинетическую энергию, Последний член – полную энергию.
Шредингер преобразовал волновое уравнение для описания состояния микрочастиц. Для этого он добавил в уравнение (а)член учитывающий потенциальную энергию для стационарных систем, (б) убрал член, описывающий изменение энергии во времени. В результате получилось Уравнение известное как уравнение Шредингера: m – масса частицы - Волновая функция U –потенциальная энергия E – полная энергия частицы. Уравнение Шредингера является уравнением сохранения Энергии. Первый член описывает кинетическую энергию, Второй член - описывает кинетическую энергию, Последний член – полную энергию.
 Для электронов волновая функция Ψ - это не столько амплитудная функция, сколько мера вероятности (вероятностная функция). Квадрат амплитуды волновой функции (x, y, z) 2 выражает относительную плотность вероятности обнаружения частицы в точке с координатами (х, y, z). Решение уравнения Шрёдингера для атома водорода позволяет определить волновые функции (x, y, z) и дискретные энергетические уровни энергии электронов в атоме.
Для электронов волновая функция Ψ - это не столько амплитудная функция, сколько мера вероятности (вероятностная функция). Квадрат амплитуды волновой функции (x, y, z) 2 выражает относительную плотность вероятности обнаружения частицы в точке с координатами (х, y, z). Решение уравнения Шрёдингера для атома водорода позволяет определить волновые функции (x, y, z) и дискретные энергетические уровни энергии электронов в атоме.
 Решение уравнения Шрёдингера для одномерного потенциального ящика Одномерным потенциальным ящиком называется область пространства, в которой потенциальная энергия равна нулю, а на границах ящика превращается в бесконечность Одномерный потенциальный ящик Граничные условия в этом случае: 1) при x = 0 =0 2) при x = а Уравнение Шредингера имеет вид:
Решение уравнения Шрёдингера для одномерного потенциального ящика Одномерным потенциальным ящиком называется область пространства, в которой потенциальная энергия равна нулю, а на границах ящика превращается в бесконечность Одномерный потенциальный ящик Граничные условия в этом случае: 1) при x = 0 =0 2) при x = а Уравнение Шредингера имеет вид:
 Обозначим Тогда уравнение Шредингера принимает вид Решением такого дифференциального уравнения в общем виде является функция Действительно, . . , ( )=
Обозначим Тогда уравнение Шредингера принимает вид Решением такого дифференциального уравнения в общем виде является функция Действительно, . . , ( )=
 С учетом первого граничного условия получим: 0= или 0 = А(0)+В(1). Для того, чтобы выполнялось это равенство, необходимо, чтобы постоянная В была равна нулю. Следовательно, . Учитывая, что при x = а, = 0 (второе граничное уравнение), получим Это равенство справедливо при А=0. Такое решение называется тривиальным, поскольку обращает волновую функцию в ноль.
С учетом первого граничного условия получим: 0= или 0 = А(0)+В(1). Для того, чтобы выполнялось это равенство, необходимо, чтобы постоянная В была равна нулю. Следовательно, . Учитывая, что при x = а, = 0 (второе граничное уравнение), получим Это равенство справедливо при А=0. Такое решение называется тривиальным, поскольку обращает волновую функцию в ноль.
 Имеется и другой способ сохранения равенства. Оно выполняется, очевидно, при , где п- целое число. Тогда решение волнового уравнения принимает вид: Постоянная А может быть определена из условия нормировки: или
Имеется и другой способ сохранения равенства. Оно выполняется, очевидно, при , где п- целое число. Тогда решение волнового уравнения принимает вид: Постоянная А может быть определена из условия нормировки: или
 Отсюда Таким образом, волновая функция описывается уравнением: Теперь вычислим энергию частицы. Поскольку Получаем: Используя уравнение Шредингера
Отсюда Таким образом, волновая функция описывается уравнением: Теперь вычислим энергию частицы. Поскольку Получаем: Используя уравнение Шредингера
 Выводы по решению уравнения Шрёдингера: 1. Энергия электрона квантована и принимает дискретные значения. 2. Энергия электрона определяется значением n – главного квантового числа, 3. Вероятность нахождения электрона в той или иной области потенциального ящика, определяется волновой функцией : Зависит от значения квантового числа n. 4. Вероятности неодинаковы для разных точек пространства. 5. В некоторых точках вероятность равна нулю. Такие точки называются узловыми.
Выводы по решению уравнения Шрёдингера: 1. Энергия электрона квантована и принимает дискретные значения. 2. Энергия электрона определяется значением n – главного квантового числа, 3. Вероятность нахождения электрона в той или иной области потенциального ящика, определяется волновой функцией : Зависит от значения квантового числа n. 4. Вероятности неодинаковы для разных точек пространства. 5. В некоторых точках вероятность равна нулю. Такие точки называются узловыми.
 Решение уравнения Шрёдингера для трёхмерного потенциального ящика Трехмерный потенциальный ящик имеет форму куба с ребром а. Задача состоит в нахождении волновой функции для уравнения: Разделим его на составляющие уравнения, каждое из которых содержит только одну из координат. С этой целью представим Е и Ψ в следующем виде: После подстановки Е и в уравнение получим:
Решение уравнения Шрёдингера для трёхмерного потенциального ящика Трехмерный потенциальный ящик имеет форму куба с ребром а. Задача состоит в нахождении волновой функции для уравнения: Разделим его на составляющие уравнения, каждое из которых содержит только одну из координат. С этой целью представим Е и Ψ в следующем виде: После подстановки Е и в уравнение получим:
 Поделим левую и правую часть этого уравнения на (X. Y, Z): Полученное уравнение можно рассматривать как сумму трех уравнений:
Поделим левую и правую часть этого уравнения на (X. Y, Z): Полученное уравнение можно рассматривать как сумму трех уравнений:
 Решение каждого из приведенных уравнений известно из задачи об одномерном потенциальном ящике: , где nx = 1, 2, 3 …; , где ny = 1, 2, 3 …; , где n z = 1, 2, 3 … Для энергии и волновой функции получаем следующее выражения: =
Решение каждого из приведенных уравнений известно из задачи об одномерном потенциальном ящике: , где nx = 1, 2, 3 …; , где ny = 1, 2, 3 …; , где n z = 1, 2, 3 … Для энергии и волновой функции получаем следующее выражения: =
 Выводы. 1. Энергия электрона квантована и принимает дискретные значения. 2. Волновая функция электрона и его энергия определяется значениями трёх квантовых чисел, 3. Количество квантовых чисел равно числу степеней свободы частицы. 4. Выводы 1 -3 можно распространить на поведение электрона в более сложных системах, например, электрона в атоме.
Выводы. 1. Энергия электрона квантована и принимает дискретные значения. 2. Волновая функция электрона и его энергия определяется значениями трёх квантовых чисел, 3. Количество квантовых чисел равно числу степеней свободы частицы. 4. Выводы 1 -3 можно распространить на поведение электрона в более сложных системах, например, электрона в атоме.
 Атом водорода В атоме водорода вокруг положительно заряженного ядра движется единственный электрон. Потенциальная энергия взаимодействия его с ядром равна: Стационарные состояния атома водорода описывается уравнением
Атом водорода В атоме водорода вокруг положительно заряженного ядра движется единственный электрон. Потенциальная энергия взаимодействия его с ядром равна: Стационарные состояния атома водорода описывается уравнением
 Решение этого уравнения приводит к следующим основным результатам. 1. Электрон в атоме водорода обладает дискретным энергетическим спектром. 2. Собственные значения энергии определяются формулой: где -универсальная постоянная, n-главное квантовое число , 2. Орбитальный момент количества движения pl может принимать лишь следующий дискретный ряд значений: где l побочное квантовое число. Состояние с l=0 (при любом n) принято называть s-состоянием, с 1=1 р-состоянием, с 1=2 - d-состоянием, с 1=3— f-состоянием и т. д.
Решение этого уравнения приводит к следующим основным результатам. 1. Электрон в атоме водорода обладает дискретным энергетическим спектром. 2. Собственные значения энергии определяются формулой: где -универсальная постоянная, n-главное квантовое число , 2. Орбитальный момент количества движения pl может принимать лишь следующий дискретный ряд значений: где l побочное квантовое число. Состояние с l=0 (при любом n) принято называть s-состоянием, с 1=1 р-состоянием, с 1=2 - d-состоянием, с 1=3— f-состоянием и т. д.
 3. Орбитальный момент количества движения может ориентироваться относительно избранного направления магнитного поля H лишь таким образом, что проекция его на это направление целократна m — называется магнитным квантовым числом. Принимает все целочисленные значения от -l до +l всего (2 l+1) значений. Ориентация орбитального момента количества движения
3. Орбитальный момент количества движения может ориентироваться относительно избранного направления магнитного поля H лишь таким образом, что проекция его на это направление целократна m — называется магнитным квантовым числом. Принимает все целочисленные значения от -l до +l всего (2 l+1) значений. Ориентация орбитального момента количества движения
 Решение уравнения Шрёдингера для атома водорода Имеет три квантовых числа: n - главное квантовое число, принимает целочисленные значения 1, 2, 3, 4, …, n L - побочное (орбитальное) квантовое число, принимающее целочисленные значения от 0 до n - 1; m - магнитное квантовое число, которое изменяться от –l до +l. Обозначение волновых функций l = 0 – s -орбитали; l = 1 – p -орбитали; l = 2 – d -орбитали; l = 3 – f - орбитали. l = 4 - q - орбитали. l = 5 -h , q и h - орбиталями. S- спиновое квантовое число s, принимает значения + 1/2 или -1/2.
Решение уравнения Шрёдингера для атома водорода Имеет три квантовых числа: n - главное квантовое число, принимает целочисленные значения 1, 2, 3, 4, …, n L - побочное (орбитальное) квантовое число, принимающее целочисленные значения от 0 до n - 1; m - магнитное квантовое число, которое изменяться от –l до +l. Обозначение волновых функций l = 0 – s -орбитали; l = 1 – p -орбитали; l = 2 – d -орбитали; l = 3 – f - орбитали. l = 4 - q - орбитали. l = 5 -h , q и h - орбиталями. S- спиновое квантовое число s, принимает значения + 1/2 или -1/2.
 Энергетические состояния атома водорода : n l m Название состояния Количество подуровней 1 0 0 1 s 1 2 0 0 2 s 1 2 1 -1 2 p 3 2 1 0 2 p 3 2 1 +1 2 p 3 Представленная комбинация квантовых чисел определяет энергию электрона
Энергетические состояния атома водорода : n l m Название состояния Количество подуровней 1 0 0 1 s 1 2 0 0 2 s 1 2 1 -1 2 p 3 2 1 0 2 p 3 2 1 +1 2 p 3 Представленная комбинация квантовых чисел определяет энергию электрона
 Форма атомных орбиталей
Форма атомных орбиталей
 Строение многоэлектронных атомов 1. В многоэлектронных атомах форма орбиталей, такая же, как в атоме водорода 2. Модель многоэлектронного атома можно построить из последовательности водородоподобных орбиталей. 3. Последовательность определяется энергией орбиталей, то есть значениями квантовых чисел n и l. 4. По сравнению с атомом водорода значительный вклад вносит число l, что обусловлено двумя эффектами: а. Эффект экранирования - действие ядра на электрон в многоэлектронном атом может ослабляться экранирующим действием внутренних электронных оболоче б. Эффект проникновения электрона к ядру (плотность е на ядре) 5 d Наибольшую плотность имеют s электроны, затем p. В связи с этим порядок возрастания энергии следующий: 1 s<2 s<2 p<3 s<3 p<4 s<3 d<4 p<5 s<4 d<5 p<6 s<5 f=5 d<6 p<7 s<7 f
Строение многоэлектронных атомов 1. В многоэлектронных атомах форма орбиталей, такая же, как в атоме водорода 2. Модель многоэлектронного атома можно построить из последовательности водородоподобных орбиталей. 3. Последовательность определяется энергией орбиталей, то есть значениями квантовых чисел n и l. 4. По сравнению с атомом водорода значительный вклад вносит число l, что обусловлено двумя эффектами: а. Эффект экранирования - действие ядра на электрон в многоэлектронном атом может ослабляться экранирующим действием внутренних электронных оболоче б. Эффект проникновения электрона к ядру (плотность е на ядре) 5 d Наибольшую плотность имеют s электроны, затем p. В связи с этим порядок возрастания энергии следующий: 1 s<2 s<2 p<3 s<3 p<4 s<3 d<4 p<5 s<4 d<5 p<6 s<5 f=5 d<6 p<7 s<7 f
 Заполнение энергетических уровней происходит в соответствии с принципом Паули. Принцип Паули запрещает находиться в одном энергетическом состоянии более чем двум электронам с различными спинами. Другими словами, в атоме не может быть двух электронов с четырьмя одинаковыми квантовыми числами. Или, в одном энергетическом состоянии могут находиться лишь два электрона с разным спинами. При не полном заполнении уровня характер заполнения электронов определяет также правило Хунда. электроны стремятся избегать одной и той же орбитали, причём, расположенные на разных орбиталях электроны имеют одинаково направленные спины.
Заполнение энергетических уровней происходит в соответствии с принципом Паули. Принцип Паули запрещает находиться в одном энергетическом состоянии более чем двум электронам с различными спинами. Другими словами, в атоме не может быть двух электронов с четырьмя одинаковыми квантовыми числами. Или, в одном энергетическом состоянии могут находиться лишь два электрона с разным спинами. При не полном заполнении уровня характер заполнения электронов определяет также правило Хунда. электроны стремятся избегать одной и той же орбитали, причём, расположенные на разных орбиталях электроны имеют одинаково направленные спины.


