 Физика горения д. ф. -м. н. О. С. Рабинович Лекция 2 Термодинамика и химическая кинетика процессов горения
Физика горения д. ф. -м. н. О. С. Рабинович Лекция 2 Термодинамика и химическая кинетика процессов горения
 Ч. I Термодинамика процессов горения
Ч. I Термодинамика процессов горения
 I. Термодинамика процессов горения Что может и чего не может термодинамика? Термодинамика позволяет ответить на следующие важные для теории и практики горения вопросы: 1. Какова температура продуктов сгорания? 2. Каков состав смеси этих продуктов? 3. Какое количество теплоты можно получить в результате сгорания реагентов? Недостаточность термодинамического подхода: 1. Не рассматривается кинетика, т. е. скорость химических процессов; 2. Не всегда температура и состав продуктов соответствуют термодинамическому равновесию.
I. Термодинамика процессов горения Что может и чего не может термодинамика? Термодинамика позволяет ответить на следующие важные для теории и практики горения вопросы: 1. Какова температура продуктов сгорания? 2. Каков состав смеси этих продуктов? 3. Какое количество теплоты можно получить в результате сгорания реагентов? Недостаточность термодинамического подхода: 1. Не рассматривается кинетика, т. е. скорость химических процессов; 2. Не всегда температура и состав продуктов соответствуют термодинамическому равновесию.
 I. Термодинамика процессов горения Пример: CH 4 + 2 O 2 (+ N 2) CO 2 + 2 H 2 O стехиометрическая смесь: 9. 5% CH 4 +19%О 2+71. 5 N 2 I. 1 Топливо, окислитель, стехиометрия (Воздух: 21% О 2 + 79% N 2) Стехиометрическое соотношение концентраций реагентов – такая их пропорция, при которой они вступают в реакцию без остатка, (F/O)st. Эквивалентное отношение (equivalence ratio) – < 1 – бедная (топливом) смесь >1 – богатая смесь Несимметричность определения - области богатой и бедной смеси имеют разную «протяженность» . Нормализованное эквивалентное отношение устраняет этот недостаток:
I. Термодинамика процессов горения Пример: CH 4 + 2 O 2 (+ N 2) CO 2 + 2 H 2 O стехиометрическая смесь: 9. 5% CH 4 +19%О 2+71. 5 N 2 I. 1 Топливо, окислитель, стехиометрия (Воздух: 21% О 2 + 79% N 2) Стехиометрическое соотношение концентраций реагентов – такая их пропорция, при которой они вступают в реакцию без остатка, (F/O)st. Эквивалентное отношение (equivalence ratio) – < 1 – бедная (топливом) смесь >1 – богатая смесь Несимметричность определения - области богатой и бедной смеси имеют разную «протяженность» . Нормализованное эквивалентное отношение устраняет этот недостаток:
 I. Термодинамика процессов горения I. 2 Химическое равновесие Основная задача – рассчитать равновесное состояние системы для заданного набора термодинамических переменных: (T, p), (T, V), (H, p), (U, V), (S, V) и т. д. I. 2. 1 Первое и второе начала термодинамики Первое начало: или Q - теплота, сообщённая системе; A - работа совершенная системой; d. U - изменение внутренней энергии системы; d. U - полный дифференциал, U является функцией состояния системы; Q и A - зависят от пути, по которому идёт процесс. Введём функцию состояния S – энтропию, таким образом, что в равновесном процессе Для равновесного процесса , т. е. U = U(S, V) – внутренняя энергия – функция энтропии и объёма. 4
I. Термодинамика процессов горения I. 2 Химическое равновесие Основная задача – рассчитать равновесное состояние системы для заданного набора термодинамических переменных: (T, p), (T, V), (H, p), (U, V), (S, V) и т. д. I. 2. 1 Первое и второе начала термодинамики Первое начало: или Q - теплота, сообщённая системе; A - работа совершенная системой; d. U - изменение внутренней энергии системы; d. U - полный дифференциал, U является функцией состояния системы; Q и A - зависят от пути, по которому идёт процесс. Введём функцию состояния S – энтропию, таким образом, что в равновесном процессе Для равновесного процесса , т. е. U = U(S, V) – внутренняя энергия – функция энтропии и объёма. 4
 Второе начало термодинамики: для необратимых процессов Тогда, с использованием I-го начала, получаем, что Равенство выполняется только в случае равновесных (обратимых) процессов. Если S и V фиксированы, то . Это означает, что при S = const и V = const все неравновесные процессы протекают с уменьшением внутренней энергии, а в равновесии, когда выполняется равенство, внутренняя энергия достигает минимума.
Второе начало термодинамики: для необратимых процессов Тогда, с использованием I-го начала, получаем, что Равенство выполняется только в случае равновесных (обратимых) процессов. Если S и V фиксированы, то . Это означает, что при S = const и V = const все неравновесные процессы протекают с уменьшением внутренней энергии, а в равновесии, когда выполняется равенство, внутренняя энергия достигает минимума.
 I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 2 Независимые переменные и термодинамические потенциалы Для однокомпо- нентной системы в равновесных условиях!!! Ni - число молей в системе; i - химический потенциал 5
I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 2 Независимые переменные и термодинамические потенциалы Для однокомпо- нентной системы в равновесных условиях!!! Ni - число молей в системе; i - химический потенциал 5
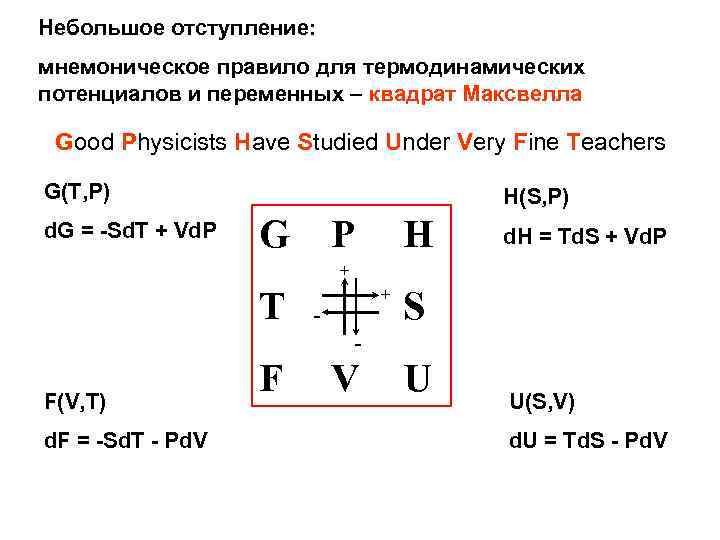 Небольшое отступление: мнемоническое правило для термодинамических потенциалов и переменных – квадрат Максвелла Good Physicists Have Studied Under Very Fine Teachers G(T, P) d. G = -Sd. T + Vd. P H(S, P) G P H d. H = Td. S + Vd. P + T F(V, T) d. F = -Sd. T - Pd. V F + - V S U U(S, V) d. U = Td. S - Pd. V
Небольшое отступление: мнемоническое правило для термодинамических потенциалов и переменных – квадрат Максвелла Good Physicists Have Studied Under Very Fine Teachers G(T, P) d. G = -Sd. T + Vd. P H(S, P) G P H d. H = Td. S + Vd. P + T F(V, T) d. F = -Sd. T - Pd. V F + - V S U U(S, V) d. U = Td. S - Pd. V
 I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 3 Неравенства для неравновесных условий Обобщение на случай многокомпонентных систем Полные дифференциалы В неравновесных условиях Td. S термодинамических потенциалов: Q и I-е начало даёт аналогично В условиях равновесия каждый потенциал имеет экстремум (минимум) при постоянстве термодинамических переменных, от которых он зависит Покажем, например, как получается неравенство для потенциала Гиббса G:
I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 3 Неравенства для неравновесных условий Обобщение на случай многокомпонентных систем Полные дифференциалы В неравновесных условиях Td. S термодинамических потенциалов: Q и I-е начало даёт аналогично В условиях равновесия каждый потенциал имеет экстремум (минимум) при постоянстве термодинамических переменных, от которых он зависит Покажем, например, как получается неравенство для потенциала Гиббса G:
 I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 3 Неравенства для неравновесных условий (продолж. ) Равенство выполняется только в случае равновесия! Тогда при T = const и p = const условие равновесия: i - химический потенциал i-го компонента , т. е. функция Гиббса, приходящаяся на одну частицу или один моль (если хим. потенциал выражен как функция T и p).
I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 3 Неравенства для неравновесных условий (продолж. ) Равенство выполняется только в случае равновесия! Тогда при T = const и p = const условие равновесия: i - химический потенциал i-го компонента , т. е. функция Гиббса, приходящаяся на одну частицу или один моль (если хим. потенциал выражен как функция T и p).
 I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 4 Критерий химического равновесия Для каждой пары постоянных термодинамических переменных в случае равновесия должно быть удовлетворено условие (*) Однако, в каждом случае i будет являться функцией выбранных переменных и, фактически, будут минимизироваться: при S=const, V=const — Внутренняя энергия U(S, V) при S=const, p=const — при V=const, T=const — Свободная энергия Гельмгольца F(V, T) при p=const, T=const Энтальпия H(S, p) — Свободная энтальпия Гиббса G(p, T) Критерий (*) дополняется условием равенства числа атомов каждого из элементов в исходной и конечной смеси
I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 4 Критерий химического равновесия Для каждой пары постоянных термодинамических переменных в случае равновесия должно быть удовлетворено условие (*) Однако, в каждом случае i будет являться функцией выбранных переменных и, фактически, будут минимизироваться: при S=const, V=const — Внутренняя энергия U(S, V) при S=const, p=const — при V=const, T=const — Свободная энергия Гельмгольца F(V, T) при p=const, T=const Энтальпия H(S, p) — Свободная энтальпия Гиббса G(p, T) Критерий (*) дополняется условием равенства числа атомов каждого из элементов в исходной и конечной смеси
 I. 2 Химическое равновесие Реализация расчетов химического равновесия I. Термодинамика процессов горения I. 2. 5 Термодинамические характеристики индивидуальных веществ Таблицы термодинамических свойств: JANAF (Joint-Army-Navy-Air Force) CHEMKIN (TERMDAT) CEA (Chemical Equilibrium with Applications) (THERMO) В таблицах приведены полиномиальные аппроксимации зависимостей от температуры при стандартном давлении (P 0 = 105 Па (1 бар)) следующих параметров: Пределы интегрирования выбраны так, чтобы и стандартная энтальпия образования при p=p 0 стандартная энтропия таблица
I. 2 Химическое равновесие Реализация расчетов химического равновесия I. Термодинамика процессов горения I. 2. 5 Термодинамические характеристики индивидуальных веществ Таблицы термодинамических свойств: JANAF (Joint-Army-Navy-Air Force) CHEMKIN (TERMDAT) CEA (Chemical Equilibrium with Applications) (THERMO) В таблицах приведены полиномиальные аппроксимации зависимостей от температуры при стандартном давлении (P 0 = 105 Па (1 бар)) следующих параметров: Пределы интегрирования выбраны так, чтобы и стандартная энтальпия образования при p=p 0 стандартная энтропия таблица
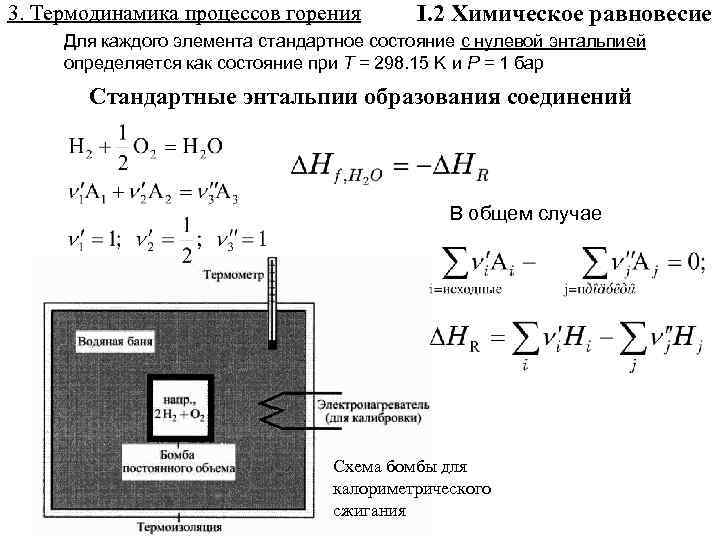 3. Термодинамика процессов горения I. 2 Химическое равновесие Для каждого элемента стандартное состояние с нулевой энтальпией определяется как состояние при T = 298. 15 K и P = 1 бар Стандартные энтальпии образования соединений В общем случае Схема бомбы для калориметрического сжигания
3. Термодинамика процессов горения I. 2 Химическое равновесие Для каждого элемента стандартное состояние с нулевой энтальпией определяется как состояние при T = 298. 15 K и P = 1 бар Стандартные энтальпии образования соединений В общем случае Схема бомбы для калориметрического сжигания
 Пример расчета энтальпии образования Этилен. Определение энтальпии образования по набору реакций (метод Гесса)
Пример расчета энтальпии образования Этилен. Определение энтальпии образования по набору реакций (метод Гесса)
 Программа для расчета термодинамический свойств элементов NASA (http: //www. grc. nasa. gov/WWW/CEAWeb/cea. Home. htm)
Программа для расчета термодинамический свойств элементов NASA (http: //www. grc. nasa. gov/WWW/CEAWeb/cea. Home. htm)

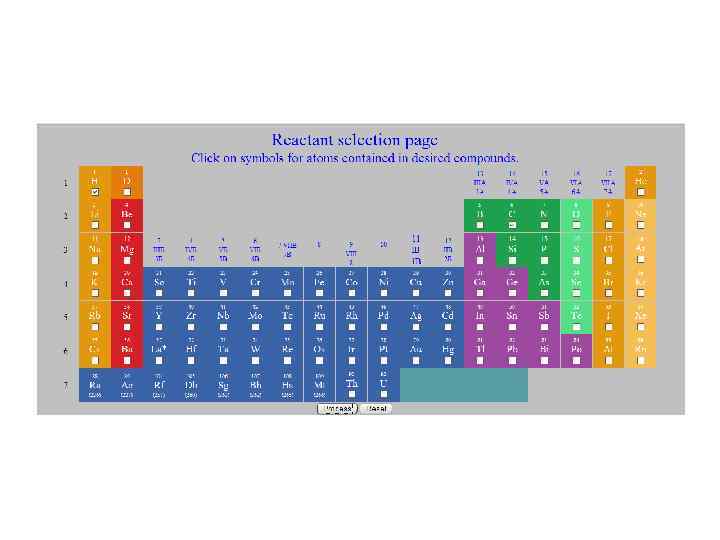
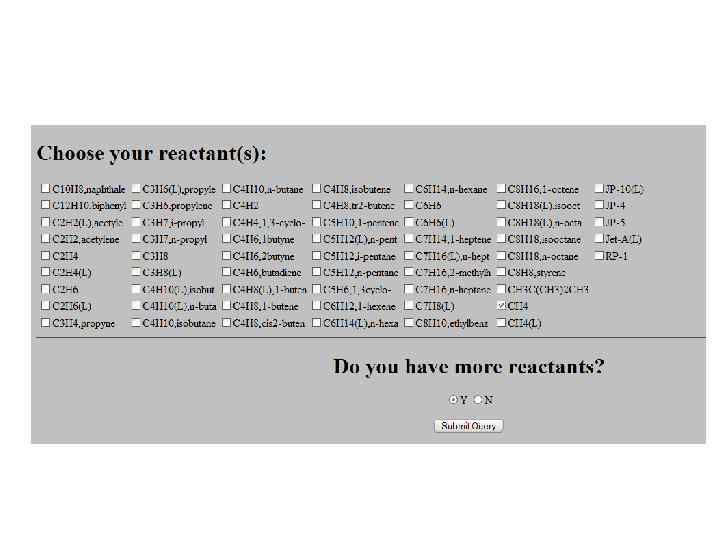

 1. Формат базы термодинамических данных для программы CEA 2. Базы термодинамических данных для программы CEA (Thermo)
1. Формат базы термодинамических данных для программы CEA 2. Базы термодинамических данных для программы CEA (Thermo)
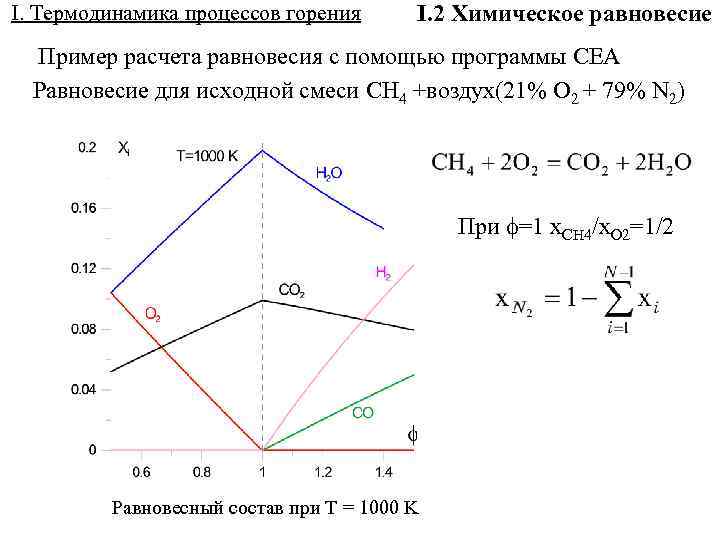 I. Термодинамика процессов горения I. 2 Химическое равновесие Пример расчета равновесия с помощью программы CEA Равновесие для исходной смеси CH 4 +воздух(21% O 2 + 79% N 2) При =1 x. CH 4/x. O 2=1/2 Равновесный состав при T = 1000 K
I. Термодинамика процессов горения I. 2 Химическое равновесие Пример расчета равновесия с помощью программы CEA Равновесие для исходной смеси CH 4 +воздух(21% O 2 + 79% N 2) При =1 x. CH 4/x. O 2=1/2 Равновесный состав при T = 1000 K
 I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 6 Теплота образования, теплота реакции и теплота сгорания Сохранение энергии в химической реакции - энтальпия образования вещества - энтальпия при температуре Т - теплота реакции при температуре T - теплота сгорания – теплота реакции окисления 1 моля топлива кислородом с образованием конечных продуктов H 2 O, CO 2 и N 2 (p = p 0, T = T 0)
I. Термодинамика процессов горения I. 2 Химическое равновесие I. 2. 6 Теплота образования, теплота реакции и теплота сгорания Сохранение энергии в химической реакции - энтальпия образования вещества - энтальпия при температуре Т - теплота реакции при температуре T - теплота сгорания – теплота реакции окисления 1 моля топлива кислородом с образованием конечных продуктов H 2 O, CO 2 и N 2 (p = p 0, T = T 0)
![Formula (gas) Hydrogen Name Qp (kcal/mol) Lower heating value [H 2 O(g)] (cal/g) H Formula (gas) Hydrogen Name Qp (kcal/mol) Lower heating value [H 2 O(g)] (cal/g) H](https://present5.com/presentation/3/14063175_100148847.pdf-img/14063175_100148847.pdf-25.jpg) Formula (gas) Hydrogen Name Qp (kcal/mol) Lower heating value [H 2 O(g)] (cal/g) H 2 57. 80 28672. 3 Methane CH 4 191. 85 11958. 7 Methanol CH 4 O 152. 55 4760. 9 CO 67. 65 2415. 2 Acetylene C 2 H 2 2300. 40 88348. 2 Ethylene C 2 H 4 316. 20 11271. 2 Ethane C 2 H 6 341. 30 11350. 3 Allene C 3 H 4 443. 25 11063. 3 Propyne C 3 H 4 441. 95 11030. 9 Cyclopropane C 3 H 6 468. 25 11127. 4 Propane C 3 H 8 488. 35 11074. 6 1. 3 -Butadiene C 4 H 6 575. 90 10646. 7 n -Butane C 4 H 10 635. 20 10928. 5 n-Pentane C 5 H 12 781. 95 10837. 8 Benzene C 6 H 6 757. 50 9697. 4 Cyclohexane C 6 Hl 2 881. 60 10475. 1 n-Hexane C 6 Hl 4 929. 00 10780. 1 Toluene C 7 H 8 901. 55 9784. 5 n-Heptane C 7 H 16 1075. 85 10736. 6 o-Xylene C 8 H 10 1046. 00 9852. 4 n-Octane C 8 H 18 1222. 70 10703. 8 iso-Octane C 8 H 18 1219. 10 10672. 2 n-Hexadecane C 16 H 34 2397. 80 10588. 8 Carbon Monoxide
Formula (gas) Hydrogen Name Qp (kcal/mol) Lower heating value [H 2 O(g)] (cal/g) H 2 57. 80 28672. 3 Methane CH 4 191. 85 11958. 7 Methanol CH 4 O 152. 55 4760. 9 CO 67. 65 2415. 2 Acetylene C 2 H 2 2300. 40 88348. 2 Ethylene C 2 H 4 316. 20 11271. 2 Ethane C 2 H 6 341. 30 11350. 3 Allene C 3 H 4 443. 25 11063. 3 Propyne C 3 H 4 441. 95 11030. 9 Cyclopropane C 3 H 6 468. 25 11127. 4 Propane C 3 H 8 488. 35 11074. 6 1. 3 -Butadiene C 4 H 6 575. 90 10646. 7 n -Butane C 4 H 10 635. 20 10928. 5 n-Pentane C 5 H 12 781. 95 10837. 8 Benzene C 6 H 6 757. 50 9697. 4 Cyclohexane C 6 Hl 2 881. 60 10475. 1 n-Hexane C 6 Hl 4 929. 00 10780. 1 Toluene C 7 H 8 901. 55 9784. 5 n-Heptane C 7 H 16 1075. 85 10736. 6 o-Xylene C 8 H 10 1046. 00 9852. 4 n-Octane C 8 H 18 1222. 70 10703. 8 iso-Octane C 8 H 18 1219. 10 10672. 2 n-Hexadecane C 16 H 34 2397. 80 10588. 8 Carbon Monoxide
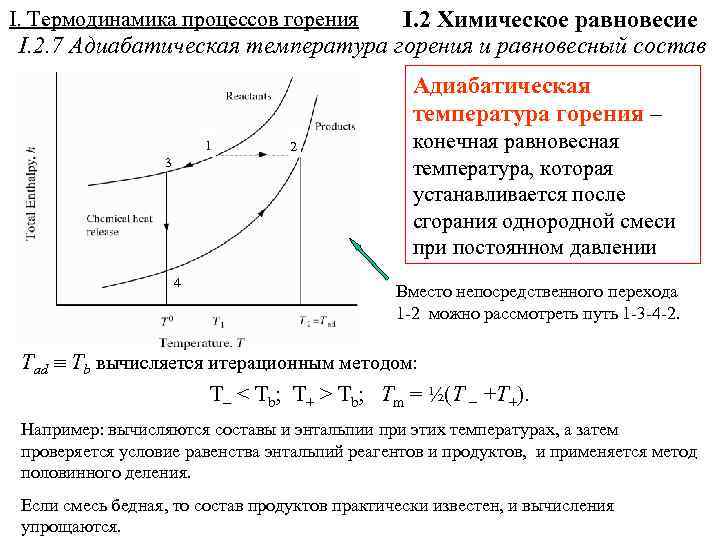 I. 2 Химическое равновесие I. 2. 7 Адиабатическая температура горения и равновесный состав I. Термодинамика процессов горения Адиабатическая температура горения – 1 3 4 2 конечная равновесная температура, которая устанавливается после сгорания однородной смеси при постоянном давлении Вместо непосредственного перехода 1 -2 можно рассмотреть путь 1 -3 -4 -2. Tad Tb вычисляется итерационным методом: T < Tb; T+ > Tb; Tm = ½(T +T+). Например: вычисляются составы и энтальпии при этих температурах, а затем проверяется условие равенства энтальпий реагентов и продуктов, и применяется метод половинного деления. Если смесь бедная, то состав продуктов практически известен, и вычисления упрощаются.
I. 2 Химическое равновесие I. 2. 7 Адиабатическая температура горения и равновесный состав I. Термодинамика процессов горения Адиабатическая температура горения – 1 3 4 2 конечная равновесная температура, которая устанавливается после сгорания однородной смеси при постоянном давлении Вместо непосредственного перехода 1 -2 можно рассмотреть путь 1 -3 -4 -2. Tad Tb вычисляется итерационным методом: T < Tb; T+ > Tb; Tm = ½(T +T+). Например: вычисляются составы и энтальпии при этих температурах, а затем проверяется условие равенства энтальпий реагентов и продуктов, и применяется метод половинного деления. Если смесь бедная, то состав продуктов практически известен, и вычисления упрощаются.
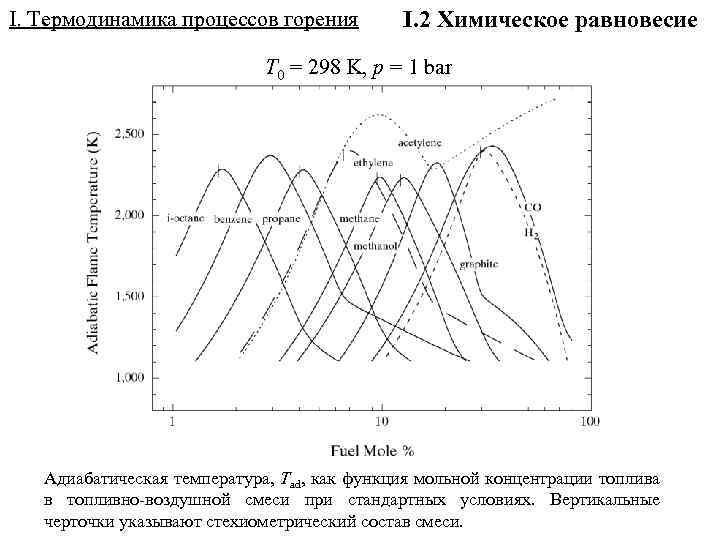 I. Термодинамика процессов горения I. 2 Химическое равновесие T 0 = 298 K, p = 1 bar Адиабатическая температура, Tad, как функция мольной концентрации топлива в топливно-воздушной смеси при стандартных условиях. Вертикальные черточки указывают стехиометрический состав смеси.
I. Термодинамика процессов горения I. 2 Химическое равновесие T 0 = 298 K, p = 1 bar Адиабатическая температура, Tad, как функция мольной концентрации топлива в топливно-воздушной смеси при стандартных условиях. Вертикальные черточки указывают стехиометрический состав смеси.
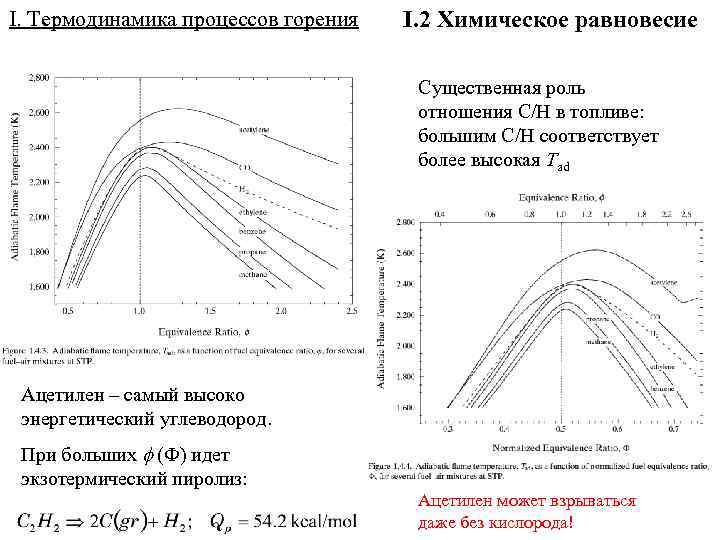 I. Термодинамика процессов горения I. 2 Химическое равновесие Существенная роль отношения C/H в топливе: большим C/H соответствует более высокая Tad Ацетилен – самый высоко энергетический углеводород. При больших (Ф) идет экзотермический пиролиз: Ацетилен может взрываться даже без кислорода!
I. Термодинамика процессов горения I. 2 Химическое равновесие Существенная роль отношения C/H в топливе: большим C/H соответствует более высокая Tad Ацетилен – самый высоко энергетический углеводород. При больших (Ф) идет экзотермический пиролиз: Ацетилен может взрываться даже без кислорода!
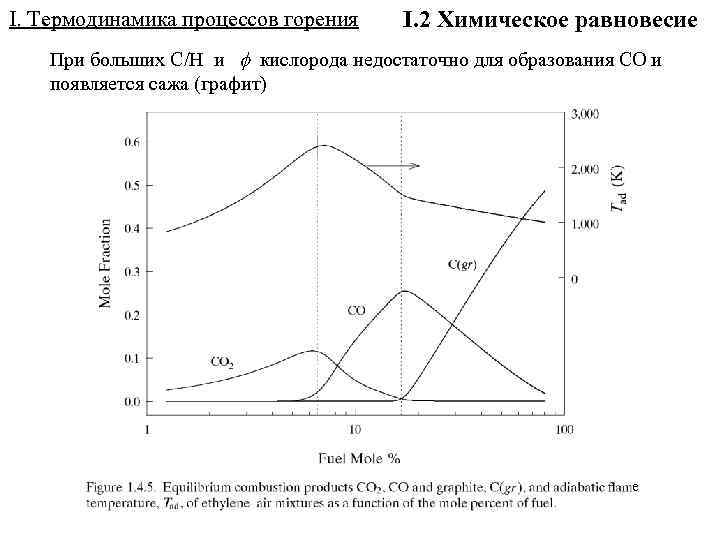 I. Термодинамика процессов горения I. 2 Химическое равновесие При больших C/H и кислорода недостаточно для образования СО и появляется сажа (графит) е
I. Термодинамика процессов горения I. 2 Химическое равновесие При больших C/H и кислорода недостаточно для образования СО и появляется сажа (графит) е
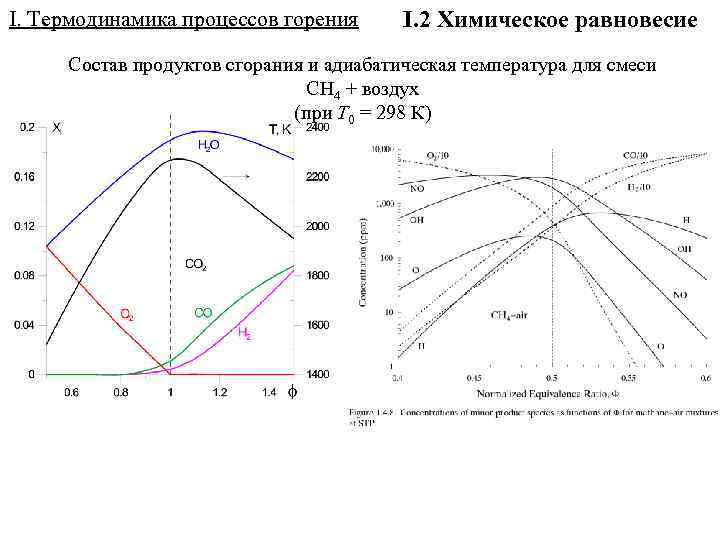 I. Термодинамика процессов горения I. 2 Химическое равновесие Состав продуктов сгорания и адиабатическая температура для смеси CH 4 + воздух (при Т 0 = 298 К)
I. Термодинамика процессов горения I. 2 Химическое равновесие Состав продуктов сгорания и адиабатическая температура для смеси CH 4 + воздух (при Т 0 = 298 К)
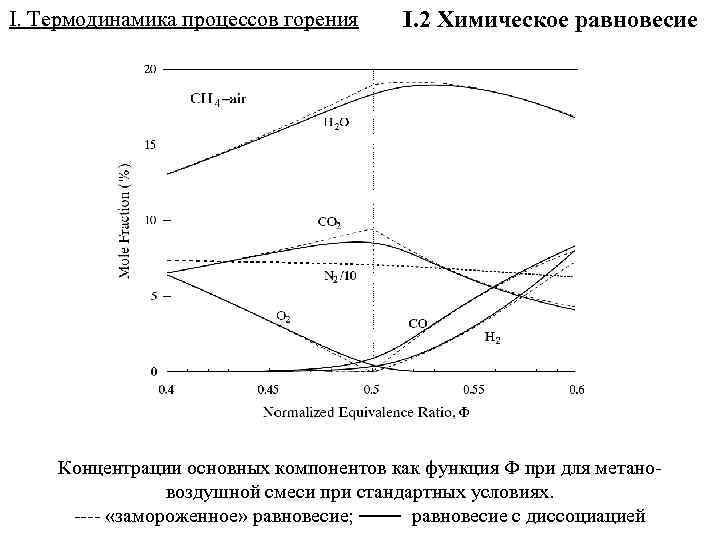 I. Термодинамика процессов горения I. 2 Химическое равновесие Концентрации основных компонентов как функция при для метановоздушной смеси при стандартных условиях. ---- «замороженное» равновесие; ─── равновесие с диссоциацией
I. Термодинамика процессов горения I. 2 Химическое равновесие Концентрации основных компонентов как функция при для метановоздушной смеси при стандартных условиях. ---- «замороженное» равновесие; ─── равновесие с диссоциацией
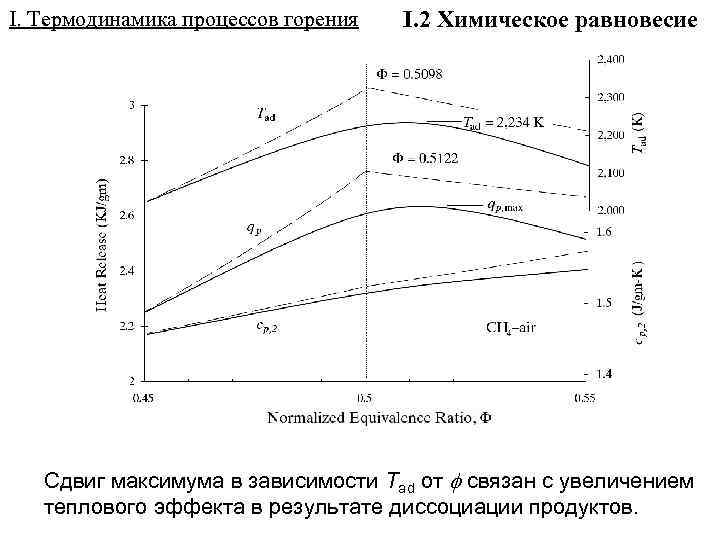 I. Термодинамика процессов горения I. 2 Химическое равновесие Сдвиг максимума в зависимости Tad от связан с увеличением теплового эффекта в результате диссоциации продуктов.
I. Термодинамика процессов горения I. 2 Химическое равновесие Сдвиг максимума в зависимости Tad от связан с увеличением теплового эффекта в результате диссоциации продуктов.
 Ч. II Химическая кинетика процессов горения
Ч. II Химическая кинетика процессов горения
 II. Химическая кинетика горения План лекции 1. Газофазные реакции 2. 1. 1 Элементарные реакции. 3. 1. 2 Молекулярность реакции. Порядок реакции по компонентам и по давлению 4. 1. 3 Теоретические модели скоростей газофазных реакций 5. 6. 1. 4 Типы кинетики газофазных реакций 1. 5 Упрощенные кинетические схемы. Глобальные механизмы. 7. 2. Гетерогенные реакции 2
II. Химическая кинетика горения План лекции 1. Газофазные реакции 2. 1. 1 Элементарные реакции. 3. 1. 2 Молекулярность реакции. Порядок реакции по компонентам и по давлению 4. 1. 3 Теоретические модели скоростей газофазных реакций 5. 6. 1. 4 Типы кинетики газофазных реакций 1. 5 Упрощенные кинетические схемы. Глобальные механизмы. 7. 2. Гетерогенные реакции 2
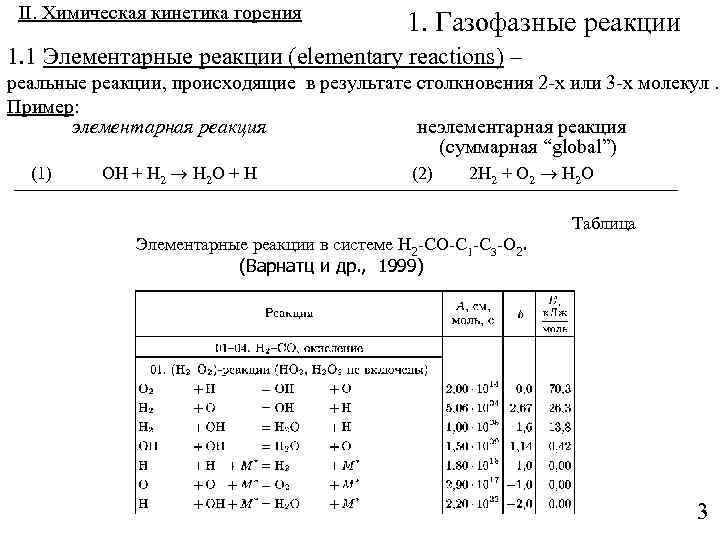 II. Химическая кинетика горения 1. Газофазные реакции 1. 1 Элементарные реакции (elementary reactions) – реальные реакции, происходящие в результате столкновения 2 -х или 3 -х молекул. Пример: элементарная реакция неэлементарная реакция (суммарная “global”) (1) OH + H 2 O + H (2) 2 H 2 + O 2 H 2 O Элементарные реакции в системе Н 2 -СО-С 1 -С 3 -О 2. (Варнатц и др. , 1999) Таблица 3
II. Химическая кинетика горения 1. Газофазные реакции 1. 1 Элементарные реакции (elementary reactions) – реальные реакции, происходящие в результате столкновения 2 -х или 3 -х молекул. Пример: элементарная реакция неэлементарная реакция (суммарная “global”) (1) OH + H 2 O + H (2) 2 H 2 + O 2 H 2 O Элементарные реакции в системе Н 2 -СО-С 1 -С 3 -О 2. (Варнатц и др. , 1999) Таблица 3
 II. Химическая кинетика горения 1. Газофазные реакции Прямая и обратная реакция прямая (forward) реакция обратная (back) реакция Скорость производства (production rate) i-го компонента в прямой реакции Скорость прямой реакции Пример: H + HO 2 → OH + OH Закон действующих масс 4
II. Химическая кинетика горения 1. Газофазные реакции Прямая и обратная реакция прямая (forward) реакция обратная (back) реакция Скорость производства (production rate) i-го компонента в прямой реакции Скорость прямой реакции Пример: H + HO 2 → OH + OH Закон действующих масс 4
 II. Химическая кинетика горения 1. Газофазные реакции 1. 2 Молекулярность реакции и порядок (molecularity and order) Молекулярность элементарной реакции по i-му компоненту - количество молекул компонента, вступающих в реакцию. Общая молекулярность элементарной реакции Порядок реакции ni характеризует зависимость скорости реакции от концентрации i-го компонента. Аналогично, общий порядок реакции – сумма порядков по компонентам. Для элементарных реакций понятия молекулярности и порядка совпадают. В общем случае, порядок реакции, определяемый экспериментально, может быть дробной величиной. Пример (горение этана): Для некоторых реакций (см. далее) порядок реакции может зависеть от давления. Порядок реакции может также меняться при изменении соотношения между концентрациями реагентов – если все реагенты, кроме одного, находятся в избытке, то порядок реакции будет определяться порядком по недостающему реагенту. Когда же влияние концентраций всех реагентов существенно, то общий порядок реакции складывается из порядков по отдельным компонентам. 5
II. Химическая кинетика горения 1. Газофазные реакции 1. 2 Молекулярность реакции и порядок (molecularity and order) Молекулярность элементарной реакции по i-му компоненту - количество молекул компонента, вступающих в реакцию. Общая молекулярность элементарной реакции Порядок реакции ni характеризует зависимость скорости реакции от концентрации i-го компонента. Аналогично, общий порядок реакции – сумма порядков по компонентам. Для элементарных реакций понятия молекулярности и порядка совпадают. В общем случае, порядок реакции, определяемый экспериментально, может быть дробной величиной. Пример (горение этана): Для некоторых реакций (см. далее) порядок реакции может зависеть от давления. Порядок реакции может также меняться при изменении соотношения между концентрациями реагентов – если все реагенты, кроме одного, находятся в избытке, то порядок реакции будет определяться порядком по недостающему реагенту. Когда же влияние концентраций всех реагентов существенно, то общий порядок реакции складывается из порядков по отдельным компонентам. 5
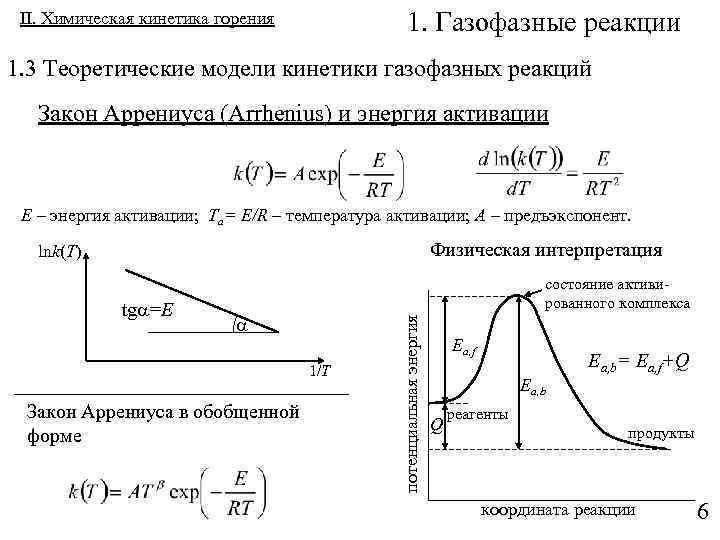 1. Газофазные реакции II. Химическая кинетика горения 1. 3 Теоретические модели кинетики газофазных реакций Закон Аррениуса (Arrhenius) и энергия активации E – энергия активации; Ta= E/R – температура активации; A – предъэкспонент. Физическая интерпретация lnk(T) 1/T Закон Аррениуса в обобщенной форме потенциальная энергия tg =E состояние активированного комплекса Ea, f Ea, b= Ea, f+Q Ea, b Q реагенты продукты координата реакции 6
1. Газофазные реакции II. Химическая кинетика горения 1. 3 Теоретические модели кинетики газофазных реакций Закон Аррениуса (Arrhenius) и энергия активации E – энергия активации; Ta= E/R – температура активации; A – предъэкспонент. Физическая интерпретация lnk(T) 1/T Закон Аррениуса в обобщенной форме потенциальная энергия tg =E состояние активированного комплекса Ea, f Ea, b= Ea, f+Q Ea, b Q реагенты продукты координата реакции 6
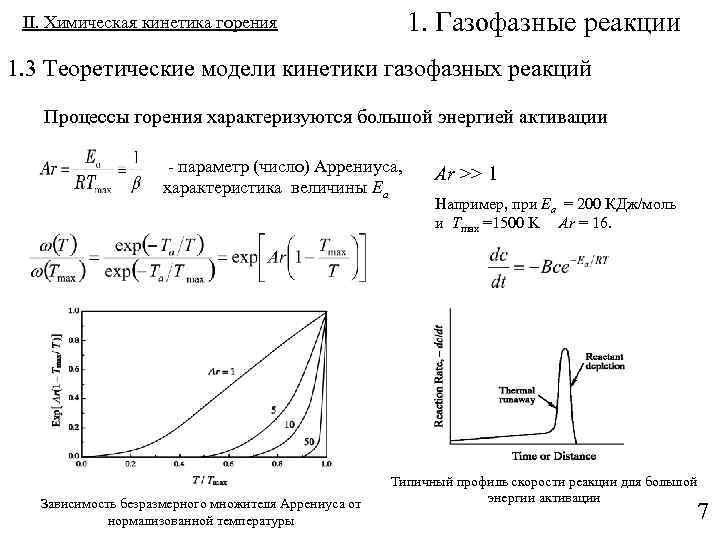 1. Газофазные реакции II. Химическая кинетика горения 1. 3 Теоретические модели кинетики газофазных реакций Процессы горения характеризуются большой энергией активации - параметр (число) Аррениуса, характеристика величины Ea Зависимость безразмерного множителя Аррениуса от нормализованной температуры Ar >> 1 Например, при Ea = 200 КДж/моль и Tmax =1500 K Ar = 16. Типичный профиль скорости реакции для большой энергии активации 7
1. Газофазные реакции II. Химическая кинетика горения 1. 3 Теоретические модели кинетики газофазных реакций Процессы горения характеризуются большой энергией активации - параметр (число) Аррениуса, характеристика величины Ea Зависимость безразмерного множителя Аррениуса от нормализованной температуры Ar >> 1 Например, при Ea = 200 КДж/моль и Tmax =1500 K Ar = 16. Типичный профиль скорости реакции для большой энергии активации 7
 1. Газофазные реакции II. Химическая кинетика горения Соотношение между скоростями прямой и обратной реакций Если известна скорость прямой реакции kf, то скорость обратной можно найти, используя константу равновесия Kp. Из определения скорости реакции (на слайде 4) следует, что в равновесии т. е. Таким образом Напомним, что где и 8
1. Газофазные реакции II. Химическая кинетика горения Соотношение между скоростями прямой и обратной реакций Если известна скорость прямой реакции kf, то скорость обратной можно найти, используя константу равновесия Kp. Из определения скорости реакции (на слайде 4) следует, что в равновесии т. е. Таким образом Напомним, что где и 8
 II. Химическая кинетика горения 1. Газофазные реакции Модели для вычисления константы скорости реакции Детальный вывод скорости реакции с учетом тройных столкновений – Фаулер, Гугенхейм, 1939 Бимолекулярные реакции. Теория столкновений (collision theory) Важна кинетич. энергия, относящаяся только к встречному движению молекул. Средняя относительная скорость Число столкновений Число молекул, имеющих необходимую энергию Ea Схематическое изображение столкновительного объема, «заметаемого» молекулами диаметрами i и j с относительной скоростью Vij Отсюда получаем скорость реакции: Однако, теория столкновений не всегда дает даже приблизительное совпадение с экспериментом. Иногда скорость реакции оказывается на несколько порядков меньше. 9
II. Химическая кинетика горения 1. Газофазные реакции Модели для вычисления константы скорости реакции Детальный вывод скорости реакции с учетом тройных столкновений – Фаулер, Гугенхейм, 1939 Бимолекулярные реакции. Теория столкновений (collision theory) Важна кинетич. энергия, относящаяся только к встречному движению молекул. Средняя относительная скорость Число столкновений Число молекул, имеющих необходимую энергию Ea Схематическое изображение столкновительного объема, «заметаемого» молекулами диаметрами i и j с относительной скоростью Vij Отсюда получаем скорость реакции: Однако, теория столкновений не всегда дает даже приблизительное совпадение с экспериментом. Иногда скорость реакции оказывается на несколько порядков меньше. 9
 II. Химическая кинетика горения 1. Газофазные реакции Модели для вычисления константы скорости реакции Теория переходного состояния (transition state theory) 1. В результате столкновения молекул с кинетической энергией > Ea образуется активированный (возбужденный) комплекс (АК). Оказываются возбужденными колебательные степени свободы. 2. АК может либо вновь распасться на исходные молекулы, либо распасться на продукты реакции. 3. Скорость (частота) распадов АК на продукты может быть оценена на основе квантовых представлений (Епост. Евр, , распад в течение неск. вибраций): Теория переходного состояния дает следующие выражения для константы скорости реакции: n – общий порядок реакции; - стерический фактор определяется энтропией образования АК. Расчеты в предположении, что энтропия АК приблизительно равна энтропии продуктов реакции, дают хорошее совпадение с экспериментом. Константа скорости бимолекулярной реакции не зависит от давления 10
II. Химическая кинетика горения 1. Газофазные реакции Модели для вычисления константы скорости реакции Теория переходного состояния (transition state theory) 1. В результате столкновения молекул с кинетической энергией > Ea образуется активированный (возбужденный) комплекс (АК). Оказываются возбужденными колебательные степени свободы. 2. АК может либо вновь распасться на исходные молекулы, либо распасться на продукты реакции. 3. Скорость (частота) распадов АК на продукты может быть оценена на основе квантовых представлений (Епост. Евр, , распад в течение неск. вибраций): Теория переходного состояния дает следующие выражения для константы скорости реакции: n – общий порядок реакции; - стерический фактор определяется энтропией образования АК. Расчеты в предположении, что энтропия АК приблизительно равна энтропии продуктов реакции, дают хорошее совпадение с экспериментом. Константа скорости бимолекулярной реакции не зависит от давления 10
 1. Газофазные реакции II. Химическая кинетика горения 1. 4 Другие типы кинетики газофазных реакций. Реакции, зависящие от давления Два типа таких реакций – а) мономолекулярный распад (диссиоциация)/ тримолекулярная рекомбинация; б) активированные бимолекулярные реакции. Мономолекулярный распад / тримолекулярная рекомбинация Unimolecular / Recombination Fall-off Reactions В этом случае для осуществления реакции необходимо присутствие дополнительно, «третей» молекулы ( приносящей избыток энергии для распада или уносящей его при рекомбинации). СH 4 + M CH 3 + H + M или HO 2 + M H + O 2 + M С 2 H 6 + M CH 3 + M 11
1. Газофазные реакции II. Химическая кинетика горения 1. 4 Другие типы кинетики газофазных реакций. Реакции, зависящие от давления Два типа таких реакций – а) мономолекулярный распад (диссиоциация)/ тримолекулярная рекомбинация; б) активированные бимолекулярные реакции. Мономолекулярный распад / тримолекулярная рекомбинация Unimolecular / Recombination Fall-off Reactions В этом случае для осуществления реакции необходимо присутствие дополнительно, «третей» молекулы ( приносящей избыток энергии для распада или уносящей его при рекомбинации). СH 4 + M CH 3 + H + M или HO 2 + M H + O 2 + M С 2 H 6 + M CH 3 + M 11
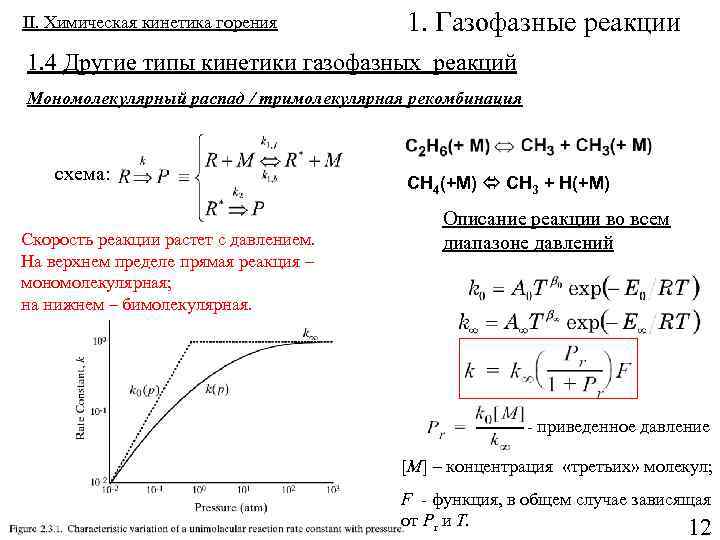 II. Химическая кинетика горения 1. Газофазные реакции 1. 4 Другие типы кинетики газофазных реакций Мономолекулярный распад / тримолекулярная рекомбинация схема: Скорость реакции растет с давлением. На верхнем пределе прямая реакция – мономолекулярная; на нижнем – бимолекулярная. CH 4(+M) CH 3 + H(+M) Описание реакции во всем диапазоне давлений - приведенное давление [M] – концентрация «третьих» молекул; F - функция, в общем случае зависящая от Pr и T. 12
II. Химическая кинетика горения 1. Газофазные реакции 1. 4 Другие типы кинетики газофазных реакций Мономолекулярный распад / тримолекулярная рекомбинация схема: Скорость реакции растет с давлением. На верхнем пределе прямая реакция – мономолекулярная; на нижнем – бимолекулярная. CH 4(+M) CH 3 + H(+M) Описание реакции во всем диапазоне давлений - приведенное давление [M] – концентрация «третьих» молекул; F - функция, в общем случае зависящая от Pr и T. 12
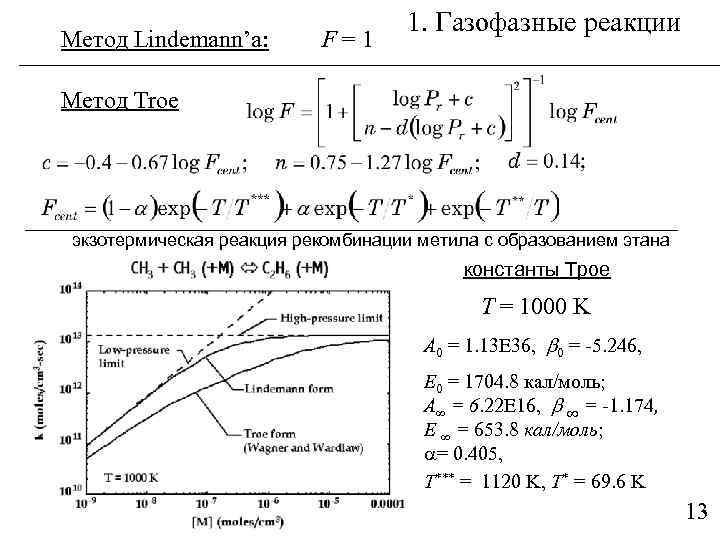 Метод Lindemann’а: F=1 1. Газофазные реакции Метод Troe экзотермическая реакция рекомбинации метила с образованием этана константы Трое T = 1000 K A 0 = 1. 13 E 36, 0 = -5. 246, E 0 = 1704. 8 кал/моль; A∞ = 6. 22 E 16, ∞ = -1. 174, E ∞ = 653. 8 кал/моль; = 0. 405, T*** = 1120 K, T* = 69. 6 K 13
Метод Lindemann’а: F=1 1. Газофазные реакции Метод Troe экзотермическая реакция рекомбинации метила с образованием этана константы Трое T = 1000 K A 0 = 1. 13 E 36, 0 = -5. 246, E 0 = 1704. 8 кал/моль; A∞ = 6. 22 E 16, ∞ = -1. 174, E ∞ = 653. 8 кал/моль; = 0. 405, T*** = 1120 K, T* = 69. 6 K 13
 II. Химическая кинетика горения 1. Газофазные реакции 1. 4 Другие типы кинетики газофазных реакций. Реакции, зависящие от давления Химически активируемые бимолекулярные реакции эндотермическая реакция рекомбинации метила с образованием этила горячий комплекс Диаграмма «энергия – координата реакции» . Конкуренция между химически активируемой тримолекулярной рекомбинацией CH 3 + M C 2 H 6 + M и химически активируемой бимолекулярной реакцией CH 3 + М C 2 H 5 +H + М этил Скорость реакции убывает с ростом давления этан 14
II. Химическая кинетика горения 1. Газофазные реакции 1. 4 Другие типы кинетики газофазных реакций. Реакции, зависящие от давления Химически активируемые бимолекулярные реакции эндотермическая реакция рекомбинации метила с образованием этила горячий комплекс Диаграмма «энергия – координата реакции» . Конкуренция между химически активируемой тримолекулярной рекомбинацией CH 3 + M C 2 H 6 + M и химически активируемой бимолекулярной реакцией CH 3 + М C 2 H 5 +H + М этил Скорость реакции убывает с ростом давления этан 14
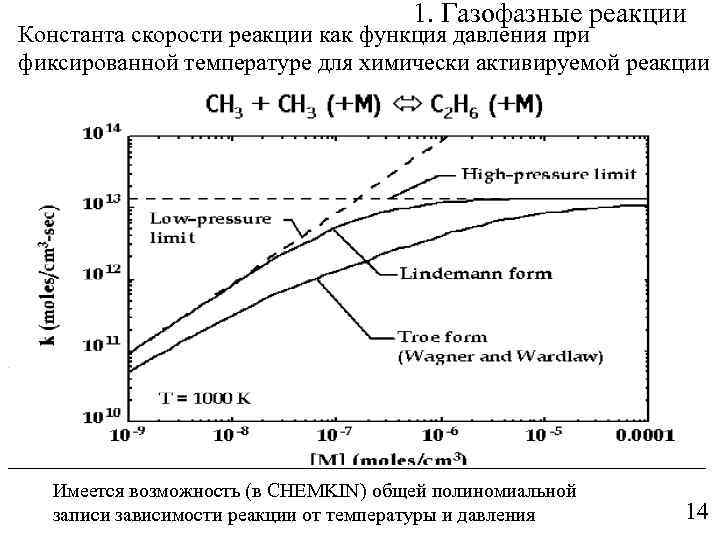 1. Газофазные реакции Константа скорости реакции как функция давления при фиксированной температуре для химически активируемой реакции Метод SRI Имеется возможность (в CHEMKIN) общей полиномиальной записи зависимости реакции от температуры и давления 14
1. Газофазные реакции Константа скорости реакции как функция давления при фиксированной температуре для химически активируемой реакции Метод SRI Имеется возможность (в CHEMKIN) общей полиномиальной записи зависимости реакции от температуры и давления 14
 1. Газофазные реакции 1. 4 Другие типы кинетики газофазных реакций Реакции с переносом колебательной энергии. Формулировка Ландау-Теллера - Ландау-Теллер - обобщенная форма 15
1. Газофазные реакции 1. 4 Другие типы кинетики газофазных реакций Реакции с переносом колебательной энергии. Формулировка Ландау-Теллера - Ландау-Теллер - обобщенная форма 15
 II. Химическая кинетика горения 1. Газофазные реакции 1. 4 Другие типы кинетики газофазных реакций Цепные реакции – реакции, протекающие с образованием промежуточных активных частиц (радикалов) Метод стационарных концентраций Неразветвленные цепные реакции (Straight-Chain Reactions) H 2+Cl 2 2 HCl - медленная реакция, в реальности не идет. Еa 170 КДж/моль Реакция зарождения (обрыва) цепи Cl 2 + M Cl + M (k 1 f, k 1 b) Реакции продолжения цепей Cl + H 2 HCl + H (k 2) быстрая реакция, Еa 20 КДж/моль H + Cl 2 HCl + Cl (k 3) самая быстрая реакция константа равновесия реакции 2 Cl Cl 2 Время реакции при P = 1 атм и T = 600 K составляет около 1 с. Другой пример неразветвленной цепной реакции – окисление азота. 16
II. Химическая кинетика горения 1. Газофазные реакции 1. 4 Другие типы кинетики газофазных реакций Цепные реакции – реакции, протекающие с образованием промежуточных активных частиц (радикалов) Метод стационарных концентраций Неразветвленные цепные реакции (Straight-Chain Reactions) H 2+Cl 2 2 HCl - медленная реакция, в реальности не идет. Еa 170 КДж/моль Реакция зарождения (обрыва) цепи Cl 2 + M Cl + M (k 1 f, k 1 b) Реакции продолжения цепей Cl + H 2 HCl + H (k 2) быстрая реакция, Еa 20 КДж/моль H + Cl 2 HCl + Cl (k 3) самая быстрая реакция константа равновесия реакции 2 Cl Cl 2 Время реакции при P = 1 атм и T = 600 K составляет около 1 с. Другой пример неразветвленной цепной реакции – окисление азота. 16
 II. Химическая кинетика горения 1. Газофазные реакции Разветвленные цепные реакции I – скорость инициирования цепи Сумма свободных радикалов (атомы кислорода учитываются дважды): 17
II. Химическая кинетика горения 1. Газофазные реакции Разветвленные цепные реакции I – скорость инициирования цепи Сумма свободных радикалов (атомы кислорода учитываются дважды): 17
 II. Химическая кинетика горения 1. Газофазные реакции Разветвленные цепные реакции P цепной взрыв T
II. Химическая кинетика горения 1. Газофазные реакции Разветвленные цепные реакции P цепной взрыв T
 II. Химическая кинетика горения 1. Газофазные реакции 1. 5 Упрощенные кинетические схемы. Анализ чувствительности. Глобальные механизмы. 1. Общий механизм горения углеводородов GRI-mech 3. 0 2. 53 химических компонента, 325 реакций 3. Необходимо решение «жестких» систем ОДУ (метод Гира и т. п. ) 4. 2. Механизм Коннова 5. 6. 7. 127 химических компонентов, 1200 реакций 3. Упрощенные механизмы 22, 19 компонентов 11, 6, 5 реакций 8. 4. Глобальная (брутто) реакция первого порядка по метану (с избытком кислорода) CH 4 + 2 O 2 CO 2 + 2 H 2 O k=2, 62 108 1/с, E=130 к. Дж/моль, Q=4, 387 104 к. Дж/кг GRI-mech 3. 0 Konnov’s mrchanizm Flatcher_H_O 18
II. Химическая кинетика горения 1. Газофазные реакции 1. 5 Упрощенные кинетические схемы. Анализ чувствительности. Глобальные механизмы. 1. Общий механизм горения углеводородов GRI-mech 3. 0 2. 53 химических компонента, 325 реакций 3. Необходимо решение «жестких» систем ОДУ (метод Гира и т. п. ) 4. 2. Механизм Коннова 5. 6. 7. 127 химических компонентов, 1200 реакций 3. Упрощенные механизмы 22, 19 компонентов 11, 6, 5 реакций 8. 4. Глобальная (брутто) реакция первого порядка по метану (с избытком кислорода) CH 4 + 2 O 2 CO 2 + 2 H 2 O k=2, 62 108 1/с, E=130 к. Дж/моль, Q=4, 387 104 к. Дж/кг GRI-mech 3. 0 Konnov’s mrchanizm Flatcher_H_O 18
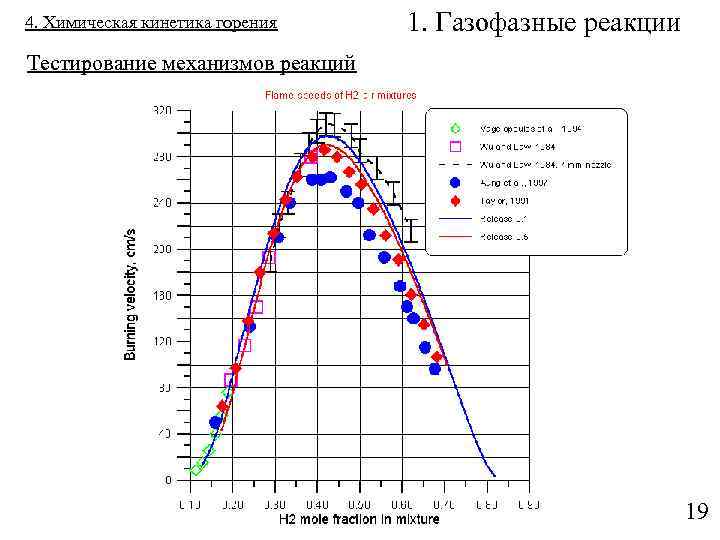 4. Химическая кинетика горения 1. Газофазные реакции Тестирование механизмов реакций Tests of the mechanism 19
4. Химическая кинетика горения 1. Газофазные реакции Тестирование механизмов реакций Tests of the mechanism 19
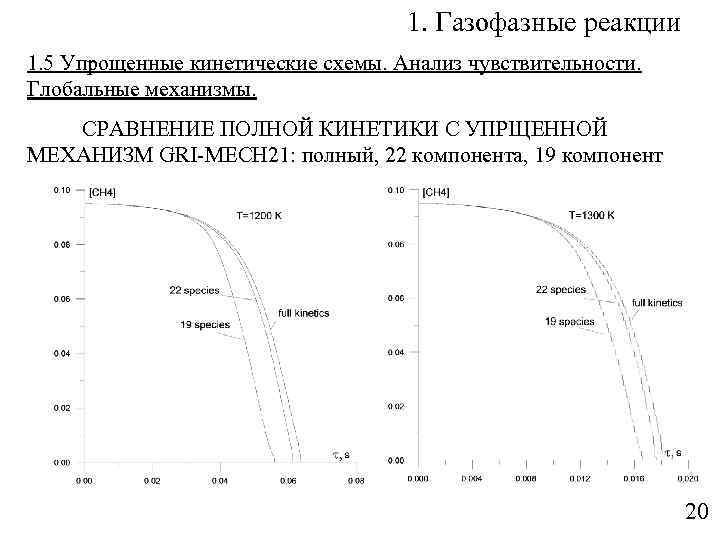 1. Газофазные реакции 1. 5 Упрощенные кинетические схемы. Анализ чувствительности. Глобальные механизмы. СРАВНЕНИЕ ПОЛНОЙ КИНЕТИКИ С УПРЩЕННОЙ МЕХАНИЗМ GRI-MECH 21: полный, 22 компонента, 19 компонент 20
1. Газофазные реакции 1. 5 Упрощенные кинетические схемы. Анализ чувствительности. Глобальные механизмы. СРАВНЕНИЕ ПОЛНОЙ КИНЕТИКИ С УПРЩЕННОЙ МЕХАНИЗМ GRI-MECH 21: полный, 22 компонента, 19 компонент 20
 4. Химическая кинетика горения 2. Гетерогенные реакции Реакции газообразных реагентов с конденсированной фазой Основной новый элемент - поверхностные активные центры и частицы, адсорбированные на этих центрах 21
4. Химическая кинетика горения 2. Гетерогенные реакции Реакции газообразных реагентов с конденсированной фазой Основной новый элемент - поверхностные активные центры и частицы, адсорбированные на этих центрах 21
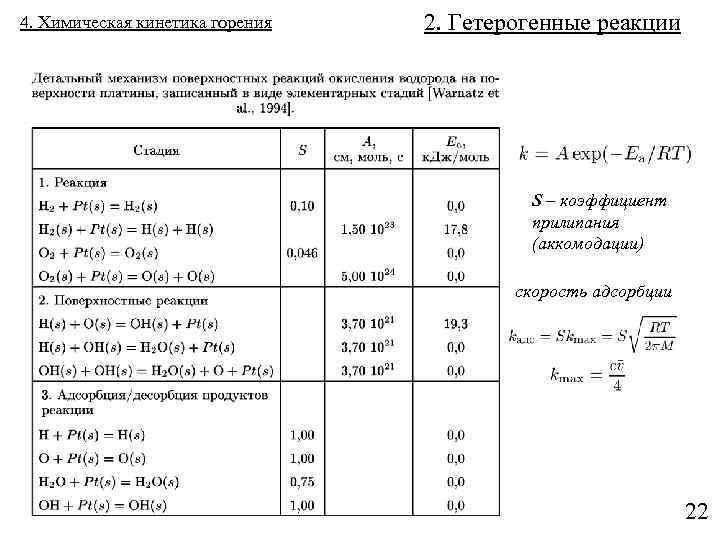 4. Химическая кинетика горения 2. Гетерогенные реакции S – коэффициент прилипания (аккомодации) скорость адсорбции 22
4. Химическая кинетика горения 2. Гетерогенные реакции S – коэффициент прилипания (аккомодации) скорость адсорбции 22
 4. Химическая кинетика горения 2. Гетерогенные реакции Феноменологическая кинетика реакций в конденсированной фазе N 2 Степень конверсии Кинетический закон Ti Диффузия через слой продукта Виды функций торможения СВС нитрида титана 23
4. Химическая кинетика горения 2. Гетерогенные реакции Феноменологическая кинетика реакций в конденсированной фазе N 2 Степень конверсии Кинетический закон Ti Диффузия через слой продукта Виды функций торможения СВС нитрида титана 23
 Моделирование кинетических процессов с помощью пакет CHEMKIN 24
Моделирование кинетических процессов с помощью пакет CHEMKIN 24
 4. Химическая кинетика горения Заключение • Данные по микрокинетики горения и кинетические расчеты дают ценнейшую информацию о процессе • Однако ни термодинамика, ни микрокинетика не определяют в полной мере ход процесса • Третьей принципиальной составляющей явлений горения является макрокинетика – процессы переноса энергии и вещества. 25
4. Химическая кинетика горения Заключение • Данные по микрокинетики горения и кинетические расчеты дают ценнейшую информацию о процессе • Однако ни термодинамика, ни микрокинетика не определяют в полной мере ход процесса • Третьей принципиальной составляющей явлений горения является макрокинетика – процессы переноса энергии и вещества. 25
 Спасибо за внимание!
Спасибо за внимание!


