5_Lect_2013_09_13_atomic spectra.ppt
- Количество слайдов: 26
 Физическое материаловедение Спектры атомов
Физическое материаловедение Спектры атомов
 Атомные спектры, получающиеся при испускании или поглощении света (электромагнитных волн) свободными или слабо связанными атомами; такими спектрами обладают, в частности, одноатомные газы и пары. Атомные спектры являются линейчатыми — они состоят из отдельных спектральных линий и наблюдаются в виде ярких цветных линий при свечении газов или паров в электрической дуге или разряде (спектры испускания) и в виде тёмных линий (спектров поглощения). Каждая спектральная линия характеризуется определённой частотой колебаний v испускаемого или поглощаемого света и соответствует определённому квантовому переходу между уровнями энергии Ei и Ek атома согласно соотношению: hv = Ei - Ek, где h — постоянная Планка).
Атомные спектры, получающиеся при испускании или поглощении света (электромагнитных волн) свободными или слабо связанными атомами; такими спектрами обладают, в частности, одноатомные газы и пары. Атомные спектры являются линейчатыми — они состоят из отдельных спектральных линий и наблюдаются в виде ярких цветных линий при свечении газов или паров в электрической дуге или разряде (спектры испускания) и в виде тёмных линий (спектров поглощения). Каждая спектральная линия характеризуется определённой частотой колебаний v испускаемого или поглощаемого света и соответствует определённому квантовому переходу между уровнями энергии Ei и Ek атома согласно соотношению: hv = Ei - Ek, где h — постоянная Планка).
 Примеры спектров излучения атомов He Ne Kr Xe
Примеры спектров излучения атомов He Ne Kr Xe
 Hg C N O Si Ca
Hg C N O Si Ca
 Атомные спектры дают как нейтральные, так и ионизованные атомы; их часто называют соответственно дуговыми и искровыми спектрами (нейтральные атомы легко возбуждаются и дают спектры испускания в электрических дугах, а положительные ионы возбуждаются труднее и дают спектры испускания преимущественно в искровых электрических разрядах). Спектры ионизованных атомов смещены по отношению к спектрам нейтральных атомов в область больших частот, т. е. в ультрафиолетовую область. Это смещение тем больше, чем выше кратность ионизации атома — чем больше электронов он потерял. Спектры нейтрального атома и его последовательных ионов обозначают в спектроскопии цифрами I, III, . . . В реально наблюдаемых спектрах часто присутствуют одновременно линии нейтрального и ионизованных атомов; так говорят, например, о линиях Fe. I, Fe. III в спектре железа, соответствующих Fe, Fe+, Fe 2+.
Атомные спектры дают как нейтральные, так и ионизованные атомы; их часто называют соответственно дуговыми и искровыми спектрами (нейтральные атомы легко возбуждаются и дают спектры испускания в электрических дугах, а положительные ионы возбуждаются труднее и дают спектры испускания преимущественно в искровых электрических разрядах). Спектры ионизованных атомов смещены по отношению к спектрам нейтральных атомов в область больших частот, т. е. в ультрафиолетовую область. Это смещение тем больше, чем выше кратность ионизации атома — чем больше электронов он потерял. Спектры нейтрального атома и его последовательных ионов обозначают в спектроскопии цифрами I, III, . . . В реально наблюдаемых спектрах часто присутствуют одновременно линии нейтрального и ионизованных атомов; так говорят, например, о линиях Fe. I, Fe. III в спектре железа, соответствующих Fe, Fe+, Fe 2+.
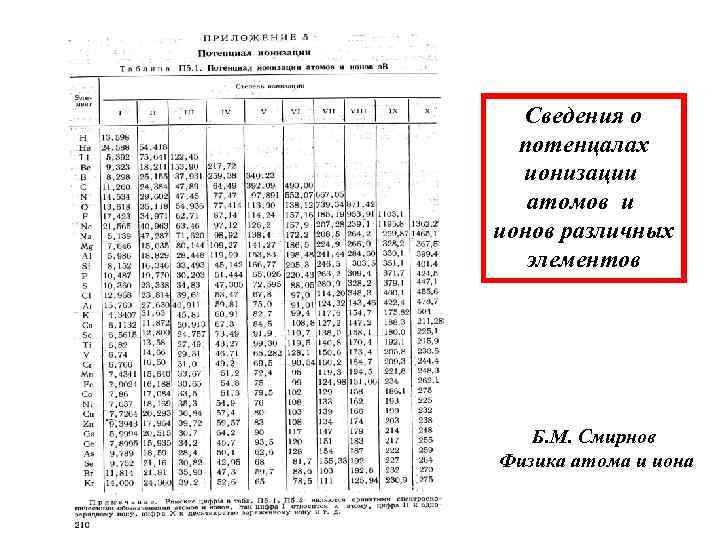 Сведения о потенцалах ионизации атомов и ионов различных элементов Б. М. Смирнов Физика атома и иона
Сведения о потенцалах ионизации атомов и ионов различных элементов Б. М. Смирнов Физика атома и иона
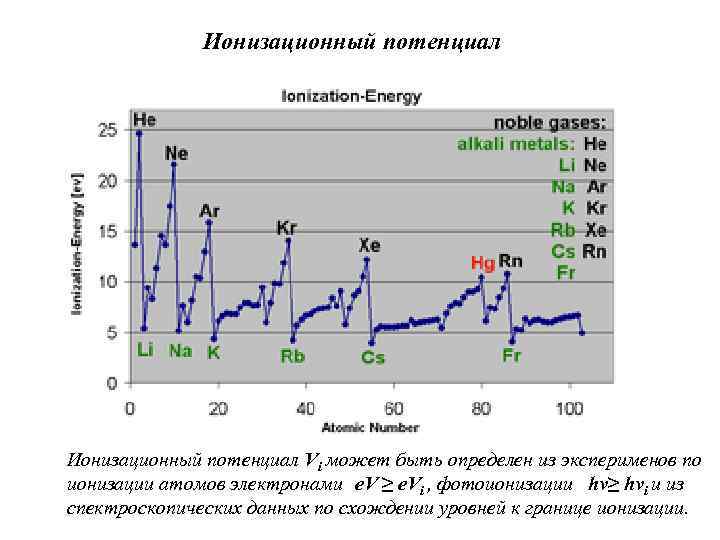 Ионизационный потенциал Vi может быть определен из эксперименов по ионизации атомов электронами e. V ≥ e. Vi , фотоионизации hν≥ hνi и из спектроскопических данных по схождении уровней к границе ионизации.
Ионизационный потенциал Vi может быть определен из эксперименов по ионизации атомов электронами e. V ≥ e. Vi , фотоионизации hν≥ hνi и из спектроскопических данных по схождении уровней к границе ионизации.
 Изоэлектронные ряды Периодичность химических, оптических, электрических и магнитных свойств атомов различных элементов в зависимости от Z связана со сходным строением внешних электронных оболочек, определяющим эти свойства. Эта периодичность сохраняется и для ионов: теряя один электрон, атом становится подобен по ряду свойств атомам предыдущей группы элементов (например, однократно ионизованные щелочноземельные атомы - атомам щелочных металлов). Сходными свойствами обладают члены изоэлектронного ряда.
Изоэлектронные ряды Периодичность химических, оптических, электрических и магнитных свойств атомов различных элементов в зависимости от Z связана со сходным строением внешних электронных оболочек, определяющим эти свойства. Эта периодичность сохраняется и для ионов: теряя один электрон, атом становится подобен по ряду свойств атомам предыдущей группы элементов (например, однократно ионизованные щелочноземельные атомы - атомам щелочных металлов). Сходными свойствами обладают члены изоэлектронного ряда.
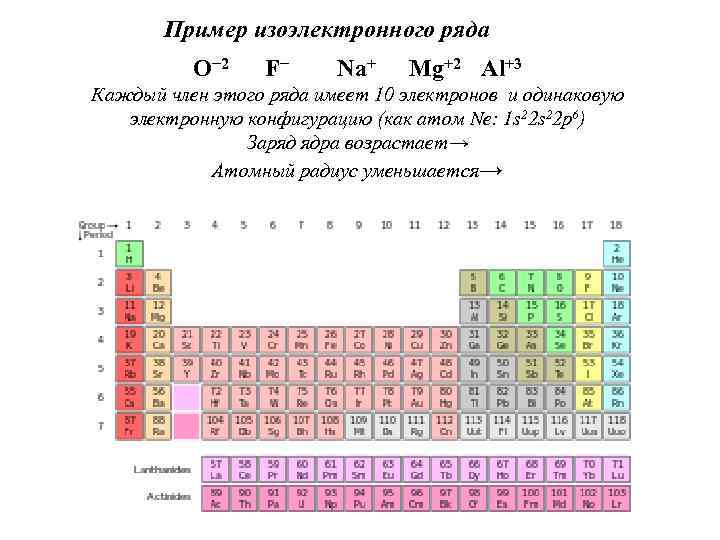 Пример изоэлектронного ряда O− 2 F− Na+ Mg+2 Al+3 Каждый член этого ряда имеет 10 электронов и одинаковую электронную конфигурацию (как атом Ne: 1 s 22 p 6) Заряд ядра возрастает→ Атомный радиус уменьшается→
Пример изоэлектронного ряда O− 2 F− Na+ Mg+2 Al+3 Каждый член этого ряда имеет 10 электронов и одинаковую электронную конфигурацию (как атом Ne: 1 s 22 p 6) Заряд ядра возрастает→ Атомный радиус уменьшается→
 Уровни энергии и переходы: одноэлектронный атом H, He+, Li++ Постулаты Бора: Нобелевская премия 1922 г. • Движущийся вокруг ядра электрон излучает энергию только при переходе системы между стационарными состояниями. • Динамическое равновесие системы в стационарных состояниях подчиняется обычным законам механики, тогда как для описания переходов они неприменимы. • Излучение, испускаемое при переходах системы из одного стационарного состояния в другое, монохроматично. E = h
Уровни энергии и переходы: одноэлектронный атом H, He+, Li++ Постулаты Бора: Нобелевская премия 1922 г. • Движущийся вокруг ядра электрон излучает энергию только при переходе системы между стационарными состояниями. • Динамическое равновесие системы в стационарных состояниях подчиняется обычным законам механики, тогда как для описания переходов они неприменимы. • Излучение, испускаемое при переходах системы из одного стационарного состояния в другое, монохроматично. E = h
 Оценка энергии электрона Электрон движется по круговой орбите под действием кулоновской силы F = Ze 2/4 0 r 2 = m. V 2/r Ekin = m. V 2/2 = Ze 2/8 0 r Epot = -Ze 2/4 0 r Полная энергия атома E = -Ze 2/4 0 r + Ze 2/8 0 r = - Ze 2/8 0 r Момент количества движения электрона P = m. Vnrn = nh/2 m. V 2 = Ze 2/4 0 r En = me 4 Z 2/8 02 h 2 n 2 rn = 0 h 2 n 2/ me 2 Z = R (1/n 22 – 1/n 12) R – постоянная Ридберга
Оценка энергии электрона Электрон движется по круговой орбите под действием кулоновской силы F = Ze 2/4 0 r 2 = m. V 2/r Ekin = m. V 2/2 = Ze 2/8 0 r Epot = -Ze 2/4 0 r Полная энергия атома E = -Ze 2/4 0 r + Ze 2/8 0 r = - Ze 2/8 0 r Момент количества движения электрона P = m. Vnrn = nh/2 m. V 2 = Ze 2/4 0 r En = me 4 Z 2/8 02 h 2 n 2 rn = 0 h 2 n 2/ me 2 Z = R (1/n 22 – 1/n 12) R – постоянная Ридберга
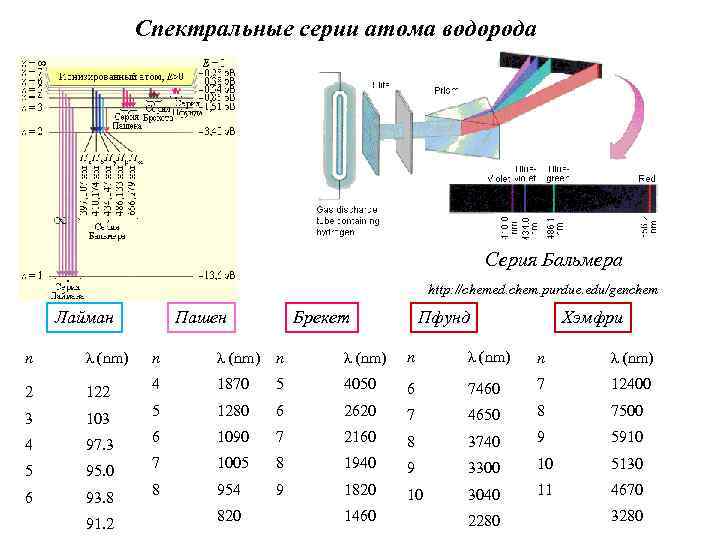 Спектральные серии атома водорода Серия Бальмера http: //chemed. chem. purdue. edu/genchem Лайман Пашен Брекет Пфунд Хэмфри n λ (nm) n λ (nm) 2 122 4 1870 5 4050 6 7460 7 12400 3 103 5 1280 6 2620 7 4650 8 7500 4 97. 3 6 1090 7 2160 8 3740 9 5910 5 95. 0 7 1005 8 1940 9 3300 10 5130 6 93. 8 8 954 9 1820 10 3040 11 4670 91. 2 820 1460 2280 3280
Спектральные серии атома водорода Серия Бальмера http: //chemed. chem. purdue. edu/genchem Лайман Пашен Брекет Пфунд Хэмфри n λ (nm) n λ (nm) 2 122 4 1870 5 4050 6 7460 7 12400 3 103 5 1280 6 2620 7 4650 8 7500 4 97. 3 6 1090 7 2160 8 3740 9 5910 5 95. 0 7 1005 8 1940 9 3300 10 5130 6 93. 8 8 954 9 1820 10 3040 11 4670 91. 2 820 1460 2280 3280
 Спектральные серии Линии атомных спектров образуют закономерные группы, которые называются спектральными сериями. Промежутки между линиями в серии убывают в сторону коротких длин волн, и линии сходятся к границе серии, т. е. к границе ионизации, соответствующей отрыву электрона. Выше границы ионизации лежит непрерывный энергетический спектр. Наиболее прост спектр атома водорода. Схема уровней энергии водородоподобных ионов He+, Li 2+… отличается от схемы уровней атома H только увеличением масштаба в Z 2 раз. Уровни различных элементов: http: //physics. nist. gov/cgi-bin/ASD/levels_pt. pl
Спектральные серии Линии атомных спектров образуют закономерные группы, которые называются спектральными сериями. Промежутки между линиями в серии убывают в сторону коротких длин волн, и линии сходятся к границе серии, т. е. к границе ионизации, соответствующей отрыву электрона. Выше границы ионизации лежит непрерывный энергетический спектр. Наиболее прост спектр атома водорода. Схема уровней энергии водородоподобных ионов He+, Li 2+… отличается от схемы уровней атома H только увеличением масштаба в Z 2 раз. Уровни различных элементов: http: //physics. nist. gov/cgi-bin/ASD/levels_pt. pl
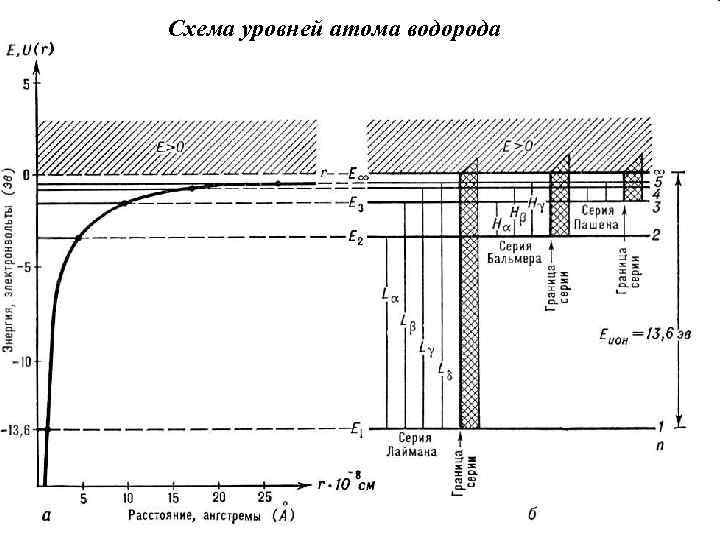 Схема уровней атома водорода
Схема уровней атома водорода
 Атом водорода – диаграмма Гротриана Б. М. Смирнов, Физика атома и иона, Энергоатомиздат, 1986
Атом водорода – диаграмма Гротриана Б. М. Смирнов, Физика атома и иона, Энергоатомиздат, 1986
 Понятие об электронных орбиталях Часть атомного пространства, где вероятность пребывания электрона > 90%, называют орбиталью ( «электронным облаком» ) Электрон в атоме участвует в двух видах движения – орбитальное движение относительно ядра и собственное вращательное движение. Для полного описания необходимо знать 4 параметра: • энергию электрона, n • величину орбитального момента количества движения, l • направление орбитального момента количества движения, ml • направление собственного момента количества движения. ms Плотность вероятности для е при различных квантовых числах
Понятие об электронных орбиталях Часть атомного пространства, где вероятность пребывания электрона > 90%, называют орбиталью ( «электронным облаком» ) Электрон в атоме участвует в двух видах движения – орбитальное движение относительно ядра и собственное вращательное движение. Для полного описания необходимо знать 4 параметра: • энергию электрона, n • величину орбитального момента количества движения, l • направление орбитального момента количества движения, ml • направление собственного момента количества движения. ms Плотность вероятности для е при различных квантовых числах
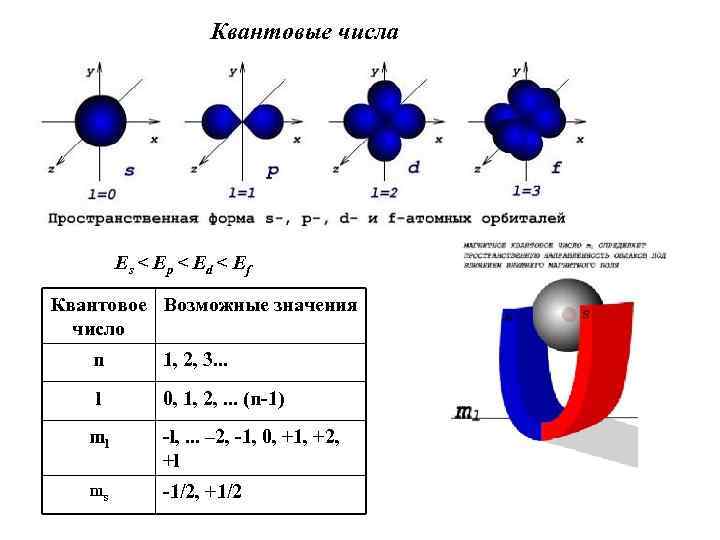 Квантовые числа Es < Ep < Ed < Ef Квантовое Возможные значения число n 1, 2, 3. . . l 0, 1, 2, . . . (n-1) ml -l, . . . – 2, -1, 0, +1, +2, +l ms -1/2, +1/2
Квантовые числа Es < Ep < Ed < Ef Квантовое Возможные значения число n 1, 2, 3. . . l 0, 1, 2, . . . (n-1) ml -l, . . . – 2, -1, 0, +1, +2, +l ms -1/2, +1/2
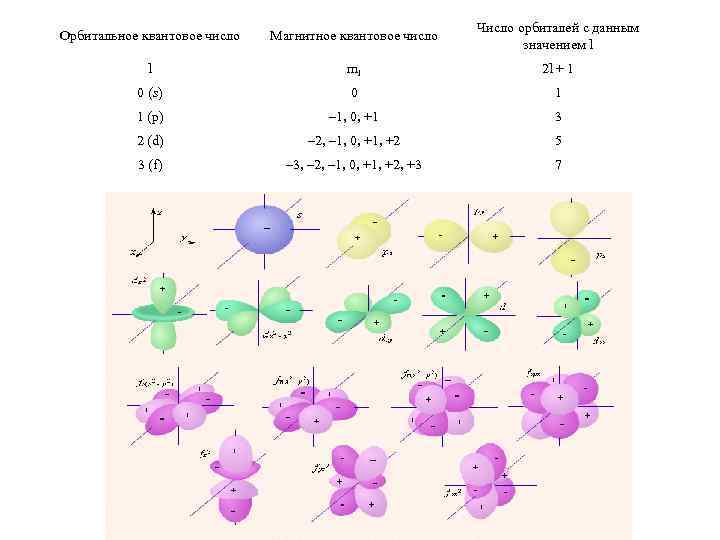 Орбитальное квантовое число Магнитное квантовое число Число орбиталей с данным значением l l ml 2 l + 1 0 (s) 0 1 1 (p) – 1, 0, +1 3 2 (d) – 2, – 1, 0, +1, +2 5 3 (f) – 3, – 2, – 1, 0, +1, +2, +3 7
Орбитальное квантовое число Магнитное квантовое число Число орбиталей с данным значением l l ml 2 l + 1 0 (s) 0 1 1 (p) – 1, 0, +1 3 2 (d) – 2, – 1, 0, +1, +2 5 3 (f) – 3, – 2, – 1, 0, +1, +2, +3 7
 Принципы заполнения атомных орбиталей Принцип минимума энергии: Электроны заполняют орбитали в порядке увеличения их энергии: на орбиталях с большей энергией электроны располагаются после того, как заполнены орбитали с меньшей энергией. Принцип Паули: В атоме не может быть двух электронов с одинаковым набором значений всех четырех квантовых чисел.
Принципы заполнения атомных орбиталей Принцип минимума энергии: Электроны заполняют орбитали в порядке увеличения их энергии: на орбиталях с большей энергией электроны располагаются после того, как заполнены орбитали с меньшей энергией. Принцип Паули: В атоме не может быть двух электронов с одинаковым набором значений всех четырех квантовых чисел.
 Правило Хунда определяет порядок заполнения орбиталей определённого подслоя : модуль суммарного значения ms подслоя должен быть максимальным. Это означает, что все свободные орбитали подслоя заполняются сначала по одному электрону, а потом только на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелыми спинами противоположного знака, которые спариваются (образуют двухэлектронное облако. В результате, суммарный спин орбитали становится равным нулю. Другая формулировка: Ниже по энергии лежит тот атомный терм, для которого выполняются два условия – • мультиплетность максимальна, • при совпадении мультиплетностей суммарный орбитальный момент L максимален.
Правило Хунда определяет порядок заполнения орбиталей определённого подслоя : модуль суммарного значения ms подслоя должен быть максимальным. Это означает, что все свободные орбитали подслоя заполняются сначала по одному электрону, а потом только на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелыми спинами противоположного знака, которые спариваются (образуют двухэлектронное облако. В результате, суммарный спин орбитали становится равным нулю. Другая формулировка: Ниже по энергии лежит тот атомный терм, для которого выполняются два условия – • мультиплетность максимальна, • при совпадении мультиплетностей суммарный орбитальный момент L максимален.
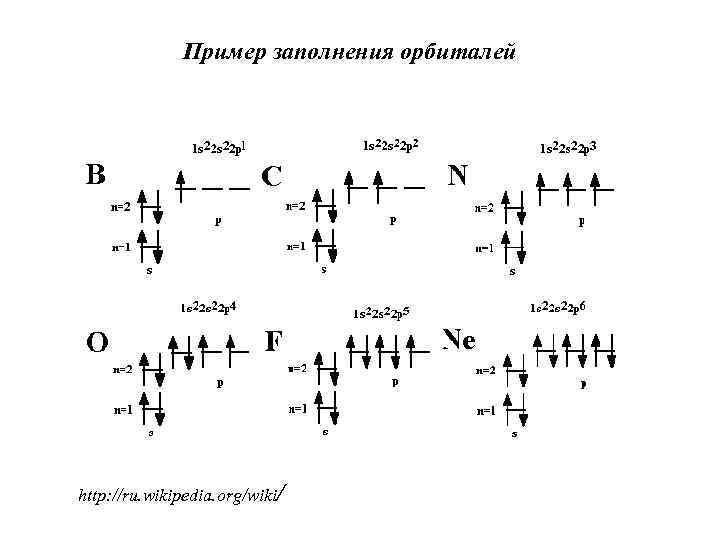 Пример заполнения орбиталей http: //ru. wikipedia. org/wiki/
Пример заполнения орбиталей http: //ru. wikipedia. org/wiki/
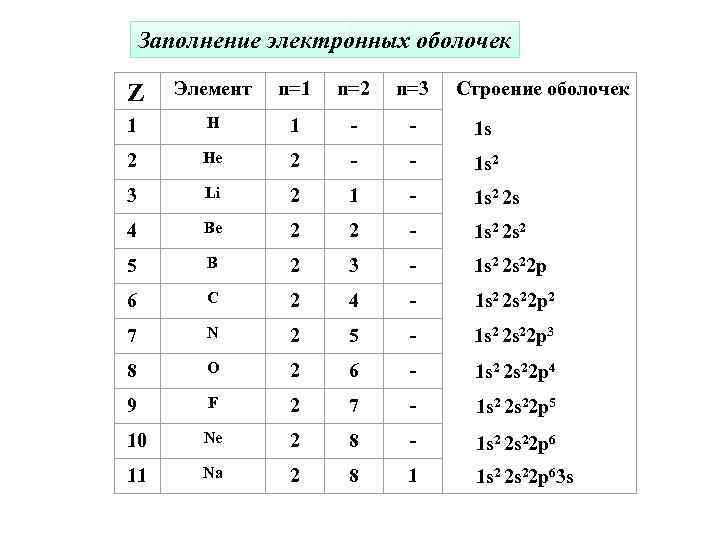 Заполнение электронных оболочек Строение оболочек Z Элемент n=1 n=2 n=3 1 H 1 - - 1 s 2 He 2 - - 1 s 2 3 Li 2 1 - 1 s 2 2 s 4 Be 2 2 - 1 s 2 2 s 2 5 B 2 3 - 1 s 2 2 s 22 p 6 C 2 4 - 1 s 2 2 s 22 p 2 7 N 2 5 - 1 s 2 2 s 22 p 3 8 O 2 6 - 1 s 2 2 s 22 p 4 9 F 2 7 - 1 s 2 2 s 22 p 5 10 Ne 2 8 - 1 s 2 2 s 22 p 6 11 Na 2 8 1 1 s 2 2 s 22 p 63 s
Заполнение электронных оболочек Строение оболочек Z Элемент n=1 n=2 n=3 1 H 1 - - 1 s 2 He 2 - - 1 s 2 3 Li 2 1 - 1 s 2 2 s 4 Be 2 2 - 1 s 2 2 s 2 5 B 2 3 - 1 s 2 2 s 22 p 6 C 2 4 - 1 s 2 2 s 22 p 2 7 N 2 5 - 1 s 2 2 s 22 p 3 8 O 2 6 - 1 s 2 2 s 22 p 4 9 F 2 7 - 1 s 2 2 s 22 p 5 10 Ne 2 8 - 1 s 2 2 s 22 p 6 11 Na 2 8 1 1 s 2 2 s 22 p 63 s
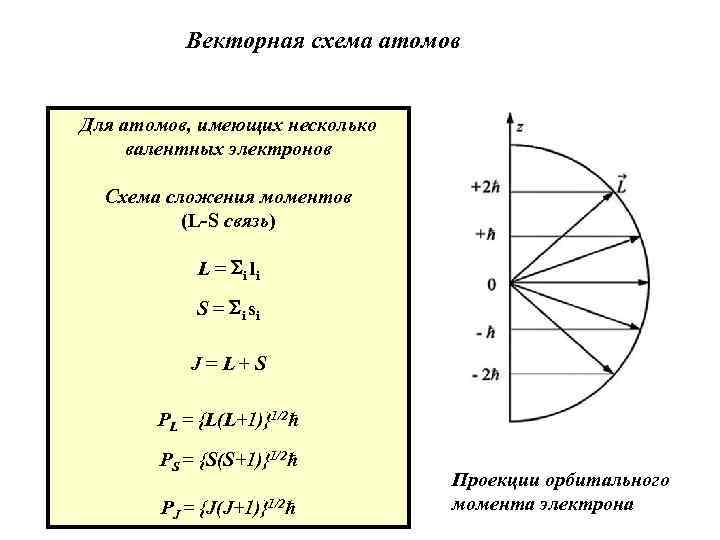 Векторная схема атомов Для атомов, имеющих несколько валентных электронов Схема сложения моментов (L-S связь) L = i li S = i si J = L+ S PL = {L(L+1)}1/2ħ PS = {S(S+1)}1/2ħ PJ = {J(J+1)}1/2ħ Проекции орбитального момента электрона
Векторная схема атомов Для атомов, имеющих несколько валентных электронов Схема сложения моментов (L-S связь) L = i li S = i si J = L+ S PL = {L(L+1)}1/2ħ PS = {S(S+1)}1/2ħ PJ = {J(J+1)}1/2ħ Проекции орбитального момента электрона
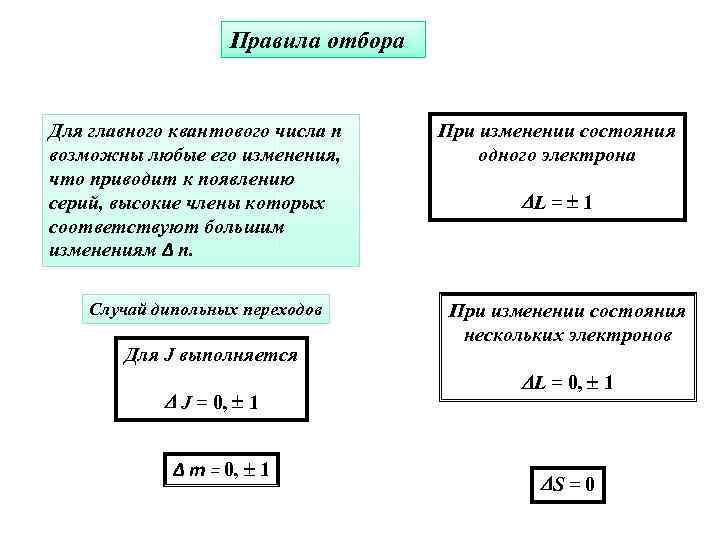 Правила отбора Для главного квантового числа n возможны любые его изменения, что приводит к появлению серий, высокие члены которых соответствуют большим изменениям Δ n. Случай дипольных переходов Для J выполняется J = 0, 1 Δ m = 0, 1 При изменении состояния одного электрона L = 1 При изменении состояния нескольких электронов L = 0, 1 S = 0
Правила отбора Для главного квантового числа n возможны любые его изменения, что приводит к появлению серий, высокие члены которых соответствуют большим изменениям Δ n. Случай дипольных переходов Для J выполняется J = 0, 1 Δ m = 0, 1 При изменении состояния одного электрона L = 1 При изменении состояния нескольких электронов L = 0, 1 S = 0
 Схема уровней атома Li электрон Серии: 22 S – n 2 P главная серия 22 P - n 2 D диффузная серия (первая побочная) 22 P - n 2 S резкая серия (вторая побочная) 32 D - n 2 F фундаментальная серия Главное квантовое число для Na увеличивается на 1, K на 2, Rb на 3, Cs на 4.
Схема уровней атома Li электрон Серии: 22 S – n 2 P главная серия 22 P - n 2 D диффузная серия (первая побочная) 22 P - n 2 S резкая серия (вторая побочная) 32 D - n 2 F фундаментальная серия Главное квантовое число для Na увеличивается на 1, K на 2, Rb на 3, Cs на 4.
 Литература: 1. 2. 3. 4. С. Э. Фриш, Оптические спектры атомов, ФМ, Москва, 1963. М. А. Ельяшевич, Атомная и молекулярная спектроскопия, ФМ, Москва, 1963. Б. М. Смирнов, Физика атома и иона, Энргоатомиздат, 1986. А. А. Бабушкин, П. А. Бажулин, Ф. А. Королев, Л. В. Левшин, В. К. Прокофьев, А. Р. Стриганов, Методы спектрального анализа, Изд. Московского университета, 1962.
Литература: 1. 2. 3. 4. С. Э. Фриш, Оптические спектры атомов, ФМ, Москва, 1963. М. А. Ельяшевич, Атомная и молекулярная спектроскопия, ФМ, Москва, 1963. Б. М. Смирнов, Физика атома и иона, Энргоатомиздат, 1986. А. А. Бабушкин, П. А. Бажулин, Ф. А. Королев, Л. В. Левшин, В. К. Прокофьев, А. Р. Стриганов, Методы спектрального анализа, Изд. Московского университета, 1962.


