8_Lect_2013_10_01_mol spectr.pptx
- Количество слайдов: 32
 Физическое материаловедение Молекулярная спектроскопия
Физическое материаловедение Молекулярная спектроскопия
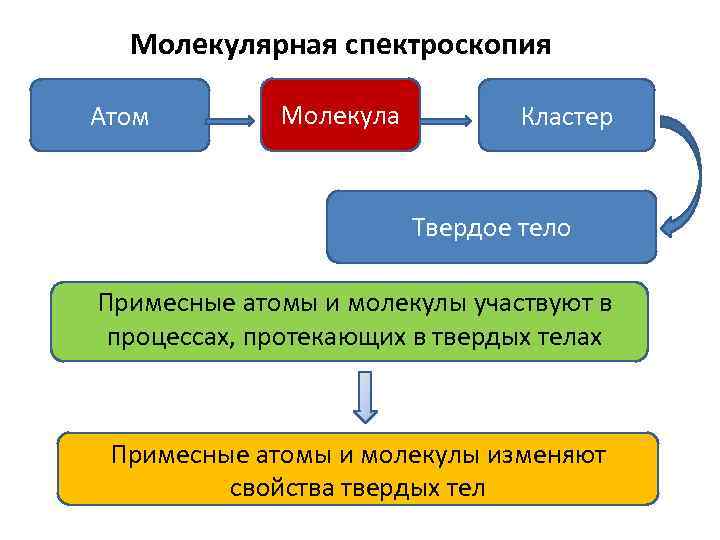 Молекулярная спектроскопия Атом Молекула Кластер Твердое тело Примесные атомы и молекулы участвуют в процессах, протекающих в твердых телах Примесные атомы и молекулы изменяют свойства твердых тел
Молекулярная спектроскопия Атом Молекула Кластер Твердое тело Примесные атомы и молекулы участвуют в процессах, протекающих в твердых телах Примесные атомы и молекулы изменяют свойства твердых тел
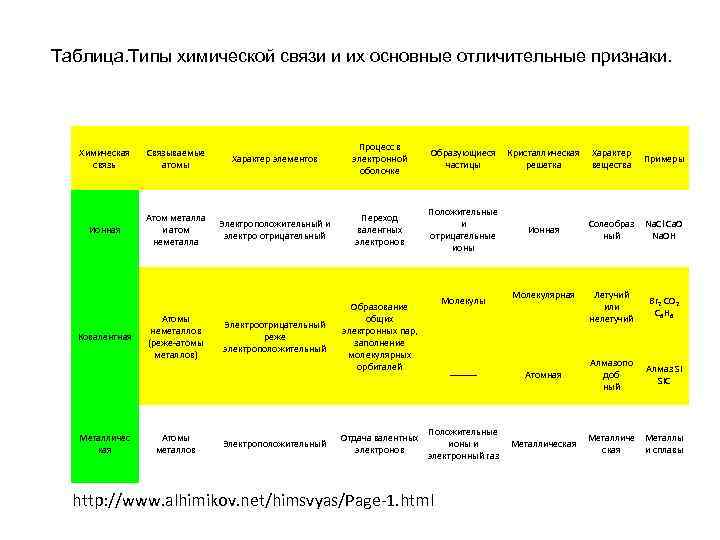 Таблица. Типы химической связи и их основные отличительные признаки. Химическая связь Связываемые атомы Характер элементов Процесс в электронной оболочке Образующиеся Кристаллическая Характер частицы решетка вещества Примеры Ионная Атом металла и атом неметалла Электроположительный и электро отрицательный Переход валентных электронов Положительные и отрицательные ионы Солеобраз ный Na. Cl Ca. O Na. OH Электроотрицательный реже электроположительный Образование общих электронных пар, заполнение молекулярных орбиталей Летучий или нелетучий Br 2 CO 2 C 6 H 6 Алмазопо доб ный Алмаз Si Si. C Ковалентная Металличес кая Атомы неметаллов (реже-атомы металлов) Атомы металлов Электроположительный Отдача валентных электронов Молекулы ----- Ионная Молекулярная Атомная Положительные ионы и Металлическая электронный газ http: //www. alhimikov. net/himsvyas/Page-1. html Металличе Металлы ская и сплавы
Таблица. Типы химической связи и их основные отличительные признаки. Химическая связь Связываемые атомы Характер элементов Процесс в электронной оболочке Образующиеся Кристаллическая Характер частицы решетка вещества Примеры Ионная Атом металла и атом неметалла Электроположительный и электро отрицательный Переход валентных электронов Положительные и отрицательные ионы Солеобраз ный Na. Cl Ca. O Na. OH Электроотрицательный реже электроположительный Образование общих электронных пар, заполнение молекулярных орбиталей Летучий или нелетучий Br 2 CO 2 C 6 H 6 Алмазопо доб ный Алмаз Si Si. C Ковалентная Металличес кая Атомы неметаллов (реже-атомы металлов) Атомы металлов Электроположительный Отдача валентных электронов Молекулы ----- Ионная Молекулярная Атомная Положительные ионы и Металлическая электронный газ http: //www. alhimikov. net/himsvyas/Page-1. html Металличе Металлы ская и сплавы
 КОВАЛЕНТНАЯ СВЯЗЬ. Ковалентная связь образуется за счёт общих электронных пар, возникающих в оболочках связываемых атомов. Она может быть образована атомами одного и того же элемента и тогда она неполярная; например, такая ковалентная связь существует в молекулах одноэлементных газов H 2, O 2, N 2, Cl 2 и др. Ковалентная связь может быть образована атомами разных элементов, сходных по химическому характеру, и тогда она полярная; например, такая ковалентная связь существует в молекулах H 2 O, NF 3, CO 2. Ковалентная связь образуется между атомами элементов, обладающих электроотрицательным характером.
КОВАЛЕНТНАЯ СВЯЗЬ. Ковалентная связь образуется за счёт общих электронных пар, возникающих в оболочках связываемых атомов. Она может быть образована атомами одного и того же элемента и тогда она неполярная; например, такая ковалентная связь существует в молекулах одноэлементных газов H 2, O 2, N 2, Cl 2 и др. Ковалентная связь может быть образована атомами разных элементов, сходных по химическому характеру, и тогда она полярная; например, такая ковалентная связь существует в молекулах H 2 O, NF 3, CO 2. Ковалентная связь образуется между атомами элементов, обладающих электроотрицательным характером.
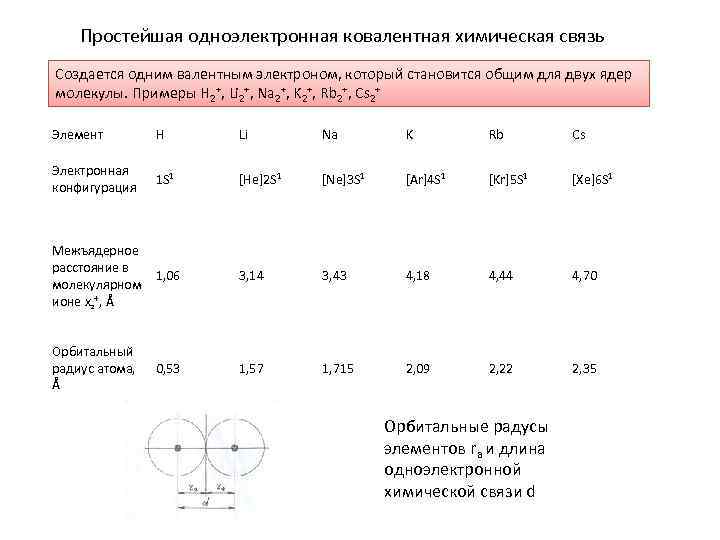 Простейшая одноэлектронная ковалентная химическая связь Создается одним валентным электроном, который становится общим для двух ядер молекулы. Примеры H 2+, Li 2+, Na 2+, K 2+, Rb 2+, Cs 2+ Элемент H Li Na K Rb Cs Электронная конфигурация 1 S 1 [He]2 S 1 [Ne]3 S 1 [Ar]4 S 1 [Kr]5 S 1 [Xe]6 S 1 Межъядерное расстояние в 1, 06 молекулярном ионе xz+, Å 3, 14 3, 43 4, 18 4, 44 4, 70 Орбитальный радиус атома, Å 1, 57 1, 715 2, 09 2, 22 2, 35 0, 53 Орбитальные радусы элементов ra и длина одноэлектронной химической связи d
Простейшая одноэлектронная ковалентная химическая связь Создается одним валентным электроном, который становится общим для двух ядер молекулы. Примеры H 2+, Li 2+, Na 2+, K 2+, Rb 2+, Cs 2+ Элемент H Li Na K Rb Cs Электронная конфигурация 1 S 1 [He]2 S 1 [Ne]3 S 1 [Ar]4 S 1 [Kr]5 S 1 [Xe]6 S 1 Межъядерное расстояние в 1, 06 молекулярном ионе xz+, Å 3, 14 3, 43 4, 18 4, 44 4, 70 Орбитальный радиус атома, Å 1, 57 1, 715 2, 09 2, 22 2, 35 0, 53 Орбитальные радусы элементов ra и длина одноэлектронной химической связи d
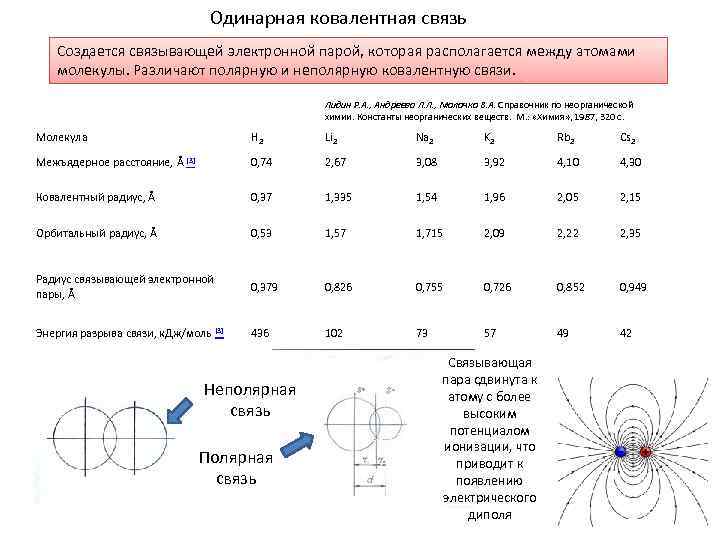 Одинарная ковалентная связь Создается связывающей электронной парой, которая располагается между атомами молекулы. Различают полярную и неполярную ковалентную связи. Лидин Р. А. , Андреева Л. Л. , Молочко В. А. Справочник по неорганической химии. Константы неорганических веществ. М. : «Химия» , 1987, 320 с. Молекула H 2 Li 2 Na 2 K 2 Rb 2 Cs 2 Межъядерное расстояние, Å [3] 0, 74 2, 67 3, 08 3, 92 4, 10 4, 30 Ковалентный радиус, Å 0, 37 1, 335 1, 54 1, 96 2, 05 2, 15 Орбитальный радиус, Å 0, 53 1, 57 1, 715 2, 09 2, 22 2, 35 Радиус связывающей электронной пары, Å 0, 379 0, 826 0, 755 0, 726 0, 852 0, 949 Энергия разрыва связи, к. Дж/моль [3] 436 102 73 57 49 42 Неполярная связь Полярная связь Связывающая пара сдвинута к атому с более высоким потенциалом ионизации, что приводит к появлению электрического диполя
Одинарная ковалентная связь Создается связывающей электронной парой, которая располагается между атомами молекулы. Различают полярную и неполярную ковалентную связи. Лидин Р. А. , Андреева Л. Л. , Молочко В. А. Справочник по неорганической химии. Константы неорганических веществ. М. : «Химия» , 1987, 320 с. Молекула H 2 Li 2 Na 2 K 2 Rb 2 Cs 2 Межъядерное расстояние, Å [3] 0, 74 2, 67 3, 08 3, 92 4, 10 4, 30 Ковалентный радиус, Å 0, 37 1, 335 1, 54 1, 96 2, 05 2, 15 Орбитальный радиус, Å 0, 53 1, 57 1, 715 2, 09 2, 22 2, 35 Радиус связывающей электронной пары, Å 0, 379 0, 826 0, 755 0, 726 0, 852 0, 949 Энергия разрыва связи, к. Дж/моль [3] 436 102 73 57 49 42 Неполярная связь Полярная связь Связывающая пара сдвинута к атому с более высоким потенциалом ионизации, что приводит к появлению электрического диполя
 Электроотрицательность (χ) — фундаментальное химическое свойство атома, количественная характеристика способности атома в молекуле смещать к себе общие электронные пары. Теоретическое определение электроотрицательности было предложено американским физиком Р. Малликеном. Исходя из очевидного положения о том, что способность атома в молекуле притягивать к себе электронный заряд зависит от энергии ионизации атома и его сродства к электрону, Р. Малликен ввёл представление об электроотрицательности атома А как о средней величине энергии связи наружных электронов при ионизации валентных состояний (например, от А− до А+) и на этой основе предложил очень простое соотношение для электроотрицательности атома: χ = 1/2 (IA + EA ) где IA и EA — соответственно энергия ионизации атома и его сродство к электрону. Шкалы электроотрицательности: шкала Малликена, шкала Полинга, шкала Сандерсона.
Электроотрицательность (χ) — фундаментальное химическое свойство атома, количественная характеристика способности атома в молекуле смещать к себе общие электронные пары. Теоретическое определение электроотрицательности было предложено американским физиком Р. Малликеном. Исходя из очевидного положения о том, что способность атома в молекуле притягивать к себе электронный заряд зависит от энергии ионизации атома и его сродства к электрону, Р. Малликен ввёл представление об электроотрицательности атома А как о средней величине энергии связи наружных электронов при ионизации валентных состояний (например, от А− до А+) и на этой основе предложил очень простое соотношение для электроотрицательности атома: χ = 1/2 (IA + EA ) где IA и EA — соответственно энергия ионизации атома и его сродство к электрону. Шкалы электроотрицательности: шкала Малликена, шкала Полинга, шкала Сандерсона.
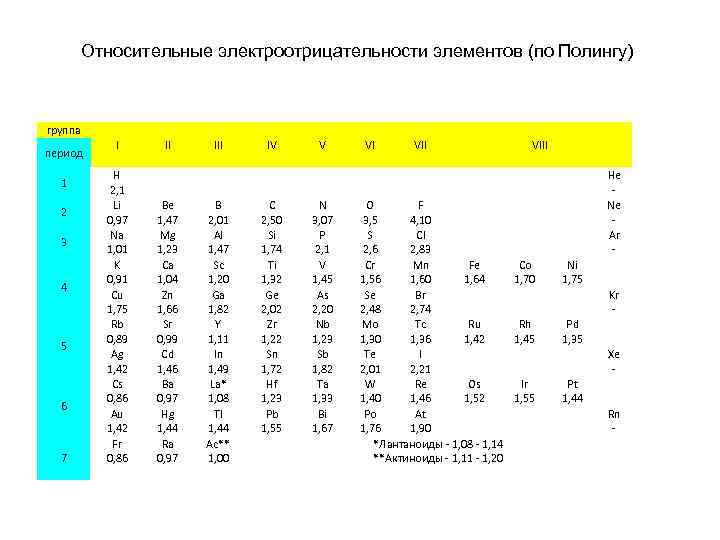 Относительные электроотрицательности элементов (по Полингу) группа период 1 2 3 4 5 6 7 I H 2, 1 Li 0, 97 Na 1, 01 K 0, 91 Cu 1, 75 Rb 0, 89 Ag 1, 42 Cs 0, 86 Au 1, 42 Fr 0, 86 II IV V VI VII Be 1, 47 Mg 1, 23 Ca 1, 04 Zn 1, 66 Sr 0, 99 Cd 1, 46 Ba 0, 97 Hg 1, 44 Ra 0, 97 B 2, 01 Al 1, 47 Sc 1, 20 Ga 1, 82 Y 1, 11 In 1, 49 La* 1, 08 Tl 1, 44 Ac** 1, 00 C 2, 50 Si 1, 74 Ti 1, 32 Ge 2, 02 Zr 1, 22 Sn 1, 72 Hf 1, 23 Pb 1, 55 N 3, 07 P 2, 1 V 1, 45 As 2, 20 Nb 1, 23 Sb 1, 82 Ta 1, 33 Bi 1, 67 VIII He Ne Ar - O F 3, 5 4, 10 S Cl 2, 6 2, 83 Cr Mn Fe Co 1, 56 1, 60 1, 64 1, 70 Se Br 2, 48 2, 74 Mo Tc Ru Rh 1, 30 1, 36 1, 42 1, 45 Te I 2, 01 2, 21 W Re Os Ir 1, 40 1, 46 1, 52 1, 55 Po At 1, 76 1, 90 *Лантаноиды - 1, 08 - 1, 14 **Актиноиды - 1, 11 - 1, 20 Ni 1, 75 Kr - Pd 1, 35 Xe - Pt 1, 44 Rn -
Относительные электроотрицательности элементов (по Полингу) группа период 1 2 3 4 5 6 7 I H 2, 1 Li 0, 97 Na 1, 01 K 0, 91 Cu 1, 75 Rb 0, 89 Ag 1, 42 Cs 0, 86 Au 1, 42 Fr 0, 86 II IV V VI VII Be 1, 47 Mg 1, 23 Ca 1, 04 Zn 1, 66 Sr 0, 99 Cd 1, 46 Ba 0, 97 Hg 1, 44 Ra 0, 97 B 2, 01 Al 1, 47 Sc 1, 20 Ga 1, 82 Y 1, 11 In 1, 49 La* 1, 08 Tl 1, 44 Ac** 1, 00 C 2, 50 Si 1, 74 Ti 1, 32 Ge 2, 02 Zr 1, 22 Sn 1, 72 Hf 1, 23 Pb 1, 55 N 3, 07 P 2, 1 V 1, 45 As 2, 20 Nb 1, 23 Sb 1, 82 Ta 1, 33 Bi 1, 67 VIII He Ne Ar - O F 3, 5 4, 10 S Cl 2, 6 2, 83 Cr Mn Fe Co 1, 56 1, 60 1, 64 1, 70 Se Br 2, 48 2, 74 Mo Tc Ru Rh 1, 30 1, 36 1, 42 1, 45 Te I 2, 01 2, 21 W Re Os Ir 1, 40 1, 46 1, 52 1, 55 Po At 1, 76 1, 90 *Лантаноиды - 1, 08 - 1, 14 **Актиноиды - 1, 11 - 1, 20 Ni 1, 75 Kr - Pd 1, 35 Xe - Pt 1, 44 Rn -
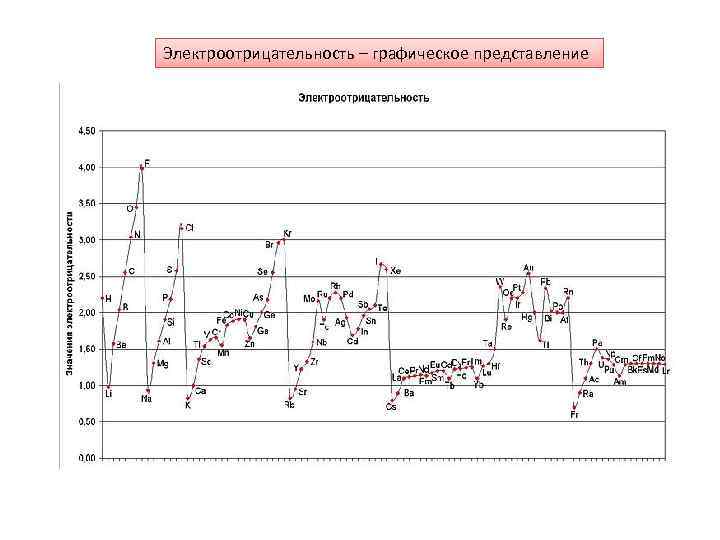 Электроотрицательность – графическое представление
Электроотрицательность – графическое представление
 Молекулярные орбитали Теория молекулярных орбиталей (МО) дает представление о распределении электронной плотности и объясняет свойства молекул. В этой теории квантовомеханические зависимости для атома распространены на более сложную систему — молекулу. По аналогии с атомными s-, p-, d- орбиталями молекулярные орбитали обозначают греческими буквами σ-, π-, δ-. МО образуются при комбинировании атомных орбиталей при достаточном сближении. Н. Ф. Степанов Химическая связь в простых двухатомных молекулах, Химия, Соросовский образовательный журнал № 10, 1998, с. 37
Молекулярные орбитали Теория молекулярных орбиталей (МО) дает представление о распределении электронной плотности и объясняет свойства молекул. В этой теории квантовомеханические зависимости для атома распространены на более сложную систему — молекулу. По аналогии с атомными s-, p-, d- орбиталями молекулярные орбитали обозначают греческими буквами σ-, π-, δ-. МО образуются при комбинировании атомных орбиталей при достаточном сближении. Н. Ф. Степанов Химическая связь в простых двухатомных молекулах, Химия, Соросовский образовательный журнал № 10, 1998, с. 37
 Химическая связь в молекулах и атомные орбитали Ковалентная связь (атомная связь, гомеополярная связь) — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. В результате обобществления электроны образуют заполненный энергетический уровень. Связь образуется, если их суммарная энергия на этом уровне будет меньше, чем в первоначальном состоянии (а разница в энергии будет не чем иным, как энергией связи). Согласно теории молекулярных орбиталей, перекрывание двух атомных орбиталей приводит в простейшем случае к образованию двух молекулярных орбиталей (МО): связывающей МО и антисвязывающей (разрыхляющей) МО. Обобществленные электроны располагаются на более низкой по энергии связывающей МО. Заполнение электронами атомных (по краям) и молекулярных (в центре) орбиталей в молекуле H 2. Вертикальная ось соответствует энергетическому уровню, электроны обозначены стрелками, отражающими их спины.
Химическая связь в молекулах и атомные орбитали Ковалентная связь (атомная связь, гомеополярная связь) — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. В результате обобществления электроны образуют заполненный энергетический уровень. Связь образуется, если их суммарная энергия на этом уровне будет меньше, чем в первоначальном состоянии (а разница в энергии будет не чем иным, как энергией связи). Согласно теории молекулярных орбиталей, перекрывание двух атомных орбиталей приводит в простейшем случае к образованию двух молекулярных орбиталей (МО): связывающей МО и антисвязывающей (разрыхляющей) МО. Обобществленные электроны располагаются на более низкой по энергии связывающей МО. Заполнение электронами атомных (по краям) и молекулярных (в центре) орбиталей в молекуле H 2. Вертикальная ось соответствует энергетическому уровню, электроны обозначены стрелками, отражающими их спины.
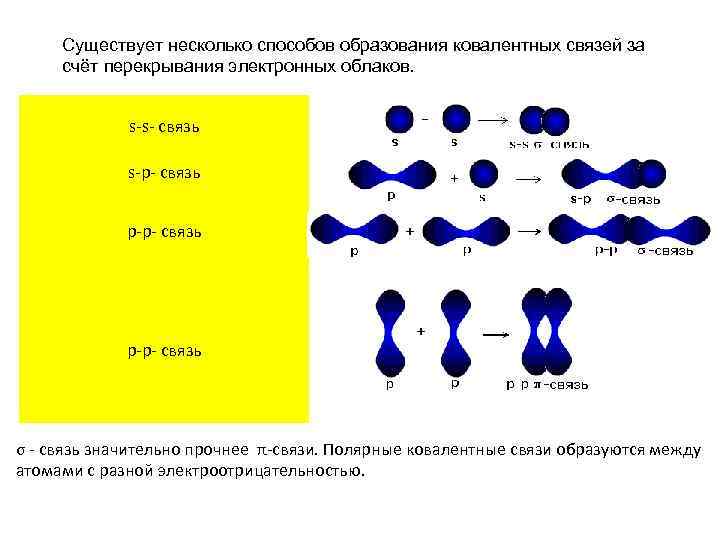 Существует несколько способов образования ковалентных связей за счёт перекрывания электронных облаков. s-s- связь s-p- связь p-p- связь σ - связь значительно прочнее π-связи. Полярные ковалентные связи образуются между атомами с разной электроотрицательностью.
Существует несколько способов образования ковалентных связей за счёт перекрывания электронных облаков. s-s- связь s-p- связь p-p- связь σ - связь значительно прочнее π-связи. Полярные ковалентные связи образуются между атомами с разной электроотрицательностью.
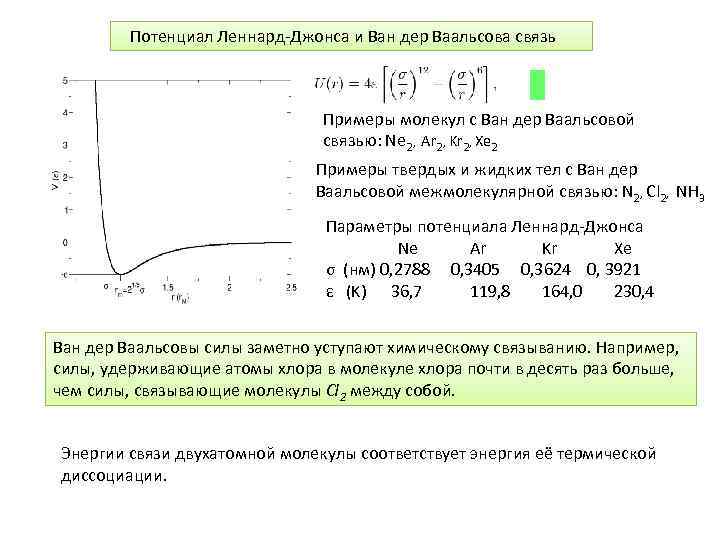 Потенциал Леннард-Джонса и Ван дер Ваальсова связь Примеры молекул с Ван дер Ваальсовой связью: Ne 2, Ar 2, Kr 2, Xe 2 Примеры твердых и жидких тел с Ван дер Ваальсовой межмолекулярной связью: N 2, Cl 2, NH 3 Параметры потенциала Леннард-Джонса Ne Ar Kr Xe σ (нм) 0, 2788 0, 3405 0, 3624 0, 3921 ε (K) 36, 7 119, 8 164, 0 230, 4 Ван дер Ваальсовы силы заметно уступают химическому связыванию. Например, силы, удерживающие атомы хлора в молекуле хлора почти в десять раз больше, чем силы, связывающие молекулы Cl 2 между собой. Энергии связи двухатомной молекулы соответствует энергия её термической диссоциации.
Потенциал Леннард-Джонса и Ван дер Ваальсова связь Примеры молекул с Ван дер Ваальсовой связью: Ne 2, Ar 2, Kr 2, Xe 2 Примеры твердых и жидких тел с Ван дер Ваальсовой межмолекулярной связью: N 2, Cl 2, NH 3 Параметры потенциала Леннард-Джонса Ne Ar Kr Xe σ (нм) 0, 2788 0, 3405 0, 3624 0, 3921 ε (K) 36, 7 119, 8 164, 0 230, 4 Ван дер Ваальсовы силы заметно уступают химическому связыванию. Например, силы, удерживающие атомы хлора в молекуле хлора почти в десять раз больше, чем силы, связывающие молекулы Cl 2 между собой. Энергии связи двухатомной молекулы соответствует энергия её термической диссоциации.
 Типы молекулярных спектров Схема уровней энергии двухатомной молекулы: а и б - электронные уровни; v' и v" - квантовые числа колебательных уровней; J' и J" - квантовые числа вращательных уровней Е = Еэл + Екол + Евращ Еэл >> Екол >> Евращ 1 : (me/M)1/2 : me/M 1 -10 : 10 -2 - 10 -1 : 10 -5 - 10 -3 (э. В)
Типы молекулярных спектров Схема уровней энергии двухатомной молекулы: а и б - электронные уровни; v' и v" - квантовые числа колебательных уровней; J' и J" - квантовые числа вращательных уровней Е = Еэл + Екол + Евращ Еэл >> Екол >> Евращ 1 : (me/M)1/2 : me/M 1 -10 : 10 -2 - 10 -1 : 10 -5 - 10 -3 (э. В)
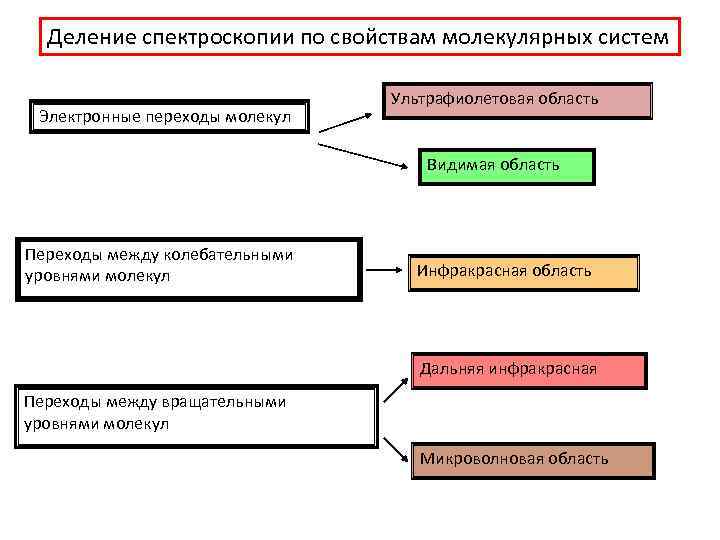 Деление спектроскопии по свойствам молекулярных систем Электронные переходы молекул Ультрафиолетовая область Видимая область Переходы между колебательными уровнями молекул Инфракрасная область Дальняя инфракрасная Переходы между вращательными уровнями молекул Микроволновая область
Деление спектроскопии по свойствам молекулярных систем Электронные переходы молекул Ультрафиолетовая область Видимая область Переходы между колебательными уровнями молекул Инфракрасная область Дальняя инфракрасная Переходы между вращательными уровнями молекул Микроволновая область
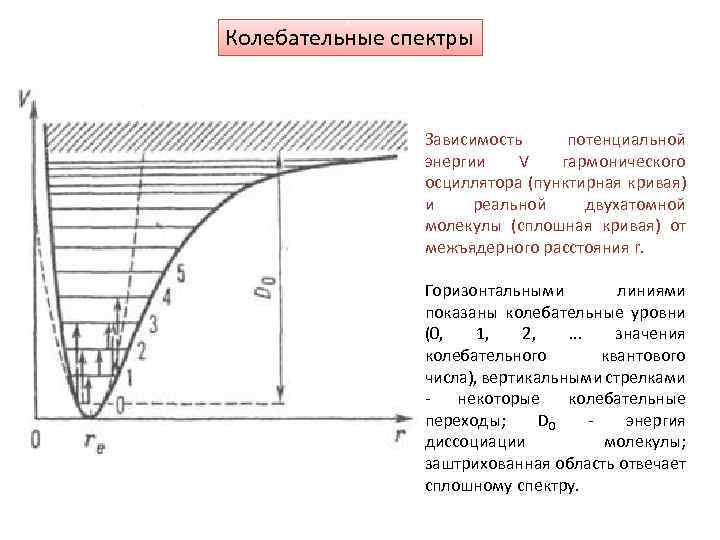 Колебательные спектры Зависимость потенциальной энергии V гармонического осциллятора (пунктирная кривая) и реальной двухатомной молекулы (сплошная кривая) от межъядерного расстояния r. Горизонтальными линиями показаны колебательные уровни (0, 1, 2, . . . значения колебательного квантового числа), вертикальными стрелками - некоторые колебательные переходы; D 0 - энергия диссоциации молекулы; заштрихованная область отвечает сплошному спектру.
Колебательные спектры Зависимость потенциальной энергии V гармонического осциллятора (пунктирная кривая) и реальной двухатомной молекулы (сплошная кривая) от межъядерного расстояния r. Горизонтальными линиями показаны колебательные уровни (0, 1, 2, . . . значения колебательного квантового числа), вертикальными стрелками - некоторые колебательные переходы; D 0 - энергия диссоциации молекулы; заштрихованная область отвечает сплошному спектру.
![Гармонические колебания μ=m 1 m 2/(m 1+m 2)]; Е=l/2(Keq 2), где μ – приведенная Гармонические колебания μ=m 1 m 2/(m 1+m 2)]; Е=l/2(Keq 2), где μ – приведенная](https://present5.com/presentation/28658028_229405396/image-17.jpg) Гармонические колебания μ=m 1 m 2/(m 1+m 2)]; Е=l/2(Keq 2), где μ – приведенная масса, q – колебательная координата, Ке=(d 2 V/dq 2)q=0 - гармоническая силовая постоянная. Ev = l/2(Keq 2) = hν (v+1/2) ν = 1/2π (Ке /μ)1/2 – частота гармонического колебания Δv = 1; ΔE = hνe E=1/2 hνe – энергия нулевых колебаний Ангармоничность колебаний Ev = ν (v +1/2) – νx(v+1/2)2, x – константа ангармоничности, здесь h опущено. ΔE = Ev+1 – Ev = ν - 2νx(v+1) = ν [1 -2 x(v+1)] 0 -1, 1 -2, 2 -3… ν(1 -2 x), ν(1 -4 x), ν (1 -6 x)… ν 0 -1 = νe(1 -2 xe) = νe - 2νexe В инфракрасном (ИК) спектре поглощения двухатомных молекул колебательные частоты наблюдаются только у гетероядерных молекул, например NO, CO, HCl, CN и т. п.
Гармонические колебания μ=m 1 m 2/(m 1+m 2)]; Е=l/2(Keq 2), где μ – приведенная масса, q – колебательная координата, Ке=(d 2 V/dq 2)q=0 - гармоническая силовая постоянная. Ev = l/2(Keq 2) = hν (v+1/2) ν = 1/2π (Ке /μ)1/2 – частота гармонического колебания Δv = 1; ΔE = hνe E=1/2 hνe – энергия нулевых колебаний Ангармоничность колебаний Ev = ν (v +1/2) – νx(v+1/2)2, x – константа ангармоничности, здесь h опущено. ΔE = Ev+1 – Ev = ν - 2νx(v+1) = ν [1 -2 x(v+1)] 0 -1, 1 -2, 2 -3… ν(1 -2 x), ν(1 -4 x), ν (1 -6 x)… ν 0 -1 = νe(1 -2 xe) = νe - 2νexe В инфракрасном (ИК) спектре поглощения двухатомных молекул колебательные частоты наблюдаются только у гетероядерных молекул, например NO, CO, HCl, CN и т. п.
![Потенциал Морзе: построение потенциальных кривых по экспериментальным данным Ur = De {1 - exp[-β(r-re)]}2 Потенциал Морзе: построение потенциальных кривых по экспериментальным данным Ur = De {1 - exp[-β(r-re)]}2](https://present5.com/presentation/28658028_229405396/image-18.jpg) Потенциал Морзе: построение потенциальных кривых по экспериментальным данным Ur = De {1 - exp[-β(r-re)]}2 β = 2πνe(μ/2 De)1/2 De, νe, re De = νe/4 xe = νe 2/4 xeνe Нижние потенциальные кривые молекулы водорода H 2
Потенциал Морзе: построение потенциальных кривых по экспериментальным данным Ur = De {1 - exp[-β(r-re)]}2 β = 2πνe(μ/2 De)1/2 De, νe, re De = νe/4 xe = νe 2/4 xeνe Нижние потенциальные кривые молекулы водорода H 2
 Принцип Франка-Кондона Pn’v’ n’’v’’ = Pn’ n’’ ∫ψкол’(ρ) ψкол’’(ρ)dρ Pn’ n’’ – дипольный момент электронного перехода, I v’v’’ = ∫ψкол’(ρ) ψкол’’(ρ)dρ – Интеграл перекрытия колебательных функций
Принцип Франка-Кондона Pn’v’ n’’v’’ = Pn’ n’’ ∫ψкол’(ρ) ψкол’’(ρ)dρ Pn’ n’’ – дипольный момент электронного перехода, I v’v’’ = ∫ψкол’(ρ) ψкол’’(ρ)dρ – Интеграл перекрытия колебательных функций
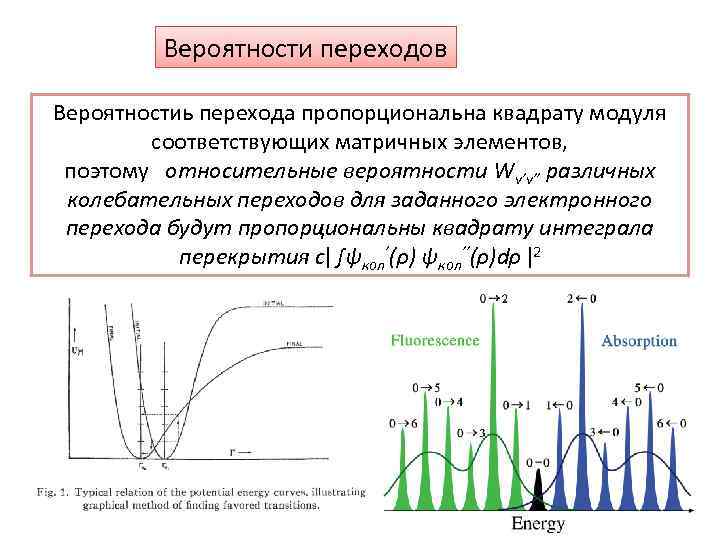 Вероятности переходов Вероятностиь перехода пропорциональна квадрату модуля соответствующих матричных элементов, поэтому относительные вероятности Wv’v’’ различных колебательных переходов для заданного электронного перехода будут пропорциональны квадрату интеграла перекрытия сǀ ∫ψкол’(ρ) ψкол’’(ρ)dρ ǀ2
Вероятности переходов Вероятностиь перехода пропорциональна квадрату модуля соответствующих матричных элементов, поэтому относительные вероятности Wv’v’’ различных колебательных переходов для заданного электронного перехода будут пропорциональны квадрату интеграла перекрытия сǀ ∫ψкол’(ρ) ψкол’’(ρ)dρ ǀ2
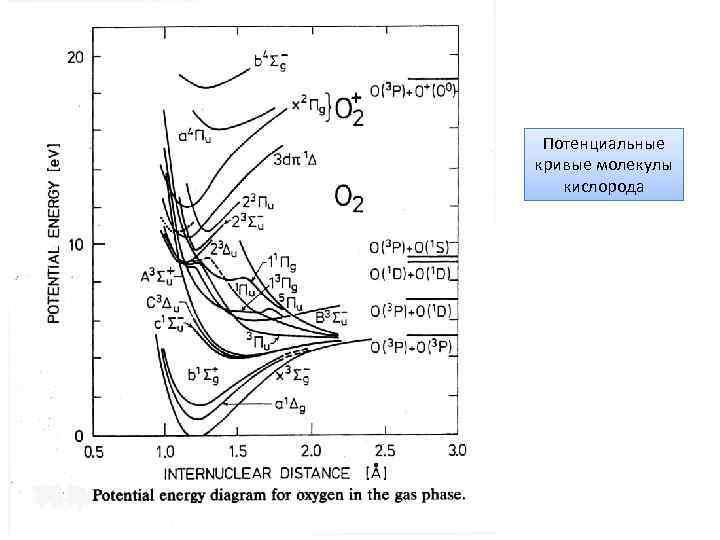 Потенциальные кривые молекулы кислорода
Потенциальные кривые молекулы кислорода
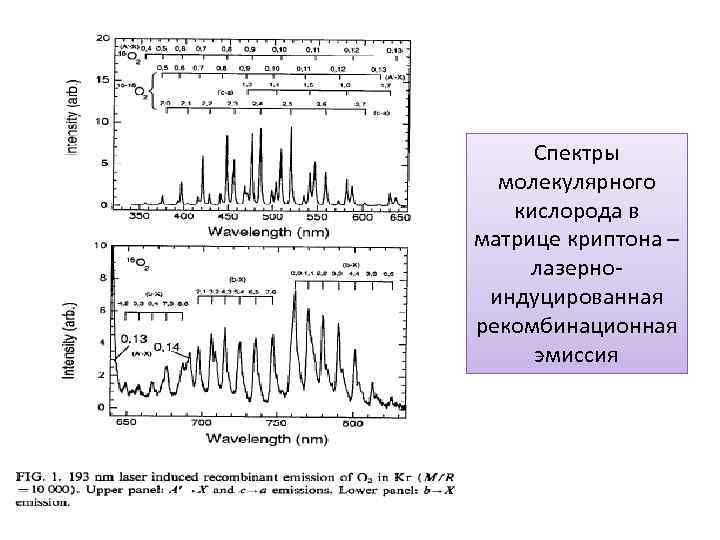 Спектры молекулярного кислорода в матрице криптона – лазерноиндуцированная рекомбинационная эмиссия
Спектры молекулярного кислорода в матрице криптона – лазерноиндуцированная рекомбинационная эмиссия
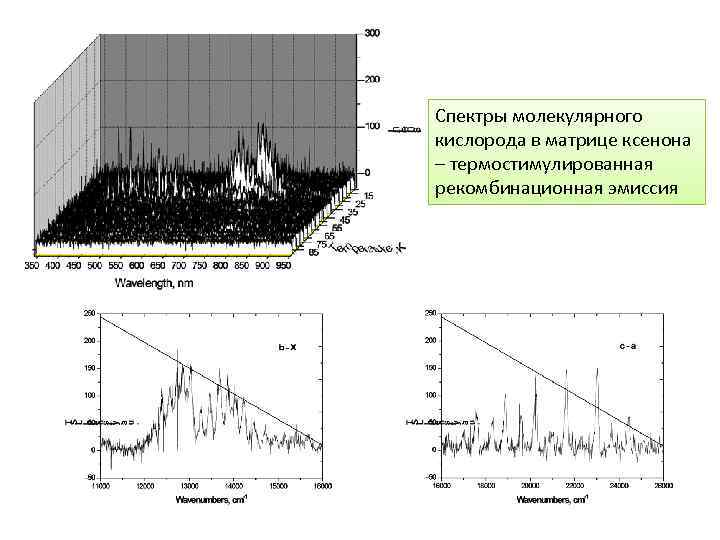 Спектры молекулярного кислорода в матрице ксенона – термостимулированная рекомбинационная эмиссия
Спектры молекулярного кислорода в матрице ксенона – термостимулированная рекомбинационная эмиссия
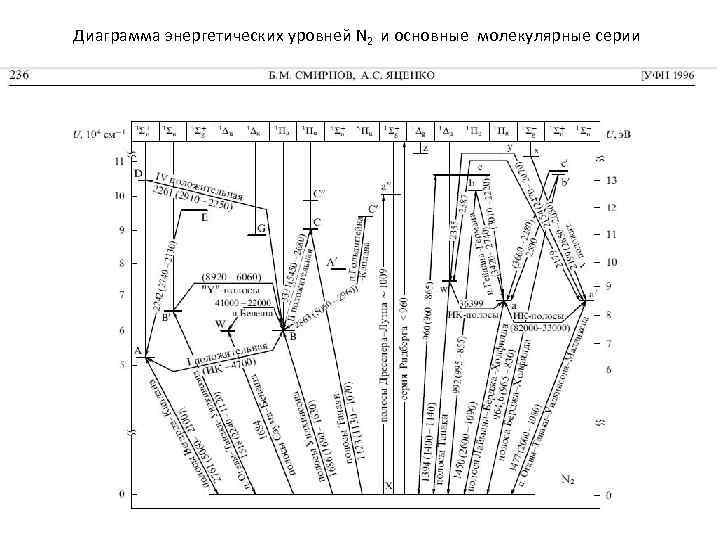 Диаграмма энергетических уровней N 2 и основные молекулярные серии
Диаграмма энергетических уровней N 2 и основные молекулярные серии
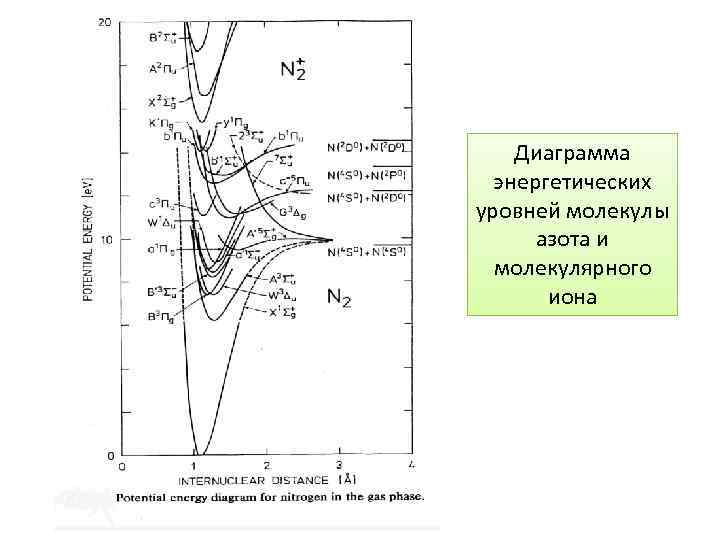 Диаграмма энергетических уровней молекулы азота и молекулярного иона
Диаграмма энергетических уровней молекулы азота и молекулярного иона
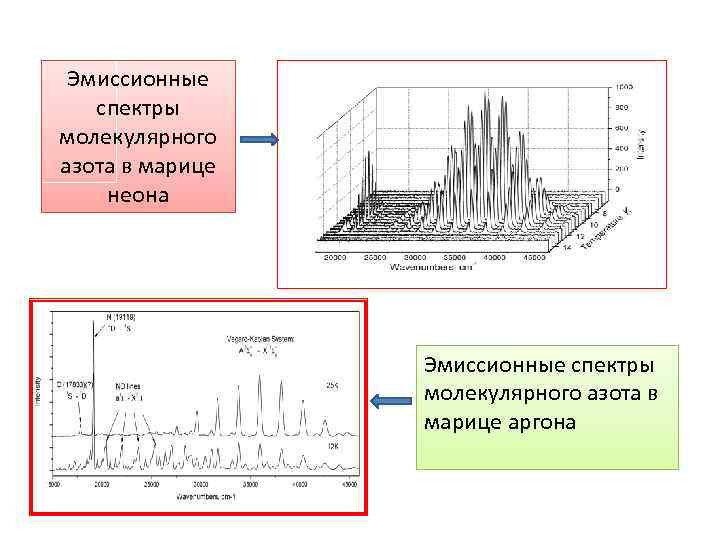 Эмиссионные спектры молекулярного азота в марице неона Эмиссионные спектры молекулярного азота в марице аргона
Эмиссионные спектры молекулярного азота в марице неона Эмиссионные спектры молекулярного азота в марице аргона
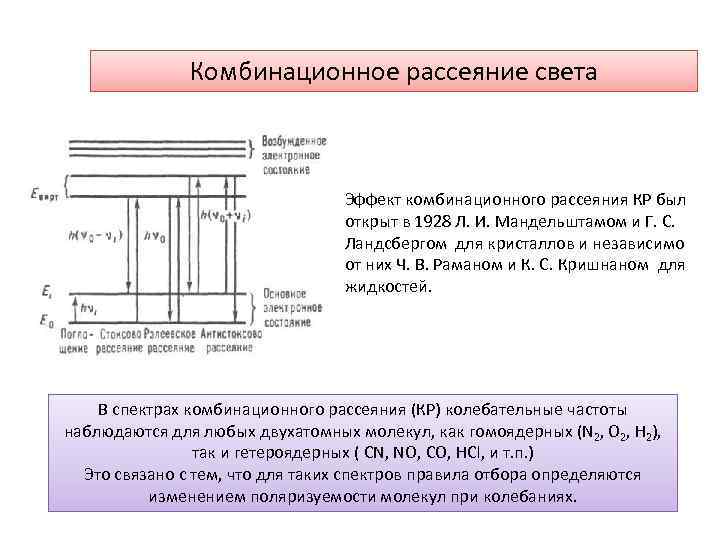 Комбинационное рассеяние света Эффект комбинационного рассеяния КР был открыт в 1928 Л. И. Мандельштамом и Г. С. Ландсбергом для кристаллов и независимо от них Ч. В. Раманом и К. С. Кришнаном для жидкостей. В спектрах комбинационного рассеяния (КР) колебательные частоты наблюдаются для любых двухатомных молекул, как гомоядерных (N 2, O 2, H 2), так и гетероядерных ( CN, NO, CO, HCl, и т. п. ) Это связано с тем, что для таких спектров правила отбора определяются изменением поляризуемости молекул при колебаниях.
Комбинационное рассеяние света Эффект комбинационного рассеяния КР был открыт в 1928 Л. И. Мандельштамом и Г. С. Ландсбергом для кристаллов и независимо от них Ч. В. Раманом и К. С. Кришнаном для жидкостей. В спектрах комбинационного рассеяния (КР) колебательные частоты наблюдаются для любых двухатомных молекул, как гомоядерных (N 2, O 2, H 2), так и гетероядерных ( CN, NO, CO, HCl, и т. п. ) Это связано с тем, что для таких спектров правила отбора определяются изменением поляризуемости молекул при колебаниях.
 Некоторые применения колебательной спектроскопии • Колебательные спектры позволяют изучать не только внутримолекулярную динамику, но и межмолекулярные взаимодействия. Из них получают данные о поверхностях потенциальной энергии, вращении молекул, движении атомов с большими амплитудами. • По колебательным спектрам исследуют ассоциацию молекул и структуру комплексов различной природы. • Колебательные спектры зависят от агрегатного состояния вещества, что позволяет получать информацию о структуре различных фаз конденсированного состояния.
Некоторые применения колебательной спектроскопии • Колебательные спектры позволяют изучать не только внутримолекулярную динамику, но и межмолекулярные взаимодействия. Из них получают данные о поверхностях потенциальной энергии, вращении молекул, движении атомов с большими амплитудами. • По колебательным спектрам исследуют ассоциацию молекул и структуру комплексов различной природы. • Колебательные спектры зависят от агрегатного состояния вещества, что позволяет получать информацию о структуре различных фаз конденсированного состояния.
 Электронно-колебательная спектроскопия применяется для исследования строения молекул веществ в газовой и жидкой фазах с низким давлением насыщенных паров, а также в твердой фазе. Благодаря тому, что метод электронно-колебательной спектроскопии исследует переходы между различными электронными уровнями, в то время как в колебательной спектроскопии ИК или КР исследуются колебательные переходы с одного и того же уровня, то становится возможным исследование переходов, не наблюдаемых в обычных ИК или КР-спектрах, запрещенных правилами отбора для колебательных переходов, но не запрещенных правилами отбора для электронноколебательных спектров.
Электронно-колебательная спектроскопия применяется для исследования строения молекул веществ в газовой и жидкой фазах с низким давлением насыщенных паров, а также в твердой фазе. Благодаря тому, что метод электронно-колебательной спектроскопии исследует переходы между различными электронными уровнями, в то время как в колебательной спектроскопии ИК или КР исследуются колебательные переходы с одного и того же уровня, то становится возможным исследование переходов, не наблюдаемых в обычных ИК или КР-спектрах, запрещенных правилами отбора для колебательных переходов, но не запрещенных правилами отбора для электронноколебательных спектров.
 Электронно-колебательные спектры Научное открытие "Явление возникновения линейчатых спектров вещества". Формула открытия: "Установлено неизвестное ранее явление возникновения линейчатых молекулярных спектров вещества в условиях матричной изоляции молекул или их групп в растворителе при низкой температуре". Авторы: Э. В. Шпольский, Л. А. Климова, А. А. Ильина. Номер и дата приоритета: № 152 от 28 сентября 1952 г. Исследовались спектры сложных органических молекулв н-парафиновых матрицах Открытое явление широко используется для высокочувствительного и селективного качественного и количественного спектрального анализа. Метод линейчатых спектров дает возможность определять сверхмалые (до 10– 11 граммов на грамм образца) количества индивидуальных веществ, одновременно присутствующих в сложной смеси, что ставит его вне конкуренции с другими спектральными методами.
Электронно-колебательные спектры Научное открытие "Явление возникновения линейчатых спектров вещества". Формула открытия: "Установлено неизвестное ранее явление возникновения линейчатых молекулярных спектров вещества в условиях матричной изоляции молекул или их групп в растворителе при низкой температуре". Авторы: Э. В. Шпольский, Л. А. Климова, А. А. Ильина. Номер и дата приоритета: № 152 от 28 сентября 1952 г. Исследовались спектры сложных органических молекулв н-парафиновых матрицах Открытое явление широко используется для высокочувствительного и селективного качественного и количественного спектрального анализа. Метод линейчатых спектров дает возможность определять сверхмалые (до 10– 11 граммов на грамм образца) количества индивидуальных веществ, одновременно присутствующих в сложной смеси, что ставит его вне конкуренции с другими спектральными методами.
 Матричная изоляция Техника матричной изоляции различных соединений в низкотемпературных химически инертных матрицах была развита в 1950 -х годах Дж. Пименталом. В качестве матриц использовались отвердевшие газы – инертные (Xe, Kr, Ar, Ne) и твердый азот N 2. Дальнейшее развитие низкотемпературной техники позволило развернуть исследования в квантовых матрицах – твердом водороде H 2 и жидком гелии He. Если на начальном этапе исследования были сфокусированы на характеризации примесных центров, то в настоящее время акцент сместился на взаимодействие примесных центров с матрицей и исследование эффектов, присущих конденсированной фазе. http: //www. chem. mun. ca/mi/mide. php
Матричная изоляция Техника матричной изоляции различных соединений в низкотемпературных химически инертных матрицах была развита в 1950 -х годах Дж. Пименталом. В качестве матриц использовались отвердевшие газы – инертные (Xe, Kr, Ar, Ne) и твердый азот N 2. Дальнейшее развитие низкотемпературной техники позволило развернуть исследования в квантовых матрицах – твердом водороде H 2 и жидком гелии He. Если на начальном этапе исследования были сфокусированы на характеризации примесных центров, то в настоящее время акцент сместился на взаимодействие примесных центров с матрицей и исследование эффектов, присущих конденсированной фазе. http: //www. chem. mun. ca/mi/mide. php
 Литература: 1. М. А. Ельяшевич, Атомная и молекулярная спектроскопия, Физ-мат Гиз, Москва, 1962. 2. Г. Герцберг, Спектры и строение двухатомных молекул, Издательство иностранной литературы, Москва, 1949. 3. http: //www. xumuk. ru 4. Ian R. Dunkin, Matrix Isolation Techniques: A Practical Approach, Oxford University Press, UK, 1998. 5. Physics and Chemistry at Low Temperatures, Leonid Khriachtchev, Ed. , Pan Stanford Publishing, 2011.
Литература: 1. М. А. Ельяшевич, Атомная и молекулярная спектроскопия, Физ-мат Гиз, Москва, 1962. 2. Г. Герцберг, Спектры и строение двухатомных молекул, Издательство иностранной литературы, Москва, 1949. 3. http: //www. xumuk. ru 4. Ian R. Dunkin, Matrix Isolation Techniques: A Practical Approach, Oxford University Press, UK, 1998. 5. Physics and Chemistry at Low Temperatures, Leonid Khriachtchev, Ed. , Pan Stanford Publishing, 2011.


