Физич материал.ppt
- Количество слайдов: 97
 Физическое материаловедение. Часть 1.
Физическое материаловедение. Часть 1.
 Лекция 1. Введение. • Традиционным способом получения конденсированного состояния является кристаллизация из расплава. Для рассмотрения результатов сплавления элементов друг с другом необходимы некоторые обобщения данных о состоянии системы, в зависимости от ее параметров (состава, давления, объема и температуры). Такое обобщение можно сделать с помощью фазовых диаграмм состояния. Диаграммы состояния – это геометрическое изображение равновесных состояний системы при различных значениях параметров, определяющих эти состояния. • По диаграммам состояния (при соблюдении равновесных условий) можно определить фазовые и структурные составляющие сплавов при различных температурах, охарактеризовать их качественно и количественно, кроме того, можно проследить за фазовыми превращениями, происходящими при нагревании или охлаждении сплавов, прогнозировать свойства, получающиеся при этих превращениях, а также изменение свойств, если превращения будут происходить в неравновесных условиях.
Лекция 1. Введение. • Традиционным способом получения конденсированного состояния является кристаллизация из расплава. Для рассмотрения результатов сплавления элементов друг с другом необходимы некоторые обобщения данных о состоянии системы, в зависимости от ее параметров (состава, давления, объема и температуры). Такое обобщение можно сделать с помощью фазовых диаграмм состояния. Диаграммы состояния – это геометрическое изображение равновесных состояний системы при различных значениях параметров, определяющих эти состояния. • По диаграммам состояния (при соблюдении равновесных условий) можно определить фазовые и структурные составляющие сплавов при различных температурах, охарактеризовать их качественно и количественно, кроме того, можно проследить за фазовыми превращениями, происходящими при нагревании или охлаждении сплавов, прогнозировать свойства, получающиеся при этих превращениях, а также изменение свойств, если превращения будут происходить в неравновесных условиях.
 1. Основы учения о фазовых равновесиях. 1. 1 Основные термодинамические понятия. Материальная система – часть пространства, заполненная веществом, которую выделяют для исследования, остальное окружающее пространство называют внешней средой. Система называется термодинамической, если между ее частями возможен обмен энергией; если возможен обмен и энергией, и веществом, то система называется физико - химической. Физико-химические системы, изучаемые в материаловедении – это или отдельный сплав заданного состава, или совокупность бесконечно большого числа сплавов, образованных данными металлами и (или) неметаллами. Системы могут быть гомогенными (состоящими из одной фазы) и гетерогенными (состоящими из нескольких фаз).
1. Основы учения о фазовых равновесиях. 1. 1 Основные термодинамические понятия. Материальная система – часть пространства, заполненная веществом, которую выделяют для исследования, остальное окружающее пространство называют внешней средой. Система называется термодинамической, если между ее частями возможен обмен энергией; если возможен обмен и энергией, и веществом, то система называется физико - химической. Физико-химические системы, изучаемые в материаловедении – это или отдельный сплав заданного состава, или совокупность бесконечно большого числа сплавов, образованных данными металлами и (или) неметаллами. Системы могут быть гомогенными (состоящими из одной фазы) и гетерогенными (состоящими из нескольких фаз).
 Фаза — это однородная часть системы или совокупность частей, имеющих одинаковый состав, строение и физикохимические свойства. Разные фазы всегда отделены друг от друга поверхностями раздела (межфазными поверхностями). Химический состав каждой фазы в сплаве можно выразить через концентрации компонентов. Компонентами называют независимые индивидуальные вещества, наименьшее число которых достаточно для образования всех фаз системы. Компоненты могут переходить из одной фазы в другую, но не могут переходить друг в друга. Компонентами в металлических сплавах обычно являются чистые металлы и неметаллы, а также химические соединения
Фаза — это однородная часть системы или совокупность частей, имеющих одинаковый состав, строение и физикохимические свойства. Разные фазы всегда отделены друг от друга поверхностями раздела (межфазными поверхностями). Химический состав каждой фазы в сплаве можно выразить через концентрации компонентов. Компонентами называют независимые индивидуальные вещества, наименьшее число которых достаточно для образования всех фаз системы. Компоненты могут переходить из одной фазы в другую, но не могут переходить друг в друга. Компонентами в металлических сплавах обычно являются чистые металлы и неметаллы, а также химические соединения
 1. 2 Правило фаз Гиббса Состояние системы определяется температурой, давлением, концентрацией компонентов в разных фазах. При изменении этих факторов система переходит из одного состояния в другое, при этом совершаются фазовые превращения, при которых появляются новые фазы или исчезают старые. Возможность изменения равновесного состояния системы определяется вариантностью или числом степеней свободы. Число факторов, которые могут изменяться независимо друг от друга, без нарушения равновесия системы, называется числом степеней свободы. Вариантность системы зависит от числа компонентов, числа равновесных фаз и количества внешних переменных. Эта зависимость была получена в 1876 г. Гиббсом и носит название правила фаз Гиббса.
1. 2 Правило фаз Гиббса Состояние системы определяется температурой, давлением, концентрацией компонентов в разных фазах. При изменении этих факторов система переходит из одного состояния в другое, при этом совершаются фазовые превращения, при которых появляются новые фазы или исчезают старые. Возможность изменения равновесного состояния системы определяется вариантностью или числом степеней свободы. Число факторов, которые могут изменяться независимо друг от друга, без нарушения равновесия системы, называется числом степеней свободы. Вариантность системы зависит от числа компонентов, числа равновесных фаз и количества внешних переменных. Эта зависимость была получена в 1876 г. Гиббсом и носит название правила фаз Гиббса.
 Рассмотрим систему, содержащую К компонентов, в которой образуется Ф фаз. Внешними переменными являются температура и давление. Пусть каждая фаза содержит все К компонентов. В качестве переменных, определяющих состояние системы, выступают концентрации всех компонентов во всех фазах. Число таких КФ. С учетом внешних переменных, КФ + 2. переменных будет равно произведению переменных, получаем общее число Пусть при любой температуре все фазы находятся в равновесии друг с другом. Это возможно при равенстве химических потенциалов компонентов во всех фазах, т. е. химический потенциал каждого компонента одинаков во всех фазах.
Рассмотрим систему, содержащую К компонентов, в которой образуется Ф фаз. Внешними переменными являются температура и давление. Пусть каждая фаза содержит все К компонентов. В качестве переменных, определяющих состояние системы, выступают концентрации всех компонентов во всех фазах. Число таких КФ. С учетом внешних переменных, КФ + 2. переменных будет равно произведению переменных, получаем общее число Пусть при любой температуре все фазы находятся в равновесии друг с другом. Это возможно при равенстве химических потенциалов компонентов во всех фазах, т. е. химический потенциал каждого компонента одинаков во всех фазах.
 Это условие можно записать в виде следующих равенств: где – химический потенциал, верхний индекс – номер компонента, нижний индекс– номер фазы. В каждой строке равенства (1) (Ф– 1) самостоятельных уравнений, число строк К, всего таких уравнений будет К(Ф– 1). К ним следует добавить еще Ф уравнений, связывающих концентрации всех равно компонентов во всех фазах. Следовательно, общее число уравнений, связывающих все переменные будет (Ф– 1)К+Ф
Это условие можно записать в виде следующих равенств: где – химический потенциал, верхний индекс – номер компонента, нижний индекс– номер фазы. В каждой строке равенства (1) (Ф– 1) самостоятельных уравнений, число строк К, всего таких уравнений будет К(Ф– 1). К ним следует добавить еще Ф уравнений, связывающих концентрации всех равно компонентов во всех фазах. Следовательно, общее число уравнений, связывающих все переменные будет (Ф– 1)К+Ф
 Если число переменных больше числа связывающих их уравнений, то не все переменные являются независимыми. Число независимых переменных определяется как разность общего числа переменных и числа уравнений, т. е. f = КФ + 2 – ((Ф – 1)К + Ф) = К – Ф + 2 (2) Выражение (2), определяющее вариантность системы, – правило фаз Гиббса, f - число степеней свободы системы. На практике процессы идут при постоянном давлении, поэтому правило фаз Гиббса запишется в виде: f = К– Ф + 1. Если f = 0 (система называется нонвариантной), то все независимые переменные, определяющие состояние системы, имеют строго фиксированные (единственные) значения, которые нельзя изменить, не нарушив фазового равновесия системы. Наличие одной, двух или большего числа степеней свободы позволяет независимо изменять одну, две или большее число переменных без изменения числа фаз, находящихся в равновесии. Диаграммы состояния (фазовые диаграммы)
Если число переменных больше числа связывающих их уравнений, то не все переменные являются независимыми. Число независимых переменных определяется как разность общего числа переменных и числа уравнений, т. е. f = КФ + 2 – ((Ф – 1)К + Ф) = К – Ф + 2 (2) Выражение (2), определяющее вариантность системы, – правило фаз Гиббса, f - число степеней свободы системы. На практике процессы идут при постоянном давлении, поэтому правило фаз Гиббса запишется в виде: f = К– Ф + 1. Если f = 0 (система называется нонвариантной), то все независимые переменные, определяющие состояние системы, имеют строго фиксированные (единственные) значения, которые нельзя изменить, не нарушив фазового равновесия системы. Наличие одной, двух или большего числа степеней свободы позволяет независимо изменять одну, две или большее число переменных без изменения числа фаз, находящихся в равновесии. Диаграммы состояния (фазовые диаграммы)
 1. 3 Методы построения диаграмм состояния Диаграммы состояния – это геометрическое изображение равновесных состояний системы при различных значениях параметров, определяющих эти состояния. Суть всех методов построения диаграмм состояния сводится к нахождению критических точек – температур, при которых происходят фазовые превращения. Для нахождения критических точек проводится изучение зависимости различных физических свойств от температуры (при фиксированном составе сплава) или от состава (при фиксированной температуре). Началу фазового превращения соответствует резкий перегиб на зависимости изучаемого свойства. Обычно для построения диаграмм используются в комплексе несколько методов. Для построения диаграмм можно использовать расчетный метод термодинамического анализа, основанный на изучении зависимости свободной энергии системы от температуры, давления, концентрации всех компонентов во всех фазах.
1. 3 Методы построения диаграмм состояния Диаграммы состояния – это геометрическое изображение равновесных состояний системы при различных значениях параметров, определяющих эти состояния. Суть всех методов построения диаграмм состояния сводится к нахождению критических точек – температур, при которых происходят фазовые превращения. Для нахождения критических точек проводится изучение зависимости различных физических свойств от температуры (при фиксированном составе сплава) или от состава (при фиксированной температуре). Началу фазового превращения соответствует резкий перегиб на зависимости изучаемого свойства. Обычно для построения диаграмм используются в комплексе несколько методов. Для построения диаграмм можно использовать расчетный метод термодинамического анализа, основанный на изучении зависимости свободной энергии системы от температуры, давления, концентрации всех компонентов во всех фазах.
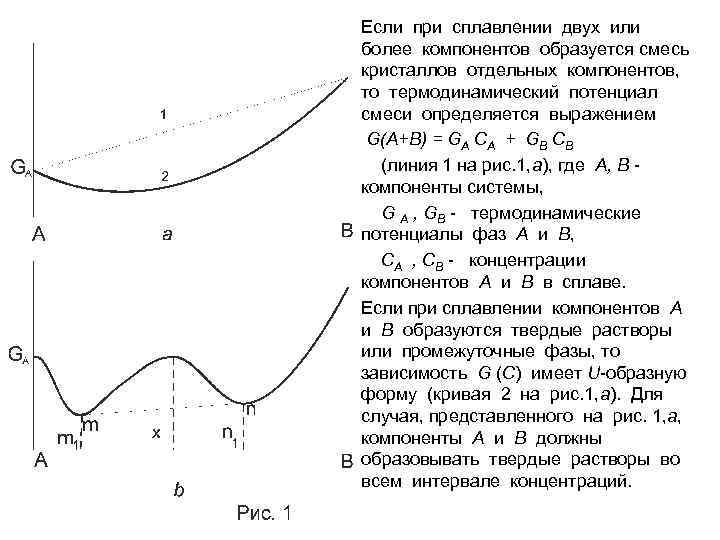 Если при сплавлении двух или более компонентов образуется смесь кристаллов отдельных компонентов, то термодинамический потенциал смеси определяется выражением G(A+B) = GA CA + GB CB (линия 1 на рис. 1, а), где А, В компоненты системы, G A , GB - термодинамические потенциалы фаз А и В, СA , СB - концентрации компонентов А и В в сплаве. Если при сплавлении компонентов А и В образуются твердые растворы или промежуточные фазы, то зависимость G (С) имеет U-образную форму (кривая 2 на рис. 1, а). Для случая, представленного на рис. 1, а, компоненты А и В должны образовывать твердые растворы во всем интервале концентраций.
Если при сплавлении двух или более компонентов образуется смесь кристаллов отдельных компонентов, то термодинамический потенциал смеси определяется выражением G(A+B) = GA CA + GB CB (линия 1 на рис. 1, а), где А, В компоненты системы, G A , GB - термодинамические потенциалы фаз А и В, СA , СB - концентрации компонентов А и В в сплаве. Если при сплавлении компонентов А и В образуются твердые растворы или промежуточные фазы, то зависимость G (С) имеет U-образную форму (кривая 2 на рис. 1, а). Для случая, представленного на рис. 1, а, компоненты А и В должны образовывать твердые растворы во всем интервале концентраций.
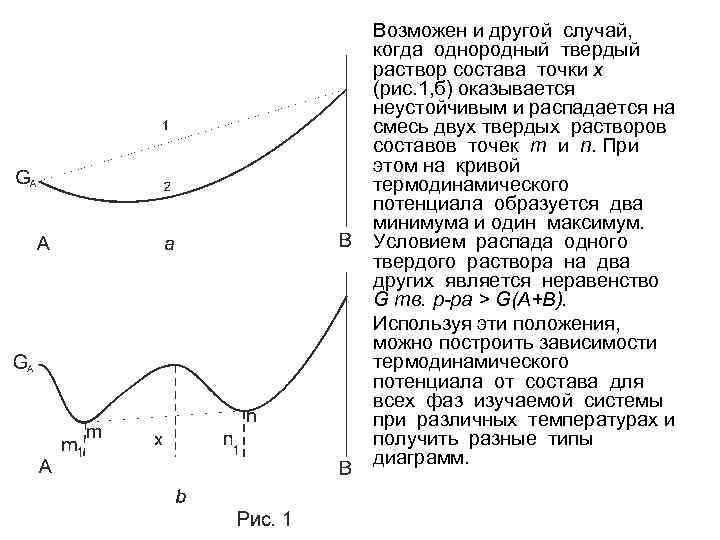 Возможен и другой случай, когда однородный твердый раствор состава точки х (рис. 1, б) оказывается неустойчивым и распадается на смесь двух твердых растворов составов точек m и n. При этом на кривой термодинамического потенциала образуется два минимума и один максимум. Условием распада одного твердого раствора на два других является неравенство G тв. р-ра > G(A+B). Используя эти положения, можно построить зависимости термодинамического потенциала от состава для всех фаз изучаемой системы при различных температурах и получить разные типы диаграмм.
Возможен и другой случай, когда однородный твердый раствор состава точки х (рис. 1, б) оказывается неустойчивым и распадается на смесь двух твердых растворов составов точек m и n. При этом на кривой термодинамического потенциала образуется два минимума и один максимум. Условием распада одного твердого раствора на два других является неравенство G тв. р-ра > G(A+B). Используя эти положения, можно построить зависимости термодинамического потенциала от состава для всех фаз изучаемой системы при различных температурах и получить разные типы диаграмм.
 Обычно диаграммы изображаются в координатах состав– температура(рис. 2, д). По горизонтальной оси определяют концентрации компонентов в сплавах, а также в фазах, из которых эти сплавы могут состоять. Отсчет концентрации чаще всего проводят в процентах (атомных или по массе). Для перехода от % по массе к % атомным пользуются соотношением: PA=CA 100/MA/(CA/MA+(100 -CA)/MB), где РA и СA – концентрации компонента А, % ат. и % по массе, соответственно. М A и МB – атомные массы компонентов А и В. Для обратного перехода служит соотношение: СA = РA МA 100 / (РA+ (100 - РA) МB). Точка А соответствует 100% компонента А, точка В – 100% компонента В. На вертикальных осях, идущих от точек А и В, отмечают температуры плавления ТA и ТB чистых компонентов. Любая точка на диаграмме, называемая фигуративной, характеризует состояние сплава заданного состава при определенной температуре.
Обычно диаграммы изображаются в координатах состав– температура(рис. 2, д). По горизонтальной оси определяют концентрации компонентов в сплавах, а также в фазах, из которых эти сплавы могут состоять. Отсчет концентрации чаще всего проводят в процентах (атомных или по массе). Для перехода от % по массе к % атомным пользуются соотношением: PA=CA 100/MA/(CA/MA+(100 -CA)/MB), где РA и СA – концентрации компонента А, % ат. и % по массе, соответственно. М A и МB – атомные массы компонентов А и В. Для обратного перехода служит соотношение: СA = РA МA 100 / (РA+ (100 - РA) МB). Точка А соответствует 100% компонента А, точка В – 100% компонента В. На вертикальных осях, идущих от точек А и В, отмечают температуры плавления ТA и ТB чистых компонентов. Любая точка на диаграмме, называемая фигуративной, характеризует состояние сплава заданного состава при определенной температуре.
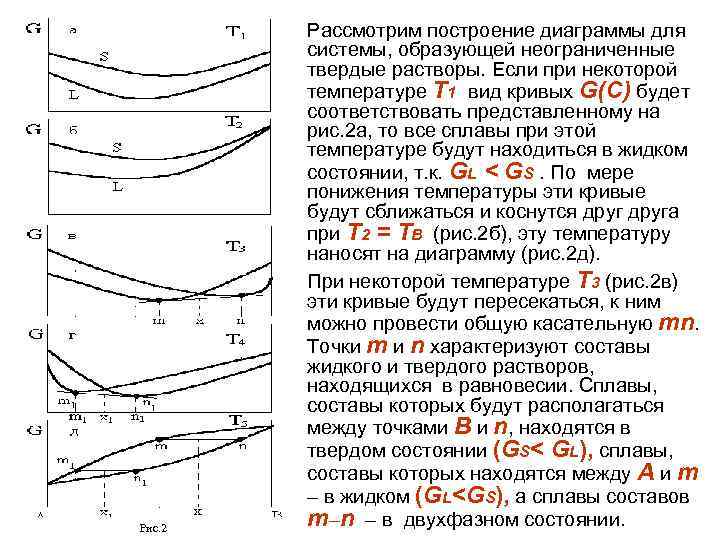 Рис. 2 Рассмотрим построение диаграммы для системы, образующей неограниченные твердые растворы. Если при некоторой температуре Т 1 вид кривых G(С) будет соответствовать представленному на рис. 2 а, то все сплавы при этой температуре будут находиться в жидком состоянии, т. к. GL < GS. По мере понижения температуры эти кривые будут сближаться и коснутся друга при Т 2 = ТB (рис. 2 б), эту температуру наносят на диаграмму (рис. 2 д). При некоторой температуре Т 3 (рис. 2 в) эти кривые будут пересекаться, к ним можно провести общую касательную mn. Точки m и n характеризуют составы жидкого и твердого растворов, находящихся в равновесии. Сплавы, составы которых будут располагаться между точками В и n, находятся в твердом состоянии (GS< GL), сплавы, составы которых находятся между А и m – в жидком (GL
Рис. 2 Рассмотрим построение диаграммы для системы, образующей неограниченные твердые растворы. Если при некоторой температуре Т 1 вид кривых G(С) будет соответствовать представленному на рис. 2 а, то все сплавы при этой температуре будут находиться в жидком состоянии, т. к. GL < GS. По мере понижения температуры эти кривые будут сближаться и коснутся друга при Т 2 = ТB (рис. 2 б), эту температуру наносят на диаграмму (рис. 2 д). При некоторой температуре Т 3 (рис. 2 в) эти кривые будут пересекаться, к ним можно провести общую касательную mn. Точки m и n характеризуют составы жидкого и твердого растворов, находящихся в равновесии. Сплавы, составы которых будут располагаться между точками В и n, находятся в твердом состоянии (GS< GL), сплавы, составы которых находятся между А и m – в жидком (GL
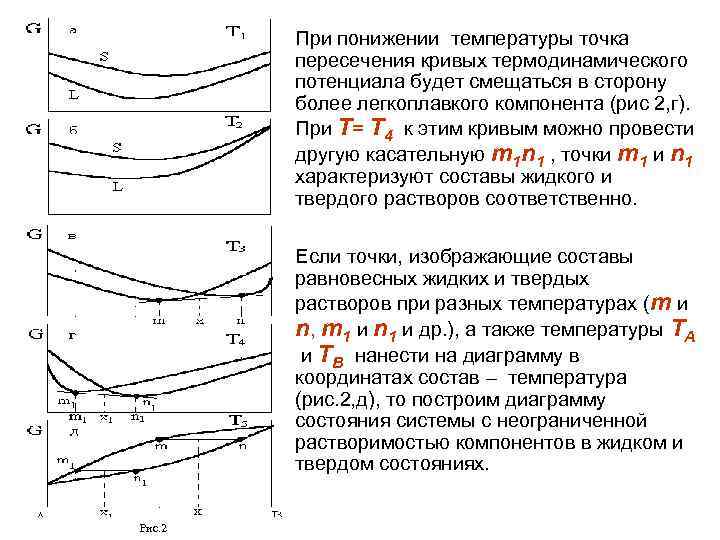 При понижении температуры точка пересечения кривых термодинамического потенциала будет смещаться в сторону более легкоплавкого компонента (рис 2, г). При Т= Т 4 к этим кривым можно провести другую касательную m 1 n 1 , точки m 1 и n 1 характеризуют составы жидкого и твердого растворов соответственно. Если точки, изображающие составы равновесных жидких и твердых растворов при разных температурах (m и n, m 1 и n 1 и др. ), а также температуры ТA и ТВ нанести на диаграмму в координатах состав – температура (рис. 2, д), то построим диаграмму состояния системы с неограниченной растворимостью компонентов в жидком и твердом состояниях. Рис. 2
При понижении температуры точка пересечения кривых термодинамического потенциала будет смещаться в сторону более легкоплавкого компонента (рис 2, г). При Т= Т 4 к этим кривым можно провести другую касательную m 1 n 1 , точки m 1 и n 1 характеризуют составы жидкого и твердого растворов соответственно. Если точки, изображающие составы равновесных жидких и твердых растворов при разных температурах (m и n, m 1 и n 1 и др. ), а также температуры ТA и ТВ нанести на диаграмму в координатах состав – температура (рис. 2, д), то построим диаграмму состояния системы с неограниченной растворимостью компонентов в жидком и твердом состояниях. Рис. 2
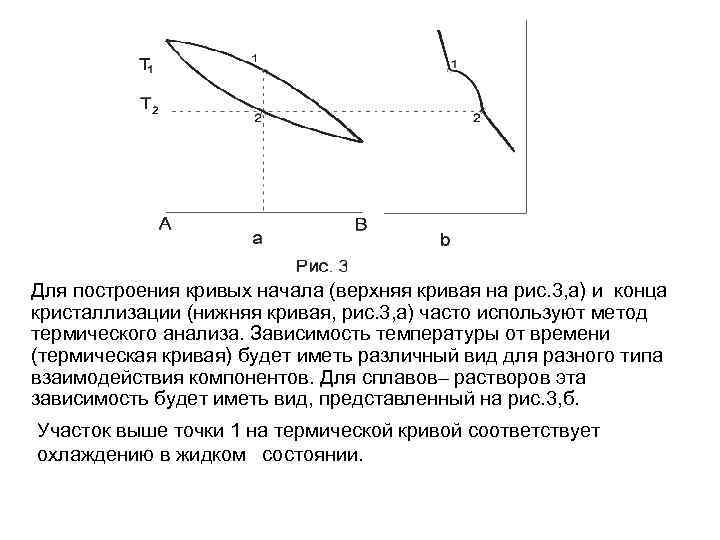 Для построения кривых начала (верхняя кривая на рис. 3, а) и конца кристаллизации (нижняя кривая, рис. 3, а) часто используют метод термического анализа. Зависимость температуры от времени (термическая кривая) будет иметь различный вид для разного типа взаимодействия компонентов. Для сплавов– растворов эта зависимость будет иметь вид, представленный на рис. 3, б. Участок выше точки 1 на термической кривой соответствует охлаждению в жидком состоянии.
Для построения кривых начала (верхняя кривая на рис. 3, а) и конца кристаллизации (нижняя кривая, рис. 3, а) часто используют метод термического анализа. Зависимость температуры от времени (термическая кривая) будет иметь различный вид для разного типа взаимодействия компонентов. Для сплавов– растворов эта зависимость будет иметь вид, представленный на рис. 3, б. Участок выше точки 1 на термической кривой соответствует охлаждению в жидком состоянии.
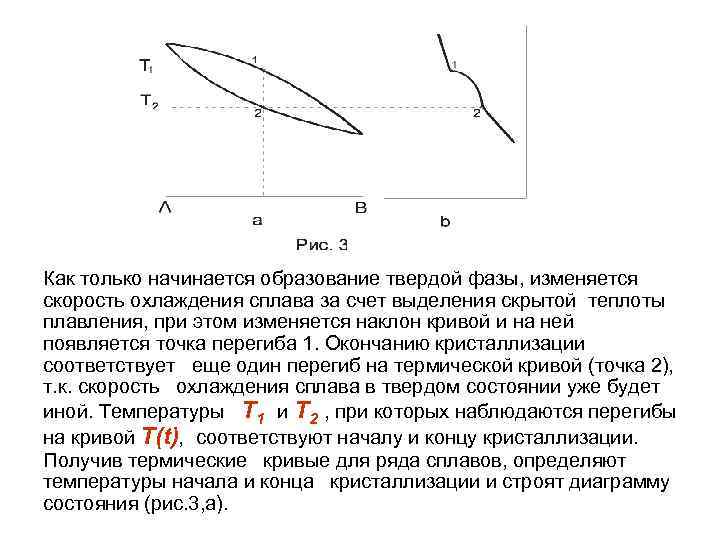 Как только начинается образование твердой фазы, изменяется скорость охлаждения сплава за счет выделения скрытой теплоты плавления, при этом изменяется наклон кривой и на ней появляется точка перегиба 1. Окончанию кристаллизации соответствует еще один перегиб на термической кривой (точка 2), т. к. скорость охлаждения сплава в твердом состоянии уже будет иной. Температуры Т 1 и Т 2 , при которых наблюдаются перегибы на кривой Т(t), соответствуют началу и концу кристаллизации. Получив термические кривые для ряда сплавов, определяют температуры начала и конца кристаллизации и строят диаграмму состояния (рис. 3, а).
Как только начинается образование твердой фазы, изменяется скорость охлаждения сплава за счет выделения скрытой теплоты плавления, при этом изменяется наклон кривой и на ней появляется точка перегиба 1. Окончанию кристаллизации соответствует еще один перегиб на термической кривой (точка 2), т. к. скорость охлаждения сплава в твердом состоянии уже будет иной. Температуры Т 1 и Т 2 , при которых наблюдаются перегибы на кривой Т(t), соответствуют началу и концу кристаллизации. Получив термические кривые для ряда сплавов, определяют температуры начала и конца кристаллизации и строят диаграмму состояния (рис. 3, а).
 • Лекция 2. 2. ФИЗИЧЕСКАЯ ПРИРОДА ФАЗ В ТВЕРДОМ СОСТОЯНИИ. 2. 1. . Твердые растворы. Твердыми растворами называются такие фазы, в которых атомы одного или нескольких компонентов располагаются в кристаллической решетке другого, не изменяя ее типа. Компонент, решетка которого сохраняется, называется растворителем, а остальные – примесью или растворенными элементами. В зависимости от того как располагаются атомы примеси в решетке растворителя, различают три типа твердых растворов: замещения, внедрения и вычитания.
• Лекция 2. 2. ФИЗИЧЕСКАЯ ПРИРОДА ФАЗ В ТВЕРДОМ СОСТОЯНИИ. 2. 1. . Твердые растворы. Твердыми растворами называются такие фазы, в которых атомы одного или нескольких компонентов располагаются в кристаллической решетке другого, не изменяя ее типа. Компонент, решетка которого сохраняется, называется растворителем, а остальные – примесью или растворенными элементами. В зависимости от того как располагаются атомы примеси в решетке растворителя, различают три типа твердых растворов: замещения, внедрения и вычитания.
 Рис. 4 В твердых растворах замещения атомы растворенного элемента замещают атомы растворителя в узлах кристаллической решетки, распределяясь, чаще всего, хаотическинеупорядоченные твердые растворы (рис. 4). При этом растворителем может быть химический элемент (металл), а также химическое соединение. В твердых растворах между химическими соединениями ионы одного сорта замещаются ионами другого сорта, например, в системе Na. Cl – KCl ионы калия замещают ионы натрия.
Рис. 4 В твердых растворах замещения атомы растворенного элемента замещают атомы растворителя в узлах кристаллической решетки, распределяясь, чаще всего, хаотическинеупорядоченные твердые растворы (рис. 4). При этом растворителем может быть химический элемент (металл), а также химическое соединение. В твердых растворах между химическими соединениями ионы одного сорта замещаются ионами другого сорта, например, в системе Na. Cl – KCl ионы калия замещают ионы натрия.
 Рис. 5 В твердых растворах внедрения атомы примеси располагаются в междоузлиях кристаллической решетки растворителя (рис. 5). Растворы типа внедрения чаще всего образуются при растворении элементов с малыми атомными радиусами ( водород, углерод, азот, бор и др. ) в металлах переходной группы (например, раствор углерода в железе). Положение атома внедрения в междоузлии устойчиво, если радиус внедренного атома достаточно мал, чтобы не слишком смещать окружающие его атомы металла, и достаточно велик, чтобы с ними соприкасаться. Растворы этого типа существуют и на базе химических соединений (раствор никеля в Ni. Sb).
Рис. 5 В твердых растворах внедрения атомы примеси располагаются в междоузлиях кристаллической решетки растворителя (рис. 5). Растворы типа внедрения чаще всего образуются при растворении элементов с малыми атомными радиусами ( водород, углерод, азот, бор и др. ) в металлах переходной группы (например, раствор углерода в железе). Положение атома внедрения в междоузлии устойчиво, если радиус внедренного атома достаточно мал, чтобы не слишком смещать окружающие его атомы металла, и достаточно велик, чтобы с ними соприкасаться. Растворы этого типа существуют и на базе химических соединений (раствор никеля в Ni. Sb).
 Рис. 6 Твердые растворы вычитания (растворы с дефектной решеткой) образуются на основе химических соединений. Типичным примером является раствор кислорода в соединении Fe. O (рис. 6) Все позиции, в которых должны находиться ионы кислорода, заняты, а часть позиций, которые должны быть заняты ионами железа, – вакантны. Дефектной может быть как металлическая подрешетка, так и неметаллическая, например в оксидах титана, содержащих от 38 до 56 атомных процентов кислорода. В кристаллах с максимальным содержанием титана (Ti. O 0, 6) все дефекты находятся в кислородной подрешетке, с уменьшением содержания титана уменьшается общее число дефектов, и они распределяются между обеими подрешетками. У оксида с максимальным содержанием кислорода все дефекты находятся в титановой подрешетке.
Рис. 6 Твердые растворы вычитания (растворы с дефектной решеткой) образуются на основе химических соединений. Типичным примером является раствор кислорода в соединении Fe. O (рис. 6) Все позиции, в которых должны находиться ионы кислорода, заняты, а часть позиций, которые должны быть заняты ионами железа, – вакантны. Дефектной может быть как металлическая подрешетка, так и неметаллическая, например в оксидах титана, содержащих от 38 до 56 атомных процентов кислорода. В кристаллах с максимальным содержанием титана (Ti. O 0, 6) все дефекты находятся в кислородной подрешетке, с уменьшением содержания титана уменьшается общее число дефектов, и они распределяются между обеими подрешетками. У оксида с максимальным содержанием кислорода все дефекты находятся в титановой подрешетке.
 Независимо от типа твердого раствора, все они имеют атомарный характер, т. е. в узлах кристаллической решетки располагаются атомы или ионы, но не молекулы. Поскольку атомы растворителя и растворенного элемента имеют разные радиусы, то кристаллическая решетка твердого раствора замещения будет искажена. Еще большие искажения возникают при образовании растворов внедрения и вычитания. Тип твердого раствора можно определить, сравнивая число атомов n, приходящихся на элементарную ячейку раствора, с числом атомов n 0 в ячейке растворителя. Если n=n 0, то твердый раствор построен по типу замещения, при n>n 0 – по типу внедрения и при n
Независимо от типа твердого раствора, все они имеют атомарный характер, т. е. в узлах кристаллической решетки располагаются атомы или ионы, но не молекулы. Поскольку атомы растворителя и растворенного элемента имеют разные радиусы, то кристаллическая решетка твердого раствора замещения будет искажена. Еще большие искажения возникают при образовании растворов внедрения и вычитания. Тип твердого раствора можно определить, сравнивая число атомов n, приходящихся на элементарную ячейку раствора, с числом атомов n 0 в ячейке растворителя. Если n=n 0, то твердый раствор построен по типу замещения, при n>n 0 – по типу внедрения и при n
 Закон Вегарда Первоначальные исследования позволили заключить, что параметр элементарной ячейки в зависимости от концентрации примеси меняется по линейному закону – закону Вегарда: a = a 1 + (a 2 – a 1) C , где а 1 – параметр элементарной ячейки растворителя, а 2 – параметр элементарной ячейки растворенного элемента, С – концентрация растворенного элемента. Более поздние исследования показали, что зависимость параметра от концентрации является более сложной и изображается, как правило, монотонными кривыми линиями без максимумов и минимумов. При образовании твердых растворов внедрения и вычитания примесь растворяется в ограниченном количестве, для твердых растворов замещения возможна как ограниченная, так и неограниченная растворимость элементов друге.
Закон Вегарда Первоначальные исследования позволили заключить, что параметр элементарной ячейки в зависимости от концентрации примеси меняется по линейному закону – закону Вегарда: a = a 1 + (a 2 – a 1) C , где а 1 – параметр элементарной ячейки растворителя, а 2 – параметр элементарной ячейки растворенного элемента, С – концентрация растворенного элемента. Более поздние исследования показали, что зависимость параметра от концентрации является более сложной и изображается, как правило, монотонными кривыми линиями без максимумов и минимумов. При образовании твердых растворов внедрения и вычитания примесь растворяется в ограниченном количестве, для твердых растворов замещения возможна как ограниченная, так и неограниченная растворимость элементов друге.
 ЛЕКЦИЯ 3. 2. 2. ПРОМЕЖУТОЧНЫЕ ФАЗЫ. Очень большое число фаз по своей природе являются промежуточными между химическими соединениями и твердыми растворами. Эти фазы часто называют металлическими соединениями [1, 3] , так как при их образовании возникают металлические или преимущественно металлические связи. Многие из этих соединений имеют структуру, характерную для металлов: кубическую объемноцентрированную, гранецентрированную или гексагональную плотноупакованную. Промежуточные фазы образуют обычно элементы, расположенные в разных подгруппах таблицы Менделеева, т. е. отличающиеся друг от друга электронным строением и физико– химическими свойствами.
ЛЕКЦИЯ 3. 2. 2. ПРОМЕЖУТОЧНЫЕ ФАЗЫ. Очень большое число фаз по своей природе являются промежуточными между химическими соединениями и твердыми растворами. Эти фазы часто называют металлическими соединениями [1, 3] , так как при их образовании возникают металлические или преимущественно металлические связи. Многие из этих соединений имеют структуру, характерную для металлов: кубическую объемноцентрированную, гранецентрированную или гексагональную плотноупакованную. Промежуточные фазы образуют обычно элементы, расположенные в разных подгруппах таблицы Менделеева, т. е. отличающиеся друг от друга электронным строением и физико– химическими свойствами.
 Электронные соединения (фазы Юм–Розери) образуются в сплавах металлов первой группы и некоторых переходных металлов с элементами II–V групп таблицы Менделеева. Кристаллическая структура этих соединений зависит от электронной концентрации, равной отношению числа валентных электронов к числу атомов. Найдено четыре типа электронных соединений: –, – и 1– фазы. Предельные электронные концентрации, при которых устойчивы эти соединения, равны: 3/2 для – и 1– фаз, 21/13 для – фаз и 7/4 для –фаз. Фазы в неупорядоченном состоянии имеют объемноцентрированную кубическую решетку, фазы – сложную кубическую решетку, элементарная ячейка которой содержит 52 атома, –фазы – гексагональную плотноупакованную и 1 –фазы – кубическую решетку с 20 атомами в элементарной ячейке. Большинство электронных соединений – фазы переменного состава с широкими областями гомогенности.
Электронные соединения (фазы Юм–Розери) образуются в сплавах металлов первой группы и некоторых переходных металлов с элементами II–V групп таблицы Менделеева. Кристаллическая структура этих соединений зависит от электронной концентрации, равной отношению числа валентных электронов к числу атомов. Найдено четыре типа электронных соединений: –, – и 1– фазы. Предельные электронные концентрации, при которых устойчивы эти соединения, равны: 3/2 для – и 1– фаз, 21/13 для – фаз и 7/4 для –фаз. Фазы в неупорядоченном состоянии имеют объемноцентрированную кубическую решетку, фазы – сложную кубическую решетку, элементарная ячейка которой содержит 52 атома, –фазы – гексагональную плотноупакованную и 1 –фазы – кубическую решетку с 20 атомами в элементарной ячейке. Большинство электронных соединений – фазы переменного состава с широкими областями гомогенности.
 Фазы внедрения возникают при взаимодействии атомов неметаллов малых размеров – водорода, бора, углерода, азота с переходными металлами. Определяющим является размерный фактор: эти фазы образуются, если выполняется соотношение rх/rме 0, 59 (rх и rме – атомные радиусы неметалла и металла соответственно). Фазы внедрения могут иметь одну из следующих решеток: гранецентрированную кубическую, объемноцентрированную кубическую, гексагональную плотноупакованную или простую гексагональную. При этом атомы металла размещаются в узлах решетки, а атомы неметалла – в междоузлиях. Составы фаз внедрения обычно близки к составам типа Ме. Х, Ме 2 Х, Ме 4 Х, Ме. Х 2. Несмотря на высокое содержание неметалла, структура и свойства этих фаз определяются сохранением в них металлической связи. Позднее высказывались предположения о ковалентной связи металл-неметалл.
Фазы внедрения возникают при взаимодействии атомов неметаллов малых размеров – водорода, бора, углерода, азота с переходными металлами. Определяющим является размерный фактор: эти фазы образуются, если выполняется соотношение rх/rме 0, 59 (rх и rме – атомные радиусы неметалла и металла соответственно). Фазы внедрения могут иметь одну из следующих решеток: гранецентрированную кубическую, объемноцентрированную кубическую, гексагональную плотноупакованную или простую гексагональную. При этом атомы металла размещаются в узлах решетки, а атомы неметалла – в междоузлиях. Составы фаз внедрения обычно близки к составам типа Ме. Х, Ме 2 Х, Ме 4 Х, Ме. Х 2. Несмотря на высокое содержание неметалла, структура и свойства этих фаз определяются сохранением в них металлической связи. Позднее высказывались предположения о ковалентной связи металл-неметалл.
 Фазы Лавеса – интерметаллические соединения постоянного состава, который можно описать формулой AB 2. Они имеют плотноупакованную структуру типа Mg. Cu 2, Mg. Ni 2 или Mg. Zn 2. Решетка Mg. Cu 2 – кубическая гранецентрированная с чередованием слоев. . . АВСАВС. . . , а у Mg. Ni 2 и Mg. Zn 2 – гексагональная плотноупакованная с чередованием слоев. . . АВАС. . . для Mg. Ni 2 и. . . АВАВ. . . для Mg. Zn 2. Области гомогенности фаз Лавеса узки. Определяющим фактором при их образовании является размерный фактор: r. A/ r. B = 1, 1 – 1, 6. Наиболее стабильны фазы, у которых отношение атомных радиусов близко к 1, 225 , так как при таком отношении реализуется плотнейшая упаковка. Компонентами фаз Лавеса могут быть металлы из любой группы таблицы Менделеева, причем один и тот же металл в различных фазах может выступать в роли компонента А или В, например магний в соединениях Mg. Cu 2 и Ca. Mg 2.
Фазы Лавеса – интерметаллические соединения постоянного состава, который можно описать формулой AB 2. Они имеют плотноупакованную структуру типа Mg. Cu 2, Mg. Ni 2 или Mg. Zn 2. Решетка Mg. Cu 2 – кубическая гранецентрированная с чередованием слоев. . . АВСАВС. . . , а у Mg. Ni 2 и Mg. Zn 2 – гексагональная плотноупакованная с чередованием слоев. . . АВАС. . . для Mg. Ni 2 и. . . АВАВ. . . для Mg. Zn 2. Области гомогенности фаз Лавеса узки. Определяющим фактором при их образовании является размерный фактор: r. A/ r. B = 1, 1 – 1, 6. Наиболее стабильны фазы, у которых отношение атомных радиусов близко к 1, 225 , так как при таком отношении реализуется плотнейшая упаковка. Компонентами фаз Лавеса могут быть металлы из любой группы таблицы Менделеева, причем один и тот же металл в различных фазах может выступать в роли компонента А или В, например магний в соединениях Mg. Cu 2 и Ca. Mg 2.
 –фазы – фазы переменного состава, которые возникают при взаимодействии переходных металлов при разности атомных радиусов не более 8%. Эти фазы имеют сложную тетрагональную решетку с 30 атомами на элементарную ячейку. Область гомогенности –фаз в двойных системах может быть довольно широкой. Экспериментальные данные показывают, что на процесс образования и стабилизации – фаз оказывает влияние как размерный фактор, так и электронный, причем в одних случаях преобладает первый в других – второй.
–фазы – фазы переменного состава, которые возникают при взаимодействии переходных металлов при разности атомных радиусов не более 8%. Эти фазы имеют сложную тетрагональную решетку с 30 атомами на элементарную ячейку. Область гомогенности –фаз в двойных системах может быть довольно широкой. Экспериментальные данные показывают, что на процесс образования и стабилизации – фаз оказывает влияние как размерный фактор, так и электронный, причем в одних случаях преобладает первый в других – второй.
 2. 3. Химические соединения Наиболее простым типом химических соединений являются соединения с нормальной валентностью, которые образуются при взаимодействии типичных металлов и элементов, обладающих и металлическими, и неметаллическими свойствами. Часто химические соединения относят к промежуточным фазам [2, 3]. Характерными особенностями соединений с нормальной валентностью являются: –постоянство состава или очень узкие области гомогенности; –состав описывается стехиометрическими формулами, подчиняющимися правилам химической валентности (Mg. Si, Mg. Sb 2, Mg. Te); –наличие нового типа решетки, отличного от типа решеток компонентов, образующих это соединение; –ярко выраженные индивидуальные свойства; –постоянство температуры кристаллизации.
2. 3. Химические соединения Наиболее простым типом химических соединений являются соединения с нормальной валентностью, которые образуются при взаимодействии типичных металлов и элементов, обладающих и металлическими, и неметаллическими свойствами. Часто химические соединения относят к промежуточным фазам [2, 3]. Характерными особенностями соединений с нормальной валентностью являются: –постоянство состава или очень узкие области гомогенности; –состав описывается стехиометрическими формулами, подчиняющимися правилам химической валентности (Mg. Si, Mg. Sb 2, Mg. Te); –наличие нового типа решетки, отличного от типа решеток компонентов, образующих это соединение; –ярко выраженные индивидуальные свойства; –постоянство температуры кристаллизации.
 ЛЕКЦИЯ 4 3. ОСНОВНЫЕ ТИПЫ ДИАГРАММ СОСТОЯНИЯ Реальные диаграммы состояния подчас являются очень сложными , поэтому имеет смысл начать рассмотрение с отдельных типов диаграмм. В основу их классификации можно положить признак образования тех или иных фаз в твердом состоянии: твердых растворов с неограниченной и ограниченной растворимостью компонентов, промежуточных фаз, химических соединений.
ЛЕКЦИЯ 4 3. ОСНОВНЫЕ ТИПЫ ДИАГРАММ СОСТОЯНИЯ Реальные диаграммы состояния подчас являются очень сложными , поэтому имеет смысл начать рассмотрение с отдельных типов диаграмм. В основу их классификации можно положить признак образования тех или иных фаз в твердом состоянии: твердых растворов с неограниченной и ограниченной растворимостью компонентов, промежуточных фаз, химических соединений.
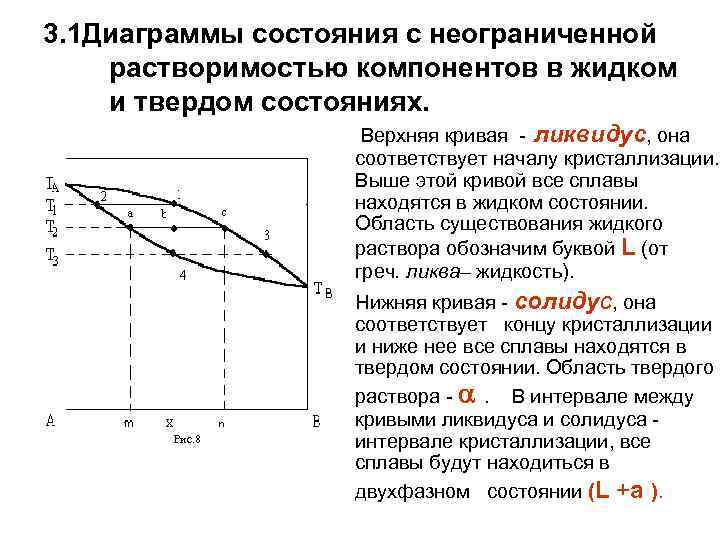 3. 1 Диаграммы состояния с неограниченной растворимостью компонентов в жидком и твердом состояниях. Верхняя кривая - ликвидус, она соответствует началу кристаллизации. Выше этой кривой все сплавы находятся в жидком состоянии. Область существования жидкого раствора обозначим буквой L (от греч. ликва– жидкость). Рис. 8 Нижняя кривая - солидус, она соответствует концу кристаллизации и ниже нее все сплавы находятся в твердом состоянии. Область твердого раствора - . В интервале между кривыми ликвидуса и солидуса интервале кристаллизации, все сплавы будут находиться в двухфазном состоянии (L +a ).
3. 1 Диаграммы состояния с неограниченной растворимостью компонентов в жидком и твердом состояниях. Верхняя кривая - ликвидус, она соответствует началу кристаллизации. Выше этой кривой все сплавы находятся в жидком состоянии. Область существования жидкого раствора обозначим буквой L (от греч. ликва– жидкость). Рис. 8 Нижняя кривая - солидус, она соответствует концу кристаллизации и ниже нее все сплавы находятся в твердом состоянии. Область твердого раствора - . В интервале между кривыми ликвидуса и солидуса интервале кристаллизации, все сплавы будут находиться в двухфазном состоянии (L +a ).
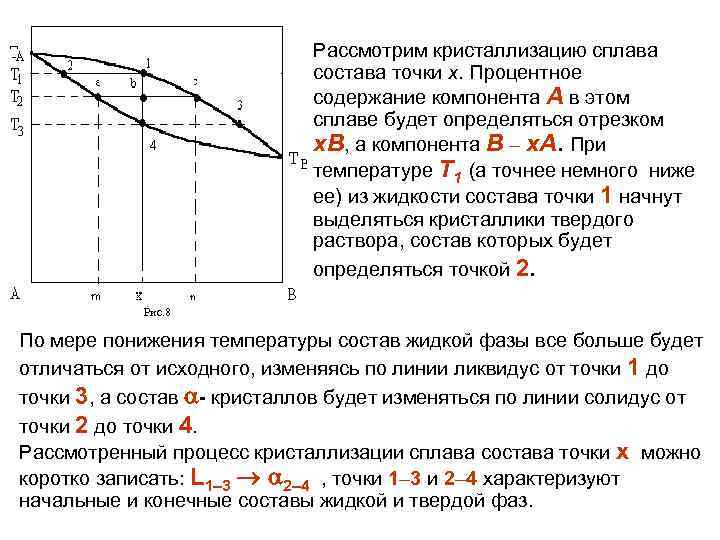 Рассмотрим кристаллизацию сплава состава точки х. Процентное содержание компонента А в этом сплаве будет определяться отрезком х. В, а компонента В – х. А. При температуре Т 1 (а точнее немного ниже ее) из жидкости состава точки 1 начнут выделяться кристаллики твердого раствора, состав которых будет определяться точкой 2. Рис. 8 По мере понижения температуры состав жидкой фазы все больше будет отличаться от исходного, изменяясь по линии ликвидус от точки 1 до точки 3, а состав - кристаллов будет изменяться по линии солидус от точки 2 до точки 4. Рассмотренный процесс кристаллизации сплава состава точки х можно коротко записать: L 1– 3 2– 4 , точки 1– 3 и 2– 4 характеризуют начальные и конечные составы жидкой и твердой фаз.
Рассмотрим кристаллизацию сплава состава точки х. Процентное содержание компонента А в этом сплаве будет определяться отрезком х. В, а компонента В – х. А. При температуре Т 1 (а точнее немного ниже ее) из жидкости состава точки 1 начнут выделяться кристаллики твердого раствора, состав которых будет определяться точкой 2. Рис. 8 По мере понижения температуры состав жидкой фазы все больше будет отличаться от исходного, изменяясь по линии ликвидус от точки 1 до точки 3, а состав - кристаллов будет изменяться по линии солидус от точки 2 до точки 4. Рассмотренный процесс кристаллизации сплава состава точки х можно коротко записать: L 1– 3 2– 4 , точки 1– 3 и 2– 4 характеризуют начальные и конечные составы жидкой и твердой фаз.
 Следует отметить, что когда говорится об изменении составов жидкого и твердого растворов, то подразумевается, что по кривой ликвидус изменяет свой состав вся жидкость, а по кривой солидус все кристаллы, т. е. в обеих равновесных фазах должна происходить диффузия, выравнивающая состав во всем объеме фазы. В реальных условиях в твердой фазе состав не успевает выравниваться и внутренние области каждого кристалла (зерна) будут обогащены более тугоплавким компонентом, а периферийные области (границы зерен) менее тугоплавким. Химическая неоднородность по объему зерна называется внутрикристаллической (или междендритной) ликвацией. Избавиться от ликвации в процессе кристаллизации не удается. Для выравнивания химического состава закристаллизовавшихся сплавов проводят гомогенизирующий отжиг (гомогенизацию). Эта процедура заключается в длительной (сотни часов) выдержке сплавов при температуре на 30 — 50 O ниже линии солидус.
Следует отметить, что когда говорится об изменении составов жидкого и твердого растворов, то подразумевается, что по кривой ликвидус изменяет свой состав вся жидкость, а по кривой солидус все кристаллы, т. е. в обеих равновесных фазах должна происходить диффузия, выравнивающая состав во всем объеме фазы. В реальных условиях в твердой фазе состав не успевает выравниваться и внутренние области каждого кристалла (зерна) будут обогащены более тугоплавким компонентом, а периферийные области (границы зерен) менее тугоплавким. Химическая неоднородность по объему зерна называется внутрикристаллической (или междендритной) ликвацией. Избавиться от ликвации в процессе кристаллизации не удается. Для выравнивания химического состава закристаллизовавшихся сплавов проводят гомогенизирующий отжиг (гомогенизацию). Эта процедура заключается в длительной (сотни часов) выдержке сплавов при температуре на 30 — 50 O ниже линии солидус.
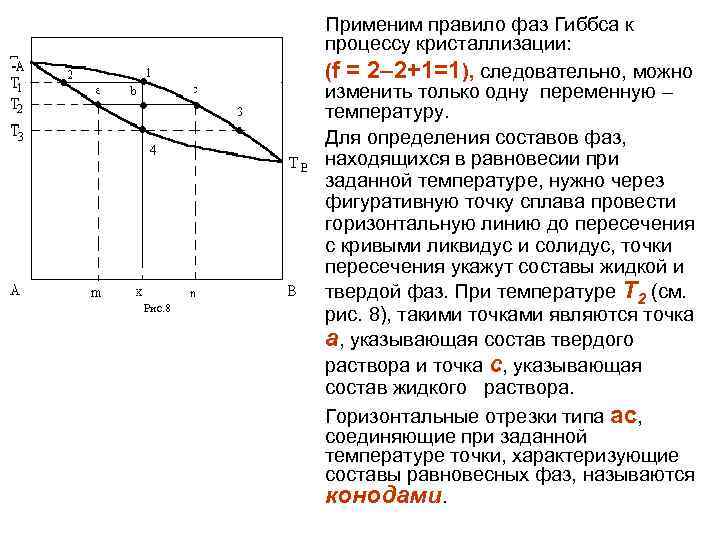 Рис. 8 Применим правило фаз Гиббса к процессу кристаллизации: (f = 2– 2+1=1), следовательно, можно изменить только одну переменную – температуру. Для определения составов фаз, находящихся в равновесии при заданной температуре, нужно через фигуративную точку сплава провести горизонтальную линию до пересечения с кривыми ликвидус и солидус, точки пересечения укажут составы жидкой и твердой фаз. При температуре Т 2 (см. рис. 8), такими точками являются точка а, указывающая состав твердого раствора и точка с, указывающая состав жидкого раствора. Горизонтальные отрезки типа ас, соединяющие при заданной температуре точки, характеризующие составы равновесных фаз, называются конодами.
Рис. 8 Применим правило фаз Гиббса к процессу кристаллизации: (f = 2– 2+1=1), следовательно, можно изменить только одну переменную – температуру. Для определения составов фаз, находящихся в равновесии при заданной температуре, нужно через фигуративную точку сплава провести горизонтальную линию до пересечения с кривыми ликвидус и солидус, точки пересечения укажут составы жидкой и твердой фаз. При температуре Т 2 (см. рис. 8), такими точками являются точка а, указывающая состав твердого раствора и точка с, указывающая состав жидкого раствора. Горизонтальные отрезки типа ас, соединяющие при заданной температуре точки, характеризующие составы равновесных фаз, называются конодами.
 Правило рычага. По конодам, используя правило рычага, можно определить относительное количество фаз, находящихся в равновесии: М =bc/ac, МL=ab/ac (4) Соотношения (4), позволяющие определить относительные количества равновесных фаз, носят названия правила рычага или правила отрезков. Умножив правые части (4) на 100%, или общую массу сплава М получим относительные количества фаз, выраженные в процентах или в единицах массы. Обычно при определении количества фаз записывают лишь отношение отрезков.
Правило рычага. По конодам, используя правило рычага, можно определить относительное количество фаз, находящихся в равновесии: М =bc/ac, МL=ab/ac (4) Соотношения (4), позволяющие определить относительные количества равновесных фаз, носят названия правила рычага или правила отрезков. Умножив правые части (4) на 100%, или общую массу сплава М получим относительные количества фаз, выраженные в процентах или в единицах массы. Обычно при определении количества фаз записывают лишь отношение отрезков.
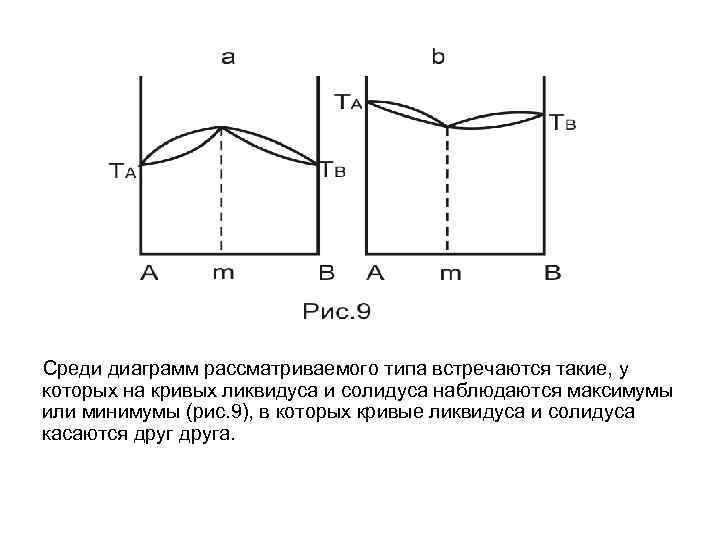 Среди диаграмм рассматриваемого типа встречаются такие, у которых на кривых ликвидуса и солидуса наблюдаются максимумы или минимумы (рис. 9), в которых кривые ликвидуса и солидуса касаются друга.
Среди диаграмм рассматриваемого типа встречаются такие, у которых на кривых ликвидуса и солидуса наблюдаются максимумы или минимумы (рис. 9), в которых кривые ликвидуса и солидуса касаются друга.
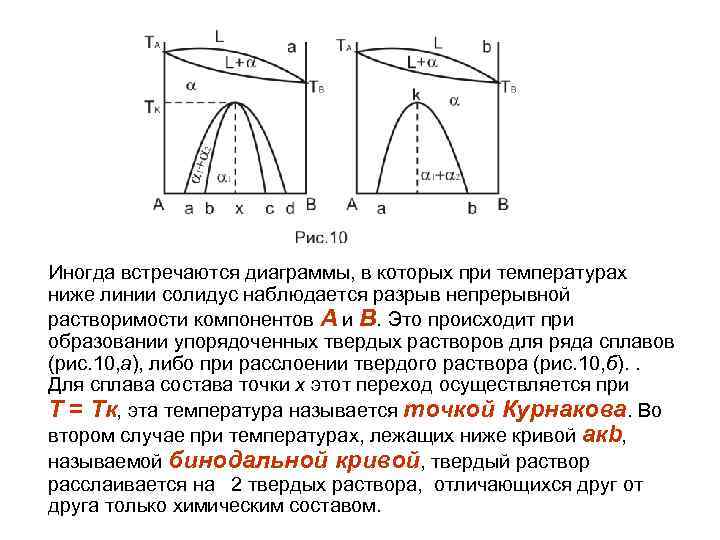 Иногда встречаются диаграммы, в которых при температурах ниже линии солидус наблюдается разрыв непрерывной растворимости компонентов А и В. Это происходит при образовании упорядоченных твердых растворов для ряда сплавов (рис. 10, а), либо при расслоении твердого раствора (рис. 10, б). . Для сплава состава точки х этот переход осуществляется при Т = Тк, эта температура называется точкой Курнакова. Во втором случае при температурах, лежащих ниже кривой акb, называемой бинодальной кривой, твердый раствор расслаивается на 2 твердых раствора, отличающихся друг от друга только химическим составом.
Иногда встречаются диаграммы, в которых при температурах ниже линии солидус наблюдается разрыв непрерывной растворимости компонентов А и В. Это происходит при образовании упорядоченных твердых растворов для ряда сплавов (рис. 10, а), либо при расслоении твердого раствора (рис. 10, б). . Для сплава состава точки х этот переход осуществляется при Т = Тк, эта температура называется точкой Курнакова. Во втором случае при температурах, лежащих ниже кривой акb, называемой бинодальной кривой, твердый раствор расслаивается на 2 твердых раствора, отличающихся друг от друга только химическим составом.
 3. 2 Диаграммы состояния с неограниченной растворимостью компонентов в жидком состоянии и ограниченной в твердом. Диаграммы этого типа являются наиболее распространенными. Растворы с ограниченной растворимостью называют граничными, они образуют диаграммы с эвтектическим или перитектическим равновесием. Если при добавлении одного компонента к другому наблюдается понижение температур начала и конца кристаллизации граничных твердых растворов, то такие компоненты образуют систему с эвтектикой (эвтектика с греч. – легко плавящаяся). Диаграмма с перитектическим равновесием характерна для случая, когда добавление компонента В к А понижает температуру начала и конца кристаллизации граничного твердого раствора, а добавление А к В повышает температуру начала и конца кристаллизации граничного твердого раствора .
3. 2 Диаграммы состояния с неограниченной растворимостью компонентов в жидком состоянии и ограниченной в твердом. Диаграммы этого типа являются наиболее распространенными. Растворы с ограниченной растворимостью называют граничными, они образуют диаграммы с эвтектическим или перитектическим равновесием. Если при добавлении одного компонента к другому наблюдается понижение температур начала и конца кристаллизации граничных твердых растворов, то такие компоненты образуют систему с эвтектикой (эвтектика с греч. – легко плавящаяся). Диаграмма с перитектическим равновесием характерна для случая, когда добавление компонента В к А понижает температуру начала и конца кристаллизации граничного твердого раствора, а добавление А к В повышает температуру начала и конца кристаллизации граничного твердого раствора .
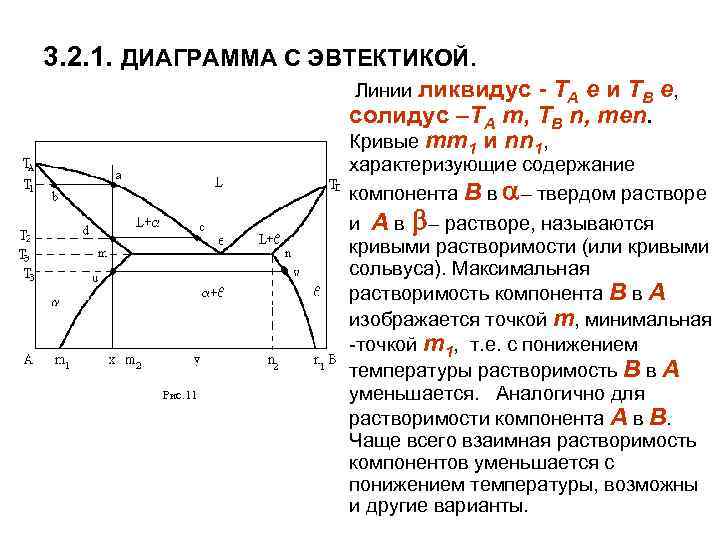 3. 2. 1. ДИАГРАММА С ЭВТЕКТИКОЙ. Линии ликвидус - ТА е и ТВ е, солидус –ТА m, ТВ n, men. Кривые mm 1 и nn 1, Рис. 11 характеризующие содержание компонента В в – твердом растворе и А в – растворе, называются кривыми растворимости (или кривыми сольвуса). Максимальная растворимость компонента В в А изображается точкой m, минимальная -точкой m 1, т. е. с понижением температуры растворимость В в А уменьшается. Аналогично для растворимости компонента А в В. Чаще всего взаимная растворимость компонентов уменьшается с понижением температуры, возможны и другие варианты.
3. 2. 1. ДИАГРАММА С ЭВТЕКТИКОЙ. Линии ликвидус - ТА е и ТВ е, солидус –ТА m, ТВ n, men. Кривые mm 1 и nn 1, Рис. 11 характеризующие содержание компонента В в – твердом растворе и А в – растворе, называются кривыми растворимости (или кривыми сольвуса). Максимальная растворимость компонента В в А изображается точкой m, минимальная -точкой m 1, т. е. с понижением температуры растворимость В в А уменьшается. Аналогично для растворимости компонента А в В. Чаще всего взаимная растворимость компонентов уменьшается с понижением температуры, возможны и другие варианты.
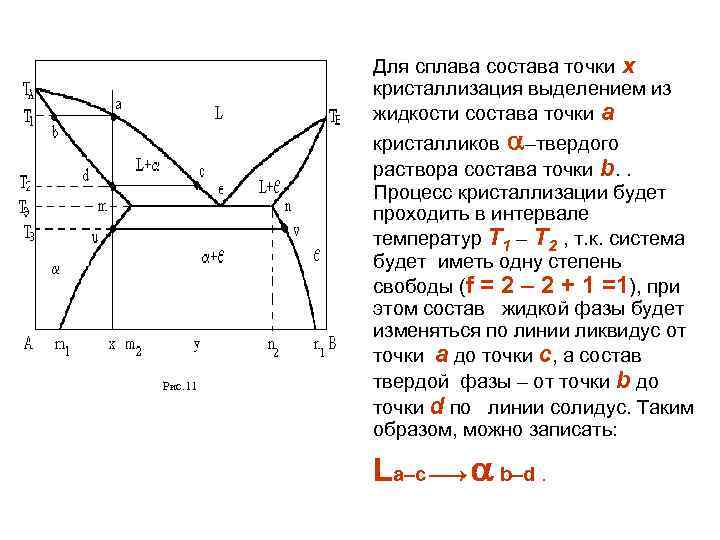 Рис. 11 Для сплава состава точки х кристаллизация выделением из жидкости состава точки а кристалликов –твердого раствора состава точки b. . Процесс кристаллизации будет проходить в интервале температур Т 1 – Т 2 , т. к. система будет иметь одну степень свободы (f = 2 – 2 + 1 =1), при этом состав жидкой фазы будет изменяться по линии ликвидус от точки а до точки с, а состав твердой фазы – от точки b до точки d по линии солидус. Таким образом, можно записать: La–c b–d.
Рис. 11 Для сплава состава точки х кристаллизация выделением из жидкости состава точки а кристалликов –твердого раствора состава точки b. . Процесс кристаллизации будет проходить в интервале температур Т 1 – Т 2 , т. к. система будет иметь одну степень свободы (f = 2 – 2 + 1 =1), при этом состав жидкой фазы будет изменяться по линии ликвидус от точки а до точки с, а состав твердой фазы – от точки b до точки d по линии солидус. Таким образом, можно записать: La–c b–d.
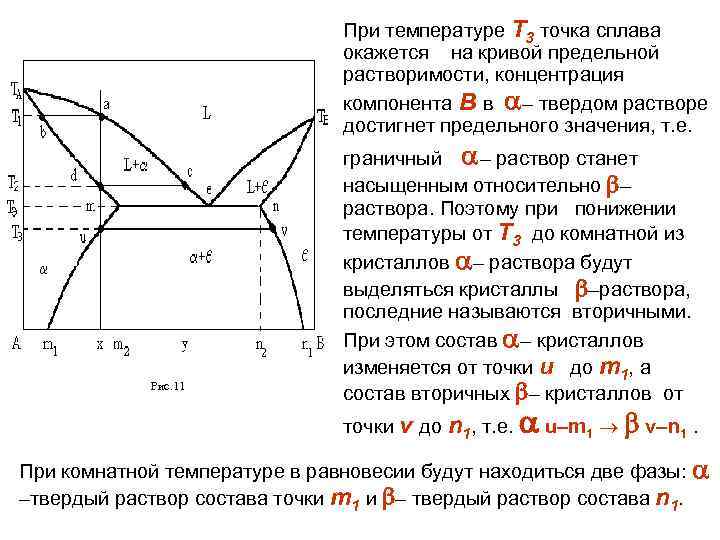 При температуре Т 3 точка сплава окажется на кривой предельной растворимости, концентрация компонента В в – твердом растворе достигнет предельного значения, т. е. Рис. 11 граничный – раствор станет насыщенным относительно – раствора. Поэтому при понижении температуры от Т 3 до комнатной из кристаллов – раствора будут выделяться кристаллы –раствора, последние называются вторичными. При этом состав – кристаллов изменяется от точки u до m 1, а состав вторичных – кристаллов от точки v до n 1, т. е. u–m 1 v–n 1. При комнатной температуре в равновесии будут находиться две фазы: –твердый раствор состава точки m 1 и – твердый раствор соcтава n 1.
При температуре Т 3 точка сплава окажется на кривой предельной растворимости, концентрация компонента В в – твердом растворе достигнет предельного значения, т. е. Рис. 11 граничный – раствор станет насыщенным относительно – раствора. Поэтому при понижении температуры от Т 3 до комнатной из кристаллов – раствора будут выделяться кристаллы –раствора, последние называются вторичными. При этом состав – кристаллов изменяется от точки u до m 1, а состав вторичных – кристаллов от точки v до n 1, т. е. u–m 1 v–n 1. При комнатной температуре в равновесии будут находиться две фазы: –твердый раствор состава точки m 1 и – твердый раствор соcтава n 1.
 Рис. 12 Под микроскопом в структуре этого сплава можно различить кристаллы двух видов или две структурные составляющие: первичные кристаллы – раствора и вторичные – кристаллы. Последние при медленном охлаждении выделяются в виде компактных частиц по границам первичных – кристаллов (рис. 12, а). При ускоренном охлаждении вторичные кристаллы могут выделяться не только по границам, но и внутри зерна, образуя характерную, видманштеттову структуру – игольчатые или пластинчатые выделения, ориентированные в каждом зерне в определенном кристаллографическом направлении (рис. 12, б). В дальнейшем под структурными составляющими будем понимать самостоятельные элементы микроструктуры сплавов, которые при рассмотрении под микроскопом при средних увеличениях имеют свое характерное строение. Понятие "фаза" и "структурная составляющая" могут совпадать, как в рассматриваемом сплаве, либо не совпадать.
Рис. 12 Под микроскопом в структуре этого сплава можно различить кристаллы двух видов или две структурные составляющие: первичные кристаллы – раствора и вторичные – кристаллы. Последние при медленном охлаждении выделяются в виде компактных частиц по границам первичных – кристаллов (рис. 12, а). При ускоренном охлаждении вторичные кристаллы могут выделяться не только по границам, но и внутри зерна, образуя характерную, видманштеттову структуру – игольчатые или пластинчатые выделения, ориентированные в каждом зерне в определенном кристаллографическом направлении (рис. 12, б). В дальнейшем под структурными составляющими будем понимать самостоятельные элементы микроструктуры сплавов, которые при рассмотрении под микроскопом при средних увеличениях имеют свое характерное строение. Понятие "фаза" и "структурная составляющая" могут совпадать, как в рассматриваемом сплаве, либо не совпадать.
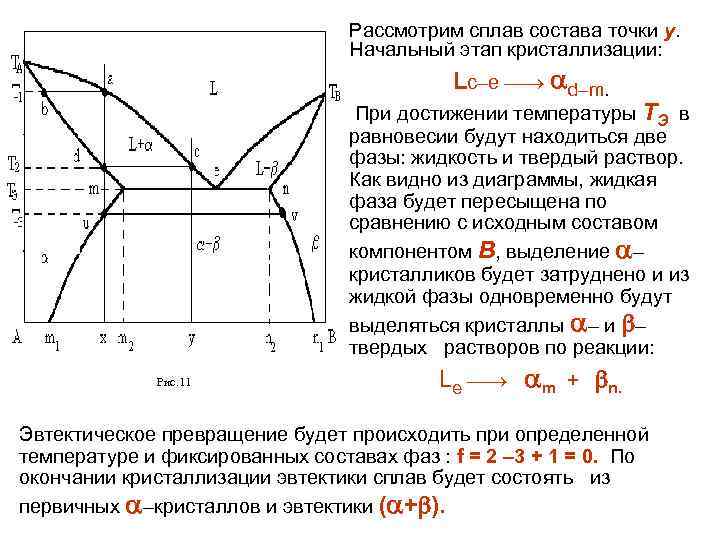 Рассмотрим сплав состава точки у. Начальный этап кристаллизации: Lc–e d–m. При достижении температуры ТЭ в равновесии будут находиться две фазы: жидкость и твердый раствор. Как видно из диаграммы, жидкая фаза будет пересыщена по сравнению с исходным составом компонентом В, выделение – кристалликов будет затруднено и из жидкой фазы одновременно будут выделяться кристаллы – и – твердых растворов по реакции: Рис. 11 Le m + n. Эвтектическое превращение будет происходить при определенной температуре и фиксированных составах фаз : f = 2 – 3 + 1 = 0. По окончании кристаллизации эвтектики сплав будет состоять из первичных –кристаллов и эвтектики ( + ).
Рассмотрим сплав состава точки у. Начальный этап кристаллизации: Lc–e d–m. При достижении температуры ТЭ в равновесии будут находиться две фазы: жидкость и твердый раствор. Как видно из диаграммы, жидкая фаза будет пересыщена по сравнению с исходным составом компонентом В, выделение – кристалликов будет затруднено и из жидкой фазы одновременно будут выделяться кристаллы – и – твердых растворов по реакции: Рис. 11 Le m + n. Эвтектическое превращение будет происходить при определенной температуре и фиксированных составах фаз : f = 2 – 3 + 1 = 0. По окончании кристаллизации эвтектики сплав будет состоять из первичных –кристаллов и эвтектики ( + ).
 Рис. 13 Рис. 14 Эвтектика представляет собой мелкодисперсную смесь чередующихся кристаллов – и – твердых растворов, имеющих чаще всего пластинчатую форму (рис. 13). Под микроскопом в структуре этого сплава можно увидеть три структурные составляющие: первичные – кристаллы, эвтектическую смесь ( + ) и вторичные – кристаллы внутри первичных. Вторичные кристаллы на фоне дисперсной эвтектической смеси обычно не заметны. Типичная микроструктура до – или заэвтектических сплавов представлена на рис. 14.
Рис. 13 Рис. 14 Эвтектика представляет собой мелкодисперсную смесь чередующихся кристаллов – и – твердых растворов, имеющих чаще всего пластинчатую форму (рис. 13). Под микроскопом в структуре этого сплава можно увидеть три структурные составляющие: первичные – кристаллы, эвтектическую смесь ( + ) и вторичные – кристаллы внутри первичных. Вторичные кристаллы на фоне дисперсной эвтектической смеси обычно не заметны. Типичная микроструктура до – или заэвтектических сплавов представлена на рис. 14.
 3. 2. 2. Диаграмма с перитектическим равновесием. • Линия ликвидус - ТАp. ТВ , линия солидус – ТА аb. ТВ. Точки аb и а 1 b 1 характеризуют предельную концентрацию компонентов В в – твердом растворе и А в – твердом растворе при температурах Т 1 и комнатной. Линии аа 1 и bb 1 – линии предельной растворимости, линия аbp – линия перитектического равновесия (линия перитектики), точка р – перитектическая точка. Перитектическая реакция, протекающая для сплавов составов а – р заключается во взаимодействии жидкости с ранее выпавшими кристаллами, в результате чего образуются кристаллы новой фазы: Lp+ a b
3. 2. 2. Диаграмма с перитектическим равновесием. • Линия ликвидус - ТАp. ТВ , линия солидус – ТА аb. ТВ. Точки аb и а 1 b 1 характеризуют предельную концентрацию компонентов В в – твердом растворе и А в – твердом растворе при температурах Т 1 и комнатной. Линии аа 1 и bb 1 – линии предельной растворимости, линия аbp – линия перитектического равновесия (линия перитектики), точка р – перитектическая точка. Перитектическая реакция, протекающая для сплавов составов а – р заключается во взаимодействии жидкости с ранее выпавшими кристаллами, в результате чего образуются кристаллы новой фазы: Lp+ a b
 Начальный этап кристаллизации сплава состава точки х запишется: Lc–p d–a. При температуре Т 2 , начнется перитектическая реакция: L p + a b. Температура сохраняется постоянной (f=2– 3+1=0). Заканчивается это превращение исчезновением одной из реагирующих фаз, в нашем случае исчезнет твердая фаза. Оставшаяся жидкость будет кристаллизоваться с образованием кристаллов – твердого раствора: Lp–s b–u. При понижении температуры точка сплава попадет на кривую растворимости (точка t). Из кристаллов –твердого раствора начнут выделяться вторичные – кристаллы. При комнатной температуре сплав будет двухфазным ( + ) и состоять из двух структурных составляющих: первичных – кристаллов и вторичных – кристаллов.
Начальный этап кристаллизации сплава состава точки х запишется: Lc–p d–a. При температуре Т 2 , начнется перитектическая реакция: L p + a b. Температура сохраняется постоянной (f=2– 3+1=0). Заканчивается это превращение исчезновением одной из реагирующих фаз, в нашем случае исчезнет твердая фаза. Оставшаяся жидкость будет кристаллизоваться с образованием кристаллов – твердого раствора: Lp–s b–u. При понижении температуры точка сплава попадет на кривую растворимости (точка t). Из кристаллов –твердого раствора начнут выделяться вторичные – кристаллы. При комнатной температуре сплав будет двухфазным ( + ) и состоять из двух структурных составляющих: первичных – кристаллов и вторичных – кристаллов.
 а б Рис. 16 Перитектика не имеет характерной структуры. Перитектическое превращение идет с образованием структуры двух типов. Кристаллы –фазы зарождаются на поверхности уже образовавшихся – кристаллов, окружая их сплошными ободками - структура окружения (рис. 16, а). Для роста новой фазы необходима диффузия обоих компонентов через –фазу. Структура окружения образуется в тех случаях, когда компоненты успевают продиффундировать через твердую фазу. В структуре окружения первичные кристаллы часто имеют зубчатые края. В структуре второго типа – кристаллы зарождаются в жидкости вдали от –кристаллов (рис. 16, б). В этом случае – кристаллы выделяются только из жидкости, а – кристаллы в ней растворяются.
а б Рис. 16 Перитектика не имеет характерной структуры. Перитектическое превращение идет с образованием структуры двух типов. Кристаллы –фазы зарождаются на поверхности уже образовавшихся – кристаллов, окружая их сплошными ободками - структура окружения (рис. 16, а). Для роста новой фазы необходима диффузия обоих компонентов через –фазу. Структура окружения образуется в тех случаях, когда компоненты успевают продиффундировать через твердую фазу. В структуре окружения первичные кристаллы часто имеют зубчатые края. В структуре второго типа – кристаллы зарождаются в жидкости вдали от –кристаллов (рис. 16, б). В этом случае – кристаллы выделяются только из жидкости, а – кристаллы в ней растворяются.
 ЛЕКЦИЯ 6 3. 3 Диаграммы состояния с промежуточными фазами Все твердые фазы, которые образуются в системе между граничными твердыми растворами, назовем промежуточными фазами. Промежуточные фазы могут иметь постоянный и переменный состав. Промежуточные фазы постоянного состава (химические соединения, фазы Лавеса, некоторые электронные соединения) на диаграмме изображаются вертикальными линиями (области гомогенности практически отсутствуют). Промежуточные фазы переменного состава (фазы внедрения, некоторые электронные соединения, –фазы и др. ) имеют сравнительно широкие области гомогенности. Эти фазы можно рассматривать как твердые растворы на базе определенных химических соединений.
ЛЕКЦИЯ 6 3. 3 Диаграммы состояния с промежуточными фазами Все твердые фазы, которые образуются в системе между граничными твердыми растворами, назовем промежуточными фазами. Промежуточные фазы могут иметь постоянный и переменный состав. Промежуточные фазы постоянного состава (химические соединения, фазы Лавеса, некоторые электронные соединения) на диаграмме изображаются вертикальными линиями (области гомогенности практически отсутствуют). Промежуточные фазы переменного состава (фазы внедрения, некоторые электронные соединения, –фазы и др. ) имеют сравнительно широкие области гомогенности. Эти фазы можно рассматривать как твердые растворы на базе определенных химических соединений.
 3. 3. 1. Диаграммы состояния систем с конгруэнтно плавящимися промежуточными соединениями. а б Рис. 17 Промежуточные фазы, при плавлении которых составы твердой и жидкой фаз совпадают, называются конгруэнтно плавящимися. Если промежуточная фаза является фазой постоянного состава, то вертикаль химического соединения Аm Вn делит всю диаграмму на две части, которые можно рассматривать как самостоятельные диаграммы (рис. 17, а). Если конгруэнтно плавящаяся промежуточная фаза является фазой переменного состава, то на диаграмме появляются области гомогенности (область фазы на рис. 17, б). Точка максимума m называется дистектической точкой (с греч. – трудно плавящийся, тугоплавкий).
3. 3. 1. Диаграммы состояния систем с конгруэнтно плавящимися промежуточными соединениями. а б Рис. 17 Промежуточные фазы, при плавлении которых составы твердой и жидкой фаз совпадают, называются конгруэнтно плавящимися. Если промежуточная фаза является фазой постоянного состава, то вертикаль химического соединения Аm Вn делит всю диаграмму на две части, которые можно рассматривать как самостоятельные диаграммы (рис. 17, а). Если конгруэнтно плавящаяся промежуточная фаза является фазой переменного состава, то на диаграмме появляются области гомогенности (область фазы на рис. 17, б). Точка максимума m называется дистектической точкой (с греч. – трудно плавящийся, тугоплавкий).
 3. 3. 2. Диаграммы состояния систем с инконгруэнтно плавящимися промежуточными фазами. а б Рис. 18 Промежуточные фазы, при плавлении которых состав образующейся жидкой фазы отличается от состава твердой фазы, называются инконгруэнтно плавящимися (инконгруэнтный – несовпадающий). химическое соединение Аm Вn (рис. 18, а) устойчиво до температуры перитектической реакции, а затем распадается по реакции Аm Вn Lp + В. Аналогично для – фазы (рис. 18, б) можно записать: m Lp + n.
3. 3. 2. Диаграммы состояния систем с инконгруэнтно плавящимися промежуточными фазами. а б Рис. 18 Промежуточные фазы, при плавлении которых состав образующейся жидкой фазы отличается от состава твердой фазы, называются инконгруэнтно плавящимися (инконгруэнтный – несовпадающий). химическое соединение Аm Вn (рис. 18, а) устойчиво до температуры перитектической реакции, а затем распадается по реакции Аm Вn Lp + В. Аналогично для – фазы (рис. 18, б) можно записать: m Lp + n.
 ЛЕКЦИЯ 7. 3. 4. Диаграммы состояния систем с превращениями в твердом состоянии. Превращения, протекающие в сплавах после затвердевания, могут привести к существенному изменению свойств материала. Наиболее важными являются полиморфные превращения, частичный распад твердого раствора за счет изменения взаимной растворимости компонентов, полный распад твердого раствора при эвтектоидном или перитектоидном превращениях.
ЛЕКЦИЯ 7. 3. 4. Диаграммы состояния систем с превращениями в твердом состоянии. Превращения, протекающие в сплавах после затвердевания, могут привести к существенному изменению свойств материала. Наиболее важными являются полиморфные превращения, частичный распад твердого раствора за счет изменения взаимной растворимости компонентов, полный распад твердого раствора при эвтектоидном или перитектоидном превращениях.
 3. 4. 1. Диаграммы состояния систем с полиморфными превращениями. Полиморфизм – способность простых и сложных веществ иметь различную кристаллическую структуру в зависимости от внешних условий температуры и давления. Различные кристаллические формы называются полиморфными модификациями, они обозначаются буквами греческого алфавита , , и т. д. Переход из одной полиморфной модификации в другую называется полиморфным превращением. Полиморфные превращения в чистых компонентах и фазах постоянного состава происходят при постоянной температуре в соответствии с правилом фаз Гиббса), а в твердых растворах или промежуточных фазах переменного состава– в интервале температур.
3. 4. 1. Диаграммы состояния систем с полиморфными превращениями. Полиморфизм – способность простых и сложных веществ иметь различную кристаллическую структуру в зависимости от внешних условий температуры и давления. Различные кристаллические формы называются полиморфными модификациями, они обозначаются буквами греческого алфавита , , и т. д. Переход из одной полиморфной модификации в другую называется полиморфным превращением. Полиморфные превращения в чистых компонентах и фазах постоянного состава происходят при постоянной температуре в соответствии с правилом фаз Гиббса), а в твердых растворах или промежуточных фазах переменного состава– в интервале температур.
 На диаграмме (рис. 19 а) чистый компонент А испытывает полиморфное превращение при температуре Т 1 , а сплавы – в интервале температур между линиями Т 1 n и Т 1 m. В сплаве состава точки х кристаллизация закончится образованием –твердого раствора, который сохраняется без изменения до температуры Т 1. При этой температуре в сплаве начинается полиморфное превращение по схеме Рис. 19 а a–c b–d. Превращение будет заключаться в образовании и росте зародышей со структурой – фазы, пока все – кристаллы не исчезнут. В сплавах составов А–m превращение протекает до конца, в сплавах составов m–n – частично, а в сплавах составов n–В полиморфное превращение отсутствует.
На диаграмме (рис. 19 а) чистый компонент А испытывает полиморфное превращение при температуре Т 1 , а сплавы – в интервале температур между линиями Т 1 n и Т 1 m. В сплаве состава точки х кристаллизация закончится образованием –твердого раствора, который сохраняется без изменения до температуры Т 1. При этой температуре в сплаве начинается полиморфное превращение по схеме Рис. 19 а a–c b–d. Превращение будет заключаться в образовании и росте зародышей со структурой – фазы, пока все – кристаллы не исчезнут. В сплавах составов А–m превращение протекает до конца, в сплавах составов m–n – частично, а в сплавах составов n–В полиморфное превращение отсутствует.
 Рис. 19 б На диаграмме (рис. 19 б) компонент А имеет три полиморфные модификации. Две из них (низко- и высокотемпературная) изоморфны другу и компоненту В и образуют с ним неограниченные твердые растворы. На основе промежуточной модификации компонента А образуется граничный твердый раствор, устойчивый в интервале температур Т 4 – Т 5. Область двухфазного равновесия ( + ) является замкнутой, поэтому в некоторых сплавах (напр. сплав х1 ) превращение идет дважды: вначале , затем , а в других (напр. сплав х2 ) превращение, начавшись как , не заканчивается, затем идет в обратном направлении. При комнатной температуре оба сплава будут в однофазном состоянии.
Рис. 19 б На диаграмме (рис. 19 б) компонент А имеет три полиморфные модификации. Две из них (низко- и высокотемпературная) изоморфны другу и компоненту В и образуют с ним неограниченные твердые растворы. На основе промежуточной модификации компонента А образуется граничный твердый раствор, устойчивый в интервале температур Т 4 – Т 5. Область двухфазного равновесия ( + ) является замкнутой, поэтому в некоторых сплавах (напр. сплав х1 ) превращение идет дважды: вначале , затем , а в других (напр. сплав х2 ) превращение, начавшись как , не заканчивается, затем идет в обратном направлении. При комнатной температуре оба сплава будут в однофазном состоянии.
 Рис. 19 в Если полиморфизмом обладают оба компонента, диаграммы будут более разнообразны, один из вариантов представлен на рис. 19, в. Полиморфное превращение будет происходить во всех сплавах.
Рис. 19 в Если полиморфизмом обладают оба компонента, диаграммы будут более разнообразны, один из вариантов представлен на рис. 19, в. Полиморфное превращение будет происходить во всех сплавах.
 3. 4. 2. Диаграммы состояния системы с эвтектоидным равновесием. Рис. 20 В этой системе компонент А имеет 2 полиморфные модификации, на основе которых компонент В образует граничные – и – растворы. La–c b–d (кристаллизация твердого раствора), s–e t–m (полиморфное превращение). При температуре Т 3 в равновесии будут находиться фазы e и m, относительное количество этих фаз : = mu/me; = ue/me. При температуре Т 3 – твердый раствор начнет распадаться по реакции, аналогичной эвтектической и называемой эвтектоидной: e m+ n превращение идет при постоянной температуре и неизменных составах фаз. Смесь ( m+ n) называется эвтектоидной смесью или эвтектоидом.
3. 4. 2. Диаграммы состояния системы с эвтектоидным равновесием. Рис. 20 В этой системе компонент А имеет 2 полиморфные модификации, на основе которых компонент В образует граничные – и – растворы. La–c b–d (кристаллизация твердого раствора), s–e t–m (полиморфное превращение). При температуре Т 3 в равновесии будут находиться фазы e и m, относительное количество этих фаз : = mu/me; = ue/me. При температуре Т 3 – твердый раствор начнет распадаться по реакции, аналогичной эвтектической и называемой эвтектоидной: e m+ n превращение идет при постоянной температуре и неизменных составах фаз. Смесь ( m+ n) называется эвтектоидной смесью или эвтектоидом.
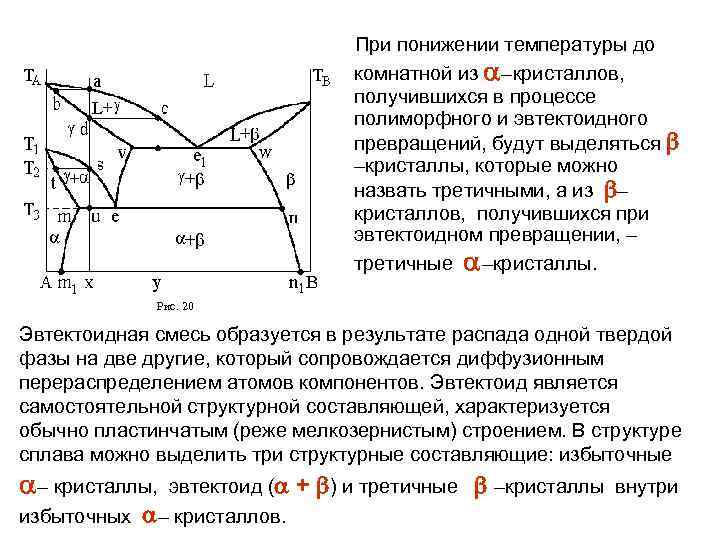 При понижении температуры до комнатной из –кристаллов, получившихся в процессе полиморфного и эвтектоидного превращений, будут выделяться –кристаллы, которые можно назвать третичными, а из – кристаллов, получившихся при эвтектоидном превращении, – третичные –кристаллы. Рис. 20 Эвтектоидная смесь образуется в результате распада одной твердой фазы на две другие, который сопровождается диффузионным перераспределением атомов компонентов. Эвтектоид является самостоятельной структурной составляющей, характеризуется обычно пластинчатым (реже мелкозернистым) строением. В структуре сплава можно выделить три структурные составляющие: избыточные – кристаллы, эвтектоид ( избыточных – кристаллов. + ) и третичные –кристаллы внутри
При понижении температуры до комнатной из –кристаллов, получившихся в процессе полиморфного и эвтектоидного превращений, будут выделяться –кристаллы, которые можно назвать третичными, а из – кристаллов, получившихся при эвтектоидном превращении, – третичные –кристаллы. Рис. 20 Эвтектоидная смесь образуется в результате распада одной твердой фазы на две другие, который сопровождается диффузионным перераспределением атомов компонентов. Эвтектоид является самостоятельной структурной составляющей, характеризуется обычно пластинчатым (реже мелкозернистым) строением. В структуре сплава можно выделить три структурные составляющие: избыточные – кристаллы, эвтектоид ( избыточных – кристаллов. + ) и третичные –кристаллы внутри
 Фазовые превращения в сплаве состава точки у можно записать следующим образом: Lc–e 1 d–v (кристаллизация твердого раствора), Le 1 v + w (эвтектическая кристаллизация), v–e w–n (выделение вторичных кристаллов за счет уменьшения растворимости компонентов), e m+ n (эвтектоидное превращение), Рис. 20 m–m 1 n–n 1 (выделение третичных кристаллов). Под микроскопом в этом сплаве обычно видны две структурные составляющие: первичные –кристаллы, которые затем претерпевают эвтектоидный распад и эвтектическую смесь ( + ), в которой – кристаллы также распались на эвтектоид. Вторичные –кристаллы, а также третичные – и –кристаллы обычно не удается увидеть.
Фазовые превращения в сплаве состава точки у можно записать следующим образом: Lc–e 1 d–v (кристаллизация твердого раствора), Le 1 v + w (эвтектическая кристаллизация), v–e w–n (выделение вторичных кристаллов за счет уменьшения растворимости компонентов), e m+ n (эвтектоидное превращение), Рис. 20 m–m 1 n–n 1 (выделение третичных кристаллов). Под микроскопом в этом сплаве обычно видны две структурные составляющие: первичные –кристаллы, которые затем претерпевают эвтектоидный распад и эвтектическую смесь ( + ), в которой – кристаллы также распались на эвтектоид. Вторичные –кристаллы, а также третичные – и –кристаллы обычно не удается увидеть.
 ЛЕКЦИЯ 8. 3. 4. 3. Диаграммы состояния систем с перитектоидным превращением. Некоторые промежуточные фазы образуются в результате взаимодействия двух твердых фаз по реакции, аналогичной перитектической, которая называется перитектоидной. Промежуточная фаза образуется при взаимодействии граничных твердых растворов: c+ d p, превращение, в соответствии с правилом фаз Гиббса, протекает при постоянной температуре и неизменных составах всех фаз. Рис. 21 В зависимости от состава сплава перитектоидная реакция заканчивается по–разному: с одновременным исчезновением обеих исходных фаз с и d (сплав состава точки р) или только одной из этих фаз (фазы c - для сплавов участка v–n и фазы d - для сплавов участка m–u). Перитектоида, как самостоятельной структурной составляющей, не существует. Фазы, находящиеся в равновесии в различных областях диаграммы, указаны на рис.
ЛЕКЦИЯ 8. 3. 4. 3. Диаграммы состояния систем с перитектоидным превращением. Некоторые промежуточные фазы образуются в результате взаимодействия двух твердых фаз по реакции, аналогичной перитектической, которая называется перитектоидной. Промежуточная фаза образуется при взаимодействии граничных твердых растворов: c+ d p, превращение, в соответствии с правилом фаз Гиббса, протекает при постоянной температуре и неизменных составах всех фаз. Рис. 21 В зависимости от состава сплава перитектоидная реакция заканчивается по–разному: с одновременным исчезновением обеих исходных фаз с и d (сплав состава точки р) или только одной из этих фаз (фазы c - для сплавов участка v–n и фазы d - для сплавов участка m–u). Перитектоида, как самостоятельной структурной составляющей, не существует. Фазы, находящиеся в равновесии в различных областях диаграммы, указаны на рис.
 3. 5. Диаграммы состояния систем с монотектическим превращением Рис. 22 Встречаются случаи ограниченной растворимости в жидком состоянии. На диаграммах при этом образуются области несмешиваемости, различные по форме и протяженности. На рис. представлена диаграмма системы, в которой расслоение в жидком состоянии характерно для сплавов, расположенных между точками m и n. На горизонтали nmu происходит превращение Lm Ln +B, называемое монотектическим, точка m называется монотектической. Монотектическое превращение (как эвтектическое и перитектическое) протекает при постоянной температуре и заканчивается исчезновением жидкости Lm, при этом образуется другая жидкость Ln и кристаллы твердой фазы, в рассматриваемом случае кристаллы В.
3. 5. Диаграммы состояния систем с монотектическим превращением Рис. 22 Встречаются случаи ограниченной растворимости в жидком состоянии. На диаграммах при этом образуются области несмешиваемости, различные по форме и протяженности. На рис. представлена диаграмма системы, в которой расслоение в жидком состоянии характерно для сплавов, расположенных между точками m и n. На горизонтали nmu происходит превращение Lm Ln +B, называемое монотектическим, точка m называется монотектической. Монотектическое превращение (как эвтектическое и перитектическое) протекает при постоянной температуре и заканчивается исчезновением жидкости Lm, при этом образуется другая жидкость Ln и кристаллы твердой фазы, в рассматриваемом случае кристаллы В.
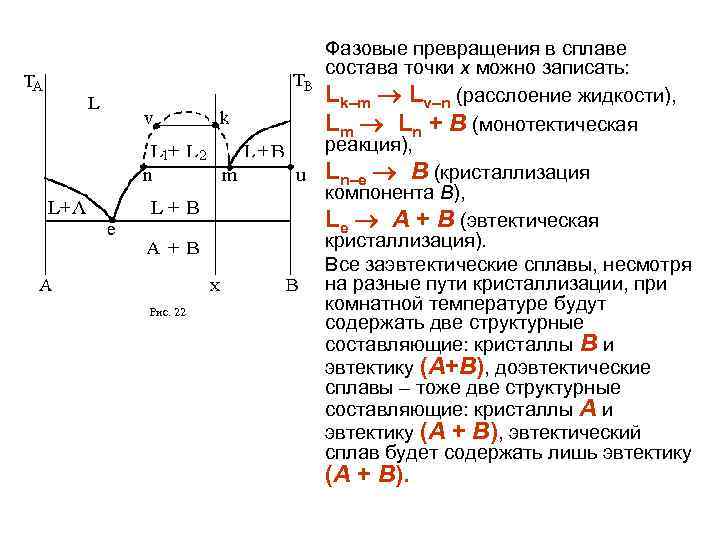 Рис. 22 Фазовые превращения в сплаве состава точки х можно записать: Lk–m Lv–n (расслоение жидкости), Lm Ln + В (монотектическая реакция), Ln–e В (кристаллизация компонента В), Le A + B (эвтектическая кристаллизация). Все заэвтектические сплавы, несмотря на разные пути кристаллизации, при комнатной температуре будут содержать две структурные составляющие: кристаллы В и эвтектику (А+В), доэвтектические сплавы – тоже две структурные составляющие: кристаллы А и эвтектику (А + В), эвтектический сплав будет содержать лишь эвтектику (А + В).
Рис. 22 Фазовые превращения в сплаве состава точки х можно записать: Lk–m Lv–n (расслоение жидкости), Lm Ln + В (монотектическая реакция), Ln–e В (кристаллизация компонента В), Le A + B (эвтектическая кристаллизация). Все заэвтектические сплавы, несмотря на разные пути кристаллизации, при комнатной температуре будут содержать две структурные составляющие: кристаллы В и эвтектику (А+В), доэвтектические сплавы – тоже две структурные составляющие: кристаллы А и эвтектику (А + В), эвтектический сплав будет содержать лишь эвтектику (А + В).
 ЗАКЛЮЧЕНИЕ Анализ различных типов диаграмм состояния двойных систем позволяет сделать некоторые обобщения относительно фазовых равновесий в этих системах. Равновесие двух фаз переменного состава при разных температурах изображается двумя сопряженными кривыми (напр. Ликвидус – солидус) или двумя ветвями одной и той же кривой (напр. двумя ветвями бинодали). При постоянной температуре составы равновесных фаз определяют две точки на этих кривых, которые можно соединить конодой. Равновесие трех фаз при постоянной температуре изображается тремя точками на нонвариантной горизонтали, две из них являются концами горизонтали, а третья располагается между ними. Эту горизонталь можно рассматривать как три конода, каждая из которых соединяет составы двух (из трех) фаз. Трехфазная реакция всегда протекает при постоянной температуре так, что: –при взаимодействии двух крайних фаз образуется третья промежуточная по составу фаза (перитектическая, перитектоидная реакции), –одна фаза промежуточного состава распадается на две другие крайних составов (эвтектическая, эвтектоидная, монотектическая реакции).
ЗАКЛЮЧЕНИЕ Анализ различных типов диаграмм состояния двойных систем позволяет сделать некоторые обобщения относительно фазовых равновесий в этих системах. Равновесие двух фаз переменного состава при разных температурах изображается двумя сопряженными кривыми (напр. Ликвидус – солидус) или двумя ветвями одной и той же кривой (напр. двумя ветвями бинодали). При постоянной температуре составы равновесных фаз определяют две точки на этих кривых, которые можно соединить конодой. Равновесие трех фаз при постоянной температуре изображается тремя точками на нонвариантной горизонтали, две из них являются концами горизонтали, а третья располагается между ними. Эту горизонталь можно рассматривать как три конода, каждая из которых соединяет составы двух (из трех) фаз. Трехфазная реакция всегда протекает при постоянной температуре так, что: –при взаимодействии двух крайних фаз образуется третья промежуточная по составу фаза (перитектическая, перитектоидная реакции), –одна фаза промежуточного состава распадается на две другие крайних составов (эвтектическая, эвтектоидная, монотектическая реакции).
 Кроме того, нужно учесть следующее: - однофазные области могут соприкасаться одна с другой только в одной точке и никогда не отделяются граничной кривой, - две однофазные области всегда отделены друг от друга двухфазной областью, в которой встречаются те же фазы, - две соседние двухфазные области отделены друг от друга однофазной областью или горизонталью нонвариантного равновесия, - ко всякой горизонтали нонвариантного равновесия примыкают в общем случае три различные двухфазные области, ограниченные парами сопряженных кривых. Рассмотрение диаграмм состояния включает следующие этапы: - определить линии ликвидус, солидус, предельной растворимости, полиморфных превращений и всех нонвариантных превращений; - определить фазовый состав во всех областях диаграммы; -указать составы (%-ное содержание компонентов) заданных сплавов; - рассмотреть равновесные процессы, протекающие в заданных сплавах при понижении температуры, применяя правило фаз Гиббса и правило отрезков; - определить фазовые и структурные составляющие при комнатной температуре; - определить, как изменятся фазовый состав и структурные составляющие при неравновесных процессах.
Кроме того, нужно учесть следующее: - однофазные области могут соприкасаться одна с другой только в одной точке и никогда не отделяются граничной кривой, - две однофазные области всегда отделены друг от друга двухфазной областью, в которой встречаются те же фазы, - две соседние двухфазные области отделены друг от друга однофазной областью или горизонталью нонвариантного равновесия, - ко всякой горизонтали нонвариантного равновесия примыкают в общем случае три различные двухфазные области, ограниченные парами сопряженных кривых. Рассмотрение диаграмм состояния включает следующие этапы: - определить линии ликвидус, солидус, предельной растворимости, полиморфных превращений и всех нонвариантных превращений; - определить фазовый состав во всех областях диаграммы; -указать составы (%-ное содержание компонентов) заданных сплавов; - рассмотреть равновесные процессы, протекающие в заданных сплавах при понижении температуры, применяя правило фаз Гиббса и правило отрезков; - определить фазовые и структурные составляющие при комнатной температуре; - определить, как изменятся фазовый состав и структурные составляющие при неравновесных процессах.
 Диаграмма состояния системы Fe-C АВСD – линия ликвидус AHMSCF – линия солидус SE –линия предельной растворимости углерода в γжелезе GPQ – линия предельной растворимости углерода в α железе PG , GE – линии полиморфного превращения α → γ HN, MN – линии полиморфного превращения δ ↔ γ HNB – линия перитектического превращения L + δ ↔ γ SCF – линия эвтектического превращения L ↔ α + Fe 3 C PEK – линия эвтектоидного превращения γ ↔ α + Fe 3 C Рис. 23
Диаграмма состояния системы Fe-C АВСD – линия ликвидус AHMSCF – линия солидус SE –линия предельной растворимости углерода в γжелезе GPQ – линия предельной растворимости углерода в α железе PG , GE – линии полиморфного превращения α → γ HN, MN – линии полиморфного превращения δ ↔ γ HNB – линия перитектического превращения L + δ ↔ γ SCF – линия эвтектического превращения L ↔ α + Fe 3 C PEK – линия эвтектоидного превращения γ ↔ α + Fe 3 C Рис. 23
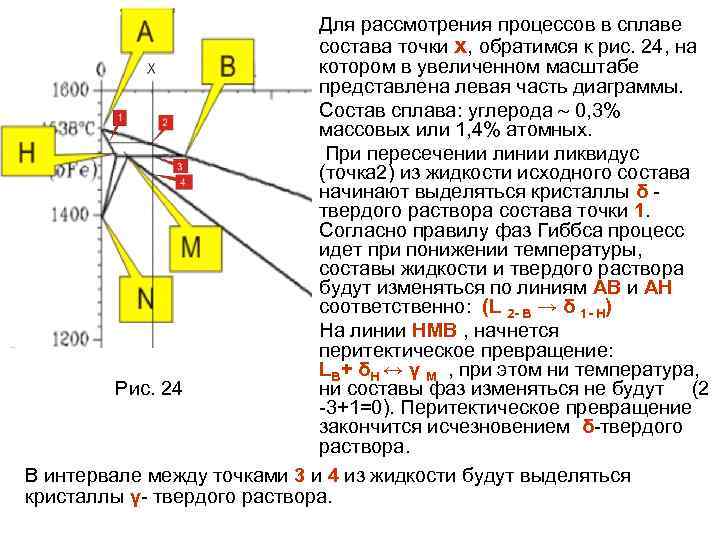 Для рассмотрения процессов в сплаве состава точки х, обратимся к рис. 24, на котором в увеличенном масштабе представлена левая часть диаграммы. Состав сплава: углерода 0, 3% массовых или 1, 4% атомных. При пересечении ликвидус (точка 2) из жидкости исходного состава начинают выделяться кристаллы δ твердого раствора состава точки 1. Согласно правилу фаз Гиббса процесс идет при понижении температуры, составы жидкости и твердого раствора будут изменяться по линиям АВ и АН соответственно: (L 2 - В → δ 1 - Н) На линии НМВ , начнется перитектическое превращение: LВ+ δН ↔ γ М , при этом ни температура, ни составы фаз изменяться не будут (2 Рис. 24 -3+1=0). Перитектическое превращение закончится исчезновением δ-твердого раствора. В интервале между точками 3 и 4 из жидкости будут выделяться кристаллы γ- твердого раствора.
Для рассмотрения процессов в сплаве состава точки х, обратимся к рис. 24, на котором в увеличенном масштабе представлена левая часть диаграммы. Состав сплава: углерода 0, 3% массовых или 1, 4% атомных. При пересечении ликвидус (точка 2) из жидкости исходного состава начинают выделяться кристаллы δ твердого раствора состава точки 1. Согласно правилу фаз Гиббса процесс идет при понижении температуры, составы жидкости и твердого раствора будут изменяться по линиям АВ и АН соответственно: (L 2 - В → δ 1 - Н) На линии НМВ , начнется перитектическое превращение: LВ+ δН ↔ γ М , при этом ни температура, ни составы фаз изменяться не будут (2 Рис. 24 -3+1=0). Перитектическое превращение закончится исчезновением δ-твердого раствора. В интервале между точками 3 и 4 из жидкости будут выделяться кристаллы γ- твердого раствора.
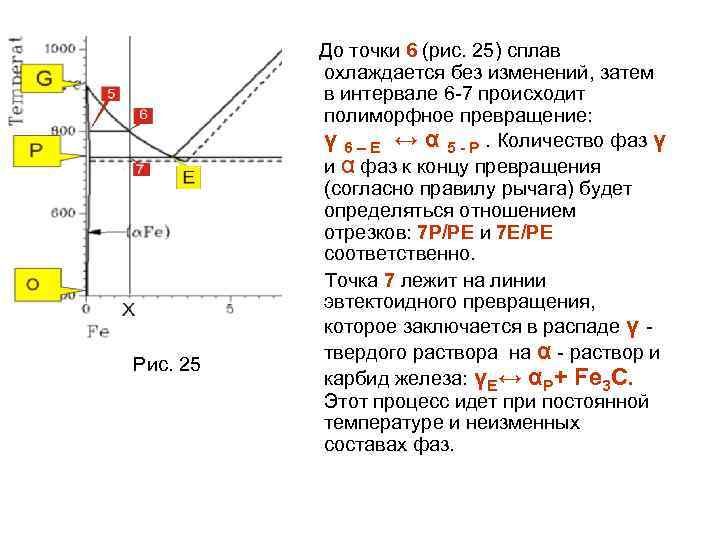 Рис. 25 До точки 6 (рис. 25) сплав охлаждается без изменений, затем в интервале 6 -7 происходит полиморфное превращение: γ 6 – Е ↔ α 5 - Р. Количество фаз γ и α фаз к концу превращения (согласно правилу рычага) будет определяться отношением отрезков: 7 P/PE и 7 E/PE соответственно. Точка 7 лежит на линии эвтектоидного превращения, которое заключается в распаде γ твердого раствора на α - раствор и карбид железа: γЕ↔ αР+ Fe 3 C. Этот процесс идет при постоянной температуре и неизменных составах фаз.
Рис. 25 До точки 6 (рис. 25) сплав охлаждается без изменений, затем в интервале 6 -7 происходит полиморфное превращение: γ 6 – Е ↔ α 5 - Р. Количество фаз γ и α фаз к концу превращения (согласно правилу рычага) будет определяться отношением отрезков: 7 P/PE и 7 E/PE соответственно. Точка 7 лежит на линии эвтектоидного превращения, которое заключается в распаде γ твердого раствора на α - раствор и карбид железа: γЕ↔ αР+ Fe 3 C. Этот процесс идет при постоянной температуре и неизменных составах фаз.
 ЛЕКЦИЯ 9. 4. НЕКОТОРЫЕ ТИПЫ ДИАГРАММ СОСТОЯНИЯ ТРОЙНЫХ СИСТЕМ. 4. 1 Изображение составов сплавов тройных систем. Для изображения состава тройных сплавов равносторонний треугольник, его называют концентрационным. В его вершинах находятся компоненты А, В, С, стороны служат для изображения составов двойных сплавов, а плоскость треугольника – для изображения составов тройных сплавов. Состав сплава можно определить двумя способами, в основе которых лежат следующие свойства равностороннего треугольника: 1. сумма перпендикуляров, опущенных из любой точки внутри треугольника на его стороны, равна высоте треугольника; 2. сумма трех отрезков, отсекаемых на сторонах треугольника прямыми, которые проходят через любую точку внутри треугольника параллельно его сторонам, равна стороне треугольника.
ЛЕКЦИЯ 9. 4. НЕКОТОРЫЕ ТИПЫ ДИАГРАММ СОСТОЯНИЯ ТРОЙНЫХ СИСТЕМ. 4. 1 Изображение составов сплавов тройных систем. Для изображения состава тройных сплавов равносторонний треугольник, его называют концентрационным. В его вершинах находятся компоненты А, В, С, стороны служат для изображения составов двойных сплавов, а плоскость треугольника – для изображения составов тройных сплавов. Состав сплава можно определить двумя способами, в основе которых лежат следующие свойства равностороннего треугольника: 1. сумма перпендикуляров, опущенных из любой точки внутри треугольника на его стороны, равна высоте треугольника; 2. сумма трех отрезков, отсекаемых на сторонах треугольника прямыми, которые проходят через любую точку внутри треугольника параллельно его сторонам, равна стороне треугольника.
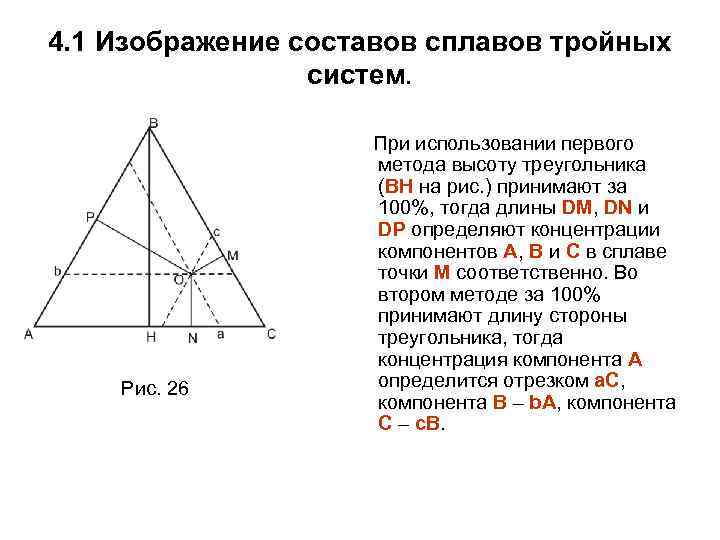 4. 1 Изображение составов сплавов тройных систем. Рис. 26 При использовании первого метода высоту треугольника (ВН на рис. ) принимают за 100%, тогда длины DM, DN и DP определяют концентрации компонентов А, В и С в сплаве точки М соответственно. Во втором методе за 100% принимают длину стороны треугольника, тогда концентрация компонента А определится отрезком а. С, компонента В – b. А, компонента С – с. В.
4. 1 Изображение составов сплавов тройных систем. Рис. 26 При использовании первого метода высоту треугольника (ВН на рис. ) принимают за 100%, тогда длины DM, DN и DP определяют концентрации компонентов А, В и С в сплаве точки М соответственно. Во втором методе за 100% принимают длину стороны треугольника, тогда концентрация компонента А определится отрезком а. С, компонента В – b. А, компонента С – с. В.
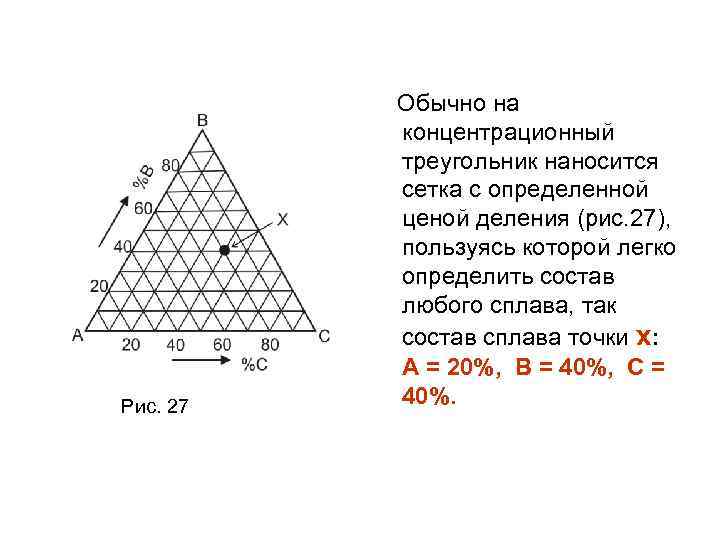 Рис. 27 Обычно на концентрационный треугольник наносится сетка с определенной ценой деления (рис. 27), пользуясь которой легко определить состав любого сплава, так состав сплава точки х: А = 20%, В = 40%, С = 40%.
Рис. 27 Обычно на концентрационный треугольник наносится сетка с определенной ценой деления (рис. 27), пользуясь которой легко определить состав любого сплава, так состав сплава точки х: А = 20%, В = 40%, С = 40%.
 4. 1. 1. Построение пространственных диаграмм. Для изображения фазовых равновесий в тройных сплавах нужно строить пространственные диаграммы состояния в координатах состав – температура. Такая диаграмма представляет собой прямоугольную трехгранную призму, основанием которой служит концентрационный треугольник, а гранями – диаграммы состояния двойных систем А-В, В-С и А-С. На вертикальных линиях, идущих от вершин А, В и С, отмечают температуры плавления чистых компонентов. Строение пространственной диаграммы состояния тройной системы определяется характером диаграмм состояния двойных систем на её боковых гранях.
4. 1. 1. Построение пространственных диаграмм. Для изображения фазовых равновесий в тройных сплавах нужно строить пространственные диаграммы состояния в координатах состав – температура. Такая диаграмма представляет собой прямоугольную трехгранную призму, основанием которой служит концентрационный треугольник, а гранями – диаграммы состояния двойных систем А-В, В-С и А-С. На вертикальных линиях, идущих от вершин А, В и С, отмечают температуры плавления чистых компонентов. Строение пространственной диаграммы состояния тройной системы определяется характером диаграмм состояния двойных систем на её боковых гранях.
 4. 2. Система с неограниченной растворимостью компонентов в твердом и жидком состояниях. Диаграмма состоит из двух поверхностей: поверхность ликвидуса проходит через линии ликвидуса двойных систем, поверхность солидуса проходит через линии солидуса двойных систем. Рис. 28 Кристаллизация сплава состава точки х начинается несколько ниже точки 1, расположенной на поверхности ликвидуса. Из жидкого раствора начинают выделяться кристаллы тройного твердого раствора состава точки a′. Состав кристаллов твердого раствора изменяется по линии а′ 2, расположенной на поверхности солидуса, а состав жидкой фазы – по линии 1 b′. Проекции этих линий на концентрационный треугольник: аех и хdb соответственно.
4. 2. Система с неограниченной растворимостью компонентов в твердом и жидком состояниях. Диаграмма состоит из двух поверхностей: поверхность ликвидуса проходит через линии ликвидуса двойных систем, поверхность солидуса проходит через линии солидуса двойных систем. Рис. 28 Кристаллизация сплава состава точки х начинается несколько ниже точки 1, расположенной на поверхности ликвидуса. Из жидкого раствора начинают выделяться кристаллы тройного твердого раствора состава точки a′. Состав кристаллов твердого раствора изменяется по линии а′ 2, расположенной на поверхности солидуса, а состав жидкой фазы – по линии 1 b′. Проекции этих линий на концентрационный треугольник: аех и хdb соответственно.
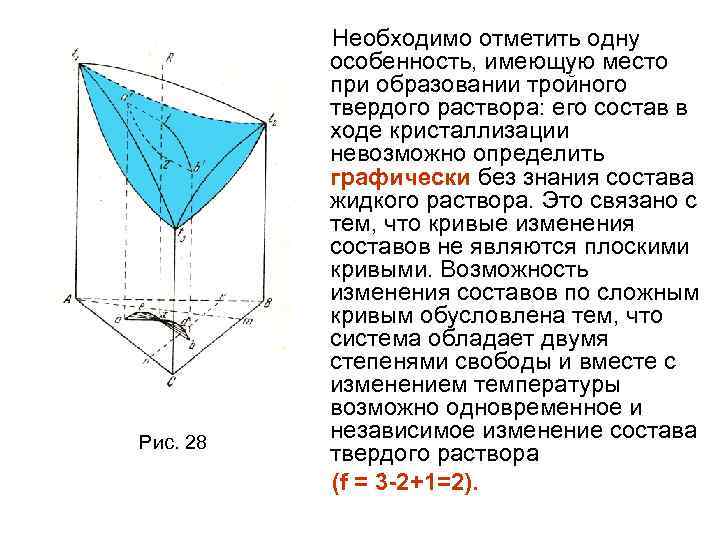 Рис. 28 Необходимо отметить одну особенность, имеющую место при образовании тройного твердого раствора: его состав в ходе кристаллизации невозможно определить графически без знания состава жидкого раствора. Это связано с тем, что кривые изменения составов не являются плоскими кривыми. Возможность изменения составов по сложным кривым обусловлена тем, что система обладает двумя степенями свободы и вместе с изменением температуры возможно одновременное и независимое изменение состава твердого раствора (f = 3 -2+1=2).
Рис. 28 Необходимо отметить одну особенность, имеющую место при образовании тройного твердого раствора: его состав в ходе кристаллизации невозможно определить графически без знания состава жидкого раствора. Это связано с тем, что кривые изменения составов не являются плоскими кривыми. Возможность изменения составов по сложным кривым обусловлена тем, что система обладает двумя степенями свободы и вместе с изменением температуры возможно одновременное и независимое изменение состава твердого раствора (f = 3 -2+1=2).
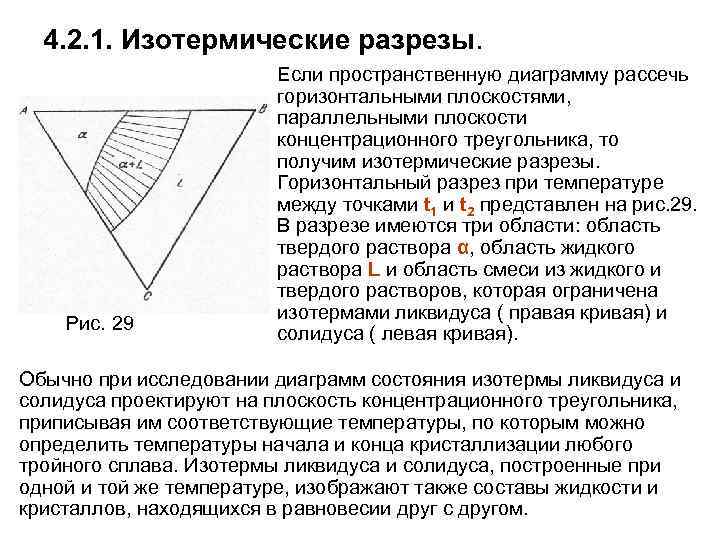 4. 2. 1. Изотермические разрезы. Рис. 29 Если пространственную диаграмму рассечь горизонтальными плоскостями, параллельными плоскости концентрационного треугольника, то получим изотермические разрезы. Горизонтальный разрез при температуре между точками t 1 и t 2 представлен на рис. 29. В разрезе имеются три области: область твердого раствора α, область жидкого раствора L и область смеси из жидкого и твердого растворов, которая ограничена изотермами ликвидуса ( правая кривая) и солидуса ( левая кривая). Обычно при исследовании диаграмм состояния изотермы ликвидуса и солидуса проектируют на плоскость концентрационного треугольника, приписывая им соответствующие температуры, по которым можно определить температуры начала и конца кристаллизации любого тройного сплава. Изотермы ликвидуса и солидуса, построенные при одной и той же температуре, изображают также составы жидкости и кристаллов, находящихся в равновесии друг с другом.
4. 2. 1. Изотермические разрезы. Рис. 29 Если пространственную диаграмму рассечь горизонтальными плоскостями, параллельными плоскости концентрационного треугольника, то получим изотермические разрезы. Горизонтальный разрез при температуре между точками t 1 и t 2 представлен на рис. 29. В разрезе имеются три области: область твердого раствора α, область жидкого раствора L и область смеси из жидкого и твердого растворов, которая ограничена изотермами ликвидуса ( правая кривая) и солидуса ( левая кривая). Обычно при исследовании диаграмм состояния изотермы ликвидуса и солидуса проектируют на плоскость концентрационного треугольника, приписывая им соответствующие температуры, по которым можно определить температуры начала и конца кристаллизации любого тройного сплава. Изотермы ликвидуса и солидуса, построенные при одной и той же температуре, изображают также составы жидкости и кристаллов, находящихся в равновесии друг с другом.
 4. 2. 2. Вертикальные разрезы. Вертикальные или политермические разрезы можно построить, рассекая пространственную диаграмму вертикальными плоскостями. На рис. 30 (а, б) представлены вертикальные разрезы, проходящие по линиям Аm и nk. Кривые пересечения разреза с поверхностями ликвидус и солидус называются кривыми ликвидуса и солидуса. Политермические разрезы позволяют прослеживать только за изменением фазового состояния тройных сплавов в зависимости от их состава и температуры, т. е судить о фазовых превращениях, протекающих в различных сплавах в условиях, которые не сильно отличаются от равновесных. Кривые ликвидуса и солидуса в общем случае не являются сопряженными и не изображают составов равновесных фаз в интервале кристаллизации,
4. 2. 2. Вертикальные разрезы. Вертикальные или политермические разрезы можно построить, рассекая пространственную диаграмму вертикальными плоскостями. На рис. 30 (а, б) представлены вертикальные разрезы, проходящие по линиям Аm и nk. Кривые пересечения разреза с поверхностями ликвидус и солидус называются кривыми ликвидуса и солидуса. Политермические разрезы позволяют прослеживать только за изменением фазового состояния тройных сплавов в зависимости от их состава и температуры, т. е судить о фазовых превращениях, протекающих в различных сплавах в условиях, которые не сильно отличаются от равновесных. Кривые ликвидуса и солидуса в общем случае не являются сопряженными и не изображают составов равновесных фаз в интервале кристаллизации,
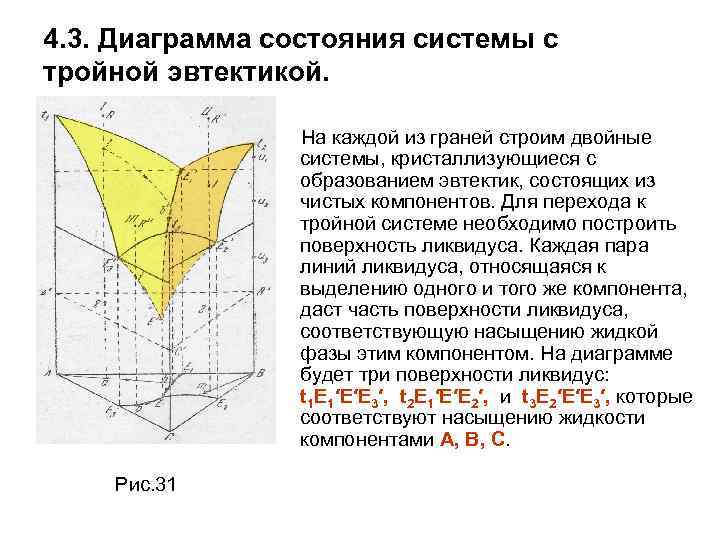 4. 3. Диаграмма состояния системы с тройной эвтектикой. На каждой из граней строим двойные системы, кристаллизующиеся с образованием эвтектик, состоящих из чистых компонентов. Для перехода к тройной системе необходимо построить поверхность ликвидуса. Каждая пара линий ликвидуса, относящаяся к выделению одного и того же компонента, даст часть поверхности ликвидуса, соответствующую насыщению жидкой фазы этим компонентом. На диаграмме будет три поверхности ликвидус: t 1 E 1′E′E 3′, t 2 Е 1′Е′Е 2′, и t 3 Е 2′Е′Е 3′, которые соответствуют насыщению жидкости компонентами А, В, С. Рис. 31
4. 3. Диаграмма состояния системы с тройной эвтектикой. На каждой из граней строим двойные системы, кристаллизующиеся с образованием эвтектик, состоящих из чистых компонентов. Для перехода к тройной системе необходимо построить поверхность ликвидуса. Каждая пара линий ликвидуса, относящаяся к выделению одного и того же компонента, даст часть поверхности ликвидуса, соответствующую насыщению жидкой фазы этим компонентом. На диаграмме будет три поверхности ликвидус: t 1 E 1′E′E 3′, t 2 Е 1′Е′Е 2′, и t 3 Е 2′Е′Е 3′, которые соответствуют насыщению жидкости компонентами А, В, С. Рис. 31
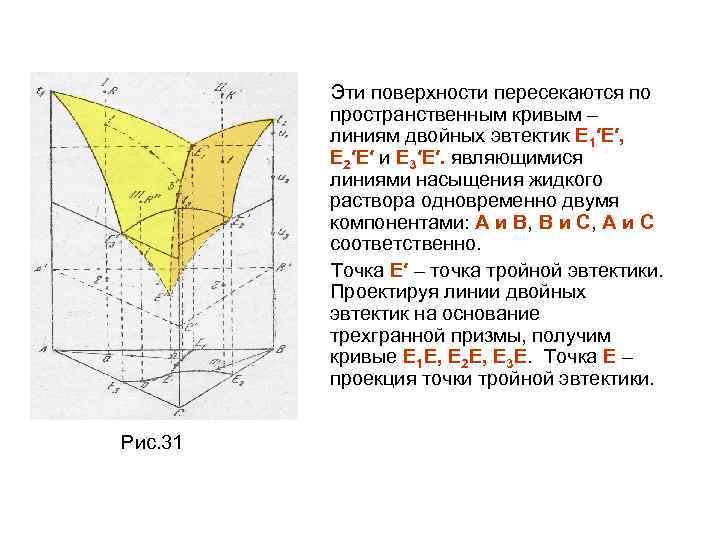 Эти поверхности пересекаются по пространственным кривым – линиям двойных эвтектик Е 1′E′, E 2′E′ и E 3′E′. являющимися линиями насыщения жидкого раствора одновременно двумя компонентами: А и В, В и С, А и С соответственно. Точка E′ – точка тройной эвтектики. Проектируя линии двойных эвтектик на основание трехгранной призмы, получим кривые E 1 E, E 2 E, E 3 E. Точка E – проекция точки тройной эвтектики. Рис. 31
Эти поверхности пересекаются по пространственным кривым – линиям двойных эвтектик Е 1′E′, E 2′E′ и E 3′E′. являющимися линиями насыщения жидкого раствора одновременно двумя компонентами: А и В, В и С, А и С соответственно. Точка E′ – точка тройной эвтектики. Проектируя линии двойных эвтектик на основание трехгранной призмы, получим кривые E 1 E, E 2 E, E 3 E. Точка E – проекция точки тройной эвтектики. Рис. 31
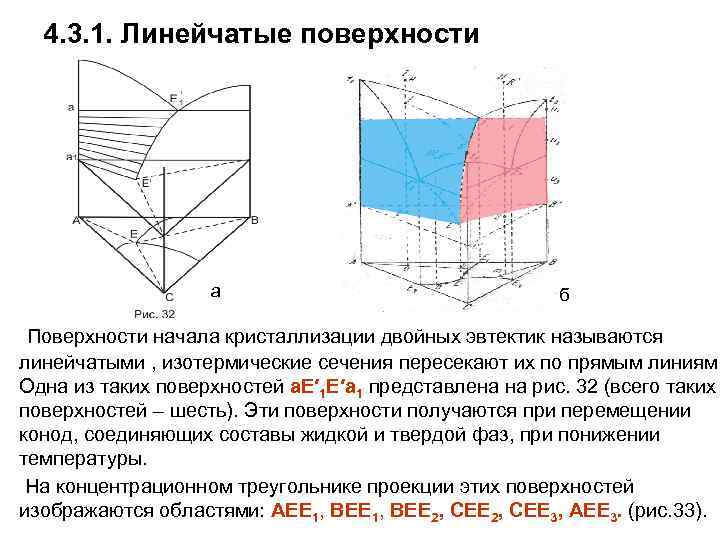 4. 3. 1. Линейчатые поверхности а б Поверхности начала кристаллизации двойных эвтектик называются линейчатыми , изотермические сечения пересекают их по прямым линиям. Одна из таких поверхностей a. E′ 1 E′a 1 представлена на рис. 32 (всего таких поверхностей – шесть). Эти поверхности получаются при перемещении конод, соединяющих составы жидкой и твердой фаз, при понижении температуры. На концентрационном треугольнике проекции этих поверхностей изображаются областями: АЕЕ 1, ВЕЕ 2, СЕЕ 3, АЕЕ 3. (рис. 33).
4. 3. 1. Линейчатые поверхности а б Поверхности начала кристаллизации двойных эвтектик называются линейчатыми , изотермические сечения пересекают их по прямым линиям. Одна из таких поверхностей a. E′ 1 E′a 1 представлена на рис. 32 (всего таких поверхностей – шесть). Эти поверхности получаются при перемещении конод, соединяющих составы жидкой и твердой фаз, при понижении температуры. На концентрационном треугольнике проекции этих поверхностей изображаются областями: АЕЕ 1, ВЕЕ 2, СЕЕ 3, АЕЕ 3. (рис. 33).
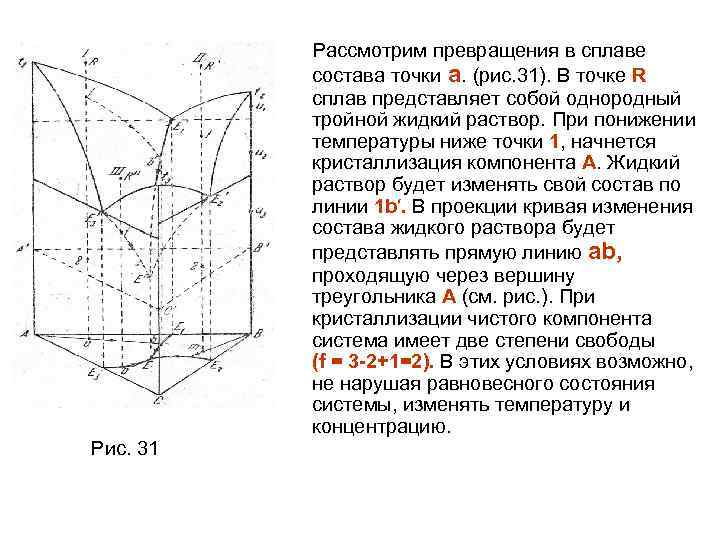 Рис. 31 Рассмотрим превращения в сплаве состава точки а. (рис. 31). В точке R сплав представляет собой однородный тройной жидкий раствор. При понижении температуры ниже точки 1, начнется кристаллизация компонента А. Жидкий раствор будет изменять свой состав по линии 1 b′. В проекции кривая изменения состава жидкого раствора будет представлять прямую линию ab, проходящую через вершину треугольника А (см. рис. ). При кристаллизации чистого компонента система имеет две степени свободы (f = 3 -2+1=2). В этих условиях возможно, не нарушая равновесного состояния системы, изменять температуру и концентрацию.
Рис. 31 Рассмотрим превращения в сплаве состава точки а. (рис. 31). В точке R сплав представляет собой однородный тройной жидкий раствор. При понижении температуры ниже точки 1, начнется кристаллизация компонента А. Жидкий раствор будет изменять свой состав по линии 1 b′. В проекции кривая изменения состава жидкого раствора будет представлять прямую линию ab, проходящую через вершину треугольника А (см. рис. ). При кристаллизации чистого компонента система имеет две степени свободы (f = 3 -2+1=2). В этих условиях возможно, не нарушая равновесного состояния системы, изменять температуру и концентрацию.
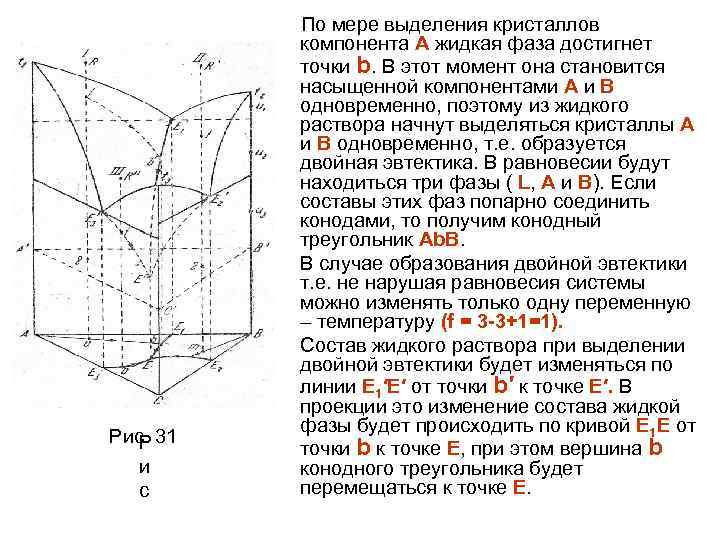 Рис. 31 Р и с По мере выделения кристаллов компонента А жидкая фаза достигнет точки b. В этот момент она становится насыщенной компонентами А и В одновременно, поэтому из жидкого раствора начнут выделяться кристаллы А и В одновременно, т. е. образуется двойная эвтектика. В равновесии будут находиться три фазы ( L, A и В). Если составы этих фаз попарно соединить конодами, то получим конодный треугольник Аb. B. В случае образования двойной эвтектики т. е. не нарушая равновесия системы можно изменять только одну переменную – температуру (f = 3 -3+1=1). Состав жидкого раствора при выделении двойной эвтектики будет изменяться по линии E 1′E′ от точки b′ к точке Е′. В проекции это изменение состава жидкой фазы будет происходить по кривой E 1 E от точки b к точке Е, при этом вершина b конодного треугольника будет перемещаться к точке Е.
Рис. 31 Р и с По мере выделения кристаллов компонента А жидкая фаза достигнет точки b. В этот момент она становится насыщенной компонентами А и В одновременно, поэтому из жидкого раствора начнут выделяться кристаллы А и В одновременно, т. е. образуется двойная эвтектика. В равновесии будут находиться три фазы ( L, A и В). Если составы этих фаз попарно соединить конодами, то получим конодный треугольник Аb. B. В случае образования двойной эвтектики т. е. не нарушая равновесия системы можно изменять только одну переменную – температуру (f = 3 -3+1=1). Состав жидкого раствора при выделении двойной эвтектики будет изменяться по линии E 1′E′ от точки b′ к точке Е′. В проекции это изменение состава жидкой фазы будет происходить по кривой E 1 E от точки b к точке Е, при этом вершина b конодного треугольника будет перемещаться к точке Е.
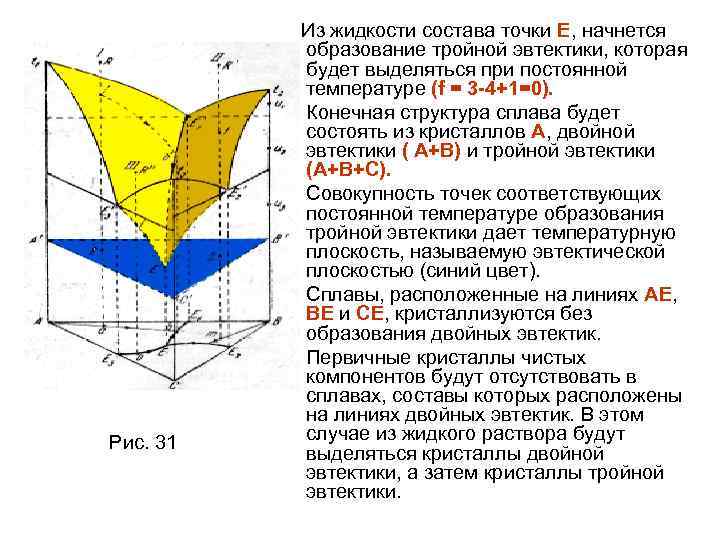 Рис. 31 Из жидкости состава точки Е, начнется образование тройной эвтектики, которая будет выделяться при постоянной температуре (f = 3 -4+1=0). Конечная структура сплава будет состоять из кристаллов А, двойной эвтектики ( А+В) и тройной эвтектики (А+В+С). Совокупность точек соответствующих постоянной температуре образования тройной эвтектики дает температурную плоскость, называемую эвтектической плоскостью (синий цвет). Сплавы, расположенные на линиях АЕ, ВЕ и СЕ, кристаллизуются без образования двойных эвтектик. Первичные кристаллы чистых компонентов будут отсутствовать в сплавах, составы которых расположены на линиях двойных эвтектик. В этом случае из жидкого раствора будут выделяться кристаллы двойной эвтектики, а затем кристаллы тройной эвтектики.
Рис. 31 Из жидкости состава точки Е, начнется образование тройной эвтектики, которая будет выделяться при постоянной температуре (f = 3 -4+1=0). Конечная структура сплава будет состоять из кристаллов А, двойной эвтектики ( А+В) и тройной эвтектики (А+В+С). Совокупность точек соответствующих постоянной температуре образования тройной эвтектики дает температурную плоскость, называемую эвтектической плоскостью (синий цвет). Сплавы, расположенные на линиях АЕ, ВЕ и СЕ, кристаллизуются без образования двойных эвтектик. Первичные кристаллы чистых компонентов будут отсутствовать в сплавах, составы которых расположены на линиях двойных эвтектик. В этом случае из жидкого раствора будут выделяться кристаллы двойной эвтектики, а затем кристаллы тройной эвтектики.
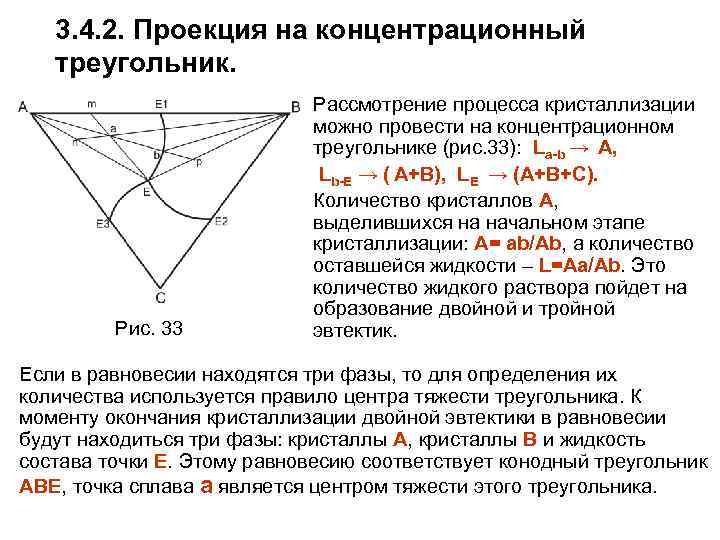 3. 4. 2. Проекция на концентрационный треугольник. Рис. 33 Рассмотрение процесса кристаллизации можно провести на концентрационном треугольнике (рис. 33): La-b → A, Lb-E → ( A+B), LE → (A+B+C). Количество кристаллов А, выделившихся на начальном этапе кристаллизации: А= ab/Ab, а количество оставшейся жидкости – L=Aa/Ab. Это количество жидкого раствора пойдет на образование двойной и тройной эвтектик. Если в равновесии находятся три фазы, то для определения их количества используется правило центра тяжести треугольника. К моменту окончания кристаллизации двойной эвтектики в равновесии будут находиться три фазы: кристаллы А, кристаллы В и жидкость состава точки Е. Этому равновесию соответствует конодный треугольник АВЕ, точка сплава а является центром тяжести этого треугольника.
3. 4. 2. Проекция на концентрационный треугольник. Рис. 33 Рассмотрение процесса кристаллизации можно провести на концентрационном треугольнике (рис. 33): La-b → A, Lb-E → ( A+B), LE → (A+B+C). Количество кристаллов А, выделившихся на начальном этапе кристаллизации: А= ab/Ab, а количество оставшейся жидкости – L=Aa/Ab. Это количество жидкого раствора пойдет на образование двойной и тройной эвтектик. Если в равновесии находятся три фазы, то для определения их количества используется правило центра тяжести треугольника. К моменту окончания кристаллизации двойной эвтектики в равновесии будут находиться три фазы: кристаллы А, кристаллы В и жидкость состава точки Е. Этому равновесию соответствует конодный треугольник АВЕ, точка сплава а является центром тяжести этого треугольника.
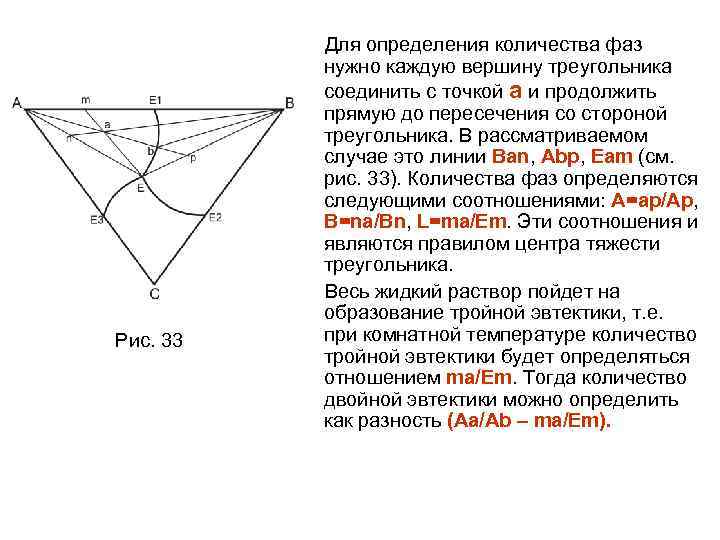 Рис. 33 Для определения количества фаз нужно каждую вершину треугольника соединить с точкой а и продолжить прямую до пересечения со стороной треугольника. В рассматриваемом случае это линии Вan, Abp, Eam (см. рис. 33). Количества фаз определяются следующими соотношениями: А=ap/Ap, B=na/Bn, L=ma/Em. Эти соотношения и являются правилом центра тяжести треугольника. Весь жидкий раствор пойдет на образование тройной эвтектики, т. е. при комнатной температуре количество тройной эвтектики будет определяться отношением ma/Em. Тогда количество двойной эвтектики можно определить как разность (Aa/Ab – ma/Em).
Рис. 33 Для определения количества фаз нужно каждую вершину треугольника соединить с точкой а и продолжить прямую до пересечения со стороной треугольника. В рассматриваемом случае это линии Вan, Abp, Eam (см. рис. 33). Количества фаз определяются следующими соотношениями: А=ap/Ap, B=na/Bn, L=ma/Em. Эти соотношения и являются правилом центра тяжести треугольника. Весь жидкий раствор пойдет на образование тройной эвтектики, т. е. при комнатной температуре количество тройной эвтектики будет определяться отношением ma/Em. Тогда количество двойной эвтектики можно определить как разность (Aa/Ab – ma/Em).
 3. 4. 3. Политермические разрезы. При построении политермических разрезов целесообразно придерживаться определенной последовательности: - на концентрационный треугольник наносится след плоскости разреза и отмечают характерные точки – точки пересечения этой плоскости с линиями концентрационного треугольника, - строят координатные оси разреза: состав – температура, на оси состава откладывают в масштабе характерные точки, на оси температур – критические температуры для крайних составов разреза, - на разрез наносят кривые ликвидуса и солидуса, являющиеся следом пересечения плоскости разреза с поверхностями ликвидус и солидус, - наносят линии, получающиеся от пересечения плоскостью разреза поверхностей начала кристаллизации двойных эвтектик, - указывают фазовый состав во всех областях разреза.
3. 4. 3. Политермические разрезы. При построении политермических разрезов целесообразно придерживаться определенной последовательности: - на концентрационный треугольник наносится след плоскости разреза и отмечают характерные точки – точки пересечения этой плоскости с линиями концентрационного треугольника, - строят координатные оси разреза: состав – температура, на оси состава откладывают в масштабе характерные точки, на оси температур – критические температуры для крайних составов разреза, - на разрез наносят кривые ликвидуса и солидуса, являющиеся следом пересечения плоскости разреза с поверхностями ликвидус и солидус, - наносят линии, получающиеся от пересечения плоскостью разреза поверхностей начала кристаллизации двойных эвтектик, - указывают фазовый состав во всех областях разреза.
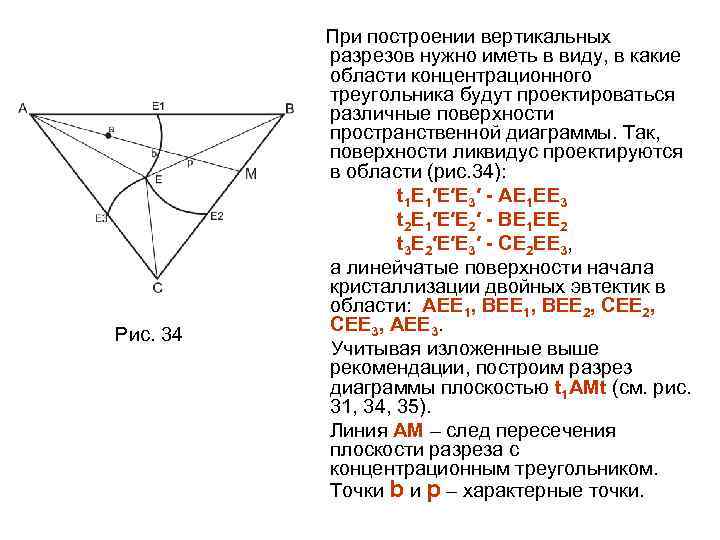 Рис. 34 При построении вертикальных разрезов нужно иметь в виду, в какие области концентрационного треугольника будут проектироваться различные поверхности пространственной диаграммы. Так, поверхности ликвидус проектируются в области (рис. 34): t 1 E 1′E′E 3′ - AE 1 EE 3 t 2 E 1′E′E 2′ - BE 1 EE 2 t 3 E 2′E′E 3′ - CE 2 EE 3, а линейчатые поверхности начала кристаллизации двойных эвтектик в области: АЕЕ 1, ВЕЕ 2, СЕЕ 3, АЕЕ 3. Учитывая изложенные выше рекомендации, построим разрез диаграммы плоскостью t 1 AМt (см. рис. 31, 34, 35). Линия АМ – след пересечения плоскости разреза с концентрационным треугольником. Точки b и p – характерные точки.
Рис. 34 При построении вертикальных разрезов нужно иметь в виду, в какие области концентрационного треугольника будут проектироваться различные поверхности пространственной диаграммы. Так, поверхности ликвидус проектируются в области (рис. 34): t 1 E 1′E′E 3′ - AE 1 EE 3 t 2 E 1′E′E 2′ - BE 1 EE 2 t 3 E 2′E′E 3′ - CE 2 EE 3, а линейчатые поверхности начала кристаллизации двойных эвтектик в области: АЕЕ 1, ВЕЕ 2, СЕЕ 3, АЕЕ 3. Учитывая изложенные выше рекомендации, построим разрез диаграммы плоскостью t 1 AМt (см. рис. 31, 34, 35). Линия АМ – след пересечения плоскости разреза с концентрационным треугольником. Точки b и p – характерные точки.
 Рис. 35 Разрез представлен на рисунке 35. Линии t 1 g и tg – линии ликвидус, линии mg, gr, ru получаются от пересечения разреза с линейчатыми поверхностями начала кристаллизации двойных эвтектик. Линия mg будет прямой, т. к. плоскость разреза проходит через вертикаль Аt 1 и пересечет линейчатую поверхность по одной коноде. Линии gr и ru будут кривыми, т. к. плоскость разреза будет пересекать две другие линейчатые поверхности по нескольким конодам. Линия nrs получится от пересечения разреза с изотермической плоскостью A′B′C′ (рис. 31), на которой лежит точка тройной эвтектики. Фазовые составляющие во всех областях разреза указаны на рис. 35.
Рис. 35 Разрез представлен на рисунке 35. Линии t 1 g и tg – линии ликвидус, линии mg, gr, ru получаются от пересечения разреза с линейчатыми поверхностями начала кристаллизации двойных эвтектик. Линия mg будет прямой, т. к. плоскость разреза проходит через вертикаль Аt 1 и пересечет линейчатую поверхность по одной коноде. Линии gr и ru будут кривыми, т. к. плоскость разреза будет пересекать две другие линейчатые поверхности по нескольким конодам. Линия nrs получится от пересечения разреза с изотермической плоскостью A′B′C′ (рис. 31), на которой лежит точка тройной эвтектики. Фазовые составляющие во всех областях разреза указаны на рис. 35.
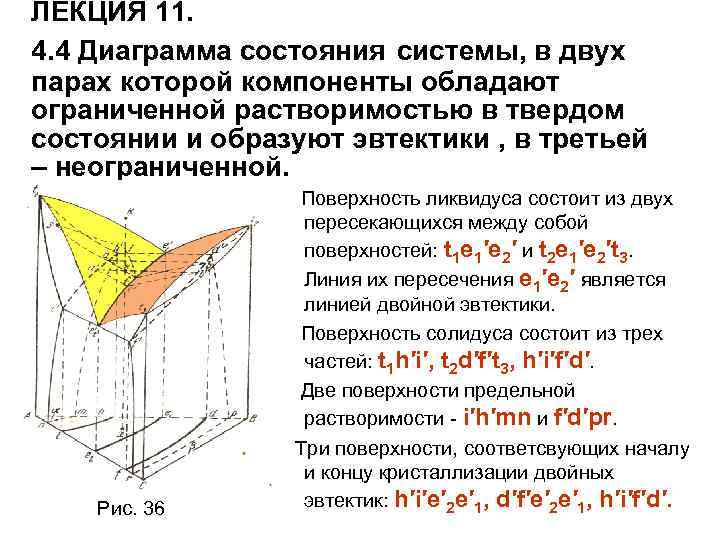 ЛЕКЦИЯ 11. 4. 4 Диаграмма состояния системы, в двух парах которой компоненты обладают ограниченной растворимостью в твердом состоянии и образуют эвтектики , в третьей – неограниченной. Рис. 36 Поверхность ликвидуса состоит из двух пересекающихся между собой поверхностей: t 1 e 1′e 2′ и t 2 e 1′e 2′t 3. Линия их пересечения e 1′e 2′ является линией двойной эвтектики. Поверхность солидуса состоит из трех частей: t 1 h′i′, t 2 d′f′t 3, h′i′f′d′. Две поверхности предельной растворимости - i′h′mn и f′d′pr. Три поверхности, соответсвующих началу и концу кристаллизации двойных эвтектик: h′i′e′ 2 e′ 1, d′f′e′ 2 e′ 1, h′i′f′d′.
ЛЕКЦИЯ 11. 4. 4 Диаграмма состояния системы, в двух парах которой компоненты обладают ограниченной растворимостью в твердом состоянии и образуют эвтектики , в третьей – неограниченной. Рис. 36 Поверхность ликвидуса состоит из двух пересекающихся между собой поверхностей: t 1 e 1′e 2′ и t 2 e 1′e 2′t 3. Линия их пересечения e 1′e 2′ является линией двойной эвтектики. Поверхность солидуса состоит из трех частей: t 1 h′i′, t 2 d′f′t 3, h′i′f′d′. Две поверхности предельной растворимости - i′h′mn и f′d′pr. Три поверхности, соответсвующих началу и концу кристаллизации двойных эвтектик: h′i′e′ 2 e′ 1, d′f′e′ 2 e′ 1, h′i′f′d′.
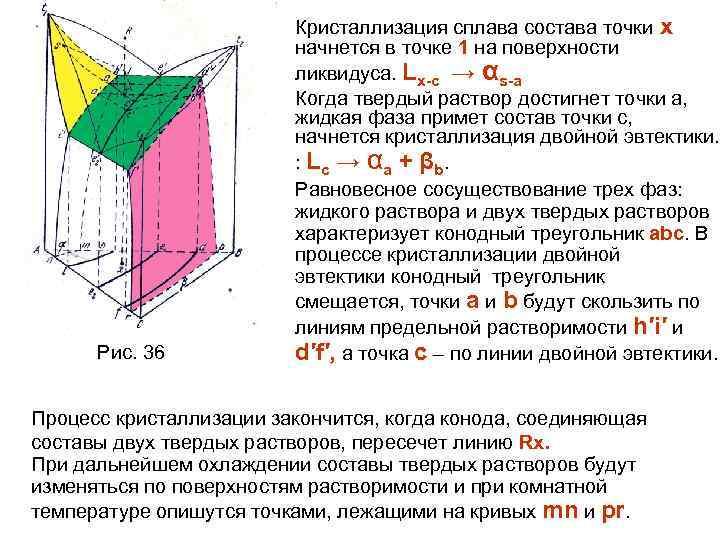 Рис. 36 Кристаллизация сплава состава точки х начнется в точке 1 на поверхности ликвидуса. Lх-с → αs-a Когда твердый раствор достигнет точки а, жидкая фаза примет состав точки с, начнется кристаллизация двойной эвтектики. : L с → αа + β b. Равновесное сосуществование трех фаз: жидкого раствора и двух твердых растворов характеризует конодный треугольник аbc. В процессе кристаллизации двойной эвтектики конодный треугольник смещается, точки a и b будут скользить по линиям предельной растворимости h′i′ и d′f′, а точка с – по линии двойной эвтектики. Процесс кристаллизации закончится, когда конода, соединяющая составы двух твердых растворов, пересечет линию Rx. При дальнейшем охлаждении составы твердых растворов будут изменяться по поверхностям растворимости и при комнатной температуре опишутся точками, лежащими на кривых mn и pr.
Рис. 36 Кристаллизация сплава состава точки х начнется в точке 1 на поверхности ликвидуса. Lх-с → αs-a Когда твердый раствор достигнет точки а, жидкая фаза примет состав точки с, начнется кристаллизация двойной эвтектики. : L с → αа + β b. Равновесное сосуществование трех фаз: жидкого раствора и двух твердых растворов характеризует конодный треугольник аbc. В процессе кристаллизации двойной эвтектики конодный треугольник смещается, точки a и b будут скользить по линиям предельной растворимости h′i′ и d′f′, а точка с – по линии двойной эвтектики. Процесс кристаллизации закончится, когда конода, соединяющая составы двух твердых растворов, пересечет линию Rx. При дальнейшем охлаждении составы твердых растворов будут изменяться по поверхностям растворимости и при комнатной температуре опишутся точками, лежащими на кривых mn и pr.
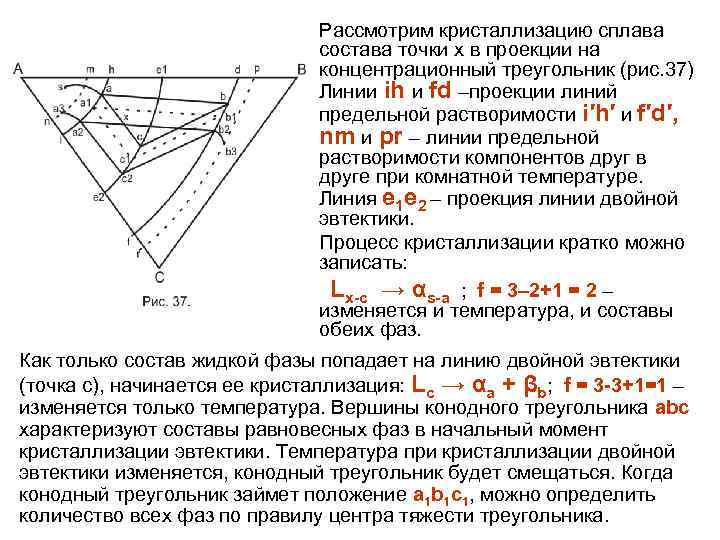 Рассмотрим кристаллизацию сплава состава точки х в проекции на концентрационный треугольник (рис. 37) Линии ih и fd –проекции линий предельной растворимости i′h′ и f′d′, nm и pr – линии предельной растворимости компонентов друге при комнатной температуре. Линия е 1 е 2 – проекция линии двойной эвтектики. Процесс кристаллизации кратко можно записать: Lх-с → αs-a ; f = 3– 2+1 = 2 – изменяется и температура, и составы обеих фаз. Как только состав жидкой фазы попадает на линию двойной эвтектики (точка с), начинается ее кристаллизация: Lс → αа + βb; f = 3 -3+1=1 – изменяется только температура. Вершины конодного треугольника abc характеризуют составы равновесных фаз в начальный момент кристаллизации эвтектики. Температура при кристаллизации двойной эвтектики изменяется, конодный треугольник будет смещаться. Когда конодный треугольник займет положение a 1 b 1 c 1, можно определить количество всех фаз по правилу центра тяжести треугольника.
Рассмотрим кристаллизацию сплава состава точки х в проекции на концентрационный треугольник (рис. 37) Линии ih и fd –проекции линий предельной растворимости i′h′ и f′d′, nm и pr – линии предельной растворимости компонентов друге при комнатной температуре. Линия е 1 е 2 – проекция линии двойной эвтектики. Процесс кристаллизации кратко можно записать: Lх-с → αs-a ; f = 3– 2+1 = 2 – изменяется и температура, и составы обеих фаз. Как только состав жидкой фазы попадает на линию двойной эвтектики (точка с), начинается ее кристаллизация: Lс → αа + βb; f = 3 -3+1=1 – изменяется только температура. Вершины конодного треугольника abc характеризуют составы равновесных фаз в начальный момент кристаллизации эвтектики. Температура при кристаллизации двойной эвтектики изменяется, конодный треугольник будет смещаться. Когда конодный треугольник займет положение a 1 b 1 c 1, можно определить количество всех фаз по правилу центра тяжести треугольника.
 Процесс кристаллизации закончится, когда конодный треугольник займет положение a 2 b 2 c 2 т. е. конода a 2 b 2 пройдет через точку х – в равновесии останутся только твердые растворы. Так как растворимость с понижением температуры уменьшается, то составы твердых растворов будут изменяться по кривым a 2 a 3 и b 2 b 3 и при комнатной температуре опишутся точками a 3 и b 3. . При этом из αраствора будут выделяться вторичные β-кристаллы, а из β-раствора – вторичные α-кристаллы. При комнатной температуре сплав будет состоять из двух фаз: α+β , структурные составляющие: кристаллы α, эвтектика (α+β) и вторичные кристаллы β-твердого раствора.
Процесс кристаллизации закончится, когда конодный треугольник займет положение a 2 b 2 c 2 т. е. конода a 2 b 2 пройдет через точку х – в равновесии останутся только твердые растворы. Так как растворимость с понижением температуры уменьшается, то составы твердых растворов будут изменяться по кривым a 2 a 3 и b 2 b 3 и при комнатной температуре опишутся точками a 3 и b 3. . При этом из αраствора будут выделяться вторичные β-кристаллы, а из β-раствора – вторичные α-кристаллы. При комнатной температуре сплав будет состоять из двух фаз: α+β , структурные составляющие: кристаллы α, эвтектика (α+β) и вторичные кристаллы β-твердого раствора.
 Построим разрез по линии MN. Поверхности пространственной диаграммы (см. рис. 36) будут проектироваться в следующие области концентрационного треугольника (рис. 38): t 1 e 1′e 2′ - Ae 1 e 2 поверхность ликвидуса t 2 e 1′e 2′t 3 - Be 1 e 2 C поверхность солидуса t 1 h′i′ - Ahi поверхность солидуса t 2 d′f′t 3 - Bdf. C поверхность солидуса h′i′f′d′ - hifd поверхность ликвидуса поверхность предельной растворимости h′i′nm - hinm поверхность предельной растворимости f′d′pr - fdpr Характерные точки: s, u, v, q, t. линейчатая поверхность h′i′e′ 2 e′ 1– hie 2 e 1 линейчатая поверхность d′f′e′ 2 e′ 1 - dfe 2 e 1 линейчатая поверхность h′i′f′d′ - hifd.
Построим разрез по линии MN. Поверхности пространственной диаграммы (см. рис. 36) будут проектироваться в следующие области концентрационного треугольника (рис. 38): t 1 e 1′e 2′ - Ae 1 e 2 поверхность ликвидуса t 2 e 1′e 2′t 3 - Be 1 e 2 C поверхность солидуса t 1 h′i′ - Ahi поверхность солидуса t 2 d′f′t 3 - Bdf. C поверхность солидуса h′i′f′d′ - hifd поверхность ликвидуса поверхность предельной растворимости h′i′nm - hinm поверхность предельной растворимости f′d′pr - fdpr Характерные точки: s, u, v, q, t. линейчатая поверхность h′i′e′ 2 e′ 1– hie 2 e 1 линейчатая поверхность d′f′e′ 2 e′ 1 - dfe 2 e 1 линейчатая поверхность h′i′f′d′ - hifd.
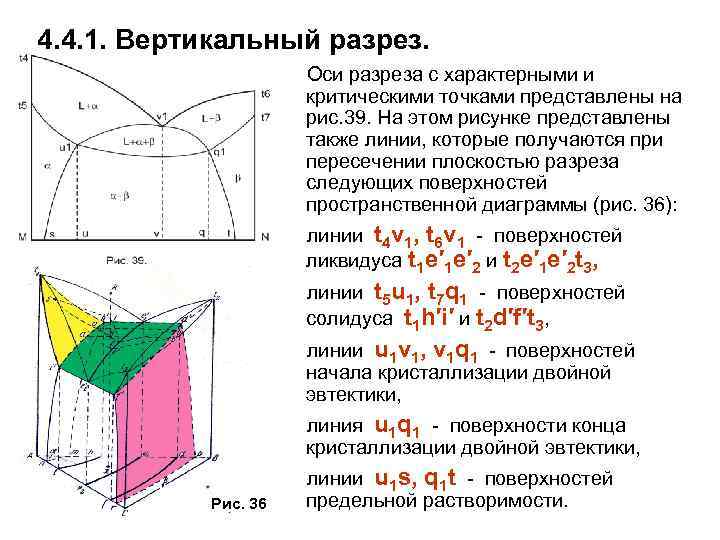 4. 4. 1. Вертикальный разрез. Оси разреза с характерными и критическими точками представлены на рис. 39. На этом рисунке представлены также линии, которые получаются при пересечении плоскостью разреза следующих поверхностей пространственной диаграммы (рис. 36): линии t 4 v 1, t 6 v 1 - поверхностей ликвидуса t 1 e′ 2 и t 2 e′ 1 e′ 2 t 3, линии t 5 u 1, t 7 q 1 - поверхностей солидуса t 1 h′i′ и t 2 d′f′t 3, линии u 1 v 1, v 1 q 1 - поверхностей начала кристаллизации двойной эвтектики, линия u 1 q 1 - поверхности конца кристаллизации двойной эвтектики, Рис. 36 линии u 1 s, q 1 t - поверхностей предельной растворимости.
4. 4. 1. Вертикальный разрез. Оси разреза с характерными и критическими точками представлены на рис. 39. На этом рисунке представлены также линии, которые получаются при пересечении плоскостью разреза следующих поверхностей пространственной диаграммы (рис. 36): линии t 4 v 1, t 6 v 1 - поверхностей ликвидуса t 1 e′ 2 и t 2 e′ 1 e′ 2 t 3, линии t 5 u 1, t 7 q 1 - поверхностей солидуса t 1 h′i′ и t 2 d′f′t 3, линии u 1 v 1, v 1 q 1 - поверхностей начала кристаллизации двойной эвтектики, линия u 1 q 1 - поверхности конца кристаллизации двойной эвтектики, Рис. 36 линии u 1 s, q 1 t - поверхностей предельной растворимости.
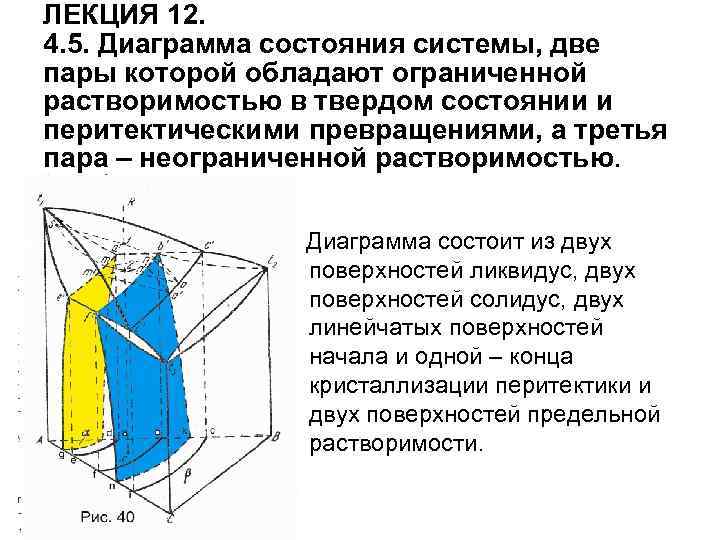 ЛЕКЦИЯ 12. 4. 5. Диаграмма состояния системы, две пары которой обладают ограниченной растворимостью в твердом состоянии и перитектическими превращениями, а третья пара – неограниченной растворимостью. Диаграмма состоит из двух поверхностей ликвидус, двух поверхностей солидус, двух линейчатых поверхностей начала и одной – конца кристаллизации перитектики и двух поверхностей предельной растворимости.
ЛЕКЦИЯ 12. 4. 5. Диаграмма состояния системы, две пары которой обладают ограниченной растворимостью в твердом состоянии и перитектическими превращениями, а третья пара – неограниченной растворимостью. Диаграмма состоит из двух поверхностей ликвидус, двух поверхностей солидус, двух линейчатых поверхностей начала и одной – конца кристаллизации перитектики и двух поверхностей предельной растворимости.
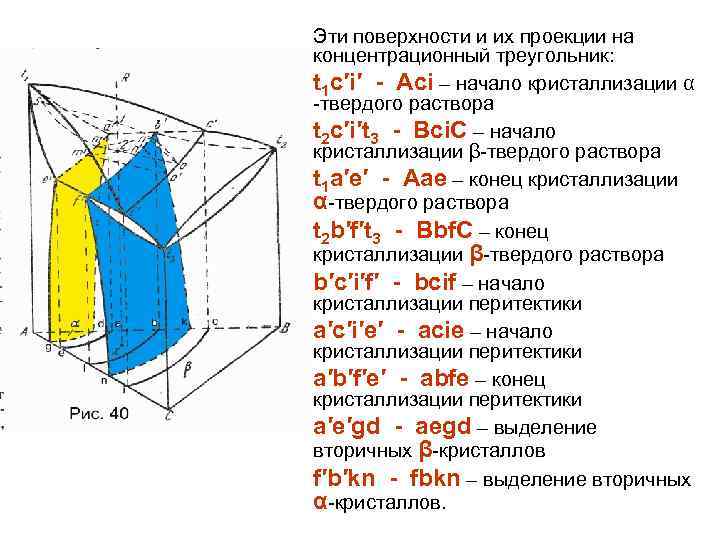 Эти поверхности и их проекции на концентрационный треугольник: t 1 c′i′ - Aci – начало кристаллизации α -твердого раствора t 2 c′i′t 3 - Bci. C – начало кристаллизации β-твердого раствора t 1 a′e′ - Aae – конец кристаллизации α-твердого раствора t 2 b′f′t 3 - Bbf. C – конец кристаллизации β-твердого раствора b′c′i′f′ - bcif – начало кристаллизации перитектики a′c′i′e′ - acie – начало кристаллизации перитектики a′b′f′e′ - abfe – конец кристаллизации перитектики a′e′gd - aegd – выделение вторичных β-кристаллов f′b′kn - fbkn – выделение вторичных α-кристаллов.
Эти поверхности и их проекции на концентрационный треугольник: t 1 c′i′ - Aci – начало кристаллизации α -твердого раствора t 2 c′i′t 3 - Bci. C – начало кристаллизации β-твердого раствора t 1 a′e′ - Aae – конец кристаллизации α-твердого раствора t 2 b′f′t 3 - Bbf. C – конец кристаллизации β-твердого раствора b′c′i′f′ - bcif – начало кристаллизации перитектики a′c′i′e′ - acie – начало кристаллизации перитектики a′b′f′e′ - abfe – конец кристаллизации перитектики a′e′gd - aegd – выделение вторичных β-кристаллов f′b′kn - fbkn – выделение вторичных α-кристаллов.
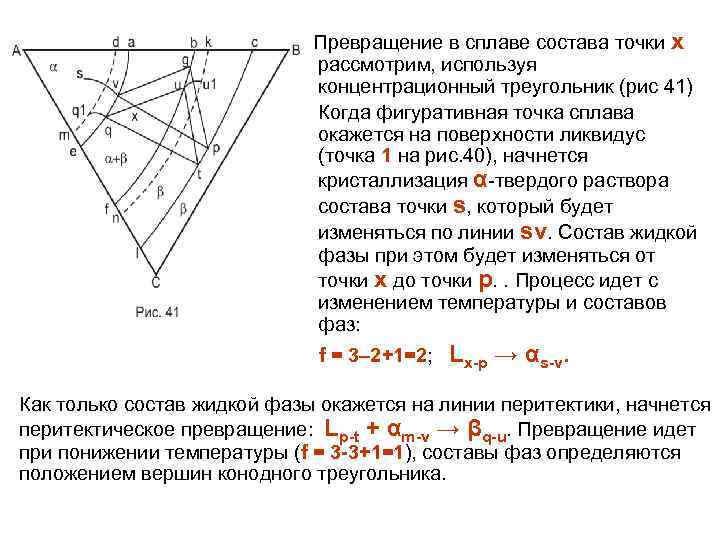 Превращение в сплаве состава точки х рассмотрим, используя концентрационный треугольник (рис 41) Когда фигуративная точка сплава окажется на поверхности ликвидус (точка 1 на рис. 40), начнется кристаллизация α-твердого раствора состава точки s, который будет изменяться по линии sv. Состав жидкой фазы при этом будет изменяться от точки х до точки p. . Процесс идет с изменением температуры и составов фаз: f = 3– 2+1=2; Lx-p → αs-v. Как только состав жидкой фазы окажется на линии перитектики, начнется перитектическое превращение: Lp-t + αm-v → βq-u. Превращение идет при понижении температуры (f = 3 -3+1=1), составы фаз определяются положением вершин конодного треугольника.
Превращение в сплаве состава точки х рассмотрим, используя концентрационный треугольник (рис 41) Когда фигуративная точка сплава окажется на поверхности ликвидус (точка 1 на рис. 40), начнется кристаллизация α-твердого раствора состава точки s, который будет изменяться по линии sv. Состав жидкой фазы при этом будет изменяться от точки х до точки p. . Процесс идет с изменением температуры и составов фаз: f = 3– 2+1=2; Lx-p → αs-v. Как только состав жидкой фазы окажется на линии перитектики, начнется перитектическое превращение: Lp-t + αm-v → βq-u. Превращение идет при понижении температуры (f = 3 -3+1=1), составы фаз определяются положением вершин конодного треугольника.
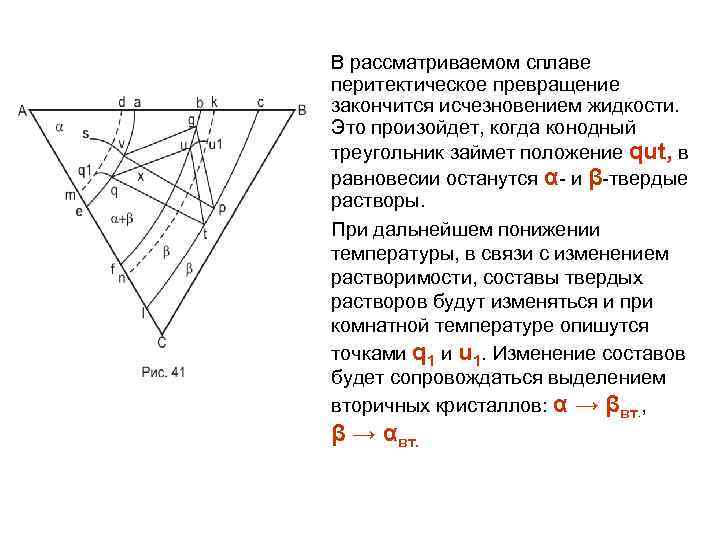 В рассматриваемом сплаве перитектическое превращение закончится исчезновением жидкости. Это произойдет, когда конодный треугольник займет положение qut, в равновесии останутся α- и β-твердые растворы. При дальнейшем понижении температуры, в связи с изменением растворимости, составы твердых растворов будут изменяться и при комнатной температуре опишутся точками q 1 и u 1. Изменение составов будет сопровождаться выделением вторичных кристаллов: α → βвт. , β → αвт.
В рассматриваемом сплаве перитектическое превращение закончится исчезновением жидкости. Это произойдет, когда конодный треугольник займет положение qut, в равновесии останутся α- и β-твердые растворы. При дальнейшем понижении температуры, в связи с изменением растворимости, составы твердых растворов будут изменяться и при комнатной температуре опишутся точками q 1 и u 1. Изменение составов будет сопровождаться выделением вторичных кристаллов: α → βвт. , β → αвт.
 4. 5. 1. вертикальный разрез . Рассмотрим вертикальный разрез по линии АД (рис. 42) Характерные точки: t, s, v, u, p. Линии t 1 m и t 4 m получаются при пересечении поверхностей ликвидуса, а линии t 1 n и t 5 k – поверхностей солидуса. Линии mn и mk получаются от пересечения плоскости разреза с линейчатыми поверхностями начала перитектического превращения, а линия nk – конца превращения. Линии nt и ku получатся при пересечении поверхностей предельной растворимости. Фазы во всех областях разреза указаны на рис. 43.
4. 5. 1. вертикальный разрез . Рассмотрим вертикальный разрез по линии АД (рис. 42) Характерные точки: t, s, v, u, p. Линии t 1 m и t 4 m получаются при пересечении поверхностей ликвидуса, а линии t 1 n и t 5 k – поверхностей солидуса. Линии mn и mk получаются от пересечения плоскости разреза с линейчатыми поверхностями начала перитектического превращения, а линия nk – конца превращения. Линии nt и ku получатся при пересечении поверхностей предельной растворимости. Фазы во всех областях разреза указаны на рис. 43.
 СПИСОК ЛИТЕРАТУРЫ 1. Уманский Я. С. , Скаков Ю. А. Физика металлов. М. , Атомиздат, 1978. 2. Захаров А. М. Диаграммы состояния двойнных и тройных систем. М. , Металлургия, 1990. 3. Горелик С. С. , Дашевский М. Я. Материаловедение полупроводников и металловедение. М. , Металлургия, 1973. 4. Штейнберг С. С. Металловедение. Свердловск, Металлургиздат, 1961.
СПИСОК ЛИТЕРАТУРЫ 1. Уманский Я. С. , Скаков Ю. А. Физика металлов. М. , Атомиздат, 1978. 2. Захаров А. М. Диаграммы состояния двойнных и тройных систем. М. , Металлургия, 1990. 3. Горелик С. С. , Дашевский М. Я. Материаловедение полупроводников и металловедение. М. , Металлургия, 1973. 4. Штейнберг С. С. Металловедение. Свердловск, Металлургиздат, 1961.
 ФЕДЕРАЛЬНОЕ АГЕНСТВО ПО ОБРАЗОВАНИЮ Государственное образовательное учреждение высшего профессионального образования « Уральский государственный университет им. А. М. Горького» Физический факультет Кафедра конденсированного состояния. Лекции по спецкурсу ФИЗИЧЕСКОЕ МАТЕРИАЛОВЕДЕНИЕ часть 1 Диаграммы состояния двойных и тройных сплавов. Составитель доцент, кандидат ф-м наук В. П. Серикова. Екатеринбург, 2010
ФЕДЕРАЛЬНОЕ АГЕНСТВО ПО ОБРАЗОВАНИЮ Государственное образовательное учреждение высшего профессионального образования « Уральский государственный университет им. А. М. Горького» Физический факультет Кафедра конденсированного состояния. Лекции по спецкурсу ФИЗИЧЕСКОЕ МАТЕРИАЛОВЕДЕНИЕ часть 1 Диаграммы состояния двойных и тройных сплавов. Составитель доцент, кандидат ф-м наук В. П. Серикова. Екатеринбург, 2010


