Физический опыт.ppt
- Количество слайдов: 8
 Физический опыт: «Шипучий коктель» Выполнили: Ученики 9 -В класса Харьковской гимназии № 82 Семенкевич Алёна и Линевич Даниил
Физический опыт: «Шипучий коктель» Выполнили: Ученики 9 -В класса Харьковской гимназии № 82 Семенкевич Алёна и Линевич Даниил
 Материалы: • • Для опыта понадобится: таблетка растворимого аспирина, вода, поваренная соль, подсолнечное масло, спирт, краска.
Материалы: • • Для опыта понадобится: таблетка растворимого аспирина, вода, поваренная соль, подсолнечное масло, спирт, краска.
 Цель: • Доказать, и показать на опыте, что три житкости, такие как: соленая вода, спирт и масло не смешиваются между собой. И почему именно они «строятся» в таком порядке. От чего это зависит?
Цель: • Доказать, и показать на опыте, что три житкости, такие как: соленая вода, спирт и масло не смешиваются между собой. И почему именно они «строятся» в таком порядке. От чего это зависит?
 Ход работы: • Наливаем в 1 стакан воду, добавляем соль и красную краску. • Выливаем содержимое 1 стакана в бокал. • Наливаем масло во 2 стакан и через воронку, аккуратно, наливаем в бокал так, что бы масло оказалось поверх соленой воды.
Ход работы: • Наливаем в 1 стакан воду, добавляем соль и красную краску. • Выливаем содержимое 1 стакана в бокал. • Наливаем масло во 2 стакан и через воронку, аккуратно, наливаем в бокал так, что бы масло оказалось поверх соленой воды.
 • Наливаем в 3 стакан спирт и добавляем зеленую краску. • Выливаем из 3 стакана в бокал через воронку так, что бы содержимое оказалось поверх подсолнечного масла. • Бросаем в бокал таблетку аспирина.
• Наливаем в 3 стакан спирт и добавляем зеленую краску. • Выливаем из 3 стакана в бокал через воронку так, что бы содержимое оказалось поверх подсолнечного масла. • Бросаем в бокал таблетку аспирина.
 Почему так происходит? ? ? • Вода, масло и спирт образуют три слоя несмешивающихся жидкостей. Почему они выстраиваются в таком порядке, понятно – вода самая плотная жидкость ρв=1 г/мл, (а если еще и соленая, то почти ρсв=1, 2 г/мл), далее идет масло ρм=0, 9 г/мл, а потом спирт ρс=0, 8 г/мл. Вода со спиртом смешиваются в любых пропорциях, но масло создает между ними непроходимое препятствие. Почему же оно не смешивается ни с одним, ни с другим? Все дело в зарядах. Вы, наверное, помните, что одноименные заряды отталкиваются, а разноименные притягиваются. Молекула воды состоит из одного атома кислорода и двух атомов водорода. Кислород более электроотрицателен (это означает, что он больше любит электроны), и поэтому оттягивает на себя отрицательный заряд, оставляя водороду положительный.
Почему так происходит? ? ? • Вода, масло и спирт образуют три слоя несмешивающихся жидкостей. Почему они выстраиваются в таком порядке, понятно – вода самая плотная жидкость ρв=1 г/мл, (а если еще и соленая, то почти ρсв=1, 2 г/мл), далее идет масло ρм=0, 9 г/мл, а потом спирт ρс=0, 8 г/мл. Вода со спиртом смешиваются в любых пропорциях, но масло создает между ними непроходимое препятствие. Почему же оно не смешивается ни с одним, ни с другим? Все дело в зарядах. Вы, наверное, помните, что одноименные заряды отталкиваются, а разноименные притягиваются. Молекула воды состоит из одного атома кислорода и двух атомов водорода. Кислород более электроотрицателен (это означает, что он больше любит электроны), и поэтому оттягивает на себя отрицательный заряд, оставляя водороду положительный.
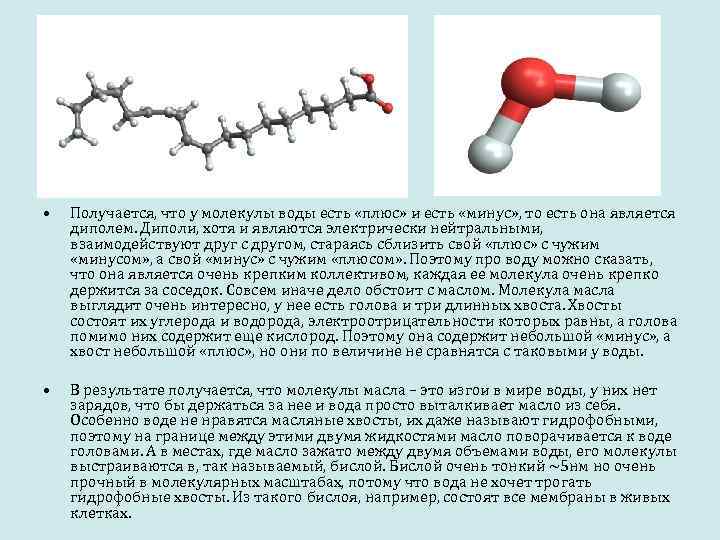 • • Получается, что у молекулы воды есть «плюс» и есть «минус» , то есть она является диполем. Диполи, хотя и являются электрически нейтральными, взаимодействуют друг с другом, стараясь сблизить свой «плюс» с чужим «минусом» , а свой «минус» с чужим «плюсом» . Поэтому про воду можно сказать, что она является очень крепким коллективом, каждая ее молекула очень крепко держится за соседок. Совсем иначе дело обстоит с маслом. Молекула масла выглядит очень интересно, у нее есть голова и три длинных хвоста. Хвосты состоят их углерода и водорода, электроотрицательности которых равны, а голова помимо них содержит еще кислород. Поэтому она содержит небольшой «минус» , а хвост небольшой «плюс» , но они по величине не сравнятся с таковыми у воды. В результате получается, что молекулы масла – это изгои в мире воды, у них нет зарядов, что бы держаться за нее и вода просто выталкивает масло из себя. Особенно воде не нравятся масляные хвосты, их даже называют гидрофобными, поэтому на границе между этими двумя жидкостями масло поворачивается к воде головами. А в местах, где масло зажато между двумя объемами воды, его молекулы выстраиваются в, так называемый, бислой. Бислой очень тонкий ~5 нм но очень прочный в молекулярных масштабах, потому что вода не хочет трогать гидрофобные хвосты. Из такого бислоя, например, состоят все мембраны в живых клетках.
• • Получается, что у молекулы воды есть «плюс» и есть «минус» , то есть она является диполем. Диполи, хотя и являются электрически нейтральными, взаимодействуют друг с другом, стараясь сблизить свой «плюс» с чужим «минусом» , а свой «минус» с чужим «плюсом» . Поэтому про воду можно сказать, что она является очень крепким коллективом, каждая ее молекула очень крепко держится за соседок. Совсем иначе дело обстоит с маслом. Молекула масла выглядит очень интересно, у нее есть голова и три длинных хвоста. Хвосты состоят их углерода и водорода, электроотрицательности которых равны, а голова помимо них содержит еще кислород. Поэтому она содержит небольшой «минус» , а хвост небольшой «плюс» , но они по величине не сравнятся с таковыми у воды. В результате получается, что молекулы масла – это изгои в мире воды, у них нет зарядов, что бы держаться за нее и вода просто выталкивает масло из себя. Особенно воде не нравятся масляные хвосты, их даже называют гидрофобными, поэтому на границе между этими двумя жидкостями масло поворачивается к воде головами. А в местах, где масло зажато между двумя объемами воды, его молекулы выстраиваются в, так называемый, бислой. Бислой очень тонкий ~5 нм но очень прочный в молекулярных масштабах, потому что вода не хочет трогать гидрофобные хвосты. Из такого бислоя, например, состоят все мембраны в живых клетках.
 • А что спирт? Спирт очень похож на воду и также не смешивается с маслом, но все-таки «плюсы» и «минусы» в нем послабее, чем в воде, поэтому спирт лучше растворяет разные неполярные вещества. Зато вода очень хорошо растворяет полярные вещества, например, соли. Соль распадается в воде на катионы и анионы с огромными «плюсами» и «минусами» , которые облепляются со всех сторон водой.
• А что спирт? Спирт очень похож на воду и также не смешивается с маслом, но все-таки «плюсы» и «минусы» в нем послабее, чем в воде, поэтому спирт лучше растворяет разные неполярные вещества. Зато вода очень хорошо растворяет полярные вещества, например, соли. Соль распадается в воде на катионы и анионы с огромными «плюсами» и «минусами» , которые облепляются со всех сторон водой.


