Физические свойства и получение металлов.pptx
- Количество слайдов: 28
 ФИЗИЧЕСКИЕ СВОЙСТВА И ПОЛУЧЕНИЕ МЕТАЛЛОВ Презентация для 9 класса
ФИЗИЧЕСКИЕ СВОЙСТВА И ПОЛУЧЕНИЕ МЕТАЛЛОВ Презентация для 9 класса
 ВАМ ПРЕДСТОИТ: • Узнать, как строение металлов влияет на их физические свойства; • Понять, почему металлы обладают особыми физическими свойствами; • Выяснить, какие металлы являются самыми – самыми; • Познакомиться с общими способами получения металлов;
ВАМ ПРЕДСТОИТ: • Узнать, как строение металлов влияет на их физические свойства; • Понять, почему металлы обладают особыми физическими свойствами; • Выяснить, какие металлы являются самыми – самыми; • Познакомиться с общими способами получения металлов;
 Мы знаем, что • В атомах металлов на внешнем слое небольшое число электронов; • Атомы металла отдают валентные электроны, превращаясь в катионы; • Атомы металла соединяются друг с другом металлической связью; • Атомы металлов, соединенные металлической связью, образуют простые вещества с металлической кристаллической решеткой;
Мы знаем, что • В атомах металлов на внешнем слое небольшое число электронов; • Атомы металла отдают валентные электроны, превращаясь в катионы; • Атомы металла соединяются друг с другом металлической связью; • Атомы металлов, соединенные металлической связью, образуют простые вещества с металлической кристаллической решеткой;
 Свойства зависят от строения Алмаз (атомная кристаллическая решетка) Свойства: • очень твердый, • прозрачный, • не проводит эл. ток.
Свойства зависят от строения Алмаз (атомная кристаллическая решетка) Свойства: • очень твердый, • прозрачный, • не проводит эл. ток.
 Почему металлы проводят Физические свойства электрический ток и тепло? металлов Электропроводность Теплопроводность
Почему металлы проводят Физические свойства электрический ток и тепло? металлов Электропроводность Теплопроводность
 Заполним таблицу Физические свойства металлов Чем обусловлены свойства? У каких металлов наиболее выражены? Электропроводность Наличием «свободных электронов» Ag, Cu, Al Теплопроводность Наличием «свободных электронов» Ag, Cu, Al
Заполним таблицу Физические свойства металлов Чем обусловлены свойства? У каких металлов наиболее выражены? Электропроводность Наличием «свободных электронов» Ag, Cu, Al Теплопроводность Наличием «свободных электронов» Ag, Cu, Al
 Физические свойства Почему металлы блестят? металлов Металлы обладают металлическим блеском
Физические свойства Почему металлы блестят? металлов Металлы обладают металлическим блеском
 Заполним таблицу Физические свойства металлов Чем обусловлены свойства? У каких металлов наиболее выражены? Металлический блеск Электронами Ag, Hg, Pd
Заполним таблицу Физические свойства металлов Чем обусловлены свойства? У каких металлов наиболее выражены? Металлический блеск Электронами Ag, Hg, Pd
 Физические свойства Почему металлы гнутся? металлов Металлы ковки и пластичны
Физические свойства Почему металлы гнутся? металлов Металлы ковки и пластичны
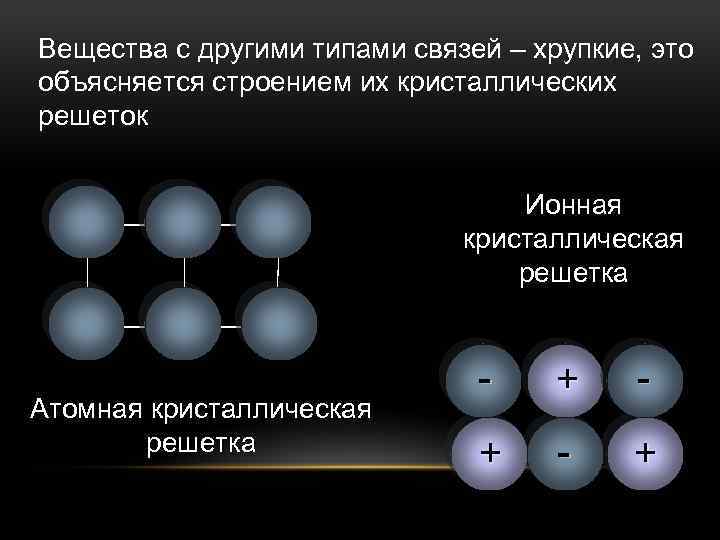 Вещества с другими типами связей – хрупкие, это объясняется строением их кристаллических решеток Ионная кристаллическая решетка Атомная кристаллическая решетка - + - +
Вещества с другими типами связей – хрупкие, это объясняется строением их кристаллических решеток Ионная кристаллическая решетка Атомная кристаллическая решетка - + - +
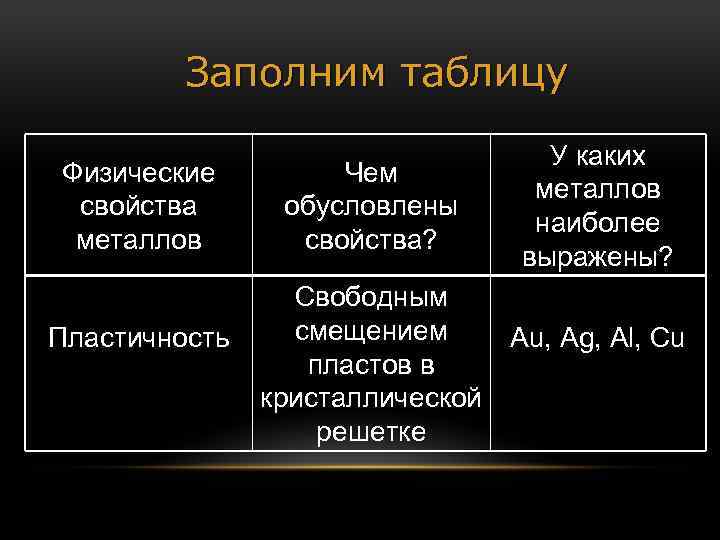 Заполним таблицу Физические свойства металлов Пластичность Чем обусловлены свойства? Свободным смещением пластов в кристаллической решетке У каких металлов наиболее выражены? Au, Ag, Al, Cu
Заполним таблицу Физические свойства металлов Пластичность Чем обусловлены свойства? Свободным смещением пластов в кристаллической решетке У каких металлов наиболее выражены? Au, Ag, Al, Cu
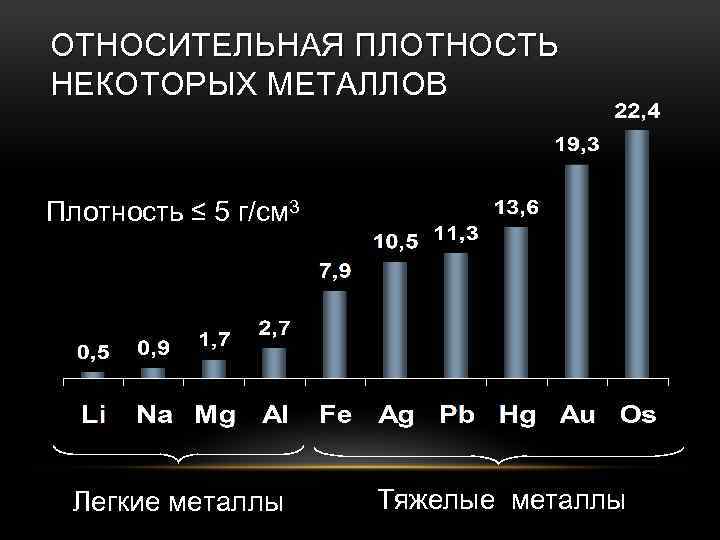 ОТНОСИТЕЛЬНАЯ ПЛОТНОСТЬ НЕКОТОРЫХ МЕТАЛЛОВ Плотность ≤ 5 г/см 3 Легкие металлы Тяжелые металлы
ОТНОСИТЕЛЬНАЯ ПЛОТНОСТЬ НЕКОТОРЫХ МЕТАЛЛОВ Плотность ≤ 5 г/см 3 Легкие металлы Тяжелые металлы
 Заполним таблицу Физические свойства металлов Чем обусловлены свойства? Плотность Атомной массой и радиусом атома У каких металлов наиболее выражены? Легкие: Li, Na, Al Тяжелые: Fe, Pb, Os
Заполним таблицу Физические свойства металлов Чем обусловлены свойства? Плотность Атомной массой и радиусом атома У каких металлов наиболее выражены? Легкие: Li, Na, Al Тяжелые: Fe, Pb, Os
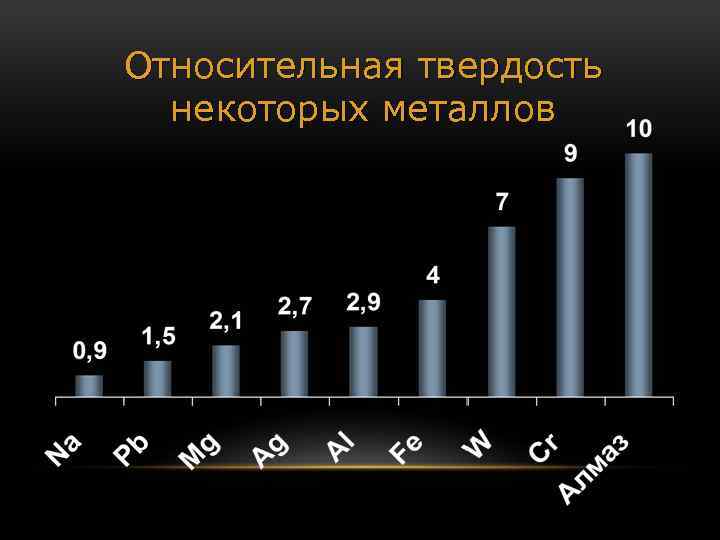 Относительная твердость некоторых металлов
Относительная твердость некоторых металлов
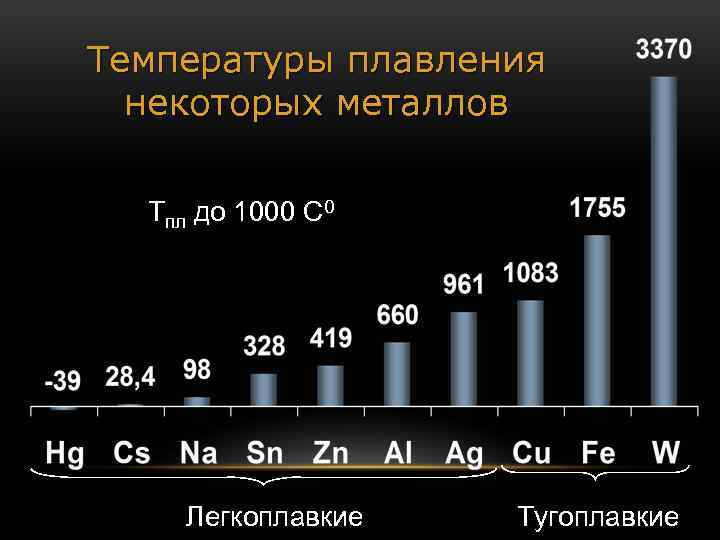 Температуры плавления некоторых металлов Тпл до 1000 С 0 Легкоплавкие Тугоплавкие
Температуры плавления некоторых металлов Тпл до 1000 С 0 Легкоплавкие Тугоплавкие
 Заполним таблицу Физические свойства металлов Твердость Tпл Чем обусловлены свойства? От прочности металлической связи (кол-ва электронов, участвующих в образовании связи) У каких металлов наиболее выражены? W, Cr Легкоплавкие: Cs, Na, Sn Тугоплавкие: Cu, Fe, W
Заполним таблицу Физические свойства металлов Твердость Tпл Чем обусловлены свойства? От прочности металлической связи (кол-ва электронов, участвующих в образовании связи) У каких металлов наиболее выражены? W, Cr Легкоплавкие: Cs, Na, Sn Тугоплавкие: Cu, Fe, W
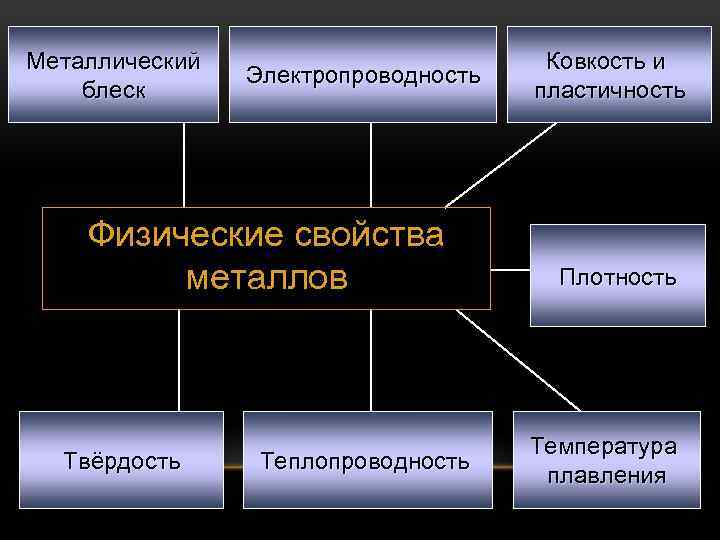 Металлический блеск Электропроводность Физические свойства металлов Твёрдость Теплопроводность Ковкость и пластичность Плотность Температура плавления
Металлический блеск Электропроводность Физические свойства металлов Твёрдость Теплопроводность Ковкость и пластичность Плотность Температура плавления
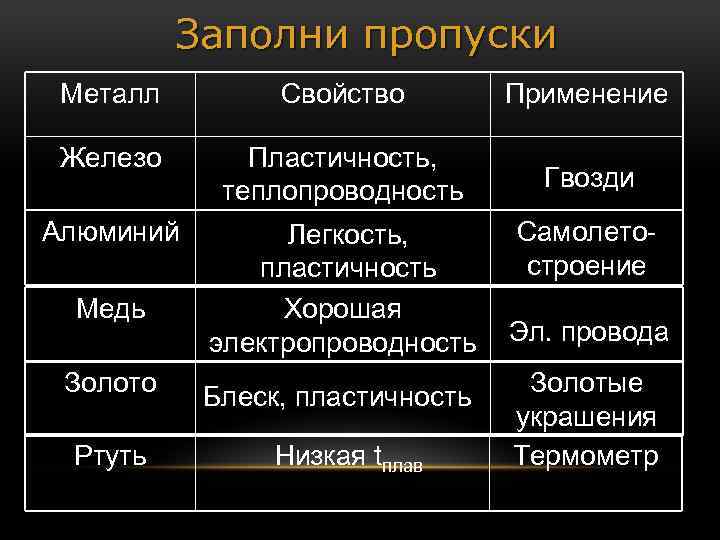 Заполни пропуски Металл Свойство Применение Железо Пластичность, теплопроводность Гвозди Алюминий Легкость, пластичность Хорошая электропроводность Медь Золото Ртуть Блеск, пластичность Низкая tплав Самолетостроение Эл. провода Золотые украшения Термометр
Заполни пропуски Металл Свойство Применение Железо Пластичность, теплопроводность Гвозди Алюминий Легкость, пластичность Хорошая электропроводность Медь Золото Ртуть Блеск, пластичность Низкая tплав Самолетостроение Эл. провода Золотые украшения Термометр
 ОБЩИЕ СПОСОБЫ ПОЛУЧЕНИЯ МЕТАЛЛОВ • Пирометаллургия – получение металлов и сплавов под воздействием высоких температур; • Гидрометаллургия – получение металлов из водных растворов; • Электрометаллургия – получение металлов под действием электрического тока;
ОБЩИЕ СПОСОБЫ ПОЛУЧЕНИЯ МЕТАЛЛОВ • Пирометаллургия – получение металлов и сплавов под воздействием высоких температур; • Гидрометаллургия – получение металлов из водных растворов; • Электрометаллургия – получение металлов под действием электрического тока;
 ПИРОМЕТАЛЛУРГИЯ • Восстановление углем (угарным газом) 2 Pb. O + C → CO 2 + 2 Pb • Восстановление алюминием (кальцием) Cr 2 O 3 + 2 Al → Al 2 O 3 + 2 Cr • Восстановление водородом Cu. O + H 2 → H 2 O + Cu
ПИРОМЕТАЛЛУРГИЯ • Восстановление углем (угарным газом) 2 Pb. O + C → CO 2 + 2 Pb • Восстановление алюминием (кальцием) Cr 2 O 3 + 2 Al → Al 2 O 3 + 2 Cr • Восстановление водородом Cu. O + H 2 → H 2 O + Cu
 ГИДРОМЕТАЛЛУРГИЯ 1 стадия: растворение в кислоте нерастворимых минералов, содержащих металлы: Сu. S + 2 HCl → Cu. Cl 2 + H 2 S 2 стадия: вытеснение металлов из растворов их солей более активными металлами: Cu. Cl 2 + Fe → Fe. Cl 2 + Cu
ГИДРОМЕТАЛЛУРГИЯ 1 стадия: растворение в кислоте нерастворимых минералов, содержащих металлы: Сu. S + 2 HCl → Cu. Cl 2 + H 2 S 2 стадия: вытеснение металлов из растворов их солей более активными металлами: Cu. Cl 2 + Fe → Fe. Cl 2 + Cu
 ЭЛЕКТРОЛИЗ РАСПЛАВОВ КCl ↔ К+ + Cl «-» К+ + 1 e → К 0 2 вос – ие «+» 2 Cl- - 2 e → Cl 20 1 ок – ие эл. ток 2 КCl → 2 К + Cl 2↑ Этим способом в промышленности получают металлы, стоящие в ряду активности до Al
ЭЛЕКТРОЛИЗ РАСПЛАВОВ КCl ↔ К+ + Cl «-» К+ + 1 e → К 0 2 вос – ие «+» 2 Cl- - 2 e → Cl 20 1 ок – ие эл. ток 2 КCl → 2 К + Cl 2↑ Этим способом в промышленности получают металлы, стоящие в ряду активности до Al
 ЭЛЕКТРОЛИЗ РАСТВОРОВ • Катодные процессы Металлы до Аl в ряду активности Восстановление водорода Металлы после Аl до Металлы после Н Н в ряду активности Параллельно идет Восстановление восстановление металла и водорода Ме+ + e → Me 0 2 Н 2 О + 2 e → Н 20↑ + 2 ОН 2 Н 2 О + 2 e = Н 2 + 2 ОН- Ме⁺ + e → Me
ЭЛЕКТРОЛИЗ РАСТВОРОВ • Катодные процессы Металлы до Аl в ряду активности Восстановление водорода Металлы после Аl до Металлы после Н Н в ряду активности Параллельно идет Восстановление восстановление металла и водорода Ме+ + e → Me 0 2 Н 2 О + 2 e → Н 20↑ + 2 ОН 2 Н 2 О + 2 e = Н 2 + 2 ОН- Ме⁺ + e → Me
 ЭЛЕКТРОЛИЗ РАСТВОРОВ • Анодные процессы Бескислородные кислотные остатки (кроме F-) ОН-, кислородсодержащие кислотные остатки и F- Ас-m – me → Ас0 2 Н 2 О – 4 е → О 2 ↑ + 4 Н+
ЭЛЕКТРОЛИЗ РАСТВОРОВ • Анодные процессы Бескислородные кислотные остатки (кроме F-) ОН-, кислородсодержащие кислотные остатки и F- Ас-m – me → Ас0 2 Н 2 О – 4 е → О 2 ↑ + 4 Н+
 ЭЛЕКТРОЛИЗ РАСТВОРОВ Металл стоит в ряду активности после Н Cu. SO 4 Кислотный остаток кислородсодержащий «-» Сu+2 + 2 e → Cu 0 «+» 2 Н 2 О – 4 е → О 2 ↑ + 4 Н+ Эл. ток 2 Cu. SO 4 + 2 Н 2 О → О 2 ↑ + 2 Н 2 SO 4 + 2 Сu
ЭЛЕКТРОЛИЗ РАСТВОРОВ Металл стоит в ряду активности после Н Cu. SO 4 Кислотный остаток кислородсодержащий «-» Сu+2 + 2 e → Cu 0 «+» 2 Н 2 О – 4 е → О 2 ↑ + 4 Н+ Эл. ток 2 Cu. SO 4 + 2 Н 2 О → О 2 ↑ + 2 Н 2 SO 4 + 2 Сu
 Электролиз растворов Металл стоит в ряду активности до Al Na 2 SO 4 Кислотный остаток кислородсодержащий «-» 2 Н 2 О + 2 e → Н 20↑ + 2 ОН «+» 2 Н 2 О – 4 е → О 2 ↑ + 4 Н+ Эл. ток Na 2 SO 4 + 2 Н 2 О → О 2↑ + Na 2 SO 4 + 2 H 2↑ Соль не участвует в электролизе, идет электролиз воды!
Электролиз растворов Металл стоит в ряду активности до Al Na 2 SO 4 Кислотный остаток кислородсодержащий «-» 2 Н 2 О + 2 e → Н 20↑ + 2 ОН «+» 2 Н 2 О – 4 е → О 2 ↑ + 4 Н+ Эл. ток Na 2 SO 4 + 2 Н 2 О → О 2↑ + Na 2 SO 4 + 2 H 2↑ Соль не участвует в электролизе, идет электролиз воды!
 Электролиз растворов Металл стоит в ряду активности до Al К 2 S Кислотный остаток бескислородный «-» 2 Н 2 О + 2 e → Н 20↑ + 2 ОН «+» S-2 – 2 е → S 0 Эл. ток К 2 S + 2 Н 2 О → H 2↑ + 2 КОН + S
Электролиз растворов Металл стоит в ряду активности до Al К 2 S Кислотный остаток бескислородный «-» 2 Н 2 О + 2 e → Н 20↑ + 2 ОН «+» S-2 – 2 е → S 0 Эл. ток К 2 S + 2 Н 2 О → H 2↑ + 2 КОН + S



