Физическая химия коллоидных систем.ppt
- Количество слайдов: 54
 Физическая химия поверхностных явлений и коллоидных систем Лекция № 2 «Коллоиды и их значение в медицине» Доцент к. х. н. Меркушева Л. А.
Физическая химия поверхностных явлений и коллоидных систем Лекция № 2 «Коллоиды и их значение в медицине» Доцент к. х. н. Меркушева Л. А.
 Таблица 1. Классификация коллоидных систем по размеру частиц 10 -9 -10 -7 (м) 10 -6 -10 -4 (м) Высокодисперсные системы: Среднедисперсные коллоидные Ультрамикрогетерогенная дисперсность (золи коллоидные растворы) системы: Микрогетерогенная системы: или дисперсность(суспензии, эмульс ии) Коллоиды – это микрогетерогенные системы, содержащие вещества в высокодисперсном состоянии (от 10 -9 -10 -4 м).
Таблица 1. Классификация коллоидных систем по размеру частиц 10 -9 -10 -7 (м) 10 -6 -10 -4 (м) Высокодисперсные системы: Среднедисперсные коллоидные Ультрамикрогетерогенная дисперсность (золи коллоидные растворы) системы: Микрогетерогенная системы: или дисперсность(суспензии, эмульс ии) Коллоиды – это микрогетерогенные системы, содержащие вещества в высокодисперсном состоянии (от 10 -9 -10 -4 м).
 Таблица 2 Примеры Дисперсных Систем Грунты: песчаные пылеватые Эритроциты крови человека Кишечная палочка Вирус гриппа Золь золота Дым (древесный уголь) Вирус ящура Молекула гликогена Тонкие поры угля 10 -9 м = 1 нм Размер частиц >5000 нм 100 – 5000 нм 700 нм 300 нм 10 нм – 100 нм 20 нм – 50 нм 30 – 40 нм 10 нм 1 – 10 нм
Таблица 2 Примеры Дисперсных Систем Грунты: песчаные пылеватые Эритроциты крови человека Кишечная палочка Вирус гриппа Золь золота Дым (древесный уголь) Вирус ящура Молекула гликогена Тонкие поры угля 10 -9 м = 1 нм Размер частиц >5000 нм 100 – 5000 нм 700 нм 300 нм 10 нм – 100 нм 20 нм – 50 нм 30 – 40 нм 10 нм 1 – 10 нм
 Эритроциты крови человека видны через микроскоп
Эритроциты крови человека видны через микроскоп
 Кровь – сложная дисперсная система • Дисперсионная среда – плазма крови - крови состоит из воды (92%), в которой содержатся (92%) хорошо растворимые органические продукты белки (6%), (6%) метаболизма, метаболизма неорганические компоненты в виде ионов Na+ , K+ , Ca 2+ , Mg 2+ , Cl- , SO 42 - , H 2 PO 4 - и др. (2%)
Кровь – сложная дисперсная система • Дисперсионная среда – плазма крови - крови состоит из воды (92%), в которой содержатся (92%) хорошо растворимые органические продукты белки (6%), (6%) метаболизма, метаболизма неорганические компоненты в виде ионов Na+ , K+ , Ca 2+ , Mg 2+ , Cl- , SO 42 - , H 2 PO 4 - и др. (2%)
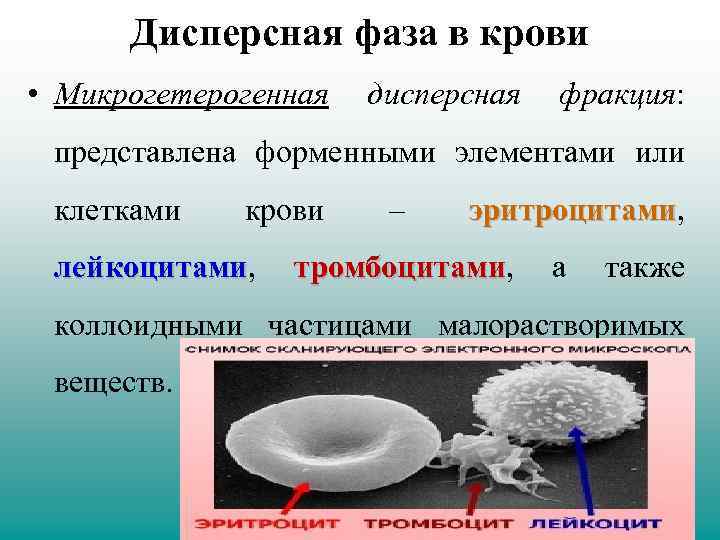 Дисперсная фаза в крови • Микрогетерогенная дисперсная фракция: представлена форменными элементами или клетками крови – эритроцитами, эритроцитами лейкоцитами, тромбоцитами, а также лейкоцитами тромбоцитами коллоидными частицами малорастворимых веществ.
Дисперсная фаза в крови • Микрогетерогенная дисперсная фракция: представлена форменными элементами или клетками крови – эритроцитами, эритроцитами лейкоцитами, тромбоцитами, а также лейкоцитами тромбоцитами коллоидными частицами малорастворимых веществ.
 • Коллоидная ультрамикрогетерогенная фракция – мицеллы липопротеинов, мицеллы белков и нерастворимые в воде ураты (кальциевые соли мочевой кислоты), лиофилизованные адсорбированными макромолекулами растворенных белков
• Коллоидная ультрамикрогетерогенная фракция – мицеллы липопротеинов, мицеллы белков и нерастворимые в воде ураты (кальциевые соли мочевой кислоты), лиофилизованные адсорбированными макромолекулами растворенных белков
 Коллоидно - дисперсные системы классифицируются: • По агрегатному состоянию дисперсионной среды: газ - аэрозоли , среды жидкость - лиозоли, вода – гидрозоли, лиозоли гидрозоли твердое вещество -солидозоли • По диапазону дисперсности: дисперсности монодисперсные (а) (одинаковый монодисперсные размер частиц; ) и полидисперсные (б).
Коллоидно - дисперсные системы классифицируются: • По агрегатному состоянию дисперсионной среды: газ - аэрозоли , среды жидкость - лиозоли, вода – гидрозоли, лиозоли гидрозоли твердое вещество -солидозоли • По диапазону дисперсности: дисперсности монодисперсные (а) (одинаковый монодисперсные размер частиц; ) и полидисперсные (б).
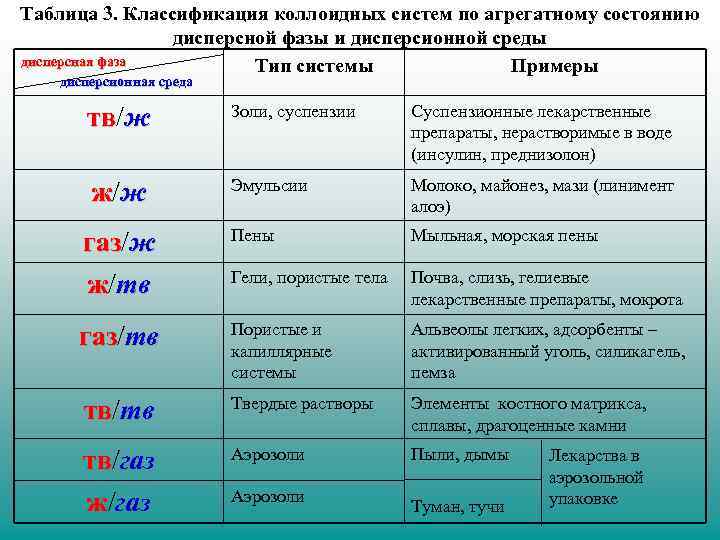 Таблица 3. Классификация коллоидных систем по агрегатному состоянию дисперсной фазы и дисперсионной среды дисперсная фаза Тип системы Примеры дисперсионная среда тв/ж тв Золи, суспензии Суспензионные лекарственные препараты, нерастворимые в воде (инсулин, преднизолон) ж/ ж Эмульсии Молоко, майонез, мази (линимент алоэ) газ/ж газ ж/тв Пены Мыльная, морская пены Гели, пористые тела Почва, слизь, гелиевые лекарственные препараты, мокрота газ/тв газ Пористые и капиллярные системы Альвеолы легких, адсорбенты – активированный уголь, силикагель, пемза тв/тв тв Твердые растворы Элементы костного матрикса, сплавы, драгоценные камни тв/газ тв ж/газ Аэрозоли Пыли, дымы Аэрозоли Туман, тучи Лекарства в аэрозольной упаковке
Таблица 3. Классификация коллоидных систем по агрегатному состоянию дисперсной фазы и дисперсионной среды дисперсная фаза Тип системы Примеры дисперсионная среда тв/ж тв Золи, суспензии Суспензионные лекарственные препараты, нерастворимые в воде (инсулин, преднизолон) ж/ ж Эмульсии Молоко, майонез, мази (линимент алоэ) газ/ж газ ж/тв Пены Мыльная, морская пены Гели, пористые тела Почва, слизь, гелиевые лекарственные препараты, мокрота газ/тв газ Пористые и капиллярные системы Альвеолы легких, адсорбенты – активированный уголь, силикагель, пемза тв/тв тв Твердые растворы Элементы костного матрикса, сплавы, драгоценные камни тв/газ тв ж/газ Аэрозоли Пыли, дымы Аэрозоли Туман, тучи Лекарства в аэрозольной упаковке
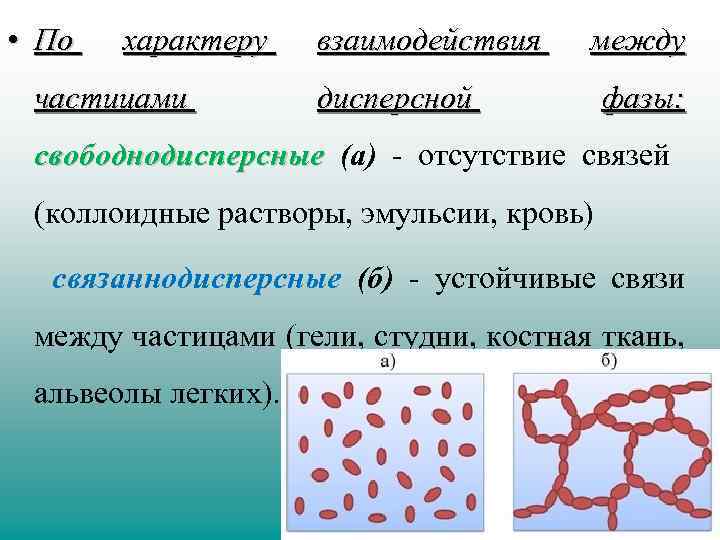 • По характеру частицами взаимодействия дисперсной между фазы: свободнодисперсные (а) - отсутствие связей свободнодисперсные (коллоидные растворы, эмульсии, кровь) связаннодисперсные (б) - устойчивые связи между частицами (гели, студни, костная ткань, альвеолы легких).
• По характеру частицами взаимодействия дисперсной между фазы: свободнодисперсные (а) - отсутствие связей свободнодисперсные (коллоидные растворы, эмульсии, кровь) связаннодисперсные (б) - устойчивые связи между частицами (гели, студни, костная ткань, альвеолы легких).
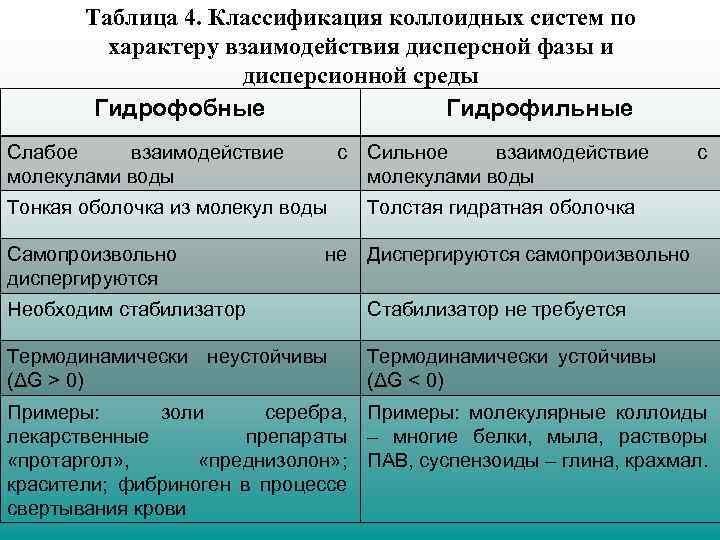 Таблица 4. Классификация коллоидных систем по характеру взаимодействия дисперсной фазы и дисперсионной среды Гидрофобные Гидрофильные Слабое взаимодействие молекулами воды с Сильное взаимодействие молекулами воды Тонкая оболочка из молекул воды Самопроизвольно диспергируются с Толстая гидратная оболочка не Диспергируются самопроизвольно Необходим стабилизатор Стабилизатор не требуется Термодинамически неустойчивы (ΔG > 0) Термодинамически устойчивы (ΔG ˂ 0) Примеры: золи серебра, Примеры: молекулярные коллоиды лекарственные препараты – многие белки, мыла, растворы «протаргол» , «преднизолон» ; ПАВ, суспензоиды – глина, крахмал. красители; фибриноген в процессе свертывания крови
Таблица 4. Классификация коллоидных систем по характеру взаимодействия дисперсной фазы и дисперсионной среды Гидрофобные Гидрофильные Слабое взаимодействие молекулами воды с Сильное взаимодействие молекулами воды Тонкая оболочка из молекул воды Самопроизвольно диспергируются с Толстая гидратная оболочка не Диспергируются самопроизвольно Необходим стабилизатор Стабилизатор не требуется Термодинамически неустойчивы (ΔG > 0) Термодинамически устойчивы (ΔG ˂ 0) Примеры: золи серебра, Примеры: молекулярные коллоиды лекарственные препараты – многие белки, мыла, растворы «протаргол» , «преднизолон» ; ПАВ, суспензоиды – глина, крахмал. красители; фибриноген в процессе свертывания крови
 Таблица 5. Сравнение свойств истинных растворов и коллоидных систем Коллоидные системы Эмульсии, суспензии 10 -4 – 10 -6 м Истинные растворы Коллоидные растворы (лиозоли) 10 -7 – 10 -9 м 10 -10 – 10 -12 м Гомогенные Гетерогенные Не проникают через поры растительных и животных Проникают через любые мембраны Частицы видимы в Частицы видимы микроскоп ультрамикроскоп Не фильтруются бумажный фильтр в Частицы не видимы ультрамикроскоп в через Фильтруются через бумажный Фильтруются через любые фильтры Непрозрачные Рассеивание опалесцируют света, Прозрачные Отражают свет Дают четкий конус Тиндаля, Неустойчивы, расслаиваются Относительно устойчивы, Устойчивы, расслаиваются со временем не расслаиваются Оптически пусты
Таблица 5. Сравнение свойств истинных растворов и коллоидных систем Коллоидные системы Эмульсии, суспензии 10 -4 – 10 -6 м Истинные растворы Коллоидные растворы (лиозоли) 10 -7 – 10 -9 м 10 -10 – 10 -12 м Гомогенные Гетерогенные Не проникают через поры растительных и животных Проникают через любые мембраны Частицы видимы в Частицы видимы микроскоп ультрамикроскоп Не фильтруются бумажный фильтр в Частицы не видимы ультрамикроскоп в через Фильтруются через бумажный Фильтруются через любые фильтры Непрозрачные Рассеивание опалесцируют света, Прозрачные Отражают свет Дают четкий конус Тиндаля, Неустойчивы, расслаиваются Относительно устойчивы, Устойчивы, расслаиваются со временем не расслаиваются Оптически пусты
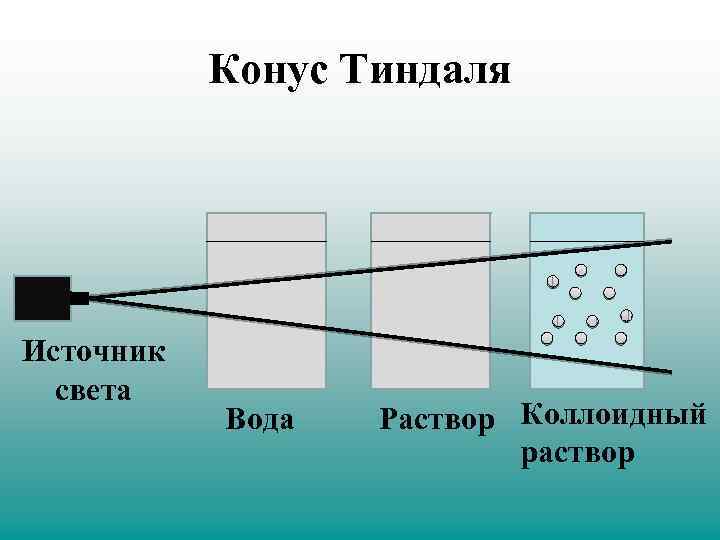 Конус Тиндаля Источник света Вода Раствор Коллоидный раствор
Конус Тиндаля Источник света Вода Раствор Коллоидный раствор
 Устойчивость коллоидов Коллоидные системы принципиально неустойчивы, т. к. вследствие малых размеров частиц и огромных площадей поверхности раздела обладают большим запасом поверхностной свободной энергии Гиббса Gs. Gсистемы = ΔGV + ΔGs Gs = σ. ΔSуд Δ Δ Sуд = Sобщая д. ф / Vд. ф
Устойчивость коллоидов Коллоидные системы принципиально неустойчивы, т. к. вследствие малых размеров частиц и огромных площадей поверхности раздела обладают большим запасом поверхностной свободной энергии Гиббса Gs. Gсистемы = ΔGV + ΔGs Gs = σ. ΔSуд Δ Δ Sуд = Sобщая д. ф / Vд. ф
 Седиментационная устойчивость Скорость оседания частиц определяется: (м/с) где g – ускорение силы тяжести (9, 8 м/с2); r – радиус частиц (м); η – вязкость среды (Н. с/м 2) ρд. ф. – плотность дисперсионной фазы (кг/м 2) ρд. с. – плотность дисперсионной среды (кг/м 2)
Седиментационная устойчивость Скорость оседания частиц определяется: (м/с) где g – ускорение силы тяжести (9, 8 м/с2); r – радиус частиц (м); η – вязкость среды (Н. с/м 2) ρд. ф. – плотность дисперсионной фазы (кг/м 2) ρд. с. – плотность дисперсионной среды (кг/м 2)
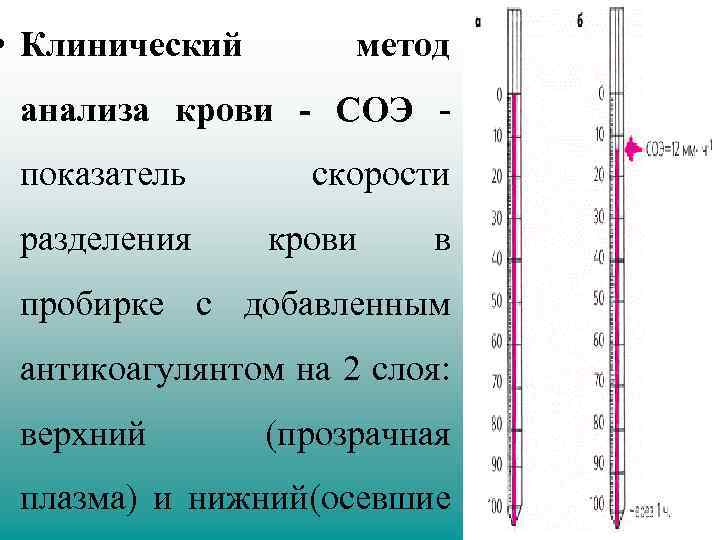 • Клинический метод анализа крови - СОЭ - показатель разделения скорости крови в пробирке с добавленным антикоагулянтом на 2 слоя: верхний (прозрачная плазма) и нижний(осевшие
• Клинический метод анализа крови - СОЭ - показатель разделения скорости крови в пробирке с добавленным антикоагулянтом на 2 слоя: верхний (прозрачная плазма) и нижний(осевшие
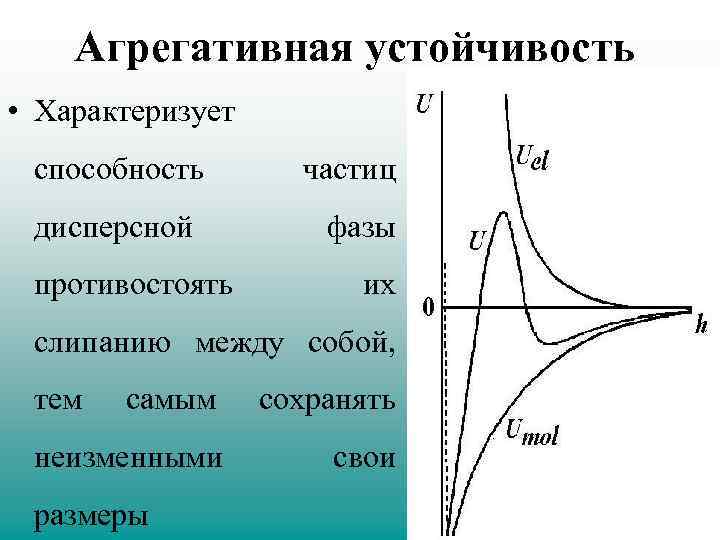 Агрегативная устойчивость • Характеризует способность дисперсной противостоять частиц фазы их слипанию между собой, тем самым сохранять неизменными свои размеры
Агрегативная устойчивость • Характеризует способность дисперсной противостоять частиц фазы их слипанию между собой, тем самым сохранять неизменными свои размеры
 • Полная энергия взаимодействия дисперсных частиц U представляет сумму энергий притяжения и отталкивания U=Umol +Uel(рис. 1). Поскольку энергии притяжения и отталкивания имеют разные знаки и по-разному зависят от толщины разделяющей частицы жидкой пленки, зависимость суммарной энергии U(h) имеет сложный вид с минимумом на больших расстояниях и максимумом на средних. Кроме того, существует первичный, или ближний, минимум (обозначенный пунктиром на рис. 1), связанный с возникновением на малых расстояниях сил отталкивания, не учтенных в теории ДЛФО. Вид зависимости U(h)показывает, что притяжение преобладает на больших и малых расстояниях, а на средних существует потенциальный барьер, препятствующий сближению частиц. Чем выше высота барьера, тем больше агрегативная устойчивость системы.
• Полная энергия взаимодействия дисперсных частиц U представляет сумму энергий притяжения и отталкивания U=Umol +Uel(рис. 1). Поскольку энергии притяжения и отталкивания имеют разные знаки и по-разному зависят от толщины разделяющей частицы жидкой пленки, зависимость суммарной энергии U(h) имеет сложный вид с минимумом на больших расстояниях и максимумом на средних. Кроме того, существует первичный, или ближний, минимум (обозначенный пунктиром на рис. 1), связанный с возникновением на малых расстояниях сил отталкивания, не учтенных в теории ДЛФО. Вид зависимости U(h)показывает, что притяжение преобладает на больших и малых расстояниях, а на средних существует потенциальный барьер, препятствующий сближению частиц. Чем выше высота барьера, тем больше агрегативная устойчивость системы.
 Методы получения коллоидных систем 1. 2. Диспергационный метод – дробление крупных частиц вещества до требуемой дисперсности. Конденсационный метод – объединение молекул или ионов в агрегаты коллоидных размеров. Способы достижения коллоидной степени дисперсности Грубодисперсная Коллоидно. Истинный раствор система дисперсная система d>10 -4 м d<10 -9 м 10 -4
Методы получения коллоидных систем 1. 2. Диспергационный метод – дробление крупных частиц вещества до требуемой дисперсности. Конденсационный метод – объединение молекул или ионов в агрегаты коллоидных размеров. Способы достижения коллоидной степени дисперсности Грубодисперсная Коллоидно. Истинный раствор система дисперсная система d>10 -4 м d<10 -9 м 10 -4
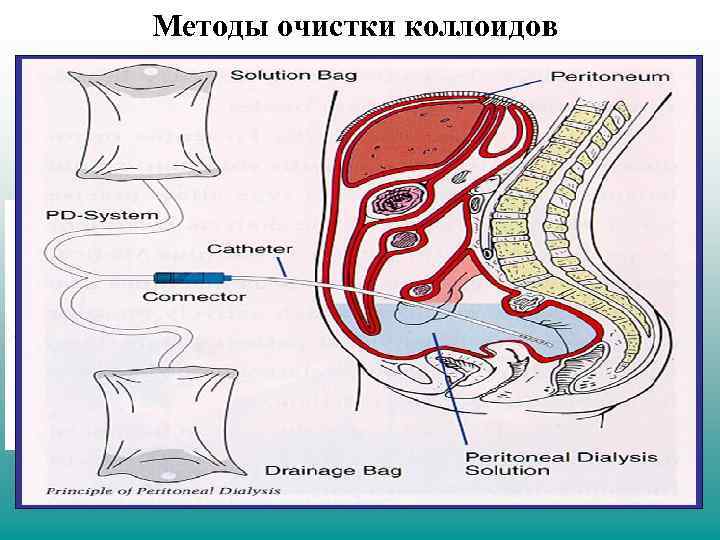 Методы очистки коллоидов Диализ - освобождение коллоидных растворов от примесей, способных проникать через растительные, животные и искусственные мембраны Гемодиализ – диализ крови, осуществляемый для удаления токсинов, образующихся при нарушении функций организма или при отравлениях. Общая схема диализатора Гремма
Методы очистки коллоидов Диализ - освобождение коллоидных растворов от примесей, способных проникать через растительные, животные и искусственные мембраны Гемодиализ – диализ крови, осуществляемый для удаления токсинов, образующихся при нарушении функций организма или при отравлениях. Общая схема диализатора Гремма
 Очистка крови в организме происходит в нефронах по принципу ультрафильтрации. Ультрафильтрация – это диализ под давлением, градиент которого создается либо повышением давления во внутреннем сосуде, содержащем очищаемую дисперсную систему, или разрежением во внешнем сосуде, содержащем растворитель. На принципе гемодиализа и ультрафильтрации основано действие аппарата «искусственная почка» , применяемого для детоксикации организма при заболеваниях почек и острых отравлениях.
Очистка крови в организме происходит в нефронах по принципу ультрафильтрации. Ультрафильтрация – это диализ под давлением, градиент которого создается либо повышением давления во внутреннем сосуде, содержащем очищаемую дисперсную систему, или разрежением во внешнем сосуде, содержащем растворитель. На принципе гемодиализа и ультрафильтрации основано действие аппарата «искусственная почка» , применяемого для детоксикации организма при заболеваниях почек и острых отравлениях.
 Конденсационные методы получения коллоидов 1. Физическая конденсация (например, метод замены растворителя, применяемый для получения коллоидных растворов белков) 2. Химическая конденсация (золь получается в результате химической сопровождающейся реакции, образованием нерастворимого соединения при избытке
Конденсационные методы получения коллоидов 1. Физическая конденсация (например, метод замены растворителя, применяемый для получения коллоидных растворов белков) 2. Химическая конденсация (золь получается в результате химической сопровождающейся реакции, образованием нерастворимого соединения при избытке
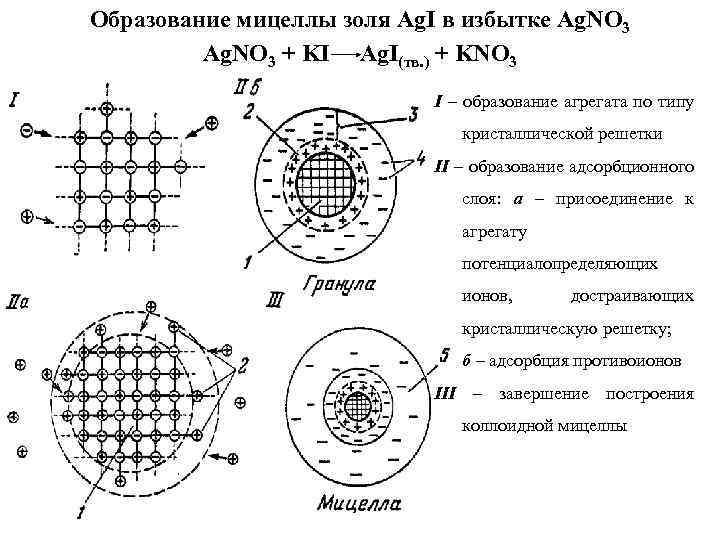 Образование мицеллы золя Ag. I в избытке Ag. NO 3 + KI Ag. I(тв. ) + KNO 3 I – образование агрегата по типу кристаллической решетки II – образование адсорбционного слоя: а – присоединение к агрегату потенциалопределяющих ионов, достраивающих кристаллическую решетку; б – адсорбция противоионов III – завершение построения коллоидной мицеллы
Образование мицеллы золя Ag. I в избытке Ag. NO 3 + KI Ag. I(тв. ) + KNO 3 I – образование агрегата по типу кристаллической решетки II – образование адсорбционного слоя: а – присоединение к агрегату потенциалопределяющих ионов, достраивающих кристаллическую решетку; б – адсорбция противоионов III – завершение построения коллоидной мицеллы
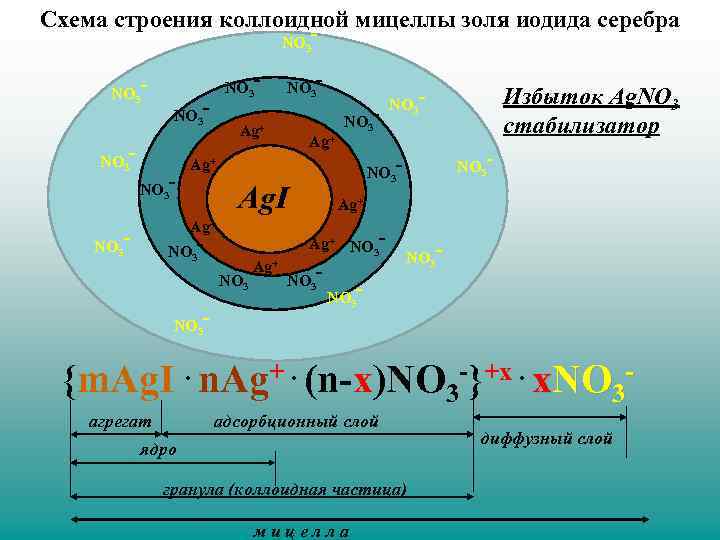 Схема строения коллоидной мицеллы золя иодида серебра - NO 3 - - NO 3 - 3 Ag+ - NO 3 - - NO NO 3 3 Ag. I NO Избыток Ag. NO 3 стабилизатор - NO 3 3 Ag+ Ag+ - NO Ag+ NO 3 - NO 3 Ag+ NO 3 - - NO 3 {m. Ag. I. n. Ag+. (n-x)NO 3 -}+x. x. NO 3 агрегат адсорбционный слой ядро гранула (коллоидная частица) м и ц е л л а диффузный слой
Схема строения коллоидной мицеллы золя иодида серебра - NO 3 - - NO 3 - 3 Ag+ - NO 3 - - NO NO 3 3 Ag. I NO Избыток Ag. NO 3 стабилизатор - NO 3 3 Ag+ Ag+ - NO Ag+ NO 3 - NO 3 Ag+ NO 3 - - NO 3 {m. Ag. I. n. Ag+. (n-x)NO 3 -}+x. x. NO 3 агрегат адсорбционный слой ядро гранула (коллоидная частица) м и ц е л л а диффузный слой
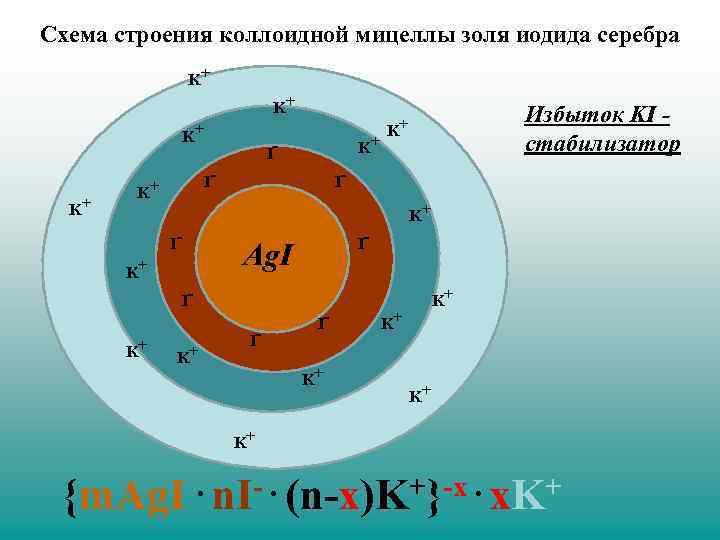 Схема строения коллоидной мицеллы золя иодида серебра K+ K+ I- I- Ag. I K+ IK+ K+ I- Избыток KI - стабилизатор K+ K+ I- IK+ K+ K+ {m. Ag. I . n. I-. (n-x)K+}-x. x. K+ (n-x)K
Схема строения коллоидной мицеллы золя иодида серебра K+ K+ I- I- Ag. I K+ IK+ K+ I- Избыток KI - стабилизатор K+ K+ I- IK+ K+ K+ {m. Ag. I . n. I-. (n-x)K+}-x. x. K+ (n-x)K
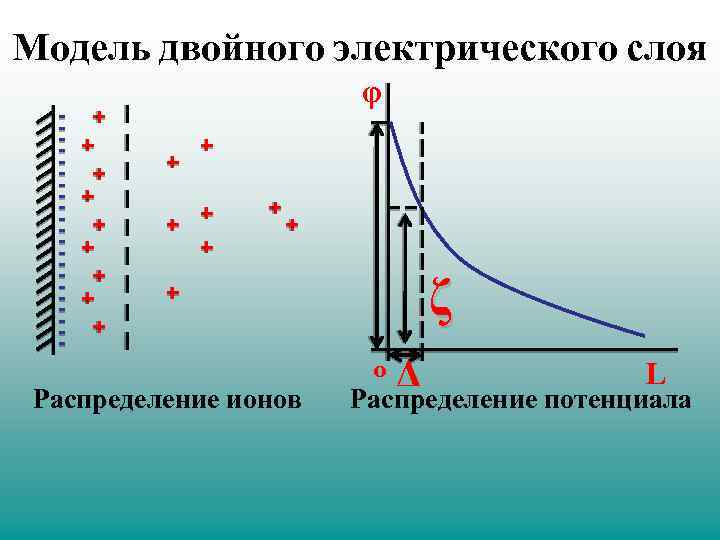 Модель двойного электрического слоя φ ζ 0 Распределение ионов Δ L Распределение потенциала
Модель двойного электрического слоя φ ζ 0 Распределение ионов Δ L Распределение потенциала
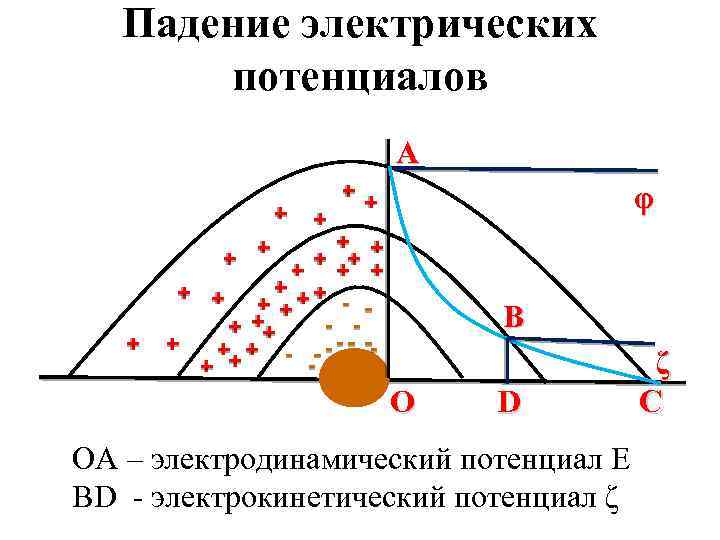 Падение электрических потенциалов А φ В O D ОА – электродинамический потенциал Е BD - электрокинетический потенциал ζ ζ C
Падение электрических потенциалов А φ В O D ОА – электродинамический потенциал Е BD - электрокинетический потенциал ζ ζ C
 ζ –потенциал (дзета) – мера устойчивости коллоидных систем и белков. Чем больше электрокинетический потенциал ζ, тем устойчивее коллоид. ε - относительная диэлектрическая проницаемость Н - напряженность электрического поля (В) η - вязкость среды (Н. с/м 2) υ - электрофоретическая скорость (подвижность) частиц, замеряемая экспериментально (м/с)
ζ –потенциал (дзета) – мера устойчивости коллоидных систем и белков. Чем больше электрокинетический потенциал ζ, тем устойчивее коллоид. ε - относительная диэлектрическая проницаемость Н - напряженность электрического поля (В) η - вязкость среды (Н. с/м 2) υ - электрофоретическая скорость (подвижность) частиц, замеряемая экспериментально (м/с)
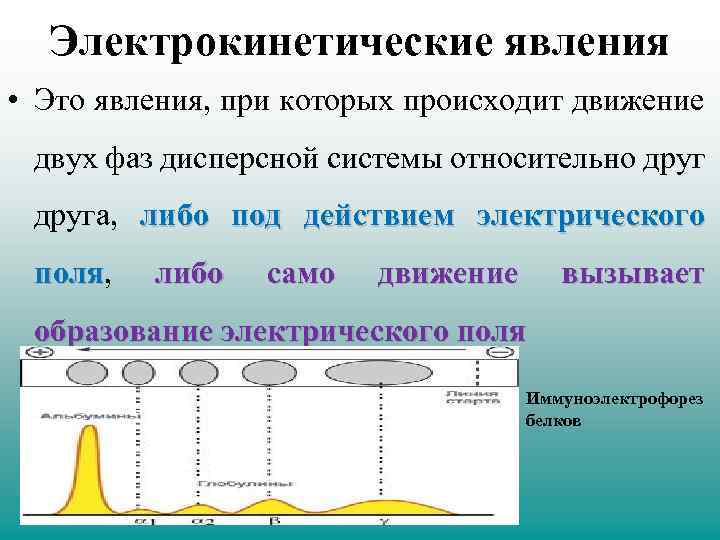 Электрокинетические явления • Это явления, при которых происходит движение двух фаз дисперсной системы относительно друга, либо под действием электрического поля, поля либо само движение вызывает образование электрического поля Иммуноэлектрофорез белков
Электрокинетические явления • Это явления, при которых происходит движение двух фаз дисперсной системы относительно друга, либо под действием электрического поля, поля либо само движение вызывает образование электрического поля Иммуноэлектрофорез белков
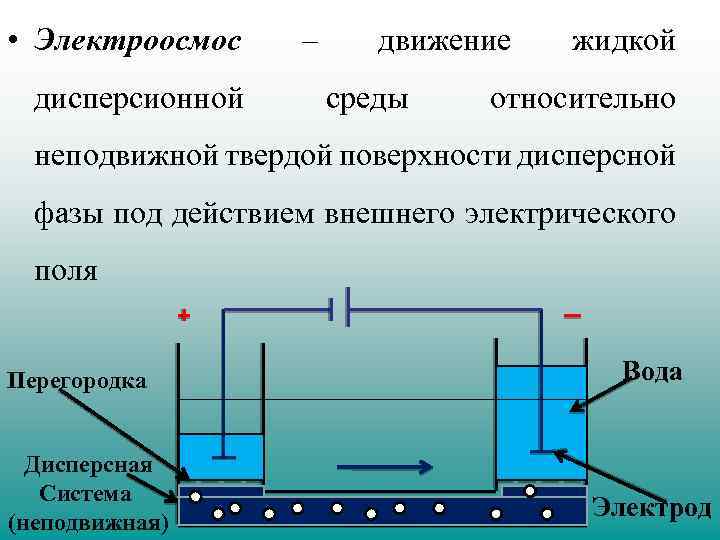 • Электроосмос дисперсионной – движение среды жидкой относительно неподвижной твердой поверхности дисперсной фазы под действием внешнего электрического поля Перегородка Дисперсная Система (неподвижная) Вода Электрод
• Электроосмос дисперсионной – движение среды жидкой относительно неподвижной твердой поверхности дисперсной фазы под действием внешнего электрического поля Перегородка Дисперсная Система (неподвижная) Вода Электрод
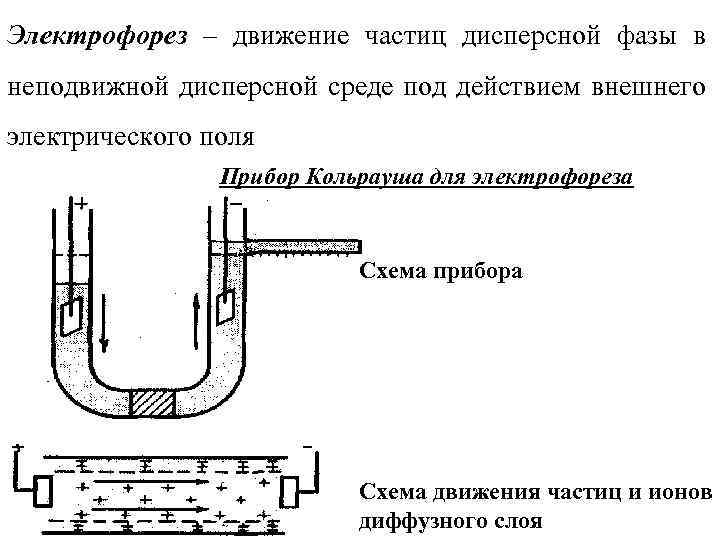 Электрофорез – движение частиц дисперсной фазы в неподвижной дисперсной среде под действием внешнего электрического поля Прибор Кольрауша для электрофореза Схема прибора Схема движения частиц и ионов диффузного слоя
Электрофорез – движение частиц дисперсной фазы в неподвижной дисперсной среде под действием внешнего электрического поля Прибор Кольрауша для электрофореза Схема прибора Схема движения частиц и ионов диффузного слоя
 • Потенциал протекания (течения) – возникает при движении жидкости дисперсионной среды через капиллярную систему дисперсной фазы. (Эффект Квинке) • Потенциал оседания (седиментации) – это (седиментации) разность потенциалов, возникающая при оседании коллоидных частиц в жидкой дисперсионной среде
• Потенциал протекания (течения) – возникает при движении жидкости дисперсионной среды через капиллярную систему дисперсной фазы. (Эффект Квинке) • Потенциал оседания (седиментации) – это (седиментации) разность потенциалов, возникающая при оседании коллоидных частиц в жидкой дисперсионной среде
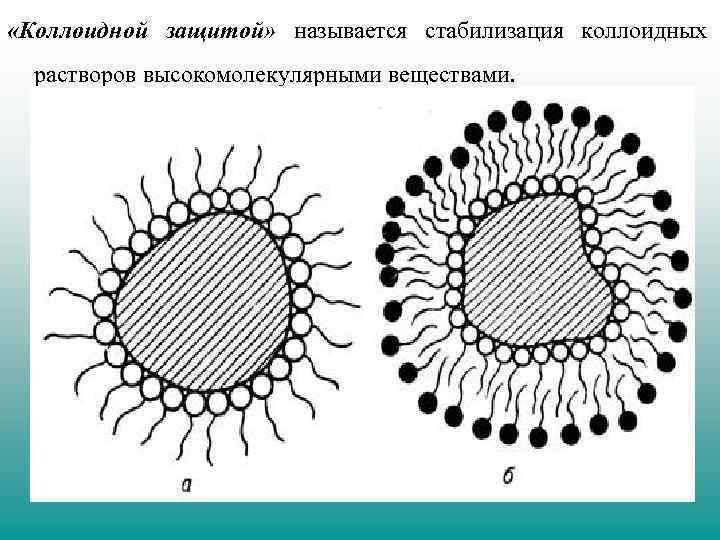 «Коллоидной защитой» называется стабилизация коллоидных растворов высокомолекулярными веществами.
«Коллоидной защитой» называется стабилизация коллоидных растворов высокомолекулярными веществами.
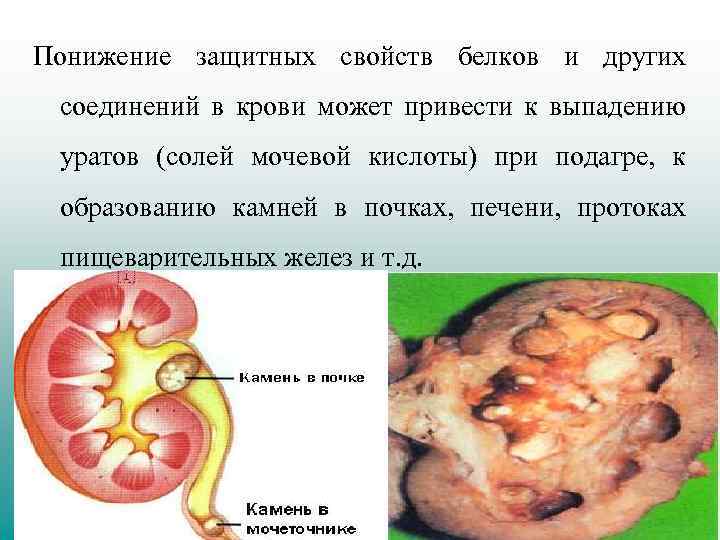 Понижение защитных свойств белков и других соединений в крови может привести к выпадению уратов (солей мочевой кислоты) при подагре, к образованию камней в почках, печени, протоках пищеварительных желез и т. д.
Понижение защитных свойств белков и других соединений в крови может привести к выпадению уратов (солей мочевой кислоты) при подагре, к образованию камней в почках, печени, протоках пищеварительных желез и т. д.
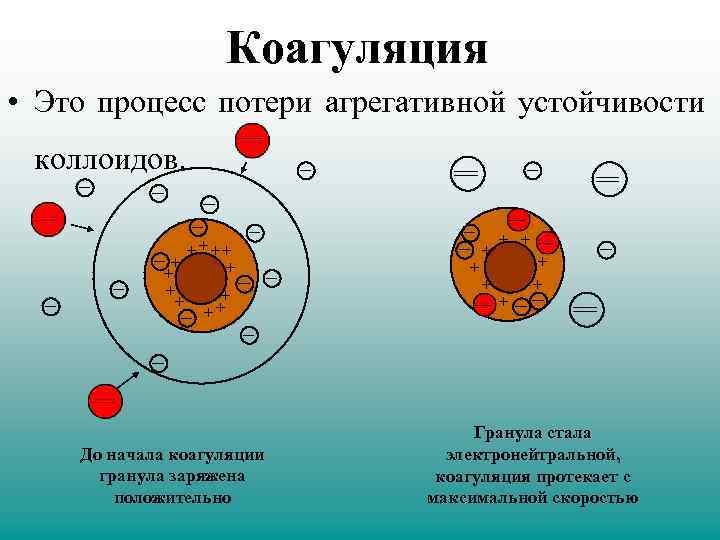 Коагуляция • Это процесс потери агрегативной устойчивости коллоидов. + +++ + + + + До начала коагуляции гранула заряжена положительно + + + + Гранула стала электронейтральной, коагуляция протекает с максимальной скоростью
Коагуляция • Это процесс потери агрегативной устойчивости коллоидов. + +++ + + + + До начала коагуляции гранула заряжена положительно + + + + Гранула стала электронейтральной, коагуляция протекает с максимальной скоростью
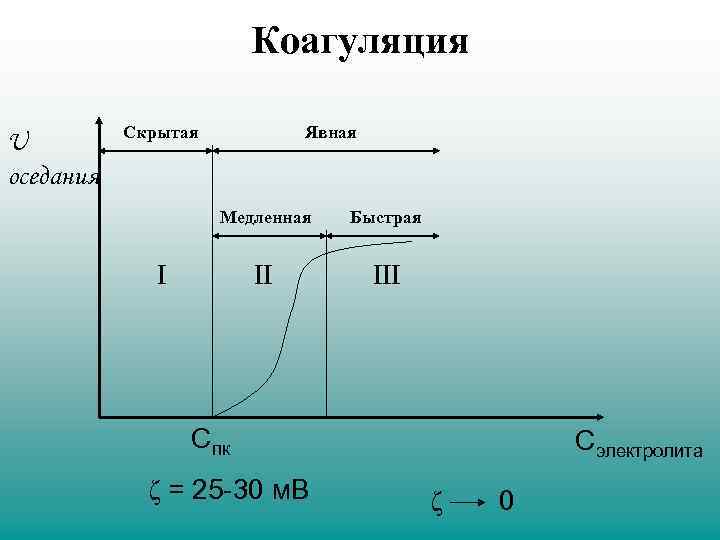 Коагуляция U оседания Скрытая Явная Медленная Быстрая II I Спк ζ = 25 -30 м. В Cэлектролита ζ 0
Коагуляция U оседания Скрытая Явная Медленная Быстрая II I Спк ζ = 25 -30 м. В Cэлектролита ζ 0
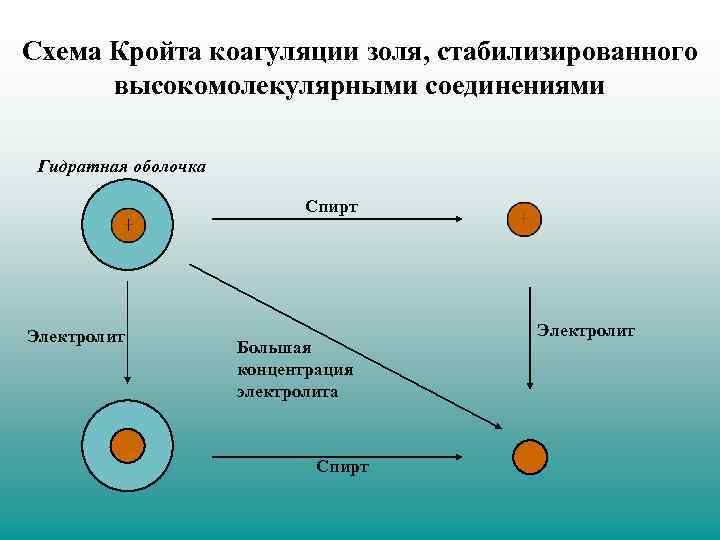 Схема Кройта коагуляции золя, стабилизированного высокомолекулярными соединениями Гидратная оболочка Спирт Электролит Большая концентрация электролита Спирт Электролит
Схема Кройта коагуляции золя, стабилизированного высокомолекулярными соединениями Гидратная оболочка Спирт Электролит Большая концентрация электролита Спирт Электролит
 Правило Шульце-Гарди: Коагулирующий ион имеет заряд, противоположный заряду коллоидной частицы, и чем он больше, тем больше его коагулирующее действие Порог коагуляции можно рассчитать по формуле Коагулирующая способность ионов разных зарядов соотносится примерно как
Правило Шульце-Гарди: Коагулирующий ион имеет заряд, противоположный заряду коллоидной частицы, и чем он больше, тем больше его коагулирующее действие Порог коагуляции можно рассчитать по формуле Коагулирующая способность ионов разных зарядов соотносится примерно как
 При одинаковом заряде коагулирующее действие ионов зависит от способности к гидратации и согласуется с лиотропным рядом Гофмейстера: Лиотропные ряды Li+ > Na+ > K+ > Rb+ > Cs+ > Mg 2+ > Ca 2+ > Sr 2+ > Ba 2+ CNS- ˂ Br - ˂ NO 3 - ˂ Cl- ˂ [ацетат]- ˂ [тартрат]2 - ˂ [цитрат]3 - ˂SO 42 Увеличение степени гидратации Увеличение размера гидратированного иона Увеличение адсорбции Увеличение коагулирующей способности
При одинаковом заряде коагулирующее действие ионов зависит от способности к гидратации и согласуется с лиотропным рядом Гофмейстера: Лиотропные ряды Li+ > Na+ > K+ > Rb+ > Cs+ > Mg 2+ > Ca 2+ > Sr 2+ > Ba 2+ CNS- ˂ Br - ˂ NO 3 - ˂ Cl- ˂ [ацетат]- ˂ [тартрат]2 - ˂ [цитрат]3 - ˂SO 42 Увеличение степени гидратации Увеличение размера гидратированного иона Увеличение адсорбции Увеличение коагулирующей способности
 Коагуляция проявляется в процессе свертывания крови, который уменьшает потерю крови при повреждении тканей и вызывает кровеносной системе. образование тромбов в
Коагуляция проявляется в процессе свертывания крови, который уменьшает потерю крови при повреждении тканей и вызывает кровеносной системе. образование тромбов в
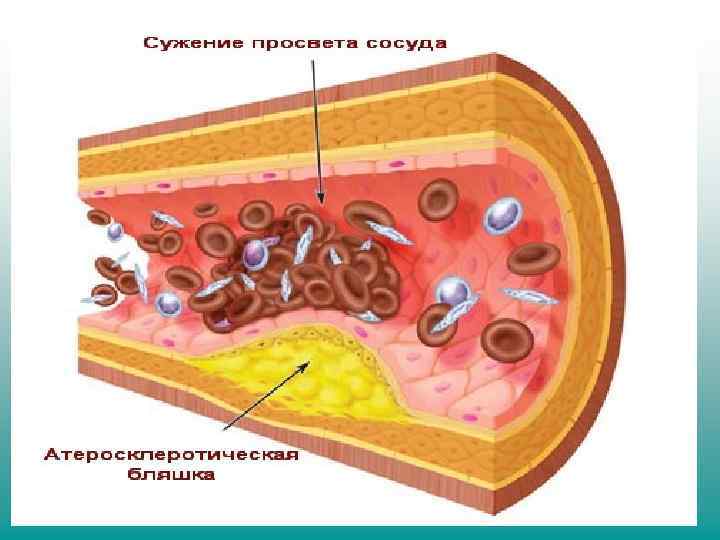
 Пептизация (процесс, обратный коагуляции) – превращение осадка, образовавшегося в результате коагуляции, в устойчивый коллоидный раствор. С этой целью в медицине применяются антикоагулянты (аспирин, гепарин и др)
Пептизация (процесс, обратный коагуляции) – превращение осадка, образовавшегося в результате коагуляции, в устойчивый коллоидный раствор. С этой целью в медицине применяются антикоагулянты (аспирин, гепарин и др)
 Эмульсии Эмульсия – это коллоидная система, состоящая из двух взаимонерастворимых жидкостей с размером капель 10 -6 – 10 -4 м. Правило образования типа эмульсий Бэнкрофта • Если эмульгатор лучше растворяется в «воде» , чем в «масле» , то образуется прямая эмульсия м/в, а если наоборот, то образуется обратная эмульсия в/м.
Эмульсии Эмульсия – это коллоидная система, состоящая из двух взаимонерастворимых жидкостей с размером капель 10 -6 – 10 -4 м. Правило образования типа эмульсий Бэнкрофта • Если эмульгатор лучше растворяется в «воде» , чем в «масле» , то образуется прямая эмульсия м/в, а если наоборот, то образуется обратная эмульсия в/м.
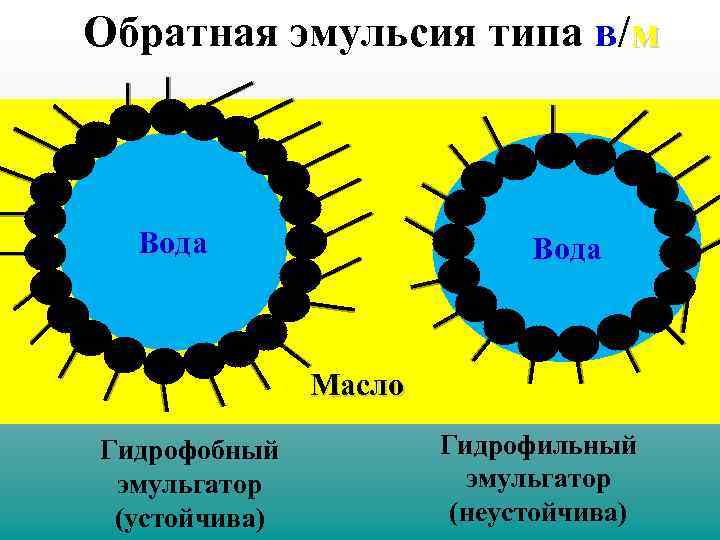 Обратная эмульсия типа в/м Вода Масло Гидрофобный эмульгатор (устойчива) Гидрофильный эмульгатор (неустойчива)
Обратная эмульсия типа в/м Вода Масло Гидрофобный эмульгатор (устойчива) Гидрофильный эмульгатор (неустойчива)
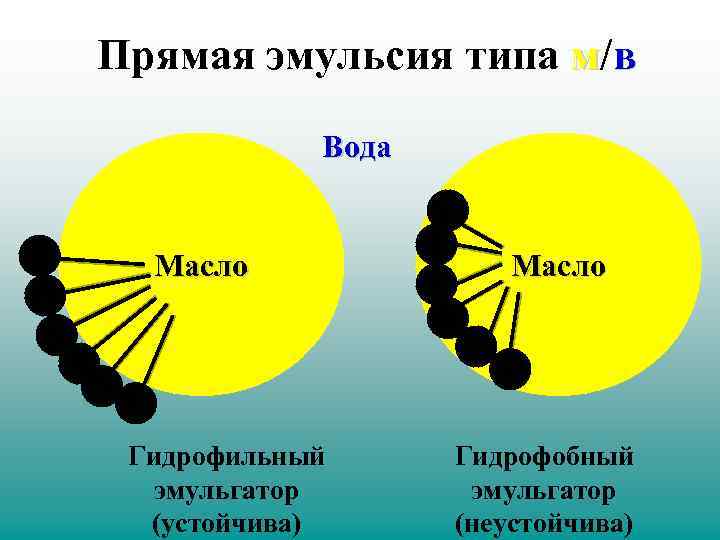 Прямая эмульсия типа м/в Вода Масло Гидрофильный эмульгатор (устойчива) Масло Гидрофобный эмульгатор (неустойчива)
Прямая эмульсия типа м/в Вода Масло Гидрофильный эмульгатор (устойчива) Масло Гидрофобный эмульгатор (неустойчива)
 Коллоидные поверхностно – активные вещества (полуколлоиды) «истинный р-р коллоидный р-р (молекулярный) (мицеллярный) Полуколлоиды являются гель» (связанодисперсная система) веществами, имеющими дифильное строение, ПАВ, соли жирных и желчных кислот, фосфолипиды, гликолипиды, мыла, детергенты, таннины, некоторые высокомолекулярные соединения и др.
Коллоидные поверхностно – активные вещества (полуколлоиды) «истинный р-р коллоидный р-р (молекулярный) (мицеллярный) Полуколлоиды являются гель» (связанодисперсная система) веществами, имеющими дифильное строение, ПАВ, соли жирных и желчных кислот, фосфолипиды, гликолипиды, мыла, детергенты, таннины, некоторые высокомолекулярные соединения и др.
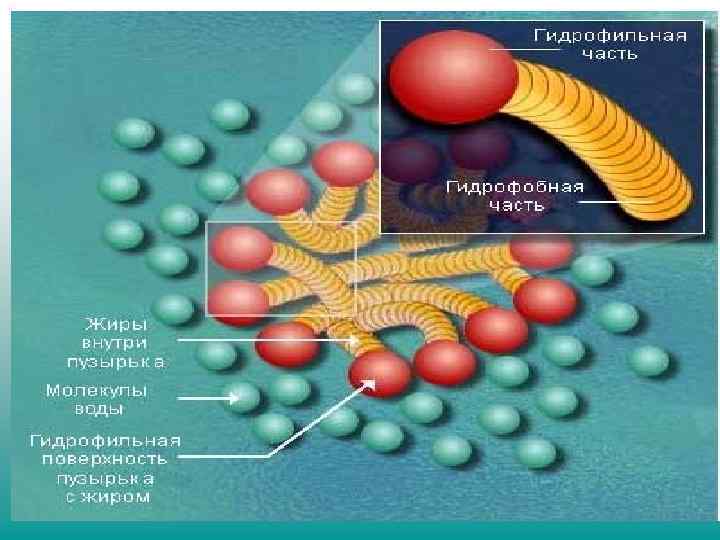
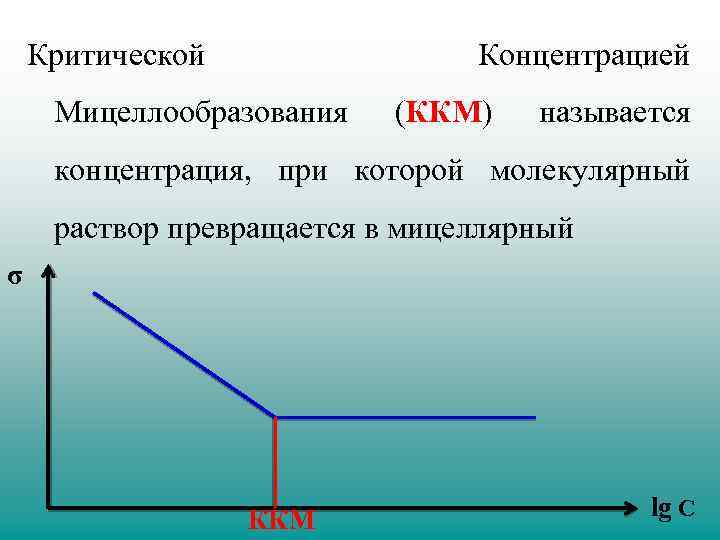 Критической Концентрацией Мицеллообразования (ККМ) называется концентрация, при которой молекулярный раствор превращается в мицеллярный σ ККМ lg C
Критической Концентрацией Мицеллообразования (ККМ) называется концентрация, при которой молекулярный раствор превращается в мицеллярный σ ККМ lg C
 Схема образования мицелл в растворах коллоидных ПАВ 1 - молекулярный разбавленный раствор ПАВ 2 – раствор ПАВ со сферическими мицеллами 3 – раствор ПАВ с пластинчатыми мицеллами 4 – концентрированный мицеллярный раствор ПАВ – ламеллярные структуры 2 4 3 1
Схема образования мицелл в растворах коллоидных ПАВ 1 - молекулярный разбавленный раствор ПАВ 2 – раствор ПАВ со сферическими мицеллами 3 – раствор ПАВ с пластинчатыми мицеллами 4 – концентрированный мицеллярный раствор ПАВ – ламеллярные структуры 2 4 3 1
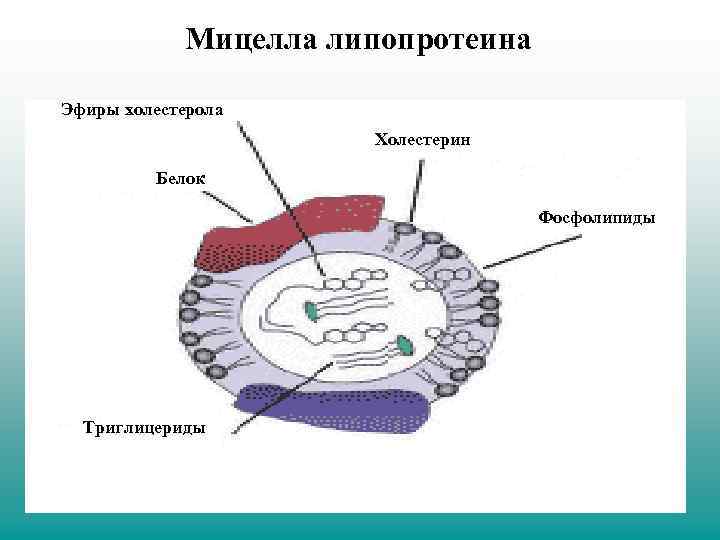 Мицелла липопротеина Эфиры холестерола Холестерин Белок Фосфолипиды Триглицериды
Мицелла липопротеина Эфиры холестерола Холестерин Белок Фосфолипиды Триглицериды
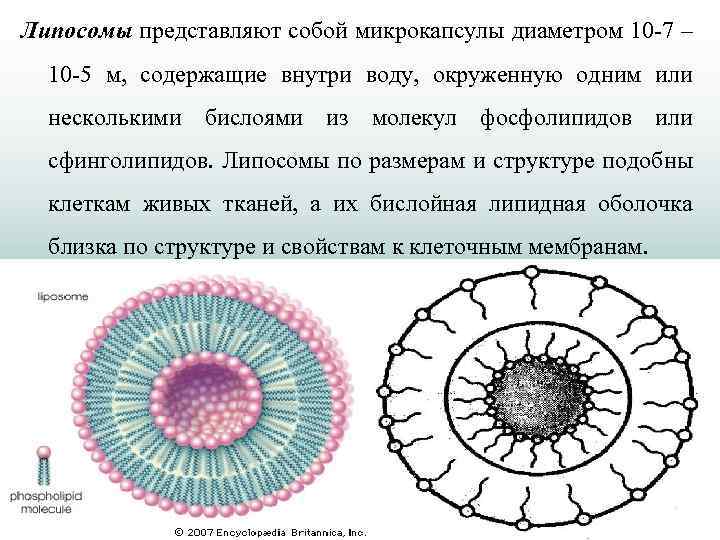 Липосомы представляют собой микрокапсулы диаметром 10 -7 – 10 -5 м, содержащие внутри воду, окруженную одним или несколькими бислоями из молекул фосфолипидов или сфинголипидов. Липосомы по размерам и структуре подобны клеткам живых тканей, а их бислойная липидная оболочка близка по структуре и свойствам к клеточным мембранам.
Липосомы представляют собой микрокапсулы диаметром 10 -7 – 10 -5 м, содержащие внутри воду, окруженную одним или несколькими бислоями из молекул фосфолипидов или сфинголипидов. Липосомы по размерам и структуре подобны клеткам живых тканей, а их бислойная липидная оболочка близка по структуре и свойствам к клеточным мембранам.
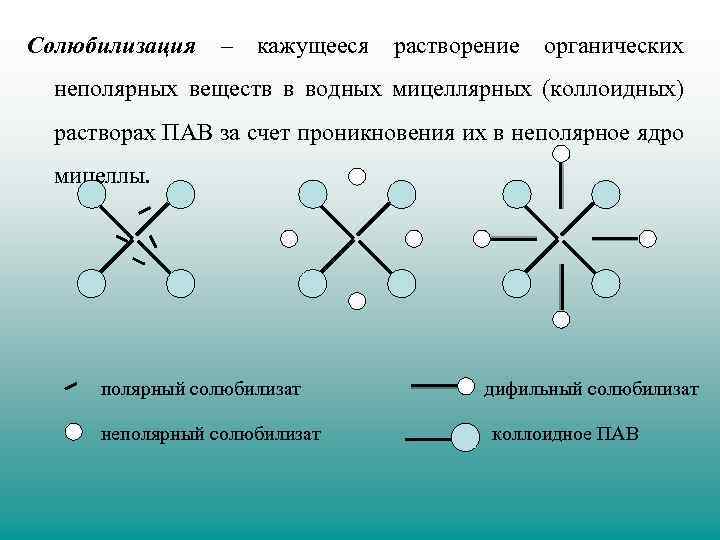 Солюбилизация – кажущееся растворение органических неполярных веществ в водных мицеллярных (коллоидных) растворах ПАВ за счет проникновения их в неполярное ядро мицеллы. полярный солюбилизат неполярный солюбилизат дифильный солюбилизат коллоидное ПАВ
Солюбилизация – кажущееся растворение органических неполярных веществ в водных мицеллярных (коллоидных) растворах ПАВ за счет проникновения их в неполярное ядро мицеллы. полярный солюбилизат неполярный солюбилизат дифильный солюбилизат коллоидное ПАВ
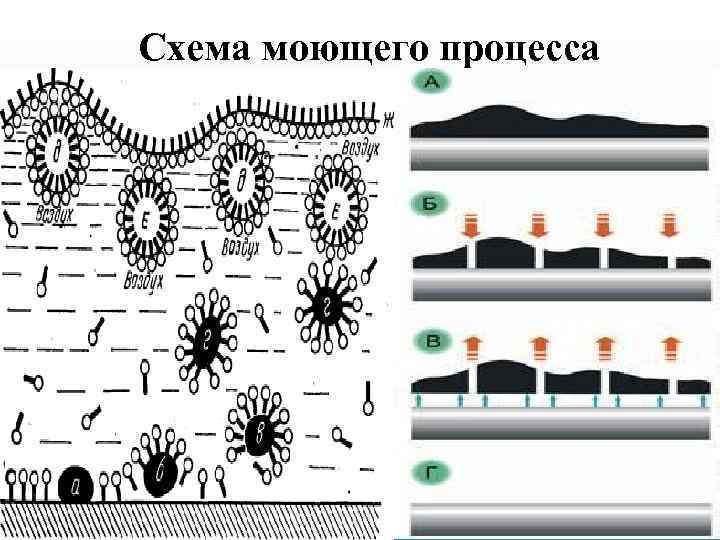 Схема моющего процесса
Схема моющего процесса
 Спасибо за внимание!
Спасибо за внимание!


