2 закон.pptx
- Количество слайдов: 25
 ФИЗИЧЕСКАЯ ХИМИЯ II закон термодинамики Он не замечает карманников. Явился он в мир стереть второй закон термодинамики и с ним тепловую смерть. А. А. Вознесенский
ФИЗИЧЕСКАЯ ХИМИЯ II закон термодинамики Он не замечает карманников. Явился он в мир стереть второй закон термодинамики и с ним тепловую смерть. А. А. Вознесенский
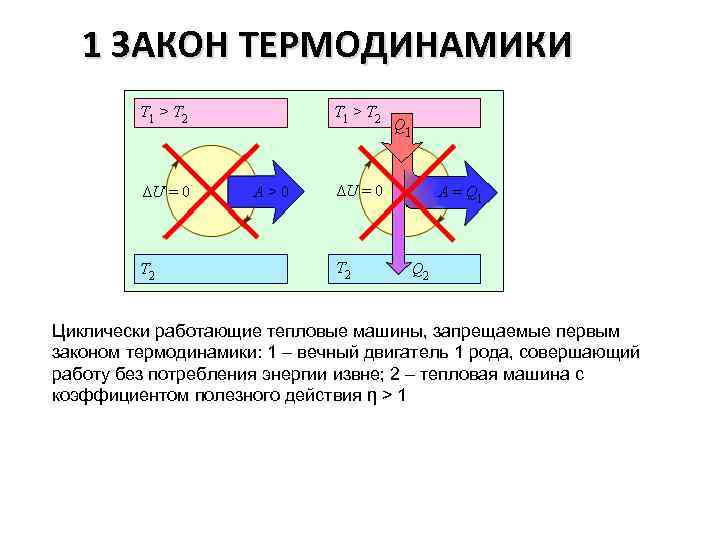 1 ЗАКОН ТЕРМОДИНАМИКИ Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: 1 – вечный двигатель 1 рода, совершающий работу без потребления энергии извне; 2 – тепловая машина с коэффициентом полезного действия η > 1
1 ЗАКОН ТЕРМОДИНАМИКИ Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: 1 – вечный двигатель 1 рода, совершающий работу без потребления энергии извне; 2 – тепловая машина с коэффициентом полезного действия η > 1
 2 ЗАКОН ТЕРМОДИНАМИКИ ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ НЕ УСТАНАВЛИВАЕТ НАПРАВЛЕНИЯ ТЕПЛОВЫХ ПРОЦЕССОВ. МНОГИЕ ТЕПЛОВЫЕ ПРОЦЕССЫ ЯВЛЯЮТСЯ НЕОБРАТИМЫМИ ПРИ ТЕПЛОВОМ КОНТАКТЕ ДВУХ ТЕЛ С РАЗНЫМИ ТЕМПЕРАТУРАМИ ТЕПЛОВОЙ ПОТОК ВСЕГДА НАПРАВЛЕН ОТ БОЛЕЕ ТЕПЛОГО ТЕЛА К БОЛЕЕ ХОЛОДНОМУ. НИКОГДА НЕ НАБЛЮДАЕТСЯ САМОПРОИЗВОЛЬНЫЙ ПРОЦЕСС ПЕРЕДАЧИ ТЕПЛА ОТ ТЕЛА С НИЗКОЙ ТЕМПЕРАТУРОЙ К ТЕЛУ С БОЛЕЕ ВЫСОКОЙ ТЕМПЕРАТУРОЙ. ОБРАТИМЫМИ ПРОЦЕССАМИ НАЗЫВАЮТ ПРОЦЕССЫ ПЕРЕХОДА СИСТЕМЫ ИЗ ОДНОГО РАВНОВЕСНОГО СОСТОЯНИЯ В ДРУГОЕ, КОТОРЫЕ МОЖНО ПРОВЕСТИ В ОБРАТНОМ НАПРАВЛЕНИИ ЧЕРЕЗ ТУ ЖЕ ПОСЛЕДОВАТЕЛЬНОСТЬ ПРОМЕЖУТОЧНЫХ РАВНОВЕСНЫХ СОСТОЯНИЙ. ПРИ ЭТОМ САМА СИСТЕМА И ОКРУЖАЮЩИЕ ТЕЛА ВОЗВРАЩАЮТСЯ К ИСХОДНОМУ СОСТОЯНИЮ. ПРОЦЕССЫ, В ХОДЕ КОТОРЫХ СИСТЕМА ВСЕ ВРЕМЯ ОСТАЕТСЯ В СОСТОЯНИИ РАВНОВЕСИЯ, НАЗЫВАЮТСЯ КВАЗИСТАТИЧЕСКИМИ. ВСЕ КВАЗИСТАТИЧЕСКИЕ ПРОЦЕССЫ ОБРАТИМЫ. ВСЕ ОБРАТИМЫЕ ПРОЦЕССЫ ЯВЛЯЮТСЯ КВАЗИСТАТИЧЕСКИМИ.
2 ЗАКОН ТЕРМОДИНАМИКИ ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ НЕ УСТАНАВЛИВАЕТ НАПРАВЛЕНИЯ ТЕПЛОВЫХ ПРОЦЕССОВ. МНОГИЕ ТЕПЛОВЫЕ ПРОЦЕССЫ ЯВЛЯЮТСЯ НЕОБРАТИМЫМИ ПРИ ТЕПЛОВОМ КОНТАКТЕ ДВУХ ТЕЛ С РАЗНЫМИ ТЕМПЕРАТУРАМИ ТЕПЛОВОЙ ПОТОК ВСЕГДА НАПРАВЛЕН ОТ БОЛЕЕ ТЕПЛОГО ТЕЛА К БОЛЕЕ ХОЛОДНОМУ. НИКОГДА НЕ НАБЛЮДАЕТСЯ САМОПРОИЗВОЛЬНЫЙ ПРОЦЕСС ПЕРЕДАЧИ ТЕПЛА ОТ ТЕЛА С НИЗКОЙ ТЕМПЕРАТУРОЙ К ТЕЛУ С БОЛЕЕ ВЫСОКОЙ ТЕМПЕРАТУРОЙ. ОБРАТИМЫМИ ПРОЦЕССАМИ НАЗЫВАЮТ ПРОЦЕССЫ ПЕРЕХОДА СИСТЕМЫ ИЗ ОДНОГО РАВНОВЕСНОГО СОСТОЯНИЯ В ДРУГОЕ, КОТОРЫЕ МОЖНО ПРОВЕСТИ В ОБРАТНОМ НАПРАВЛЕНИИ ЧЕРЕЗ ТУ ЖЕ ПОСЛЕДОВАТЕЛЬНОСТЬ ПРОМЕЖУТОЧНЫХ РАВНОВЕСНЫХ СОСТОЯНИЙ. ПРИ ЭТОМ САМА СИСТЕМА И ОКРУЖАЮЩИЕ ТЕЛА ВОЗВРАЩАЮТСЯ К ИСХОДНОМУ СОСТОЯНИЮ. ПРОЦЕССЫ, В ХОДЕ КОТОРЫХ СИСТЕМА ВСЕ ВРЕМЯ ОСТАЕТСЯ В СОСТОЯНИИ РАВНОВЕСИЯ, НАЗЫВАЮТСЯ КВАЗИСТАТИЧЕСКИМИ. ВСЕ КВАЗИСТАТИЧЕСКИЕ ПРОЦЕССЫ ОБРАТИМЫ. ВСЕ ОБРАТИМЫЕ ПРОЦЕССЫ ЯВЛЯЮТСЯ КВАЗИСТАТИЧЕСКИМИ.
 2 ЗАКОН ТЕРМОДИНАМИКИ Карно Никола Леонар Сади (1796 -1832 гг. )
2 ЗАКОН ТЕРМОДИНАМИКИ Карно Никола Леонар Сади (1796 -1832 гг. )
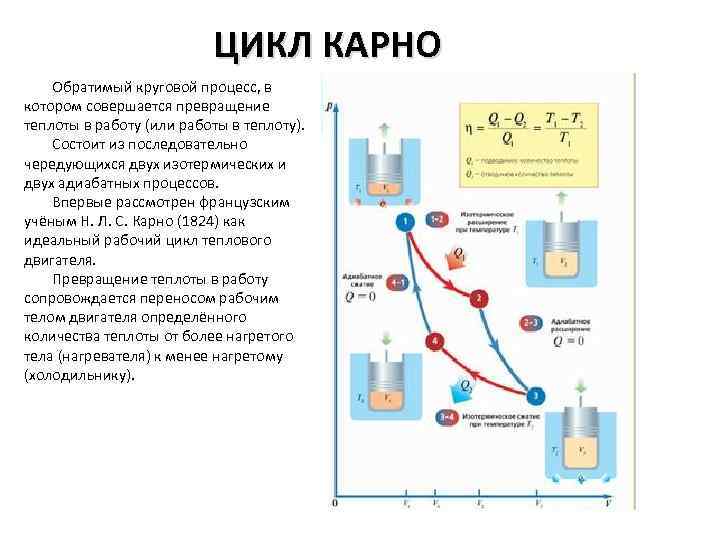 ЦИКЛ КАРНО Обратимый круговой процесс, в котором совершается превращение теплоты в работу (или работы в теплоту). Состоит из последовательно чередующихся двух изотермических и двух адиабатных процессов. Впервые рассмотрен французским учёным Н. Л. С. Карно (1824) как идеальный рабочий цикл теплового двигателя. Превращение теплоты в работу сопровождается переносом рабочим телом двигателя определённого количества теплоты от более нагретого тела (нагревателя) к менее нагретому (холодильнику).
ЦИКЛ КАРНО Обратимый круговой процесс, в котором совершается превращение теплоты в работу (или работы в теплоту). Состоит из последовательно чередующихся двух изотермических и двух адиабатных процессов. Впервые рассмотрен французским учёным Н. Л. С. Карно (1824) как идеальный рабочий цикл теплового двигателя. Превращение теплоты в работу сопровождается переносом рабочим телом двигателя определённого количества теплоты от более нагретого тела (нагревателя) к менее нагретому (холодильнику).
 2 ЗАКОН ТЕРМОДИНАМИКИ В ЦИКЛИЧЕСКИ ДЕЙСТВУЮЩЕЙ ТЕПЛОВОЙ МАШИНЕ НЕВОЗМОЖЕН ПРОЦЕСС, ЕДИНСТВЕННЫМ РЕЗУЛЬТАТОМ КОТОРОГО БЫЛО БЫ ПРЕОБРАЗОВАНИЕ В МЕХАНИЧЕСКУЮ РАБОТУ ВСЕГО КОЛИЧЕСТВА ТЕПЛОТЫ, ПОЛУЧЕННОГО ОТ ЕДИНСТВЕННОГО ТЕПЛОВОГО РЕЗЕРВУАРА. Кельвин (Kelvin) Вильям (26. VI. 1824– 17. XII. 1907). ВЕЧНЫЙ ДВИГАТЕЛЬ ВТОРОГО РОДА
2 ЗАКОН ТЕРМОДИНАМИКИ В ЦИКЛИЧЕСКИ ДЕЙСТВУЮЩЕЙ ТЕПЛОВОЙ МАШИНЕ НЕВОЗМОЖЕН ПРОЦЕСС, ЕДИНСТВЕННЫМ РЕЗУЛЬТАТОМ КОТОРОГО БЫЛО БЫ ПРЕОБРАЗОВАНИЕ В МЕХАНИЧЕСКУЮ РАБОТУ ВСЕГО КОЛИЧЕСТВА ТЕПЛОТЫ, ПОЛУЧЕННОГО ОТ ЕДИНСТВЕННОГО ТЕПЛОВОГО РЕЗЕРВУАРА. Кельвин (Kelvin) Вильям (26. VI. 1824– 17. XII. 1907). ВЕЧНЫЙ ДВИГАТЕЛЬ ВТОРОГО РОДА
 2 ЗАКОН ТЕРМОДИНАМИКИ НЕВОЗМОЖЕН ПРОЦЕСС, ЕДИНСТВЕННЫМ РЕЗУЛЬТАТОМ КОТОРОГО БЫЛА БЫ ПЕРЕДАЧА ЭНЕРГИИ ПУТЕМ ТЕПЛООБМЕНА ОТ ТЕЛА С НИЗКОЙ ТЕМПЕРАТУРОЙ К ТЕЛУ С БОЛЕЕ ВЫСОКОЙ ТЕМПЕРАТУРОЙ. Клаузиус (Clausius) Рудольф Юлиус Эмануэль (2. I. 1822– 24. VIII. 1888)
2 ЗАКОН ТЕРМОДИНАМИКИ НЕВОЗМОЖЕН ПРОЦЕСС, ЕДИНСТВЕННЫМ РЕЗУЛЬТАТОМ КОТОРОГО БЫЛА БЫ ПЕРЕДАЧА ЭНЕРГИИ ПУТЕМ ТЕПЛООБМЕНА ОТ ТЕЛА С НИЗКОЙ ТЕМПЕРАТУРОЙ К ТЕЛУ С БОЛЕЕ ВЫСОКОЙ ТЕМПЕРАТУРОЙ. Клаузиус (Clausius) Рудольф Юлиус Эмануэль (2. I. 1822– 24. VIII. 1888)
 2 ЗАКОН ТЕРМОДИНАМИКИ НЕВОЗМОЖНО СОЗДАТЬ ВЕЧНЫЙ ДВИГАТЕЛЬ ВТОРОГО РОДА Оствальд (Ostvald) Вильгельм (1853 -1932)
2 ЗАКОН ТЕРМОДИНАМИКИ НЕВОЗМОЖНО СОЗДАТЬ ВЕЧНЫЙ ДВИГАТЕЛЬ ВТОРОГО РОДА Оствальд (Ostvald) Вильгельм (1853 -1932)
 2 ЗАКОН ТЕРМОДИНАМИКИ НЕВОЗМОЖЕН КРУГОВОЙ ПРОЦЕСС, ЕДИНСТВЕННЫМ РЕЗУЛЬТАТОМ КОТОРОГО БЫЛО БЫ ПРОИЗВОДСТВО РАБОТЫ ЗА СЧЕТ ОХЛАЖДЕНИЯ ТЕПЛОВОГО РЕЗЕРВУАРА» (ПРОЦЕСС ТОМСОНА) Джозеф Джон Томсон (1856 — 1940)
2 ЗАКОН ТЕРМОДИНАМИКИ НЕВОЗМОЖЕН КРУГОВОЙ ПРОЦЕСС, ЕДИНСТВЕННЫМ РЕЗУЛЬТАТОМ КОТОРОГО БЫЛО БЫ ПРОИЗВОДСТВО РАБОТЫ ЗА СЧЕТ ОХЛАЖДЕНИЯ ТЕПЛОВОГО РЕЗЕРВУАРА» (ПРОЦЕСС ТОМСОНА) Джозеф Джон Томсон (1856 — 1940)
 2 ЗАКОН ТЕРМОДИНАМИКИ ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ НЕПОСРЕДСТВЕННО СВЯЗАН С НЕОБРАТИМОСТЬЮ РЕАЛЬНЫХ ТЕПЛОВЫХ ПРОЦЕССОВ. ОБЩИМ СВОЙСТВОМ ВСЕХ НЕОБРАТИМЫХ ПРОЦЕССОВ ЯВЛЯЕТСЯ ТО, ЧТО ОНИ ПРОТЕКАЮТ В ТЕРМОДИНАМИЧЕСКИ НЕРАВНОВЕСНОЙ СИСТЕМЕ И В РЕЗУЛЬТАТЕ ЭТИХ ПРОЦЕССОВ ЗАМКНУТАЯ СИСТЕМА ПРИБЛИЖАЕТСЯ К СОСТОЯНИЮ ТЕРМОДИНАМИЧЕСКОГО РАВНОВЕСИЯ.
2 ЗАКОН ТЕРМОДИНАМИКИ ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ НЕПОСРЕДСТВЕННО СВЯЗАН С НЕОБРАТИМОСТЬЮ РЕАЛЬНЫХ ТЕПЛОВЫХ ПРОЦЕССОВ. ОБЩИМ СВОЙСТВОМ ВСЕХ НЕОБРАТИМЫХ ПРОЦЕССОВ ЯВЛЯЕТСЯ ТО, ЧТО ОНИ ПРОТЕКАЮТ В ТЕРМОДИНАМИЧЕСКИ НЕРАВНОВЕСНОЙ СИСТЕМЕ И В РЕЗУЛЬТАТЕ ЭТИХ ПРОЦЕССОВ ЗАМКНУТАЯ СИСТЕМА ПРИБЛИЖАЕТСЯ К СОСТОЯНИЮ ТЕРМОДИНАМИЧЕСКОГО РАВНОВЕСИЯ.
 2 ЗАКОН ТЕРМОДИНАМИКИ ТЕОРЕМЫ КАРНО: КОЭФФИЦИЕНТ ПОЛЕЗНОГО ДЕЙСТВИЯ ТЕПЛОВОЙ МАШИНЫ, РАБОТАЮЩЕЙ ПРИ ДАННЫХ ЗНАЧЕНИЯХ ТЕМПЕРАТУР НАГРЕВАТЕЛЯ И ХОЛОДИЛЬНИКА, НЕ МОЖЕТ БЫТЬ БОЛЬШЕ, ЧЕМ КОЭФФИЦИЕНТ ПОЛЕЗНОГО ДЕЙСТВИЯ МАШИНЫ, РАБОТАЮЩЕЙ ПО ОБРАТИМОМУ ЦИКЛУ КАРНО ПРИ ТЕХ ЖЕ ЗНАЧЕНИЯХ ТЕМПЕРАТУР НАГРЕВАТЕЛЯ И ХОЛОДИЛЬНИКА. КОЭФФИЦИЕНТ ПОЛЕЗНОГО ДЕЙСТВИЯ ТЕПЛОВОЙ МАШИНЫ, РАБОТАЮЩЕЙ ПО ЦИКЛУ КАРНО, НЕ ЗАВИСИТ ОТ РОДА РАБОЧЕГО ТЕЛА, А ТОЛЬКО ОТ ТЕМПЕРАТУР НАГРЕВАТЕЛЯ И ХОЛОДИЛЬНИКА.
2 ЗАКОН ТЕРМОДИНАМИКИ ТЕОРЕМЫ КАРНО: КОЭФФИЦИЕНТ ПОЛЕЗНОГО ДЕЙСТВИЯ ТЕПЛОВОЙ МАШИНЫ, РАБОТАЮЩЕЙ ПРИ ДАННЫХ ЗНАЧЕНИЯХ ТЕМПЕРАТУР НАГРЕВАТЕЛЯ И ХОЛОДИЛЬНИКА, НЕ МОЖЕТ БЫТЬ БОЛЬШЕ, ЧЕМ КОЭФФИЦИЕНТ ПОЛЕЗНОГО ДЕЙСТВИЯ МАШИНЫ, РАБОТАЮЩЕЙ ПО ОБРАТИМОМУ ЦИКЛУ КАРНО ПРИ ТЕХ ЖЕ ЗНАЧЕНИЯХ ТЕМПЕРАТУР НАГРЕВАТЕЛЯ И ХОЛОДИЛЬНИКА. КОЭФФИЦИЕНТ ПОЛЕЗНОГО ДЕЙСТВИЯ ТЕПЛОВОЙ МАШИНЫ, РАБОТАЮЩЕЙ ПО ЦИКЛУ КАРНО, НЕ ЗАВИСИТ ОТ РОДА РАБОЧЕГО ТЕЛА, А ТОЛЬКО ОТ ТЕМПЕРАТУР НАГРЕВАТЕЛЯ И ХОЛОДИЛЬНИКА.
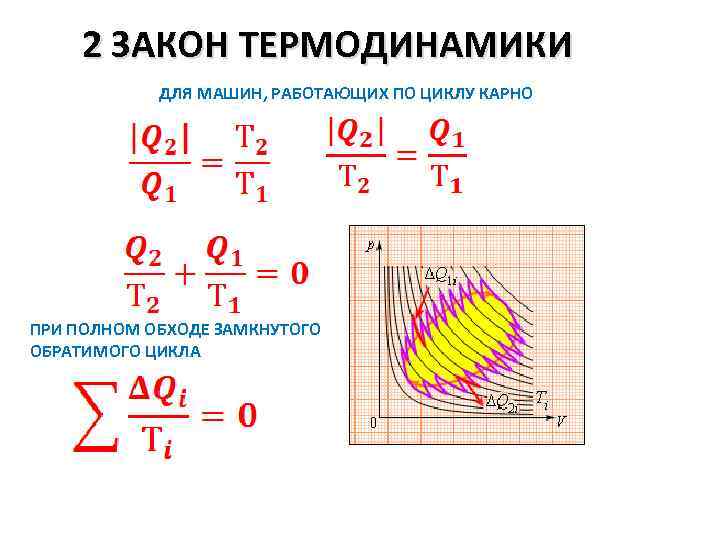 2 ЗАКОН ТЕРМОДИНАМИКИ ДЛЯ МАШИН, РАБОТАЮЩИХ ПО ЦИКЛУ КАРНО ПРИ ПОЛНОМ ОБХОДЕ ЗАМКНУТОГО ОБРАТИМОГО ЦИКЛА
2 ЗАКОН ТЕРМОДИНАМИКИ ДЛЯ МАШИН, РАБОТАЮЩИХ ПО ЦИКЛУ КАРНО ПРИ ПОЛНОМ ОБХОДЕ ЗАМКНУТОГО ОБРАТИМОГО ЦИКЛА
 2 ЗАКОН ТЕРМОДИНАМИКИ ОТНОШЕНИЕ ΔQi / Ti НАЗЫВАЕТСЯ ПРИВЕДЕННЫМ ТЕПЛОМ или ЭНТРОПИЕЙ S (Р. КЛАУЗИУС, 1865 г. ). ПОЛУЧЕННАЯ ФОРМУЛА ПОКАЗЫВАЕТ, ЧТО ПОЛНОЕ ПРИВЕДЕННОЕ ТЕПЛО НА ЛЮБОМ ОБРАТИМОМ ЦИКЛЕ РАВНО НУЛЮ. Если термодинамическая система переходит из одного равновесного состояния в другое, то ее энтропия изменяется. Разность значений энтропии в двух состояниях равна приведенному теплу, полученному системой при обратимом переходе из одного состояния в другое. ДЛЯ ОБРАТИМЫХ ПРОЦЕССОВ
2 ЗАКОН ТЕРМОДИНАМИКИ ОТНОШЕНИЕ ΔQi / Ti НАЗЫВАЕТСЯ ПРИВЕДЕННЫМ ТЕПЛОМ или ЭНТРОПИЕЙ S (Р. КЛАУЗИУС, 1865 г. ). ПОЛУЧЕННАЯ ФОРМУЛА ПОКАЗЫВАЕТ, ЧТО ПОЛНОЕ ПРИВЕДЕННОЕ ТЕПЛО НА ЛЮБОМ ОБРАТИМОМ ЦИКЛЕ РАВНО НУЛЮ. Если термодинамическая система переходит из одного равновесного состояния в другое, то ее энтропия изменяется. Разность значений энтропии в двух состояниях равна приведенному теплу, полученному системой при обратимом переходе из одного состояния в другое. ДЛЯ ОБРАТИМЫХ ПРОЦЕССОВ
 2 ЗАКОН ТЕРМОДИНАМИКИ ЗАКОН ВОЗРАСТАНИЯ ЭНТРОПИИ РОСТ ЭНТРОПИИ ЯВЛЯЕТСЯ ОБЩИМ СВОЙСТВОМ ВСЕХ САМОПРОИЗВОЛЬНО ПРОТЕКАЮЩИХ НЕОБРАТИМЫХ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ ТЕРМОДИНАМИЧЕСКИХ СИСТЕМАХ. ПРИ ОБРАТИМЫХ ПРОЦЕССАХ В ИЗОЛИРОВАННЫХ СИСТЕМАХ ЭНТРОПИЯ НЕ ИЗМЕНЯЕТСЯ. ΔS ≥ 0
2 ЗАКОН ТЕРМОДИНАМИКИ ЗАКОН ВОЗРАСТАНИЯ ЭНТРОПИИ РОСТ ЭНТРОПИИ ЯВЛЯЕТСЯ ОБЩИМ СВОЙСТВОМ ВСЕХ САМОПРОИЗВОЛЬНО ПРОТЕКАЮЩИХ НЕОБРАТИМЫХ ПРОЦЕССОВ В ИЗОЛИРОВАННЫХ ТЕРМОДИНАМИЧЕСКИХ СИСТЕМАХ. ПРИ ОБРАТИМЫХ ПРОЦЕССАХ В ИЗОЛИРОВАННЫХ СИСТЕМАХ ЭНТРОПИЯ НЕ ИЗМЕНЯЕТСЯ. ΔS ≥ 0
 2 ЗАКОН ТЕРМОДИНАМИКИ ЭНТРОПИЯ - МЕРА СТАТИСТИЧЕСКОГО БЕСПОРЯДКА В ЗАМКНУТОЙ ТЕРМОДИНАМИЧЕСКОЙ СИСТЕМЕ. Больцман (Boltzmann) Людвиг (20. II. 1844– 5. IX. 1906) ВСЕ САМОПРОИЗВОЛЬНО ПРОТЕКАЮЩИЕ ПРОЦЕССЫ В ЗАМКНУТОЙ СИСТЕМЕ, ПРИБЛИЖАЮЩИЕ СИСТЕМУ К СОСТОЯНИЮ РАВНОВЕСИЯ И СОПРОВОЖДАЮЩИЕСЯ РОСТОМ ЭНТРОПИИ, НАПРАВЛЕНЫ В СТОРОНУ УВЕЛИЧЕНИЯ ВЕРОЯТНОСТИ СОСТОЯНИЯ. S = k ln. W k = 1, 38· 10– 23 Дж/К
2 ЗАКОН ТЕРМОДИНАМИКИ ЭНТРОПИЯ - МЕРА СТАТИСТИЧЕСКОГО БЕСПОРЯДКА В ЗАМКНУТОЙ ТЕРМОДИНАМИЧЕСКОЙ СИСТЕМЕ. Больцман (Boltzmann) Людвиг (20. II. 1844– 5. IX. 1906) ВСЕ САМОПРОИЗВОЛЬНО ПРОТЕКАЮЩИЕ ПРОЦЕССЫ В ЗАМКНУТОЙ СИСТЕМЕ, ПРИБЛИЖАЮЩИЕ СИСТЕМУ К СОСТОЯНИЮ РАВНОВЕСИЯ И СОПРОВОЖДАЮЩИЕСЯ РОСТОМ ЭНТРОПИИ, НАПРАВЛЕНЫ В СТОРОНУ УВЕЛИЧЕНИЯ ВЕРОЯТНОСТИ СОСТОЯНИЯ. S = k ln. W k = 1, 38· 10– 23 Дж/К
 2 ЗАКОН ТЕРМОДИНАМИКИ
2 ЗАКОН ТЕРМОДИНАМИКИ
 2 ЗАКОН ТЕРМОДИНАМИКИ
2 ЗАКОН ТЕРМОДИНАМИКИ
 2 ЗАКОН ТЕРМОДИНАМИКИ КЛАУЗИУС, РАССМАТРИВАЯ ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ, ПРИШЁЛ К ВЫВОДУ, ЧТО ЭНТРОПИЯ ВСЕЛЕННОЙ КАК ЗАМКНУТОЙ СИСТЕМЫ СТРЕМИТСЯ К МАКСИМУМУ, И В КОНЦЕ КОНЦОВ ВО ВСЕЛЕННОЙ ЗАКОНЧАТСЯ ВСЕ МАКРОСКОПИЧЕСКИЕ ПРОЦЕССЫ. ЭТО СОСТОЯНИЕ ВСЕЛЕННОЙ ПОЛУЧИЛО НАЗВАНИЕ «ТЕПЛОВОЙ СМЕРТИ» . БОЛЬЦМАН ВЫСКАЗАЛ МНЕНИЕ, ЧТО НЫНЕШНЕЕ СОСТОЯНИЕ ВСЕЛЕННОЙ — ЭТО ГИГАНТСКАЯ ФЛУКТУАЦИЯ, ИЗ ЧЕГО СЛЕДУЕТ, ЧТО БОЛЬШУЮ ЧАСТЬ ВРЕМЕНИ ВСЕЛЕННАЯ ВСЕ РАВНО ПРЕБЫВАЕТ В СОСТОЯНИИ ТЕРМОДИНАМИЧЕСКОГО РАВНОВЕСИЯ ( «ТЕПЛОВОЙ СМЕРТИ» ). ОБЩАЯ ТЕОРИЯ ОТНОСИТЕЛЬНОСТИ РАССМАТРИВАЕТ ВСЕЛЕННУЮ КАК СИСТЕМУ, НАХОДЯЩУЮСЯ В ПЕРЕМЕННОМ ГРАВИТАЦИОННОМ ПОЛЕ, И В ТАКИХ УСЛОВИЯХ ЗАКОН ВОЗРАСТАНИЯ ЭНТРОПИИ НЕПРИМЕНИМ
2 ЗАКОН ТЕРМОДИНАМИКИ КЛАУЗИУС, РАССМАТРИВАЯ ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ, ПРИШЁЛ К ВЫВОДУ, ЧТО ЭНТРОПИЯ ВСЕЛЕННОЙ КАК ЗАМКНУТОЙ СИСТЕМЫ СТРЕМИТСЯ К МАКСИМУМУ, И В КОНЦЕ КОНЦОВ ВО ВСЕЛЕННОЙ ЗАКОНЧАТСЯ ВСЕ МАКРОСКОПИЧЕСКИЕ ПРОЦЕССЫ. ЭТО СОСТОЯНИЕ ВСЕЛЕННОЙ ПОЛУЧИЛО НАЗВАНИЕ «ТЕПЛОВОЙ СМЕРТИ» . БОЛЬЦМАН ВЫСКАЗАЛ МНЕНИЕ, ЧТО НЫНЕШНЕЕ СОСТОЯНИЕ ВСЕЛЕННОЙ — ЭТО ГИГАНТСКАЯ ФЛУКТУАЦИЯ, ИЗ ЧЕГО СЛЕДУЕТ, ЧТО БОЛЬШУЮ ЧАСТЬ ВРЕМЕНИ ВСЕЛЕННАЯ ВСЕ РАВНО ПРЕБЫВАЕТ В СОСТОЯНИИ ТЕРМОДИНАМИЧЕСКОГО РАВНОВЕСИЯ ( «ТЕПЛОВОЙ СМЕРТИ» ). ОБЩАЯ ТЕОРИЯ ОТНОСИТЕЛЬНОСТИ РАССМАТРИВАЕТ ВСЕЛЕННУЮ КАК СИСТЕМУ, НАХОДЯЩУЮСЯ В ПЕРЕМЕННОМ ГРАВИТАЦИОННОМ ПОЛЕ, И В ТАКИХ УСЛОВИЯХ ЗАКОН ВОЗРАСТАНИЯ ЭНТРОПИИ НЕПРИМЕНИМ
 2 ЗАКОН ТЕРМОДИНАМИКИ Энергия Гиббса ПОЛНАЯ ХИМИЧЕСКАЯ ЭНЕРГИЯ СИСТЕМЫ ДЛЯ СИСТЕМЫ С ПОСТОЯННЫМ ЧИСЛОМ ЧАСТИЦ: ДЛЯ СИСТЕМЫ С ПЕРЕМЕННЫМ ЧИСЛОМ ЧАСТИЦ - ХИМИЧЕСКИЙ ПОТЕНЦИАЛ
2 ЗАКОН ТЕРМОДИНАМИКИ Энергия Гиббса ПОЛНАЯ ХИМИЧЕСКАЯ ЭНЕРГИЯ СИСТЕМЫ ДЛЯ СИСТЕМЫ С ПОСТОЯННЫМ ЧИСЛОМ ЧАСТИЦ: ДЛЯ СИСТЕМЫ С ПЕРЕМЕННЫМ ЧИСЛОМ ЧАСТИЦ - ХИМИЧЕСКИЙ ПОТЕНЦИАЛ
 2 ЗАКОН ТЕРМОДИНАМИКИ В ХИМИЧЕСКИХ ПРОЦЕССАХ ОДНОВРЕМЕННО ДЕЙСТВУЮТ ДВА ПРОТИВОПОЛОЖНЫХ ФАКТОРА — ЭНТРОПИЙНЫЙ И ЭНТАЛЬПИЙНЫЙ . СУММАРНЫЙ ЭФФЕКТ ЭТИХ ПРОТИВОПОЛОЖНЫХ ФАКТОРОВ В ПРОЦЕССАХ, ПРОТЕКАЮЩИХ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ И ТЕМПЕРАТУРЕ ОПРЕДЕЛЯЕТ ИЗМЕНЕНИЕ ЭНЕРГИИ ГИББСА ГИББС (Gibbs), Джозайя Уиллард 1839 г. – 1903 г
2 ЗАКОН ТЕРМОДИНАМИКИ В ХИМИЧЕСКИХ ПРОЦЕССАХ ОДНОВРЕМЕННО ДЕЙСТВУЮТ ДВА ПРОТИВОПОЛОЖНЫХ ФАКТОРА — ЭНТРОПИЙНЫЙ И ЭНТАЛЬПИЙНЫЙ . СУММАРНЫЙ ЭФФЕКТ ЭТИХ ПРОТИВОПОЛОЖНЫХ ФАКТОРОВ В ПРОЦЕССАХ, ПРОТЕКАЮЩИХ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ И ТЕМПЕРАТУРЕ ОПРЕДЕЛЯЕТ ИЗМЕНЕНИЕ ЭНЕРГИИ ГИББСА ГИББС (Gibbs), Джозайя Уиллард 1839 г. – 1903 г
 3 ЗАКОН ТЕРМОДИНАМИКИ ИЗМЕНЕНИЕ ЭНТРОПИИ (ΔS) ПРИ ЛЮБЫХ ОБРАТИМЫХ ИЗОТЕРМИЧЕСКИХ ПРОЦЕССАХ, СОВЕРШАЕМЫХ МЕЖДУ ДВУМЯ РАВНОВЕСНЫМИ СОСТОЯНИЯМИ ПРИ ТЕМПЕРАТУРАХ Т, ПРИБЛИЖАЮЩИХСЯ К АБСОЛЮТНОМУ НУЛЮ, СТРЕМИТСЯ К НУЛЮ: ПРИ ПОМОЩИ КОНЕЧНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ ТЕРМОДИНАМИЧЕСКИХ ПРОЦЕССОВ НЕЛЬЗЯ ДОСТИЧЬ ТЕМПЕРАТУРЫ, РАВНОЙ АБСОЛЮТНОМУ НУЛЮ. Нернст (Nernst) Вальтер Фридрих Герман (25. 6. 1864 — 18. 11. 194)
3 ЗАКОН ТЕРМОДИНАМИКИ ИЗМЕНЕНИЕ ЭНТРОПИИ (ΔS) ПРИ ЛЮБЫХ ОБРАТИМЫХ ИЗОТЕРМИЧЕСКИХ ПРОЦЕССАХ, СОВЕРШАЕМЫХ МЕЖДУ ДВУМЯ РАВНОВЕСНЫМИ СОСТОЯНИЯМИ ПРИ ТЕМПЕРАТУРАХ Т, ПРИБЛИЖАЮЩИХСЯ К АБСОЛЮТНОМУ НУЛЮ, СТРЕМИТСЯ К НУЛЮ: ПРИ ПОМОЩИ КОНЕЧНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ ТЕРМОДИНАМИЧЕСКИХ ПРОЦЕССОВ НЕЛЬЗЯ ДОСТИЧЬ ТЕМПЕРАТУРЫ, РАВНОЙ АБСОЛЮТНОМУ НУЛЮ. Нернст (Nernst) Вальтер Фридрих Герман (25. 6. 1864 — 18. 11. 194)
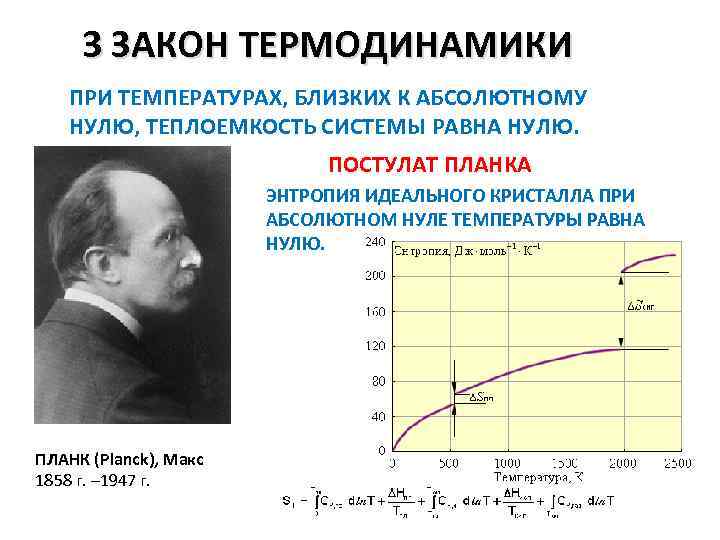 3 ЗАКОН ТЕРМОДИНАМИКИ ПРИ ТЕМПЕРАТУРАХ, БЛИЗКИХ К АБСОЛЮТНОМУ НУЛЮ, ТЕПЛОЕМКОСТЬ СИСТЕМЫ РАВНА НУЛЮ. ПОСТУЛАТ ПЛАНКА ЭНТРОПИЯ ИДЕАЛЬНОГО КРИСТАЛЛА ПРИ АБСОЛЮТНОМ НУЛЕ ТЕМПЕРАТУРЫ РАВНА НУЛЮ. ПЛАНК (Planck), Макс 1858 г. – 1947 г.
3 ЗАКОН ТЕРМОДИНАМИКИ ПРИ ТЕМПЕРАТУРАХ, БЛИЗКИХ К АБСОЛЮТНОМУ НУЛЮ, ТЕПЛОЕМКОСТЬ СИСТЕМЫ РАВНА НУЛЮ. ПОСТУЛАТ ПЛАНКА ЭНТРОПИЯ ИДЕАЛЬНОГО КРИСТАЛЛА ПРИ АБСОЛЮТНОМ НУЛЕ ТЕМПЕРАТУРЫ РАВНА НУЛЮ. ПЛАНК (Planck), Макс 1858 г. – 1947 г.
 2 ЗАКОН ТЕРМОДИНАМИКИ
2 ЗАКОН ТЕРМОДИНАМИКИ
 2 ЗАКОН ТЕРМОДИНАМИКИ
2 ЗАКОН ТЕРМОДИНАМИКИ
 2 ЗАКОН ТЕРМОДИНАМИКИ
2 ЗАКОН ТЕРМОДИНАМИКИ


