ФизХим_МВТМ_Гетерогенные коллоидные Системы.ppt
- Количество слайдов: 46
 Физическая Гетерогенные системы и их химия коллоидные получение. Профессор Кособудский Игорь Донатович
Физическая Гетерогенные системы и их химия коллоидные получение. Профессор Кособудский Игорь Донатович
 Гетерогенные коллоидные системы и их получение. Строение коллоидных частиц. Агрегативная и кинетическая устойчивость систем. Коагуляция. Эмульсии. Суспензии.
Гетерогенные коллоидные системы и их получение. Строение коллоидных частиц. Агрегативная и кинетическая устойчивость систем. Коагуляция. Эмульсии. Суспензии.
 Классификация дисперсных материалов по размерам дисперсной фазы
Классификация дисперсных материалов по размерам дисперсной фазы
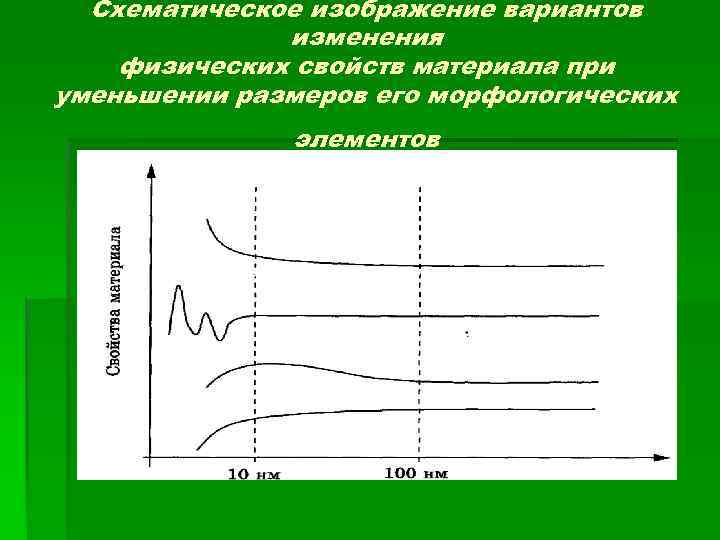 Схематическое изображение вариантов изменения физических свойств материала при уменьшении размеров его морфологических элементов Размеры морфологических элементов
Схематическое изображение вариантов изменения физических свойств материала при уменьшении размеров его морфологических элементов Размеры морфологических элементов
 § Коллоидные системы (коллоидно дисперсные системы, коллоиды) – предельно высокодисперсные (микрогетерогенные) системы. Частицы дисперсной фазы в коллоидной системе – коллоидные частицы – обычно имеют размер от 1 нм до 100 нм. В газе или жидкости они свободно и независимо одна от другой участвуют в интенсивном броуновском движении, равномерно заполняя весь объем дисперсной среды.
§ Коллоидные системы (коллоидно дисперсные системы, коллоиды) – предельно высокодисперсные (микрогетерогенные) системы. Частицы дисперсной фазы в коллоидной системе – коллоидные частицы – обычно имеют размер от 1 нм до 100 нм. В газе или жидкости они свободно и независимо одна от другой участвуют в интенсивном броуновском движении, равномерно заполняя весь объем дисперсной среды.
 § Коллоидные частицы имеют весьма малые размеры и поэтому участвуют в броуновском движении, в то же время они обладают заметной скоростью диффузии (10 1 10 3 см 2/с), что способствует выравниванию концентрации частиц по объему. Кроме того, если раздробить 1 см 3 вещества до размера коллоидной частицы, то суммарная площадь всех граней дисперсной фазы составит от 60 до 600 м 2. В этом случае частицы приобретают избыточную энергию, вследствие чего увеличивается адсорбция. § Коллоидные растворы – принципиально неустойчивые системы. § Свойство коллоидных систем увеличивать размер частиц путем их агрегации называется агрегативной неустойчивостью.
§ Коллоидные частицы имеют весьма малые размеры и поэтому участвуют в броуновском движении, в то же время они обладают заметной скоростью диффузии (10 1 10 3 см 2/с), что способствует выравниванию концентрации частиц по объему. Кроме того, если раздробить 1 см 3 вещества до размера коллоидной частицы, то суммарная площадь всех граней дисперсной фазы составит от 60 до 600 м 2. В этом случае частицы приобретают избыточную энергию, вследствие чего увеличивается адсорбция. § Коллоидные растворы – принципиально неустойчивые системы. § Свойство коллоидных систем увеличивать размер частиц путем их агрегации называется агрегативной неустойчивостью.
 § Агрегативная неустойчивость преодолевается путем адсорбции ионов или молекул на частицах дисперсной фазы, за счет чего на границе раздела фаз формируется скачок потенциала. Благодаря этому коллоидные системы обладают весьма высокой агрегативной устойчивостью, что при малых размерах частиц способствует седиментационной устойчивости, так как гравитационная сила, вызывающая седиментацию, нивелируется силами диффузии. § Способность дисперсных систем сохранять определенное распределение частиц по объему называется седиментационной или кинетической устойчивостью. Sedimentum (лат. ) – осадок.
§ Агрегативная неустойчивость преодолевается путем адсорбции ионов или молекул на частицах дисперсной фазы, за счет чего на границе раздела фаз формируется скачок потенциала. Благодаря этому коллоидные системы обладают весьма высокой агрегативной устойчивостью, что при малых размерах частиц способствует седиментационной устойчивости, так как гравитационная сила, вызывающая седиментацию, нивелируется силами диффузии. § Способность дисперсных систем сохранять определенное распределение частиц по объему называется седиментационной или кинетической устойчивостью. Sedimentum (лат. ) – осадок.
 § По характеру взаимодействия дисперсной фазы и дисперсионной среды коллоидные растворы можно подразделить на лиофобные (частицы дисперсной фазы практически не взаимодействуют с дисперсионной средой) и лиофильные коллоиды (растворы высокомолекулярных соединений), которые могут образовываться самопроизвольно, благодаря сильному взаимодействию дисперсной фазы и дисперсионной среды. § Они способны сохранять агрегативную устойчивость без стабилизатора в двухкомпонентном растворе.
§ По характеру взаимодействия дисперсной фазы и дисперсионной среды коллоидные растворы можно подразделить на лиофобные (частицы дисперсной фазы практически не взаимодействуют с дисперсионной средой) и лиофильные коллоиды (растворы высокомолекулярных соединений), которые могут образовываться самопроизвольно, благодаря сильному взаимодействию дисперсной фазы и дисперсионной среды. § Они способны сохранять агрегативную устойчивость без стабилизатора в двухкомпонентном растворе.
 § Лиофильные системы термодинамически устойчивы (ΔG≤ 0) и характеризуются самопроизвольным диспергированием. Так, мыла и многие глины (например, бентонитовая) самопроизвольно «распускаются» в воде, а ВМС растворяются в «хорошем» растворителе до отдельных макромолекул и представляют собой истинные растворы
§ Лиофильные системы термодинамически устойчивы (ΔG≤ 0) и характеризуются самопроизвольным диспергированием. Так, мыла и многие глины (например, бентонитовая) самопроизвольно «распускаются» в воде, а ВМС растворяются в «хорошем» растворителе до отдельных макромолекул и представляют собой истинные растворы
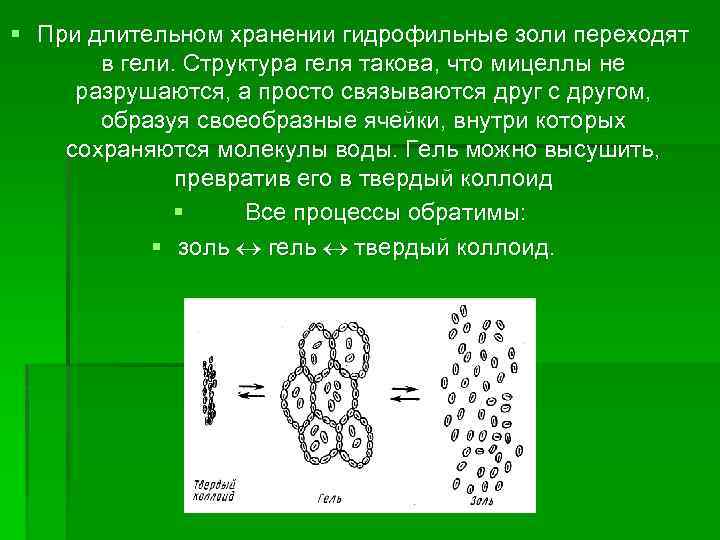 § При длительном хранении гидрофильные золи переходят в гели. Структура геля такова, что мицеллы не разрушаются, а просто связываются друг с другом, образуя своеобразные ячейки, внутри которых сохраняются молекулы воды. Гель можно высушить, превратив его в твердый коллоид § Все процессы обратимы: § золь гель твердый коллоид.
§ При длительном хранении гидрофильные золи переходят в гели. Структура геля такова, что мицеллы не разрушаются, а просто связываются друг с другом, образуя своеобразные ячейки, внутри которых сохраняются молекулы воды. Гель можно высушить, превратив его в твердый коллоид § Все процессы обратимы: § золь гель твердый коллоид.
 Рис. 2. Колодные растворы Si. O 2 в воде, полученные золь – гель методом. Влияние размера частиц на седиментационную устойчивость. Размер частиц, нм 500 280 150 87 менее 20
Рис. 2. Колодные растворы Si. O 2 в воде, полученные золь – гель методом. Влияние размера частиц на седиментационную устойчивость. Размер частиц, нм 500 280 150 87 менее 20
 Получены по реакции: Si(OC 2 H 5)4 + H 2 O → Si. O 2 + 4 C 2 H 5 OH (в присутствии раствора аммиака (катализатор) и этилового спирта NH 3 (0. 1 -0. 5 M), C 2 H 5 OH (1 -7 M), T= 50 0 C Cнимок с оптического микроскопа (не видна микроструктура частиц), частицы сферические. Cнимок с электронного микроскопа (видна микроструктура частиц), каждая частица размером – 100 – 200 нм, состоит из множества более мелких.
Получены по реакции: Si(OC 2 H 5)4 + H 2 O → Si. O 2 + 4 C 2 H 5 OH (в присутствии раствора аммиака (катализатор) и этилового спирта NH 3 (0. 1 -0. 5 M), C 2 H 5 OH (1 -7 M), T= 50 0 C Cнимок с оптического микроскопа (не видна микроструктура частиц), частицы сферические. Cнимок с электронного микроскопа (видна микроструктура частиц), каждая частица размером – 100 – 200 нм, состоит из множества более мелких.
 СТРОЕНИЕ КОЛЛОИДНЫХ ЧАСТИЦ § В основу современных представлений о строении коллоидных частиц легли работы российских ученых А. В. Думанского, Н. П. Пескова, С. М. Липатова, А. Н. Фрумкина, а также зарубежных исследователей Паули, Фаянса, Кройта и других. Строение коллоидных частиц удобнее рассматривать, если проследить процессы образования частиц на примере образования коллоидной частицы Ag. I: § Ag. NO 3 + KI↔ Ag. I + KNO 3 § Молекулы Ag. I объединяются в практически нерастворимые частицы, в которых ионы Ag+ и I образуют кристаллическую решетку. Если Ag. NO 3 и KI взяты в эквивалентных количествах, то частицы кристаллы растут, достигая значительной величины, превосходящей размеры коллоидных
СТРОЕНИЕ КОЛЛОИДНЫХ ЧАСТИЦ § В основу современных представлений о строении коллоидных частиц легли работы российских ученых А. В. Думанского, Н. П. Пескова, С. М. Липатова, А. Н. Фрумкина, а также зарубежных исследователей Паули, Фаянса, Кройта и других. Строение коллоидных частиц удобнее рассматривать, если проследить процессы образования частиц на примере образования коллоидной частицы Ag. I: § Ag. NO 3 + KI↔ Ag. I + KNO 3 § Молекулы Ag. I объединяются в практически нерастворимые частицы, в которых ионы Ag+ и I образуют кристаллическую решетку. Если Ag. NO 3 и KI взяты в эквивалентных количествах, то частицы кристаллы растут, достигая значительной величины, превосходящей размеры коллоидных
 § § Если же одно из исходных веществ взято в небольшом избытке, то оно служит стабилизатором, сообщающим устойчивость коллоидным частицам Ag. I. При избытке Ag. NO 3 в растворе будут находиться ионы Ag+ и NO 3–. Построение кристаллической решетки Ag. I, согласно правилу Панета-Фаянса, может идти только за счет ионов, входящих в ее состав, в данном случае – за счет ионов Ag+. Ионы Ag+ будут продолжать достраивать кристал лическую решетку ядра, входя в его структуру и сообщая ему электрический заряд (1) определяющий так называемый электротермодинамический потенциал. Ионы, достроившие кристаллическую решетку ядра, называются потенциалопределяющими ионами(2 Б). Величина электротермодинамического потенциала (φ или E потенциала) у многих коллоидных частиц достигает 1 В. Частицы с таким высоким зарядом будут притягивать оставшиеся в растворе противоположно заряженные ионы NO 3 (противоионы)(2 а).
§ § Если же одно из исходных веществ взято в небольшом избытке, то оно служит стабилизатором, сообщающим устойчивость коллоидным частицам Ag. I. При избытке Ag. NO 3 в растворе будут находиться ионы Ag+ и NO 3–. Построение кристаллической решетки Ag. I, согласно правилу Панета-Фаянса, может идти только за счет ионов, входящих в ее состав, в данном случае – за счет ионов Ag+. Ионы Ag+ будут продолжать достраивать кристал лическую решетку ядра, входя в его структуру и сообщая ему электрический заряд (1) определяющий так называемый электротермодинамический потенциал. Ионы, достроившие кристаллическую решетку ядра, называются потенциалопределяющими ионами(2 Б). Величина электротермодинамического потенциала (φ или E потенциала) у многих коллоидных частиц достигает 1 В. Частицы с таким высоким зарядом будут притягивать оставшиеся в растворе противоположно заряженные ионы NO 3 (противоионы)(2 а).
 В процесс адсорбции противо ионов устанавливается динамическое равновесие между адсорбированными и свободными ионами. Основная часть всех противоионов, адсорбированная на ядре коллоидной частицы, образует вместе с потенциалопределяющими ионами адсорбционный слой или плотную часть двойного электрического слоя. Ядро и адсорбционный слой вместе составляют гранулу. Гранула вместе с диффузным слоем образует мицеллу (III).
В процесс адсорбции противо ионов устанавливается динамическое равновесие между адсорбированными и свободными ионами. Основная часть всех противоионов, адсорбированная на ядре коллоидной частицы, образует вместе с потенциалопределяющими ионами адсорбционный слой или плотную часть двойного электрического слоя. Ядро и адсорбционный слой вместе составляют гранулу. Гранула вместе с диффузным слоем образует мицеллу (III).
 § Строение электрического § На поверхности твердой фазы находятся потенциалопределяющие ионы 1. Противоионы распределяются между двумя слоями: часть противоионов входит в адсорбционный слой 2, толщина его очень невелика и противоионы распределяются в нем в плоскости параллельной поверхности твердой фазы, другая часть противоионов образует диффузный слой 3 с закономерно убывающей концентрацией ионов.
§ Строение электрического § На поверхности твердой фазы находятся потенциалопределяющие ионы 1. Противоионы распределяются между двумя слоями: часть противоионов входит в адсорбционный слой 2, толщина его очень невелика и противоионы распределяются в нем в плоскости параллельной поверхности твердой фазы, другая часть противоионов образует диффузный слой 3 с закономерно убывающей концентрацией ионов.
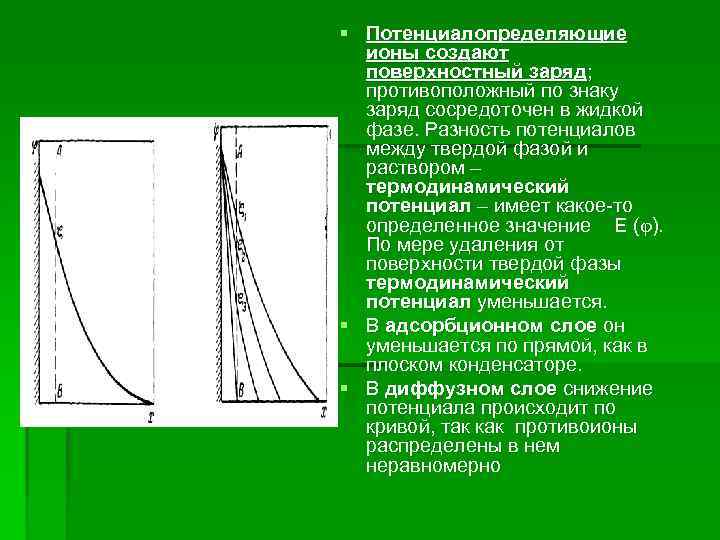 § Потенциалопределяющие ионы создают поверхностный заряд; противоположный по знаку заряд сосредоточен в жидкой фазе. Разность потенциалов между твердой фазой и раствором – термодинамический потенциал – имеет какое то определенное значение Е ( ). По мере удаления от поверхности твердой фазы термодинамический потенциал уменьшается. § В адсорбционном слое он уменьшается по прямой, как в плоском конденсаторе. § В диффузном слое снижение потенциала происходит по кривой, так как противоионы распределены в нем неравномерно
§ Потенциалопределяющие ионы создают поверхностный заряд; противоположный по знаку заряд сосредоточен в жидкой фазе. Разность потенциалов между твердой фазой и раствором – термодинамический потенциал – имеет какое то определенное значение Е ( ). По мере удаления от поверхности твердой фазы термодинамический потенциал уменьшается. § В адсорбционном слое он уменьшается по прямой, как в плоском конденсаторе. § В диффузном слое снижение потенциала происходит по кривой, так как противоионы распределены в нем неравномерно
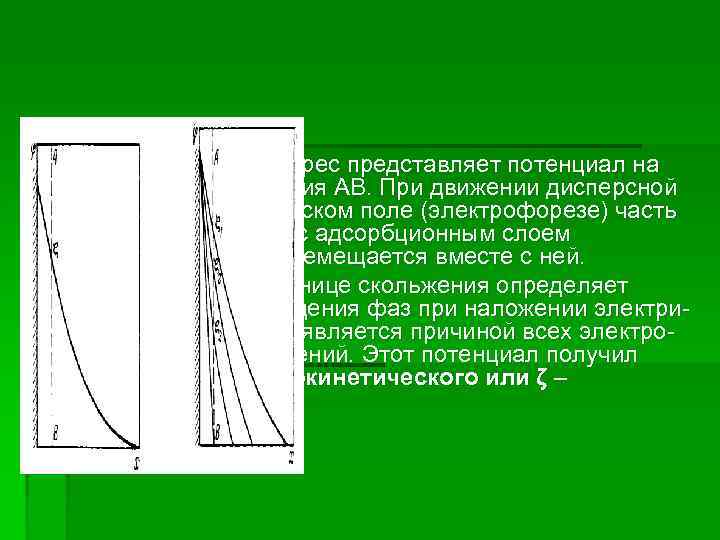 § Наибольший интерес представляет потенциал на границе скольжения АВ. При движении дисперсной фазы в электрическом поле (электрофорезе) часть жидкости вместе с адсорбционным слоем противоионов перемещается вместе с ней. § Потенциал на границе скольжения определяет скорость перемещения фаз при наложении электри ческого поля, т. е. является причиной всех электро кинетических явлений. Этот потенциал получил название электрокинетического или ζ – потенциала.
§ Наибольший интерес представляет потенциал на границе скольжения АВ. При движении дисперсной фазы в электрическом поле (электрофорезе) часть жидкости вместе с адсорбционным слоем противоионов перемещается вместе с ней. § Потенциал на границе скольжения определяет скорость перемещения фаз при наложении электри ческого поля, т. е. является причиной всех электро кинетических явлений. Этот потенциал получил название электрокинетического или ζ – потенциала.
 Типы потенциалопределяющих ионов Потенциалопределяющим ионом может быть любой ион, способный достраивать кристаллическую решетку нерастворимого соединения. Различают три типа потенциалопределяющих ионов: § 1) ионы одноименные с ионами агрегата § {m Fe. PO 4 (n. PO 4 )3 3 (n x ) N a + }3 x Na +; § 2) изоморфные ионы (т. е. ионы, имеющие близкое строение по отношению к ионам кристаллической решетки); {m Ag. I n. Cl (n x ) K + } x K + ; (иону I изоморфны ионы галогенидов Сl , Br ); § 3) органические ионы большого размера, обладающие высокой адсорбционной способностью, например, соли жирных кислот, являющихся стабилизаторами латексов : {m. П n. RCOO (n x) Na + } x Na +.
Типы потенциалопределяющих ионов Потенциалопределяющим ионом может быть любой ион, способный достраивать кристаллическую решетку нерастворимого соединения. Различают три типа потенциалопределяющих ионов: § 1) ионы одноименные с ионами агрегата § {m Fe. PO 4 (n. PO 4 )3 3 (n x ) N a + }3 x Na +; § 2) изоморфные ионы (т. е. ионы, имеющие близкое строение по отношению к ионам кристаллической решетки); {m Ag. I n. Cl (n x ) K + } x K + ; (иону I изоморфны ионы галогенидов Сl , Br ); § 3) органические ионы большого размера, обладающие высокой адсорбционной способностью, например, соли жирных кислот, являющихся стабилизаторами латексов : {m. П n. RCOO (n x) Na + } x Na +.
 Принципы построения мицелл § 1) Агрегат мицеллы должен быть нерастворимым соединением. § 2) Потенциалопределяющими ионами могут быть ионы, входящие в дисперсную фазу, изоморфные им ионы, органические ионы с высокой адсорбционной способностью. § 3) Противоионы образуют с потенциалопределяющим ионом растворимое соединение. § 4) Мицелла в целом электронейтральна.
Принципы построения мицелл § 1) Агрегат мицеллы должен быть нерастворимым соединением. § 2) Потенциалопределяющими ионами могут быть ионы, входящие в дисперсную фазу, изоморфные им ионы, органические ионы с высокой адсорбционной способностью. § 3) Противоионы образуют с потенциалопределяющим ионом растворимое соединение. § 4) Мицелла в целом электронейтральна.
 КОАГУЛЯЦИЯ КОЛЛОИДОВ § Процесс слипания коллоидных частиц называется коагуляцией. Её можно вызвать нагреванием, замораживанием, интенсивным перемешиванием, центрифугированием, добавлением различных электролитов. Прибавление электролита к коллоидному раствору приводит к снижению электрокинетического потенциала и, следовательно, к уменьшению сил отталкивания. § Вещество, коагулирующее дисперсную фазу коллоидной системы, называется коагулянтом, а ион, вызывающийэтот процесс – коагулятором.
КОАГУЛЯЦИЯ КОЛЛОИДОВ § Процесс слипания коллоидных частиц называется коагуляцией. Её можно вызвать нагреванием, замораживанием, интенсивным перемешиванием, центрифугированием, добавлением различных электролитов. Прибавление электролита к коллоидному раствору приводит к снижению электрокинетического потенциала и, следовательно, к уменьшению сил отталкивания. § Вещество, коагулирующее дисперсную фазу коллоидной системы, называется коагулянтом, а ион, вызывающийэтот процесс – коагулятором.
 § Закономерности коагуляции можно объединить в общие правила. § 1. Все электролиты вызывают коагуляцию коллоидных растворов при увеличении концентрации до некоторого значения. Минимальная концентрация, вызывающая коагуляцию, называется порогом коагуляции. § 2. Коагулирующим действием обладает ион, который имеет заряд, одноименный с зарядом противоионов мицеллы. § 3. Ионы высшей валентности вызывают коагуляцию при гораздо меньших концентрациях, чем ионы низшей валентности. По сравнению с одновалентным ионом коагулирующая способность двухвалентного будет больше в несколько десятков раз, а трехвалентного – в несколько сот раз. § 4. Коагулирующая способность ионов одинаковой валентности возрастает с увеличением радиуса иона. Ионы органических соединений всегда обладают более высокой коагулирующей способностью. § 5. При увеличении концентрации электролита в растворе уменьшается электрокинетический потенциал, и коагуляция наступает при его определенном значении – критическом потенциале. В большинстве случаев критический потенциал равен 0, 03 В.
§ Закономерности коагуляции можно объединить в общие правила. § 1. Все электролиты вызывают коагуляцию коллоидных растворов при увеличении концентрации до некоторого значения. Минимальная концентрация, вызывающая коагуляцию, называется порогом коагуляции. § 2. Коагулирующим действием обладает ион, который имеет заряд, одноименный с зарядом противоионов мицеллы. § 3. Ионы высшей валентности вызывают коагуляцию при гораздо меньших концентрациях, чем ионы низшей валентности. По сравнению с одновалентным ионом коагулирующая способность двухвалентного будет больше в несколько десятков раз, а трехвалентного – в несколько сот раз. § 4. Коагулирующая способность ионов одинаковой валентности возрастает с увеличением радиуса иона. Ионы органических соединений всегда обладают более высокой коагулирующей способностью. § 5. При увеличении концентрации электролита в растворе уменьшается электрокинетический потенциал, и коагуляция наступает при его определенном значении – критическом потенциале. В большинстве случаев критический потенциал равен 0, 03 В.
 § Различают два вида коагуляции коллоидных растворов электролитами: концентрационную и нейтрализационную. § 1. концентрационная наблюдается при увеличении концентрации индифферентного электролита, не вступающего в химическое взаимодействие с компонентами коллоидного раствора. Такие электролиты не должны иметь ионов, способных достраивать кристаллическую решетку агрегата коллоидной мицеллы и вступать в реакцию с потенциалопределяющими ионами. При увеличении концентрации индифферентного электролита диффузный слой противоионов мицеллы сжимается, в результате чего электрокинетический потенциал уменьшается вплоть до нуля. Такое состояние коллоидной системы называется изоэлектрическим. §
§ Различают два вида коагуляции коллоидных растворов электролитами: концентрационную и нейтрализационную. § 1. концентрационная наблюдается при увеличении концентрации индифферентного электролита, не вступающего в химическое взаимодействие с компонентами коллоидного раствора. Такие электролиты не должны иметь ионов, способных достраивать кристаллическую решетку агрегата коллоидной мицеллы и вступать в реакцию с потенциалопределяющими ионами. При увеличении концентрации индифферентного электролита диффузный слой противоионов мицеллы сжимается, в результате чего электрокинетический потенциал уменьшается вплоть до нуля. Такое состояние коллоидной системы называется изоэлектрическим. §
 § 2. При нейтрализационной коагуляции ионы прибавляемого электролита нейтрализуют потенциалопределяющие ионы, уменьшается термодинамический потенциал и, соответственно, уменьшается и ζ потенциал.
§ 2. При нейтрализационной коагуляции ионы прибавляемого электролита нейтрализуют потенциалопределяющие ионы, уменьшается термодинамический потенциал и, соответственно, уменьшается и ζ потенциал.
 § Основная причина коагуляции частиц заключается не столько в достижении некоторого (для всех случаев постоянного) критического ζ потенциала, сколько в понижении расклинивающего давления, которое перестает препятствовать объединению частиц. § Необходимое понижение этого давления достигается уменьшением диффузного слоя, что в свою очередь ведет к соответствующему понижению величины ζ потенциала. § Коагуляцию можно ускорить, повышая скорость движения частиц, что помогает им преодолевать расклинивающее давление. § Ускорения движения частиц можно добиться, например, повышением температуры раствора. § Повышением концентрации золя также можно ускорить его коагуляцию, поскольку с увеличением концентрации растет число эффективных столкновений между мицеллами.
§ Основная причина коагуляции частиц заключается не столько в достижении некоторого (для всех случаев постоянного) критического ζ потенциала, сколько в понижении расклинивающего давления, которое перестает препятствовать объединению частиц. § Необходимое понижение этого давления достигается уменьшением диффузного слоя, что в свою очередь ведет к соответствующему понижению величины ζ потенциала. § Коагуляцию можно ускорить, повышая скорость движения частиц, что помогает им преодолевать расклинивающее давление. § Ускорения движения частиц можно добиться, например, повышением температуры раствора. § Повышением концентрации золя также можно ускорить его коагуляцию, поскольку с увеличением концентрации растет число эффективных столкновений между мицеллами.
 § Коагулирующее действие электролитов зависит от величины заряда иона, который противоположен заряду коллоидной частицы. § При достаточной концентрации электролита практически все противоионы окажутся в адсорбционном слое, заряд частицы снизится до нуля; § отсутствие диффузного слоя обусловит значительное понижение давления расклинивания, и коагуляция пойдет с максимальной скоростью. § Коагулирующее действие иона коагулятора тем больше, чем больше его заряд (правило Шульце Гарди). Значения порогов коагуляции для одно , двух и трехвалентных ионов относятся как 1: 0, 016: 0, 0013.
§ Коагулирующее действие электролитов зависит от величины заряда иона, который противоположен заряду коллоидной частицы. § При достаточной концентрации электролита практически все противоионы окажутся в адсорбционном слое, заряд частицы снизится до нуля; § отсутствие диффузного слоя обусловит значительное понижение давления расклинивания, и коагуляция пойдет с максимальной скоростью. § Коагулирующее действие иона коагулятора тем больше, чем больше его заряд (правило Шульце Гарди). Значения порогов коагуляции для одно , двух и трехвалентных ионов относятся как 1: 0, 016: 0, 0013.
 МЕТОДЫ ПОЛУЧЕНИЯ ЛИОФОБНЫХ КОЛЛОИДОВ § Коллоидные растворы могут быть получены либо путем ассоциации (конденсации) молекул и ионов истинных растворов, либо раздроблением частиц грубодисперсных систем. В отдельную группу может быть выделен метод получения с помощью пептизации.
МЕТОДЫ ПОЛУЧЕНИЯ ЛИОФОБНЫХ КОЛЛОИДОВ § Коллоидные растворы могут быть получены либо путем ассоциации (конденсации) молекул и ионов истинных растворов, либо раздроблением частиц грубодисперсных систем. В отдельную группу может быть выделен метод получения с помощью пептизации.
 Методы конденсации 1. Метод физической конденсации § Этот метод основан на конденсации паров в вакууме на поверхности сосуда, охлажденного жидким воздухом (рис. 14. 5). Для этого в отростках 1 и 3 прибора подвергаются испарению одновременно диспергируемое вещество (например, натрий) и дисперсионная среда (например, бензол) при температуре 673 К. Пары этих веществ конденсируются на поверхности сосуда 4, охлаждаемого жидким воздухом до 197 К, при этом охлажденный твердый бензол, намерзающий на стенках, содержит затвердевший натрий. После удаления из сосуда 4 жидкого воздуха температура постепенно повышается, оттаявшая смесь бензола с натрием попадает в отросток 2, образуя коллоидный раствор натрия в бензоле.
Методы конденсации 1. Метод физической конденсации § Этот метод основан на конденсации паров в вакууме на поверхности сосуда, охлажденного жидким воздухом (рис. 14. 5). Для этого в отростках 1 и 3 прибора подвергаются испарению одновременно диспергируемое вещество (например, натрий) и дисперсионная среда (например, бензол) при температуре 673 К. Пары этих веществ конденсируются на поверхности сосуда 4, охлаждаемого жидким воздухом до 197 К, при этом охлажденный твердый бензол, намерзающий на стенках, содержит затвердевший натрий. После удаления из сосуда 4 жидкого воздуха температура постепенно повышается, оттаявшая смесь бензола с натрием попадает в отросток 2, образуя коллоидный раствор натрия в бензоле.
 § Перевести растворенное вещество, находящееся в молекулярно дисперсном раздроблении в коллоидное раздробление можно заменой одного растворителя другим. Для этого необходимо иметь два смешивающихся между собой растворителя, один из которых хорошо растворяет вещество, а другой – не растворяет. § Так, канифоль хорошо растворима в спирте и почти не растворима в воде. При добавлении к спиртовому раствору мастики воды происходит резкое понижение растворимости мастики, в результате чего
§ Перевести растворенное вещество, находящееся в молекулярно дисперсном раздроблении в коллоидное раздробление можно заменой одного растворителя другим. Для этого необходимо иметь два смешивающихся между собой растворителя, один из которых хорошо растворяет вещество, а другой – не растворяет. § Так, канифоль хорошо растворима в спирте и почти не растворима в воде. При добавлении к спиртовому раствору мастики воды происходит резкое понижение растворимости мастики, в результате чего
 § К этой Методы химической конденсации группе относятся методы, основанные на проведении в растворе химических реакций, сопровождающихся образованием нерастворимых или труднорастворимых веществ. Так, красный золь золота получают восстановлением соли золота формальдегидом до металлического золота с образованием золя золота по схеме: § 2 Na. Au. O 2+3 HCOH+Na 2 CO 3 = 2 Au+3 HCOONa+Na. HCO 3+H 2 § На образующихся частичках (кристалликах золота) адсорбируются ионы Au. O 2–. Аналогичным образом получают желто коричневый золь серебра. § При действии на каменную соль Na. Cl радиоактивного излучения выделяется металлический натрий, который, распределяясь в кристаллической среде, обусловливает голубое окрашивание кристаллов. § Золи образуются также в результате химической реакции двойного обмена, в результате которых образуется нерастворимое вещество, которое при соответствующих условиях превращается в коллоидный раствор. § Процесс гидролиза различных растворимых соединений (например, Fe. Cl 3) часто сопровождается образованием нерастворимых веществ, которые превращаются в коллоидные растворы.
§ К этой Методы химической конденсации группе относятся методы, основанные на проведении в растворе химических реакций, сопровождающихся образованием нерастворимых или труднорастворимых веществ. Так, красный золь золота получают восстановлением соли золота формальдегидом до металлического золота с образованием золя золота по схеме: § 2 Na. Au. O 2+3 HCOH+Na 2 CO 3 = 2 Au+3 HCOONa+Na. HCO 3+H 2 § На образующихся частичках (кристалликах золота) адсорбируются ионы Au. O 2–. Аналогичным образом получают желто коричневый золь серебра. § При действии на каменную соль Na. Cl радиоактивного излучения выделяется металлический натрий, который, распределяясь в кристаллической среде, обусловливает голубое окрашивание кристаллов. § Золи образуются также в результате химической реакции двойного обмена, в результате которых образуется нерастворимое вещество, которое при соответствующих условиях превращается в коллоидный раствор. § Процесс гидролиза различных растворимых соединений (например, Fe. Cl 3) часто сопровождается образованием нерастворимых веществ, которые превращаются в коллоидные растворы.
 К образованию золей приводят различные химические реакции: − окисления восстановления, − обмена, − гидролиза и др. § 1. Реакции окисления. 2 H 2 S + О 2 = 2 S + 2 H 2 O(реакция образование золя при взаимодействии сероводорода, растворенного в гидротермальных водах § 2. Реакции обмена. Этим способом получают золи галогенидов, сульфидов, оксидов и гидроксидов металлов. Аg N O 3 + К I = Ag I↓ + K N O 3 § 3. Гидролиз солей. Реакция гидролиза хлорного железа. Fe. Cl 3 + 3 Н 2 0 (гор. ) → Fe (OH)3 + 3 НСl
К образованию золей приводят различные химические реакции: − окисления восстановления, − обмена, − гидролиза и др. § 1. Реакции окисления. 2 H 2 S + О 2 = 2 S + 2 H 2 O(реакция образование золя при взаимодействии сероводорода, растворенного в гидротермальных водах § 2. Реакции обмена. Этим способом получают золи галогенидов, сульфидов, оксидов и гидроксидов металлов. Аg N O 3 + К I = Ag I↓ + K N O 3 § 3. Гидролиз солей. Реакция гидролиза хлорного железа. Fe. Cl 3 + 3 Н 2 0 (гор. ) → Fe (OH)3 + 3 НСl
 Дисперсионные методы Метод механического раздробления § В основе этих методов лежит раздробление твердых тел до частиц коллоидного размера. Процесс раздробления осуществляется: механическим или электрическим раздроблением, действием ультразвука. Механическое раздробление проводят в коллоидных мельницах. Частички вещества в предварительно измельченном виде смешиваются с соответствующей жидкостью, содержащей стабилизатор, и в виде взвеси подаются через загрузочное отверстие. При помощи быстро вращающихся лопастей взвесь приводится в быстрое вращение, в результате чего частицы вещества приобретают скорость и, ударяясь о неподвижные выступы, разбиваются на мелкие частицы.
Дисперсионные методы Метод механического раздробления § В основе этих методов лежит раздробление твердых тел до частиц коллоидного размера. Процесс раздробления осуществляется: механическим или электрическим раздроблением, действием ультразвука. Механическое раздробление проводят в коллоидных мельницах. Частички вещества в предварительно измельченном виде смешиваются с соответствующей жидкостью, содержащей стабилизатор, и в виде взвеси подаются через загрузочное отверстие. При помощи быстро вращающихся лопастей взвесь приводится в быстрое вращение, в результате чего частицы вещества приобретают скорость и, ударяясь о неподвижные выступы, разбиваются на мелкие частицы.
 Получение коллоидных частиц методом электрического распыления § Этот метод состоит в том, что через какую либо дисперсионную среду (воду, например) пропускают электрический ток между электродами, изготовленными из материала, коллоидный раствор которого хотят получить. Так, для получения золя платины используют платиновые электроды, пропуская между ними электрическую дугу. При этом один электрод распыляется.
Получение коллоидных частиц методом электрического распыления § Этот метод состоит в том, что через какую либо дисперсионную среду (воду, например) пропускают электрический ток между электродами, изготовленными из материала, коллоидный раствор которого хотят получить. Так, для получения золя платины используют платиновые электроды, пропуская между ними электрическую дугу. При этом один электрод распыляется.
 Получение коллоидных растворов с помощью ультразвука § Колебания воздуха с большой частотой (105 106 Гц) называются ультразвуковыми волнами, которые образуются благодаря применению так называемых пьезоэлектрических осцилляторов. При этом взвесь грубодисперсного вещества под действием ультразвуковых волн размельчается до коллоидного состояния. Этим методом можно получить коллоидные растворы смол, гипса, графита, металлов, красителей, крахмала и многих других веществ.
Получение коллоидных растворов с помощью ультразвука § Колебания воздуха с большой частотой (105 106 Гц) называются ультразвуковыми волнами, которые образуются благодаря применению так называемых пьезоэлектрических осцилляторов. При этом взвесь грубодисперсного вещества под действием ультразвуковых волн размельчается до коллоидного состояния. Этим методом можно получить коллоидные растворы смол, гипса, графита, металлов, красителей, крахмала и многих других веществ.
 § § § Метод пептизации В отличие от других методов образования коллоидных растворов при пептизации не происходит изменения степени дисперсности частиц. Ионы пептизатора хорошо адсорбируются на поверхности коллоидных частиц осадка и обусловливают их переход в золь. Различают непосредственную (если на поверхности частиц адсорбируется непосредственно добавленный пептизатор) и посредственную пептизацию (на поверхности адсорбируется продукт взаимодействия пептизатора с веществом дисперсной фазы). Пример непосредственной пептизации – диспергирование студенистого осадка Fe(OH)3 при действии на него Fe. Cl 3. Примером посредственной пептизации может служить получение того же золя Fe(OH)3 при действии разбавленной соляной кислоты. При этом часть молекул Fe(OH)3, взаимодействуя с соляной кислотой, переходят в оксохлорид железа (Fe. OCl). Молекулы Fe. OCl, адсорбируясь на поверхности частиц осадка Fe(OH)3, переводят его в коллоидное состояние.
§ § § Метод пептизации В отличие от других методов образования коллоидных растворов при пептизации не происходит изменения степени дисперсности частиц. Ионы пептизатора хорошо адсорбируются на поверхности коллоидных частиц осадка и обусловливают их переход в золь. Различают непосредственную (если на поверхности частиц адсорбируется непосредственно добавленный пептизатор) и посредственную пептизацию (на поверхности адсорбируется продукт взаимодействия пептизатора с веществом дисперсной фазы). Пример непосредственной пептизации – диспергирование студенистого осадка Fe(OH)3 при действии на него Fe. Cl 3. Примером посредственной пептизации может служить получение того же золя Fe(OH)3 при действии разбавленной соляной кислоты. При этом часть молекул Fe(OH)3, взаимодействуя с соляной кислотой, переходят в оксохлорид железа (Fe. OCl). Молекулы Fe. OCl, адсорбируясь на поверхности частиц осадка Fe(OH)3, переводят его в коллоидное состояние.
 ГРУБОДИСПЕРСНЫЕ СИСТЕМЫ § К грубодисперсным относятся системы, в которых частицы дисперсной фазы имеют размеры 10– 5 м. К ним относятся эмульсии, пены, суспензии, порошки. § Эмульсиями называются грубодисперсные системы из несмешивающихся жидкостей (Ж/Ж). В таких системах одна жидкость (дисперсная фаза) взвешена в другой (дисперсной среде) в виде капелек. Размеры капелек могут достигать 5000 мкм и более. Эмульсии имеют выраженную поверхность раздела, неустойчивы и
ГРУБОДИСПЕРСНЫЕ СИСТЕМЫ § К грубодисперсным относятся системы, в которых частицы дисперсной фазы имеют размеры 10– 5 м. К ним относятся эмульсии, пены, суспензии, порошки. § Эмульсиями называются грубодисперсные системы из несмешивающихся жидкостей (Ж/Ж). В таких системах одна жидкость (дисперсная фаза) взвешена в другой (дисперсной среде) в виде капелек. Размеры капелек могут достигать 5000 мкм и более. Эмульсии имеют выраженную поверхность раздела, неустойчивы и
 § Главным фактором их устойчивости является заряд. Чаще всего эмульсии состоят из воды и жидкости, которую принято называть «масло» . Возможны два типа эмульсий: масло в воде (м/в) , и вода в масле (в/м).
§ Главным фактором их устойчивости является заряд. Чаще всего эмульсии состоят из воды и жидкости, которую принято называть «масло» . Возможны два типа эмульсий: масло в воде (м/в) , и вода в масле (в/м).
 § Гидрофобные эмульгаторы стабилизируют эмульсии типа в/м: их молекула, находящаяся большей своей частью в дисперсионной среде (масле), удерживается на поверхности капелек воды своей гидрофильной группировкой. В результате вокруг каждой капельки воды образуется плотная оболочка из молекул эмульгатора, препятствующая слиянию дисперсной фазы (воды). Эмульгаторы разных классов соединений могут сообщать системе различную степень дисперсности(см. табл. ). Тип эмульсии определяется добавленным стабилизатором: если к смеси равных объемов воды и бензола добавить гидрофильный эмульгатор, то образуется эмульсия типа м/в, добавление гидрофобного эмульгатора приводит к возникновению эмульсии типа в/м.
§ Гидрофобные эмульгаторы стабилизируют эмульсии типа в/м: их молекула, находящаяся большей своей частью в дисперсионной среде (масле), удерживается на поверхности капелек воды своей гидрофильной группировкой. В результате вокруг каждой капельки воды образуется плотная оболочка из молекул эмульгатора, препятствующая слиянию дисперсной фазы (воды). Эмульгаторы разных классов соединений могут сообщать системе различную степень дисперсности(см. табл. ). Тип эмульсии определяется добавленным стабилизатором: если к смеси равных объемов воды и бензола добавить гидрофильный эмульгатор, то образуется эмульсия типа м/в, добавление гидрофобного эмульгатора приводит к возникновению эмульсии типа в/м.
 § Образование эмульсии происходит и при отмывании жирных пятен мылом. По своему строению к эмульсиям приближаются пены. § Пены характеризуются сплошным ячеистым строением и наличием газовой дисперсной фазы. Устойчивые пены образуются в присутствии поверхностно активных веществ (мыла, белки и т. п. ). Пенообразование используется, например, для обогащения руд способом флотации.
§ Образование эмульсии происходит и при отмывании жирных пятен мылом. По своему строению к эмульсиям приближаются пены. § Пены характеризуются сплошным ячеистым строением и наличием газовой дисперсной фазы. Устойчивые пены образуются в присутствии поверхностно активных веществ (мыла, белки и т. п. ). Пенообразование используется, например, для обогащения руд способом флотации.
 § К грубодисперсным системам могут быть отнесены также суспензии и порошки. § § Дисперсные системы, у которых дисперсионной средой является газ, называются аэрозолями. Диспергированным веществом в аэрозолях могут быть частицы твердого вещества (дым и др. ), а также капельки жидкости (облака, туман и др. ). Устойчивость аэрозолей объясняется наличием электрического заряда, возникающего на поверхности раздела двух фаз, а, кроме того, каждая частичка твердого или жидкого вещества адсорбирует на своей поверхности газ, в результате чего образуется оболочка, которая препятствует их объединению и, следовательно, быстрому оседанию.
§ К грубодисперсным системам могут быть отнесены также суспензии и порошки. § § Дисперсные системы, у которых дисперсионной средой является газ, называются аэрозолями. Диспергированным веществом в аэрозолях могут быть частицы твердого вещества (дым и др. ), а также капельки жидкости (облака, туман и др. ). Устойчивость аэрозолей объясняется наличием электрического заряда, возникающего на поверхности раздела двух фаз, а, кроме того, каждая частичка твердого или жидкого вещества адсорбирует на своей поверхности газ, в результате чего образуется оболочка, которая препятствует их объединению и, следовательно, быстрому оседанию.
 § Аэрозоли широко применяются в военном деле (дымовые завесы и др. ), в сельском хозяйстве и других отраслях народного хозяйства (распыление различных дезинфицирующих веществ: инсектицидов, гербицидов и т. п. ).
§ Аэрозоли широко применяются в военном деле (дымовые завесы и др. ), в сельском хозяйстве и других отраслях народного хозяйства (распыление различных дезинфицирующих веществ: инсектицидов, гербицидов и т. п. ).
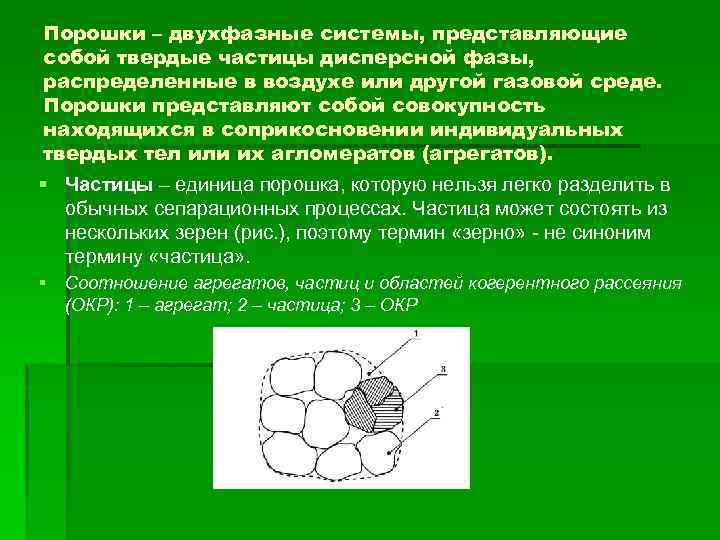 Порошки – двухфазные системы, представляющие собой твердые частицы дисперсной фазы, распределенные в воздухе или другой газовой среде. Порошки представляют собой совокупность находящихся в соприкосновении индивидуальных твердых тел или их агломератов (агрегатов). § Частицы – единица порошка, которую нельзя легко разделить в обычных сепарационных процессах. Частица может состоять из нескольких зерен (рис. ), поэтому термин «зерно» не синоним термину «частица» . § Соотношение агрегатов, частиц и областей когерентного рассеяния (ОКР): 1 – агрегат; 2 – частица; 3 – ОКР
Порошки – двухфазные системы, представляющие собой твердые частицы дисперсной фазы, распределенные в воздухе или другой газовой среде. Порошки представляют собой совокупность находящихся в соприкосновении индивидуальных твердых тел или их агломератов (агрегатов). § Частицы – единица порошка, которую нельзя легко разделить в обычных сепарационных процессах. Частица может состоять из нескольких зерен (рис. ), поэтому термин «зерно» не синоним термину «частица» . § Соотношение агрегатов, частиц и областей когерентного рассеяния (ОКР): 1 – агрегат; 2 – частица; 3 – ОКР
 Агломерат (агрегат) – несколько частиц, соединенных в более крупные образования. Агрегаты и агломераты различают по наличию внутренней пористости. В агломератах присутствуют межчастичные пустоты (рис. а), в агрегатах – нет (рис. б). Схематическое изображение агломерированного (а) и агрегированного (б) порошка; 1 – агломерат, 2 – первичная частица, 3 – внутриагломератная пора, 4 – межагломератная пора, 5 – агрегат, 6 – межагрегатная пора
Агломерат (агрегат) – несколько частиц, соединенных в более крупные образования. Агрегаты и агломераты различают по наличию внутренней пористости. В агломератах присутствуют межчастичные пустоты (рис. а), в агрегатах – нет (рис. б). Схематическое изображение агломерированного (а) и агрегированного (б) порошка; 1 – агломерат, 2 – первичная частица, 3 – внутриагломератная пора, 4 – межагломератная пора, 5 – агрегат, 6 – межагрегатная пора
 Задание на дом для всех § 1. Назовите два характерных признака коллоидных систем. 2. По каким признакам можно провести классификацию дисперсных систем? Каковы общие и частные признаки классификации? 3. Что такое коллоидная мицелла? Назовите принципы построения коллоидной мицеллы. § 4. Назовите три типа потенциа лопределяющих ионов.
Задание на дом для всех § 1. Назовите два характерных признака коллоидных систем. 2. По каким признакам можно провести классификацию дисперсных систем? Каковы общие и частные признаки классификации? 3. Что такое коллоидная мицелла? Назовите принципы построения коллоидной мицеллы. § 4. Назовите три типа потенциа лопределяющих ионов.
 Вариант 1 1. Золь сернокислого бария получен смешением равных объемов растворов Ва(NО 3)2 и Н 2 SО 4. Написать формулу мицеллы. Одинаковы ли исходные концентрации растворов, если частицы золя перемещаются к аноду? 2. Для получения золя Аg. Cl смешали 10 х10 6 м 3 0, 02 н раствора КCl и 100 х10 6 м 3 0, 05 н раствора Ag. NO 3. Написать формулу мицеллы этого золя и указать направление движения частиц при электрофорезе. § Вариант 2 § 1. Золь Аl(ОН)3 получен смешением равных объемов растворов Аl. Cl 3 и Na. ОН. Написать формулу мицеллы золя. Одинаковы ли исходные концентрации электролитов, если при электрофорезе частицы движутся к катоду? § 2. Золь Fe(OH)3 получен методом гидролиза Fe. Cl 3. Напишите формулу мицеллы, если считать, что стабилизатором золя является раствор оксихлорида железа (Fe. OCl).
Вариант 1 1. Золь сернокислого бария получен смешением равных объемов растворов Ва(NО 3)2 и Н 2 SО 4. Написать формулу мицеллы. Одинаковы ли исходные концентрации растворов, если частицы золя перемещаются к аноду? 2. Для получения золя Аg. Cl смешали 10 х10 6 м 3 0, 02 н раствора КCl и 100 х10 6 м 3 0, 05 н раствора Ag. NO 3. Написать формулу мицеллы этого золя и указать направление движения частиц при электрофорезе. § Вариант 2 § 1. Золь Аl(ОН)3 получен смешением равных объемов растворов Аl. Cl 3 и Na. ОН. Написать формулу мицеллы золя. Одинаковы ли исходные концентрации электролитов, если при электрофорезе частицы движутся к катоду? § 2. Золь Fe(OH)3 получен методом гидролиза Fe. Cl 3. Напишите формулу мицеллы, если считать, что стабилизатором золя является раствор оксихлорида железа (Fe. OCl).
 § СПАСИБО ЗА ВНИМАНИЕ!
§ СПАСИБО ЗА ВНИМАНИЕ!


