413081.ppt
- Количество слайдов: 38

ФГБУ «НАУЧНЫЙ ЦЕНТР НЕВРОЛОГИИ» РОССИЙСКОЙ АКАДЕМИИ МЕДИЦИНСКИХ НАУК ГЕННАЯ ТЕРАПИЯ БОКОВОГО АМИОТРОФИЧЕСКОГО СКЛЕРОЗА: З. А. Суслина, Б. С. Народицкий, В. З. Тарантул, С. Н. Иллариошкин, М. Н. Захарова, И. А. Завалишин, М. М. Шмаров, А. Л. Гинцбург, Н. П. Бочков ФГБУ «Научный центр неврологии» РАМН, Институт молекулярной генетики РАН, НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи МЗ РФ Москва, 2013

БАС – прогрессирующее нейродегенеративное заболевание, обусловленное избирательным поражением периферических мотонейронов передних рогов спинного мозга и двигательных ядер мозгового ствола, а также центральных мотонейронов. Заболевание проявляется неуклонно нарастающими парезами, мышечными атрофиями, фасцикулляциями и пирамидным синдромом Стивен Хокинг астрофизик

Спорадическая форма – 90 -95% больных Частота - 3 -5 на 100000 населения Возраст 55 -60 лет Соотношение мужчин и женщин 1, 6: 1 Семейная форма – 5 -10% больных Ювенильная форма – 10% Западно-Тихоокеанская форма (БАС + паркинсонизм + деменция) Частота - в 100 раз чаще, чем спорадическая

Индукторы запрограммированной клеточной гибели при БАС Экзогенные q Вирусы q Токсины Эндогенные q q q Мутации (Cu/Zn-СОД 1, алсин) Экзайтотоксичность Окислительный стресс Нарушение Са 2+ гомеостаза Митохондриальная дисфункция Конформационные изменения белков и нарушения их деградации q Дефицит нейротрофических факторов q Нарушение структуры и функции цитоскелетных белков и аксонального транспорта
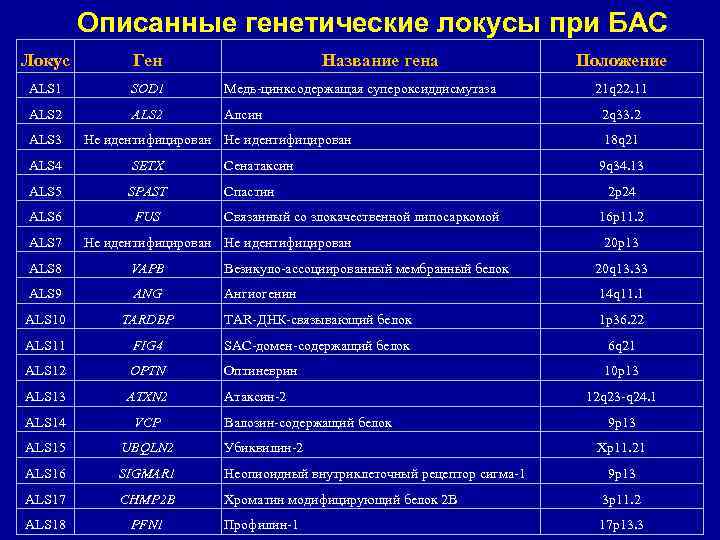
Описанные генетические локусы при БАС Локус Ген ALS 1 SOD 1 Медь-цинксодержащая супероксиддисмутаза ALS 2 Алсин ALS 3 Название гена Не идентифицирован ALS 4 SETX Сенатаксин ALS 5 SPAST Спастин ALS 6 FUS ALS 7 Связанный со злокачественной липосаркомой Не идентифицирован Положение 21 q 22. 11 2 q 33. 2 18 q 21 9 q 34. 13 2 p 24 16 p 11. 2 20 p 13 ALS 8 VAPB Везикуло-ассоциированный мембранный белок 20 q 13. 33 ALS 9 ANG Ангиогенин 14 q 11. 1 ALS 10 TARDBP TAR-ДНК-связывающий белок 1 p 36. 22 ALS 11 FIG 4 SAC-домен-содержащий белок 6 q 21 ALS 12 OPTN Оптиневрин 10 p 13 ALS 13 ATXN 2 Атаксин-2 ALS 14 VCP ALS 15 UBQLN 2 Убиквилин-2 ALS 16 SIGMAR 1 Неопиоидный внутриклеточный рецептор сигма-1 ALS 17 CHMP 2 B Хроматин модифицирующий белок 2 В 3 p 11. 2 ALS 18 PFN 1 Профилин-1 17 p 13. 3 Валозин-содержащий белок 12 q 23 -q 24. 1 9 p 13 Xp 11. 21 9 p 13

Подходы к разработке новых методов терапии БАС • • • основываются на современных представлениях о механизмах гибели мотонейрона используются препараты, доказавшие свою эффективность на различных природных и трансгенных моделях болезни двигательного нейрона у животных при БАС могут быть эффективны и препараты, которые с успехом уже применяются при других нейродегенеративных заболеваниях (болезнь Паркинсона, болезнь Альцгеймера, хорея Гентингтона, прионные болезни)

Нейротрофические факторы, регулирующие выживание мотонейронов • Нейротрофины (BDNF, NT-3, NT 4/5) • Цитокины (CNTF, LIF, CT-1 (кардиотрофин-1)) • Трансформирующие ростковые факторы (GDNF, neuroturin, persephin) • Инсулиноподобные ростковые факторы (IGF-1, IGF-2) • Гипоксия индуцибельные факторы (VEGF, эритропоэтин, ангиогенин)

Особенности регуляции выживания мотонейронов 1. Синергизм действия НТФ (CNTF и IGF-1; CNTF и BDNF; CNTF и LIF; GDNF и NT 3, 4/5) 2. Способность замещать друга 3. Гетерогенность действия на различные субпопуляции мотонейронов спинного мозга, ядер черепно-мозговых нервов, двигательной коры

VEGF (vascular endothelial growth factor) - фактор роста эндотелия кровеносных сосудов, относящийся к новому классу соединений - гипоксия индуцибельных нейротрофических факторов. • • В экспериментах на животных показано, что уменьшение уровня VEGF приводит не только к снижению нейрональной перфузии, но и к недостаточности VEGF опосредованной нейропротекции Делеция промоторного элемента, в гене VEGF, определяющего реакцию на гипоксию (HRE) вызывает БДН у мышей Данная мутация приводит к избирательному снижению VEGF в МН на 40%, при гипоксии - на 75% Полиморфизмы в гене VEGF, приводящие к снижению его экспрессии, повышают риск заболевания БАС в 1, 8 раза Снижение уровня VEGF в биологических жидкостях больных БАС и корреляция с тяжестью заболевания

Ангиогенин (ANG) • является ключевым фактором • • регулирования ростковых факторов ангиогенеза функции ANG разнообразны и включают стимуляцию процессов транскрипции и трансляции белков, регуляцию биогенеза рибосом, пролиферацию и рост эндотелиальных клеток частота встречаемости мутаций в гене ANG у больных БАС 1, 5%

Клинические испытания НТФ при БАС (подкожное, внутримышечное, интратекальное введение) Положительные эффекты • Замедление прогрессирования при в/м введении IGF-1 • Улучшение ЖЕЛ после в/м введения BDNF Отрицательные эффекты • Быстрая деградация пептидных молекул и, соответственно, кратковременный эффект • Низкая проницаемость через ГЭБ • Выраженность периферических побочных эффектов • Токсичность при введении больших доз • Образование аутоантител к нейротрофическим факторам

Свойства рекомбинантных аденовирусов Безопасность • не вызывают вирусной инфекции; • не встраиваются в геном клеток-мишеней; • выводятся из организма в течение 4 - 5 недель Эффективность • способны проникать в широкий спектр как делящихся, так и неделящихся клеток; • осуществляют высокоэффективную экспрессию генов терапевтического вмешательства
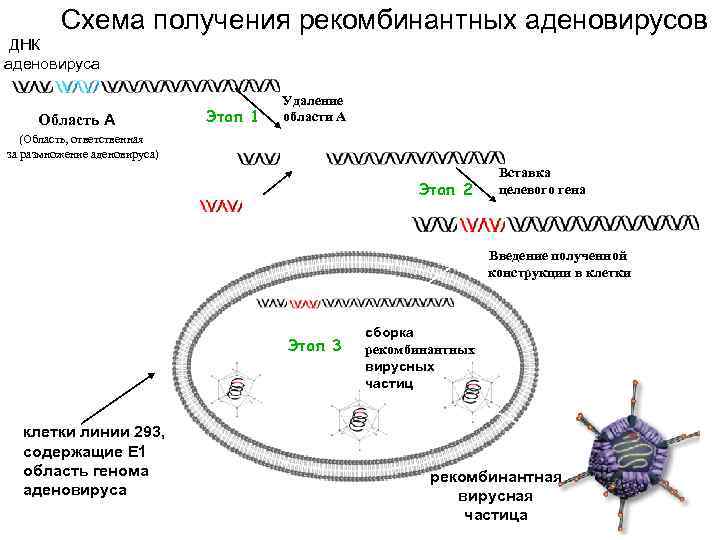
Схема получения рекомбинантных аденовирусов ДНК аденовируса Область А Этап 1 Удаление области А (Область, ответственная за размножение аденовируса) Этап 2 VEGF Вставка целевого гена Введение полученной конструкции в клетки Этап 3 клетки линии 293, содержащие E 1 область генома аденовируса сборка рекомбинантных вирусных частиц рекомбинантная вирусная частица
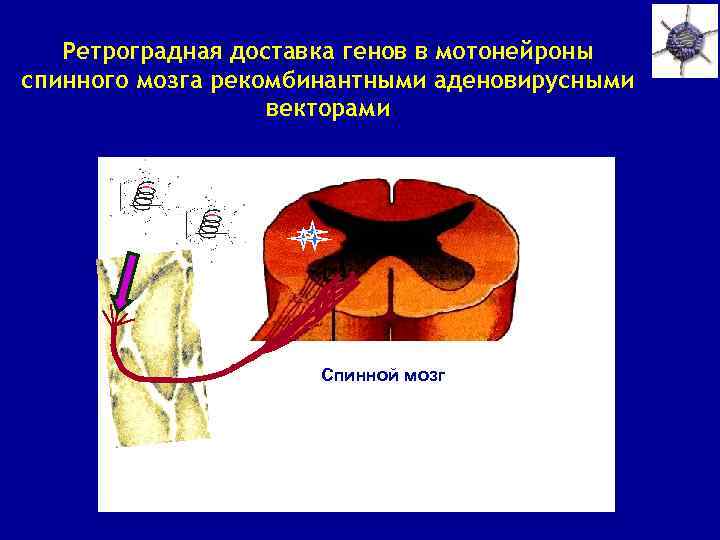
Ретроградная доставка генов в мотонейроны спинного мозга рекомбинантными аденовирусными векторами Спинной мозг

Характеристика препарата Аде. Васк™ Торговое название препарата: Аде. Васк™ Международное непатентованное название: нет Лекарственная форма: раствор для внутримышечного введения, доза/3 мл. Состав: смесь (1: 1) рекомбинантных псевдоаденовирусных частиц, экспрессирующих гены фактора роста эндотелия сосудов человека и ангиогенина человека, в суммарной концентрации (7, 0± 1, 4)х1011 частиц в 3 мл буферного раствора.

Экспериментальная модель БАС трансгенные мыши линии B 6 SJL-Tg(SOD 1*G 93 A)dl 1 Gur/J (мыши линии SOD 1*G 93 A). • экспрессируют мутантный ген Cu/Zn-супероксиддисмутазы SOD 1 • характеризуются прогрессирующей дегенерацией мотонейронов, • в возрасте 6– 7 месяцев появляются первые клинические признаки заболевания: парез и последующий паралич одной или двух конечностей, с последующей генерализацией • умирают через 4– 6 недель после клинической манифестации заболевания в возрасте около 8 месяцев

Дизайн исследования на трансгенных животных • Начало инъекций с 5 -месячного возраста до конца жизни • Курс инъекций через каждые 2 недели • Раствор вводился билатерально в разные группы мышц передних, задних конечностей и спины (всего 6 групп); в каждой из указанных мышечных зон было по 5 точек введения, каждое введение – по 30 мкл препарата или сравниваемого контрольного раствора (в каждую группу мышц по 150 мкл, соответственно) • общее количество вводимого препарата 0, 9 мл
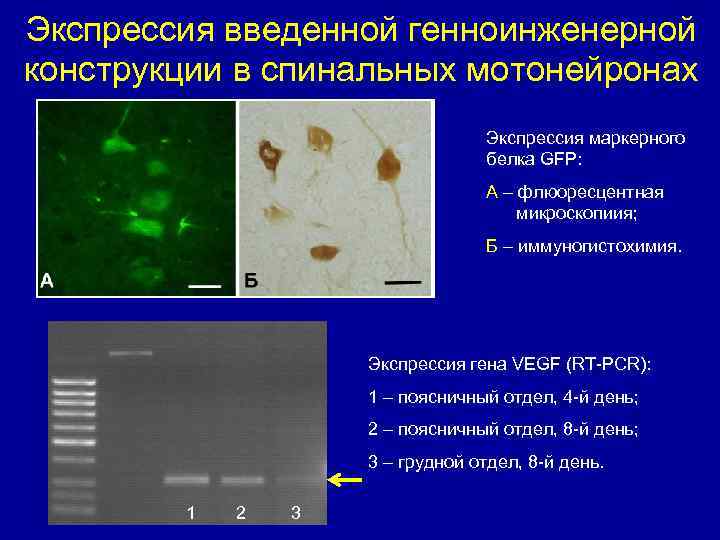
Экспрессия введенной генноинженерной конструкции в спинальных мотонейронах Экспрессия маркерного белка GFP: A – флюоресцентная микроскопиия; Б – иммуногистохимия. Экспрессия гена VEGF (RT-PCR): 1 – поясничный отдел, 4 -й день; 2 – поясничный отдел, 8 -й день; 3 – грудной отдел, 8 -й день. 1 2 3

Безопасность • повторные инъекции не приводили к летальным исходам и выбраковке экспериментальных животных • после введения препарата (сравниваемого раствора) у животных не наблюдалось явных признаков воспалительных, аллергических реакций или проявлений системной интоксикации • в экспериментальных группах не зафиксировано каких-либо ассоциированных патологических состояний, которые могли бы быть прямо или косвенно связаны с введением рекомбинантного препарата
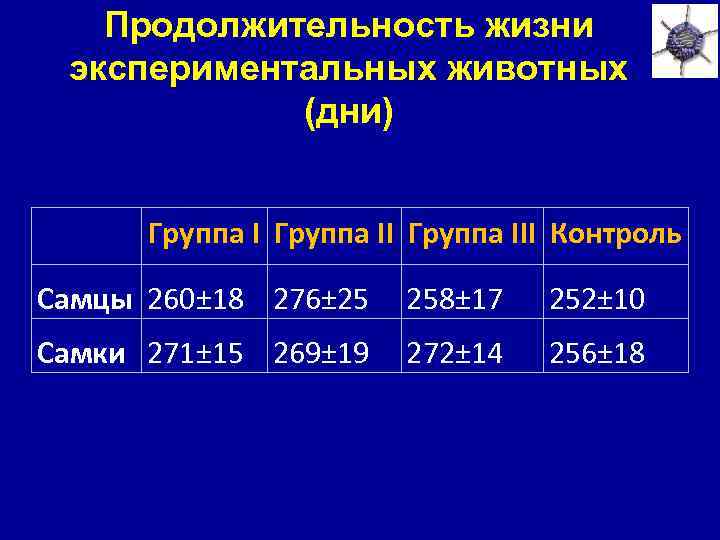
Продолжительность жизни экспериментальных животных (дни) Группа III Контроль Самцы 260± 18 276± 25 258± 17 252± 10 Самки 271± 15 269± 19 272± 14 256± 18
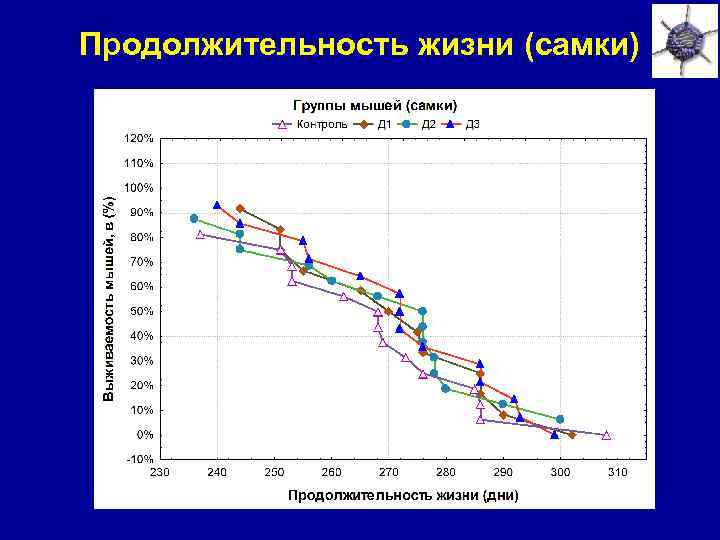
Продолжительность жизни (самки)
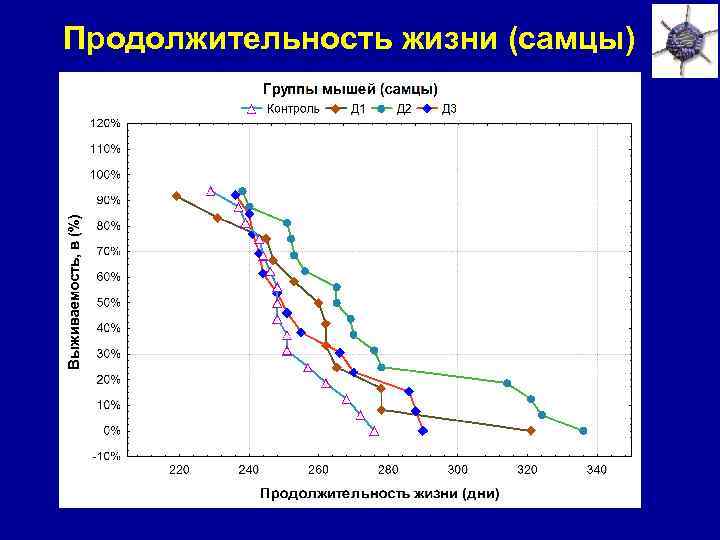
Продолжительность жизни (самцы)
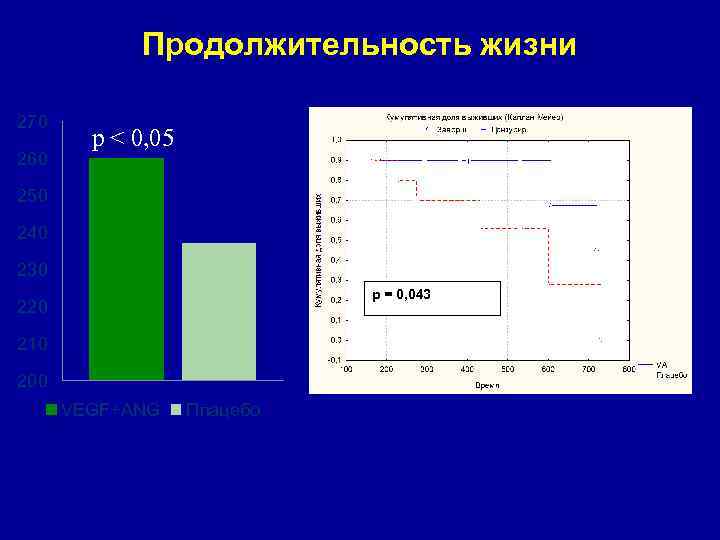
Продолжительность жизни 270 260 p < 0, 05 250 240 230 p = 0, 043 220 210 200 VEGF+ANG Плацебо

Оценка показателей двигательной активности и неврологического статуса Установка Opto-Varimex-3 ("Columbus instruments", США) Оценка неврологического статуса: паралич задних конечностей
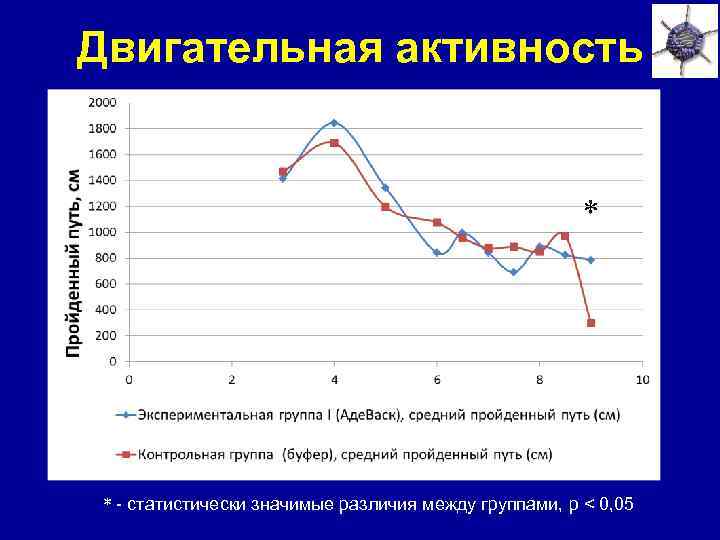
Двигательная активность * * * - статистически значимые различия между группами, p < 0, 05
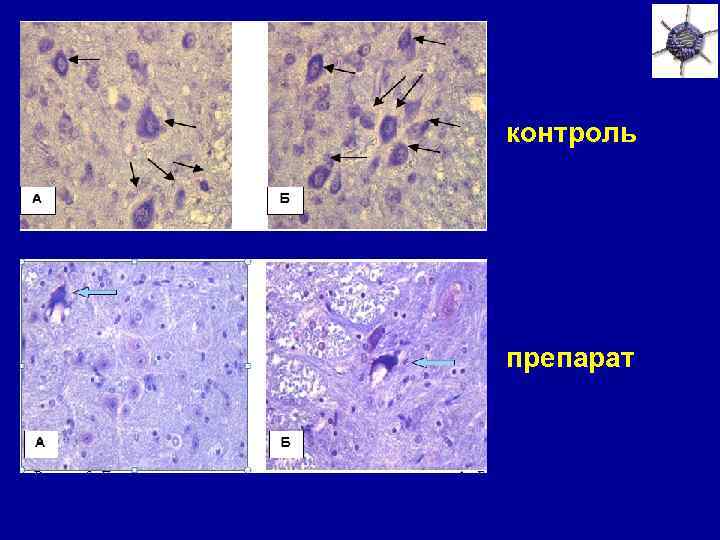
контроль препарат

Цель исследования Оценить безопасность и переносимость Ad. V терапии с введением генов VEGF 121 и ANG у больных со спорадической формой БАС

Критерии включения больных в исследование: • • Письменное информированное согласие Мужчины и женщины в возрасте от 18 до 69 лет Достоверный диагноз БАС, согласно международным критериям El Escorial (1998) Длительность заболевания не более 3 -х лет Значение по шкале ALSFRS не менее 30 баллов ЖЕЛ не менее 70% Женщины могут включаться в исследование при следующих условиях: - не обладающие репродуктивным потенциалом - обладающие репродуктивным потенциалом с отрицательным результатом теста мочи на беременность во время скрининга при условии согласия постоянно использовать один из указанных методов контрацепции (ВМС, барьерные методы контрацепции)

Критерии исключения • Пациенты, получавшие или получающие рилузол • Пациенты с клинически значимыми изменениями лабораторных показателей функции почек и печени • Наличие онкологических заболеваний у пациентов • Любое клинически значимое отклонение от нормы на ЭКГ, зарегистрированное в любом из 12 отведениях • Кормление грудью, беременные женщины или пациентки, планирующие беременность • Наличие сахарного диабета I-II типов • Наркотическая и лекарственная зависимость, алкогольная зависимость в течение последних 6 месяцев • Пациенты, позитивные по гепатитам В, С или ВИЧ • Участие в других клинических испытаниях • Наличие у больных трахеостомы или гастростомы • Высокий исходный уровень вируснейтрализующих антител (>1: 80)

Дизайн исследования • Рандомизированное плацебо-контролируемое исследование • 50 больных спорадическим БАС (25 пациентов получающих Ad. V VEGF+ANG, 25 получающих плацебо) • Введение препарата (или плацебо) внутримышечное в 3 мышцы (m. trapezius, m. deltoideus, m. quadriceps) с каждой стороны каждые 3 недели • Общая однократно вводимая доза препарата 1, 2 мл, содержащие 3 х109 БОЕ (бляшкообразующих единиц) (в каждую мышцу по 0, 2 мл) • Количество визитов – 26 (в течение 18 месяцев)

Безопасность и переносимость • Контроль за физиологическими показателями (АД, ЧСС, t тела, масса тела, ЭКГ) • Контроль лабораторных данных (клинический и биохимический анализы крови, мочи, исследование онкомаркёров) • Оценка нежелательных явлений (местных, системных, лабораторных отклонений)

Оценка прогрессирования заболевания • Исследование жизненной ёмкости лёгких (ЖЕЛ/ДЖЕЛ) • Оценка по функциональной шкале ALSFRSR • Исследование мышечной силы с оценкой по шкале ММТ (manual muscle test) • Выживаемость больных БАС
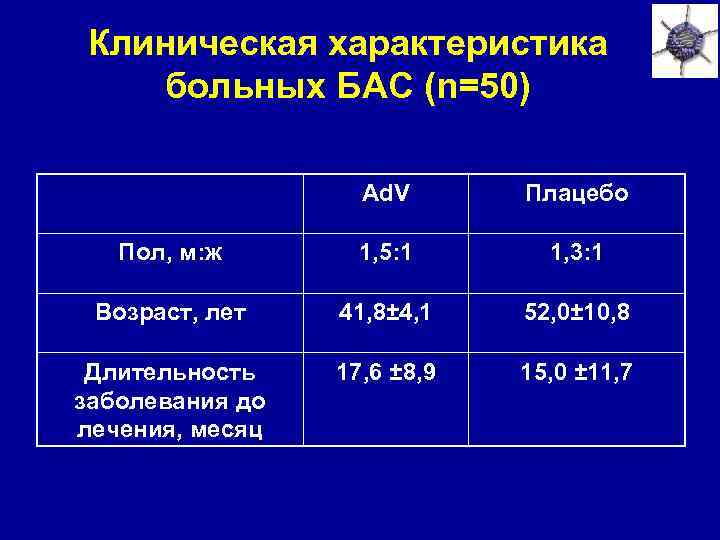
Клиническая характеристика больных БАС (n=50) Ad. V Плацебо Пол, м: ж 1, 5: 1 1, 3: 1 Возраст, лет 41, 8± 4, 1 52, 0± 10, 8 Длительность заболевания до лечения, месяц 17, 6 ± 8, 9 15, 0 ± 11, 7
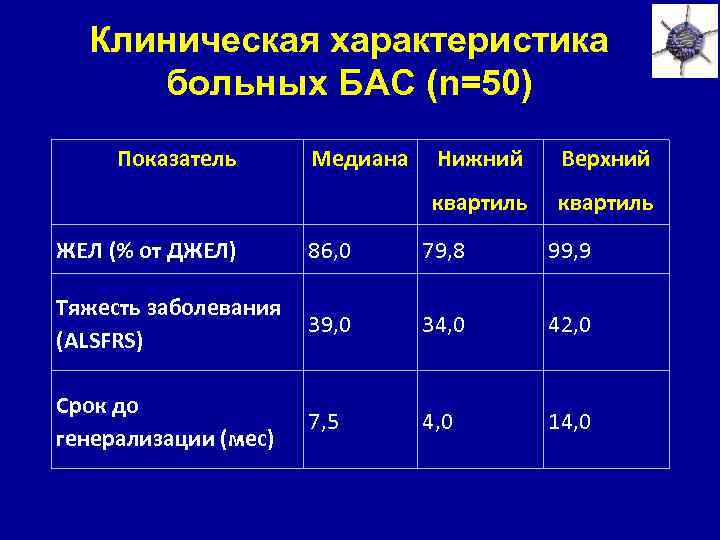
Клиническая характеристика больных БАС (n=50) Показатель Медиана Нижний Верхний квартиль ЖЕЛ (% от ДЖЕЛ) 86, 0 79, 8 99, 9 Тяжесть заболевания (ALSFRS) 39, 0 34, 0 42, 0 Срок до генерализации (мес) 7, 5 4, 0 14, 0
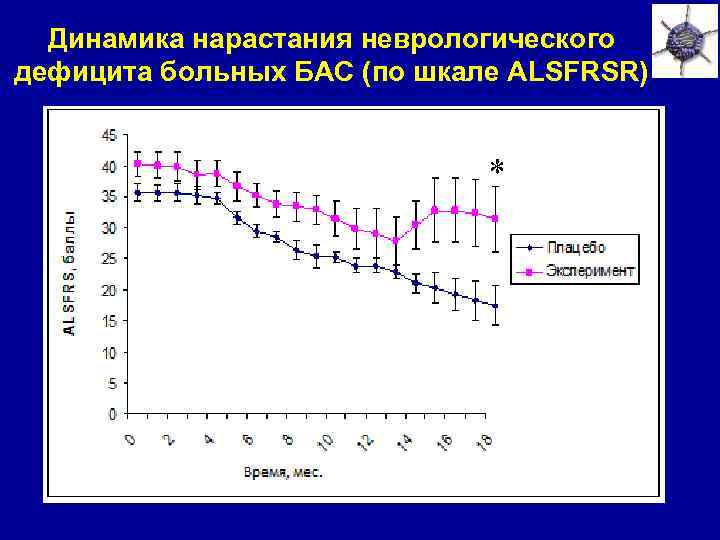
Динамика нарастания неврологического дефицита больных БАС (по шкале ALSFRSR) *
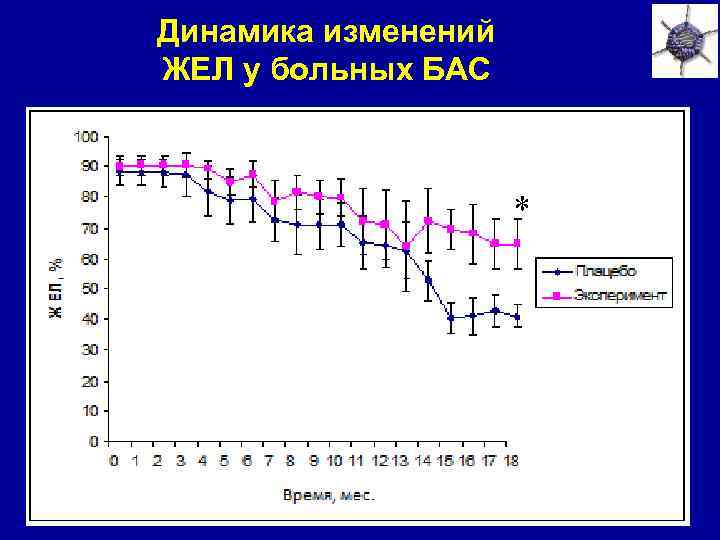
Динамика изменений ЖЕЛ у больных БАС *
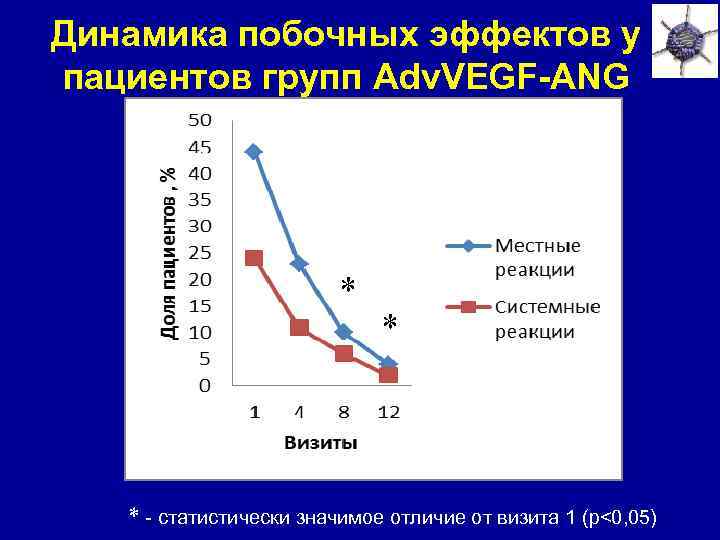
Динамика побочных эффектов у пациентов групп Adv. VEGF-ANG * * * - статистически значимое отличие от визита 1 (p<0, 05)

Заключение • Лечение препаратом Adv. VEGF+ANG замедляет нарастание неврологического дефицита у больных БАС • Лечение препаратом Adv. VEGF+ANG замедляет снижение жизненной емкости легких у больных БАС. • Во время исследования серьезных нежелательных явлений не было
413081.ppt