v побочная подгруппа.pptx
- Количество слайдов: 27

ФГБОУВПО Воронежский Государственный Университет Инженерных Технологий Кафедра неорганической химии и химической технологии V группа побочная подгруппа Выполнила: студентка I курса факультета ЭХТ группы х112 Пихтерева Елена Руководитель: к. х. н. , доц. НХ и ХТ Перегудов Ю. С.

Элементы V побочной подгруппы

Общая характеристика группы Электронное строение: V … 3 d 34 s 2 +23 Nb … 4 d 45 s 1 +41 Ta … 4 f 145 d 36 s 2 +73 Db … 5 f 146 d 37 s 2 +105 Степень окисления: Характерная степень окисления +5, известны и др. степени окисления +2, +3, +4
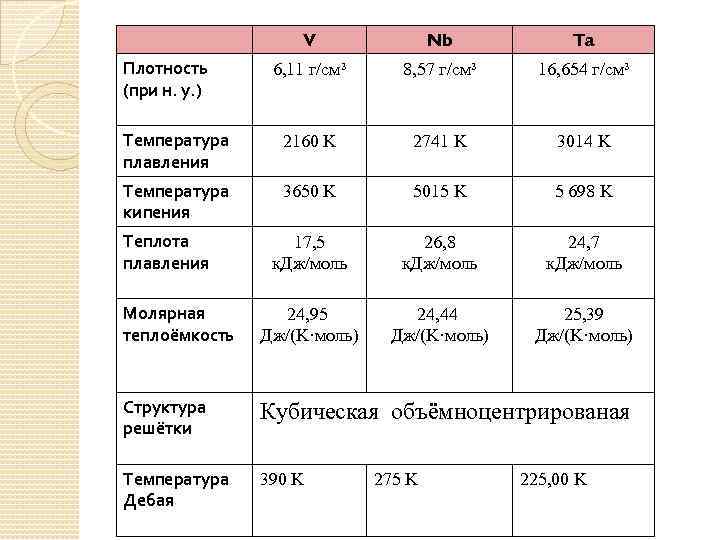
V Nb Ta 6, 11 г/см³ 8, 57 г/см³ 16, 654 г/см³ Температура плавления 2160 K 2741 K 3014 K Температура кипения 3650 K 5015 K 5 698 K 17, 5 к. Дж/моль 26, 8 к. Дж/моль 24, 7 к. Дж/моль Молярная теплоёмкость 24, 95 Дж/(K·моль) 24, 44 Дж/(K·моль) 25, 39 Дж/(K·моль) Структура решётки Кубическая объёмноцентрированая Температура Дебая 390 K Плотность (при н. у. ) Теплота плавления 275 K 225, 00 K

Bанадий Bанадий - пластичный металл серебристо- серого цвета. Ванадий был открыт в 1801 г. профессором минералогии из Мехико. Андресом Мануэлем Дель Рио в свинцовых рудах. Он обнаружил новый металл и предложил для него название «панхромий» из-за широкого диапазона цвета его соединений, сменив затем название на «эритроний» . В 1830 году ванадий был открыт заново шведским химиком Нильсом Сефстрёмом в железной руде. Новому элементу название дали Берцелиус и Сефстрём. Этот элемент образует соединения с красивой окраской, отсюда и название элемента, связанное с именем скандинавской богини любви и красоты Фрейи

Нахождение в природе Ванадий относится к рассеянным элементам и в природе в свободном виде не встречается. Содержание ванадия в земной коре 1, 6· 10− 2% по массе, в воде океанов 3· 10− 7%. Наиболее высокие средние содержания ванадия в магматических породах отмечаются в габбро и базальтах (230— 290 г/т). Важнейшие минералы: патронит V(S 2)2, ванадинит Pb 5(VO 4)3 Cl. Основной источник получения ванадия — железные руды, содержащие ванадий как примесь. Месторождения Известны месторождения в Перу, Колорадо, США, ЮАР, Финляндии, Австралии, Армении, России.

Получение ванадия В промышленности при получении ванадия из железных руд с его примесью сначала готовят концентрат, в котором содержание ванадия достигает 8 -16 %. Далее окислительной обработкой ванадий переводят в высшую степень окисления +5 и отделяют легко растворимый в воде ванадат натрия (Na) Na. VO 3. При подкислении раствора серной кислотой выпадает осадок, который после высушивания содержит более 90 % ванадия. Металлический ванадий можно приготовить восстановлением хлорида ванадия водородом (H 2), термическим восстановлением оксидов ванадия (V 2 O 5 или V 2 O 3) кальцием, термической диссоциацией VI 2 и другими методами.

Химические свойства ванадия Химически ванадий довольно инертен. Он стоек к действию морской воды, разбавленных растворов соляной, азотной и серной кислот, щелочей. Ванадий растворяется в плавиковой кислоте, кислотах окислителях и царской водке. Реакция с азот кислотой: V+5 HNO 3=HVO 3+5 NO 2+2 H 2 O В присутствии окислителей ванадий взаимодействует с расплавами щелочей 4 V+4 Na. OH+5 O 2=4 Na. VO 3+2 H 2 O С кислородом ванадий образует несколько оксидов: VO, V 2 O 3, VO 2, V 2 O 5 — кислотный оксид, VO 2 — амфотерный, остальные оксиды ванадия — основные. Галогениды ванадия гидролизуются. V+O 2=VO 2 V+ Cl 2=VCl 2

Оксид VO 2 растворяется в кислотах с образованием солей ванадила VO 2: VO 2 +2 HCl=VOCl 2+H 2 O В водном растворе соли ванадия подвергаются гидролизу : VOSO 4+H 2 O=VO 2+H 2 SO 4 VO 2 взаимодействует с растворами щелочей : 4 VO 2+4 Na. OH=Na 2 V 4 O 9+H 2 O V 2 O 5 растворим в воде : V 2 O 5+H 2 O=2 HVO 3 V 2 O 5 взаимодействует со щелочами: V 2 O 5+2 KOH=2 KVO 3+H 2 O V 2 O 5 взаимодействует с кислотами: V 2 O 5+ 6 HCl(конц. )=2 VOCl 2+3 H 2 O

С галогенами ванадий образует довольно летучие галогениды составов VX 2 (X = F, Cl, Br, I), VX 3, VX 4 (X = F, Cl, Br), VF 5 и несколько оксогалогенидов (VOCl, VOCl 2, VOF 3 и др. ). Известны следующие оксиды ванадия: Соединения ванадия в степенях окисления +2 и +3 — сильные восстановители, в степени окисления +5 проявляют свойства окислителей. Известны тугоплавкий карбид ванадия VC (tпл=2800 °C), нитрид ванадия VN, сульфид ванадия V 2 S 5, силицид ванадия V 3 Si и другие соединения ванадия. Ванадий растворяется в плавиковой кислоте, кислотах окислителях и царской водке. При взаимодействии V 2 O 5 с основными оксидами образуются ванадаты — соли ванадиевой кислоты вероятного состава HVO 3.
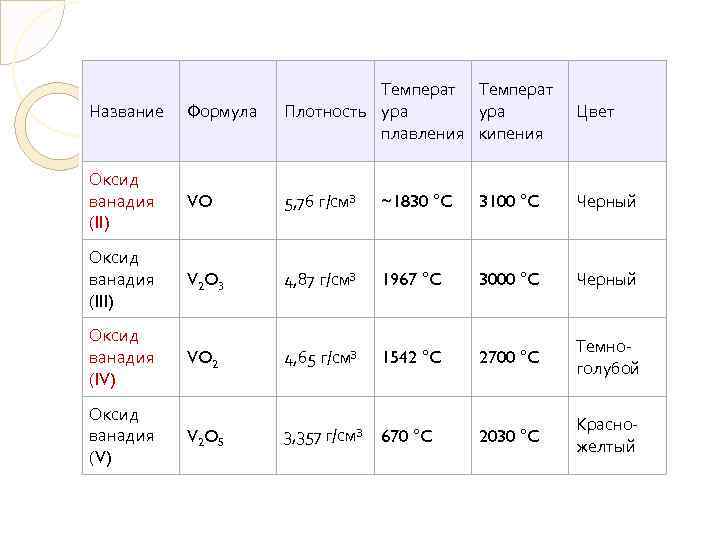
Название Формула Температ Плотность ура плавления кипения Оксид ванадия (II) VO 5, 76 г/см³ ~1830 °C 3100 °C Черный Оксид ванадия (III) V 2 O 3 4, 87 г/см³ 1967 °C 3000 °C Черный Оксид ванадия (IV) VO 2 4, 65 г/см³ 1542 °C 2700 °C Темноголубой Оксид ванадия (V) V 2 O 5 3, 357 г/см³ 670 °C 2030 °C Красножелтый Цвет

Применение ванадия 80 % всего производимого ванадия находит применение в сплавах, в основном для нержавеющих и инструментальных сталей. Атомно-водородная энергетика Хлорид ванадия применяется при термохимическом разложении воды в атомноводородной энергетике • Химические источники тока Пентаоксид ванадия широко применяется в качестве положительного электрода(анода) в мощных литиевых батареях и аккумуляторах. Ванадат серебра в резервных батареях в качестве катода. В производстве серной кислоты Оксид ванадия(V) используется как катализатор на стадии превращения сернистого ангидрида в серный.

Ниобий Блестящий металл серебристо-серого цвета. Нио бий был открыт в 1801 г. английским учёным Ч. Хатчетом в минерале (колумбите), найденном в бассейне р. Колумбии, и потому получил название «колумбий» . В 1844 году немецкий химик Генрих Розе переименовал его в «ниобий» в честь дочери Тантала Ниобы, чем подчеркнул сходство между ниобием и танталом. В 1950 году решением Международного союза теоретической и прикладной химии (ИЮПАК, IUPAC) элементу окончательно было присвоено название ниобий.

Нахождение в природе Ниобию всегда сопутствует тантал. Минералы: колумбит-танталит (Fe, Mn)(Nb, Ta)2 O 6, пирохлор (Na, Ca, TR, U)2(Nb, Ta, Ti)2 O 6(OH, F) (Nb 2 O 5 0 — 63 %), лопарит (Na, Ce)(Ti, Nb)O 3 ((Nb, Ta)2 O 5 8 — 10 %). Концентрация ниобия в морской воде 1· 10− 5 мг/л. Месторождения ниобия расположены в США, Японии, России, Бразилии, Канаде.

Получение ниобия Металлический ниобий получают из рудных концентратов по сложной технологии в три стадии: 1)вскрытие концентрата; 2) разделение ниобия и тантала и получение их чистых химических соединений; 3) восстановление и рафинирование металлического ниобия и его сплавов. Основные промышленные методы производства Nb и сплавов — алюмотермический-ниобий восстанавливают алюминием из Nb 2 O 5, натрийтермический- восстанавливают натрием из K 2 Nb. F 7 карботермический- из смеси Nb 2 O 5 и сажи вначале получают при 1800 °C в атмосфере водорода карбид, затем из смеси карбида и пятиокиси при 1800— 1900 °C в вакууме — металл; по другому варианту ниобий восстанавливают при высокой температуре в вакууме непосредственно из Nb 2 O 5 сажей.

Химические свойства Химически ниобий довольно устойчив. При прокаливании на воздухе окисляется до Nb 2 О 5. При сплавлении Nb 2 О 5 с различными оксидами получают ниобаты: Ti 2 Nb 10 О 29, Fe. Nb 49 О 124. Ниобаты могут рассматриваться как соли гипотетических ниобиевых кислот. Они делятся на метаниобаты MNb. O 3, ортониобаты M 3 Nb. O 4, пирониоб аты M 4 Nb 2 O 7 или полиниобаты M 2 O·n. Nb 2 O 5 (M — однозарядный катион, n = 2 -12). Известны ниобаты двух- и трехзарядных катионов. Ниобаты реагируют с HF, расплавами гидрофторидов щелочных металлов (KHF 2) и аммония. Некоторые ниобаты с высоким отношением M 2 O/Nb 2 O 5 гидролизуются: 6 Na 3 Nb. O 4 + 5 H 2 O = Na 8 Nb 6 O 19 + 10 Na. OH.

Nb 2 O 5 растворяется в расплавах щелочей: Nb 2 O 5 + 2 Na. OH=Na Nb. O 3 +H 2 O С галогенами ниобий образует пентагалогениды Nb. Hal 5, тетрагалогениды Nb. Hal 4 и фазы Nb. Hal 2, 67 — Nb. Hal 3+x, в которых имеются группировки Nb 3 или Nb 2. Пентагалогениды ниобия легко гидролизуются водой. В присутствии паров воды и кислорода Nb. Cl 5 и Nb. Br 5 образуют оксигалогениды Nb. OCl 3 и Nb. OBr 3 — рыхлые ватообразные вещества. При взаимодействии ниобия и графита образуются карбиды Nb 2 C и Nb. C, твердые жаропрочные соединения. В системе Nb — N существуют несколько фаз переменного состава инитриды Nb 2 N и Nb. N. Сходным образом ведет себя ниобий в системах с фосфором и мышьяком. При взаимодействии ниобия с серой получены сульфиды: Nb. S, Nb. S 2 и Nb. S 3. Синтезированы двойные фториды Nb и калия (натрия) — K 2[Nb. F 7].

Применение Из чистого ниобия или его сплавов изготовляют детали летательных аппаратов; оболочки для урановых и плутониевых тепловыделяющих элементов; контейнеры и трубы для жидких металлов; детали электролитических конденсаторов; «горячую» арматуру электронных (для радарных установок) и мощных генераторных ламп (аноды, катоды, сетки и др. ); коррозионноустойчивую аппаратуру в химической промышленности. Ниобием легируют другие цветные металлы, в том числе уран. Ниобий применяют в криотронах — сверхпроводящих элементах вычислительных машин. Ниобий также известен тем, что он используется в ускоряющих структурах большого адронного коллайдера.

Тантал Металл серого цвета (со слабым свинцовым оттенком вследствие образования плотной оксидной плёнки). Тантал открыт в 1802 г. шведским химиком А. Г. Экебергом в двух минералах, найденных в Финляндии и Швеции. В последующем тантал и колумбий считали тождественными. Лишь в 1844 г. немецкий химик Розе доказал, что минерал колумбит содержит два различных элемента — ниобий и тантал. Пластичный металлический тантал впервые получен немецким учёным В. Больтеном в 1903 г. Элемент назван по имени героя древнегреческой мифологии Тантала, из-за трудностей его получения в чистом виде.

Нахождение в природе В природе встречается в виде двух изотопов: стабильного 181 Та (99, 9877 %) и радиоактивного с периодом полураспада 1012 лет180 Та (0, 0123 %). Известно около 20 собственно минералов тантала — серия колумбит — танталит, воджинит, лопарит, манганотанталит и другие, а также более 60 минералов, содержащих тантал. В минералах тантал всегда находится совместно с ниобием вследствие сходства их физических и химических свойств. Тантал — типично рассеянный элемент, так как изоморфен со многими химическими элементами. Месторождения Самые крупные месторождения танталовых руд находятся во Франции, Египте, Таиланде, Китае, Австралии

Химические свойства тантала При нормальных условиях тантал малоактивен, на воздухе окисляется лишь при температуре свыше 280 °C, покрываясь защитной плёнкой Ta 2 O 5; с галогенами реагирует при температуре свыше 250 °C. При нагревании реагирует с С, В, Si, P, Se, Те, Н 2 О, СО 2, NO, HCl, H 2 S. Химически чистый тантал исключительно устойчив к действию жидких щелочных металлов, большинства неорганических и органических кислот, а также многих других агрессивных сред (за исключением расплавленных щелочей). В отношении химической устойчивости к реагентам, тантал подобен стеклу. Тантал нерастворим в кислотах и их смесях, его не растворяет даже царская водка. Растворим только в смеси плавиковой и азотной кислот: 3 Ta+5 HNO 3+21 HF=3 H 2[Ta. F 7]+5 NO+10 H 2 O

Получение тантала Основным сырьём для производства тантала и его сплавов служат танталитовые и лопаритовые концентраты, содержащие около 8 % Та 2 О 5, 60 % и более Nb 2 O 5. Концентраты разлагают кислотами или щелочами, лопаритовые — хлорируют. Разделение Та и Nb производят с помощью экстракции. Металлический тантал обычно получают восстановлением Ta 2 O 5 углеродом, либо электрохимически из расплавов. Компактный металл производят вакуумно-дуговой, плазменной плавкой или методом порошковой металлургии.

Применение тантала Ø Ø Ø Первоначально использовался для изготовления проволоки для ламп накаливания. Сегодня из тантала и его сплавов изготовляют: жаропрочные и коррозионностойкие сплавы; коррозионно-устойчивую аппаратуру для химической промышленности, фильеры, лабораторную посуду и тигли для получения, плавки, и литья редкоземельных элементов, а также иттрия и скандия; теплообменники для ядерно-энергетических систем (тантал наиболее из всех металлов устойчив в перегретых расплавах и парах цезия); в хирургии листы, фольгу и проволоку из тантала используют для скрепления тканей, нервов, наложения швов, изготовления протезов, заменяющих повреждённые части костей (ввиду биологической совместимости); карбид тантала (температура плавления 3880 °C) применяется в производстве твёрдых сплавов (смеси карбидов вольфрама и тантала — марки с индексом ТТ, для тяжелейших условий металлообработки и ударно-поворотного бурения крепчайших

тантал и ниобий используют для производства электролитических конденсаторов высокой удельной емкости (но тантал позволяет производить более качественные конденсаторы); Ø тантал используется в последние годы в качестве ювелирного металла, в связи с его способностью образовывать на поверхности прочные пленки оксида любого цвета; Ø Бериллид тантала чрезвычайно тверд и устойчив к окислению на воздухе до 1650 °C, применяется в авиакосмической технике. Ø Пятиокись тантала используется в атомной технике для варки стекла поглощающего гамма-излучение. Один из наиболее широко применяемых составов такого стекла: кремния двуокись — 2 %, монооксид свинца (глет) — 82 %, оксид бора — 14 %, пятиокись тантала — 2 %. Ø

Дубний (Db) (до 1997 г. в СССР и России известен как Нильсборий (Ns)) — 105 й элемент таблицы Менделеева. Элемент 105 впервые получен на ускорителе в наукограде Дубне в 1970 г. группой Г. Н. Флёрова путём бомбардировки ядер 243 Amионами 22 Ne и независимо в Беркли (США) в реакции 249 Cf+15 N→ 260 Db+4 n. Рабочая группа ИЮПАК в 1993 году сделала вывод, что честь открытия элемента 105 должна быть разделена между группами из Дубны и Беркли. Предположительно серебристо-белый
![Известные изотопы Изотоп Масса Период полураспада[7] Тип распада 255 Db 255 1, 6+0, 6− Известные изотопы Изотоп Масса Период полураспада[7] Тип распада 255 Db 255 1, 6+0, 6−](https://present5.com/presentation/1/45088442_108809555.pdf-img/45088442_108809555.pdf-26.jpg)
Известные изотопы Изотоп Масса Период полураспада[7] Тип распада 255 Db 255 1, 6+0, 6− 0, 4 с α-распад в 251 Lr (80 %); спонтанное деление 256 Db 256 1, 6+0, 5− 0, 3 с α-распад в 252 Lr (64 %); β-распад в 256 Rf (36 %); спонтанное деление (0, 02 %) 257 Db 257 1, 50+0, 19− 0, 15 с α-распад в 253 Lr 258 Db 258 4, 0± 1, 0 с α-распад в 254 Lr (67 %); β-распад в 258 Rf 259 Db 259 0, 51± 0, 16 с α-распад в 255 Lr 260 Db 260 1, 52± 0, 13 с α-распад в 256 Lr 261 Db 261 1, 8± 0, 4 с α-распад в 257 Lr 262 Db 262 35± 5 с α-распад в 258 Lr (67 %); спонтанное деление 263 Db 263 27+10− 7 с спонтанное деление (55 %); α-распад в 259 Lr (41 %); β-распад в 263 Rf (3 %) 267 Db 267 73+350− 33 мин спонтанное деление 268 Db 268 32+11− 7 часа спонтанное деление

Спасибо за внимание.
v побочная подгруппа.pptx