Кузик Катерина БП-32..pptx
- Количество слайдов: 14

Ферум(Залізо) Fe ВИКОНАЛА: СТУДЕНТКА ГРУПИ БП-32 ХІМІКО-БІОЛОГІЧНОГО ФАКУЛЬТЕТУ КУЗИК КАТЕРИНА

Історія виникнення заліза Використання заліза почалося набагато раніше, ніж його виробництво. Перші залізні вироби мали космічне (метеоритне) походження і були виготовлені з уламків метеоритів ще в III–II тис. до н. е. Час від часу знаходили шматки сірувато-чорного металу, який перековували на кинджал або наконечник списа, що був зброєю міцнішою і пластичнішою, ніж бронза, і довше тримав гостре лезо. Першим кроком у зародженні металургії заліза було отримання його шляхом відновлення з окису. Руда перемішувалася з деревним вугіллям і закладалася в піч. При високій температурі, створюваної горінням вугілля, вуглець починав з'єднуватися не лише з атмосферним киснем, але і з тим, що пов'язаний з атомами заліза. Після вигоряння вугілля в печі залишалася так звана криця — грудка речовини з домішкою відновленого заліза. Крицю потім знову розігрівали і піддавали обробці куванням, вибиваючи залізо із шлаку. Вперше залізо навчилися обробляти народи Анатолії. Давньогрецька традиція вважала відкривачем заліза народ халібів, для яких традиційно вживалася стійка назва «батько заліза» , і сама назва народу бере початок саме від грецького слова Χάλυβας ( «залізо» ). «Залізна революція» почалася на межі I тисячоліття до н. е. в Ассирії. З VIII століття до н. е. зварне залізо швидко стало поширюватися в Європі. Першими, хто почав на землях сучасної України виплавляти з болотної руди залізо, були кіммерійці (VII ст. до н. е. )[8]. У IV–III ст. до н. е. більша частина арсеналу зброї скіфських воїнів — мечі, кинджали, бойові сокири тощо було виготовлено з заліза. У III столітті до н. е. залізо витіснило бронзу в Галлії, у II столітті нової ери з'явилося у Німеччині, а в VI столітті нашої ери вже широко вживалося в Скандинавії. В Японії залізний вік настав лише в VIII столітті нашої ери. Технологічніший шлях одержання пружної сталі, при якому не потрібні ні особливо чиста руда, ні графіт, ні спеціальні печі, було винайдено в Китаї в II столітті нашої ери. Сталь перековували дуже багато разів, під час кожного кування складаючи пластину вдвічі, внаслідок чого виходив відмінний матеріал для зброї, що отримав назву дамаська сталь, з якого, зокрема, робилися японськікатани.

Загальна характеристика Феруму Ферум – металічний елемент побічної підгрупи VІІІ групи 4 періоду періодичної системи хімічних елементів. Він є представником d-елементів. На зовнішньому енергетичному рівні атома Феруму знаходиться два sелектрони, а на передзовнішньому енергетичному рівні відбувається заповнення d-підрівня. У своїх сполуках Ферум здатен проявляти ступені окиснення +2 та +3. Масова частка Феруму в земній корі становить 5 %. Він займає четверте місце по розповсюдженості в природі. Найважливішими залізними рудами є: магнетит Fе 3 О 4, гематит Fe 2 О 3, лімоніт — Fe 2 O 3 · n. H 2 O, сидерит Fе. СО 3, пірит Fе. S 2.

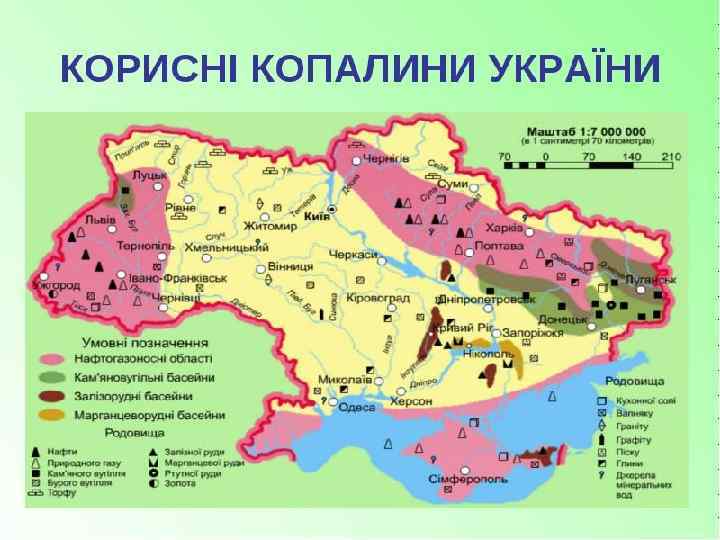
Поширення в природі Залізо — один з найбільш поширених у природі елементів: за вмістом у земній корі — 4, 7 % (масових). Зустрічається у вигляді оксидів і сульфідів, сконцентрованих у вигляді родовищ, придатних для промислової розробки. Найважливіші руди: • бурі залізняки (НFе. O 2 x Н 20), пірит Fе. S 2; • червоні залізняки (Fе 2 O 3); • магнітні залізняки (Fе 3 O 4); • шпатові залізняки (Fе. СO 3):

Фізичні властивості За звичайних умов чисте залізо – це сріблясто білий блискучий метал, воно досить мяке і пластичнее, легко кується. Густина його становить 7, 87 г/см 3, температура плавлення 1535 ºС. Має магнітні властивості. Використовують в основному не чисте залізо, а його сплави – чавун і сталь.

Хімічні властивості Залізо належить до середньої хімічної активності. Взаємодія з киснем: 3 Fe + 2 O 2 = Fe 3 O 4 4 Fe + 3 O 2 = Fe 2 O 3 (у вологому повітрі) Взаємодія з сіркою: Fe + S = Fe. S Інші характерні реакції 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 3 Fe + C = Fe 3 C Fe + H 2 O = Fe. O + H 2 ↑ Fe + H 2 SO 4 = Fe. SO 4 + H 2 ↑ Fe + Cu. SO 4 = Fe. SO 4 + Cu

Залізо в природі Природне залізо складається з чотирьох стабільних ізотопів: 54 Fe (ізотопна поширеність 5, 845%), 56 Fe (91, 754%), 57 Fe (2, 119%) і 58 Fe (0, 282%). Також відомо більше 20 нестабільних ізотопів заліза з масовими числами від 45 до 72, найстійкіші з яких — 60 Fe (період напіврозпаду за уточненими в 2009 році даними становить 2, 6 мільйона років[5]), 55 Fe (2, 737 року), 59 Fe (44, 495 доби) і 52 Fe (8, 275 години); інші ізотопи мають період напіврозпаду менше 10 хвилин. Ізотоп заліза 56 Fe належить до найстабільніших ядер із найменшою енергією зв'язку у розрахунку на один нуклон. Усі попередні елементи можуть зменшити енергію зв'язку за рахунок синтезу, а всі наступні — шляхом розпаду. Вважають, що залізом закінчується процес синтезу елементів в ядрах нормальних зірок. Раніше вважалося, що всі наступні елементи можуть утворитися тільки в результаті вибухів наднових. Проте за сучасними уявленнями, синтез елементів, важчих заліза, відбувається не лише у наднових, а й у надрах зір-гігантів на пізніх стадіях їх еволюції завдяки s-процесу.

Ферум є життєво важливим елементом. В організмі людини, як і тварин, ферум присутній в усіх тканинах, проте найбільша його частина (приблизно три грами) зосереджена в кров’яних кульках. Атоми Феруму займають центральне положення в молекулах гемоглобіну, їм гемоглобін зобов’язаний своїм забарвленням і здатністю приєднувати та відщеплювати кисень. Залізо Ферум бере участь у процесі перенесення кисню від легенів до тканин організму. Добова потреба організму у Ферумі становить 15 -20 мг. Загальна його кількість потрапляє в організм людини з рослинною їжею та м’ясом. При втраті крові потреба у Ферумі перевищує кількість, яку людина отримує з їжею. Нестача Феруму в організмі може привести до стану, який характеризується зменшенням кількості еритроцитів та гемоглобіну крові. Медичні препарати Феруму слід вживати тільки за призначенням лікаря.

Обмін заліза в організмі
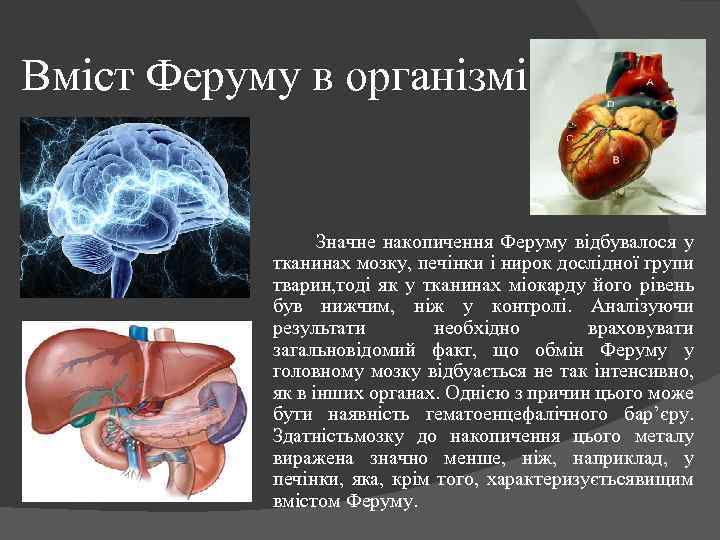
Вміст Феруму в організмі Значне накопичення Феруму відбувалося у тканинах мозку, печінки і нирок дослідної групи тварин, тоді як у тканинах міокарду його рівень був нижчим, ніж у контролі. Аналізуючи результати необхідно враховувати загальновідомий факт, що обмін Феруму у головному мозку відбуається не так інтенсивно, як в інших органах. Однією з причин цього може бути наявність гематоенцефалічного бар’єру. Здатністьмозку до накопичення цього металу виражена значно менше, ніж, наприклад, у печінки, яка, крім того, характеризуєтьсявищим вмістом Феруму.

Ізотопи заліза Ізотоп заліза 56 Fe належить до найстабільніших ядер із найменшою енергією зв'язку у розрахунку на один нуклон. Усі попередні елементи можуть зменшити енергію зв'язку за рахунок синтезу, а всі наступні — шляхом розпаду. Вважають, що залізом закінчується процес синтезу елементів в ядрах нормальних зірок. Раніше вважалося, що всі наступні елементи можуть утворитися тільки в результаті вибухів наднових. Проте за сучасними уявленнями, синтез елементів, важчих заліза, відбувається не лише у наднових, а й у надрах зір-гігантів на пізніх стадіях їх еволюції завдяки s-процесу.
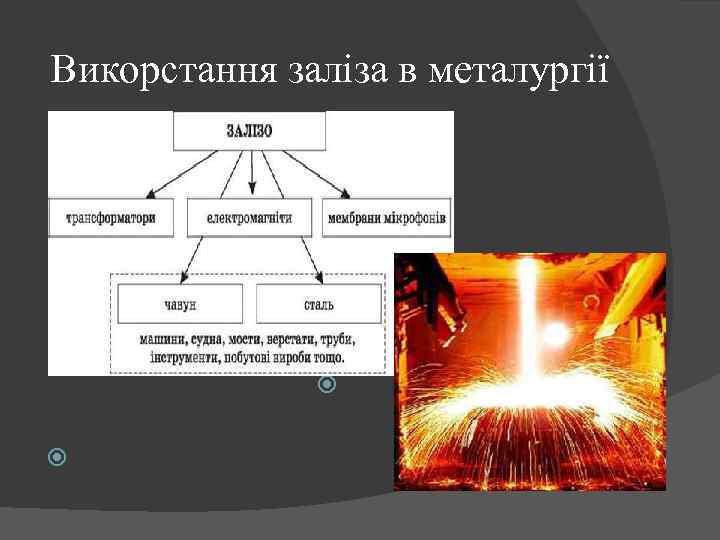
Викорстання заліза в металургії

Кінець.
Кузик Катерина БП-32..pptx