1156168.ppt
- Количество слайдов: 20

Ферум. Залізо: будова атома, фізичні і хімічні властивості. Генетичні ряди Феруму (II) і Феруму (III).
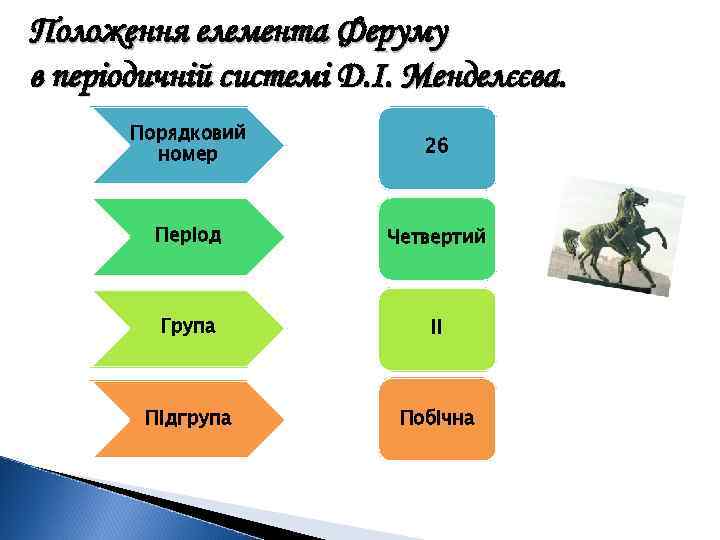
Положення елемента Феруму в періодичній системі Д. І. Менделєєва. Порядковий номер 26 Період Четвертий Група II Підгрупа Побічна

Будова атома Феруму Дописати 2 1 s 2 2 s електронну формулу 6 2 р 2 3 s 6…. 3 р

2 2 s 2 2 р6 3 s 2 1 s 6 3 d 6 4 s 2 3 р Які електрони для елементів головних підгруп являються валентними? А які електрони для елементів побічних підгруп являються валентними? Запам’ятай! Особливістю електронної будови елементів побічних підгруп являється заповнення електронами не останнього, а передостаннього рівня.

Запам’ятай! Валентні електрони атомів елементів побічних підгруп розприділяються на останньому і передостанньому рівнях.

Для Феруму характерні два основні ступені окиснення: +2, +3. 0 – 2 e = Fe+2 Fe Fe 0 – 3 e = Fe+3
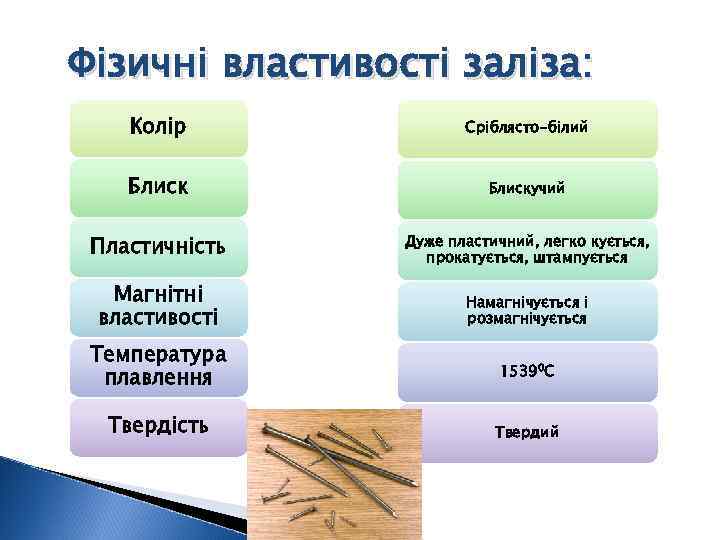
Фізичні властивості заліза: Колір Сріблясто-білий Блискучий Пластичність Дуже пластичний, легко кується, прокатується, штампується Магнітні властивості Намагнічується і розмагнічується Температура плавлення 15390 С Твердість Твердий
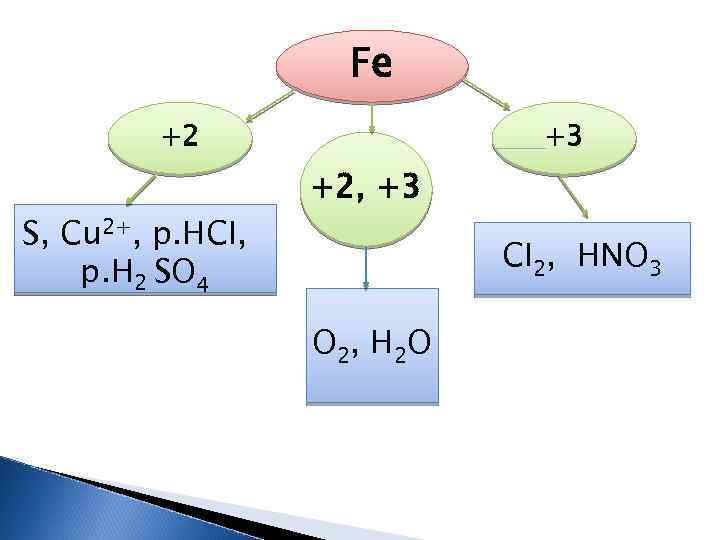
Fe +2 S, Cu 2+, p. HCI, p. H 2 SO 4 +3 +2, +3 CI 2, HNO 3 O 2, H 2 O

Закінчити рівняння хімічних реакцій: Ø Fe Ø Fe + + + + CI 2 = S= HCI = O 2 = Cu. SO 4 = H 2 O = O 2 + H 2 O =

Хімічні властивості заліза Взаємодія з простими речовинами -неметалами 1) З киснем. 0 0 +2, +3 -2 3 Fe + 2 O 2 —>Fe 3 O 4 2) З сіркою і хлором. +2 -2 +3 -2 (Fe. O • Fe 2 O 3) Запишіть рівняння реакції і складіть електронний баланс.

0 0 +2 -2 Fe + S —>Fe. S електронний баланс Fe 0 – 2 e- —> Fe 2+ S 0 + 2 e- —> S 2 - +3 -1 2 Fe 0 + 3 Cl 20 —> 2 Fe. Cl 3 електронний баланс Fe 0 – 3 e- —> Fe 3+ Cl 20 +2 e- —> 2 Cl 1 -

Хімічні властивості заліза Взаємодія з складними речовинами 1) З водою. 3 Fe 0 +2, +3 + 4 H 2 O —> Fe 3 O 4 + 4 H 20 при t =7000 - 9000 2) З кислотами. Дослід: здійснити реакцію між порошком заліза і хлоридною кислотою. В якому випадку можливі реакції між металом і кислотою? Скласти рівняння реакції. Зробити висновок.

Fe + 2 HCl —>Fe. Cl 2 + H 2 Метали Взаємодіють з кислотами коли: 1. Метал знаходиться в ряду активності металів до водню. 2. Повинні одержати розчинну сіль. 3. Реакція характерна для розчинів кислот. 4. Метал + кислота → сіль + водень

Хімічні властивості заліза 3) З солями. Дослід: здійснити реакцію між порошком заліза і розчином купрум (II) хлориду В якому випадку можливі реакції між металом і розчином солі? Скласти рівняння реакції. Зробити висновок.

Fe + Cu. Cl 2 —> Fe. Cl 2 + Cu Метали Взаємодіють з розчинами солей коли: 1. Кожний метал витісняє із розчинів солей всі інші метали, які розміщенні правіше нього в ряду напруг. 2. Обидві солі (і реагуюча і утворена в результаті реакції) повинні бути розчинні.

Сполуки Феруму : Fe 3 O 4 – магнітний залізняк Fe 2 O 3 – червоний залізняк (гематит) 2 Fe 2 O 3 * 3 H 2 O – бурий залізняк Fe. S 2 –залізний колчедан

Ступінь окиснення металу в оксиді повинна відповідати ступеню окиснення металу у відповідному гідроксиді +2 +2 Fe. O —>Fe(OH)2 Даний оксид проявляє основний характер. Які реакції підтверджують основний характер оксидів? +3 +3 Fe 2 O 3 —> Fe(OH)3 Які сполуки називають амфотерними?

Які реакції відповідають схемі Fe+2 =>Fe+3 ? 1) 2 Fe. CI 2 + CI 2 = 2 Fe. CI 3 2) Fe. CI 3 + 3 Na. OH = Fe(OH)3 + 3 Na. CI 3) 4 Fe(OH)2 + O 2 + 2 H 2 O = 4 Fe(OH)3
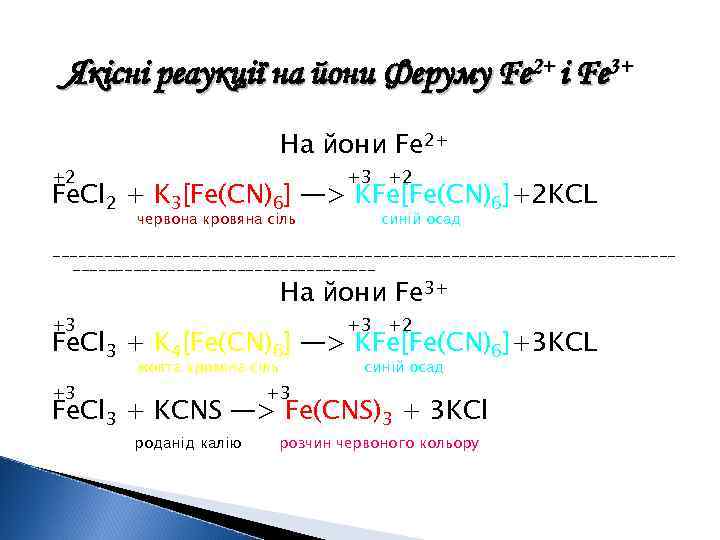
Якісні реаукції на йони Феруму Fe 2+ і Fe 3+ На йони Fe 2+ +2 +3 +2 Fe. Cl 2 + K 3[Fe(CN)6] —> KFe[Fe(CN)6]+2 KCL червона кровяна сіль синій осад ----------------------------------------------------- На йони Fe 3+ +3 +3 +2 Fe. Cl 3 + K 4[Fe(CN)6] —> KFe[Fe(CN)6]+3 KCL жовта кровяна сіль +3 синій осад +3 Fe. Cl 3 + KCNS —> Fe(CNS)3 + 3 KCl роданід калію розчин червоного кольору

Лабораторний дослід Здійснити практично ланцюг хімічних перетворень. Скласти рівняння хімічних реакцій. Вариант 1: Fe —> Fe. Cl 2 —> Fe(OH)2 —> Fe. O Вариант 2: Fe —> Fe. Cl 3 —> Fe(OH)3 —> Fe 2 O 3
1156168.ppt