лекция 5.ppt
- Количество слайдов: 31
ФЕРМЕНТЫ Строение, свойства, применение
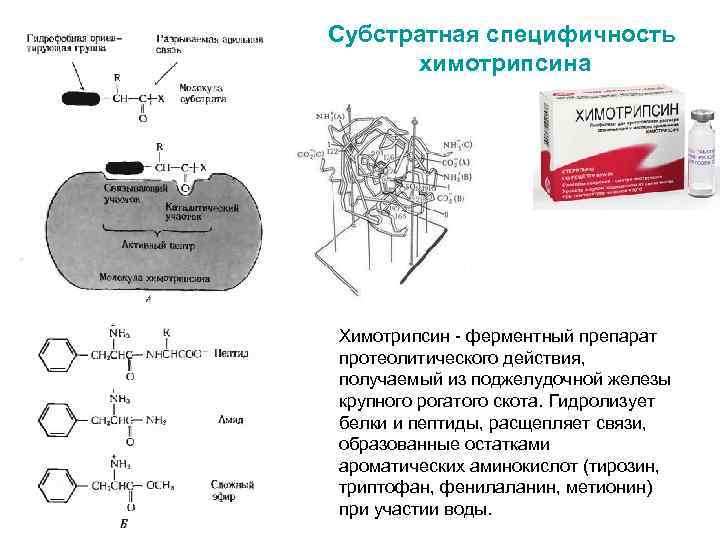
Субстратная специфичность химотрипсина Химотрипсин - ферментный препарат протеолитического действия, получаемый из поджелудочной железы крупного рогатого скота. Гидролизует белки и пептиды, расщепляет связи, образованные остатками ароматических аминокислот (тирозин, триптофан, фенилаланин, метионин) при участии воды.
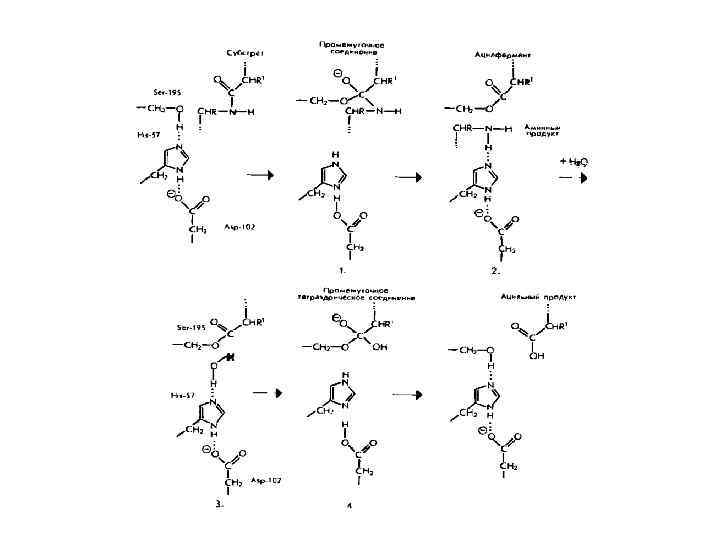
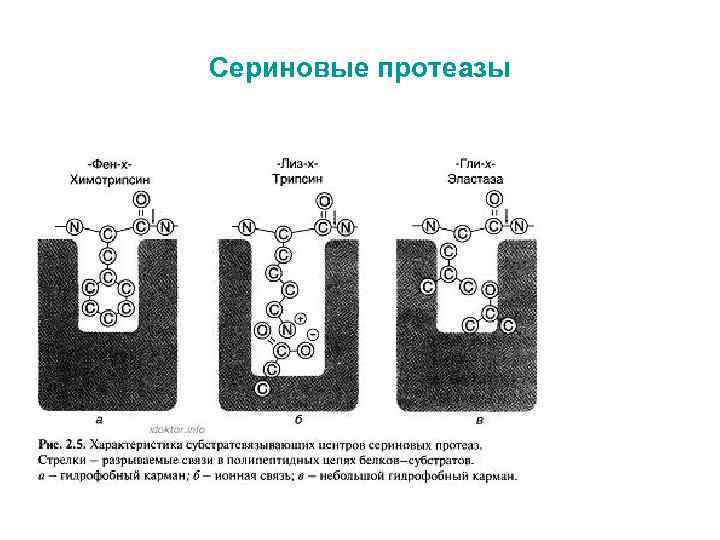
Сериновые протеазы
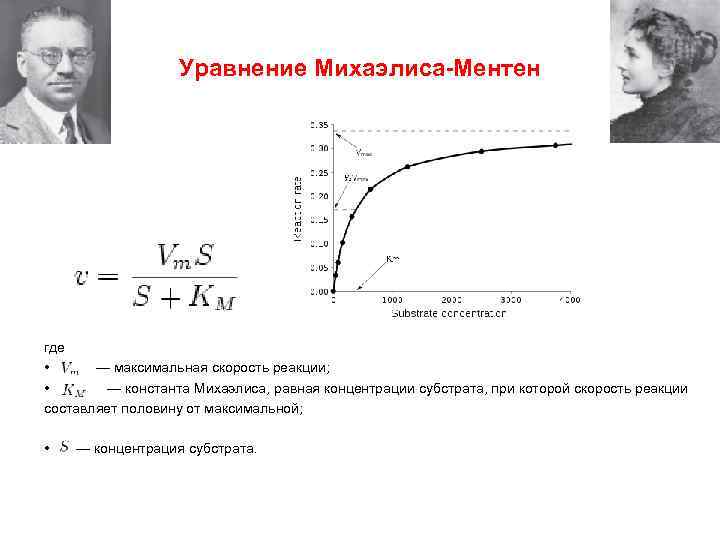
Уравнение Михаэлиса-Ментен где • — максимальная скорость реакции; • — константа Михаэлиса, равная концентрации субстрата, при которой скорость реакции составляет половину от максимальной; • — концентрация субстрата.
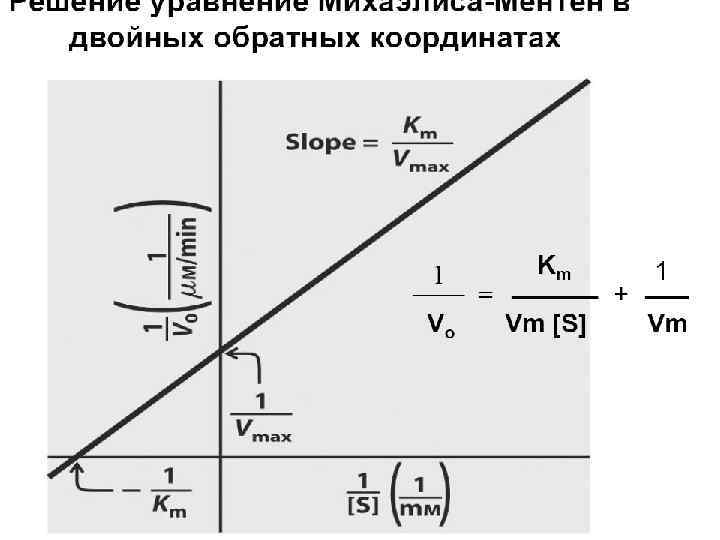

Вывод уравнения Михаэлиса-Ментен • • k 1 — константа скорости реакции образования фермент-субстратного комплекса из фермента и субстрата k-1 — константа скорости реакции диссоциации фермент-субстратного комплекса на фермент и субстрат k 2 — константа скорости реакции превращения фермент-субстратного комплекса в фермент и продукт Для фермент-субстратного комплекса применим метод квазистационарности Фермент в процессе реакции находится в виде фермент-субстратного комплекса и в виде молекул свободного фермента [E]0 = [E] + [ES] Подставим в первое уравнение [E] = [E]0 − [ES] концентрация фермент-субстратного комплекса: Скорость ферментативной реакции в целом (то есть скорость образования продукта) v = k 2[ES] Разделим числитель и знаменатель на k 1.


• За единицу активности фермента принимают такое его количество, которое катализирует превращение одного микромоля субстрата в 1 минуту в оптимальных условиях действия фермента. Удельной активностью называют число единиц ферментативной активности в расчете на мг белка.
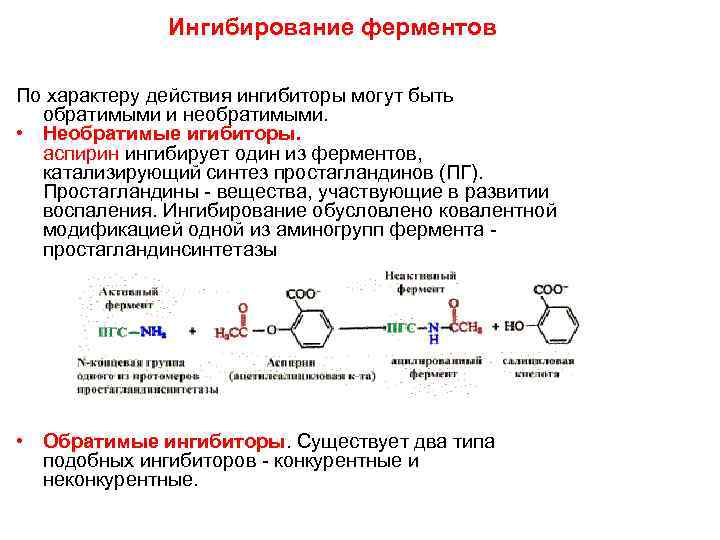
Ингибирование ферментов По характеру действия ингибиторы могут быть обратимыми и необратимыми. • Необратимые игибиторы. аспирин ингибирует один из ферментов, катализирующий синтез простагландинов (ПГ). Простагландины - вещества, участвующие в развитии воспаления. Ингибирование обусловлено ковалентной модификацией одной из аминогрупп фермента - простагландинсинтетазы • Обратимые ингибиторы. Существует два типа подобных ингибиторов - конкурентные и неконкурентные.

Конкурентное ингибирование • Конкурентный ингибитор конкурирует с субстратом за связывание с активным центром. Это происходит потому, что ингибитор и субстрат имеют сходные структуры. Конкурентное ингибирование: S-субстрат, I- ингибитор (своей трехмерной структурой похож на субстрат). Ингибитор связывается с ферментом, но реакция не протекает.

Конкурентное ингибирование примеры Сульфаниламиды – это структурные аналоги парааминобензойной кислоты, из которой в клетке микроорганизма синтезируется кофермент (Н 4 - фолат), участвующий в биосинтезе нуклеиновых оснований. Нарушение синтеза нуклеиновых кислот приводит к гибели микроорганизмов.

Аллостерические ферменты Помимо активного центра в состав ряда ферментов входит также аллостерический центр. С аллостерическим центром связывают молекулы отличные по структуре от субстрата. Их называют эффекторами или модификаторами. Связывание эффекторов или модификаторов с аллостерическим центром приводит к изменению его конформации, изменению структуры каталитического центра, а как следствие уменьшению или увеличению активности фермента.

Неконкурентное ингибирование Неконкурентный ингибитор связывается с ферментом и фермент-субстратным комплексом не в активном центре. При этом конформация молекулы фермента изменяется т. о. , что происходит обратимая инактивация его каталитического центра.
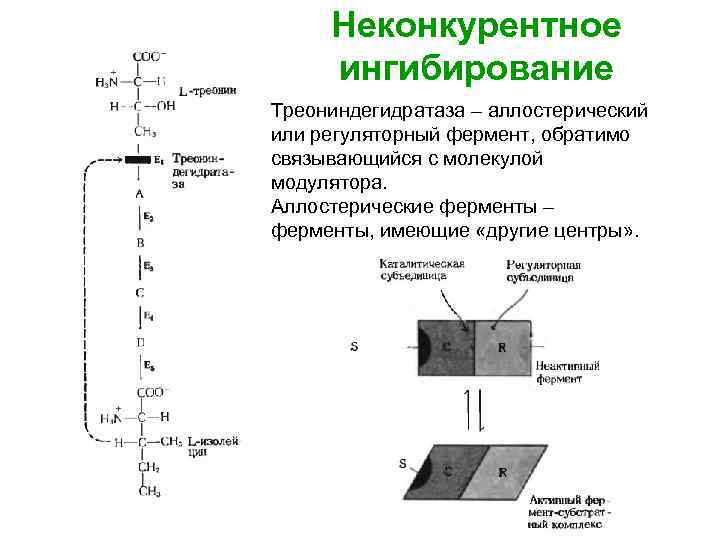
Неконкурентное ингибирование Треониндегидратаза – аллостерический или регуляторный фермент, обратимо связывающийся с молекулой модулятора. Аллостерические ферменты – ферменты, имеющие «другие центры» .
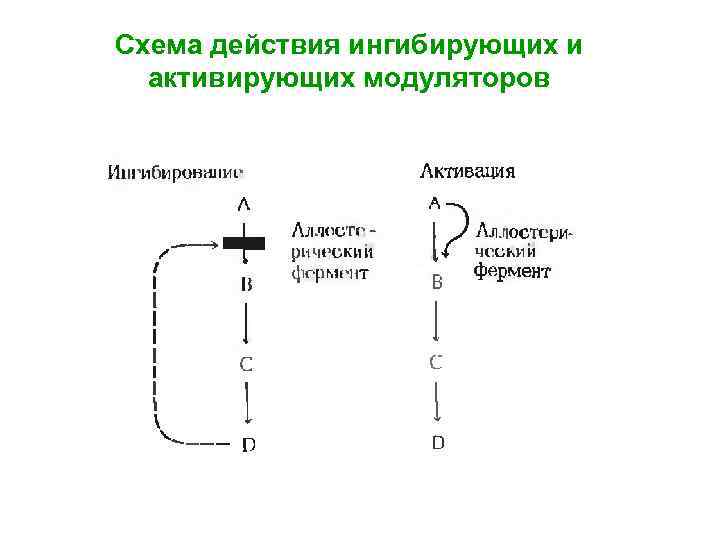
Схема действия ингибирующих и активирующих модуляторов

инженерная энзимология • Включает методы получения, очистки, стабилизации и применения ферментов.

В производстве стиральных порошков используются следующие ферменты: * протеаза щелочная; * липаза щелочная; * амилаза; * целлюлаза; * пектиназа щелочная; * кератиназы.

Ферментативный анализ Обычный метод определения глюкозы в крови основан на двух последовательных реакциях: 1) образование глюконолактона и пероксида водорода H 2 O 2 под действием фермента глюкозооксидазы ; 2) окисление бесцветного вещества пероксидом водорода в окрашенное зеленое соединение в реакции, катализируемой пероксидазой. Когда вся имеющаяся в пробе глюкоза израсходована, количество образованного окрашенного вещества можно определить по светопоглощению, которое прямо пропорционально первоначальному содержанию глюкозы.

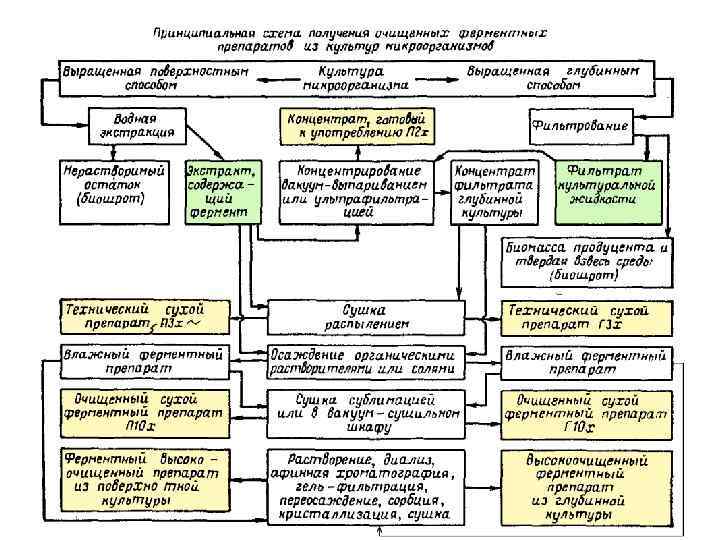
Получение ферментных препаратов Название ферментных препаратов складывается из сокращенного названия основного фермента и видового названия микроорганизма-продуцента. Например, препарат, содержащий в своей основе амилолитические ферменты и полученный при помощи культуры Aspergillus oryzae, называется амилоризин. В названии препарата указывается также способ культивирования и степень концентрирования и очистки: Aspergillus oryzae Амилосубтилин Г 3 х Амилосубтилин Г 10 х Bacillus sp. I – название основного фермента; II – название микроорганизма-продуцента; III – окончание; IV – способ культивирования: "П" – поверхностный, "Г" – глубинный; V – степень очистки (концентрирования)

ФП имеют разную степень концентрирования и очистки: х, 3 х-Ф, 10 х, 20 х, 25 х (дорогие). Гх: неочищенная культурная жидкость. Г 3 х: имеют ферментативную активность в 3 раза выше, чем Гх. Получены путем распылительной сушки концентрированной культуральной жидкости. Концентрируют вакуум-выпариванием при 30˚С с добавлением стабилизаторов (Na. Cl). Это тоже "грязные" ФП (1010 спор/г). Г 3 х-Ф: культуральную жидкость фильтруют, концентрируют, сушат. Это частично очищенные ФП, так как удалена биомасса, активность выше, чем у Г 3 х. Г 10 х: обрабатывают коагулянтами культуральную жидкость, фильтруют, концентрируют, осаждают ферменты органическими растворителями, ферментный осадок отделяют от жидкой фазы и высушивают. Г 20 х: для получения используют ультрафильтрацию, остальное - как в Г 10 х. Пх: получают высушиванием культуры грибов, "грязные", аналогичны Г 3 х. П 10 х, П 25 х: водная экстракция ферментов, отделение экстракта; осаждение органических соединений; отделение осадка в Н 2 О, добавление стабилизатора и наполнителя, сушка.

Поверхностный способ производства ферментов

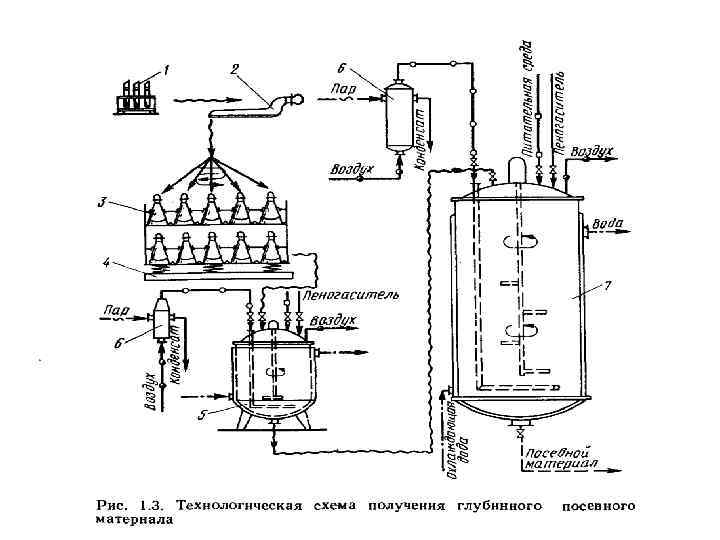
Глубинный способ производства ферментов
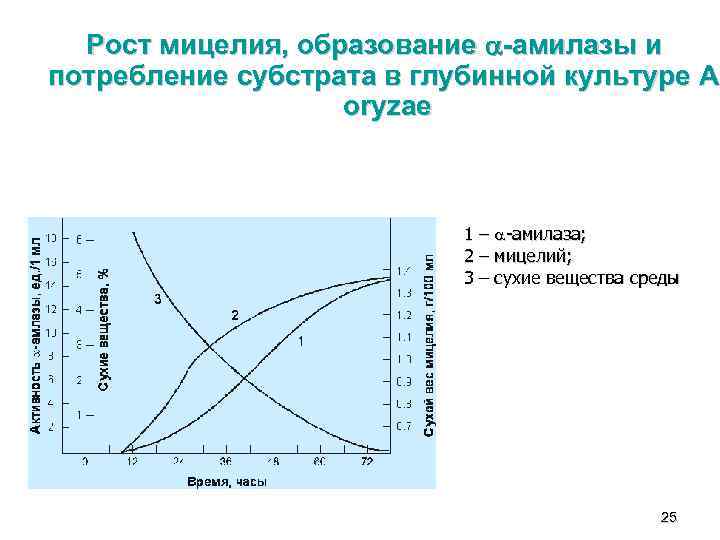
Рост мицелия, образование -амилазы и потребление субстрата в глубинной культуре A. oryzae 1 – -амилаза; 2 – мицелий; 3 – сухие вещества среды 25
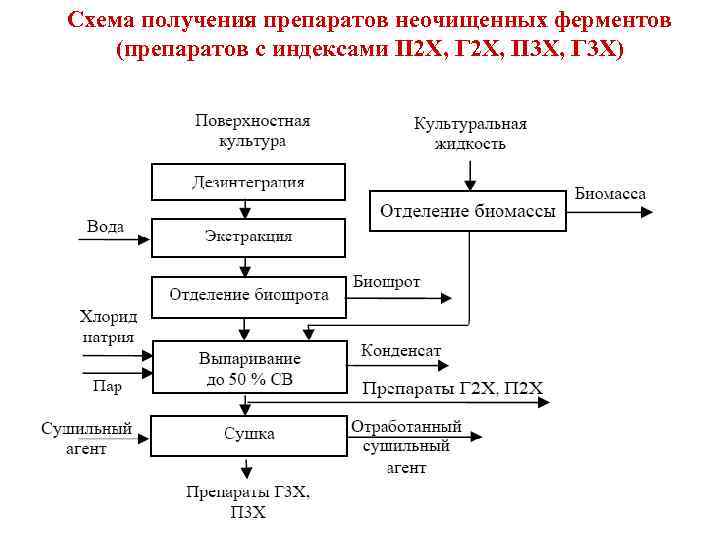
Схема получения препаратов неочищенных ферментов (препаратов с индексами П 2 Х, Г 2 Х, П 3 Х, Г 3 Х)
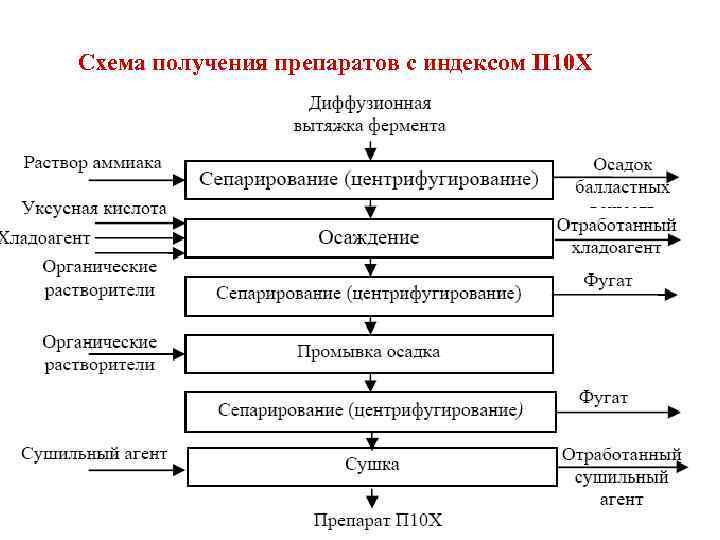
Схема получения препаратов с индексом П 10 Х
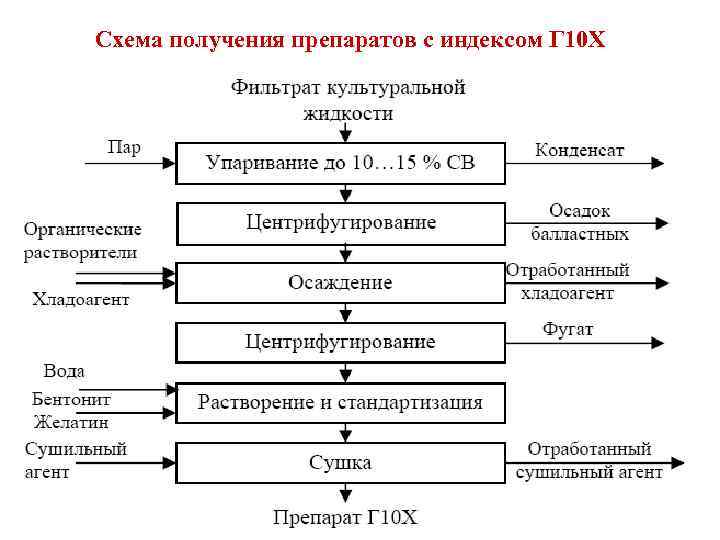
Схема получения препаратов с индексом Г 10 Х
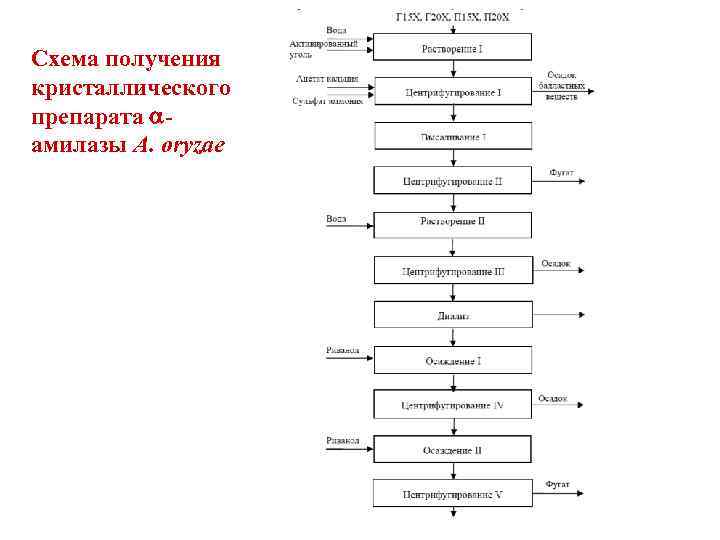
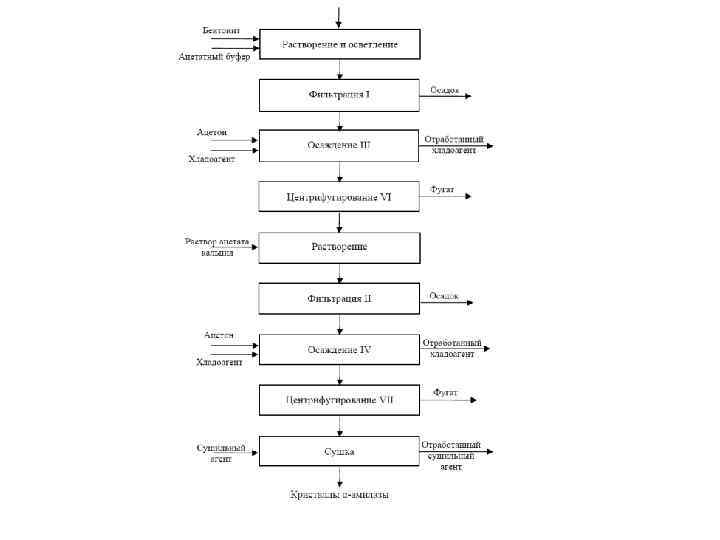
Схема получения кристаллического препарата амилазы A. oryzae
лекция 5.ppt