Окисление, кат-мое разл оксидазами.ppt
- Количество слайдов: 26
 Ферменты как мишени действия ФАВ Реакции окисления, катализируемые различными оксидазами и монооксигеназами Составитель – асс. КХПВМС ЮФУ, А. В. Ткачук 1
Ферменты как мишени действия ФАВ Реакции окисления, катализируемые различными оксидазами и монооксигеназами Составитель – асс. КХПВМС ЮФУ, А. В. Ткачук 1
 Окисление, катализируемое различными оксидазами и монооксигеназами 1. Катализ гемоглобином 2. Катализ дофамин β монооксигеназой 3. Катализ моноаминооксидазой (МАО) 4. Катализ молибденгидролазами 5. Медьсодержащие аминооксидазы и другие оксидоредуктазы 2
Окисление, катализируемое различными оксидазами и монооксигеназами 1. Катализ гемоглобином 2. Катализ дофамин β монооксигеназой 3. Катализ моноаминооксидазой (МАО) 4. Катализ молибденгидролазами 5. Медьсодержащие аминооксидазы и другие оксидоредуктазы 2
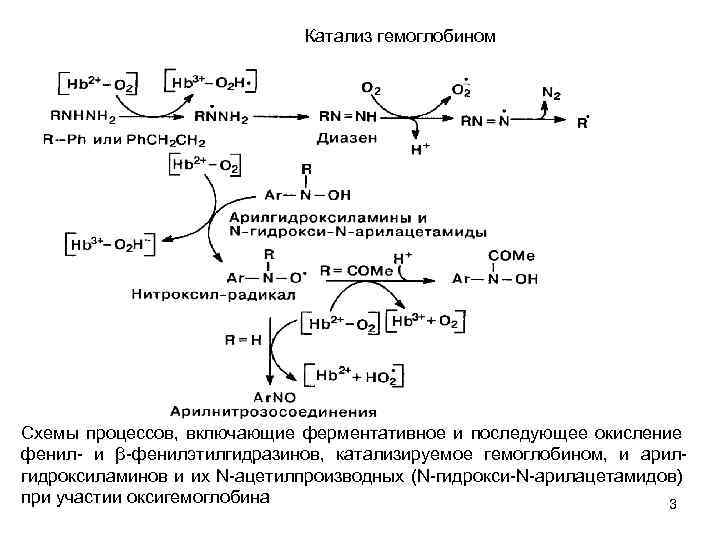 Катализ гемоглобином Схемы процессов, включающие ферментативное и последующее окисление фенил и β фенилэтилгидразинов, катализируемое гемоглобином, и арил гидроксиламинов и их N ацетилпроизводных (N гидрокси N арилацетамидов) при участии оксигемоглобина 3
Катализ гемоглобином Схемы процессов, включающие ферментативное и последующее окисление фенил и β фенилэтилгидразинов, катализируемое гемоглобином, и арил гидроксиламинов и их N ацетилпроизводных (N гидрокси N арилацетамидов) при участии оксигемоглобина 3
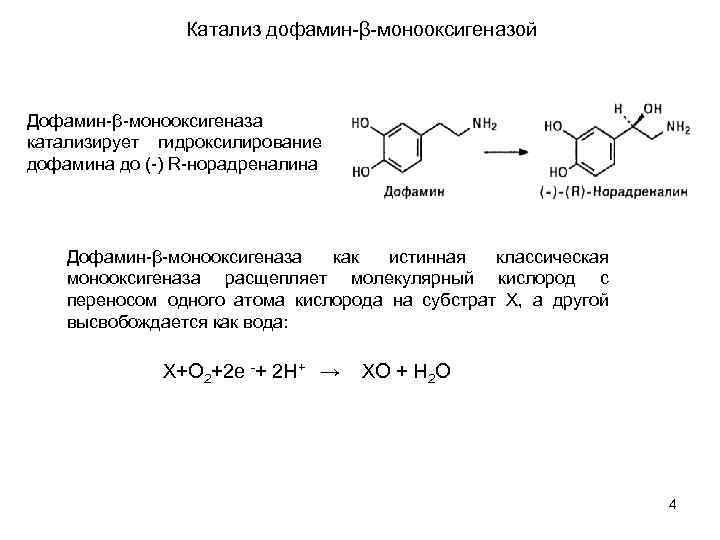 Катализ дофамин β монооксигеназой Дофамин β монооксигеназа катализирует гидроксилирование дофамина до ( ) R норадреналина Дофамин β монооксигеназа как истинная классическая монооксигеназа расщепляет молекулярный кислород с переносом одного атома кислорода на субстрат Х, а другой высвобождается как вода: Х+О 2+2 е + 2 Н+ → ХО + Н 2 О 4
Катализ дофамин β монооксигеназой Дофамин β монооксигеназа катализирует гидроксилирование дофамина до ( ) R норадреналина Дофамин β монооксигеназа как истинная классическая монооксигеназа расщепляет молекулярный кислород с переносом одного атома кислорода на субстрат Х, а другой высвобождается как вода: Х+О 2+2 е + 2 Н+ → ХО + Н 2 О 4
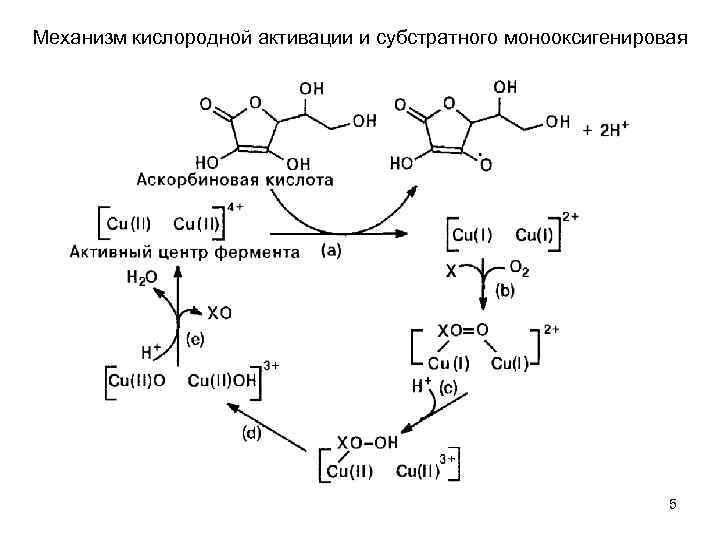 Механизм кислородной активации и субстратного монооксигенировая 5
Механизм кислородной активации и субстратного монооксигенировая 5
 Стадии процесса окисления а) восстановление ионов Сu(II) в основном состоянии фермента двумя молекулами аскорбата; b) связывание субстрата X и молекулярного кислорода, ведущее к триадному комплексу; с) активация молекулярного кислорода; d) расщепление активированного комплекса; е) субстратное оксигенирование и высвобождение продукта реакций Мишенями дофамин β монооксигеназы являются Sр3 и Sр2 гибридизованные атомы углерода и азота, атомы серы и селена. Имеются данные об участии ее в окислении фенолов. 6
Стадии процесса окисления а) восстановление ионов Сu(II) в основном состоянии фермента двумя молекулами аскорбата; b) связывание субстрата X и молекулярного кислорода, ведущее к триадному комплексу; с) активация молекулярного кислорода; d) расщепление активированного комплекса; е) субстратное оксигенирование и высвобождение продукта реакций Мишенями дофамин β монооксигеназы являются Sр3 и Sр2 гибридизованные атомы углерода и азота, атомы серы и селена. Имеются данные об участии ее в окислении фенолов. 6
 7
7
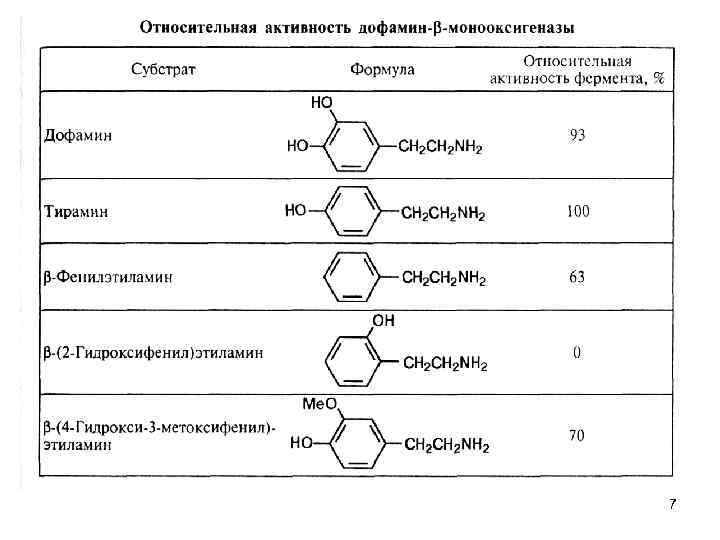
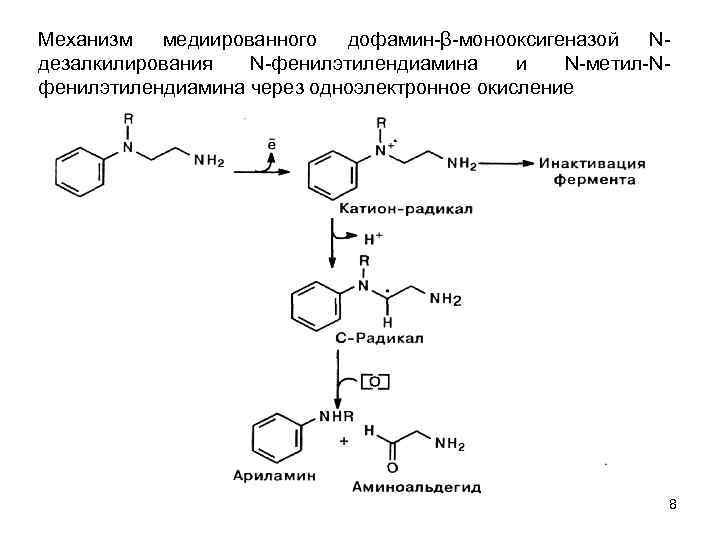 Механизм медиированного дофамин β монооксигеназой N дезалкилирования N фенилэтилендиамина и N метил N фенилэтилендиамина через одноэлектронное окисление 8
Механизм медиированного дофамин β монооксигеназой N дезалкилирования N фенилэтилендиамина и N метил N фенилэтилендиамина через одноэлектронное окисление 8
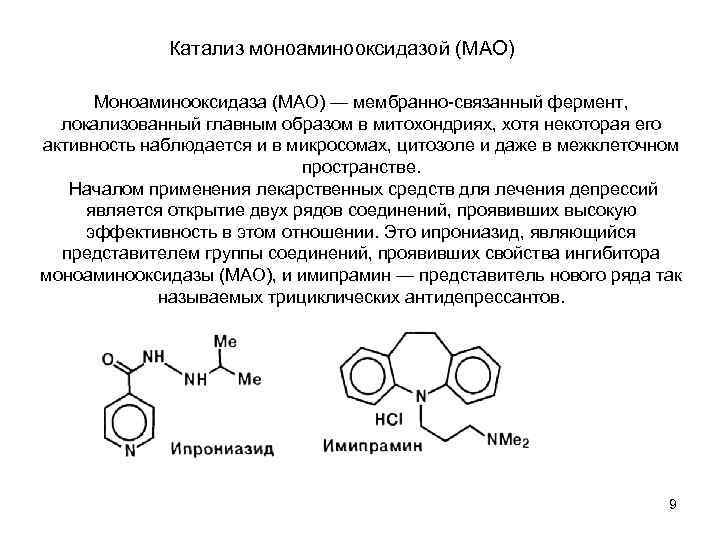 Катализ моноаминооксидазой (МАО) Моноаминооксидаза (МАО) — мембранно связанный фермент, локализованный главным образом в митохондриях, хотя некоторая его активность наблюдается и в микросомах, цитозоле и даже в межклеточном пространстве. Началом применения лекарственных средств для лечения депрессий является открытие двух рядов соединений, проявивших высокую эффективность в этом отношении. Это ипрониазид, являющийся представителем группы соединений, проявивших свойства ингибитора моноаминооксидазы (МАО), и имипрамин — представитель нового ряда так называемых трициклических антидепрессантов. 9
Катализ моноаминооксидазой (МАО) Моноаминооксидаза (МАО) — мембранно связанный фермент, локализованный главным образом в митохондриях, хотя некоторая его активность наблюдается и в микросомах, цитозоле и даже в межклеточном пространстве. Началом применения лекарственных средств для лечения депрессий является открытие двух рядов соединений, проявивших высокую эффективность в этом отношении. Это ипрониазид, являющийся представителем группы соединений, проявивших свойства ингибитора моноаминооксидазы (МАО), и имипрамин — представитель нового ряда так называемых трициклических антидепрессантов. 9
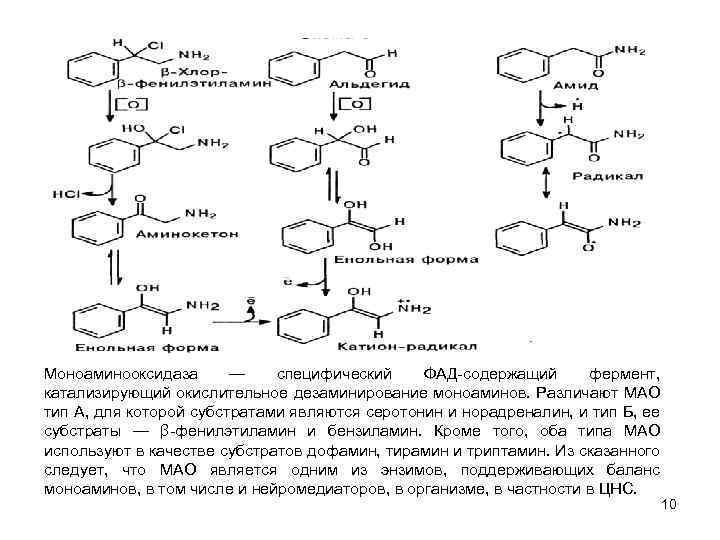 Моноаминооксидаза — специфический ФАД содержащий фермент, катализирующий окислительное дезаминирование моноаминов. Различают МАО тип А, для которой субстратами являются серотонин и норадреналин, и тип Б, ее субстраты — β фенилэтиламин и бензиламин. Кроме того, оба типа МАО используют в качестве субстратов дофамин, тирамин и триптамин. Из сказанного следует, что МАО является одним из энзимов, поддерживающих баланс моноаминов, в том числе и нейромедиаторов, в организме, в частности в ЦНС. 10
Моноаминооксидаза — специфический ФАД содержащий фермент, катализирующий окислительное дезаминирование моноаминов. Различают МАО тип А, для которой субстратами являются серотонин и норадреналин, и тип Б, ее субстраты — β фенилэтиламин и бензиламин. Кроме того, оба типа МАО используют в качестве субстратов дофамин, тирамин и триптамин. Из сказанного следует, что МАО является одним из энзимов, поддерживающих баланс моноаминов, в том числе и нейромедиаторов, в организме, в частности в ЦНС. 10
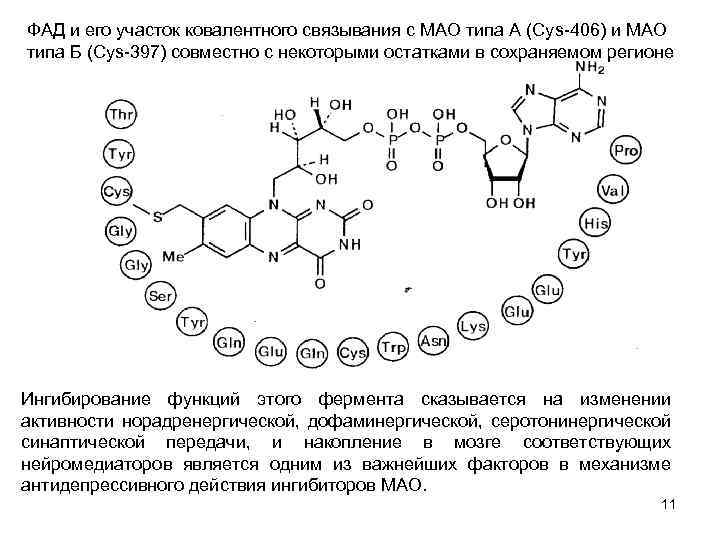 ФАД и его участок ковалентного связывания с МАО типа А (Суs 406) и МАО типа Б (Суs 397) совместно с некоторыми остатками в сохраняемом регионе Ингибирование функций этого фермента сказывается на изменении активности норадренергической, дофаминергической, серотонинергической синаптической передачи, и накопление в мозге соответствующих нейромедиаторов является одним из важнейших факторов в механизме антидепрессивного действия ингибиторов МАО. 11
ФАД и его участок ковалентного связывания с МАО типа А (Суs 406) и МАО типа Б (Суs 397) совместно с некоторыми остатками в сохраняемом регионе Ингибирование функций этого фермента сказывается на изменении активности норадренергической, дофаминергической, серотонинергической синаптической передачи, и накопление в мозге соответствующих нейромедиаторов является одним из важнейших факторов в механизме антидепрессивного действия ингибиторов МАО. 11
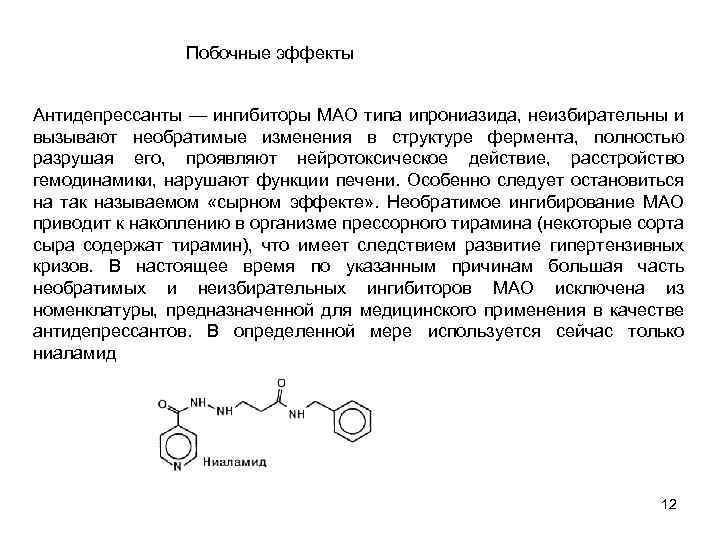 Побочные эффекты Антидепрессанты — ингибиторы МАО типа ипрониазида, неизбирательны и вызывают необратимые изменения в структуре фермента, полностью разрушая его, проявляют нейротоксическое действие, расстройство гемодинамики, нарушают функции печени. Особенно следует остановиться на так называемом «сырном эффекте» . Необратимое ингибирование МАО приводит к накоплению в организме прессорного тирамина (некоторые сорта сыра содержат тирамин), что имеет следствием развитие гипертензивных кризов. В настоящее время по указанным причинам большая часть необратимых и неизбирательных ингибиторов МАО исключена из номенклатуры, предназначенной для медицинского применения в качестве антидепрессантов. В определенной мере используется сейчас только ниаламид 12
Побочные эффекты Антидепрессанты — ингибиторы МАО типа ипрониазида, неизбирательны и вызывают необратимые изменения в структуре фермента, полностью разрушая его, проявляют нейротоксическое действие, расстройство гемодинамики, нарушают функции печени. Особенно следует остановиться на так называемом «сырном эффекте» . Необратимое ингибирование МАО приводит к накоплению в организме прессорного тирамина (некоторые сорта сыра содержат тирамин), что имеет следствием развитие гипертензивных кризов. В настоящее время по указанным причинам большая часть необратимых и неизбирательных ингибиторов МАО исключена из номенклатуры, предназначенной для медицинского применения в качестве антидепрессантов. В определенной мере используется сейчас только ниаламид 12
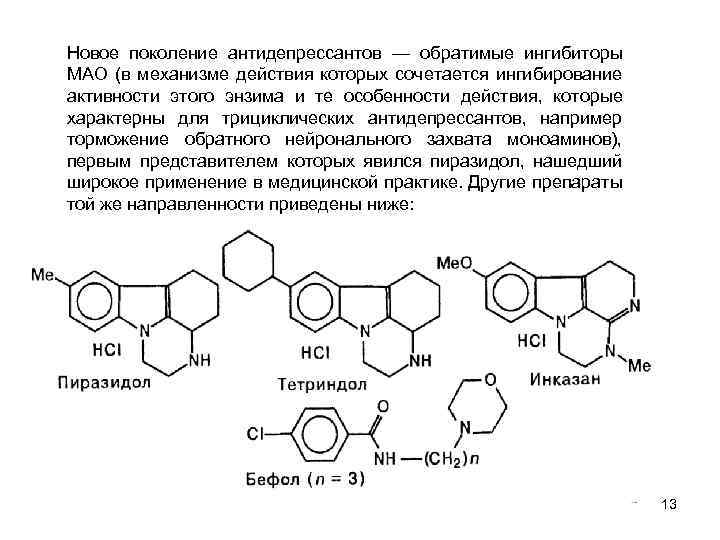 Новое поколение антидепрессантов — обратимые ингибиторы МАО (в механизме действия которых сочетается ингибирование активности этого энзима и те особенности действия, которые характерны для трициклических антидепрессантов, например торможение обратного нейронального захвата моноаминов), первым представителем которых явился пиразидол, нашедший широкое применение в медицинской практике. Другие препараты той же направленности приведены ниже: 13
Новое поколение антидепрессантов — обратимые ингибиторы МАО (в механизме действия которых сочетается ингибирование активности этого энзима и те особенности действия, которые характерны для трициклических антидепрессантов, например торможение обратного нейронального захвата моноаминов), первым представителем которых явился пиразидол, нашедший широкое применение в медицинской практике. Другие препараты той же направленности приведены ниже: 13
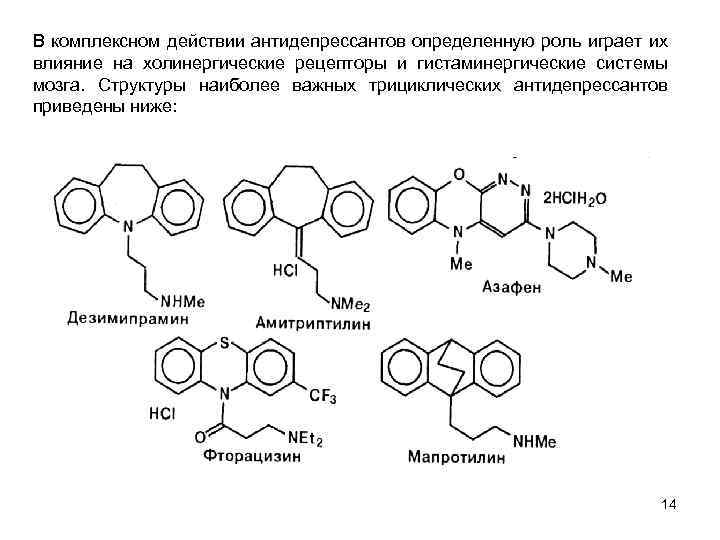 В комплексном действии антидепрессантов определенную роль играет их влияние на холинергические рецепторы и гистаминергические системы мозга. Структуры наиболее важных трициклических антидепрессантов приведены ниже: 14
В комплексном действии антидепрессантов определенную роль играет их влияние на холинергические рецепторы и гистаминергические системы мозга. Структуры наиболее важных трициклических антидепрессантов приведены ниже: 14
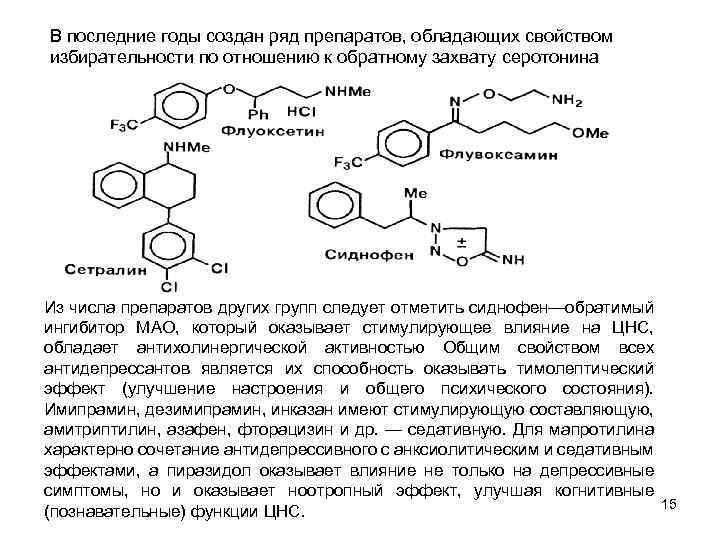 В последние годы создан ряд препаратов, обладающих свойством избирательности по отношению к обратному захвату серотонина Из числа препаратов других групп следует отметить сиднофен—обратимый ингибитор МАО, который оказывает стимулирующее влияние на ЦНС, обладает антихолинергической активностью Общим свойством всех антидепрессантов является их способность оказывать тимолептический эффект (улучшение настроения и общего психического состояния). Имипрамин, дезимипрамин, инказан имеют стимулирующую составляющую, амитриптилин, азафен, фторацизин и др. — седативную. Для мапротилина характерно сочетание антидепрессивного с анксиолитическим и седативным эффектами, а пиразидол оказывает влияние не только на депрессивные симптомы, но и оказывает ноотропный эффект, улучшая когнитивные 15 (познавательные) функции ЦНС.
В последние годы создан ряд препаратов, обладающих свойством избирательности по отношению к обратному захвату серотонина Из числа препаратов других групп следует отметить сиднофен—обратимый ингибитор МАО, который оказывает стимулирующее влияние на ЦНС, обладает антихолинергической активностью Общим свойством всех антидепрессантов является их способность оказывать тимолептический эффект (улучшение настроения и общего психического состояния). Имипрамин, дезимипрамин, инказан имеют стимулирующую составляющую, амитриптилин, азафен, фторацизин и др. — седативную. Для мапротилина характерно сочетание антидепрессивного с анксиолитическим и седативным эффектами, а пиразидол оказывает влияние не только на депрессивные симптомы, но и оказывает ноотропный эффект, улучшая когнитивные 15 (познавательные) функции ЦНС.
 Каталитический механизм действия моноаминооксидазы Ниже дана схема окислительного дезаминирования β фенилэтиламина Реакция начинается с одноэлектронного окисления по аминогруппе β фенилэтиламина. Полагают, что именно эта реакция (а)) является стадией, лимитирующей скорость процесса в целом. Это одноэлектронное окисление амина побуждает к его превращению за счет наличия достаточно кислого a протона в радикал катион, что, в свою очередь, облегчает отрыв этого протона с образованием бирадикального продукта (стадии (b) и (с)). На следующей окислительной ступени возникает имминий катион, а фермент переходит в двухэлектронное восстановленное состояние (реакция (d). Эта медиированная ФАД вторичная окислительная ступень характерна для субстратов с относительно низким окислительным потенциалом. А для субстратов с высоким окислительным потенциалом и облегченным переносом второго электрона предполагаются альтернативные механизмы, включающие стадии (е) и (f) Рассмотренный выше имминиевый ион гидролизуется до альдегида (реакция (g)) и далее восстановленный энзим связывается с молекулярным кислородом (реакции (h), (i) и на последнем этапе (j), завершающая циклический процесс). Удаление протонов в подобных реакциях катализируется нуклеофильной группой апофермента. 16
Каталитический механизм действия моноаминооксидазы Ниже дана схема окислительного дезаминирования β фенилэтиламина Реакция начинается с одноэлектронного окисления по аминогруппе β фенилэтиламина. Полагают, что именно эта реакция (а)) является стадией, лимитирующей скорость процесса в целом. Это одноэлектронное окисление амина побуждает к его превращению за счет наличия достаточно кислого a протона в радикал катион, что, в свою очередь, облегчает отрыв этого протона с образованием бирадикального продукта (стадии (b) и (с)). На следующей окислительной ступени возникает имминий катион, а фермент переходит в двухэлектронное восстановленное состояние (реакция (d). Эта медиированная ФАД вторичная окислительная ступень характерна для субстратов с относительно низким окислительным потенциалом. А для субстратов с высоким окислительным потенциалом и облегченным переносом второго электрона предполагаются альтернативные механизмы, включающие стадии (е) и (f) Рассмотренный выше имминиевый ион гидролизуется до альдегида (реакция (g)) и далее восстановленный энзим связывается с молекулярным кислородом (реакции (h), (i) и на последнем этапе (j), завершающая циклический процесс). Удаление протонов в подобных реакциях катализируется нуклеофильной группой апофермента. 16
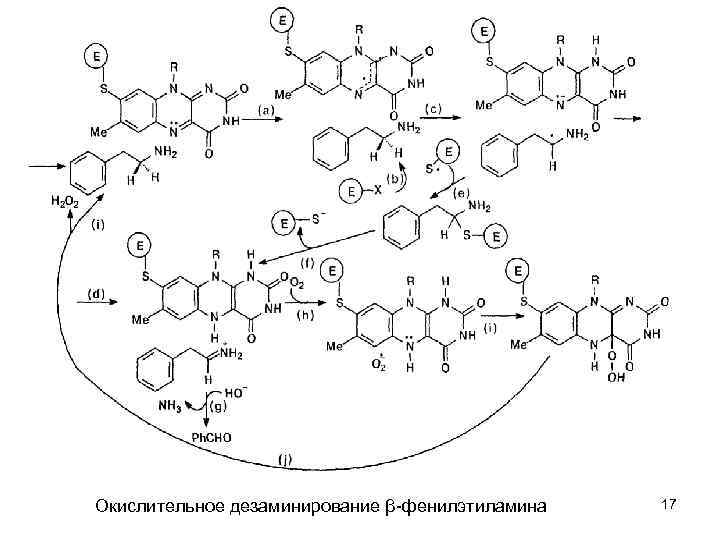 Окислительное дезаминирование β фенилэтиламина 17
Окислительное дезаминирование β фенилэтиламина 17
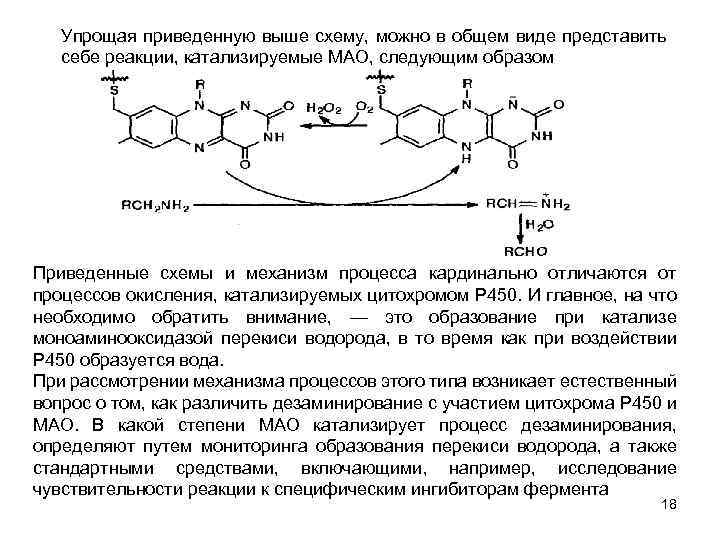 Упрощая приведенную выше схему, можно в общем виде представить себе реакции, катализируемые МАО, следующим образом Приведенные схемы и механизм процесса кардинально отличаются от процессов окисления, катализируемых цитохромом Р 450. И главное, на что необходимо обратить внимание, — это образование при катализе моноаминооксидазой перекиси водорода, в то время как при воздействии Р 450 образуется вода. При рассмотрении механизма процессов этого типа возникает естественный вопрос о том, как различить дезаминирование с участием цитохрома Р 450 и МАО. В какой степени МАО катализирует процесс дезаминирования, определяют путем мониторинга образования перекиси водорода, а также стандартными средствами, включающими, например, исследование чувствительности реакции к специфическим ингибиторам фермента 18
Упрощая приведенную выше схему, можно в общем виде представить себе реакции, катализируемые МАО, следующим образом Приведенные схемы и механизм процесса кардинально отличаются от процессов окисления, катализируемых цитохромом Р 450. И главное, на что необходимо обратить внимание, — это образование при катализе моноаминооксидазой перекиси водорода, в то время как при воздействии Р 450 образуется вода. При рассмотрении механизма процессов этого типа возникает естественный вопрос о том, как различить дезаминирование с участием цитохрома Р 450 и МАО. В какой степени МАО катализирует процесс дезаминирования, определяют путем мониторинга образования перекиси водорода, а также стандартными средствами, включающими, например, исследование чувствительности реакции к специфическим ингибиторам фермента 18
 Катализ молибденгидролазами Рассматриваемые здесь ферменты — ксантиноксидаза, ксантинде гидрогеназа и альдегидоксидаза — обозначаются как молибденгидро лазы. Человеческие ксантиноксидаза и ксантиндегидрогеназа содержат как кофакторы одну молекулу ФАД, один атом молибдена — важный компонент молибденптеринового кофактора, четыре негемных атома железа в форме двух Fе 2/S 2 кластеров ферредоксинового типа. В данном случае имеется уникальное сочетание простетических групп, и понятно, почему эти ферменты группируют под названием молибденфлавопротеины. Обобщенное уравнение процессов, катализируемых этими ферментами, представлено ниже Атом кислорода, входящий в молекулу субстрата, производится из молекулы воды, в реакции формально высвобождаются два электрона и существует необходимость в присутствии в системе акцептора электронов 19
Катализ молибденгидролазами Рассматриваемые здесь ферменты — ксантиноксидаза, ксантинде гидрогеназа и альдегидоксидаза — обозначаются как молибденгидро лазы. Человеческие ксантиноксидаза и ксантиндегидрогеназа содержат как кофакторы одну молекулу ФАД, один атом молибдена — важный компонент молибденптеринового кофактора, четыре негемных атома железа в форме двух Fе 2/S 2 кластеров ферредоксинового типа. В данном случае имеется уникальное сочетание простетических групп, и понятно, почему эти ферменты группируют под названием молибденфлавопротеины. Обобщенное уравнение процессов, катализируемых этими ферментами, представлено ниже Атом кислорода, входящий в молекулу субстрата, производится из молекулы воды, в реакции формально высвобождаются два электрона и существует необходимость в присутствии в системе акцептора электронов 19
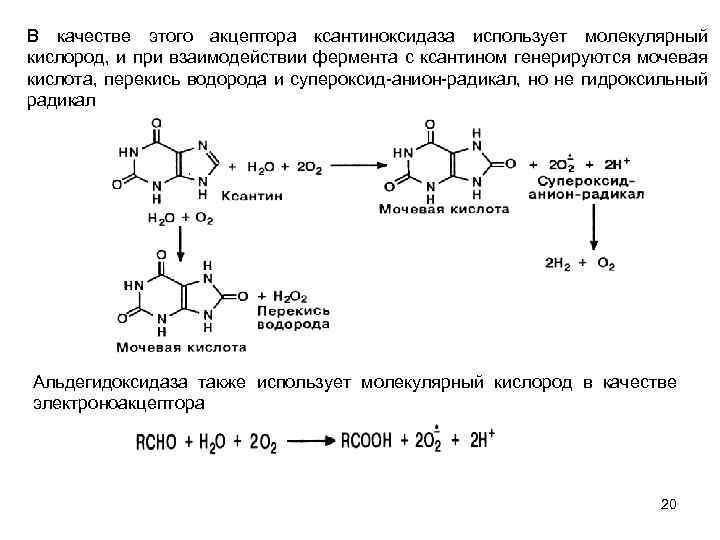 В качестве этого акцептора ксантиноксидаза использует молекулярный кислород, и при взаимодействии фермента с ксантином генерируются мочевая кислота, перекись водорода и супероксид анион радикал, но не гидроксильный радикал Альдегидоксидаза также использует молекулярный кислород в качестве электроноакцептора 20
В качестве этого акцептора ксантиноксидаза использует молекулярный кислород, и при взаимодействии фермента с ксантином генерируются мочевая кислота, перекись водорода и супероксид анион радикал, но не гидроксильный радикал Альдегидоксидаза также использует молекулярный кислород в качестве электроноакцептора 20
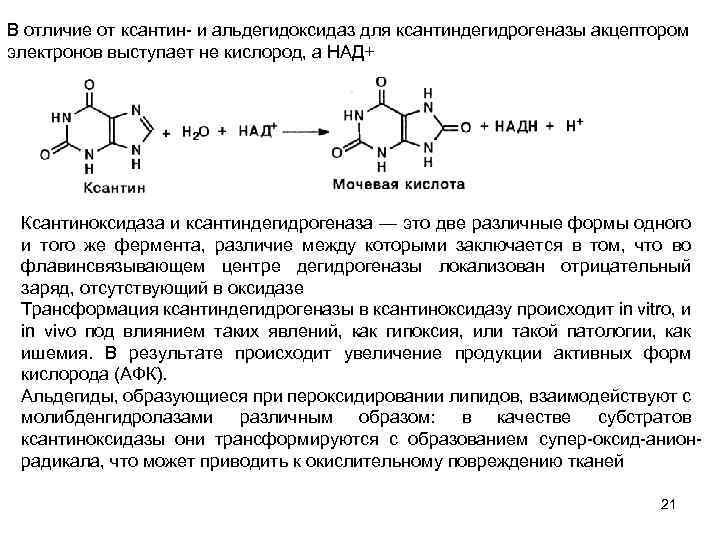 В отличие от ксантин и альдегидоксидаз для ксантиндегидрогеназы акцептором электронов выступает не кислород, а НАД+ Ксантиноксидаза и ксантиндегидрогеназа — это две различные формы одного и того же фермента, различие между которыми заключается в том, что во флавинсвязывающем центре дегидрогеназы локализован отрицательный заряд, отсутствующий в оксидазе Трансформация ксантиндегидрогеназы в ксантиноксидазу происходит in vitro, и in vivo под влиянием таких явлений, как гипоксия, или такой патологии, как ишемия. В результате происходит увеличение продукции активных форм кислорода (АФК). Альдегиды, образующиеся при пероксидировании липидов, взаимодействуют с молибденгидролазами различным образом: в качестве субстратов ксантиноксидазы они трансформируются с образованием супер оксид анион радикала, что может приводить к окислительному повреждению тканей 21
В отличие от ксантин и альдегидоксидаз для ксантиндегидрогеназы акцептором электронов выступает не кислород, а НАД+ Ксантиноксидаза и ксантиндегидрогеназа — это две различные формы одного и того же фермента, различие между которыми заключается в том, что во флавинсвязывающем центре дегидрогеназы локализован отрицательный заряд, отсутствующий в оксидазе Трансформация ксантиндегидрогеназы в ксантиноксидазу происходит in vitro, и in vivo под влиянием таких явлений, как гипоксия, или такой патологии, как ишемия. В результате происходит увеличение продукции активных форм кислорода (АФК). Альдегиды, образующиеся при пероксидировании липидов, взаимодействуют с молибденгидролазами различным образом: в качестве субстратов ксантиноксидазы они трансформируются с образованием супер оксид анион радикала, что может приводить к окислительному повреждению тканей 21
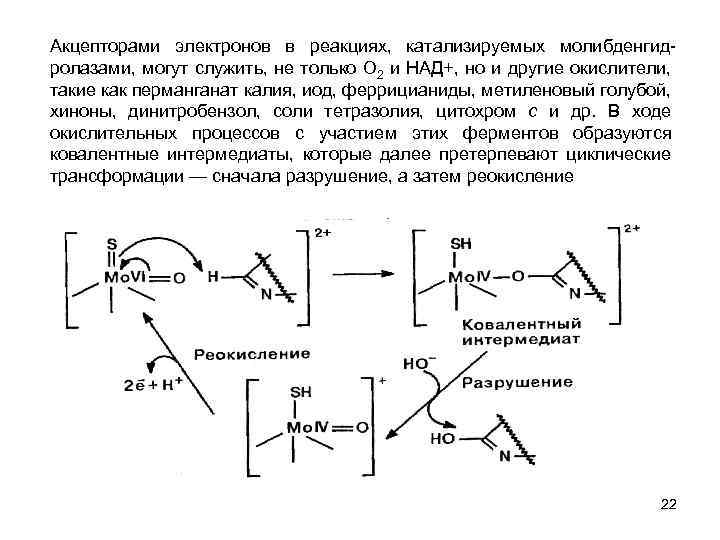 Акцепторами электронов в реакциях, катализируемых молибденгид ролазами, могут служить, не только О 2 и НАД+, но и другие окислители, такие как перманганат калия, иод, феррицианиды, метиленовый голубой, хиноны, динитробензол, соли тетразолия, цитохром с и др. В ходе окислительных процессов с участием этих ферментов образуются ковалентные интермедиаты, которые далее претерпевают циклические трансформации — сначала разрушение, а затем реокисление 22
Акцепторами электронов в реакциях, катализируемых молибденгид ролазами, могут служить, не только О 2 и НАД+, но и другие окислители, такие как перманганат калия, иод, феррицианиды, метиленовый голубой, хиноны, динитробензол, соли тетразолия, цитохром с и др. В ходе окислительных процессов с участием этих ферментов образуются ковалентные интермедиаты, которые далее претерпевают циклические трансформации — сначала разрушение, а затем реокисление 22
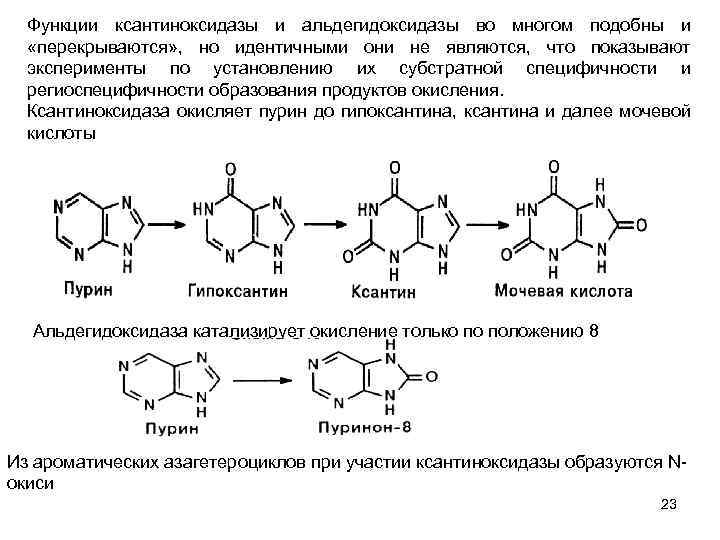 Функции ксантиноксидазы и альдегидоксидазы во многом подобны и «перекрываются» , но идентичными они не являются, что показывают эксперименты по установлению их субстратной специфичности и региоспецифичности образования продуктов окисления. Ксантиноксидаза окисляет пурин до гипоксантина, ксантина и далее мочевой кислоты Альдегидоксидаза катализирует окисление только по положению 8 Из ароматических азагетероциклов при участии ксантиноксидазы образуются N окиси 23
Функции ксантиноксидазы и альдегидоксидазы во многом подобны и «перекрываются» , но идентичными они не являются, что показывают эксперименты по установлению их субстратной специфичности и региоспецифичности образования продуктов окисления. Ксантиноксидаза окисляет пурин до гипоксантина, ксантина и далее мочевой кислоты Альдегидоксидаза катализирует окисление только по положению 8 Из ароматических азагетероциклов при участии ксантиноксидазы образуются N окиси 23
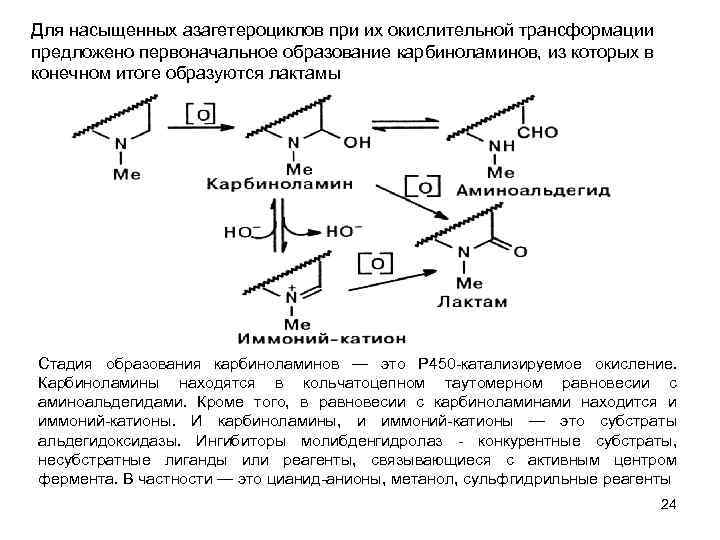 Для насыщенных азагетероциклов при их окислительной трансформации предложено первоначальное образование карбиноламинов, из которых в конечном итоге образуются лактамы Стадия образования карбиноламинов — это Р 450 катализируемое окисление. Карбиноламины находятся в кольчатоцепном таутомерном равновесии с аминоальдегидами. Кроме того, в равновесии с карбиноламинами находится и иммоний катионы. И карбиноламины, и иммоний катионы — это субстраты альдегидоксидазы. Ингибиторы молибденгидролаз конкурентные субстраты, несубстратные лиганды или реагенты, связывающиеся с активным центром фермента. В частности — это цианид анионы, метанол, сульфгидрильные реагенты 24
Для насыщенных азагетероциклов при их окислительной трансформации предложено первоначальное образование карбиноламинов, из которых в конечном итоге образуются лактамы Стадия образования карбиноламинов — это Р 450 катализируемое окисление. Карбиноламины находятся в кольчатоцепном таутомерном равновесии с аминоальдегидами. Кроме того, в равновесии с карбиноламинами находится и иммоний катионы. И карбиноламины, и иммоний катионы — это субстраты альдегидоксидазы. Ингибиторы молибденгидролаз конкурентные субстраты, несубстратные лиганды или реагенты, связывающиеся с активным центром фермента. В частности — это цианид анионы, метанол, сульфгидрильные реагенты 24
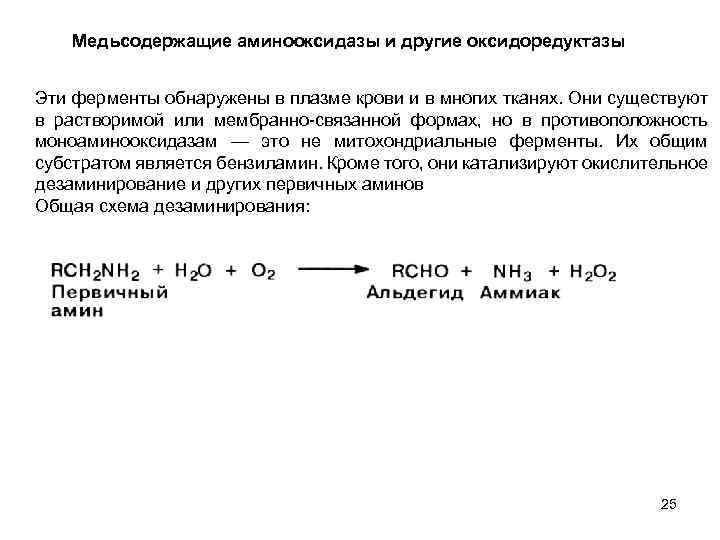 Медьсодержащие аминооксидазы и другие оксидоредуктазы Эти ферменты обнаружены в плазме крови и в многих тканях. Они существуют в растворимой или мембранно связанной формах, но в противоположность моноаминооксидазам — это не митохондриальные ферменты. Их общим субстратом является бензиламин. Кроме того, они катализируют окислительное дезаминирование и других первичных аминов Общая схема дезаминирования: 25
Медьсодержащие аминооксидазы и другие оксидоредуктазы Эти ферменты обнаружены в плазме крови и в многих тканях. Они существуют в растворимой или мембранно связанной формах, но в противоположность моноаминооксидазам — это не митохондриальные ферменты. Их общим субстратом является бензиламин. Кроме того, они катализируют окислительное дезаминирование и других первичных аминов Общая схема дезаминирования: 25
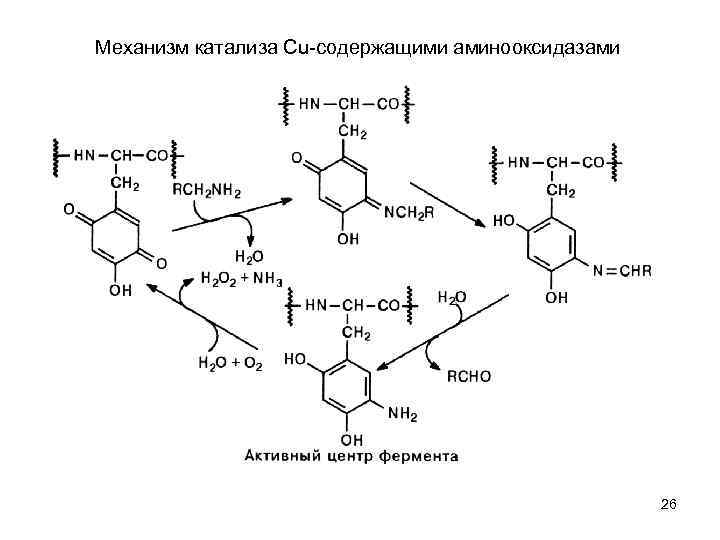 Механизм катализа Сu содержащими аминооксидазами 26
Механизм катализа Сu содержащими аминооксидазами 26


