Лекция 9 инженерная энзимология.ppt
- Количество слайдов: 68

Ферменты или энзимы o Ферменты (энзимы) – биологические катализаторы, обладающие способностью избирательно катализировать многие химические превращения как в живой клетке, так и вне организма.

История применения ферментов

Роль и значение ферментов o o o Ферменты (энзимы) это биологические катализаторы, способные катализировать многие химические превращения как в живой клетке, так и вне организма. Ферменты – как правило белковые молекулы. В 1926 г. был впервые очищен и выделен в виде белковых кристаллов фермент уреаза, катализирующий реакции расщепления мочевины до аммиака и углекислого газа.
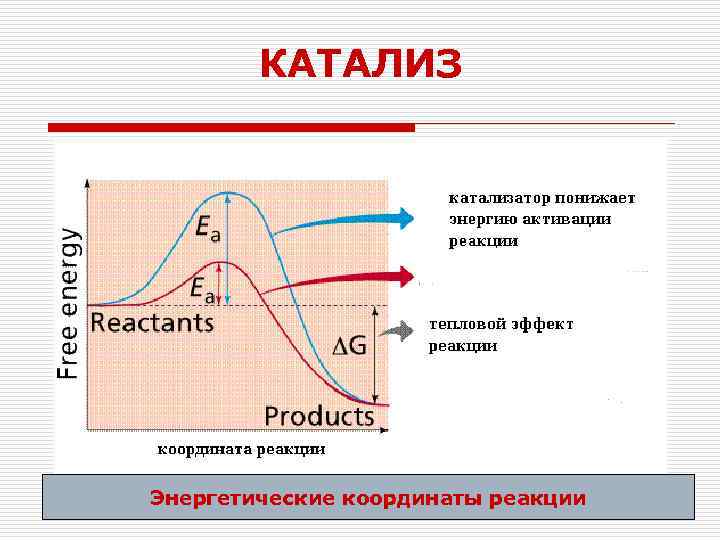
КАТАЛИЗ Энергетические координаты реакции
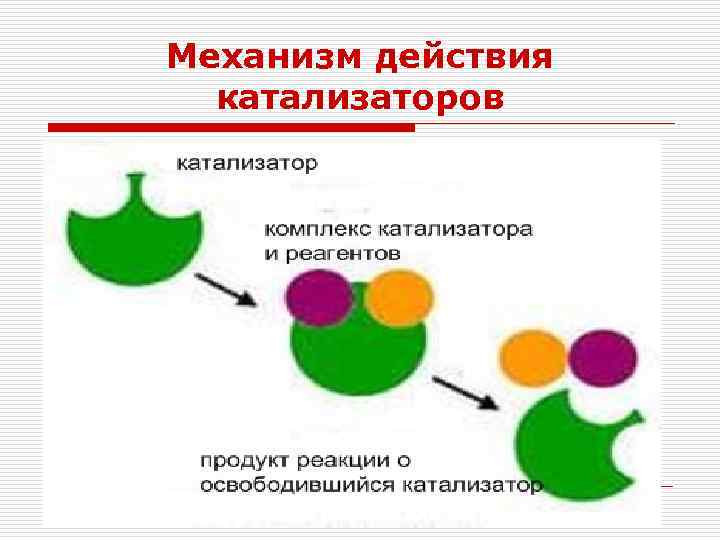
Механизм действия катализаторов

Механизм действия ферментов o o o 1. 2. Биологическая функция фермента, как и любого белка, обусловлена наличием в его структуре активного центра. Лиганд, взаимодействующий с активным центром фермента, называют субстратом В активном центре фермента есть: (участок связывания) аминокислотные остатки и его функциональные группы обеспечивают связывания субстрата (каталитический участок) аминокислотные остатки и его функциональные группы осуществляют химические превращения субстрата

Механизм действия ферментов o o В участке связывания субстрат при помощи нековалентных связей взаимодействует с ферментом, формируя фермент-субстратный комплекс. В каталитическом участке субстрат претерпевает химическое превращение в продукт, который затем высвобождается из активного центра фермента
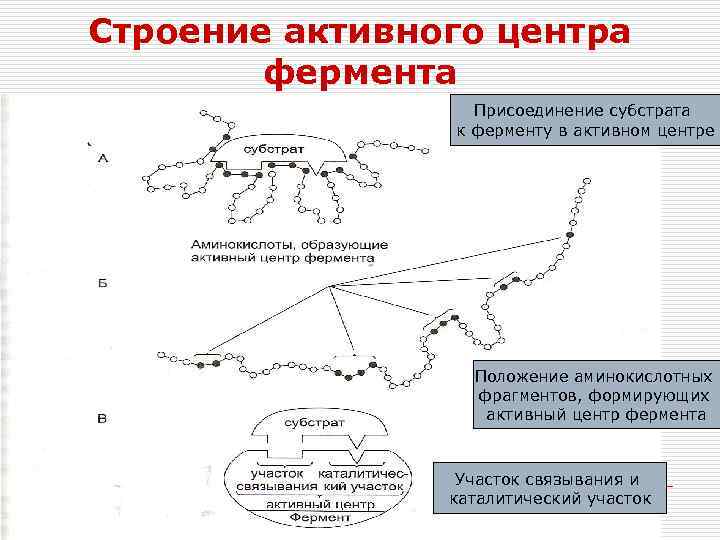
Строение активного центра фермента Присоединение субстрата к ферменту в активном центре Положение аминокислотных фрагментов, формирующих активный центр фермента Участок связывания и каталитический участок

Специфичность o o o Специфичность – наиболее важное свойство ферментов, определяющее биологическую значимость этих молекул. Различают субстратную и каталитическую специфичность ферментов. Специфичность определяется строением активного центра.

Субстратная специфичность o o 1. 2. 3. Субстратная специфичность – способность каждого фермента взаимодействовать лишь с одним или несколькими определенными субстратами. Типы субстратной специфичности: Абсолютная Групповая Стереоспецифичность

Абсолютная субстратная специфичность o o o Активный центр ферментов, обладающих абсолютной субстратной специфичностью взаимодействует только с одним определенным субстратом. Абсолютная субстратная специфичность довольно редкое явление. Пример – аргиназа катализирующая реакцию расщепления аргинина до мочевины и орнитина.

Групповая субстратная специфичность o o 1. 2. Большинство ферментов катализирует однотипные реакции с небольшим количеством структурно похожих субстратов Примеры: панкреатическая липаза катализирует гидролиз любой молекулы жира (триацилглицерола) до моноацилглицерола и двух молекул высших жирных кислот. ферменты гидролизующие белки имеют групповую субстратную специфичность, гидролизуя пептидные связи , образованные разными аминокислотами.
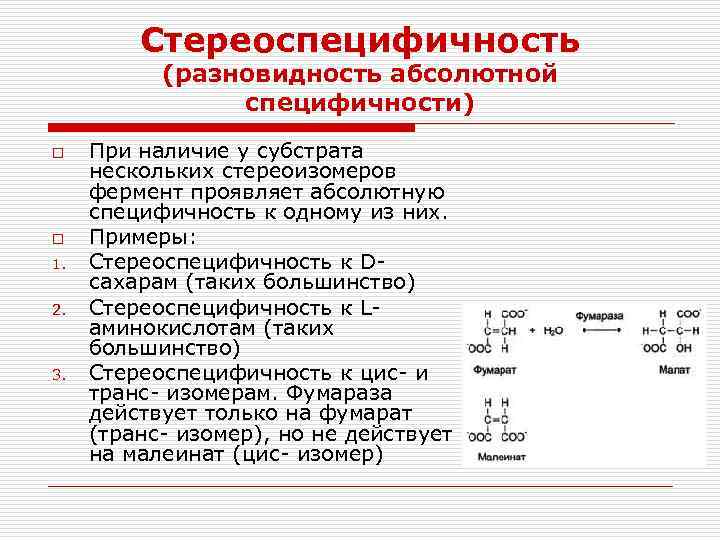
Стереоспецифичность (разновидность абсолютной специфичности) o o 1. 2. 3. При наличие у субстрата нескольких стереоизомеров фермент проявляет абсолютную специфичность к одному из них. Примеры: Стереоспецифичность к Dсахарам (таких большинство) Стереоспецифичность к Lаминокислотам (таких большинство) Стереоспецифичность к цис- и транс- изомерам. Фумараза действует только на фумарат (транс- изомер), но не действует на малеинат (цис- изомер)

Каталитическая специфичность o o Строение каталитического участка активного центра фермента обеспечивает и катализирует превращение присоединенного субстрата. Это свойство фермента и называется каталитической специфичностью.

Каталитическая эффективность o o o Большинство катализируемых ферментами реакций высокоэффективны, они протекают в 108 -1014 раз быстрее, чем некатализируемые реакции. Каждая молекула фермента способна за секунду трансформировать от 100 до 1000 молекул субстрата в продукт. Количество молекул субстрата, превращенных в продукт с помощью одной молекулы фермента за 1 секунду, называют числом оборота фермента или молярной активностью

Классы ферментов o o Оксиредуктазы – катализируют различные окислительновосстановительные реакции с участием двух субстратов (перенос электрона (-) или протона (+) с одного субстрата на другой. Трансферазы – катализируют перенос функциональных групп от одного соединения к другому (аминотрансферазы, ацилтрансферазы, метилтрансферазы, гликозилтрансферазы и киназы (форфортрансферазы))

Классы ферментов o o Гидролазы – катализируют реакции гидролиза (расщепления ковалентной связи и присоединение молекулы воды). Лиазы – катализируют отщепление определенной функциональной группы (CO 2, H 2 O, NH 2, SH и др. )

Классы ферментов o o Изомеразы – катализируют различные внутримолекулярные превращения (окислительновосстановительные реакции, взаимопревращение альдоз и кетоз, перемещение двойных связей). Лигазы (синтазы) – катализируют реакции соединения двух молекул с образованием ковалентной связи

Кофакторы и коферменты o Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой природы (коферментах) и/или в ионах металлов (кофакторах).

Кофакторы (ионы металлов Zn, Mg, Fe, Mn, Co, Mo, K, Cu) o 1. 2. 3. 4. Роль кофакторов в ферментном катализе: Стабилизация молекул субстрата Стабилизация активного центра фермента Стабизизация вторичной и третичной структуры фермента Участие в электрофильном катализе и окислительно-восстановительных реакциях

Коферменты (низкомолекулярные органические соединения) o Кофермент, локализуясь в каталитическом участке активного центра, принимает непосредственное участие в химической реакции, выступая в качестве акцептора или донора химических группировок, атомов и электронов
Коферменты o 1. 2. 3. 4. 5. К коферментам относят: Производные витаминов Гемы Нуклеотиды – доноры и акцепторы остатка фосфорной кислоты S-аденозилметионин – донор метильной группы Убихинон или кофермент Q – участвует в переносе электронов и протонов Coenzyme Q 10

Применение ферментов в биотехнологии o o Ферменты широко применяют на практике, они нетоксичны, работают в мягких условиях и используют доступное сырье (часто отходы). Применение ферментов в промышленности выгодно с экономической и экологической точек зрения

Производство ферментов o o o 1. 2. 3. 4. 5. По объему мирового биотехнологического производства ферменты занимают третье место после аминокислот и антибиотиков. Известно около 2000 ферментов. В промышленности используются около 30. Основная часть производства ферментов приходится на долю гидролаз (моющие средства и пищевая промышленность: Гидролиз крахмала до декстринов, мальтозы и глюкозы Гидролиз целлюлозы Гидролиз жиров и масел Лизис белка Изомеризация D-глюкозы в D-фруктозу (приготовление обогащенной фруктозой кукурузных сиропов)
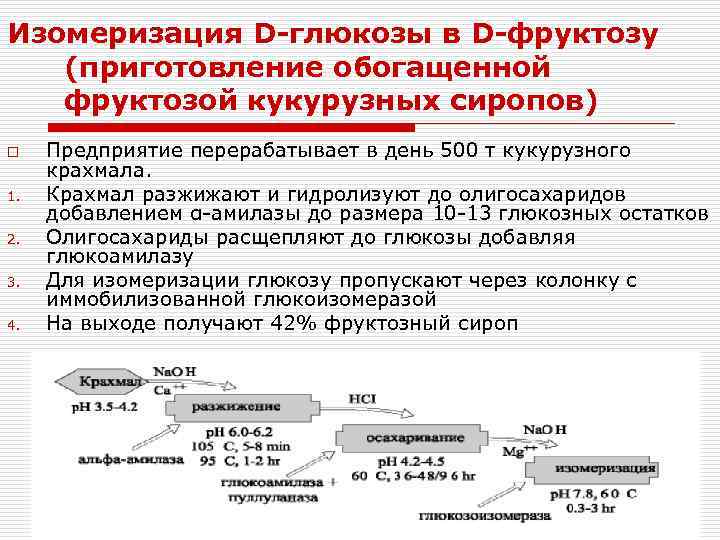
Изомеризация D-глюкозы в D-фруктозу (приготовление обогащенной фруктозой кукурузных сиропов) o 1. 2. 3. 4. Предприятие перерабатывает в день 500 т кукурузного крахмала. Крахмал разжижают и гидролизуют до олигосахаридов добавлением α-амилазы до размера 10 -13 глюкозных остатков Олигосахариды расщепляют до глюкозы добавляя глюкоамилазу Для изомеризации глюкозу пропускают через колонку с иммобилизованной глюкоизомеразой На выходе получают 42% фруктозный сироп

Источники ферментов для биотехнологических производств o o 1. 2. 3. Для получения (выделения) ферментов для промышленных целей используют те природные объекты, в которых содержание искомого энзима не менее 1 % Источники ферментов: Растительные организмы (проростки, латекс, сок зеленой массы) Ткани и органы животных (поджелудочная железа, слизистая оболочка желудка, сычуг групного рогатого скота и др) Микроорганизмы (бактерии, грибы, дрожжи)

В солодовом процессе при пивоварении используется фермент - амилаза o Амилаза получается из проростков ячменя.

Перерыв

Технология получения ферментных препаратов o o o Технология получения ферментных препаратов зависит от вида исходного сырья. Из растительного сырья или животных тканей ферменты экстрагируют и очищают от балластных веществ. Получение ферментов из микробиологического сырья более сложная и требует дополнительного этапа культивирования микроорганизмовпродуцентов

Преимущества микроорганизмов в качестве источников производства ферментов • высокая степенью специфической активности в пересчете на единицу сухого веса продукта; • отсутствие сезонных колебаниями количества и качества сырьевых материалов и возможностью их длительного сохранения. независимость от климатических изменений; • возможностью выбора нужного фермента из широкого спектра микробных катализаторов, характеризующихся различной степенью устойчивости к повышенным температурам и р. Н среды; • возможностями промышленной генетики оптимизировать характеристики ферментов и способы селекции штаммовпродуцентов путем мутагенеза, изменения условий культивирования, а также (в последнее время) применения практически неограниченных возможностей методов генетической инженерии.

Селекция продуцентов ферментов При селекции продуцентов ферментов генетики промышленных микроорганизмов стремятся улучшить желаемые их свойства: o высокий выход фермента, o стабильность фермента, o независимость синтеза фермента от индуктора, o легкое его извлечение из среды и т. п. Нежелательные качества стараются устранить или ингибировать: o наличие вредных побочных метаболитов, o неприятный запах, нежелательный цвет препарата и т. п.

Биореакторы для производства ферментов Микробные ферменты являются малообъемными препаратами относительно невысокой стоимости, методы, применяемые для их производства, обычно осуществляются с использованием биореакторов (ферментеров), аналогичных по конструкции и функциях таковым, которые применяются при производстве антибиотиков. Выбор культуральной среды является весьма важным моментом в процессе производства, так как она обеспечивает растущий микроорганизм энергией, а также является источником необходимых элементов (углерода, азота и т. д. ). Стоимость сырьевого материала непосредственно связана с ценой конечного продукта.

Технология культивирования микроорганизмов – продуцентов ферментов o o Получение посевного материала из исходного штамма продуцента, его консервация и хранение. Получение производственной культуры микроорганизма-продуцента. Выращивание посевного материала микроорганизмов происходит на поверхности твердых или жидких сред (поверхностное культивирование), а также в глубине жидких питательных сред (глубинный метод).

Твердофазная поверхностная ферментация o o Твердофазная поверхностная ферментация заключается в выращивании продуцента на поверхности тонкого слоя твердой сыпучей среды. Поверхностное культивирование обеспечивает наиболее близкие к физиологическим условия роста гриба.

Поверхностный метод выращивания продуцентов o o o Посевной материал направляют на стадию ферментации, которая осуществляется на поверхности сыпучей среды в металлических лотках или вертикальных перфорированных с обеих сторон кюветах. Основу питательной среды составляют пшеничные отруби или зерновая шелуха (источник ростовых веществ). Для разрыхления среды в отруби добавляют древесные опилки (5– 10 %), овсяную шелуху. Смесь перед автоклавированием увлажняют до 20– 40 % влажности и подкисляют для улучшения условий стерилизации. Прогрев сыпучей среды осуществляют острым паром в специальных стерилизаторах при непрерывном перемешивании среды; длительность процесса – 60– 90 минут при 105– 140 °С.

Поверхностный метод выращивания продуцентов o o o В охлажденную до 30 °С среду вносят посевной материал (0. 02– 0. 1 % от массы среды), быстро перемешивают ручным способом и раскладывают слоем 2– 3 см в лотки, которые устанавливают в герметичные аэрируемые камеры. Исходная влажность среды – 58 – 60 %, температура культивирования 28– 32 °С, длительность ферментации около 36– 48 ч. В течение первых 10– 12 ч происходит прорастание конидий при 28 °С. В последующие 14– 18 ч реализуется быстрый рост мицелия, в этот период потребляется основное количество питательных веществ из среды и скорость образования фермента достигает максимальных значений. В последующие 12– 18 ч процессы метаболизма ослабевают, но синтез ферментов еще продолжается. Мицелий обволакивает и прочно скрепляет твердые частицы среды, поэтому для нормального транспорта и окисления веществ среда должна быть достаточно рыхлой и влажной. Эффективный транспорт кислорода из газовой фазы и растворение в среде происходит при условии хорошей аэрируемости довольно тонкого слоя твердой сыпучей среды. Поверхностный метод ферментации является экстенсивным методом с большой долей ручного

Промышленные установки для поверхностного культивирования o o Применяемые в промышленности колонные аппараты объемной аэрации еще более улучшают процесс твердофазной ферментации. Такой аппарат разделен на секции перфорированными пластинами, закрепленными на поворотных осях. Среда в ходе ферментации разрыхляется с помощью вращающихся перемешивающих устройств. Это позволяет увеличить высоту слоя до 30 см. Режим перегрузки среды на тарелках задается автоматически. Производительность аппарата достигает 1 т культуры в сутки.
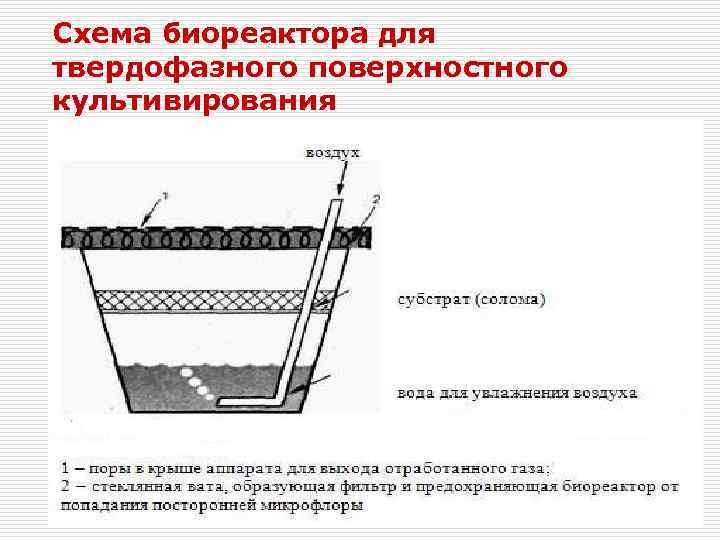
Схема биореактора для твердофазного поверхностного культивирования

Поверхностный метод выращивания продуцентов o o После завершения стадии ферментации выросшая культура представляет собой корж (пек) из набухших частиц среды, плотно связанных разросшимся мицелием. Данную массу измельчают до частиц размером 5– 6 мм. Для предотвращения инактивации ферментов массу подсушивают до остаточной влажности около 10– 12 %. Технические препараты ферментов, используемые в текстильной, кожевенной промышленности, упаковывают в бумажные многослойные крафтмешки и отправляют потребителю.

Очистка ферментов o o 1. 2. 3. В пищевой и особенно медицинской промышленности используются ферменты только высокой степени очистки. Схема очистки сводится к следующему: - освобождение от нерастворимых веществ; - освобождение от сопутствующих растворимых веществ; - фракционирование (как правило, хроматографическими методами).

Глубинный метод производства ферментов o o o Микроорганизмы выращиваются в жидкой питательной среде. Глубинная ферментация в жидкой среде может быть реализована как в условиях периодического процесса, так и с применением проточных систем. Глубинный метод технически более совершенен, чем поверхностный, так как легко поддается автоматизации и механизации.

При глубинном культивировании ферментов выделяют 5 этапов: 1. 2. 3. 4. 5. Приготовление питательных сред, стерилизацию среды, воды и воздуха. Получение посевного материала состоит в увеличении массы продуцента в 3 -4 стадии. Производственное культивирование. Биосинтез ферментов в глубинной культуре протекает в течение 2 -4 суток при непрерывной подаче воздуха и перемешивании. Температурный оптимум находится в интервале 22 -32 о. С. В современных технологических процессах ведется непрерывное автоматическое определение содержания в среде углеводов, количества образовавшихся метаболитов и концентрации клеток. Данные поступают в компьютер, который определяет стратегию коррекции процесса и автоматически регулирует его. Этим достигается максимальная производительность и наилучшее качество продуктов. Выделение. В мицелии трёхсуточной культуры обычно остается не более 15% ферментов. Остальные выделяются в культуральную жидкость. Получение товарной формы.

Технология выделения и очистки ферментных препаратов o o o Выделение и очистка фермента трудоемкая и дорогостоящая процедура. Поэтому, если фермент можно использовать в неочищенном виде, его и не очищают. В спиртовой, кожевенной и текстильной промышленности, сельском хозяйстве и бытовой химии применяют коммерческие препараты ферментов с чистотой 1 %

Технология выделения и очистки ферментных препаратов o o o Грубая очистка: упаривание, высушивание, экстракция, гомогенизация, разрушение клеток, центрифугирование (чистота до 50%) Различные виды фракционирования (термическое, осаждение органическими растворителями, солями и тяжелыми металлами, фильтрация на молекулярных ситах. Тонкая очистка: хроматография (ионообменная, афинная) и электорофорез

Инженерная энзимология o 1. 2. 3. 4. Задачи инженерной энзимологии Развитие прогрессивных методов выделения ферментов Стабилизация выделенных ферментов Иммобилизация ферментов Конструирование катализаторов с нужными свойствами

Иммобилизованные ферменты o o o Сущность иммобилизации ферментов — прикрепление их в активной форме к нерастворимой основе или заключение в полупроницаемую мембранную систему. Прикрепление фермента к носителю осуществляется адсорбционно, химической связью или путем механического включения фермента в органический или неорганический гель (в капсулу и т. п. ). При этом допускается прикрепление фермента только за счет функциональных групп, не входящих в активный центр фермента и не участвующих в образовании фермент-субстратного комплекса.

Преимущества иммобилизованных ферментов o o Гетерогенный катализатор легко отделим от реакционной среды, что дает возможность использовать фермент повторно, а также получать чистый от фермента продукт. Ферментативный процесс с использованием иммобилизованных ферментов можно проводить непрерывно, регулируя скорость катализируемой реакции и выход продукта. Модификация фермента целенаправленно изменяет его свойства, такие как специфичность, зависимость каталитической активности от р. Н, ионного состава и других параметров среды, стабильность к денатурирующим воздействиям. Можно регулировать каталитическую активность иммобилизованных ферментов путем изменения свойств носителя.

Методы иммобилизации ферментов o o 1. 2. 3. 4. Существует два основных метода иммобилизации ферментов: физический и химический. Физическая иммобилизация ферментов представляет собой включение фермента в такую среду, в которой для него доступной является лишь ограниченная часть общего объема. При физической иммобилизации фермент не связан с носителем ковалентными связями. Существует четыре типа связывания ферментов: - адсорбция на нерастворимых носителях; - включение в поры геля; - пространственное отделение фермента от остального объема реакционной системы с помощью полупроницаемой перегородки (мембраны); - включение в двухфазную среду, где фермент растворим и может находиться только в одной из фаз.
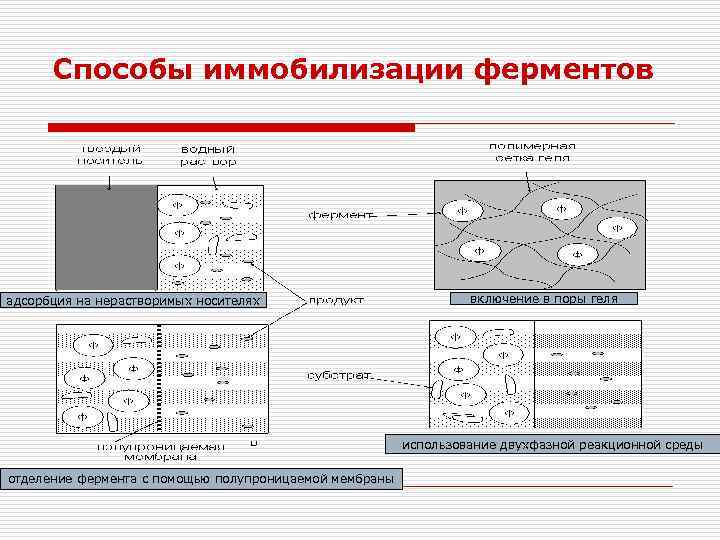
Способы иммобилизации ферментов адсорбция на нерастворимых носителях включение в поры геля использование двухфазной реакционной среды отделение фермента с помощью полупроницаемой мембраны

o Инженерная энзимология (энзиматическая инженерия) (биоиндустрия ферментов) Ферментная технология включает продукцию, выделение, очистку, использование в растворенной форме и, наконец, применение в иммобилизованном виде ферментов в широком круге реакторных систем.
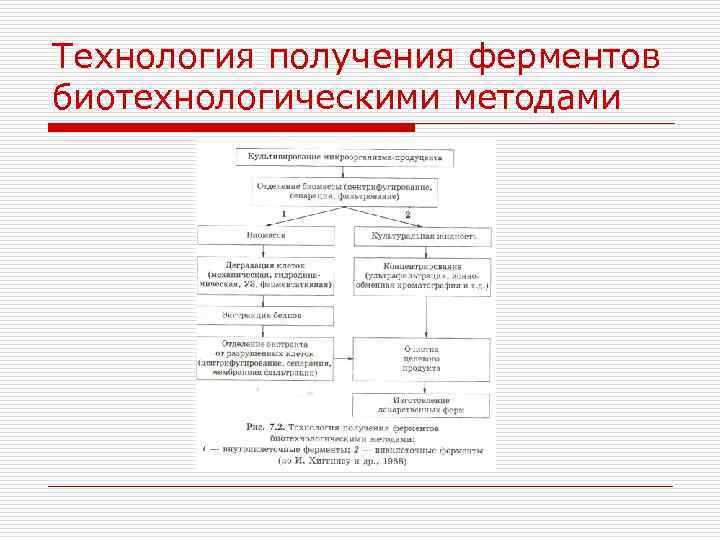
Технология получения ферментов биотехнологическими методами

Иммобилизация и ее использование в биотехнологическом производстве o o Иммобилизация – искусственное связывание ферментов, клеточных органел и клеток с нерастворимым носителем, при этом фермент сохраняет свои каталитические свойства. Иммобилизация – полное или частичное ограничение свободы движения белковых молекул.

Иммобилизация и ее использование в биотехнологическом производстве o 1. 2. 3. 4. Преимущества иммобилизованных ферментов Гетерогенность (легко отделяются от реакционной среды) Многократность использования Обеспечивают непрерывность каталитического процесса Повышение устойчивости ферментов (иммобилизованные ферменты долговечы и в тысячи раз стабильнее свободных энзимов)

Носители для иммобилизации ферментов o o 1. 2. 3. o Органические полимерные носители Природные: белковые(кератин, фиброин, коллаген, желатин) полисахаридные (целлюлоза, декстран, агароза, хитин, хитозан, губчатый крахмал) Липидные в виде монослоя или бислоя (наиболее приближены к естественным комплексам клетки) Синтетические (полимерные): полиметиленовые полиамидные Полиэфирные Неорганические носители (глина, стекло, силикагель, керамика, уголь и т. п. )
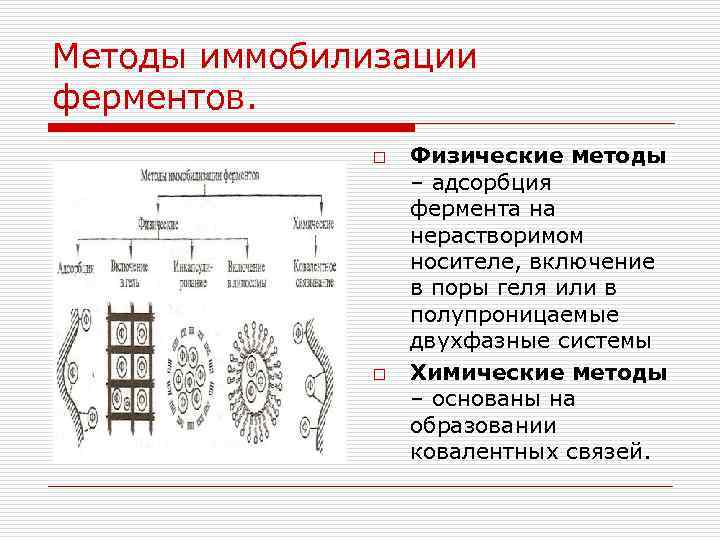
Методы иммобилизации ферментов. o o Физические методы – адсорбция фермента на нерастворимом носителе, включение в поры геля или в полупроницаемые двухфазные системы Химические методы – основаны на образовании ковалентных связей.

Применение иммобилизованных ферментов o o o В промышленности – стиральные и моющие средства в дубильных и пищевых процессах, биокатализаторы В медицине – противовоспалительные, тромболитические и фибрионолитические препараты. Иммобилизованная уреаза используется в аппарате «искусственная почка» В фармации – диагностика лекарственных веществ белковой природы

Иммобилизация клеток o o Преимущество – нет необходимости выделения и очистки ферментных препаратов, создается возможность получения полиферментных систем, осуществляющих многостадийные непрерывно действующие процессы. Иммобилизованные клетки микроорганизмов применяют для биотрансформации органических соединений, разделения рацемических смесей, инверсии сахарозы и синтезе стероидов.

Промышленные процессы с использованием иммобилизованных ферментов и клеток o o o o o Получение глюкофруктозных сиропов Синтез L-аспаргиновой кислоты из фумарата аммония Синтез L-аланина из L-аспаргиновой кислоты Синтез L-яблочной кислоты из фумаровой кислоты Получение безлактозного молока Получение сахаров их молочной сыворотки Получение 6 -аминопенициллановой кислоты Трансформация гидрокортизона в преднизолон Получение белковых гидролизатов Получение триптофана их L-серина и индола

Биосенсоры o o o Биосенсоры – это аналитические устройства, в которых чувствительный слой, содержащий биологический материал (фермент или клетка), реагирует на присутствие определяемого компонента и генерирует электрический сигнал, связанный с наличием и концентрацией этого вещества. Биосенсоры - позволяют быстро и качественно анализировать сложные, многокомпонентные смеси веществ. В настоящее время биосенсоры находят все более широкое применение в целом ряде отраслей науки, промышленности, сельского хозяйства и здравоохранения.

Как работает биосенсор o o Принцип работы биосенсора достаточно прост: Определяемое вещество диффундирует через полупроницаемую мембрану в тонкий слой биокатализатора, в котором и протекает ферментативная реакция. Поскольку в данном случае продукт ферментативной реакции определяется с помощью электрода, на поверхности которого закреплен фермент, то такое устройство еще называют ферментным электродом. Таким образом, определения "биосенсор" и "ферментный электрод" в данном случае синонимы.

Мировой рынок биосенсоров и биочипов o o Объем мирового рынка биосенсоров и биочипов – составляют около 70 млрд. долларов Объем рынка биосенсорных приборов для измерения глюкозы в крови составляет от 3. 0 до 4. 0 млрд. долларов ежегодно, а в 2002 году, по оценкам экспертов American Diabetes Association, он превысил 4. 7 млрд. долларов, при этом продажи в США составляют 50– 60 %, а в Западной Европе – около 30%.

Применение биосенсоров Примеры: 1. Определение содержания сахара в крови больных диабетом. Для этого прибора используется амперометрический биосенсор на основе иммобилизованной глюкозоксидазы и электрода Кларка. 2. Измерение пищевой ценности, свежести и безопасности продуктов питания 3. Детекция ВВ, ОВ, токсинов и биологического оружия 4. Анализ степени загрязнения окружающей среды и сточных вод

Индустриальный рынок ферментов до 1965 г. был сравнительно небольшим, когда ферменты начали широко использоваться для изготовления различного рода детергентов. В последующие несколько лет промышленное производство ферментов резко возросло. Естественно, увеличивается и мощность производств, выпускающих ферменты и для других целей, например гидролиза крахмала, изомеризации глюкозы во фруктозу, изготовления молочных продуктов (в том числе сыров). Многие ферменты, такие, как протеазы, амилазы, глюкозоизомеразы, производятся десятками тонн, на сумму около 1 млрд. долларов.

Применение иммобилизованных ферментов o o Промышленные процессы с применением иммобилизованных ферментов внедрены прежде всего в пищевую и фармацевтическую промышленность. В пищевой промышленности с участием иммобилизованных ферментов идут процессы получения глюкозо-фруктовых сиропов, глюкозы, яблочной и аспарагиновой кислоты, оптически активных L- аминокислот, диетического безлактозного молока, сахаров из молочной сыворотки и др. В медицине иммобилизованные ферменты используются как лекарственные препараты, особенно в тех случаях, когда необходимо локальное воздействие. Ферменты широко используются в различных аппаратах для перфузионной очистки различных биологических жидкостей.

Промышленные процессы с использованием иммобилизованных ферментов

Роль ферментов в медицине o o o Амилазы, липазы, пепсин, трипсин в виде ферментных препаратов и их смесей применяют для лечения желудочно-кишечного тракта и печени – фестал, панзинорм, мезим и др. Протеазы – для лечения злокачественных новообразований – плазмин. Стрептокиназа и урокиназа – для растворения тромбов в кровеносных сосудах Галактозидаза – для восстановления способности к усвоению молочных продуктов Эластаза – задерживает развитие атеросклероза.

Применение ферментов в качестве лекарственных средств (энзимотерапия): o o o Заменительная терапия и комплексная терапия при недостатке ферментов в организме: желудочно-кишечные заболевания, например, ферменты поджелудочной железы (фестал, энзистал, мезим-форте) Обработка гнойных ран (трипсин, химотрипсин) Лечение тромбозов (фибринолизин) Устранение рубцов после ожогов и операций (лидаза)

Применение ферментов в медицине o Энзимодиагностика – постановка диагноза заболевания на основе определения активности фермента в биологических жидкостях человека (при повреждении клеток в крови или моче увеличивается концентрация внутриклеточных ферментов поврежденных клеток). Диагностика заболеваний сердца, печени, скелетной мускулатуры и др. уровень активности фермента в плазме коррелирует со степенью повреждения клеток
Лекция 9 инженерная энзимология.ppt