химия.pptx
- Количество слайдов: 32

Ферменты «Ферменты – возбудители жизни и первый акт жизненной необходимости» . Академик И. П. Павлов

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература

Ферменты Все процессы в живом организме – дыхание, пищеварение, мышечное сокращение, фотосинтез и другие – осуществляются с помощью ферментов. Ферменты находятся во всех живых клетках и составляют большую часть всех их белков. Они во много миллионов раз ускоряют самые разнообразные химические превращения, из которых складывается обмен веществ. Под действием различных ферментов составные компоненты пищи: белки, жиры и углеводы – расщепляются до более простых соединений, из которых затем в организме синтезируются новые макромолекулы, свойственные данному типу. Все ферменты - белки, но не все белки – ферменты. Ферменты – это высокоспециализированные белки, которые ускоряют химические реакции в клетке, т. е. являются биологическими катализаторами.

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература
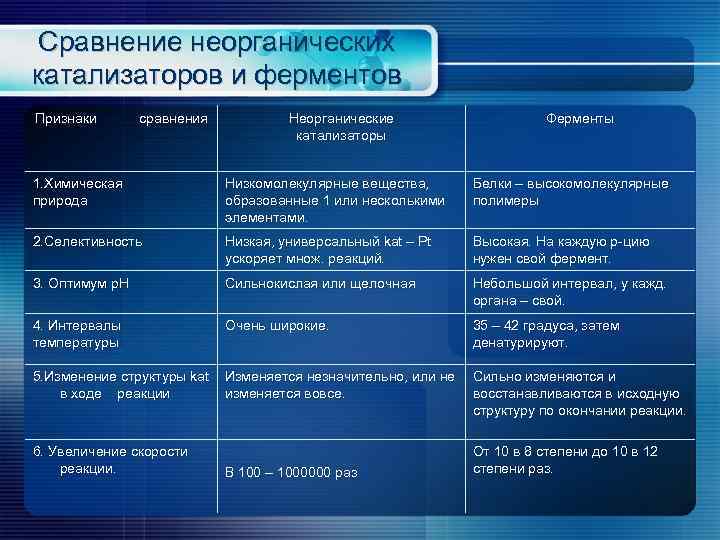
Сравнение неорганических катализаторов и ферментов Признаки сравнения Неорганические катализаторы Ферменты 1. Химическая природа Низкомолекулярные вещества, образованные 1 или несколькими элементами. Белки – высокомолекулярные полимеры 2. Селективность Низкая, универсальный kat – Pt ускоряет множ. реакций. Высокая. На каждую р-цию нужен свой фермент. 3. Оптимум p. H Сильнокислая или щелочная Небольшой интервал, у кажд. органа – свой. 4. Интервалы температуры Очень широкие. 35 – 42 градуса, затем денатурируют. 5. Изменение структуры kat Изменяется незначительно, или не Сильно изменяются и в ходе реакции изменяется вовсе. восстанавливаются в исходную структуру по окончании реакции. 6. Увеличение скорости реакции. В 100 – 1000000 раз От 10 в 8 степени до 10 в 12 степени раз.

Сравнение неорганических катализаторов и ферментов В отличие от неорганических катализаторов действие ферментов строго специфично. Например, фермент лактаза расщепляет только молочный сахар – лактозу – с образованием глюкозы и галактозы. Фермент действует строго на определенный вид связи. На пример реакция расщепления мочевины: О ║ уреаза H 2 N — С — NH 2 + H 2 O 2 NH 3↑ + СО 2↑ Этот пример знаком всем владельцам кошек: мочевина, содержащаяся в моче кошек, разлагается на аммиак и СО 2 - именно аммиаком и пахнет кошачий ящик с песком, если песок долго не меняли. Уреазу образуют бактерии, попадающие в песок из воздуха и начинающие расти и размножаться. За 1 секунду 1 молекула уреазы расщепляет 30. 000 молекул мочевины. Если бы не было уреазы, то на это потребовалось бы 3 млн. лет.

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература

Свойства ферментов • специфичность • способны образовывать промежуточные компоненты (фермент - субстрат) • субстрат комплементарен АЦ фермента • способность утрачивать каталитическую способность под действие факторов среды • свойства фермента связаны со свойствами белка (денатурация + ренатурация) − Общие свойства − Специфические свойства

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература

Общие свойства • способны к растворению в воде и образованию коллоидных растворов; • увеличивают скорость реакции; • не расходуются в реакции; • амфотерны; • их присутствие не влияет на свойства продуктов реакции; • характерно протекание цветных реакций; • изменяют энергию активации, при которой может произойти реакция; • не изменяют сколько-нибудь значительно температуру, при которой происходит реакция; • способны к денатурации и гидролизу.

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература

Специфические свойства • Сочетание высочайшей активности с соблюдением строгого ряда условий; • Специфичность действия по принципу «ключ – замок» или «рука – перчатка» ; • Стабильность; • Обратимость действия: Е + S ↔ ES → E + P, где Е – энзим; S – субстрат; P – продукт реакции; ES – фермент-субстратный комплекс.

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература

Влияние температуры и PH –среды на активность ферментов Активность ферментов лежит в температурном пределе 38 -60°С. С повышением температуры до 70 -80°С активность фермента падает, что связано с изменением природной структуры фермента и разрушением его центров. При повышении температуры более 80°С происходит инактивация фермента вследствие денатурации белка. PН среда влияет на заряд молекулы фермента, а значит на работу АЦ. Оптимальная PН для каждого фермента своя, но для большинства ферментов от 4 до 7. Различные ферменты имеют различное значение РН: • амилаза слюны: РН = 7 (нейтральная среда); • пепсин желудочного сока действует в кислой среде (РН=1, 5 -2, 5), • трипсин кишечного сока имеет РН = 8 -9 (щелочная среда).

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература

Роль ферментов в жизнедеятельности организмов • • • • Врожденные нарушения обмена; Взаимопревращения веществ; Биохимическая революция; Превращение энергии; Биосинтез; Фармакология; Ультраструктура мембран; Генетический аппарат; Питание; Клеточный метаболизм; Катализ; Физиологическая регуляция; Бактериальное брожение.

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература

Номенклатура • В 1961 году специальной комиссией международного биохимического союза была предложена систематическая номенклатура ферментов. Ферменты были подразделены на 6 групп в соответствии с общим типом реакции, которую они катализируют. Каждый фермент получил систематическое наименование, точно описывающее катализируемую им реакцию. Однако, поскольку многие из этих систематических названий оказались очень длинными и сложными, каждому ферменту было присвоено рабочее название для повседневного употребления. • Рабочее название складывалось из названия субстрата, типа катализируемой реакции и окончания –аза. Например: Лактат + дегидрогенизация + аза = лактатдегидрогеназа Но для давно известных ферментов оставлены следующие названия, т. е. прежние названия пепсин, трипсин.

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература

Многообразие ферментов • • В настоящее время известно более 2000 ферментов. Все ферменты разделены на шесть классов, каждый из которых имеет строго определенный номер. Классы ферментов делятся на подклассы, в свою очередь, на подподклассы. Подкласс уточняет действие фермента, так как указывает в общих чертах на природу химической группы субстрата. Подподкласс еще более конкретизирует действие фермента, уточняя природу атакуемой связи субстрата или природу акцептора, который участвует в реакции. Система классификации предусматривает для каждого фермента специальный шифр, состоящий из четырех кодовых чисел, разделенных точками. Первая цифра в шифре обозначает номер класса, вторая — номер подкласса, третья — подподкласса и четвертая — порядковый номер в данном подподклассе. Так, лактатдегидро-геназа имеет шифр КФ 1. 1. 1. 27, т. е. относится к первому классу, первому подклассу, первому подподклассу и занимает 27 -е место в перечне ферментов упомянутого подподкласса.

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература

Классификация

Классификация продолжение

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература
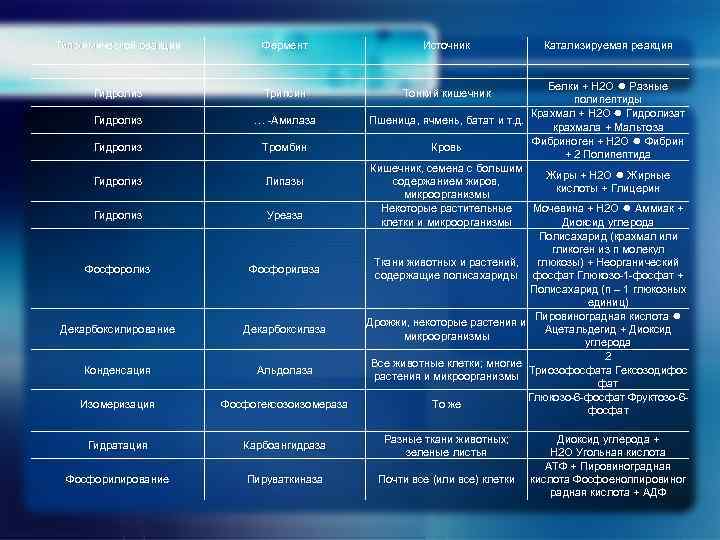
Некоторые ферменты и катализируемые ими реакции Тип химической реакции Фермент Источник Гидролиз Трипсин Гидролиз … -Амилаза Гидролиз Тромбин Гидролиз Липазы Гидролиз Уреаза Фосфоролиз Фосфорилаза Декарбоксилирование Декарбоксилаза Конденсация Альдолаза Изомеризация Фосфогексозоизомераза Гидратация Карбоангидраза Разные ткани животных; зеленые листья Фосфорилирование Пируваткиназа Почти все (или все) клетки Катализируемая реакция Белки + H 2 O Разные Белки + H 2 O полипептиды Крахмал + H 2 O Гидролизат Крахмал + H 2 O Пшеница, ячмень, батат и т. д. крахмала + Мальтоза Фибриноген + H 2 O Кровь + 2 Полипептида Кишечник, семена с большим Жиры + H 2 O Жирные Жиры + H 2 O содержанием жиров, кислоты + Глицерин микроорганизмы Мочевина + H 2 O Аммиак + Некоторые растительные Мочевина + H 2 O клетки и микроорганизмы Диоксид углерода Полисахарид (крахмал или гликоген из n молекул Ткани животных и растений, глюкозы) + Неорганический содержащие полисахариды фосфат Глюкозо-1 -фосфат + Полисахарид (n – 1 глюкозных единиц) Пировиноградная кислота Дрожжи, некоторые растения и Ацетальдегид + Диоксид микроорганизмы углерода 2 Все животные клетки; многие Триозофосфата Гексозодифос растения и микроорганизмы фат Глюкозо-6 -фосфат Фруктозо-6 То же фосфат Тонкий кишечник Диоксид углерода + H 2 O Угольная кислота АТФ + Пировиноградная кислота Фосфоенолпировиног радная кислота + АДФ

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература
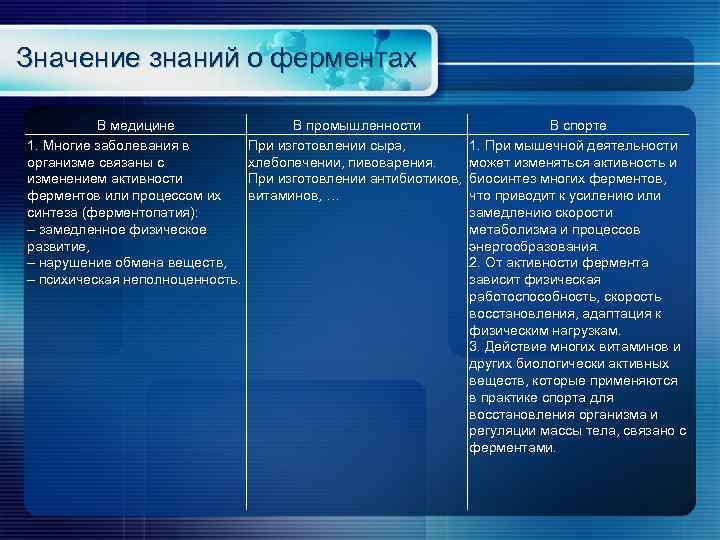
Значение знаний о ферментах В медицине 1. Многие заболевания в организме связаны с изменением активности ферментов или процессом их синтеза (ферментопатия): – замедленное физическое развитие, – нарушение обмена веществ, – психическая неполноценность. В промышленности В спорте При изготовлении сыра, 1. При мышечной деятельности хлебопечении, пивоварения. может изменяться активность и При изготовлении антибиотиков, биосинтез многих ферментов, витаминов, … что приводит к усилению или замедлению скорости метаболизма и процессов энергообразования. 2. От активности фермента зависит физическая работоспособность, скорость восстановления, адаптация к физическим нагрузкам. 3. Действие многих витаминов и других биологически активных веществ, которые применяются в практике спорта для восстановления организма и регуляции массы тела, связано с ферментами.

Значение знаний о ферментах продолжение Энзимология – учение о ферментах, выделено в самостоятельную науку. Ферменты получили широкое применение в легкой, пищевой и химической промышленности, а также в медицинской практике. -В пищевой промышленности ферменты используют приготовлении безалкогольных напитков, сыров, консервов, колбас, копченостей. -В животноводстве ферменты используют приготовлении кормов. -Ферменты используют при изготовлении фотоматериалов. -Ферменты используют при обработке овса и конопли. -Ферменты используют для смягчения кожи в кожевенной промышленности. -Ферменты входят в состав стиральных порошков, зубных паст. -В медицине ферменты имеют диагностическое значение – определение отдельных ферментов в клетке помогает распознаванию природы заболевания (например вирусный гепатит – по активности фермента в плазме крови) их используют для замещения недостающего фермента в организме.

Значение знаний о ферментах продолжение - Достаточно очищенные ферменты применяют в производстве аминокислот и их смесей для искусственного питания, в производстве сахарных сиропов из углеводсодержащего сырья, для удаления лактозы из молока и в производстве ряда лек. средств. Ферменты применяются более чем в 25 отраслях промышленности, медицине, ведутся разработки по применению ферментов для превращения химической энергии в электрическую. И это лишь малая часть того поля деятельности, которое отвел ферментам человек.

Значение знаний о ферментах продолжение Фермент Промышленность Использование _________________________________________ _ Амилазы Пивоваренная Осахаривание содерж. в солоде крахмала (расщепляют Текстильная Удаление крахмала, наносимого на нити во крахмал) время шлихтования Хлебопекарная Крахмал в глюкозу. Дрожжевые клетки сбраживая глюкозу, образуют CO 2 , которые разрыхляют тесто. Протеазы (расщепляют белки) Папаин Пивоваренная Этапы процесса пивоварения, регулирующие количество пены Мясная Мягчение мяса. Фицин Фармацевтическая Добавки к зубным пастам для удаления зубного налета Фотография Смывание желатины с использованной пленки Трипсин Пищевая Произ-во продуктов для детского питания Пепсин Пищевая Произ-во “готовых” каш

План 01. Ферменты 02. Строение ферментов 03. Сравнение неорганических катализаторов и ферментов 04. Свойства ферментов: • общее положение о свойствах ферментов; • общие свойства; • специфические свойства. • влияние t и PH среды 05. Роль ферментов в жизнедеятельности организмов 06. Номенклатура 07. Многообразие ферментов 08. Классификация 09. Некоторые ферменты и катализируемые ими реакции 10. Значение знаний о ферментах. Практическое использование ферментов 11. Использованная литература
Использованная литература Фёршт Э. Структура и механизм действия ферментов. М. , Т. Л. Богданова, Е. А. Солодова. Биология. Справочник для 1980 старшеклассников и поступающих в вузы. Полный курс подготовки к выпускным и вступительным экзаменам. Москва. АСТ – ПРЕСС ШКОЛА. 2004. Ферменты, М. , 1964; Диксон М. , Уэбб Э. , Ферменты, пер. с англ. , М. , 1966; ''Ферменты-двигатели жизни'' (В. И. Розенгарт) Березов Т. Т. Биологическая химия, Москва, 1998 http: //www. erudition. ru/ http: //festival. 1 september. ru/
химия.pptx