ХИМИЯ.pptx
- Количество слайдов: 22

Ферменты. Биологически активные вещества
Определение. Ферменты ( от лат. брожение, закваска), или энзимы, - это органические катализаторы белковой природы, которые ускоряют реакции, необходимые для функционирования живых организмов, включая синтез, распад и взаимопревращение огромного множества разнообразных химических соединений.

История изучения. Термин фермент предложен в XVII веке химиком Ван Гельмонтом при обсуждении механизмов пищеварения. В кон. ХVIII — нач. XIX вв. уже было известно, что мясо переваривается желудочным соком, а крахмал превращается в сахар под действием слюны. Однако механизм этих явлений был неизвестен. В XIX в. Луи Пастер, изучая превращение углеводов в этиловый спирт под действием дрожжей, пришел к выводу, что этот процесс (брожение) катализируется некой жизненной силой, находящейся в дрожжевых клетках. В 1897 году Э. Бухнер опубликовал работу «Спиртовое брожение без дрожжевых клеток» , в которой показал, что бесклеточный дрожжевой сок осуществляет спиртовое брожение так же, как и неразрушенные дрожжевые клетки. В 1907 году за эту работу он был удостоен Нобелевской премии. Впервые высокоочищенный кристаллический фермент (уреаза) был выделен в 1926 году Дж. Самнером. В течение последующих 10 лет было выделено еще несколько ферментов, и белковая природа ферментов была окончательно доказана. Сейчас химикам известно более 2000 ферментов. Все они обладают рядом специфических свойств, отличающих их от неорганических катализаторов.
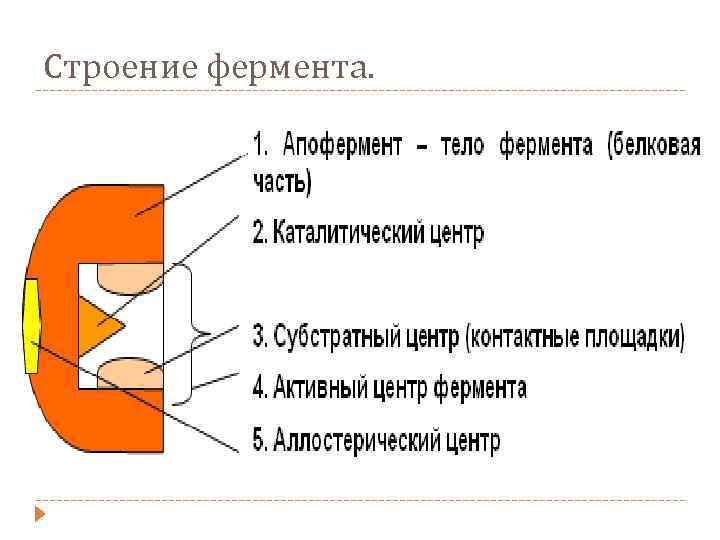
Строение фермента.
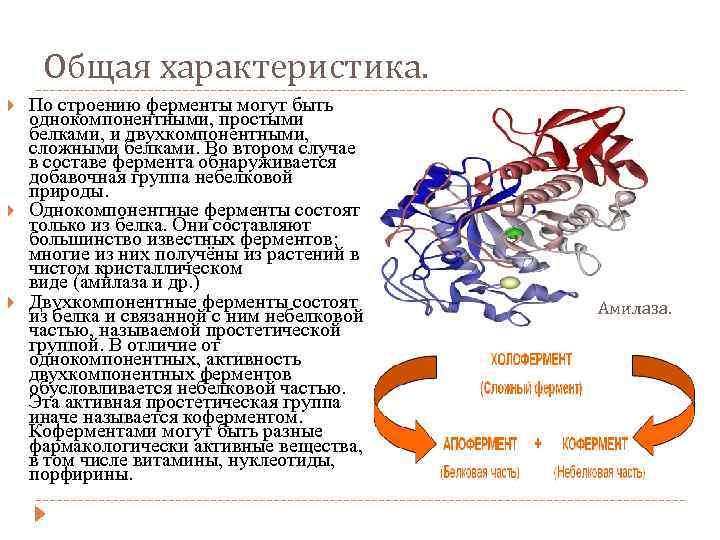
Общая характеристика. По строению ферменты могут быть однокомпонентными, простыми белками, и двухкомпонентными, сложными белками. Во втором случае в составе фермента обнаруживается добавочная группа небелковой природы. Однокомпонентные ферменты состоят только из белка. Они составляют большинство известных ферментов; многие из них получёны из растений в чистом кристаллическом виде (амилаза и др. ) Двухкомпонентные ферменты состоят из белка и связанной с ним небелковой частью, называемой простетической группой. В отличие от однокомпонентных, активность двухкомпонентных ферментов обусловливается небелковой частью. Эта активная простетическая группа иначе называется коферментом. Коферментами могут быть разные фармакологически активные вещества, в том числе витамины, нуклеотиды, порфирины. Амилаза.

Функции Ферментов. Ферменты присутствуют во всех живых клетках и способствуют превращению одних веществ (субстратов) в другие (продукты). Ферменты выступают в роли катализаторов практически во всех биохимических реакциях, протекающих в живых организмах — ими катализируется более 4000 разных биохимических реакций. Ферменты играют важнейшую роль во всех процессах жизнедеятельности, направляя и регулируя обмен веществ организма. Подобно всем катализаторам, ферменты ускоряют как прямую, так и обратную реакцию, понижая энергию активации процесса. Химическое равновесие при этом не смещается ни в прямую, ни в обратную сторону. Большинство ферментов обладает очень высокой эффективностью. Скорость некоторых ферментативных реакций может быть в 1015 раз больше скорости реакций, протекающих в их отсутствие. Такая высокая эффективность ферментов объясняется тем, что их молекулы в процессе «работы» очень быстро восстанавливаются (регенерируют).

Мультиферментные комплексы. В мультиферментном комплексе несколько ферментов прочно связаны между собой в единый комплекс и осуществляют ряд последовательных реакций, в которых продукт реакции непосредственно передается на следующий фермент и является только его субстратом. Благодаря таким комплексам значительно ускоряется скорость превращения молекул. пируватдегидрогеназный комплекс α-кетоглутаратдегидрогеназный комплекс"синтеза жирных кислот" (или пальмитатсинтаза) В ферментативной реакции можно выделить следующие этапы: 1. Присоединение субстрата (S) к ферменту (E) с образованием фермент-субстратного комплекса (E-S). 2. Преобразование фермент-субстратного комплекса в один или несколько переходных комплексов (E-X) за одну или несколько стадий. 3. Превращение переходного комплекса в комплекс фермент-продукт (E-P). 4. Отделение конечных продуктов от фермента.
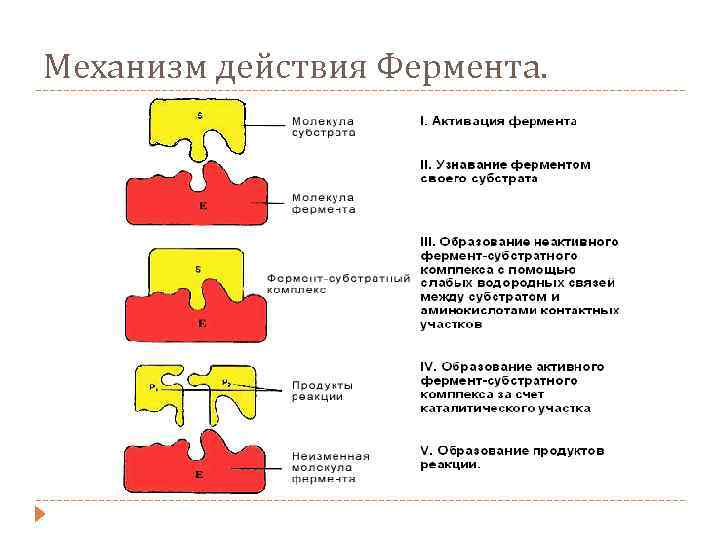
Механизм действия Фермента.
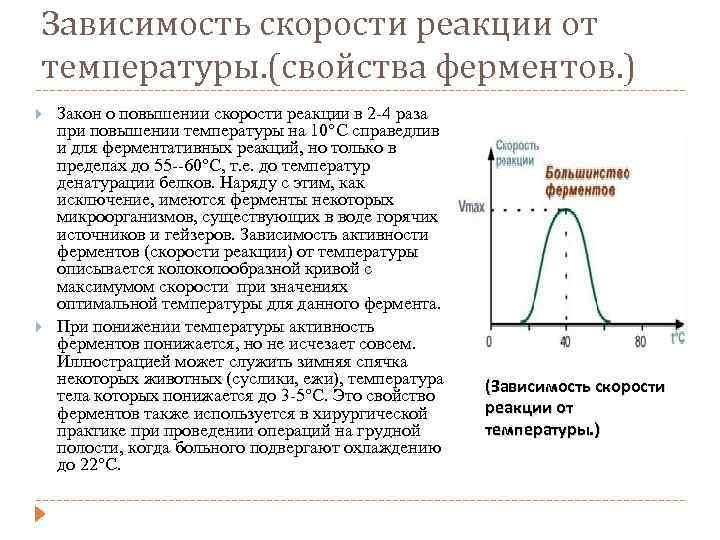
Зависимость скорости реакции от температуры. (свойства ферментов. ) Закон о повышении скорости реакции в 2 -4 раза при повышении температуры на 10°С справедлив и для ферментативных реакций, но только в пределах до 55‑-60°С, т. е. до температур денатурации белков. Наряду с этим, как исключение, имеются ферменты некоторых микроорганизмов, существующих в воде горячих источников и гейзеров. Зависимость активности ферментов (скорости реакции) от температуры описывается колообразной кривой с максимумом скорости при значениях оптимальной температуры для данного фермента. При понижении температуры активность ферментов понижается, но не исчезает совсем. Иллюстрацией может служить зимняя спячка некоторых животных (суслики, ежи), температура тела которых понижается до 3 -5°С. Это свойство ферментов также используется в хирургической практике при проведении операций на грудной полости, когда больного подвергают охлаждению до 22°С. (Зависимость скорости реакции от температуры. )
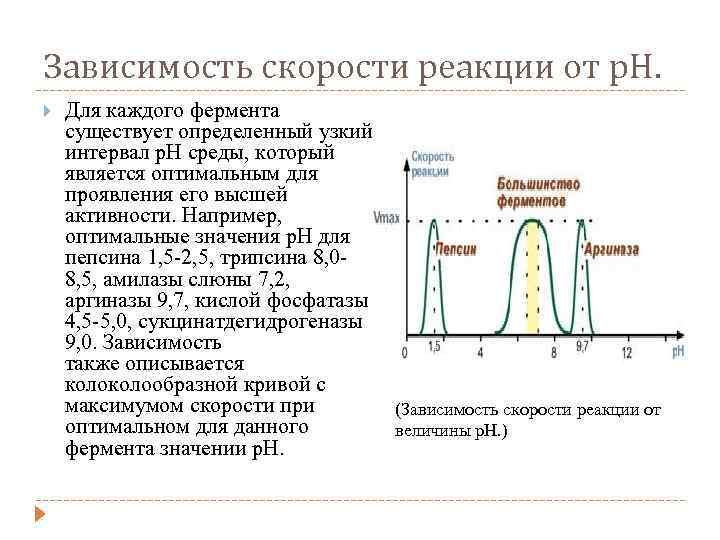
Зависимость скорости реакции от р. Н. Для каждого фермента существует определенный узкий интервал р. Н среды, который является оптимальным для проявления его высшей активности. Например, оптимальные значения р. Н для пепсина 1, 5 -2, 5, трипсина 8, 08, 5, амилазы слюны 7, 2, аргиназы 9, 7, кислой фосфатазы 4, 5‑ 5, 0, сукцинатдегидрогеназы 9, 0. Зависимость также описывается колообразной кривой с максимумом скорости при (Зависимость скорости реакции от оптимальном для данного величины p. H. ) фермента значении р. Н.
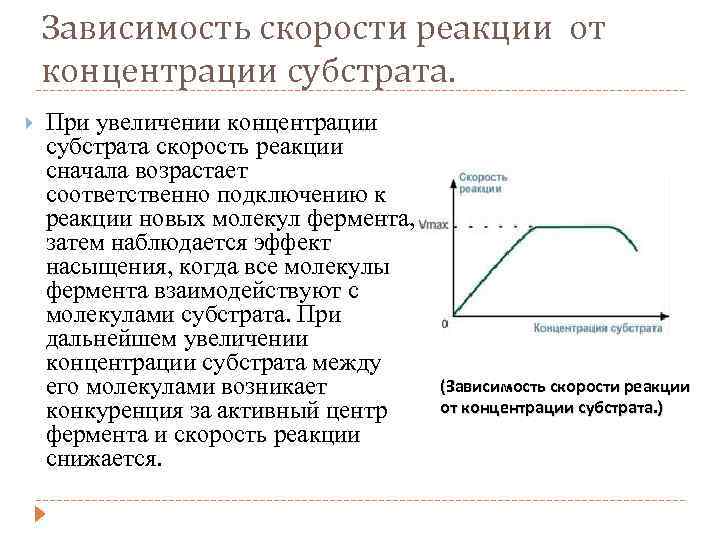
Зависимость скорости реакции от концентрации субстрата. При увеличении концентрации субстрата скорость реакции сначала возрастает соответственно подключению к реакции новых молекул фермента, затем наблюдается эффект насыщения, когда все молекулы фермента взаимодействуют с молекулами субстрата. При дальнейшем увеличении концентрации субстрата между его молекулами возникает конкуренция за активный центр фермента и скорость реакции снижается. (Зависимость скорости реакции от концентрации субстрата. )
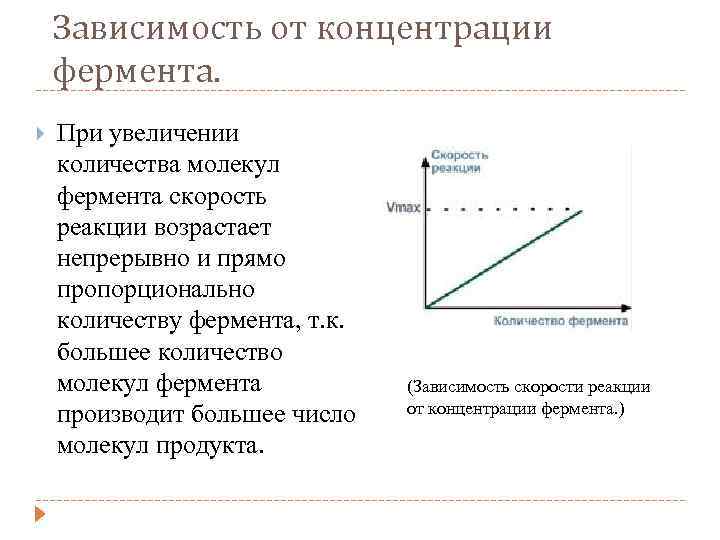
Зависимость от концентрации фермента. При увеличении количества молекул фермента скорость реакции возрастает непрерывно и прямо пропорционально количеству фермента, т. к. большее количество молекул фермента производит большее число молекул продукта. (Зависимость скорости реакции от концентрации фермента. )

Классификация Ферментов. По типу катализируемых реакций ферменты подразделяются на 6 классов согласно иерархической классификации ферментов. Классификация была предложена Международным союзом биохимии и молекулярной биологии. Каждый класс содержит подклассы.
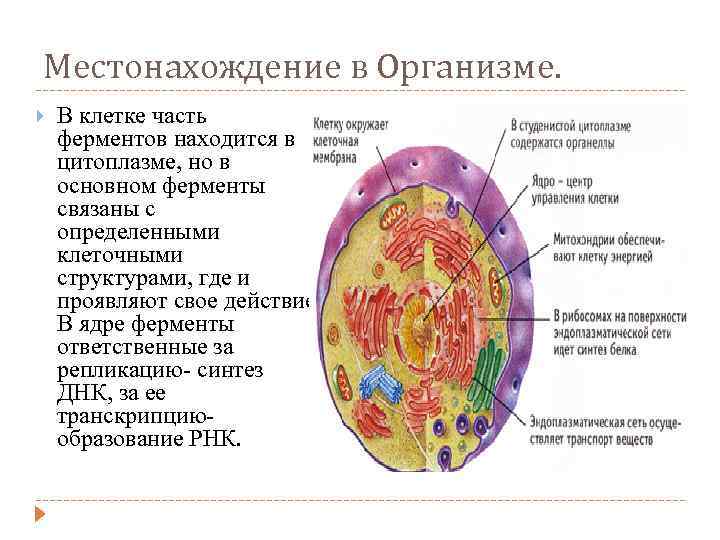
Местонахождение в Организме. В клетке часть ферментов находится в цитоплазме, но в основном ферменты связаны с определенными клеточными структурами, где и проявляют свое действие. В ядре ферменты ответственные за репликацию- синтез ДНК, за ее транскрипциюобразование РНК.
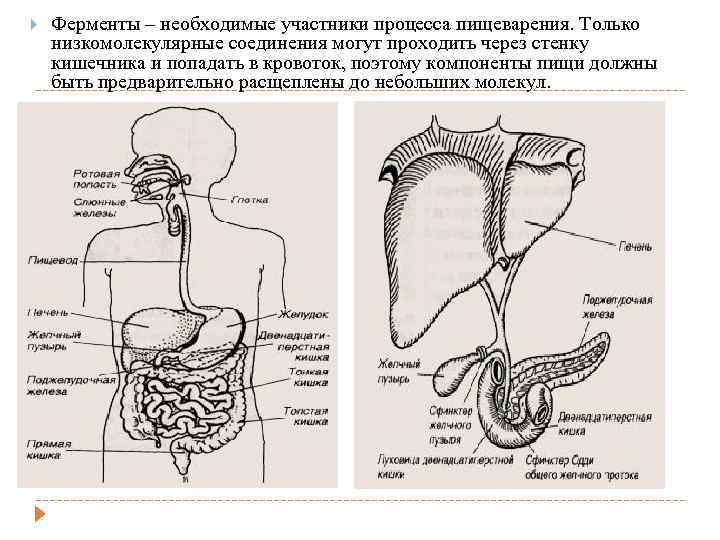
Ферменты – необходимые участники процесса пищеварения. Только низкомолекулярные соединения могут проходить через стенку кишечника и попадать в кровоток, поэтому компоненты пищи должны быть предварительно расщеплены до небольших молекул.

Ферменты необходимы для переваривания пищевых продуктов, стимуляции деятельности головного мозга, процессов энергообеспечения клеток, восстановления органов и тканей. Наиболее важной функцией ферментов является канализация биохимических реакций в организме, многие, если не большинство которых, идут только в присутствии соответствующих энзимов. Функция каждого из ферментов уникальна, т. е. каждый фермент активизирует только один биохимический процесс. В связи с этим в организме существует огромное количество энзимов. В зависимости от того, какие виды реакций организма катализируют ферменты, они выполняют различные функции. Чаще всего их подразделяют на две основные группы: пищеварительные и метаболические. Пищеварительные ферменты выделяются в желудочно-кишечном тракте, разрушают питательные вещества, способствуя их абсорбции в системный кровоток. Различают три основные категории таких ферментов: амилаза протеазы липаза. Амилаза расщепляет углеводы и находятся в слюне, панкреатическом секрете и в содержимом кишечника. Различные виды амилазы расщепляют различные сахара. Протеазы, находящиеся в желудочном соке, панкреатическом секрете и в содержимом кишечника, помогают переваривать белки. Липаза, находящаяся в желудочном соке и панкреатическом секрете, расщепляет жиры.

Продукты богатые ферментами. Для того чтобы организм получил дополнительное количество ферментов, следует или есть продукты, содержащие их, в сыром виде или принимать биологически активные пищевые добавки с такими ферментами. Ферментами богаты продукты растительного происхождения: авокадо папайя ананасы бананы манго ростки.

Практическое использование Ферментов. Ферменты широко используются в народном хозяйстве — пищевой, текстильной промышленности и в фармакологии. Еще шире область использования ферментов в научных исследованиях и в медицине.

Практическое использование Ферментов. Продукты питания, в процессе приготовления которых используют ферменты.

Медицинское значение Ферментов. Связь между ферментами и наследственными болезнями обмена веществ была впервые установлена А. Гэрродом в 1910 -е гг. Гэррод назвал заболевания, связанные с дефектами ферментов, «врожденными ошибками метаболизма» . В настоящее время известны сотни наследственных заболеваний, связанные с дефектами ферментов. Разработаны методы лечения и профилактики многих из таких болезней.

Ферменты в будущем. Будущее ферментов очень интересно. Граница познаний в области ферментов постоянно передвигается вперед. Чем больше получают новой информации, тем больше разрабатывается новых возможностей применения ферментов. Благодаря новым исследованиям в области ферментов медицина и промышленность постоянно движутся вперёд, открывая перед нами новые возможности.

Конец
ХИМИЯ.pptx