Лекция Номенклатура и классификация ферментов.ppt
- Количество слайдов: 42


 Ферментология очень долго не располагала строго научной номенклатурой ферментов. Наименование ферментам давали по: § случайным признакам (тривиальная номенклатура) § названию субстрата (рациональная) § химическому составу фермента § типу катализируемой реакции и характеру субстрата Наибольшее распространение получила рациональная номенклатура. Согласно ей название фермента составляется из названия субстрата и характерного окончания «аза» . Так, фермент, ускоряющий реакцию гидролиза крахмала, получил название амилаза (от греч. амилон - крахмал), гидролиза жиров – липаза (от греч. липос - жир), белков (протеинов) – протеаза, и т. п.
Ферментология очень долго не располагала строго научной номенклатурой ферментов. Наименование ферментам давали по: § случайным признакам (тривиальная номенклатура) § названию субстрата (рациональная) § химическому составу фермента § типу катализируемой реакции и характеру субстрата Наибольшее распространение получила рациональная номенклатура. Согласно ей название фермента составляется из названия субстрата и характерного окончания «аза» . Так, фермент, ускоряющий реакцию гидролиза крахмала, получил название амилаза (от греч. амилон - крахмал), гидролиза жиров – липаза (от греч. липос - жир), белков (протеинов) – протеаза, и т. п.
 В 1961 г. Международная комиссия по номенклатуре ферментов разработала новую научную номенклатуру ферментов. Согласно этой номенклатуре название фермента составляют из химического названия субстрата и названия реакции, осуществляемой ферментом. Если химическая реакция, ускоряемая ферментом, сопровождается переносом группировки атомов от одного партнера (донора) к другому (акцептору), то название фермента включает также химическое наименование акцептора.
В 1961 г. Международная комиссия по номенклатуре ферментов разработала новую научную номенклатуру ферментов. Согласно этой номенклатуре название фермента составляют из химического названия субстрата и названия реакции, осуществляемой ферментом. Если химическая реакция, ускоряемая ферментом, сопровождается переносом группировки атомов от одного партнера (донора) к другому (акцептору), то название фермента включает также химическое наименование акцептора.
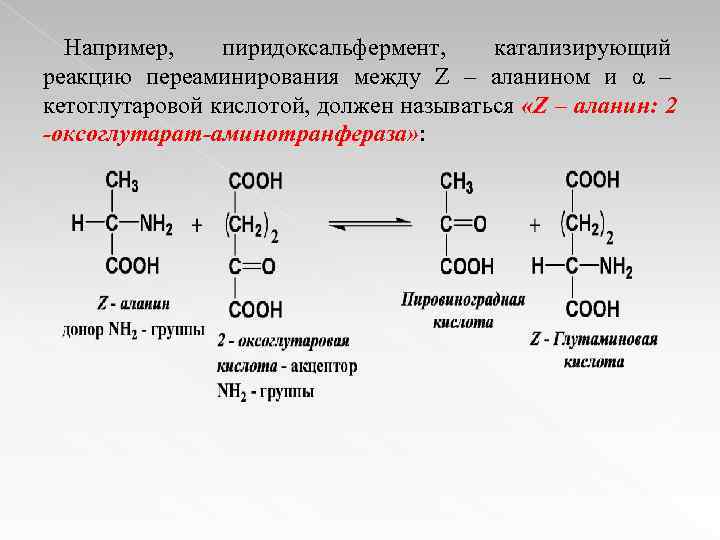 Например, пиридоксальфермент, катализирующий реакцию переаминирования между Z – аланином и α – кетоглутаровой кислотой, должен называться «Z – аланин: 2 -оксоглутарат-аминотранфераза» :
Например, пиридоксальфермент, катализирующий реакцию переаминирования между Z – аланином и α – кетоглутаровой кислотой, должен называться «Z – аланин: 2 -оксоглутарат-аминотранфераза» :
 Классификация ферментов
Классификация ферментов
 В основу современной классификации ферментов положено объединение ферментов в группы по типу катализируемой ими химической реакции. Все ферменты делят на 6 классов: 1. Оксидоредуктазы – ускоряют реакции окислениявосстановления. 2. Транферазы – ускоряют реакции переноса атомных групп и молекулярных остатков. 3. Гидролазы – ускоряют реакции гидролитического распада и синтеза. 4. Лиазы – ускоряют негидролитическое отщепление от субстратов определенных групп атомов с образованием двойной связи (или присоединяют группы атомов по двойной связи). 5. Изомеразы – ускоряют внутримолекулярные превращения. 6. Лигазы – ускоряют реакции синтеза, сопряженные с распадом донаторов энергии.
В основу современной классификации ферментов положено объединение ферментов в группы по типу катализируемой ими химической реакции. Все ферменты делят на 6 классов: 1. Оксидоредуктазы – ускоряют реакции окислениявосстановления. 2. Транферазы – ускоряют реакции переноса атомных групп и молекулярных остатков. 3. Гидролазы – ускоряют реакции гидролитического распада и синтеза. 4. Лиазы – ускоряют негидролитическое отщепление от субстратов определенных групп атомов с образованием двойной связи (или присоединяют группы атомов по двойной связи). 5. Изомеразы – ускоряют внутримолекулярные превращения. 6. Лигазы – ускоряют реакции синтеза, сопряженные с распадом донаторов энергии.

 К классу гидролаз относят ферменты, ускоряющие реакции расщепления (а иногда и синтеза) органических соединений при участии воды: В зависимости от характера субстрата, подвергающегося гидролизу, гидролазы делят на ряд групп.
К классу гидролаз относят ферменты, ускоряющие реакции расщепления (а иногда и синтеза) органических соединений при участии воды: В зависимости от характера субстрата, подвергающегося гидролизу, гидролазы делят на ряд групп.
 Эстеразы Катализируют реакции гидролиза и синтеза сложных эфиров спиртов с органическими и неорганическими кислотами в соответствии с общим уравнением: Важнейшими подгруппами эстераз являются: гидролазы эфиров карбоновых кислот и фосфатазы. Фосфатазы катализируют гидролиз фосфорных эфиров. Особенно широко распространены фосфатазы, действующие на сложные эфиры фосфорной кислоты и углеводов. Примером их может служить глюкозо-1 -фосфатаза:
Эстеразы Катализируют реакции гидролиза и синтеза сложных эфиров спиртов с органическими и неорганическими кислотами в соответствии с общим уравнением: Важнейшими подгруппами эстераз являются: гидролазы эфиров карбоновых кислот и фосфатазы. Фосфатазы катализируют гидролиз фосфорных эфиров. Особенно широко распространены фосфатазы, действующие на сложные эфиры фосфорной кислоты и углеводов. Примером их может служить глюкозо-1 -фосфатаза:

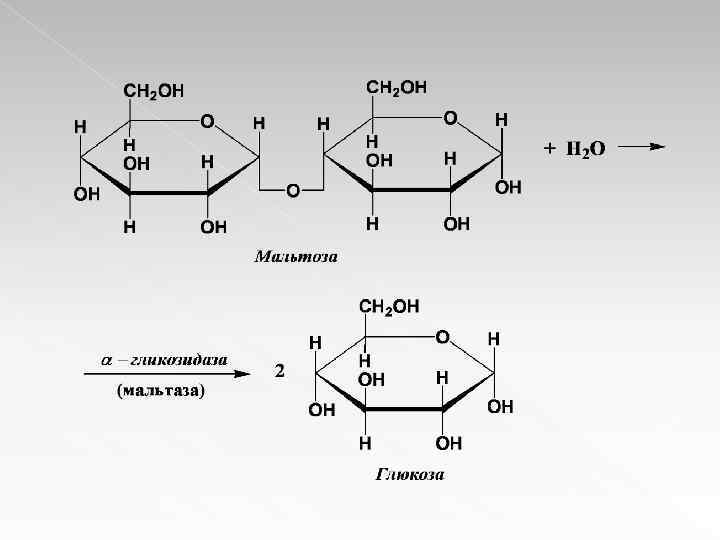
 Гликозидазы Катализируют реакции гидролиза олиго- и полисахаридов. Из гликозидаз, ускоряющих гидролиз полисахаридов, известно несколько различных амилаз. Из гликозидаз, действующих на олигосахариды, хорошо известна α-гликозидаза (мальтаза), ускоряющая гидролиз дисахарида мальтозы (связь α – 1, 4) до глюкозы:
Гликозидазы Катализируют реакции гидролиза олиго- и полисахаридов. Из гликозидаз, ускоряющих гидролиз полисахаридов, известно несколько различных амилаз. Из гликозидаз, действующих на олигосахариды, хорошо известна α-гликозидаза (мальтаза), ускоряющая гидролиз дисахарида мальтозы (связь α – 1, 4) до глюкозы:
 Пептидгидролазы Ускоряют гидролиз пептидных связей в белках и петидах.
Пептидгидролазы Ускоряют гидролиз пептидных связей в белках и петидах.

 В этот класс входят ферменты, ускоряющие реакции переноса органических радикалов или целых молекулярных остатков от одного соединения к другому. В зависимости от характера переносимых атомных группировок различают: § фосфотрансферазы § аминотрансферазы § гликозилтрансферазы § ацилтрансферазы и др.
В этот класс входят ферменты, ускоряющие реакции переноса органических радикалов или целых молекулярных остатков от одного соединения к другому. В зависимости от характера переносимых атомных группировок различают: § фосфотрансферазы § аминотрансферазы § гликозилтрансферазы § ацилтрансферазы и др.
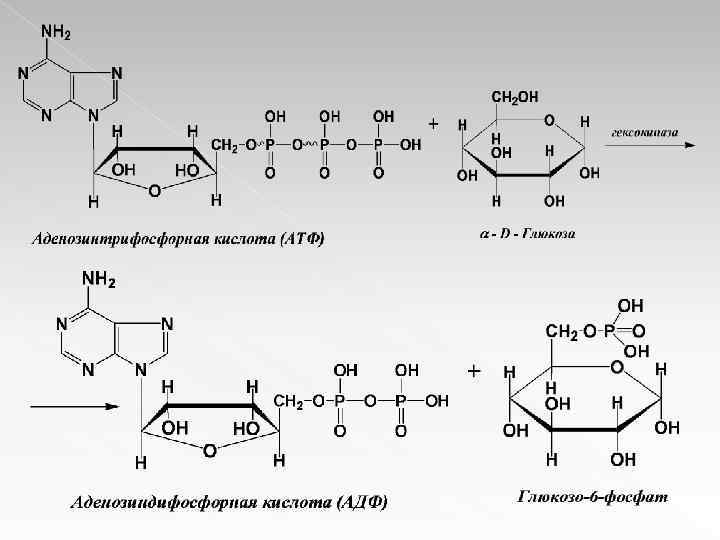
 Фосфотрансферазы Ускоряют перенос остатка фосфорной кислоты. Эти реакции обеспечивают превращение ряда органических соединений в фосфорные эфиры, обладающие повышенной химической активностью и более легко вступающие в последующие реакции. Перенос фосфатных групп идет на спиртовые, карбоксильные, азотсодержащие, фосфорсодержащие и другие группы тех или иных органических соединений. Донор фосфатных остатков - в большинстве случаев аденозинтрифосфорная кислота (АТФ). В качестве представителя фосфотранфераз укажем гексокиназу – фермент, ускоряющий перенос остатка фосфорной кислоты от молекулы АТФ к глюкозе:
Фосфотрансферазы Ускоряют перенос остатка фосфорной кислоты. Эти реакции обеспечивают превращение ряда органических соединений в фосфорные эфиры, обладающие повышенной химической активностью и более легко вступающие в последующие реакции. Перенос фосфатных групп идет на спиртовые, карбоксильные, азотсодержащие, фосфорсодержащие и другие группы тех или иных органических соединений. Донор фосфатных остатков - в большинстве случаев аденозинтрифосфорная кислота (АТФ). В качестве представителя фосфотранфераз укажем гексокиназу – фермент, ускоряющий перенос остатка фосфорной кислоты от молекулы АТФ к глюкозе:
 Аминотрансферазы Ускоряют реакции переаминирования. Очень важны для обеспечения нормального преобразования аминокислот. Аминотранферазы двухкомпонентны: простетической группой их во всех случаях является пиридоксальфосфат. Различные аминотранферазы отличаются друг от друга белковой частью.
Аминотрансферазы Ускоряют реакции переаминирования. Очень важны для обеспечения нормального преобразования аминокислот. Аминотранферазы двухкомпонентны: простетической группой их во всех случаях является пиридоксальфосфат. Различные аминотранферазы отличаются друг от друга белковой частью.
 Гликозилтрансферазы Ускоряют реакции переноса гликозидных остатков из молекул фосфорных эфиров или других соединений к молекулам моносахаридов, полисахаридов или иных веществ. Эти ферменты обеспечивают реакции биосинтеза олигои полисахаридов в животном и растительном мире. Эту группу ферментов называют также фосфорилазами. Перенос гликозильных остатков легко осуществляется ферментами данной группы в тех случаях, когда субстратами являются нуклеозидфосфатсахара – соединения, более богатые энергией, чем фосфорные эфиры сахаров.
Гликозилтрансферазы Ускоряют реакции переноса гликозидных остатков из молекул фосфорных эфиров или других соединений к молекулам моносахаридов, полисахаридов или иных веществ. Эти ферменты обеспечивают реакции биосинтеза олигои полисахаридов в животном и растительном мире. Эту группу ферментов называют также фосфорилазами. Перенос гликозильных остатков легко осуществляется ферментами данной группы в тех случаях, когда субстратами являются нуклеозидфосфатсахара – соединения, более богатые энергией, чем фосфорные эфиры сахаров.
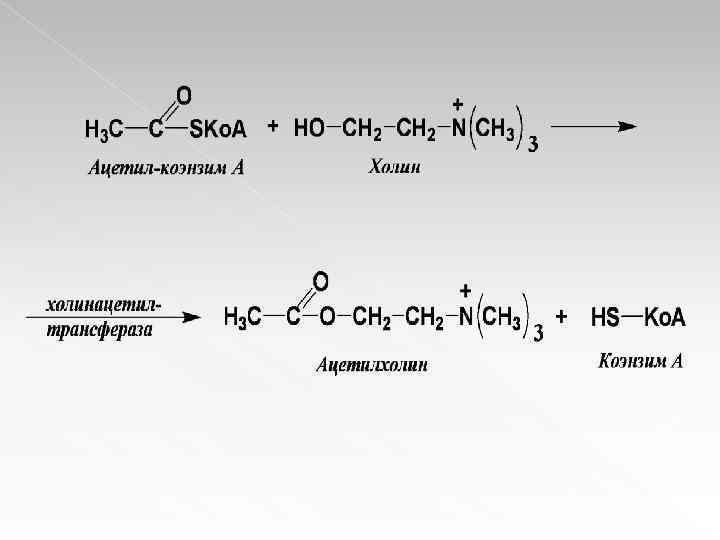
 Ацилтрансферазы Ускоряют перенос ацилов (остатков карбоновых кислот) на аминокислоты, амины, спирты и другие соединения. Универсальный источник ацильных групп – ацил-Ко. А. Чаще всего переносу в биологических объектах подвергается ацил уксусной кислоты – ацетил (СН 3 – С = О). Коэнзим А, соединяясь с ацетильным остатком образует ацетил-коэнзим А, который служит субстратом в соответствующей реакции переноса. В качестве одного из примеров реакции трансацилирования можно привести синтез ацетилхолина:
Ацилтрансферазы Ускоряют перенос ацилов (остатков карбоновых кислот) на аминокислоты, амины, спирты и другие соединения. Универсальный источник ацильных групп – ацил-Ко. А. Чаще всего переносу в биологических объектах подвергается ацил уксусной кислоты – ацетил (СН 3 – С = О). Коэнзим А, соединяясь с ацетильным остатком образует ацетил-коэнзим А, который служит субстратом в соответствующей реакции переноса. В качестве одного из примеров реакции трансацилирования можно привести синтез ацетилхолина:

 К классу оксидоредуктаз относятся ферменты, катализирующие реакции окисления-восстановления. Общая схема их может быть представлена следующим образом: Окисление протекает как процесс отнятия водорода (или электронов) от субстрата, а восстановление – как присоединение водорода (или электрона) к акцептору. Таким образом, оксидоредуктазы являются трансферазами, ускоряющими перенос атомов водорода или электронов от одного вещества к другому.
К классу оксидоредуктаз относятся ферменты, катализирующие реакции окисления-восстановления. Общая схема их может быть представлена следующим образом: Окисление протекает как процесс отнятия водорода (или электронов) от субстрата, а восстановление – как присоединение водорода (или электрона) к акцептору. Таким образом, оксидоредуктазы являются трансферазами, ускоряющими перенос атомов водорода или электронов от одного вещества к другому.
 Различают группы трансфераз: • трангидрогеназ, т. е. ферментов, ускоряющих передачу атомов водрода • трансэлектроназ, т. е. ферментов, ускоряющих процесс передачи электронов от субстрата к акцептору. Трансгидрогеназывают также дегидрогеназами, так как их действие всегда связано со снятием водорода с того или иного субстрата. Различают: – первичную дегидрогеназу (если отнятие водорода непосредственно от окисляемого вещества) – вторичную дегидрогеназу (если отнятие атомов водорода со вторичного субстрата, который получил атомы водорода при посредстве первичной дегидрогеназы)
Различают группы трансфераз: • трангидрогеназ, т. е. ферментов, ускоряющих передачу атомов водрода • трансэлектроназ, т. е. ферментов, ускоряющих процесс передачи электронов от субстрата к акцептору. Трансгидрогеназывают также дегидрогеназами, так как их действие всегда связано со снятием водорода с того или иного субстрата. Различают: – первичную дегидрогеназу (если отнятие водорода непосредственно от окисляемого вещества) – вторичную дегидрогеназу (если отнятие атомов водорода со вторичного субстрата, который получил атомы водорода при посредстве первичной дегидрогеназы)
 Оксидоредуктазы образуют системы (цепи окислительновосстановительных ферментов), в которых осуществляется многоступенчатый перенос атомов водорода или электронов от первичного субстрата к конечномуакцептору. В природных объектах обнаружено около двухсот индивидуальных оксидоредуктаз. Наиболее распространены оксидоредуктазы, содержащие в качестве активной группы никотинамидадениндинуклеотид (НАД). Соединяясь с тем или иным специфическим белком в виде комплекса, который можно сокращенно назвать пиридинпротеином (ПП), НАД резко усиливает свою способность восстанавливаться по ядру никотинамида. Все пиридинпротеины являются анаэробными дегидрогеназами.
Оксидоредуктазы образуют системы (цепи окислительновосстановительных ферментов), в которых осуществляется многоступенчатый перенос атомов водорода или электронов от первичного субстрата к конечномуакцептору. В природных объектах обнаружено около двухсот индивидуальных оксидоредуктаз. Наиболее распространены оксидоредуктазы, содержащие в качестве активной группы никотинамидадениндинуклеотид (НАД). Соединяясь с тем или иным специфическим белком в виде комплекса, который можно сокращенно назвать пиридинпротеином (ПП), НАД резко усиливает свою способность восстанавливаться по ядру никотинамида. Все пиридинпротеины являются анаэробными дегидрогеназами.
 Партнером восстановленной формы пиридинпротеина в окислительной цепи служит флавопротеин (ФП) – оксидоредуктаза, имеющая в качестве простетической группы флавинадениндинуклеотид (ФАД) или флавинмононуклеотид (ФМН).
Партнером восстановленной формы пиридинпротеина в окислительной цепи служит флавопротеин (ФП) – оксидоредуктаза, имеющая в качестве простетической группы флавинадениндинуклеотид (ФАД) или флавинмононуклеотид (ФМН).
 Начало окислительной цепи складывается из двух ферментов-протеинов: пиридинпротеина (ПП) и флавопротеина (ФП). Их взаимодействие с субстратом и друг с другом может быть представлено следующей схемой: В данном случае флавопротеин является вторичной дегидрогеназой. Судьба водорода, передаваемого по системе окислительновосстановительных ферментов, может быть различной.
Начало окислительной цепи складывается из двух ферментов-протеинов: пиридинпротеина (ПП) и флавопротеина (ФП). Их взаимодействие с субстратом и друг с другом может быть представлено следующей схемой: В данном случае флавопротеин является вторичной дегидрогеназой. Судьба водорода, передаваемого по системе окислительновосстановительных ферментов, может быть различной.
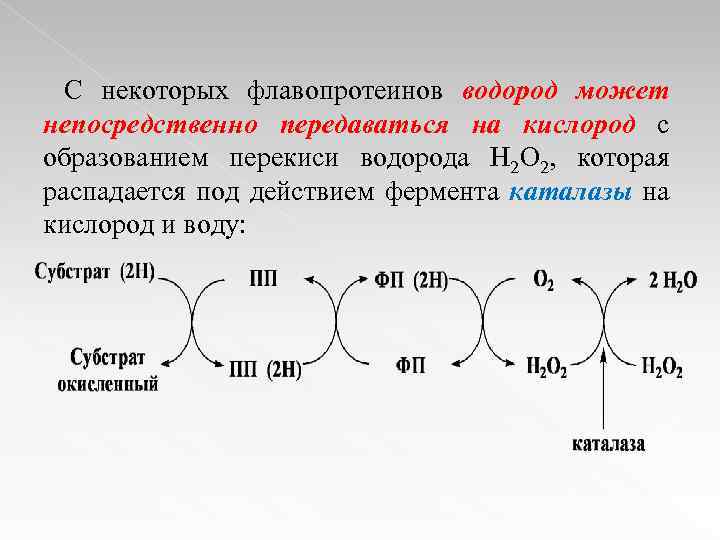 С некоторых флавопротеинов водород может непосредственно передаваться на кислород с образованием перекиси водорода Н 2 О 2, которая распадается под действием фермента каталазы на кислород и воду:
С некоторых флавопротеинов водород может непосредственно передаваться на кислород с образованием перекиси водорода Н 2 О 2, которая распадается под действием фермента каталазы на кислород и воду:
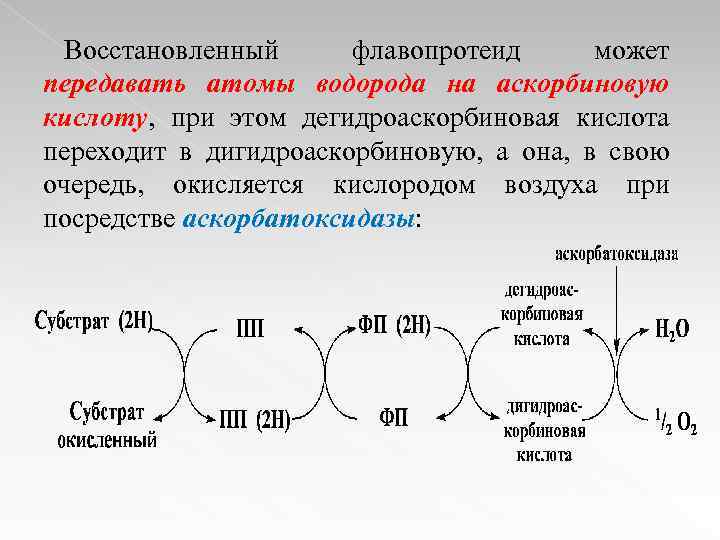 Восстановленный флавопротеид может передавать атомы водорода на аскорбиновую кислоту, при этом дегидроаскорбиновая кислота переходит в дигидроаскорбиновую, а она, в свою очередь, окисляется кислородом воздуха при посредстве аскорбатоксидазы:
Восстановленный флавопротеид может передавать атомы водорода на аскорбиновую кислоту, при этом дегидроаскорбиновая кислота переходит в дигидроаскорбиновую, а она, в свою очередь, окисляется кислородом воздуха при посредстве аскорбатоксидазы:
 Наиболее сложный и важный с энергетической точки зрения путь переноса электронов осуществляется цитохромной системой в составе дыхательной цепи ферментов. Цитохромную систему образуют несколько оксидоредуктаз. В качестве простетической группы – гем – группировку атомов, легко переходящую из окисленного состояния в восстановленное присоединении электрона к атому железа:
Наиболее сложный и важный с энергетической точки зрения путь переноса электронов осуществляется цитохромной системой в составе дыхательной цепи ферментов. Цитохромную систему образуют несколько оксидоредуктаз. В качестве простетической группы – гем – группировку атомов, легко переходящую из окисленного состояния в восстановленное присоединении электрона к атому железа:
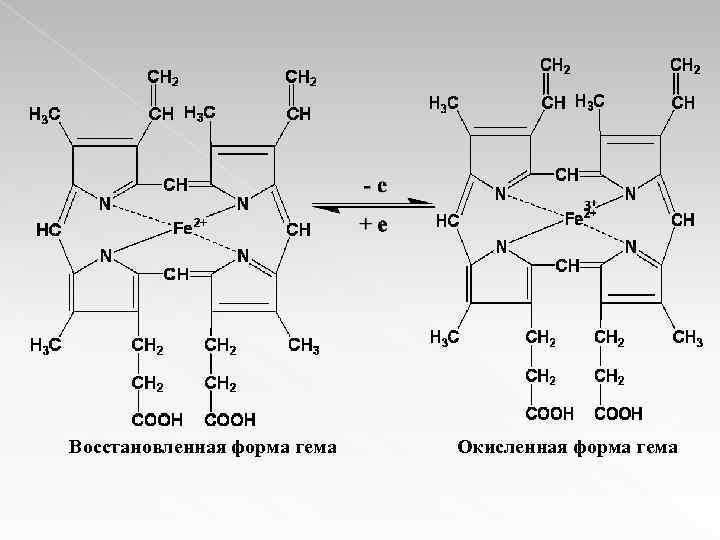 Восстановленная форма гема Окисленная форма гема
Восстановленная форма гема Окисленная форма гема
 В зависимости от характера белковой части фермента различают индивидуальные цитохромы a, b, c, d. Цитохромная система не принимает атомов водорода с восстановленного флавопротеида, но способна принимать электроны, снятые с этих атомов, и передавать их далее по цепи цитохромов и, наконец, на кислородный атом.
В зависимости от характера белковой части фермента различают индивидуальные цитохромы a, b, c, d. Цитохромная система не принимает атомов водорода с восстановленного флавопротеида, но способна принимать электроны, снятые с этих атомов, и передавать их далее по цепи цитохромов и, наконец, на кислородный атом.
 Окисление субстрата при участии дыхательной цепи ферментов можно выразить краткой схемой:
Окисление субстрата при участии дыхательной цепи ферментов можно выразить краткой схемой:
 Энергия выделяющаяся в процессе окисления органических соединений, может либо превращаться в тепло, либо переходить в энергию макроэргических связей аденозинтрифосфорной кислоты (АТФ). Биосинтез АТФ осуществляется из аденозиндифосфорной кислоты (АДФ) и активизированного в процессе биологического окисления неорганического фосфата Н 3 РО 4. Фосфорилирование АДФ, идущее сопряжено с процессами окисления в организме и сопровождающееся образованием АТФ, называется окислительным фосфорилированием.
Энергия выделяющаяся в процессе окисления органических соединений, может либо превращаться в тепло, либо переходить в энергию макроэргических связей аденозинтрифосфорной кислоты (АТФ). Биосинтез АТФ осуществляется из аденозиндифосфорной кислоты (АДФ) и активизированного в процессе биологического окисления неорганического фосфата Н 3 РО 4. Фосфорилирование АДФ, идущее сопряжено с процессами окисления в организме и сопровождающееся образованием АТФ, называется окислительным фосфорилированием.
 К классу лиаз относятся ферменты, ускоряющие реакции негидролитического распада органических соединений по связям: С – С; С – N; С – О и т. д. В подходящих условиях катализируют реакции не только распада, но и синтеза. Важнейшими представителями этого класса ферментов являются декарбоксилазы карбоновых кислот. Характерным представителем лиаз является альдолаза, катализирующая обратимую реакцию расщепления фруктозодифосфата до фосфотриоз.
К классу лиаз относятся ферменты, ускоряющие реакции негидролитического распада органических соединений по связям: С – С; С – N; С – О и т. д. В подходящих условиях катализируют реакции не только распада, но и синтеза. Важнейшими представителями этого класса ферментов являются декарбоксилазы карбоновых кислот. Характерным представителем лиаз является альдолаза, катализирующая обратимую реакцию расщепления фруктозодифосфата до фосфотриоз.

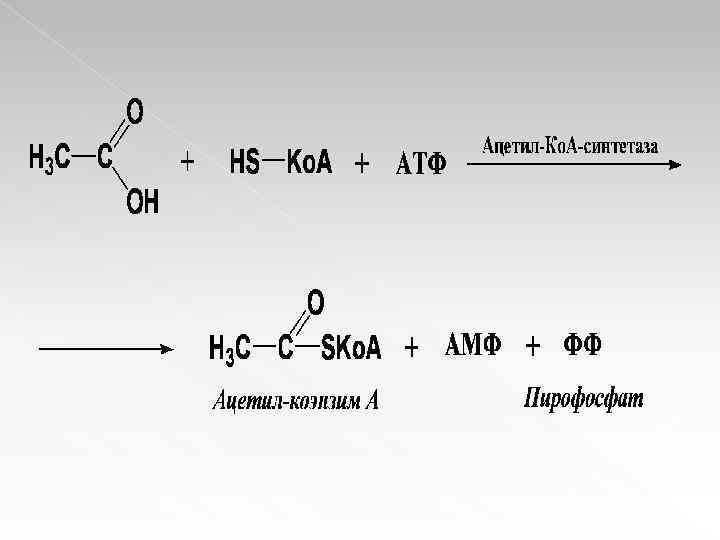
 Характерная черта - сопряженность синтеза с распадом веществ, способных поставлять энергию для осуществления биосинтетического процесса. При отрыве от молекулы АТФ одного или двух концевых остатков фосфорной кислоты выделяется большое количество энергии, используемой для активирования реагирующих веществ. Лигазы каталитически ускоряют синтез органических соединений в присутствии распадающейся АТФ и аналогичных ей соединений Лигазы, катализирующие синтез С – О связей, обеспечивают активирование аминокислот перед вступлением в пептидную связь. Лигазы, катализирующие образования С – S связей, являются ацил-коэнзим-А-синтетазами. В качестве примера можно привести образование ацетил-коэнзима А, протекающее сопряжено с распадом АТФ:
Характерная черта - сопряженность синтеза с распадом веществ, способных поставлять энергию для осуществления биосинтетического процесса. При отрыве от молекулы АТФ одного или двух концевых остатков фосфорной кислоты выделяется большое количество энергии, используемой для активирования реагирующих веществ. Лигазы каталитически ускоряют синтез органических соединений в присутствии распадающейся АТФ и аналогичных ей соединений Лигазы, катализирующие синтез С – О связей, обеспечивают активирование аминокислот перед вступлением в пептидную связь. Лигазы, катализирующие образования С – S связей, являются ацил-коэнзим-А-синтетазами. В качестве примера можно привести образование ацетил-коэнзима А, протекающее сопряжено с распадом АТФ:

 Ферменты, относящиеся к этому классу, ускоряют процессы внутримолекулярных превращений. Превращения могут состоять: • во внутримолекулярном переносе водорода • в переносе фосфатных и ацильных групп • в изменении пространственного расположения атомных группировок • в перемещении двойных связей и т. п. В качестве одного из представителей изомераз отметим триозофосфатизомеразу. Другой фермент – фосфоглицератфосфомутаза – обеспечивает превращение 2 -фосфоглицериновой кислоты в 3 -фосфоглицериновую кислоту и обратно.
Ферменты, относящиеся к этому классу, ускоряют процессы внутримолекулярных превращений. Превращения могут состоять: • во внутримолекулярном переносе водорода • в переносе фосфатных и ацильных групп • в изменении пространственного расположения атомных группировок • в перемещении двойных связей и т. п. В качестве одного из представителей изомераз отметим триозофосфатизомеразу. Другой фермент – фосфоглицератфосфомутаза – обеспечивает превращение 2 -фосфоглицериновой кислоты в 3 -фосфоглицериновую кислоту и обратно.


