Ферменти (96) 19.11.2012 (фон1).ppt
- Количество слайдов: 96
Ферменти

Ферменти (ензими) – це біокаталізатори білкової природи. (К. С. Кірхгоф 1814 р) • ензим” (від грецького en zyme - в дріжджах), • “фермент” (від латинського fermentatio), • Значення ферментів: приймають участь вусіх процесах обміну речовин • реакціях синтезу, • розпаду речовин, • всмоктування, • перетравлювання, • вивільнення енергії, • забезпечують координацію біохімічних реакцій, та в цілому усіх процесів метаболізму

v. Ананьев Г. Б. Ферментные препараты в производстве спирта / Г. Б. Ананьев // Пиво и напитки. – 2000. - № 2. – С. 56. v. Бентли И. Ферменты в пивоварении /И. Бентли // Продукты и ингредиенты. - 2006. - № 9. – С. 24 -26. v. Білько М. Використання ферментних препаратів / М. Білько, В. Гержикова // Харч. і перероб. пром-сть. - 2006. - № 3. – С. 14 -15. v. Грачева И. М. Технология ферментных препаратов: Учеб. / И. М. Грачева, А. Ю. Кривова. -3 -е изд. перераб. и доп. – М. : Елеватор, 2000. - 512 с. v. Исследование биохимических особенностей получения и сбраживания спиртового сусла с использованием ферментных препаратов / Е. А. Цед, С. В. Волкова, Л. М. Королева, А. А. Кузьмина // Пр-во спирта и ликероводоч. изделий. – 2007. – № 4. – С. 27 -29. v. Исследования концентрированных ферментных препаратов в спиртовой промышленности / Н. В. Цурикова, Н. Я. Васильева, К. В. Кобелев, А. Ю. Плохов // Пр-во спирта и ликероводоч. изделий. - 2001. - № 2. – С. 24 -25. v. Калунянц К. А. Микробные ферментные препараты: Технология и оборудование / К. А. Калунянц, Л. И. Голгер. – М. : Пищевая промышленность, 1979. -304 с. v. Камышова Н. В. Новые ферментные препараты для производства сусла и пива / Н. В. Камышова, Е. А. Чернова // Пиво и напитки. - 1996. - № 2. - С. 10. v. Кретович В. Л. Ферментные препараты в пищевой промышленности / В. Л. Кретович. -Под ред. В. Л. Кретовича, В. Л. Яковенко. -М. : Пищевая промышленнность, 1975. -535 с. v. Миронюк С. Ферментні препарати: економічна доцільність, ефективність / С. Миронюк // Харч. і перероб. пром-сть. – 2004. - № 6. - С. 30 -31. v. Никулышина Л. Г. Ферментные препараты концерна Genencor на службе у пивоваров / Л. Г. Никулышина // Пиво и напитки. – 2000. - № 1. -С. 16. v. Плохов А. Ю. Ферментные препараты «Эрбле Гайзенхай. Технологии напитков» / А. Ю. Плохов, Ю. В. Сахаров // Прво спирта и ликероводоч. изделий. – 2001. - № 4. – С. 30 -31. v. Получение комплексного ферментного препарата термостабильной а-милазы и протеазы / Е. В. Костылева, Н. В. Сурикова, Л. И. Нефедова, Л. В. Римарева // Пр-во спирта и ликероводоч. изделий. – 2003. - № 2. - С. 18 -20. v. Римарева Л. В. Использование протеолитического ферментного препарата из Aspergillus oryzal в спиртовом брожении / Л. В. Римарева, М. Б. Оверченко // Пр-во спирта и ликероводоч. изделий. - 2005. - № 4. - С. 12 -14. v. Солярек Л. Эволюция ферментных препаратов «Новозаймс» для производства спирта / Л. Солярек, П. Назарова, Р. Чечнев // Пр-во спирта и ликероводоч. изделий. - 2003. - № 2. – С. 23 -25. v. Тиченко М. Ферментні препарати /М. Тиченко, С. Циганков, А. Новак //Харч. і перероб. пром-сть. – 2004. - № 4. – С. 29 -30. v. Фурсова Т. И. Комплексное влияние ферментных препаратов на степень деструкции полисахаридов зерна кукурузи / Т. И. Фурсова, О. С. Коренева, С. В. Востриков // Пр-во спирта и ликероводоч. изделий. - 2007. - № 4. – С. 36 -38.

v. Ананьев Г. Б. Ферментные препараты в производстве спирта / Г. Б. Ананьев // Пиво и напитки. – 2000. - № 2. – С. 56. v. Бентли И. Ферменты в пивоварении /И. Бентли // Продукты и ингредиенты. - 2006. - № 9. – С. 24 -26. v. Грачева И. М. Технология ферментных препаратов: Учеб. / И. М. Грачева, А. Ю. Кривова. -3 -е изд. перераб. и доп. – М. : Елеватор, 2000. - 512 с. v. Калунянц К. А. Микробные ферментные препараты: Технология и оборудование / К. А. Калунянц, Л. И. Голгер. – М. : Пищевая промышленность, 1979. -304 с. v. Кретович В. Л. Ферментные препараты в пищевой промышленности -М. : Пищевая промышленнность, 1975. 535 с. v. Миронюк С. Ферментні препарати: економічна доцільність, ефективність / С. Миронюк // Харч. і перероб. пром-сть. – 2004. - № 6. - С. 30 -31.

Історія Початок XX ст. Еміль Фішер провів перші систематичні дослідження з вивчення специфічності ферментів 1926 р. вперше отриманий очищений фермент в кристалічному вигляді. уреаза, Джеймсом Самнером який виявив, що кристали уреази повністю складаються з білка в 30 -ті роки, після того як Джон Нортроп та його співробітники отримали в кристалічному вигляді пепсин та трипсин і остаточно було зясовано, що всі ферменти представляють собою білки. роботи І. П. Павлова На сьогодні ідентифіковано понад 2000 ферментів.

Локалізація ферментів у клітині Ферменти виявлено у всіх структурних компонентах клітини. Мітохондрії – протікають аеробні процеси, що забезпечують клітину енергією, тому знаходяться ферменти дихального ланцюга, ферменти циклу Кребса та β-окислення жирних кислот. Ядро – відбувається синтез нуклеотидів та НК, містить ферменти, що відповідають за їх синтез (ДНКполімераза). Рибосоми – ферменти, що каталізують синтез білка. Лізосоми – містять гідролази, оскільки там відбуваються процеси деструкції органічних сполук. Цитоплазма – ферменти гліколізу, біосинтезу ліпідів, вуглеводів, амінокислот.
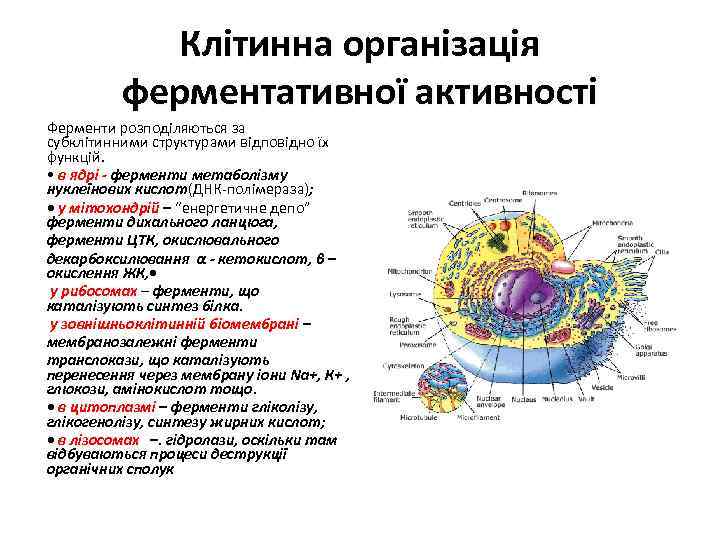
Клітинна організація ферментативної активності Ферменти розподіляються за субклітинними структурами відповідно їх функцій. • в ядрі - ферменти метаболізму нуклеїнових кислот(ДНК-полімераза); • у мітохондрій – “енергетичне депо” ферменти дихального ланцюга, ферменти ЦТК, окислювального декарбоксилювання α - кетокислот, β – окислення ЖК, • у рибосомах – ферменти, що каталізують синтез білка. у зовнішньоклітинній біомембрані – мембранозалежні ферменти транслокази, що каталізують перенесення через мембрану іони Nа+, К+ , глюкози, амінокислот тощо. • в цитоплазмі – ферменти гліколізу, глікогенолізу, синтезу жирних кислот; • в лізосомах –. гідролази, оскільки там відбуваються процеси деструкції органічних сполук

Хімічна природа та структура ферментів. В основному ферменти мають білкову природу, за винятком м-РНК, яка теж володіє ферментативною активністю (Томас Чека 2008 -2010 р). Докази білкової природи: • втрата активності при кип’ятінні, дії У/Ф та Rо– променів, УЗ, кислот, лугів, важких металів; • виділення у формі кришталів; • гідроліз до амінокислот; • осадження висалюванням без втрати каталітичних властивостей; • висока молекулярна маса, амфотерність, здатність до електрофорезу; • штучний синтез рибонуклеази у 1998 році Структура ферментів Ферменти є прості і складні. Прості ферменти складаються тільки з амінокислот (наприклад, гідролази). Складні ферменти - з білкового компонента (апоферменту) та небілкового (кофактора).

Прості ферменти Представлені одним або кількома поліпептидними ланцюгами і при гідролізі розщеплюються до амінокислот. Альбуміни (фермент – естерази печінки) Глобуліни ( ферменти – уреаза та трипсин)

Активний центр- ділянка ферменту, з якою безпосередньо зв’язується субстрат (у ферментів може бути декілька активних центрів 2, 4, 6, 8…. ) в активному центрі розрізняють: каталітичну ділянку –, що безпосередньо вступає в хімічну взаємодію з субстратом контактну (якірну) ділянку, - яка забезпечує специфічну ділянку спорідненість до субстрату та формування його комплексу з ферментом.
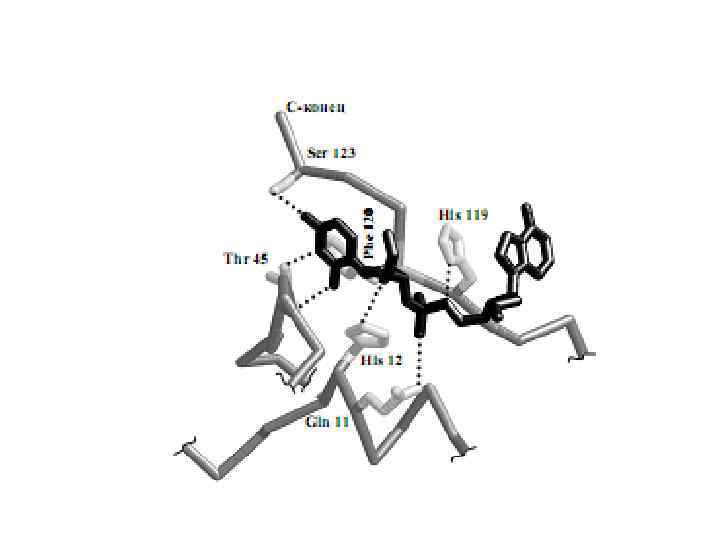

Складні ферменти Такі ферменти крім білкової частини містять групу небілкової природи – кофактор.
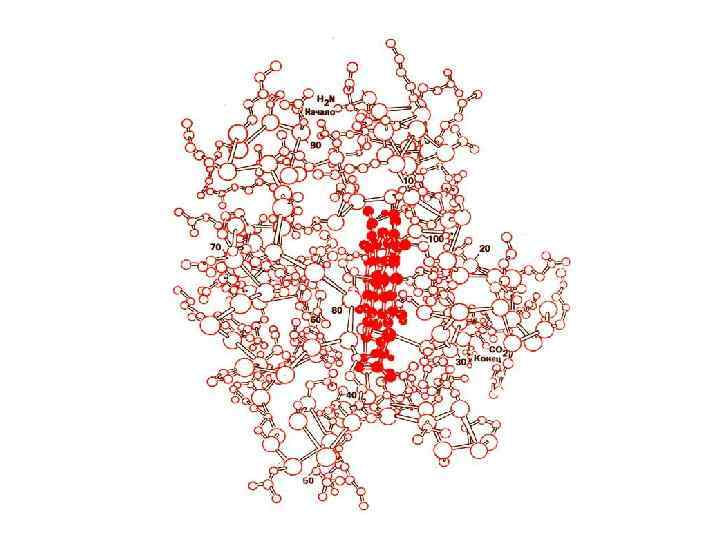

БУДОВА ФЕРМЕНТІВ Білкова частина + небілкова частина = складний фермент Апофермент Кофактор Голофермент Кофактори : коферменти, простетичні групи, активатори Кофактор може бути зв’язаний з апоферментом міцно ковалентими зв’язками. Такий небілковий компонент називається простетичною групою (ФАД; гем (залізовмісна група), яка входить до складу цитохромів, каталаз та пероксидаз Хімічні зв’язки між кофакторами та пептидним ланцюгами можуть бути відносно слабкими. В таких випадках небілковий компонент називається коферментом (НАД, НАДФ, Ко. А-SН, Гл-SН. ) Апофермент зумовлює специфічність дії ферменту
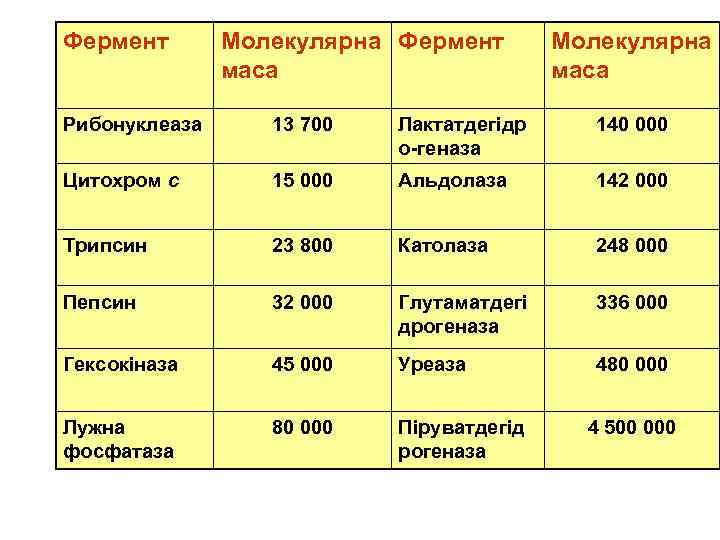
Фермент Молекулярна Фермент маса Молекулярна маса Рибонуклеаза 13 700 Лактатдегідр о-геназа 140 000 Цитохром с 15 000 Альдолаза 142 000 Трипсин 23 800 Католаза 248 000 Пепсин 32 000 Глутаматдегі дрогеназа 336 000 Гексокіназа 45 000 Уреаза 480 000 Лужна фосфатаза 80 000 Піруватдегід рогеназа 4 500 000
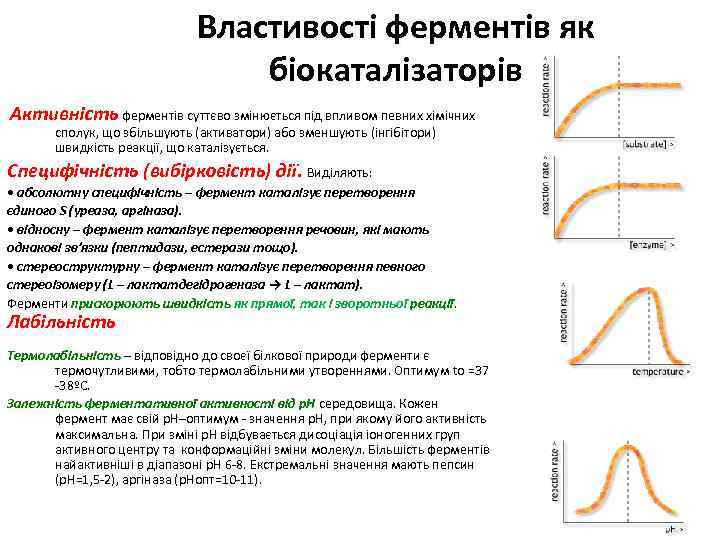
Властивості ферментів як біокаталізаторів Активність ферментів суттєво змінюється під впливом певних хімічних сполук, що збільшують (активатори) або зменшують (інгібітори) швидкість реакції, що каталізується. Специфічність (вибірковість) дії. Виділяють: • абсолютну специфічність – фермент каталізує перетворення єдиного S (уреаза, аргіназа). • відносну – фермент каталізує перетворення речовин, які мають однакові зв’язки (пептидази, естерази тощо). • стереоструктурну – фермент каталізує перетворення певного стереоізомеру (L – лактатдегідрогеназа → L – лактат). Ферменти прискорюють швидкість як прямої, так і зворотньої реакції. Лабільність Термолабільність – відповідно до своєї білкової природи ферменти є термочутливими, тобто термолабільними утвореннями. Оптимум to =37 -38ºС. Залежність ферментативної активності від р. Н середовища. Кожен фермент має свій р. Н–оптимум - значення р. Н, при якому його активність максимальна. При зміні р. Н відбувається дисоціація іоногенних груп активного центру та конформаційні зміни молекул. Більшість ферментів найактивніші в діапазоні р. Н 6 -8. Екстремальні значення мають пепсин (р. Н=1, 5 -2), аргіназа (р. Нопт=10 -11).

Активність. Для ферментів активність, 108, 1020 разів вища за неорганічні каталізатори Е - активність - така кількість ферменту, яка каталітично перетворює 1 мкмоль субстрату (S) за 1 хв. (Умови оптимальні). Існують різні одиниці активності: загальні (стандартні), промислові (спеціальні). • Загальна - стандартна - кількість ферменту, який перетворює 1 мкмоль субстрату за 1 хвилину. • Молярна активність (число обертів) - це число молей субстрату, яке перетворюється 1 молем ферменту за 1 хвилину. • Існує декілька міжнар. одиниць. • Є поняття - число оборотів ферменту - число молекул субстрату перетвореного за 1 хв.

Принципи визначення активності ферментів Øза швидкістю перетворення субстрату; Øза швидкістю накопичення продуктів реакції. Одиниці активності ферментів Одиницею ферменту (U-unit, англ. ) є така кількість ферменту, що каталізує перетворення 1 мк молю S за 1 хв. за оптимальних умов (1 U= 1 мк моль/хв). В системі СІ (SІ) активність виражають в каталах: це така кількість ферменту, яка каталізує перетворення 1 моля S за 1 с. (1 кат. = 1 моль/с). Питома активність визначається кількістю одиниць ферментативної активності на 1 мг білка в біологічному об’єкті (U/мг білка). У медичній ензимології активність ферменту виражають в одиницях (U) на 1 л біологічної рідини (сироватки крові, сечі тощо): U/л.

Розмірність ферментативної активності. Катал - це каталітична активність, яка здійснює хімічне перетворення 1 моля субстрату за 1 с. (мілікаталах – мл-кат, мікрокаталах – мк-кат. ). для порівняння активності різних препаратів одного й того ж ферменту молекулярна активність. - це кількість молекул субстрату, яка перетворюється за 1 хв однією молекулою ферменту. для порівняння активності різних ферментів використовують Число одиниць ферменту, яка припадає на 1 мг білка ферментного препарату, називається питомою активністю. (Одна молекула реніну, створожує близько 106 молекул казеїногену молока за 10 хвилин при 37 С;

В харчовій промисловості активність називають здатністю: q Мольтазна здатність (М 3) - це кількість ферменту, яка розщеплює 1 мг мальтози за 1 годину. q Амілазна здатність (АЗ) - це кількість ферменту, яка розщеплює 1 г крохмалю до декстринів, які не забарвлюються йодом. q Інвертазна здатність - це кількість ферменту, яка розкладає 1, 25 г сахарози за 1 хвилину. q Протеолітична здатність (ПЗ) - це кількість фермента, яка утворює 1 мг амінного азоту за 1 годину

Специфічність. В залежності від механізму дії розрізняють ферменти з абсолютною, груповою та стереохімічною специфічністю. q Абсолютна - характерна для ферментів, які каталізують лише одну реакцію і діють на один точно визначений субстрат. Наприклад, уреаза діє лише на сечовину і не діє на похідні сечовини, напр. метилсечовину; аргіназа, розщепляє аргінін. q Абсолютно групова специфічність – здатність ферментів діяти на певний тип хімічного звязку, утворений певними радікалами (атомними групами). q Відносно групова специфічність (специфічність за типом звязку) – здатність ферменту діяти на певний тип хімічного звязку, утворений радікалами будь-якої хімічної будови. q Оптична або стереохімічна специфічність – здатність ферменту діяти лише на одину стереоізомерну форму субстрату.

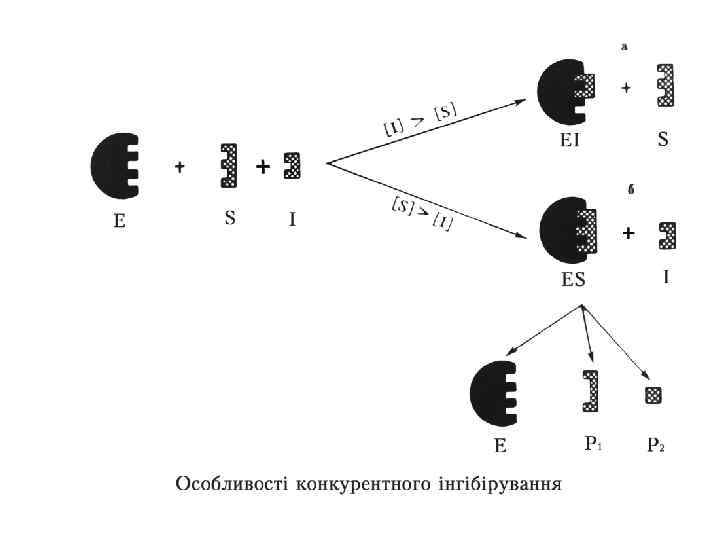
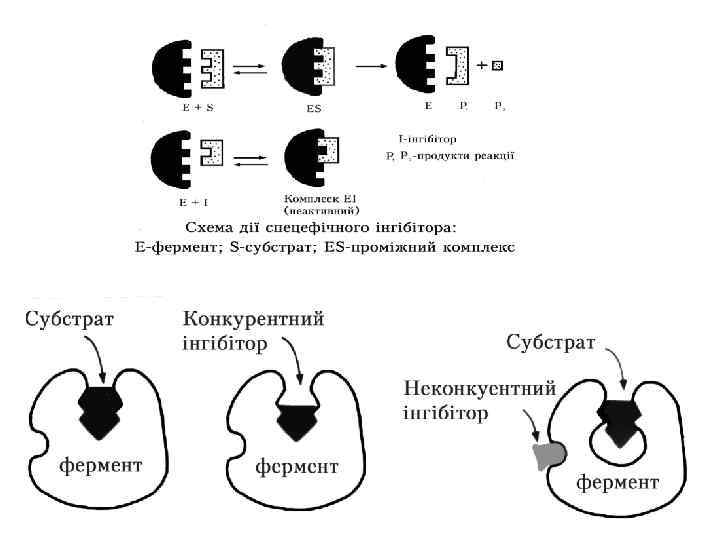
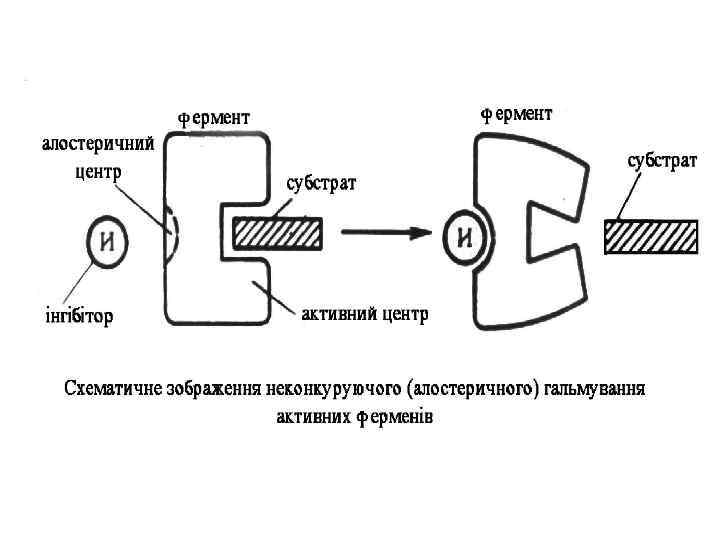
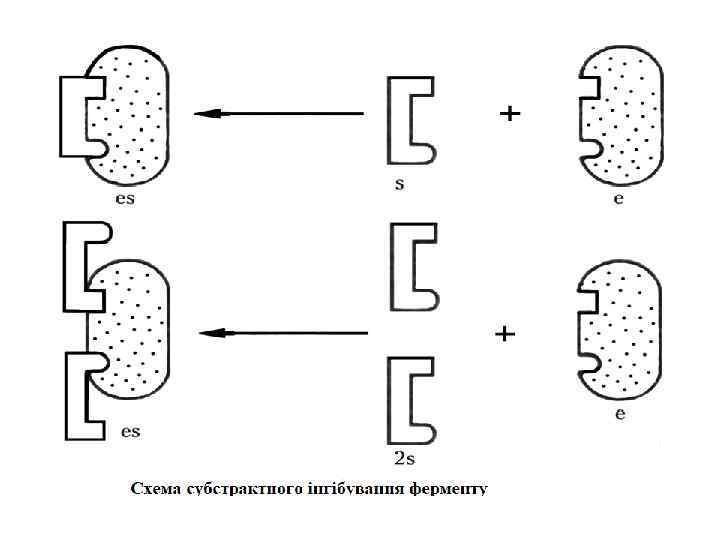
ЕФЕКТОРИ Активатори - катіони металів і деякі аніони , мінеральні кислоти (НСl), жовчні кислоти, деякі сполуки з функціональними групами (цистеїн, глютатіон), ферменти (ентерокіназа, трипсин Інгібітори – (білкові осаджувачі — ССl 3 СООН, танін, концентровані кислоти, солі важких металів та ін. ). Інгібірування буває оборотним і необоротним. Оборотне – це коли інгібітор утворює з ферментом слабкий комплекс. Необоротне – інгібітор міцно зв’язаний з ферментом (малі концентрації іонів важких металів (ртуть, срібло, миш’як, йод, оцтова кислота). Оборотне інгібірування поділяють ще (за спорідненістю до субстрату) – конкурентне, неконкурентне. Конкурентне – це коли інгібітор має структуру подібну до структури субстрату, Неконкурентне – це коли інгібітори взаємодіє з важливими функціональними групами. ферменту, які не відносяться до активного центру. Ця ділянка ферменту називається алостеричний центр. Такий тип гальмування каталітичної активності назву алостеричного інгібуванням. Ділянка молекули ферменту, з якою зв’язуються ефектори, називається алостеричинм центром.

Активатори та інгібітори ферментів • Активатори – це ферменти що підвищують активність ферментів. • Інгібітори – це ферменти що знижують активність ферментів

Активатори – бувають органічної та неорганічної природи. Органічної природи: q жовчні кислоти (активують підшлункову ліпазу в кишечнику); q ентерокіназа (активує трипсиноген). qглутатіон, цистеїн, вітамін С підвищують активність оскидоредуктаз. Неорганічної природи: q. HCl активує пепсиноген; qіони металів 1 та 2 -х валентні (Na, Cl, K, Mg, Mn, Zn); Роль металів: • сприяють утворенню фермент-субстратного комплексу; • є донорами та акцепторами електронів; • беруть участь в утворенні активного центру ферментів (Zn → в карбоангідразі, Fe → у цитохромах); • виступають в ролі алостеричних регуляторів

Глютатіон

Мультиферменти Це надмолекулярні комплекси з різних ферментів та коферментів, що каталізують послідовні етапи перетворення субстрату. Прикладами дії мультиферментів є реакції окислювального декарбоксилювання Біологічне значення мультиферментів: скорочується відстань між реагуючими речовинами і зменшується (час) тривалість реакції
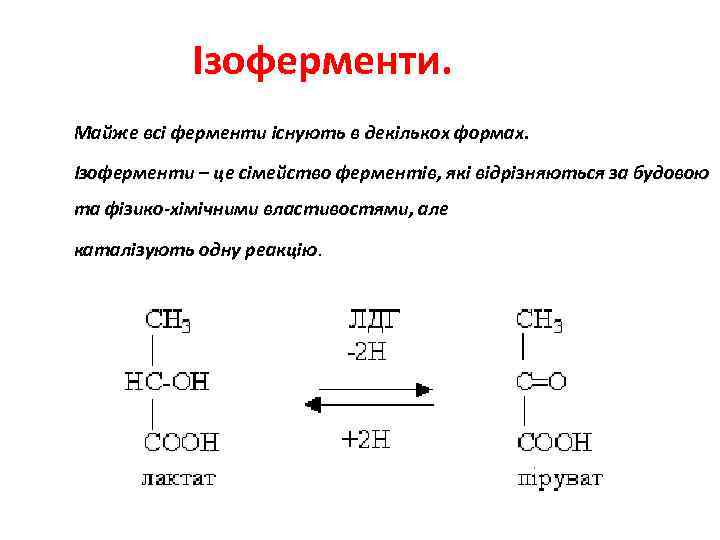
Ізоферменти. Майже всі ферменти існують в декількох формах. Ізоферменти – це сімейство ферментів, які відрізняються за будовою та фізико-хімічними властивостями, але каталізують одну реакцію.

Механізм дії ферментів Взаємодія фермента з субстратом відбувається за законом комплементарності конфігурації активних центрів, конформації та зарядів. В процесі взаємодії виділяють 5 етапів: • Приєднання ферменту до S з утворенням ферментсубстратного комплексу; • Квантово – механічні зрушення, що приводять до послаблення зв’язків; • Розрив, або утворення зв’язків; • Зміна конфігурації субстрату, він не відповідає активному центру фермента; • Вивільнення продуктів реакції від ферменту. Поняття про “енергію активації” та “енергетичний бар’єр” Ферменти прискорюють хімічну реакцію за рахунок зниження енергії активації. Енергія активації – це енергія для переведення всіх молекул в активований стан. Енергетичний бар’єр – енергія, яку небхыдно подолати молекулам, щоб вступити в хімічну взаємодію. Фермент знижує енергетичний бар’єр. Величина енергії активації дорівнює величині енергетичного бар’єру.

Регуляція ферментативної активності q на генетичному рівні: за рахунок конститутивних ферментів, що синтезуються завжди згідно генетичного коду; q на адаптивному (індуцибельному), що синтезуються за умов надходження субстрату. напрямок реакції, у відповідності до закону діючих мас: зміщується у бік речовин з меншою концентрацією. Перетворення проферменту в активний фермент. Øза принципом зворотного зв’язку (ретрогальмування): кінцевий продукт послідовних стадій перетворення певного субстрату гальмує перший фермент. Øхімічною модифікацією ферменту: здебільшого фосфорилюванням. Øшвидкістю синтезу та розпаду субстрату. Øпід дією активаторів та інгібіторів. Øшляхом компартменталізації (англ. compartmentation — відділення) регуляція хімічних перетворень відбувається за участю біомембран. Наприклад: мембрани лізосом обмежують активність лізосомальних гідролаз.
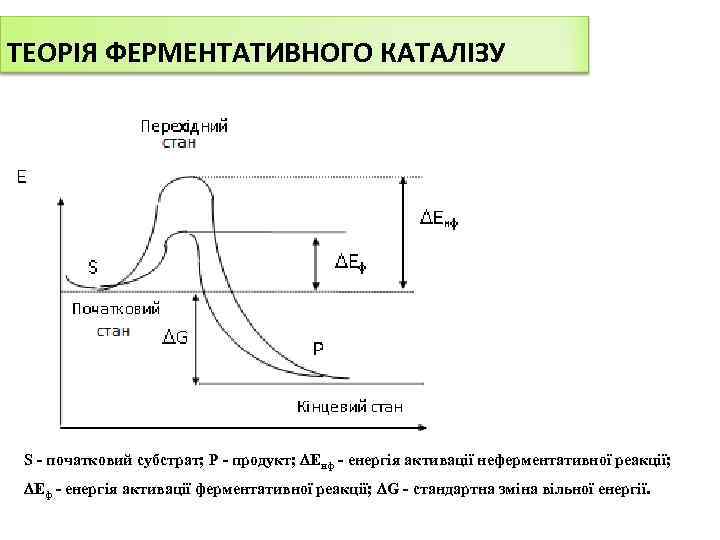
ТЕОРІЯ ФЕРМЕНТАТИВНОГО КАТАЛІЗУ S - початковий субстрат; Р - продукт; Енф - енергія активації неферментативної реакції; Еф - енергія активації ферментативної реакції; G - стандартна зміна вільної енергії.

Основна роль у механізмі ферментативного каталізу належить фермент-субстратним комплексам. теорія (гіпотеза) Фішера“ключа та замка” 1890 р. : теорія (гіпотеза) Кошланда індукованої відповідності, або “руки та рукавички”. 1959 р, (субстрат, з’єднуючись з ферментом, викликає зміну в структурі останнього. ) Розділ ензимології про швидкість ферментативних реакцій та її залежність від різних факторів вивчає ферментативна кінетика

Кінетика ферментативних реакцій Міхаеліс та Ментен розробили загальну теорію ферментативної кінетики, яка вбражає кількісне співвідношення між концентрацією субстрату та швидкістю ферментативної реакції: v=vmax[S] /(Ks + [S]), де v - швидкість реакції при даній концентрації субстрату[S], vmax - максимальна швидкість реакції при повному насиченні ферменту субстратом; Ks - константа дисоціації фермент-субстратного комплексу, моль/л. Ks = k-1/ k+1 З рівняння Міхаеліса–Ментен витікає, що: за високої концентрації субстрату та низькому значенні Ks швидкість реакції є максимальною, тобто v=vmax, при низькій концентрації субстрату, навпаки, швидкість реакції виявляється пропорційною концентрації субстрату в кожний даний момент.

Рівняння Міхаеліса - Ментен в його класичному вигляді не враховує впливу на швидкість ферментативного процесу продуктів реакції, тому Бріггс та Холдейн вдосконалили це рівняння: v=vmax[S] /( Кm + [S]), Km = (k-1 + k+2)/ k+1, або Km = ks + k+2/ k+1 константа Міхаеліса – це така концентрація субстрату, за якої швидкість даної ферментативної реакції відповідає половині максимальної v vmax ½ vmax Km [S]

Конкурентне інгібування

Неконкурентне інгібування

Класифікація і номенклатура ферментів Ферменти мають тривіальні та системні. назви Назви багатьох ферментів утворюються шляхом додавання суфіксу -аза до назви субстрату. Тому в 1961 році на V Міжнародному біохімічному конгресі в Москві Комісією з ферментів Міжнародної біохімічної спілки була розроблена сучасна класифікація та номенклатура ферментів. В основу прийнятої класифікації був покладений тип каталізованої реакції, який є специфічним для дії будь-якого ферменту. Таким чином, тип реакції разом з назвою субстрату і є основою для системної назви ферментів.

Міжнародна комісія з ферментів у 1961 р. принцип класифікації ферментів за типом хімічної реакції

Класифікація ферментів 1. Оксидоредуктази 2. Трансферази 3. Гідролази 4. Ліази 5. Ізомерази 6. Лігази

Характеристика окремих класів ферментів 1 КЛАС Оксидоредуктази каталізують окисновідновні процеси -(дегідрогенази, оксигенази, оксидази, пероксидази, гідроксилази, та ін. ) 19 підкласів Небілковою частиною дегідрогеназ є у більшості випадків динуклеотиди. Залежно від виду динуклеотиду дегідрогенази поділяються на піридинові та флавінові.
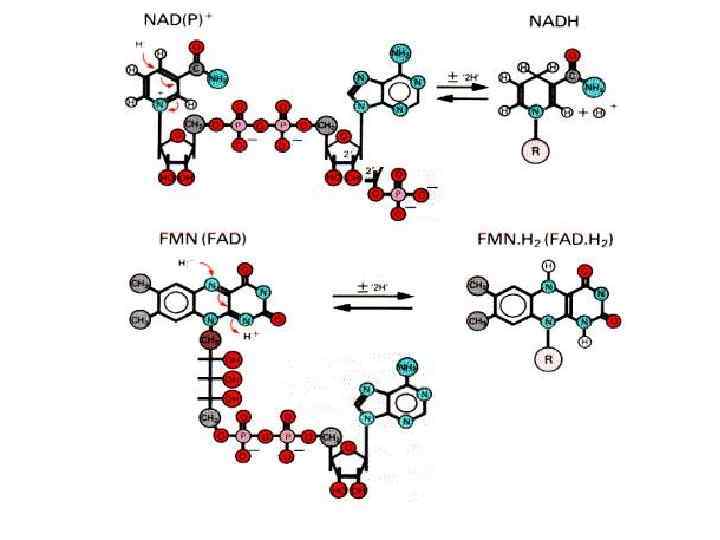
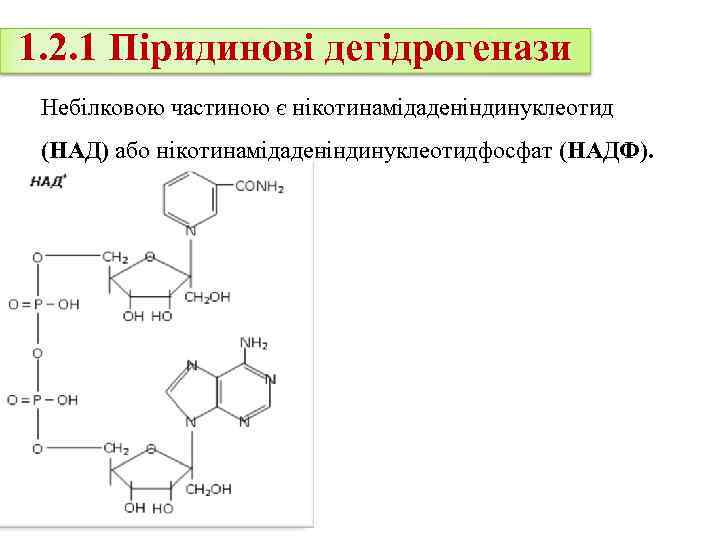
1. 2. 1 Піридинові дегідрогенази Небілковою частиною є нікотинамідаденіндинуклеотид (НАД) або нікотинамідаденіндинуклеотидфосфат (НАДФ).
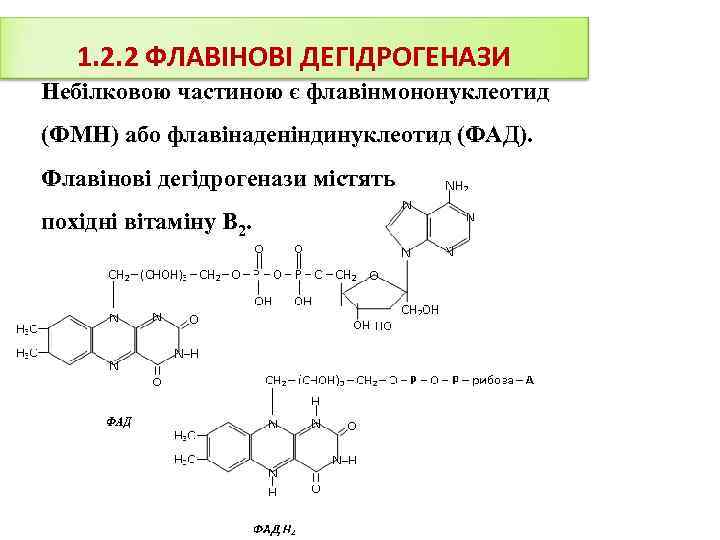
1. 2. 2 ФЛАВІНОВІ ДЕГІДРОГЕНАЗИ Небілковою частиною є флавінмононуклеотид (ФМН) або флавінаденіндинуклеотид (ФАД). Флавінові дегідрогенази містять похідні вітаміну В 2.

Реакції що відбуваються за участі піридинзалежних дегідрогеназ: Субстрат - Н 2 + НАД+=субстрат + НАД. Н + Н+ Піридинові дегідрогенази, активною групою яких є НАД беруть участь у спиртовому бродінні (алкогольдегідрогеназа), молочнокислому бродінні (лактатдегідрогеназа). Важливе значення мають ферменти в діагностиці різних захворювань. Зміна їх активнсті в крові порівняно з нормою є важливим показником патологічних змін в організмі. Наприклад: підвищення активності креатинкінзи та лактатдегідрогенази у перші часи захворювання на інфаркт, коли ще ЕКГ не помічає ніяких змін, вже свідчить про початок хвороби.

1. 2 Оксигенази - oxygenases Ферменти, за допомогою яких відбувається пряме приєднання одного або двох атомів кисню до органічного субстрату. В цих реакціях кисень відновлюється до води (H 2 O) або пероксиду водню (H 2 O 2). Цитохроми (система, яка складається з ряду геммісних білків (гемопротеїнів). здійснюють перенесення електронів (Fe 2+ ↔ Fe 3+) цитохром b цитохром с цитохром а 3 цитохроми b, с переносники електронів, а а, а 3 (цитохромоксидаза) термінальний дихальний фермент, безпосередньо взаємодіє з киснем.

1. 2 Оксигенази - oxygenases Ферменти, за допомогою яких відбувається пряме приєднання одного або двох атомів кисню до органічного субстрату. В цих реакціях кисень відновлюється до води (H 2 O) або пероксиду водню (H 2 O 2). Цитохроми (система, яка складається з ряду геммісних білків (гемопротеїнів). здійснюють перенесення електронів (Fe 2+ ↔ Fe 3+) цитохром b цитохром с цитохром а 3 цитохроми b, с переносники електронів, а а, а 3 (цитохромоксидаза) термінальний дихальний фермент, безпосередньо взаємодіє з киснем.

1. 3 Оксидази - коли субстратом (акцептором O 2) служить водень. . Ліпоксигеназа (ліпоксидаза) широко розповсюджений у рослинах, каталізує окислення киснем повітря деяких ненасичених ВЖК та утворених ними ефірів. Присутні в насінні рослин ліпоксигенази обумовлюють згіркнення борошна та круп

1. 4 Гідрогенази – ферменти, що каталізують оборотне окислення водню за участю ферредоксину, НАД+ або цитохрому с3. Пероксидаза – ферменти, що каталізують окислення органічних сполук пероксидом водню. Каталаза – фермент під дією якого відбувається розклад пероксиду водню на воду і молекулярний кисень: 2 Н 2 О 2 2 Н 2 О + О 2

Згідно з міжнородною класифікацією оксидоредуктаз виділяють 22 підкласи: КФ 1. 1 — ферменти, що взаємодіють з CH—OH—групою донорів; КФ 1. 2 — ферменти, що взаємодіють з альдегідною або окси-групою донорів; КФ 1. 3 — ферменти, що взаємодіють з CH—CH—групою донорів; КФ 1. 4 — ферменти, що взаємодіють з CH—NH 2 групою донорів; КФ 1. 5 — ферменти, що взаємодіють з CH—NH групою донорів; КФ 1. 6 — ферменти, що взаємодіють з НАД · H або НАДФ · H; КФ 1. 7 — ферменти, що взаємодіють з іншими азотмістними сполуками в якості донорів; КФ 1. 8 — ферменти, що взаємодіють з сіркомістною групою донорів; КФ 1. 9 — ферменти, що взаємодіють з гемовою групою донорів; КФ 1. 10 — ферменти, що взаємодіють з дифенолами та спорідненими сполуками в якості донорів; КФ 1. 11 — ферменти, що взаємодіють з пероксидом в якості акцептора (пероксидази); КФ 1. 12 — ферменти, що взаємодіють з воднем в якості донорів; КФ 1. 13 — ферменти, що взаємодіють з одиночними кисневмісними донорами (оксигенази); КФ 1. 14 — ферменти, що взаємодіють з парними кисневмісними донорами; КФ 1. 15 — ферменти, що взаємодіють з супероксид-радікалами в якосі акцепторів; КФ 1. 16 — ферменти, що окилюють іони металів; КФ 1. 17 — ферменти, що взаємодіють з CH или CH 2 групами; КФ 1. 18 — ферменти, що взаємодіють з залізосірчаними білками в якості донорів; КФ 1. 19 — ферменти, що взаємодіють з відновленим флаводоксином в якості донора; КФ 1. 20 — ферменти, що взаємодіють з фосфором або миш'яком в яксті донора; КФ 1. 21 — ферменти, що взаємодіють з молекулами виду X—H и Y—H з утворенням зв'язку X—Y; КФ 1. 97 — решта оксидоредуктаз.

2 клас Трансферази: переносять групи атомів, від яких і беруть назву (метил-, сульфо-, аміно-, фосфо-, ацилтрансферази та ін. ). A-X + B ↔ A + B-X. A тут є донором групи атомів (X), а молекула B — акцептором групи. Номенклатура назви ферментів утворюються за схемою: «донор: акцептор + група + трансфераза» . Або ж використовуються загальніші назви, коли в назву ферменту включається ім'я або донора, або акцептора аспартатамінотрансфераза каталізує перенесення групи амінів з молекули аспарагінової кислоти, катехол-О-метилтрансферази здійснює перенесення метильної групи. Крім того, ферменти 7 підгрупи трансфераз, що переносять залишок фосфорної кислоти, використовуючи як донора фосфатної групи АТФ, часто називають також кіназами; амінотрансферази (6 підгрупа) часто називають трансаміназ.
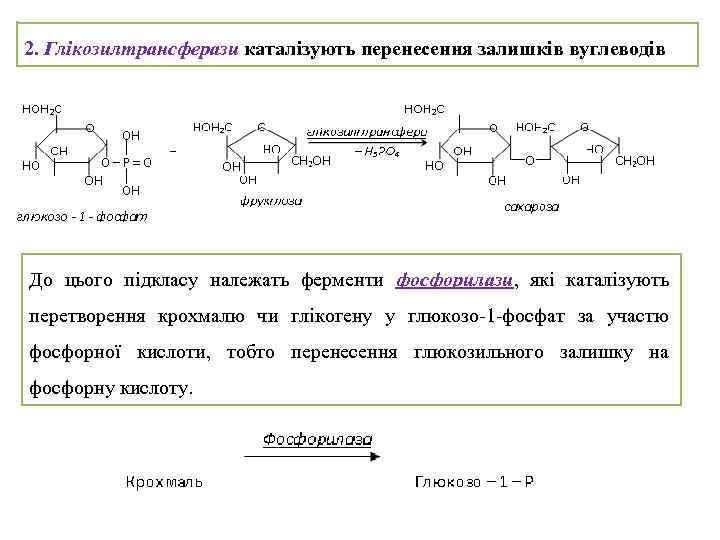
2. Глікозилтрансферази каталізують перенесення залишків вуглеводів До цього підкласу належать ферменти фосфорилази, які каталізують перетворення крохмалю чи глікогену у глюкозо-1 -фосфат за участю фосфорної кислоти, тобто перенесення глюкозильного залишку на фосфорну кислоту.
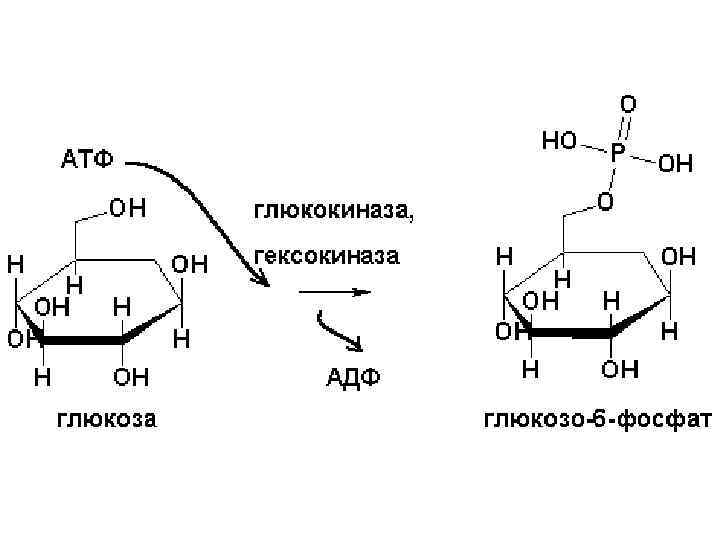
Ацилтрансферази беруть участь в перенесенні залишків органічних кислот, головним чином залишку оцтової кислоти - ацетилу (СН 3 СО-). Метилтрансферази – каталізують перенесення метальних груп. Це має велике значення в процесі синтезу холіну, що є складовою частиною лецитинів. Холін регулює жировий обмін у тваринному організмі. Амінотрасферзи – каталізують реакції переамінування (перенесення аміногрупи з амінокислоти на кетокислоту). Амінотрансферази містять як кофермент вітамін В 6.
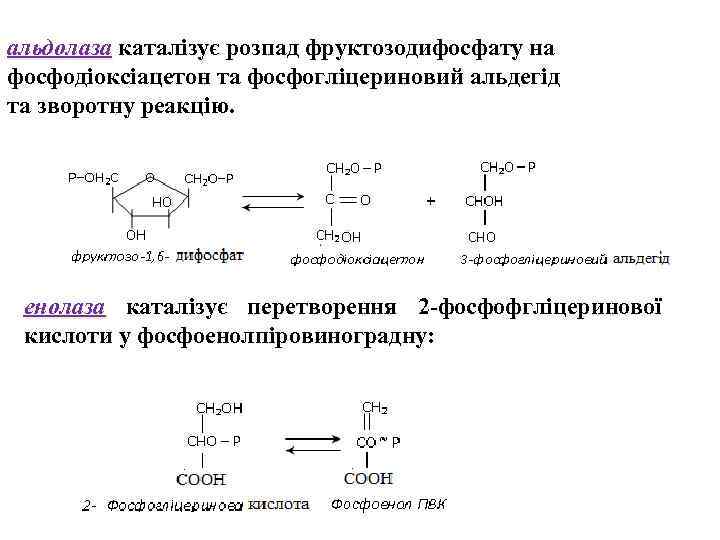
альдолаза каталізує розпад фруктозодифосфату на фосфодіоксіацетон та фосфогліцериновий альдегід та зворотну реакцію. енолаза каталізує перетворення 2 -фосфофгліцеринової кислоти у фосфоенолпіровиноградну:

2. 4. Метилтрансферази – каталізують перенесення метальних груп. Це має велике значення в процесі синтезу холіну, що є складовою частиною лецитинів. Холін регулює жировий обмін у тваринному організмі. 2. 5. Амінотрасферази – каталізують реакції переамінування (перенесення аміногрупи з амінокислоти на кетокислоту). Амінотрансферази містять як кофермент - вітамін В 6.

Класифікація згідно з міжнародною класифікацією і номенклатурою ферментів трансферази відносяться до 2 класу, в межах якого виділяють дев'ять підкласів: КФ 2. 1 включає ферменти, що переносять одновуглецеві групи; КФ 2. 2 — ферменти, переносять альдегідні та кетонні групи; КФ 2. 3 — переносять ацильні залишки (ацилтрансферази); КФ 2. 4 — переносять залишки цукрів (глікозилтрансферази); КФ 2. 5 — переносять алкільні групи за винятком метильного залишку; КФ 2. 6 — переносять групи атомів, що містять азот; КФ 2. 7 — переносять групи атомів, що містять фосфор; КФ 2. 8 — переносять групи атомів, що містять сірку; КФ 2. 9 — переносять групи атомів, що містять селен.

2 клас Гідролази- каталізують гідролітичні реакції. Діють: • на складні ефіри • на глікозильні сполуки • На прості ефіри • На пептидні звязки • На С-N-зв’язки • На ангідриди кислот • На С-С зв’язки

Згідно з міжнародною класифікацією ферментів гідролази віднесені до класу (КФ 3). Клас, в свою чергу, підрозділяється на 13 підкласів в залежності від типу зв'язку, що гідролізується. КФ 3. 1 складноефірний (естерази: зв'язок нуклеаза, фосфодіестераза, ліпаза, фосфатаза) КФ 3. 2 цукри (глікозидази: амілаза, гіалуронідаза, лізоцим та ін. ) КФ 3. 3 простий ефірний зв'язок КФ 3. 4 пептидний зв'язок (протеази: трипсин, хімотрипсин, еластаза, тромбін, ренін та ін. ) КФ 3. 5 непептидний вуглець-азотний зв'язок КФ 3. 6 кислотний ангідрид (кислотний ангідридгідролаза (геліказа, ГТФаза)) КФ 3. 7 вуглець-вуглецевий зв'язок (C-C) КФ 3. 8 галогенний зв'язок КФ 3. 9 азотно-фосфорний зв'язок (P-N) КФ 3. 10 азотно-сірчаний зв'язок (S-N) КФ 3. 11 вуглецево-фосфорний зв'язок (C-P) КФ 3. 12 дисульфідний зв'язок (S-S) КФ 3. 13 сірчано-вуглецевий зв'язок (C-S)

Найбільше значення мають естерази, глікозидази, пептидгідролази, амідази: 1. Естерази здійснюють гідроліз та синтез складних ефірів. R-CO-O-R 1 + HOH ↔ RCOOH + R 1 OH R – залишок кислоти, R 1 – залишок спирту.

Найбільш важливими є: Карбоксиестерази (ліпаза) каталізує гідроліз та синтез жирів. Ліпази діють на складно ефірний зв’язок між гліцерином та ВЖК. R 1, R 2, R 3 – радикали ВЖК.

2. Глікозидази (карбогідрази) розщеплюють глікозидні зв’язки, здійснюючи гідроліз вуглеводів та інших глюкозидів. R-O-R 1 + HOH ↔ ROH + R 1 OH R – залишок вуглеводу, R – залишок вуглеводу або речовини не 1 вуглеводної природи (аглікон). Поділяються на олігази, що гідролізують олігосахариди та поліази, що гідролізують полісахариди другого порядку
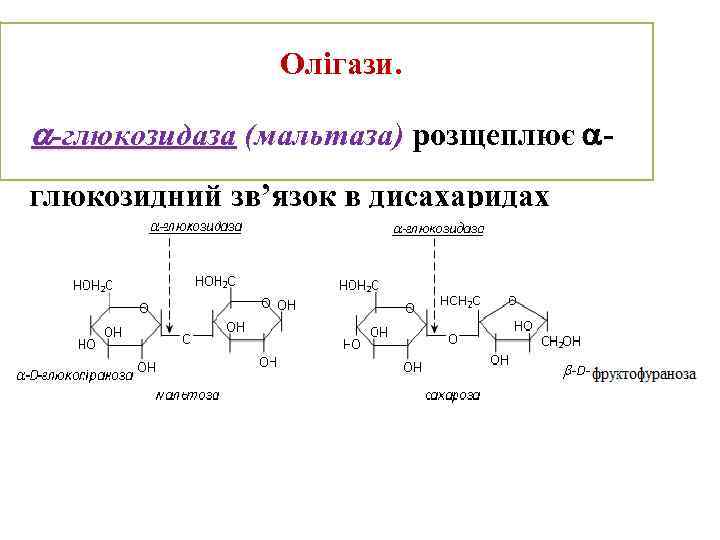
Олігази. -глюкозидаза (мальтаза) розщеплює глюкозидний зв’язок в дисахаридах (мальтозі) та глюкозидах (сахарозі):
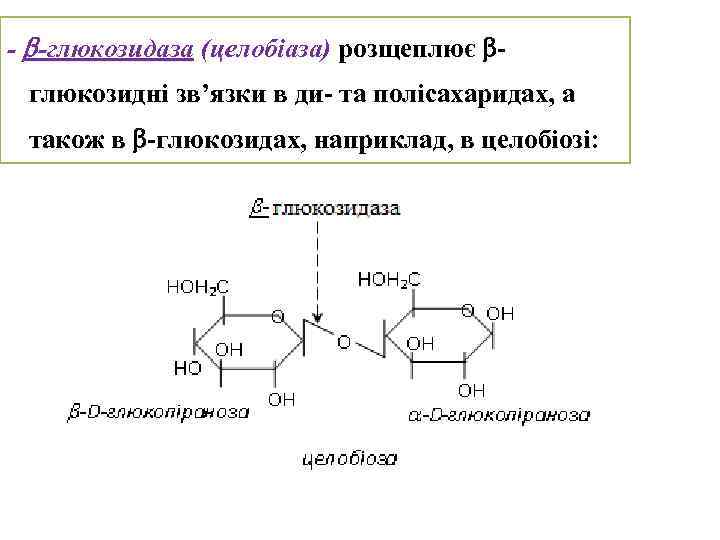
- -глюкозидаза (целобіаза) розщеплює глюкозидні зв’язки в ди- та полісахаридах, а також в -глюкозидах, наприклад, в целобіозі:
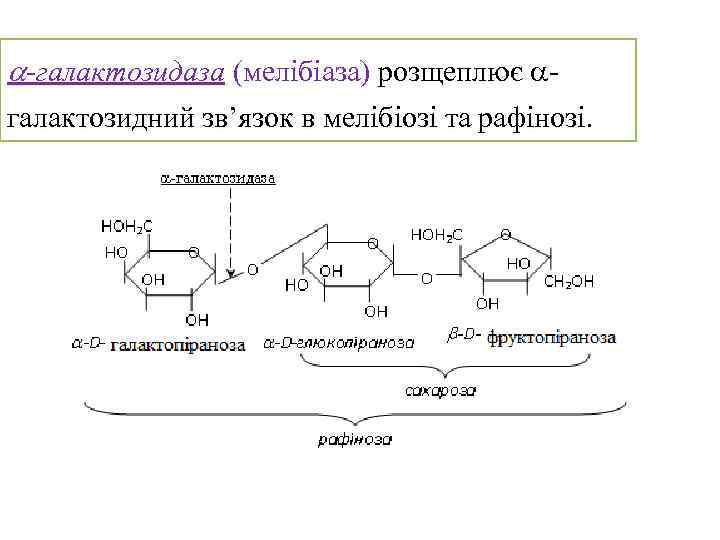
-галактозидаза (мелібіаза) розщеплює галактозидний зв’язок в мелібіозі та рафінозі
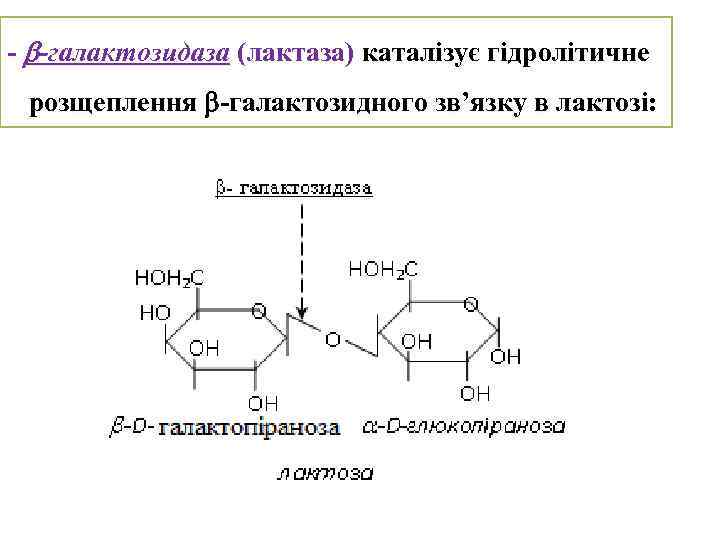
- -галактозидаза (лактаза) каталізує гідролітичне розщеплення -галактозидного зв’язку в лактозі:
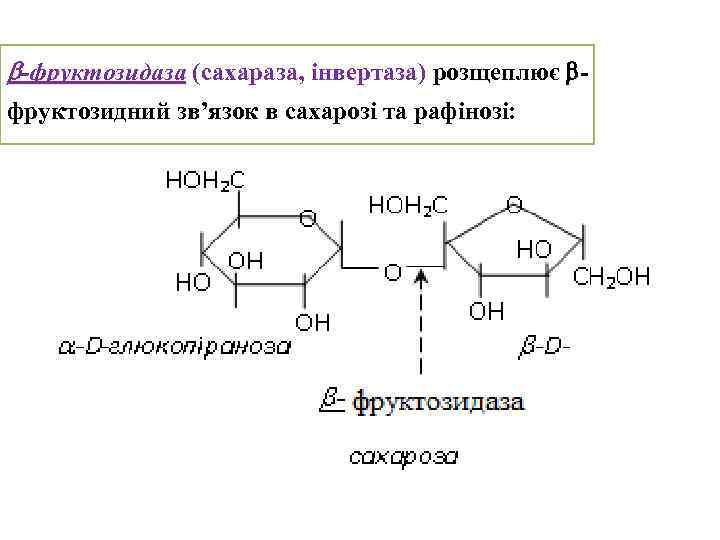
-фруктозидаза (сахараза, інвертаза) розщеплює фруктозидний зв’язок в сахарозі та рафінозі:

Поліази: - амілази - група ферментів, що гідролізують крохмаль. Встановлена наявність трьох амілаз. Фермент -амілаза (тваринна амілаза, декстриногенамілаза), в організмі тварин її міститься більше, ніж у рослинах. Ферменти -амілази гідролізують розщеплення лише -1– 4 -глюкозидні зв’язки всередині молекулі високополімеризованого субстрату (вивільняє глюкозу в -мутамерній формі).

-амілаза (рослинна амілаза, сахарогенамілаза) міститься головним чином в рослинах (зерні пшениці, жита, ячменю, соєвих бобах. Ферменти амілази гідролізують розщеплення передостаннього -1– 4 -глюкозидного зв’язку з нередукуючого кінця лінійної ділянки амілози та амілопектину.

3. Пептидгідролази (протеази, протеолітичні ферменти) гідролізують білки (протеїнази) та пептиди (пептидази). R – CO – NH – R 1 + HOH R – COOH + R 1 – NH 2, де R, R 1 - залишки амінокислот, пептидів. 3. 1. Протеїнази. - пепсин - гідролізує переважно пептидні зв’язки, що утворені аміногрупою тирозину та фенілаланіну. - трипсин - розщеплює пептидні зв’язки, утворені карбоксильною групою лізину та аргініну. - ренін - розщеплює пептидні зв’язки між фенілаланіном та метіоніном в казеїні. - хімотрипсин - розщеплює пептидні зв’язки, утворені карбоксильною групою тирозину та фенілаланіну - папаїн - рослинний протеолітичний фермент. Отримують у вигляді сухого порошку з соку плодів динного
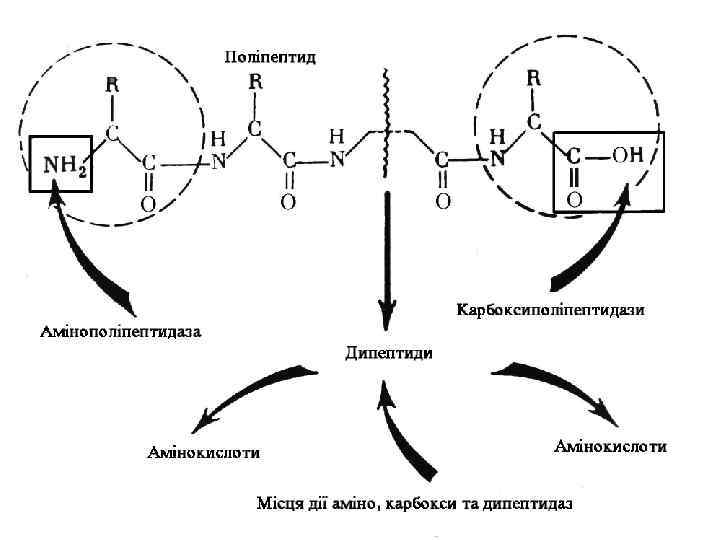

3. 2. Пептидази амінопептидази – розщепляють пептидний зв’язок, що знаходиться поряд із вільною аміногрупою. Для дії амінопептидаз необхідна наявність в молекулі субстрату вільної -аміногрупи. карбоксипептидази – розщепляють пептидний зв’язок, що знаходиться поряд із вільною карбокс

дипептидази – каталізують гідролітичне розщеплення дипептидів на вільні амінокислоти.

4. Амідази – каталізують гідроліз амідів (уреаза, аргіназа, аспарагіназа, глютаміназа). уреаза – розщеплює сечовину на аміак та діоксид вуглецю; аспарагіназа – каталізує гідролітичне розщеплення аспарагіну на аспарагінову кислоту та аміак; глютаміназа – каталізує гідролітичне розщеплення глютаміну на глютамінову кислоту та аміак; аргіназа – каталізує гідролітичне розщеплення L-аргініну на орнітин та сечовину.

4 клас Ліази: негідролітичного розщеплення без участі води. (декарбоксилази, альдолази, тощо. ) Розчеплюють С-С ; С-О ; С-N; тощо, В загальному вигляді назви ферментів отримуються за схемою «субстрат + ліаза» . В назві фермента присутні слова "декарбоксилаза" та "альдолаза" або "ліаза" (пируват-декарбоксилаза, оксалатдекарбоксилаза, оксалоацетат-декарбоксилаза, та ін. ), а для ферментів, що каталізують реакції відщеплення води від субстрату, - "дегідратаза" (карбонат-дегідратаза, цитратдегідратаза, серин-дегідратаза та ін. ). Приклади: .
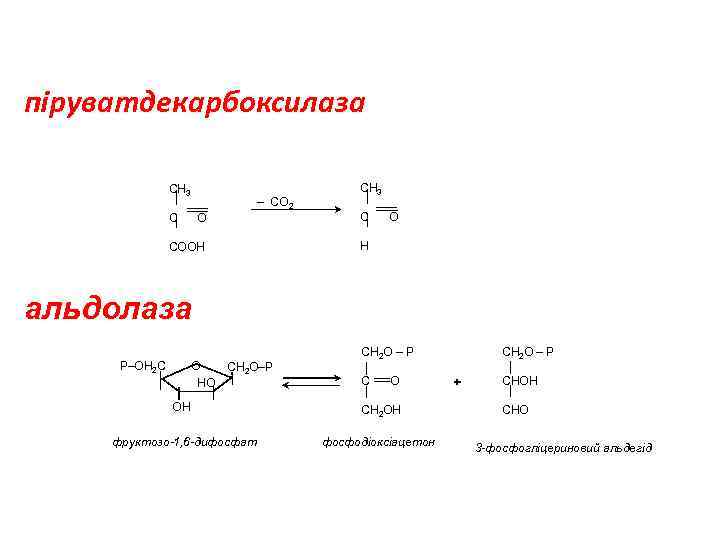
піруватдекарбоксилаза СН 3 – СО 2 СН 3 О С СООН Н С О альдолаза О НО Р–ОН 2 С СН 2 О–Р СН 2 О – Р С О ОН СН 2 ОН фруктозо-1, 6 -дифосфат фосфодіоксіацетон СН 2 О – Р + СНОН СНО 3 -фосфогліцериновий альдегід

енолаза СН 2 ОН СН 2 СНО – Р СО ~ Р СООН 2 -Фосфогліцеринова кислота Фосфоенол ПВК

Згідно з міжнародною класифікацією ферментів ліази віднесені до класу (КФ 4). Клас, в свою чергу, підрозділяється на 7 підкласів: КФ 4. 1 – включає ферменти, що розщіплюють вуглець-вуглецеві зв’язки, наприклад, декарбоксилази (карбоксиліази); КФ 4. 2 — ферменти, що розщіплюють вуглець-кисневі зв’язки, наприклад, дегідратази; КФ 4. 3 — ферменти, що розщіплюють вуглець-азотні зв’язки (амідин-ліази); КФ 4. 4 — ферменти, що розщіплюють вуглець-сірчисті зв’язки; КФ 4. 5 — включає ферменти, що розщіплюють зв’язки вуглець-галоген, наприклад, ДДТ-дегідрохлориназа; КФ 4. 6 — ферменти, що розщіплюють фосфоро-кисневі зв’язки, наприклад, аденілатциклаза; КФ 4. 99 — включає інші ліази.

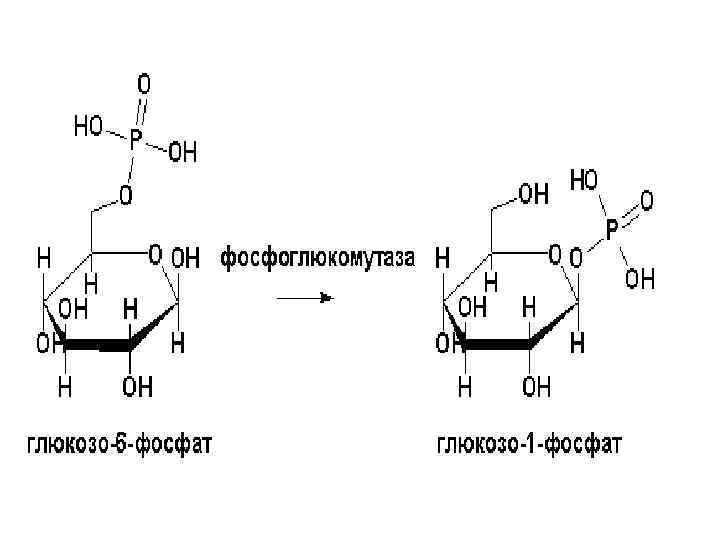
5 клас Ізомерази — ферменти, що каталізують структурні або просторові зміни в молекулі субстрату. В назві ферменту присутнє слово "рацемаза" (аланін-рацемаза, метионін-рацемаза, гідроксипролін-рацемаза, лактат-рацемаза та ін. ), «епімераза" (альдоза-1 -епімераза, рибулозофосфат-4 епімераза, УДФ-глюкуронат-4 -епімераза та ін. ), «ізомераза" (рибозофосфат-ізомераза, ксилозоізомераза, глюкозамінфосфат-ізомераза, еноіл-Со. А ізомераза та ін. ), "мутаза" (фосфогліцерат-мутаза, метиласпартат-мутаза, фосфоглюкомутаза та ін. ).

5. 1. Рацемази – діють на субстрати з одним асиметричним атомом, наприклад бактеріальна рацемаза перетворює Lамінокислоти в D-амінокислоти. 5. 2. Епімерази – діють на субстрати з декількома асиметричними атомами. – тріозофосфат-ізомераза бере участь у процесі бродіння, каталізує перетворення 3 -фосфогліцеринового альдегіду в фосфодіоксіацетон:
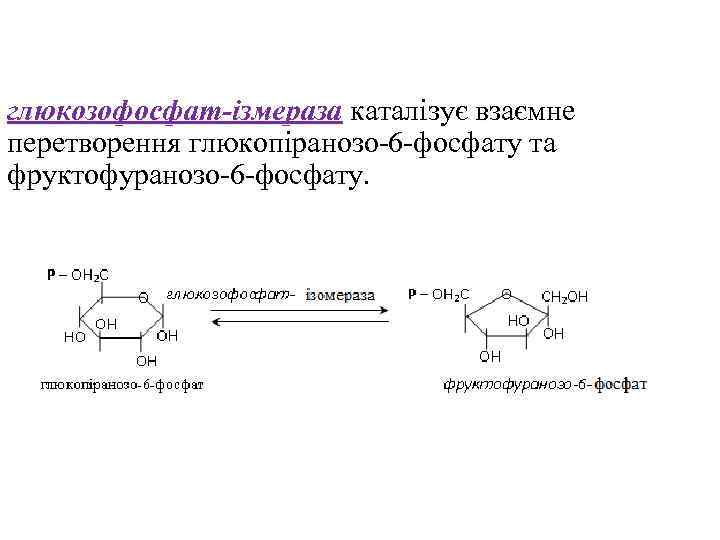
глюкозофосфат-ізмераза каталізує взаємне перетворення глюкопіранозо-6 -фосфату та фруктофуранозо-6 -фосфату.

Ізомерази мають власну класифікацію, КФ 5 та мають наступні підкласи: КФ 5. 1 ферменти, що каталізують рацемізацію (рацемази) та епімеризацію (епімерази) КФ 5. 2 ферменти, що каталізують геометричну ізомеризацію (цис-транс ізомерази) КФ 5. 3 внутрішньомолекулярні оксидоредуктази КФ 5. 4 включає трансферази (мутази) КФ 5. 5 включає внутрішньомолекулярні ліази КФ 5. 99 включає інші ізомерази, в тому числі, топоізомерази

6 клас Лігази (від лат. ligāre — «зшивати» , «зв'язувати» ) — клас ферментів (КФ 6), здатних каталізувати взємодію двох молекул з утворенням нового хімічного зв'язку (лігування). При цьому відбувається відщеплення (гідроліз) невеликої хімічної групи від однієї з молекул. Ab + C → A—C + b Або Ab + c. D → A—D + b + c Зазвичай назви лігаз включаються в себе слово «лігаза» (наприклад, ДНКлігаза) або слово «синтетаза» (наприклад, аміноацил-т. РНК-синтетаза). Через те, що деякі лігази додають вуглекислоту до молекули, вони мають назву карбоксилаз.

Лігази, що утворюють C–N-зв’язок. глютамінсинтетаза – каталізує реакцію синтезу глютаміну з глютамінової кислоти та аміаку. аспарагінсинтетаза – каталізує реакцію синтезу аспарагіну з аспарагінової кислоти та аміаку.

4. Лігази, що утворюють C–O-зв’язок – ферменти, що каталізують приєднання залишків амінокислот до т-РНК (відіграють віжливу роль в біосинтезі білка). - аланіл-т. РНК-синтетаза

У класифікації міжнародної комісії з ферментів, лігази класифікуються як КФ 6 та поділяються на 6 підгруп: КФ 6. 1 лігази, що формують зв'язки вуглець-кисень КФ 6. 2 лігази, що формують зв'язки вуглець-сірка КФ 6. 3 лігази, що формують зв'язки вуглець-азот (включаючи аргінінсукцинат-синтетазу) КФ 6. 4 лігази, що формують зв'язки вуглець-вуглець КФ 6. 5 лігази, що формують фосфодиестерні зв'язки КФ 6. 6 лігази, що формують зв'язки азот-метал

Ферменти, застосування в промисловості Промислове отримання. Вживані нині ферменти отримують з сировини тваринного, рослинного або мікробного походження. Різні способи виробництва можуть розрізнятися в деталях, проте усі вони включають стадії qекстракції, qконцентрації, qочищення, qстабілізації і qстандартизації. Застосування.

Хлібопекарська промисловість Øамілази Øпротеази Øліпоксидази Молочна промисловість ліполітичні та протеолітичні ферменти Øренін-використовують для звурджування молока, лактазу-при заморожуванні молочних концентратів Øглюкозооксидазу-одержання яєчного альбуміну і яєчного порошку.

Øпанкреатин, ренин, пепсин, трипсин, каталаза і ліпаза - для лікування диспепсії та шлунково-кишкових розладів. Øхімотрипсин, застосовують - при запальних процесах, для прискорення загоєння хронічних виразок, а також при флебітах. Øлізоцим - як антибактеріальний та антивірусний засіб. Øстрептокіназа і стрептодорназа - для прискорення розсмоктування тромбів і фибринозних або гнійних утворень. Øпапаїн - в косметиці як засіб, що очищає шкіру.

Пектин, глюкозооксидазу, амілазу інвертазу і нарингіназу застосовують в різних процесах при переробці фруктів, для руйнування фруктової пульпи і освітлення соків, вин, спиртових напоїв Протеолітичні ферменти - при виробництві м'ясних продуктів для надання м'ясу ніжніших смакових якостей. Ферменти тосовують: Ø для відновлення смакових якостей і запаху, у виробництві кондитерських виробів, в текстильній промисловості, а також для дублення шкур. Øдля поліпшення процесів травленняв корм твариною для полегшення і поліпшення засвоєння кормів.
Ферменти (96) 19.11.2012 (фон1).ppt