Фенолформальдегидные смолы.pptx
- Количество слайдов: 26
 Фенолформальдегидные смолы
Фенолформальдегидные смолы
 • Фенолформальдегидные смолы — синтетические реактопласты или термореактопласты, жидкие или твердые олигомерные продукты поликонденсации фенола с форм альдегидом в щелочной или кислой среде (бакелиты, новолачные и резольные смолы), что соответственно влияет на их свойства.
• Фенолформальдегидные смолы — синтетические реактопласты или термореактопласты, жидкие или твердые олигомерные продукты поликонденсации фенола с форм альдегидом в щелочной или кислой среде (бакелиты, новолачные и резольные смолы), что соответственно влияет на их свойства.
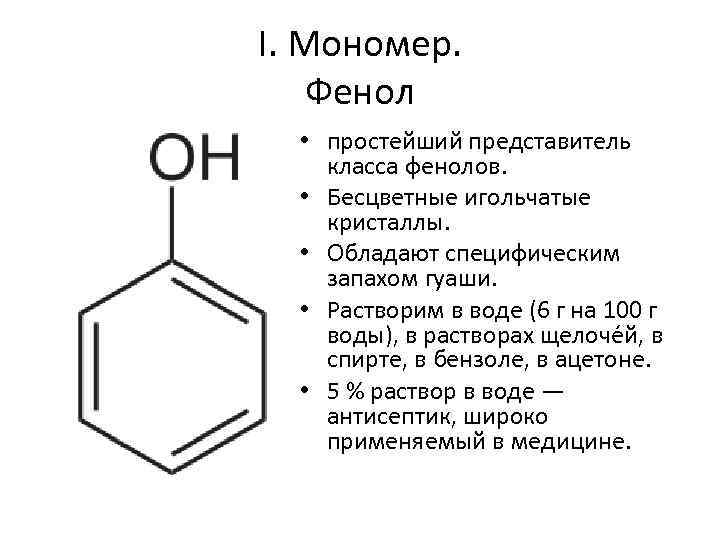 I. Мономер. Фенол • простейший представитель класса фенолов. • Бесцветные игольчатые кристаллы. • Обладают специфическим запахом гуаши. • Растворим в воде (6 г на 100 г воды), в растворах щелоче й, в спирте, в бензоле, в ацетоне. • 5 % раствор в воде — антисептик, широко применяемый в медицине.
I. Мономер. Фенол • простейший представитель класса фенолов. • Бесцветные игольчатые кристаллы. • Обладают специфическим запахом гуаши. • Растворим в воде (6 г на 100 г воды), в растворах щелоче й, в спирте, в бензоле, в ацетоне. • 5 % раствор в воде — антисептик, широко применяемый в медицине.
 Химические свойства фенола: • Обладает слабыми кислотными свойствами, при действии щелочей образует соли — феноляты (например, фенолят натрия - C 6 H 5 ONa): C 6 H 5 OH + Na. OH → C 6 H 5 ONa + H 2 O • Взаимодействует с металлическим натрием: 2 C 6 H 5 OH + 2 Na → 2 C 6 H 5 ONa + H 2↑ • Ацилирование. Легко ацилирование осуществляется действием галогенангидридов и ангидридов карбоновых кислот по механизму нуклеофильного замещения: C 6 H 5 OH + СH 3 C(O)Cl → C 6 H 5 OC(O)CH 3 + HCl
Химические свойства фенола: • Обладает слабыми кислотными свойствами, при действии щелочей образует соли — феноляты (например, фенолят натрия - C 6 H 5 ONa): C 6 H 5 OH + Na. OH → C 6 H 5 ONa + H 2 O • Взаимодействует с металлическим натрием: 2 C 6 H 5 OH + 2 Na → 2 C 6 H 5 ONa + H 2↑ • Ацилирование. Легко ацилирование осуществляется действием галогенангидридов и ангидридов карбоновых кислот по механизму нуклеофильного замещения: C 6 H 5 OH + СH 3 C(O)Cl → C 6 H 5 OC(O)CH 3 + HCl
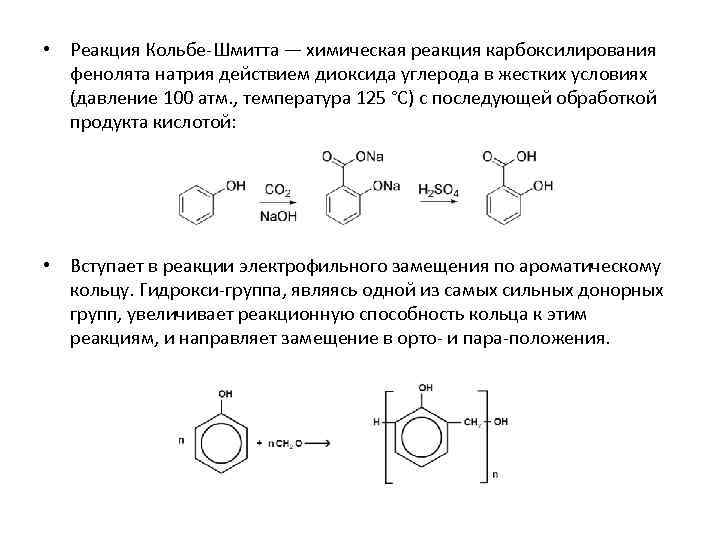 • Реакция Кольбе-Шмитта — химическая реакция карбоксилирования фенолята натрия действием диоксида углерода в жестких условиях (давление 100 атм. , температура 125 °C) с последующей обработкой продукта кислотой: • Вступает в реакции электрофильного замещения по ароматическому кольцу. Гидрокси-группа, являясь одной из самых сильных донорных групп, увеличивает реакционную способность кольца к этим реакциям, и направляет замещение в орто- и пара-положения.
• Реакция Кольбе-Шмитта — химическая реакция карбоксилирования фенолята натрия действием диоксида углерода в жестких условиях (давление 100 атм. , температура 125 °C) с последующей обработкой продукта кислотой: • Вступает в реакции электрофильного замещения по ароматическому кольцу. Гидрокси-группа, являясь одной из самых сильных донорных групп, увеличивает реакционную способность кольца к этим реакциям, и направляет замещение в орто- и пара-положения.
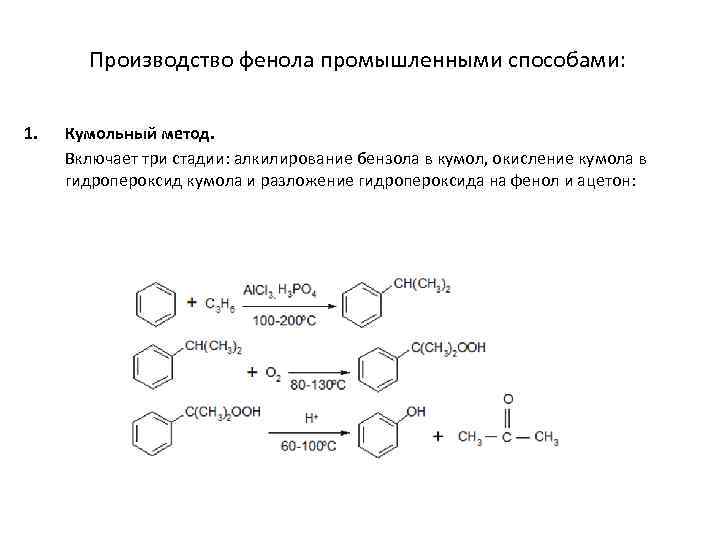 Производство фенола промышленными способами: 1. Кумольный метод. Включает три стадии: алкилирование бензола в кумол, окисление кумола в гидропероксид кумола и разложение гидропероксида на фенол и ацетон:
Производство фенола промышленными способами: 1. Кумольный метод. Включает три стадии: алкилирование бензола в кумол, окисление кумола в гидропероксид кумола и разложение гидропероксида на фенол и ацетон:
 Недостатки кумольного метода. • • • наличие взрывоопасного промежуточного соединения (гидропероксид кумола), многостадийность метода (это требует повышенных капитальных затрат и делает труднодостижимым высокий выход фенола в расчете на исходный бензол). побочный продукт - ацетон. (ацетон не находит эквивалентного рынка сбыта). Об остроте ситуации говорит тот факт, что в Японии разработана технология, предусматривающая рецикл ацетона. С этой целью к традиционной кумольной схеме добавляются еще две стадии - гидрирование ацетона в изопропиловый спирт и дегидратация последнего в пропилен:
Недостатки кумольного метода. • • • наличие взрывоопасного промежуточного соединения (гидропероксид кумола), многостадийность метода (это требует повышенных капитальных затрат и делает труднодостижимым высокий выход фенола в расчете на исходный бензол). побочный продукт - ацетон. (ацетон не находит эквивалентного рынка сбыта). Об остроте ситуации говорит тот факт, что в Японии разработана технология, предусматривающая рецикл ацетона. С этой целью к традиционной кумольной схеме добавляются еще две стадии - гидрирование ацетона в изопропиловый спирт и дегидратация последнего в пропилен:
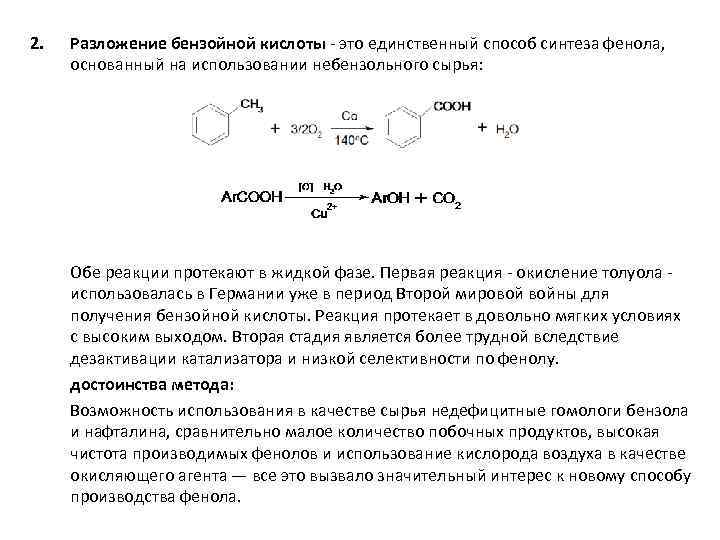 2. Разложение бензойной кислоты - это единственный способ синтеза фенола, основанный на использовании небензольного сырья: Обе реакции протекают в жидкой фазе. Первая реакция - окисление толуола - использовалась в Германии уже в период Второй мировой войны для получения бензойной кислоты. Реакция протекает в довольно мягких условиях с высоким выходом. Вторая стадия является более трудной вследствие дезактивации катализатора и низкой селективности по фенолу. достоинства метода: Возможность использования в качестве сырья недефицитные гомологи бензола и нафталина, сравнительно малое количество побочных продуктов, высокая чистота производимых фенолов и использование кислорода воздуха в качестве окисляющего агента — все это вызвало значительный интерес к новому способу производства фенола.
2. Разложение бензойной кислоты - это единственный способ синтеза фенола, основанный на использовании небензольного сырья: Обе реакции протекают в жидкой фазе. Первая реакция - окисление толуола - использовалась в Германии уже в период Второй мировой войны для получения бензойной кислоты. Реакция протекает в довольно мягких условиях с высоким выходом. Вторая стадия является более трудной вследствие дезактивации катализатора и низкой селективности по фенолу. достоинства метода: Возможность использования в качестве сырья недефицитные гомологи бензола и нафталина, сравнительно малое количество побочных продуктов, высокая чистота производимых фенолов и использование кислорода воздуха в качестве окисляющего агента — все это вызвало значительный интерес к новому способу производства фенола.
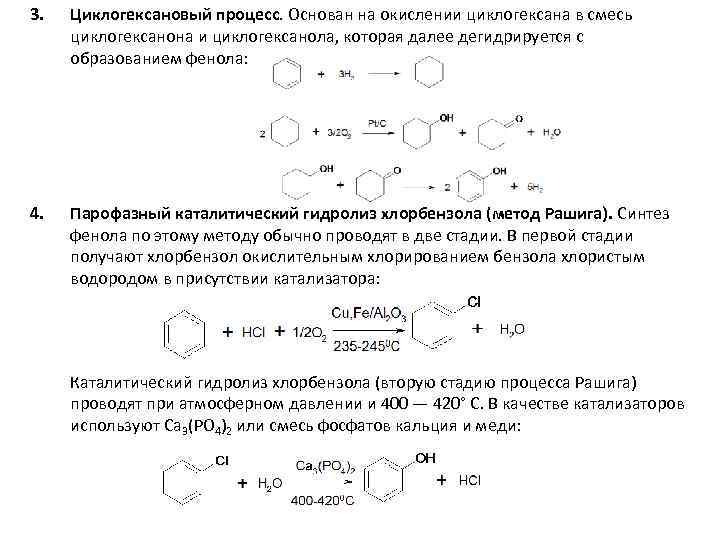 3. Циклогексановый процесс. Основан на окислении циклогексана в смесь циклогексанона и циклогексанола, которая далее дегидрируется с образованием фенола: 4. Парофазный каталитический гидролиз хлорбензола (метод Рашига). Синтез фенола по этому методу обычно проводят в две стадии. В первой стадии получают хлорбензол окислительным хлорированием бензола хлористым водородом в присутствии катализатора: Каталитический гидролиз хлорбензола (вторую стадию процесса Рашига) проводят при атмосферном давлении и 400 — 420° С. В качестве катализаторов используют Са 3(РО 4)2 или смесь фосфатов кальция и меди:
3. Циклогексановый процесс. Основан на окислении циклогексана в смесь циклогексанона и циклогексанола, которая далее дегидрируется с образованием фенола: 4. Парофазный каталитический гидролиз хлорбензола (метод Рашига). Синтез фенола по этому методу обычно проводят в две стадии. В первой стадии получают хлорбензол окислительным хлорированием бензола хлористым водородом в присутствии катализатора: Каталитический гидролиз хлорбензола (вторую стадию процесса Рашига) проводят при атмосферном давлении и 400 — 420° С. В качестве катализаторов используют Са 3(РО 4)2 или смесь фосфатов кальция и меди:
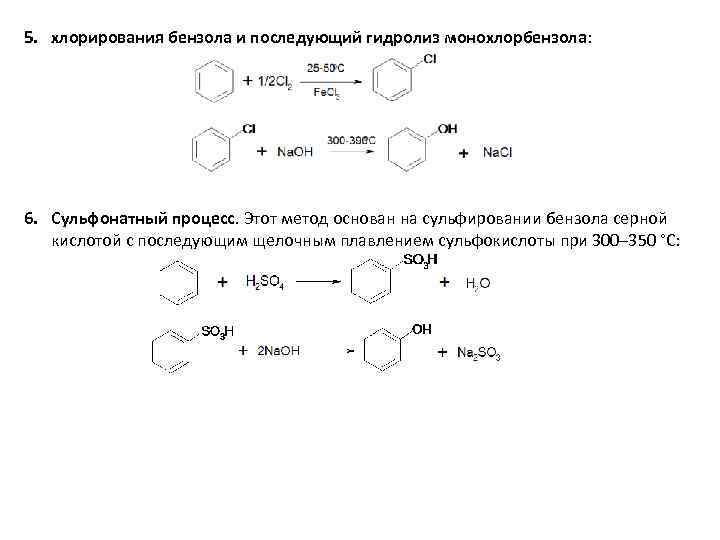 5. хлорирования бензола и последующий гидролиз монохлорбензола: 6. Сульфонатный процесс. Этот метод основан на сульфировании бензола серной кислотой с последующим щелочным плавлением сульфокислоты при 300– 350 °С:
5. хлорирования бензола и последующий гидролиз монохлорбензола: 6. Сульфонатный процесс. Этот метод основан на сульфировании бензола серной кислотой с последующим щелочным плавлением сульфокислоты при 300– 350 °С:
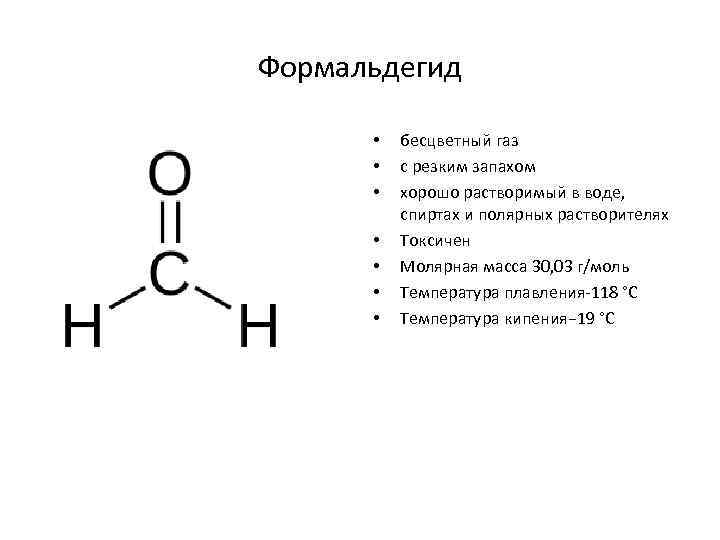 Формальдегид • • бесцветный газ с резким запахом хорошо растворимый в воде, спиртах и полярных растворителях Токсичен Молярная масса 30, 03 г/моль Температура плавления-118 °C Температура кипения− 19 °C
Формальдегид • • бесцветный газ с резким запахом хорошо растворимый в воде, спиртах и полярных растворителях Токсичен Молярная масса 30, 03 г/моль Температура плавления-118 °C Температура кипения− 19 °C
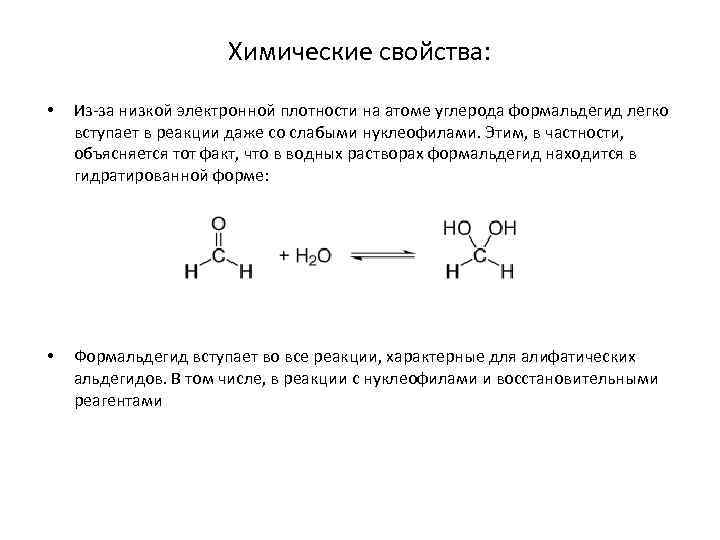 Химические свойства: • Из-за низкой электронной плотности на атоме углерода формальдегид легко вступает в реакции даже со слабыми нуклеофилами. Этим, в частности, объясняется тот факт, что в водных растворах формальдегид находится в гидратированной форме: • Формальдегид вступает во все реакции, характерные для алифатических альдегидов. В том числе, в реакции с нуклеофилами и восстановительными реагентами
Химические свойства: • Из-за низкой электронной плотности на атоме углерода формальдегид легко вступает в реакции даже со слабыми нуклеофилами. Этим, в частности, объясняется тот факт, что в водных растворах формальдегид находится в гидратированной форме: • Формальдегид вступает во все реакции, характерные для алифатических альдегидов. В том числе, в реакции с нуклеофилами и восстановительными реагентами
 Промышленные способы получения: • • Основной промышленный метод получения формальдегида — окисление метанола. Окисление метанола в формальдегид проводится с использованием серебряного катализатора при температуре 650 °C и атмосферном давлении. Это хорошо освоенный технологический процесс, и 80 % формальдегида получается именно по этому методу: Существует также промышленный способ получения формальдегида окислением метана: Процесс проводят при температуре 450 °C и давлении 1— 2 МПа, в качестве катализатора применяется фосфат алюминия Al. PO 4:
Промышленные способы получения: • • Основной промышленный метод получения формальдегида — окисление метанола. Окисление метанола в формальдегид проводится с использованием серебряного катализатора при температуре 650 °C и атмосферном давлении. Это хорошо освоенный технологический процесс, и 80 % формальдегида получается именно по этому методу: Существует также промышленный способ получения формальдегида окислением метана: Процесс проводят при температуре 450 °C и давлении 1— 2 МПа, в качестве катализатора применяется фосфат алюминия Al. PO 4:
![II. Синтез полимера. • Фенолформальдегидные смолы [-C 6 H 3(OH)-CH 2 -]n – продукты II. Синтез полимера. • Фенолформальдегидные смолы [-C 6 H 3(OH)-CH 2 -]n – продукты](https://present5.com/presentation/44521949_147905035/image-14.jpg) II. Синтез полимера. • Фенолформальдегидные смолы [-C 6 H 3(OH)-CH 2 -]n – продукты поликонденсации фенола с формальдегидом. Взаимодействие фенола с формальдегидом идет по схеме: • Роль реакционноспособных функциональных групп в этих соединениях играют: – в феноле – три С-Н-связи в орто- и пара-положениях (легче идет замещение в двух орто-положениях); – в формальдегиде – двойная связь С=О, способная к присоединению по атомам С и О.
II. Синтез полимера. • Фенолформальдегидные смолы [-C 6 H 3(OH)-CH 2 -]n – продукты поликонденсации фенола с формальдегидом. Взаимодействие фенола с формальдегидом идет по схеме: • Роль реакционноспособных функциональных групп в этих соединениях играют: – в феноле – три С-Н-связи в орто- и пара-положениях (легче идет замещение в двух орто-положениях); – в формальдегиде – двойная связь С=О, способная к присоединению по атомам С и О.
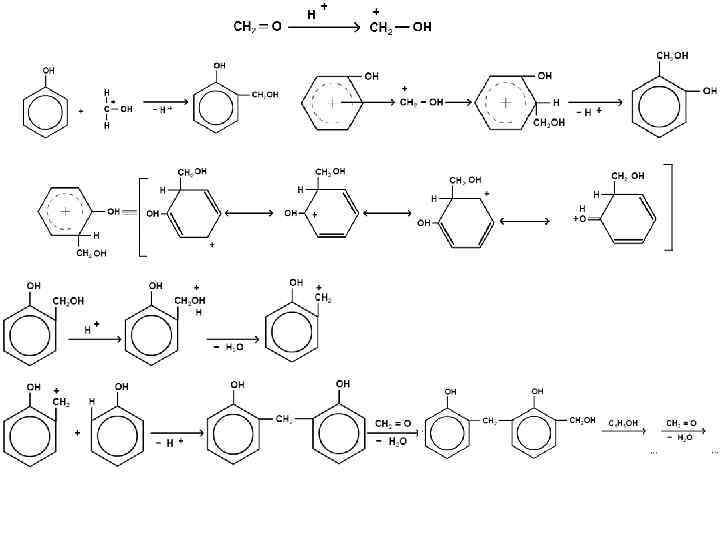
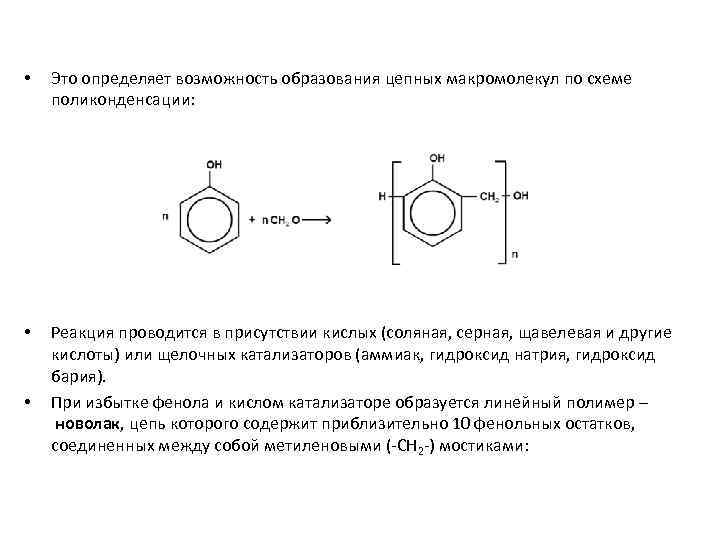 • Это определяет возможность образования цепных макромолекул по схеме поликонденсации: • Реакция проводится в присутствии кислых (соляная, серная, щавелевая и другие кислоты) или щелочных катализаторов (аммиак, гидроксид натрия, гидроксид бария). При избытке фенола и кислом катализаторе образуется линейный полимер – новолак, цепь которого содержит приблизительно 10 фенольных остатков, соединенных между собой метиленовыми (-СН 2 -) мостиками: •
• Это определяет возможность образования цепных макромолекул по схеме поликонденсации: • Реакция проводится в присутствии кислых (соляная, серная, щавелевая и другие кислоты) или щелочных катализаторов (аммиак, гидроксид натрия, гидроксид бария). При избытке фенола и кислом катализаторе образуется линейный полимер – новолак, цепь которого содержит приблизительно 10 фенольных остатков, соединенных между собой метиленовыми (-СН 2 -) мостиками: •
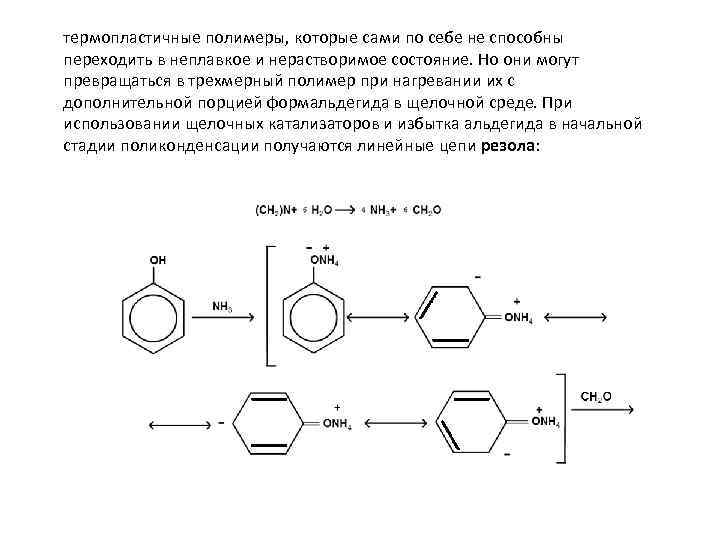 термопластичные полимеры, которые сами по себе не способны переходить в неплавкое и нерастворимое состояние. Но они могут превращаться в трехмерный полимер при нагревании их с дополнительной порцией формальдегида в щелочной среде. При использовании щелочных катализаторов и избытка альдегида в начальной стадии поликонденсации получаются линейные цепи резола:
термопластичные полимеры, которые сами по себе не способны переходить в неплавкое и нерастворимое состояние. Но они могут превращаться в трехмерный полимер при нагревании их с дополнительной порцией формальдегида в щелочной среде. При использовании щелочных катализаторов и избытка альдегида в начальной стадии поликонденсации получаются линейные цепи резола:
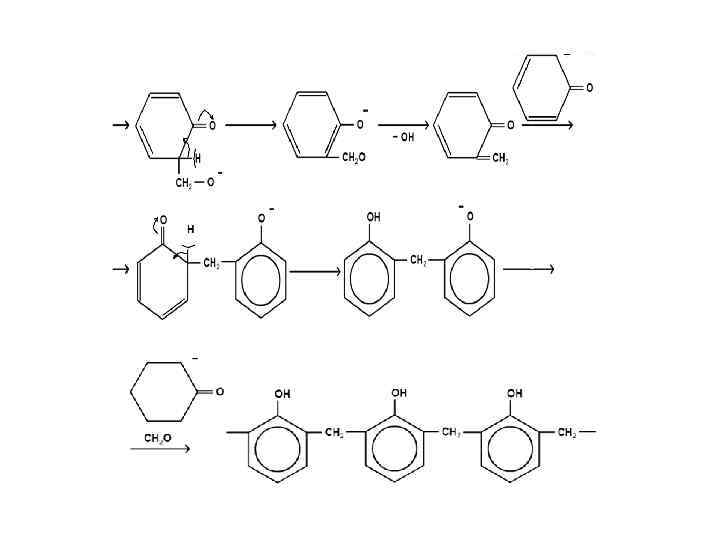
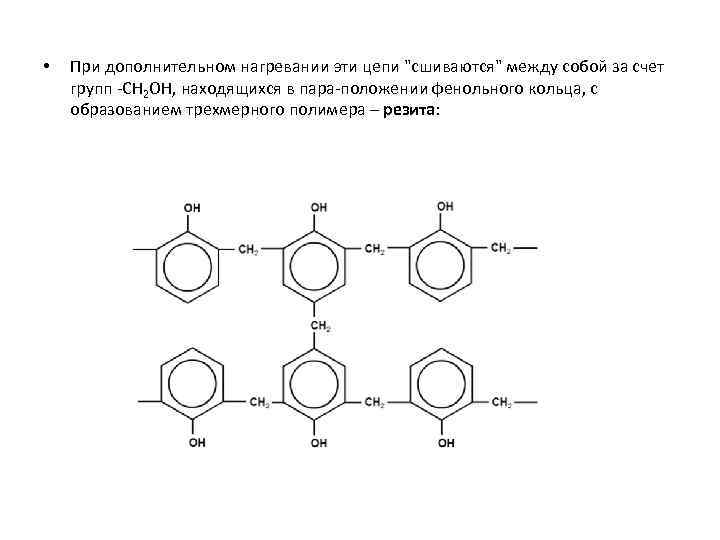 • При дополнительном нагревании эти цепи "сшиваются" между собой за счет групп -CH 2 OH, находящихся в пара-положении фенольного кольца, с образованием трехмерного полимера – резита:
• При дополнительном нагревании эти цепи "сшиваются" между собой за счет групп -CH 2 OH, находящихся в пара-положении фенольного кольца, с образованием трехмерного полимера – резита:
 III. Свойства полимера • Физические: • • • Стеклообразные вещества От светло-желтого до темно-коричневого цвета Средняя молекулярная масса 500 -900 г/моль Температура каплепадения 90 -130 ‘C Растворимы в спиртах, сложных эфирах, кетонах и водных растворах едких щелочей
III. Свойства полимера • Физические: • • • Стеклообразные вещества От светло-желтого до темно-коричневого цвета Средняя молекулярная масса 500 -900 г/моль Температура каплепадения 90 -130 ‘C Растворимы в спиртах, сложных эфирах, кетонах и водных растворах едких щелочей
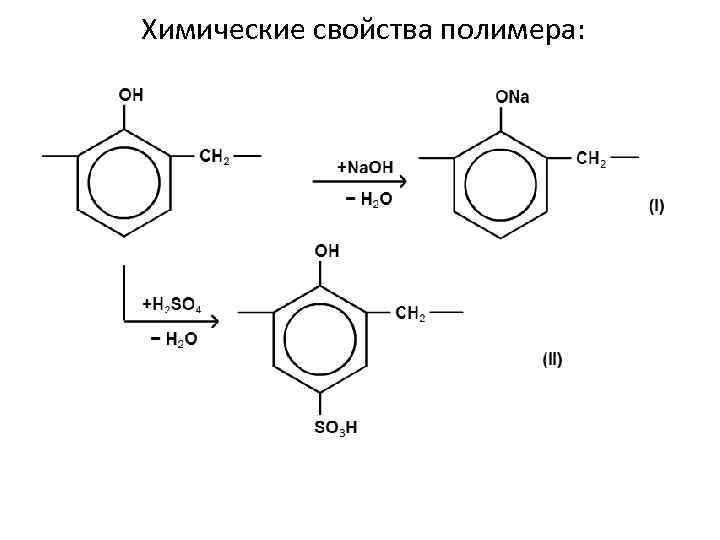 Химические свойства полимера:
Химические свойства полимера:
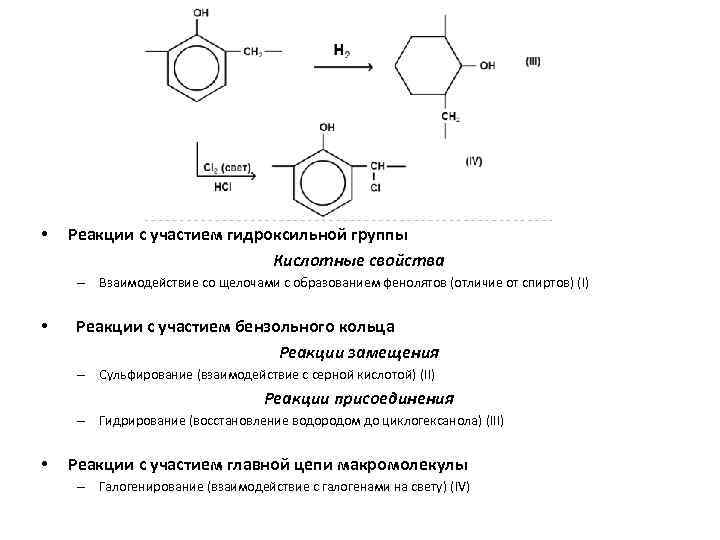 • Реакции с участием гидроксильной группы Кислотные свойства – Взаимодействие со щелочами с образованием фенолятов (отличие от спиртов) (I) • Реакции с участием бензольного кольца Реакции замещения – Сульфирование (взаимодействие с серной кислотой) (II) Реакции присоединения – Гидрирование (восстановление водородом до циклогексанола) (III) • Реакции с участием главной цепи макромолекулы – Галогенирование (взаимодействие с галогенами на свету) (IV)
• Реакции с участием гидроксильной группы Кислотные свойства – Взаимодействие со щелочами с образованием фенолятов (отличие от спиртов) (I) • Реакции с участием бензольного кольца Реакции замещения – Сульфирование (взаимодействие с серной кислотой) (II) Реакции присоединения – Гидрирование (восстановление водородом до циклогексанола) (III) • Реакции с участием главной цепи макромолекулы – Галогенирование (взаимодействие с галогенами на свету) (IV)
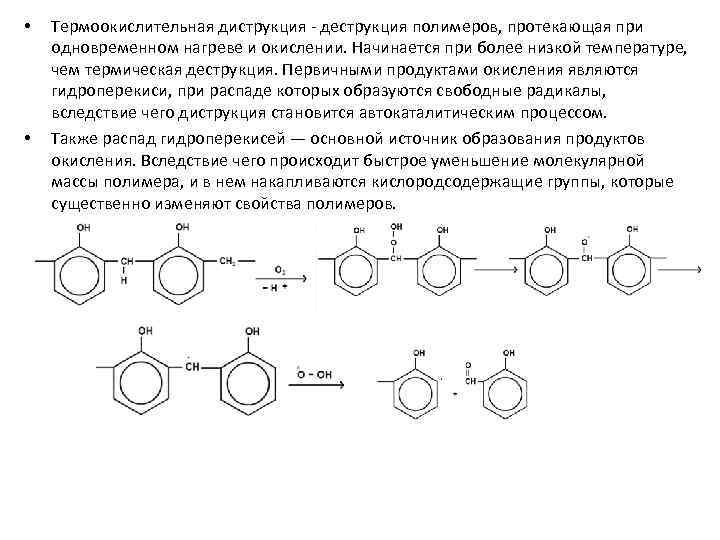 • • Термоокислительная диструкция - деструкция полимеров, протекающая при одновременном нагреве и окислении. Начинается при более низкой температуре, чем термическая деструкция. Первичными продуктами окисления являются гидроперекиси, при распаде которых образуются свободные радикалы, вследствие чего диструкция становится автокаталитическим процессом. Также распад гидроперекисей — основной источник образования продуктов окисления. Вследствие чего происходит быстрое уменьшение молекулярной массы полимера, и в нем накапливаются кислородсодержащие группы, которые существенно изменяют свойства полимеров.
• • Термоокислительная диструкция - деструкция полимеров, протекающая при одновременном нагреве и окислении. Начинается при более низкой температуре, чем термическая деструкция. Первичными продуктами окисления являются гидроперекиси, при распаде которых образуются свободные радикалы, вследствие чего диструкция становится автокаталитическим процессом. Также распад гидроперекисей — основной источник образования продуктов окисления. Вследствие чего происходит быстрое уменьшение молекулярной массы полимера, и в нем накапливаются кислородсодержащие группы, которые существенно изменяют свойства полимеров.
 Классификация полимера: • • По происхождению: Синтетические По химическому составу молекулы: Органические, гомоцепные По строению цепи: Линейные (Новолачные смолы) По однородности звеньев, составляющих макромолекулы ВМС: Сополимеры По отношению к нагреванию: Термореактивные По методу синтеза: Реакции поликонденсации В соответствии с величиной обратимой деформации: Пластики (Пластмассы)
Классификация полимера: • • По происхождению: Синтетические По химическому составу молекулы: Органические, гомоцепные По строению цепи: Линейные (Новолачные смолы) По однородности звеньев, составляющих макромолекулы ВМС: Сополимеры По отношению к нагреванию: Термореактивные По методу синтеза: Реакции поликонденсации В соответствии с величиной обратимой деформации: Пластики (Пластмассы)
 IV. Применение • Из фенолформальдегидного полимера, добавляя различные наполнители, получают фенолформальдегидные пластмассы. Их применение очень широко: – шарикоподшипники, шестерни и тормозные накладки для машин; – хороший электроизоляционный материал в радио- и электротехнике; – Изготовляют детали больших размеров, телефонные аппараты, электрические контактные платы; – Для склеивания пенополистирольных плит, применяемых для изготовления моделей в литейном производстве.
IV. Применение • Из фенолформальдегидного полимера, добавляя различные наполнители, получают фенолформальдегидные пластмассы. Их применение очень широко: – шарикоподшипники, шестерни и тормозные накладки для машин; – хороший электроизоляционный материал в радио- и электротехнике; – Изготовляют детали больших размеров, телефонные аппараты, электрические контактные платы; – Для склеивания пенополистирольных плит, применяемых для изготовления моделей в литейном производстве.
 Литература: • • • Органическая химия, Иванов В. Г. , Горленко В. А. , Гева О. Н. , Мастерство: 2003; Шабаров Ю. С. , Органическая химия. Учебник для вузов. Издательство: Москва, "Химия» : 1994; Энциклопедя полимеров. В. А. Каргин, издательство «советская энциклопедия» ; http: //cnit. ssau. ru/organics/chem 4/o 254_1. htm; http: //www. kristallikov. net/page 46. html; http: //delta-grup. ru/bibliot/12/66. htm.
Литература: • • • Органическая химия, Иванов В. Г. , Горленко В. А. , Гева О. Н. , Мастерство: 2003; Шабаров Ю. С. , Органическая химия. Учебник для вузов. Издательство: Москва, "Химия» : 1994; Энциклопедя полимеров. В. А. Каргин, издательство «советская энциклопедия» ; http: //cnit. ssau. ru/organics/chem 4/o 254_1. htm; http: //www. kristallikov. net/page 46. html; http: //delta-grup. ru/bibliot/12/66. htm.


