Федеральное государственное образовательное учреждение высшего и профессионального


Федеральное государственное образовательное учреждение высшего и профессионального образования «Сибирский федеральный университет» кафедра физиологии растений и биотехнологии ФИЗИОЛОГИЯ РАСТЕНИЙ (иллюстративное сопровождение дисциплины) направление 020200 -биология Красноярск 2007

Лекция 7. Физиологическая роль клеточного дыхания. Специфика дыхания растений. План лекции 1. Определение процесса клеточного дыхания 2. Общая схема процесса дыхания 3. Типы окислительно-восстановительных реакций 4. Каталитические системы дыхания. Механизмы активации водорода субстрата и молекулярного кислорода. 5. Специфика дыхания у растений. 7. 1 Физиология растений
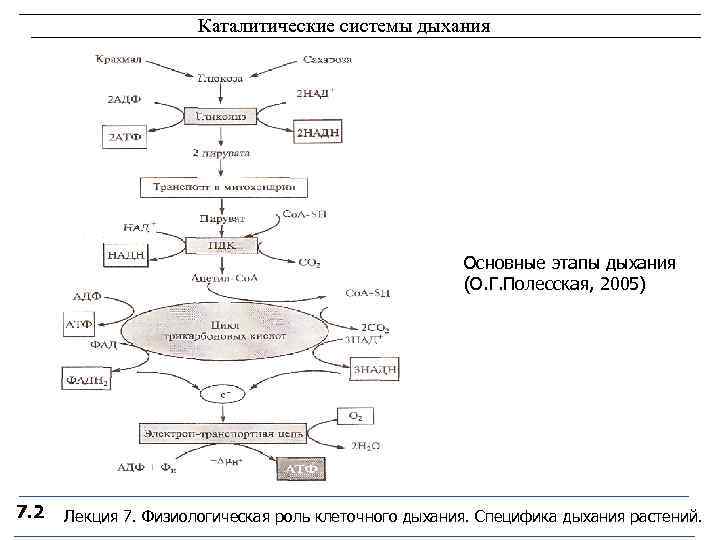
Каталитические системы дыхания Основные этапы дыхания (О. Г. Полесская, 2005) 7. 2 Лекция 7. Физиологическая роль клеточного дыхания. Специфика дыхания растений.
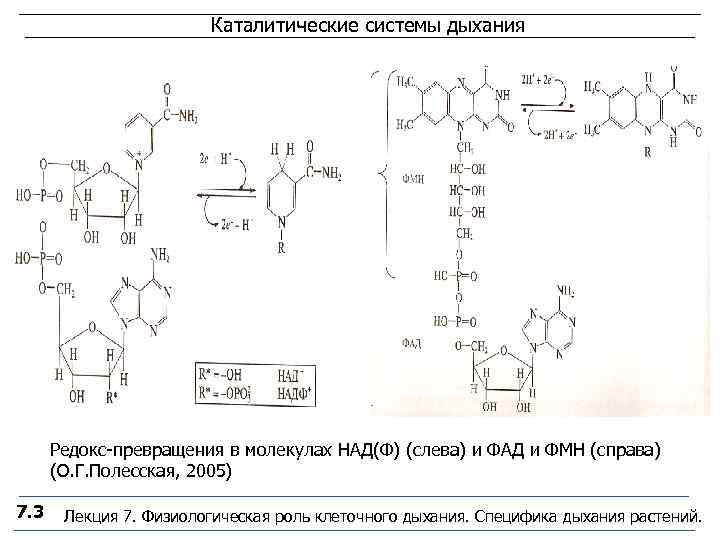
Каталитические системы дыхания Редокс-превращения в молекулах НАД(Ф) (слева) и ФАД и ФМН (справа) (О. Г. Полесская, 2005) 7. 3 Лекция 7. Физиологическая роль клеточного дыхания. Специфика дыхания растений.
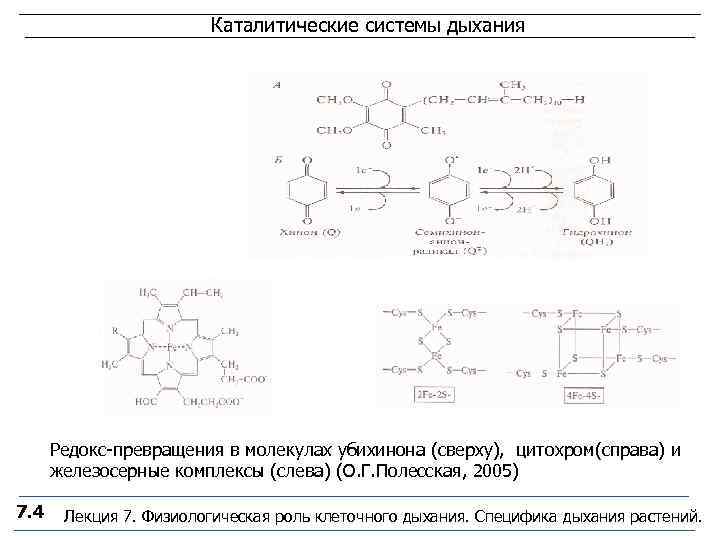
Каталитические системы дыхания Редокс-превращения в молекулах убихинона (сверху), цитохром(справа) и железосерные комплексы (слева) (О. Г. Полесская, 2005) 7. 4 Лекция 7. Физиологическая роль клеточного дыхания. Специфика дыхания растений.

Лекция 8. Основные пути диссимиляции углеводов. План лекции 1. Гликолиз 2. Превращение пирувата 3. Цикл Кребса 4. Глиоксилатный шунт 5. Апотомическое окисление глюкозы. 8. 1 Физиология растений
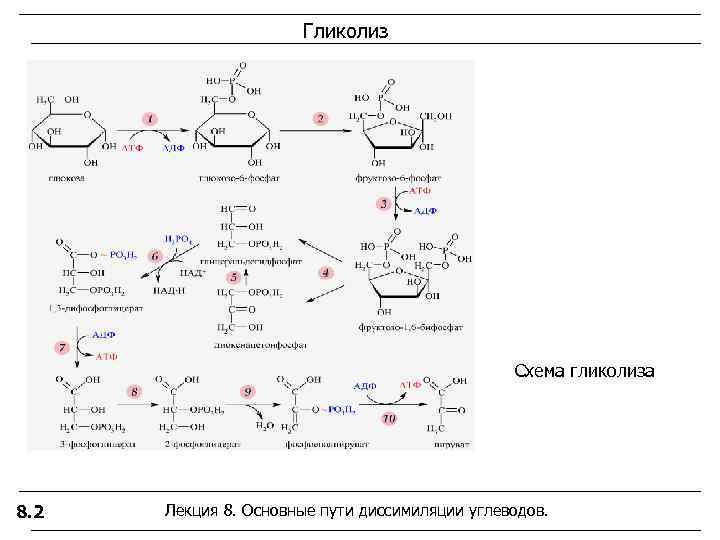
Гликолиз Схема гликолиза 8. 2 Лекция 8. Основные пути диссимиляции углеводов.
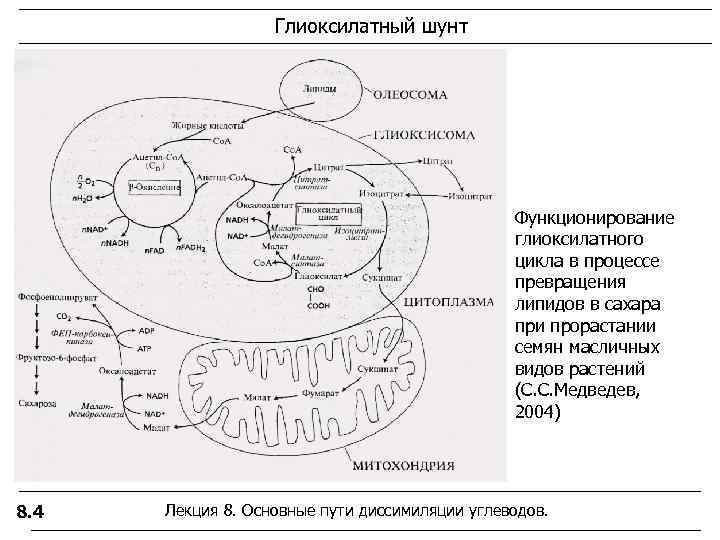
Глиоксилатный шунт Функционирование глиоксилатного цикла в процессе превращения липидов в сахара при прорастании семян масличных видов растений (С. С. Медведев, 2004) 8. 4 Лекция 8. Основные пути диссимиляции углеводов.
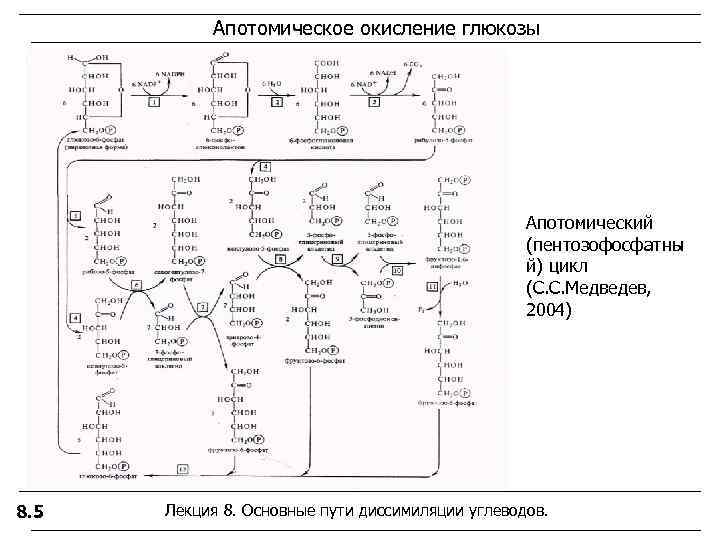
Апотомическое окисление глюкозы Апотомический (пентозофосфатны й) цикл (С. С. Медведев, 2004) 8. 5 Лекция 8. Основные пути диссимиляции углеводов.

Лекция 9. Электронно-транспортная цепь дыхания растений. План лекции 1. Структурная организация ЭТЦ дыхания 2. Комплексы переносчиков электронов 3. Образование трансмембранного потенциала протонов. 4. Особенности ЭТЦ растений 9. 1 Физиология растений
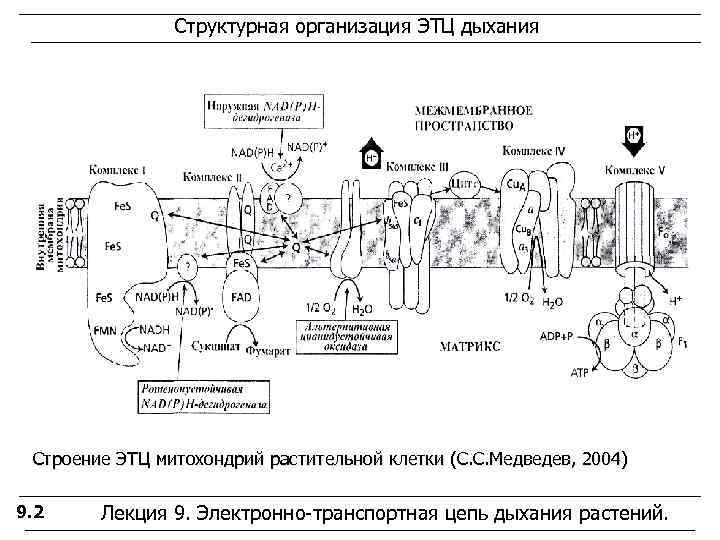
Структурная организация ЭТЦ дыхания Строение ЭТЦ митохондрий растительной клетки (С. С. Медведев, 2004) 9. 2 Лекция 9. Электронно-транспортная цепь дыхания растений.
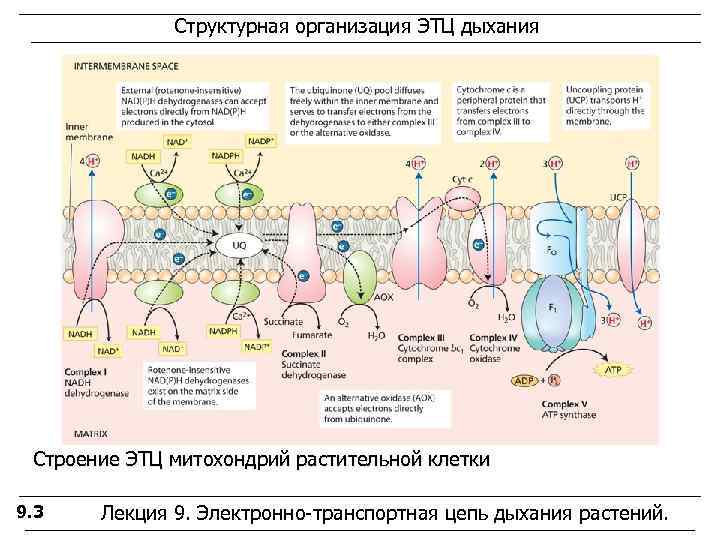
Структурная организация ЭТЦ дыхания Строение ЭТЦ митохондрий растительной клетки 9. 3 Лекция 9. Электронно-транспортная цепь дыхания растений.
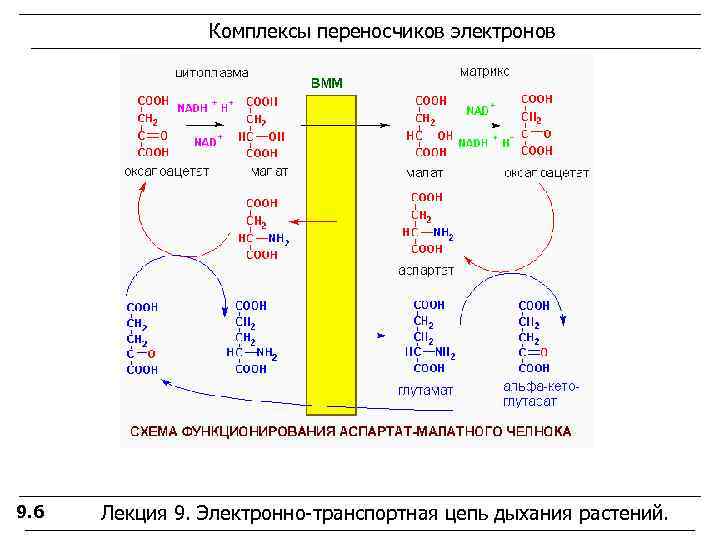
Комплексы переносчиков электронов 9. 6 Лекция 9. Электронно-транспортная цепь дыхания растений.
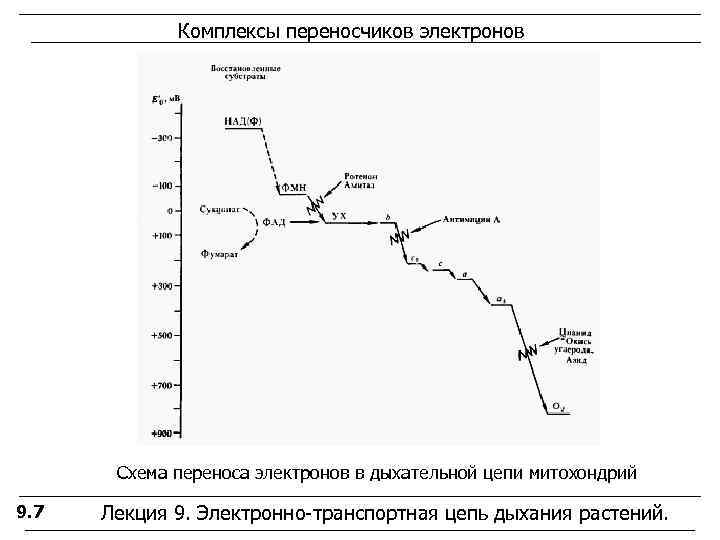
Комплексы переносчиков электронов Схема переноса электронов в дыхательной цепи митохондрий 9. 7 Лекция 9. Электронно-транспортная цепь дыхания растений.

Лекция 10. Фосфорилирование. План лекции 1. Субстратное фосфорилирование 2. Окислительное фосфорилирование 3. Хемиосмотический принцип сопряжения 4. АТФ-синтаза 10. 1 Физиология растений
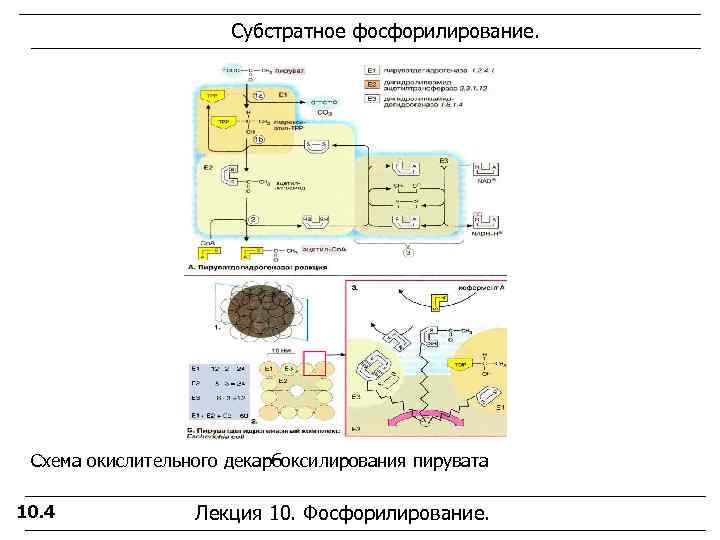
Субстратное фосфорилирование. Схема окислительного декарбоксилирования пирувата 10. 4 Лекция 10. Фосфорилирование.
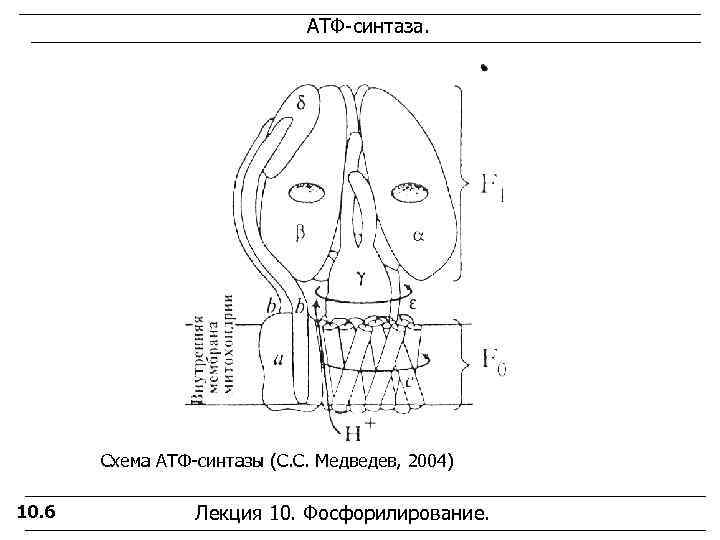
АТФ-синтаза. Схема АТФ-синтазы (С. С. Медведев, 2004) 10. 6 Лекция 10. Фосфорилирование.

Лекция 11. Роль дыхания в продукционном процессе. Влияние внешних и внутренних факторов на дыхание. План лекции 1. Взаимосвязь дыхания с другими процессами обмена 2. Составляющие дыхания: дыхание роста, дыхание поддержания 3. Соотношение в онтогенезе и в условиях меняющихся факторов среды 4. Влияние внешних факторов на процесс дыхания 5. Изменение интенсивности дыхания в онтогенезе. 11. 1 Физиология растений
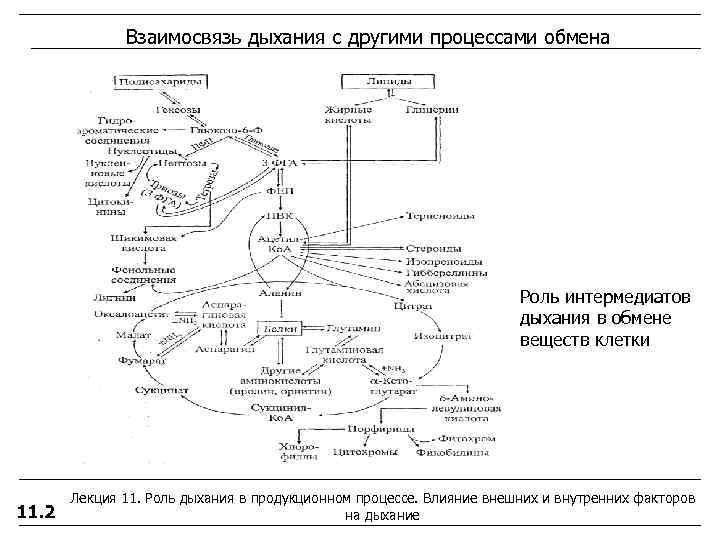
Взаимосвязь дыхания с другими процессами обмена Роль интермедиатов дыхания в обмене веществ клетки Лекция 11. Роль дыхания в продукционном процессе. Влияние внешних и внутренних факторов 11. 2 на дыхание
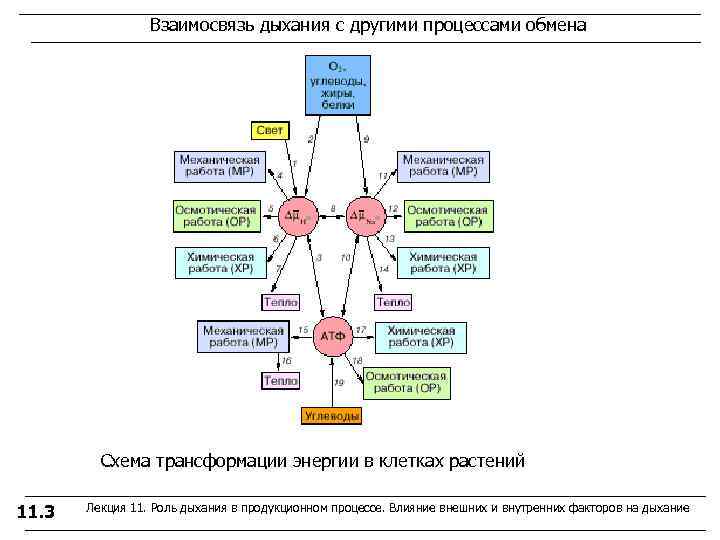
Взаимосвязь дыхания с другими процессами обмена Схема трансформации энергии в клетках растений 11. 3 Лекция 11. Роль дыхания в продукционном процессе. Влияние внешних и внутренних факторов на дыхание
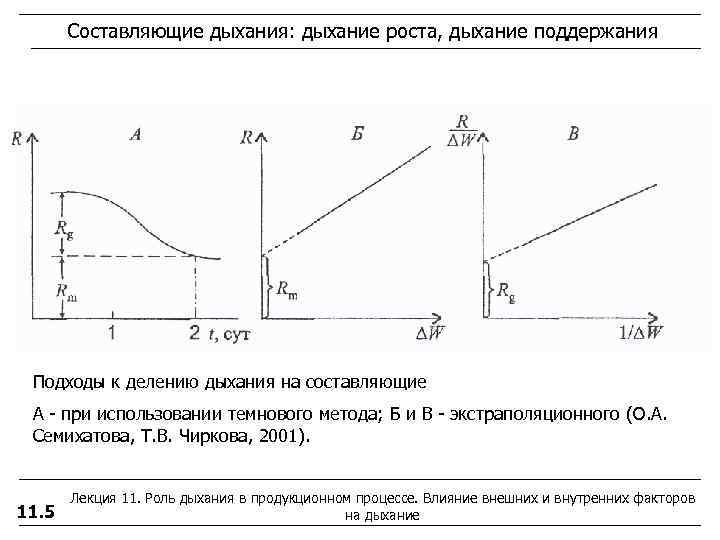
Составляющие дыхания: дыхание роста, дыхание поддержания Подходы к делению дыхания на составляющие А - при использовании темнового метода; Б и В - экстраполяционного (О. А. Семихатова, Т. В. Чиркова, 2001). Лекция 11. Роль дыхания в продукционном процессе. Влияние внешних и внутренних факторов 11. 5 на дыхание
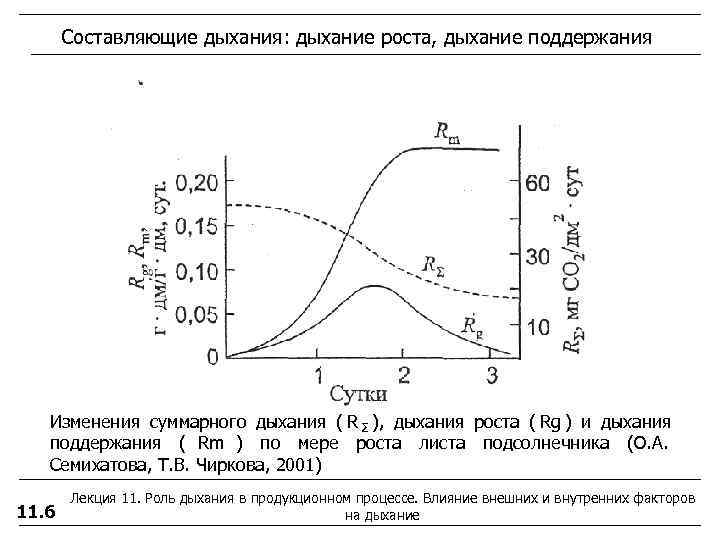
Составляющие дыхания: дыхание роста, дыхание поддержания Изменения суммарного дыхания ( R Σ ), дыхания роста ( Rg ) и дыхания поддержания ( Rm ) по мере роста листа подсолнечника (О. А. Семихатова, Т. В. Чиркова, 2001) Лекция 11. Роль дыхания в продукционном процессе. Влияние внешних и внутренних факторов 11. 6 на дыхание
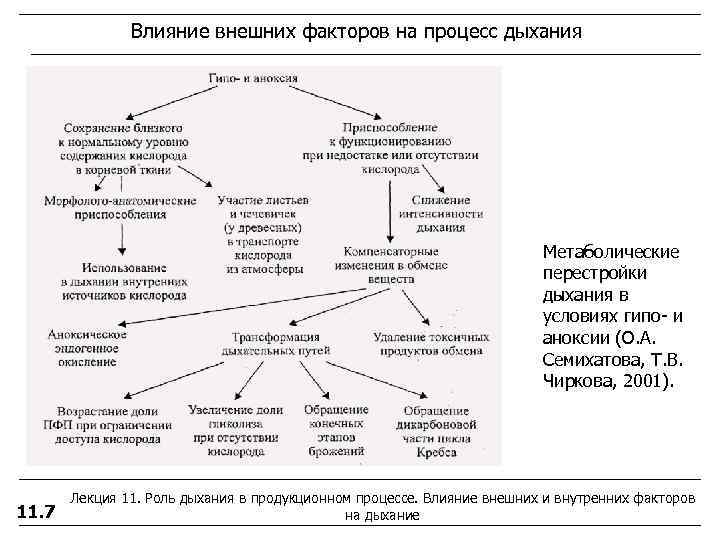
Влияние внешних факторов на процесс дыхания Метаболические перестройки дыхания в условиях гипо- и аноксии (О. А. Семихатова, Т. В. Чиркова, 2001). Лекция 11. Роль дыхания в продукционном процессе. Влияние внешних и внутренних факторов 11. 7 на дыхание
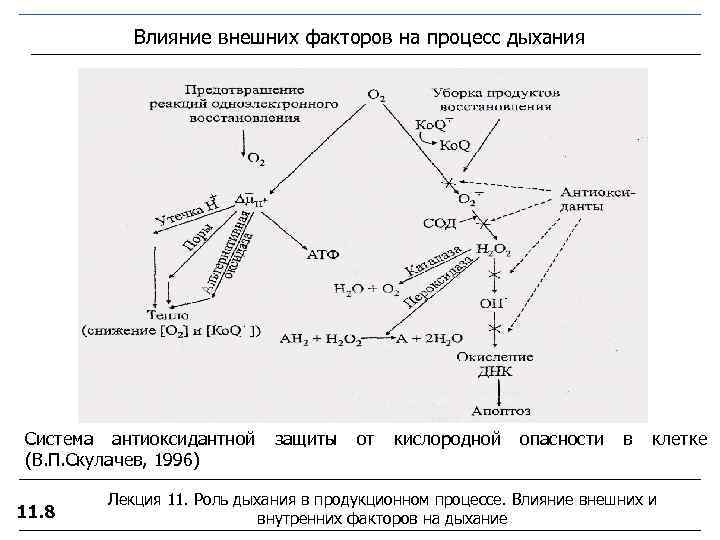
Влияние внешних факторов на процесс дыхания Система антиоксидантной защиты от кислородной опасности в клетке (В. П. Скулачев, 1996) Лекция 11. Роль дыхания в продукционном процессе. Влияние внешних и 11. 8 внутренних факторов на дыхание
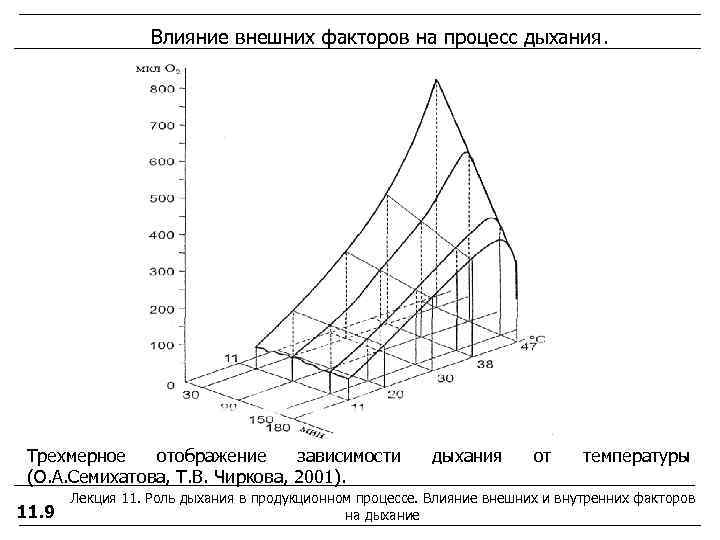
Влияние внешних факторов на процесс дыхания. Трехмерное отображение зависимости дыхания от температуры (О. А. Семихатова, Т. В. Чиркова, 2001). Лекция 11. Роль дыхания в продукционном процессе. Влияние внешних и внутренних факторов 11. 9 на дыхание

СИГНАЛЬНЫЕ СИСТЕМЫ МИТОХОНДРИЙ РАСТЕНИЙ: РЕТРОГРАДНАЯ РЕГУЛЯЦИЯ «Митохондриальная ретроградная регуляция (МРР) у растений обнаруживается при дисфункции митохондрий, вызванной мутациями, химическими агентами или действием стрессов, и пока мало изучена» (2010 г. Н. П. Юрина, М. С. Одинцова).

Клетки растений содержат энергообразующие органеллы: хлоропласты и митохондрии. Последние преобразуют запасенную энергию в АТФ. Клеточные органеллы содержат тысячи различных белков, большинство которых кодируется ядерными генами, и только немногие гены, кодирующие компоненты, главным образом, самой системы экспрессии генов и дыхательной цепи локализованы в геномах органелл. Сохранение функциональной активности митохондрий в процессе роста и развития клеток зависит преимущественно от ядерного генома, кодирующего подавляющее большинство белков, а также от их собственного генома, кодирующего ограниченное, но существенное число белков. В связи с этим, рибосомы митохондрий, комплексы митохондриальной дыхательной цепи мозаичны: они представляют собой мультибелковые комплексы, состоящие из кодируемых ядром и митохондриями субъединиц.
Поэтому должны существовать механизмы, координирующие экспрессию генов. Антероградная регуляция (МАР) контролирует поток информации, идущей от ядра и цитоплазмы к митохондриям. Ретроградная регуляция (МРР) направлена от митохондрии к ядру. С ее помощью митохондрии могут управлять экспрессией ядерных генов. Об стало известно с начала 90 х годов ХХ века.
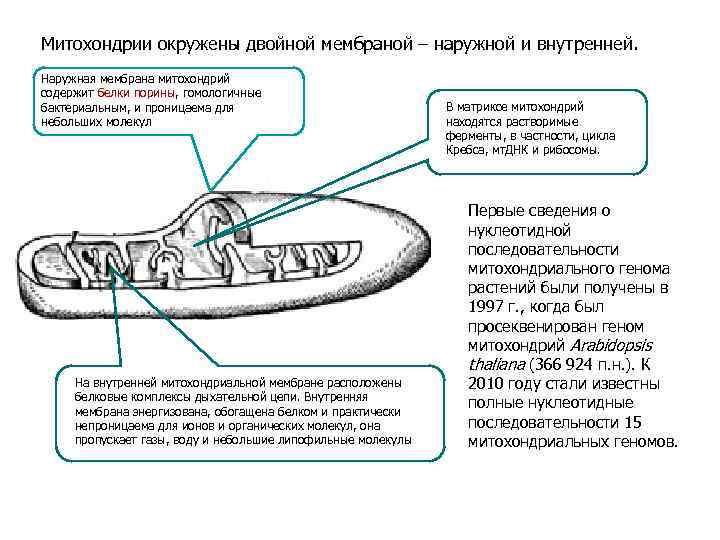
Митохондрии окружены двойной мембраной – наружной и внутренней. Наружная мембрана митохондрий содержит белки порины, гомологичные бактериальным, и проницаема для В матриксе митохондрий небольших молекул находятся растворимые ферменты, в частности, цикла Кребса, мт. ДНК и рибосомы. Первые сведения о нуклеотидной последовательности митохондриального генома растений были получены в 1997 г. , когда был просеквенирован геном митохондрий Arabidopsis thaliana (366 924 п. н. ). К На внутренней митохондриальной мембране расположены 2010 году стали известны белковые комплексы дыхательной цепи. Внутренняя мембрана энергизована, обогащена белком и практически полные нуклеотидные непроницаема для ионов и органических молекул, она последовательности 15 пропускает газы, воду и небольшие липофильные молекулы митохондриальных геномов.

Митохондрии растений по сравнению с митохондриями животных, протистов и грибов имеют наибольший геном (у покрытосеменных от 200 до 2400 т. п. н). Увеличение размера генома произошло после того, как растения заселили сушу. В этот же эволюционный период митохондриальные геномы растений потеряли ряд генов, передав их ядру. Увеличение размера генома митохондрий произошло за счет межгенных участков. Структура этих участков генома непостоянна. В них преобладают видоспецифичные последовательности. Таким образом, направленность эволюции митохондриального генома растений противоположна направленности эволюции митохондриального генома животных клеток, у которых геном митохондрий в процессе эволюции стал меньше и компактнее.

Геном митохондрий растений обычно описывают как одиночную кольцевую молекулу ДНК, содержащую полный набор генов, называемую “мастерхромосомой”. Каждая “мастерхромосома” содержит протяженные и короткие повторяющиеся последовательности. Между копиями протяженных повторяющихся последовательностей происходит рекомбинация, благодаря чему образуются разнообразные изомерные формы мт. ДНК. Короткие повторы обычно неактивны и, в основном, не способны к рекомбинации. Считают, что у покрытосеменных они, по всей видимости, играют центральную роль в эволюции митохондриальных геномов. Кроме кольцевых молекул, в митохондриях некоторых растений встречаются линейные молекулы ДНК, а также кольцевые и линейные плазмиды. Наличие линейных плазмид в митохондриях свойственно растениям и грибам. В митохондриях животных клеток линейные плазмиды не встречаются. Поэтому реально митохондриальный геном растений представляет собой смесь различных молекул ДНК.

В составе мт. ДНК содержится от 25 (у хламидомонады) до 104 (у печеночника) генов. У высших растений мт. ДНК содержит 50– 60 генов. Гены составляют 7– 17% митохондриального генома покрытосеменных. Некоторые межгенные участки содержат последовательности хп. ДНК (1. 6– 6. 2% генома) и я. ДНК (0. 1– 13. 4% генома). Такая “смешанная” ДНК не обнаружена в митохондриальных геномах животных клеток. Состав генов т. РНК в митохондриях растений уникален. Покрытосеменные растения со держат 15– 21 генов т. РНК. Часть генов т. РНК обладает значительной гомологией с генами хп. ДНК. Нуклеотидные последовательности остальных генов не соответствуют последовательностям т. РНК ни одного из известных источников. Для митохондрий растений типичен импорт молекул т. РНК из цитозоля. При секвенировании митохондриальных геномов было установлено, что в них отсутствуют обычно гены т. РНК аланина, аргинина, лейцина, треонина и валина (соответствующие т. РНК, вероятно, импортируются). У некоторых растений, например, у A. thaliana, импортируются также т. РНК фенилаланина, метионина и триптофана [4]. Молекулы т. РНК, как предполагают, поступают в митохондрии через потенциалзависимые анионные каналы наружной мембраны.

МИТОХОНДРИАЛЬНАЯ РЕТРОГРАДНАЯ РЕГУЛЯЦИЯ У РАСТЕНИЙ Наиболее хорошо изученной моделью с точки зрения МРР являются дрожжи Saccharomyces cerevisiae. Клетки дрожжей S. cerevisiae в ответ на нарушение функций митохондрий изменяют азотный и углеродный обмен. Обмен сдвигается таким образом, чтобы сохранить уровень глутамата путем восстановления уровня интермедиатов ЦТК. Глутамат является источником всего азота, используемого клетками S. cerevisiae в биосинтетических реакциях. Основные данные о Экспрессия ряда ядерных генов растений активируется в ответ на нарушения мт. ЭТЦ, ЦТК, а также мт. ДНК. Дисфункция митохондрий, вызванная мутациями, у растений часто приводит к мужской стерильности, летальному фенотипу зародышей или к возникновению хлоротичности у растений, которые не доживают до созревания семян. Кроме того, дисфункция митохондрий у растений может вызываться абиотическими и биотическими стрессами. Получено большое число доказательств того, что митохондрии вносят существенный вклад в общий ответ растения на стресс.
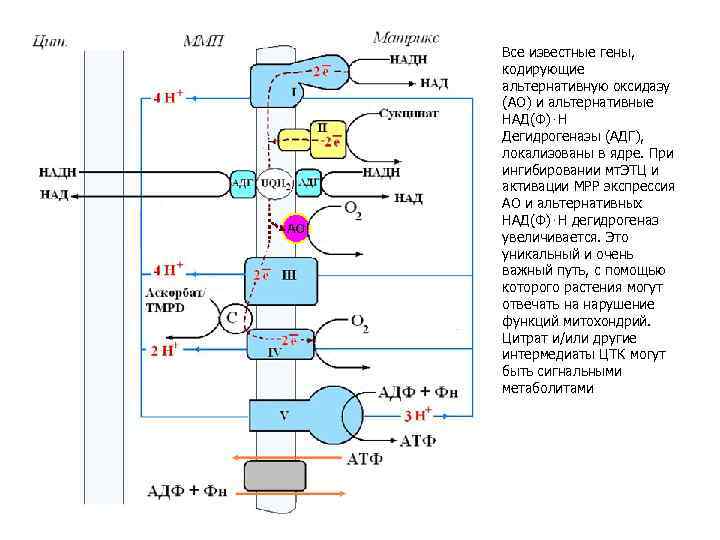
Все известные гены, кодирующие альтернативную оксидазу (АО) и альтернативные НАД(Ф)⋅Н Дегидрогеназы (АДГ), локализованы в ядре. При ингибировании мт. ЭТЦ и активации МРР экспрессия АО и альтернативных НАД(Ф)⋅Н дегидрогеназ увеличивается. Это уникальный и очень важный путь, с помощью которого растения могут отвечать на нарушение функций митохондрий. Цитрат и/или другие интермедиаты ЦТК могут быть сигнальными метаболитами

Цитоплазматическая мужская стерильность (ЦМС) – неспособность растений образовывать жизнеспособную пыльцу – вызывается сигналами митохондрий и является одним из наиболее часто приводимых примеров МРР у растений. Дисфункция митохондрий, вызванная мутациями, часто приводит к мужской стерильности. Изменения в мт. ДНК или экспрессии митохондриальных генов индуцируют изменения экспрессии ядерных генов, ведут к модифицированному фенотипу тычинок и, в конечном счете, к ингибированию образования пыльцы. ЦМС – широко распространенное и разнообразное явление, обнаруженное более, чем у 150 видов, которое часто встречается у гибридных линий, полученных при внутри или межвидовых скрещиваниях, т. е. у аллоплазматических линий, у которых ядро одного вида объединено с цитоплазмой другого вида. Растения с ЦМС используются в сельском хозяйстве для получения гибридов экономически важных сельскохозяйственных культур, таких как Zea mays, Beta vulgaris, Brassica napus, Sorhum bicolor, Helianthus annuus.

То, что ЦМС вызывается нарушениями взаимодействия ядра с митохондрия ми, доказано материнской наследуемостью фенотипа мужской стерильности и подавлением мужской стерильности с помощью ядерных генов “восстановителей фертильности” (Rfгены). Эти гены (кроме одного) кодируют белки, относящиеся к семейству белков, содержащих пентатрикопептидные повторы (PPRбелки). Предполагают, что у Arabidopsis PPRбелки локализованы в митохондриях или пластидах. Некоторые из них участвуют в процессинге разных видов РНК в органеллах.

МРР В ОТВЕТНЫХ РЕАКЦИЯХ КЛЕТОК НА ДЕЙСТВИЕ СТРЕССОВ Митохондрии растений реагируют на абиотические и биотические стрессы. Они могут служить сенсорами стрессов и инициировать ответные реакции (или участвовать в ответных реакциях) на от дельные виды стрессов. МРР участвует в ответной реакции растительных клеток на кислородный стресс. Известно, что в определенных условиях (например, при затоплении) кислород является ограничивающим фактором для роста и выживания растений. Растения также испытывают гипоксию в процессе нормального роста и развития, так как в тканях с плотно расположенными клетками и небольшими межклеточными пространствами диффузия кислорода незначительна. Известно также, что даже приспособившиеся к наземным условиям растения обладают значительной толерантностью к недостатку кислорода, что указывает на наличие у них высокочувствительной кислородсенсорной системы и мощных ответных реакций на кислородный стресс. Адаптация к быстро изменяющемуся уровню кислорода включает быстрые изменения экспрессии генов (потенциально индуцированные предшествующими быстрыми изменениями уровня АФК и/или редокс состояния и/или энергетического статуса), позволяющими скорректировать метаболизм (например, снизить поступление углерода в ЦТК с параллельным увеличением поступления углерода в гликолитические и ферментативные пути). Реакции, ведущие к запрограммированной гибели клеток (ЗГК), также являются частичным ответом растений на анаэробиоз.

Показано, что ионы Са 2+ являются существенным компонентом связанного с гипоксией сигнального пути у Arabidopsis, риса и ячменя, что указывает на консерватизм этого пути у растений. Вывод о том, что митохондрии являются источником [Са 2+]цит сигнала, который инициирует активацию ядерных генов, подтвержден динамикой митохондриального Са 2+ ([Са 2+]мт) в ответ на аноксию. При этом было показано, что освобождение [Са 2+]мт происходит в клетках кукурузы сразу же после прекращения поступления кислорода. На экспрессию БТШ может влиять индуцированная теплом МРР. Общим компонентом абиотических стрессов является окислительный стресс, вызываемый образованием АФК. Окислительный стресс может вызывать дисфункцию митохондрий у растений и приводить к инактивации определенных гормональных сигналов. Использование протеомного под хода для идентификации митохондриальных компонентов, чувствительных к окислительному повреждению, показало, что ими являются ферменты ЦТК, компоненты мт. ЭТЦ и окислительного фосфорилирования [49]. В листьях особенно чувствительной к окислительному повреждению, вызван ному охлаждением или засухой, оказалась глициндекарбоксилаза, фермент фотодыхательного пути.

Установлено, что митохондрии, в частности МРР, играют важную роль в ответных реакциях растений на атаку патогенов. В этих условиях усиливается дыхание, что может быть обусловлено повышенными потребностями клеток в энергии при инфекции, а также усиленным образованием мт. АФК в результате ингибирования дыхания, вызванного патогеном. Наиболее строгим доказательством участия МРР в ответе растений на действие патогенов является то, что ряд токсинов, образуемых патогенами растений, называемых элиситорами, нарушают функцию митохондрий и индуцируют экспрессию ядерных генов. Харпин является элиситором бактериальных патогенов, включая Pseudomonas syringae, который индуцирует сверхчувствительную реакцию и нарушает синтез АТФ в культуре клеток табака и суспензионной культуре клеток Arabidopsis. Сверхчувствительная реакция растений на заражение патогенном – это форма ЗГК, которая локализована в месте внедрения патогена и направлена на то, что бы ограничить его распространение.

Большой интерес представляет взаимодействие ретроградных сигнальных систем пластид и митохондрий, поскольку эти сигналы регулируют экспрессию ядерных генов органелл в зависимости от функционального состояния последних. Известно, что хлоропласты и митохондрии взаимосвязаны метаболически. Фотосинтез снабжает субстратами дыхание митохондрий и зависит, в свою очередь, от ряда соединений, синтезируемых митохондриями. В темноте митохондрии являются основным источником АТФ для клеточных процессов, включая таковые в хлоропластах. Кроме того, в темноте АТФ поддерживает протонный градиент через тилакоидную мембрану, защищая, таким образом, хлоропласты от фотоингибирования после начала освещения. На свету митохондрии снабжают хлоропласты соединениями углерода, полученными из ЦТК, для ассимиляции в то время как АТФ поддерживает различные биосинтетические реакции, включая восстановление функций ФС II. Предполагают, что роль сигналов между митохондриями и хлоропластами могут выполнять оксид азота, аскорбат и АФК. Однако, как соответствующие сигналы передаются от органелл к ядру и как они включаются в общую систему регуляции экспрессии, пока неизвестно.
УМКД_ФР(дыхание).ppt
- Количество слайдов: 40

