ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ СРЕДНЕГО


ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ СРЕДНЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «КРАСНОЯРСКИЙ МЕДИКО-ФАРМАЦЕВТИЧЕСКИЙ КОЛЛЕДЖ ФЕДЕРАЛЬНОГО АГЕНТСТВА ПО ЗДРАВООХРАНЕНИЮ И СОЦИАЛЬНОМУ РАЗВИТИЮ» Лекция № 12 тема: Кислородсодержащие органические соединения Преподаватель Ростовцева Л. В. , 2010 г.

Кислородсодержащие органические соединения План лекции: 1. Классификация кислородсодержащих органических соединений 2. Спирты. Фенолы 3. Альдегиды 4. Карбоновые кислоты 5. Триглицериды (жиры)
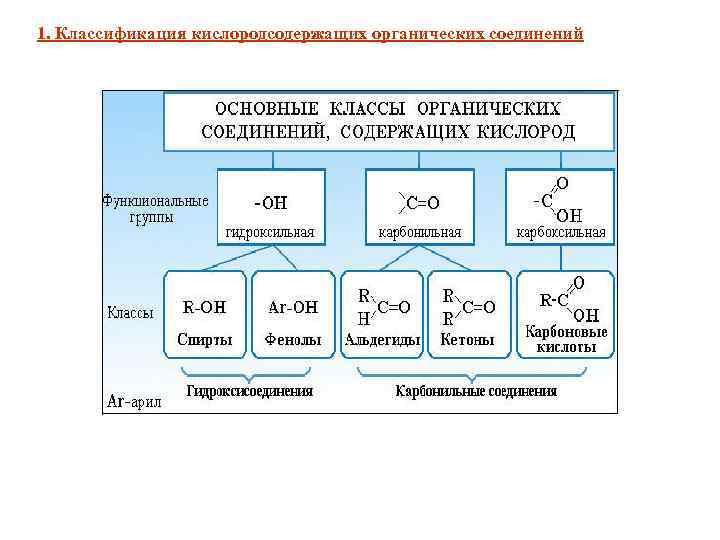
1. Классификация кислородсодержащих органических соединений

2. Спирты. Фенолы Спирты (алкоголи) - производные углеводородов, содержащие в молекуле одну или несколько гидроксильных групп – ОН у насыщенных атомов углерода. R (ОН)m m ≥ 1, определяет атомность спирта
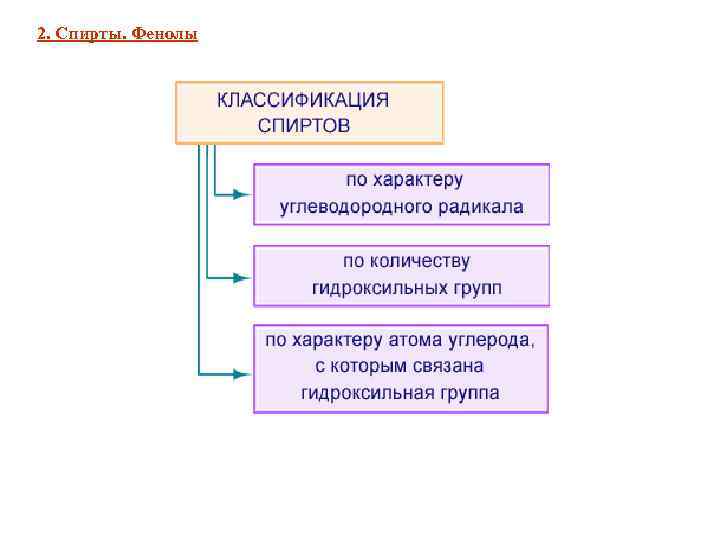
2. Спирты. Фенолы
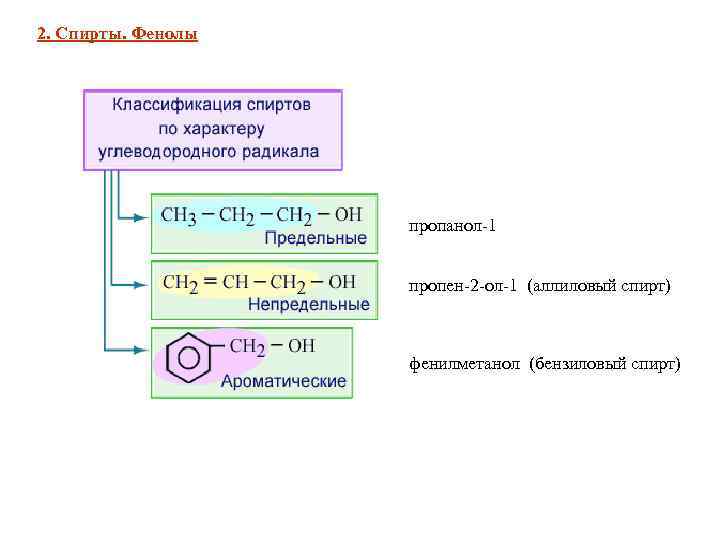
2. Спирты. Фенолы пропанол-1 пропен-2 -ол-1 (аллиловый спирт) фенилметанол (бензиловый спирт)
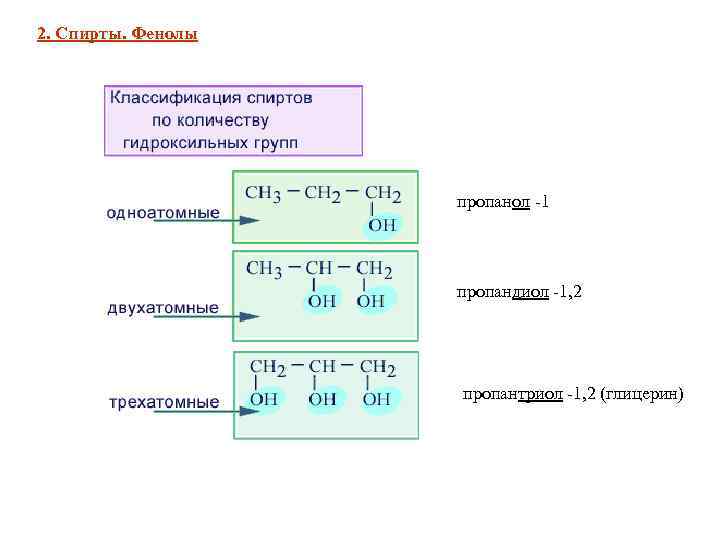
2. Спирты. Фенолы пропанол -1 пропандиол -1, 2 пропантриол -1, 2 (глицерин)
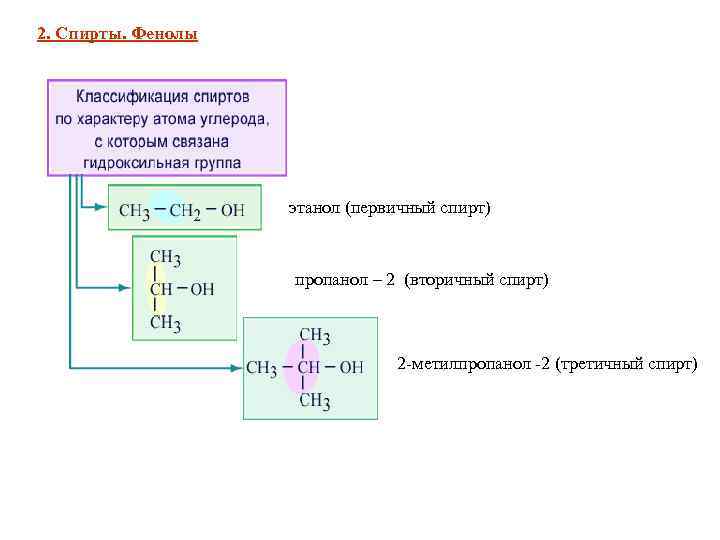
2. Спирты. Фенолы этанол (первичный спирт) пропанол – 2 (вторичный спирт) 2 -метилпропанол -2 (третичный спирт)

2. Спирты. Фенолы Предельные одноатомные спирты (алканолы) Сп. Н 2 п+1 ОН, п ≥ 1 СН 3 ОН метанол (метиловый спирт) С 2 Н 5 ОН этанол (этиловый спирт) С 3 Н 7 ОН пропанол (пропиловый спирт) С 4 Н 9 ОН бутанол (бутиловый спирт)

2. Спирты. Фенолы Характерные виды изомерии 1. изомерия углеродной цепи (начиная с бутанола) 2. изомерия положения функциональной группы – ОН (начиная с пропанола) 3. межклассовая изомерия (начиная с этанола)

2. Спирты. Фенолы Электронное строение Н ↓δ+ δ- δ+ R → С→О←Н ↑ Н

2. Спирты. Фенолы Физические свойства спиртов Для спиртов характерно образование межмолекулярных водородных связей Поэтому в гомологическом ряду спиртов нет газообразных веществ. Все алканолы легче воды, жидкие имеют резкий запах, твердые запаха не имеют. Метанол, этанол пропанол неограниченно растворяются в воде, с ↑ числа атомов углерода растворимость алканолов в воде уменьшается, высшие спирты в воде не растворяются.

2. Спирты. Фенолы Химические свойства предельных одноатомных спирты 1. Реакции замещения атома водорода гидроксильной группы вследствие разрыва связи О─Н а) взаимодействие с активными металлами 2 С 2 Н 5 О[ + 2 Na Н 2 C 2 H 5 ONa + H 2↑ б) взаимодействие с органическими и неорганическими кислотами с образованием сложных эфиров – реакция этерификации С 2 Н 5 О [ + НО]ОС─СН 3 Н СН 3 – СО─О – С 2 Н 5 + Н 2 О этиловый эфир уксусной кислоты (этилацетат)

2. Спирты. Фенолы 2. Реакции замещения гидроксильной группы вследствие разрыва связи С─О а) взаимодействие с галогеноводородами б) взаимодействие с аммиаком с образованием аминов С 2 Н 5[ОН +Н]NН 2 С 2 Н 5─NН 2 + Н 2 О (Аl 2 О 3, t=3000 С) этиламин

2. Спирты. Фенолы 3. Реакции отщепления а) дегидратация • межмолекулярная с образованием простых эфиров 2 • внутримолекулярная с образованием алкенов

2. Спирты. Фенолы б) дегидрирование (реакция окисления) При дегидрировании первичных спиртов образуются альдегиды При дегидрировании вторичных спиртов образуются кетоны: Третичные спирты не дегидрируются

2. Спирты. Фенолы 4. Реакции окисления а) горение С 2 Н 5 ОН + 3 О 2 2 СО 2↑+3 Н 2 О +Q б) неполное окисление под действием окислителей (кислород воздуха в присутствии катализатора (например, Сu. О), KMn. O 4 , K 2 Cr 2 O 7 и др. ) С 2 Н 5 ОН + [O]
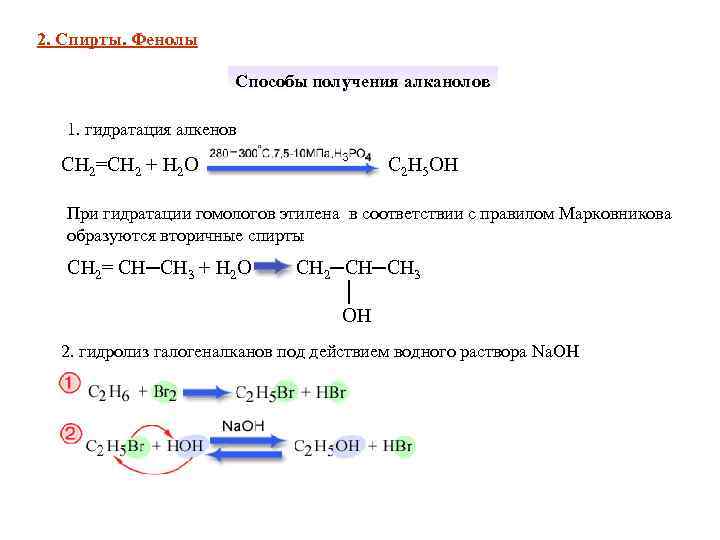
2. Спирты. Фенолы Способы получения алканолов 1. гидратация алкенов СН 2=СН 2 + Н 2 О С 2 Н 5 ОН При гидратации гомологов этилена в соответствии с правилом Марковникова образуются вторичные спирты СН 2= СН─СН 3 + Н 2 О СН 2─СН─СН 3 │ ОН 2. гидролиз галогеналканов под действием водного раствора Nа. ОН
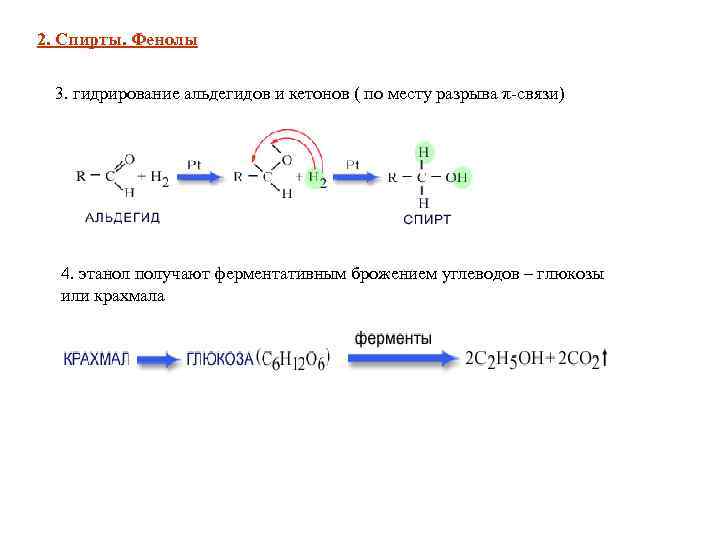
2. Спирты. Фенолы 3. гидрирование альдегидов и кетонов ( по месту разрыва π-связи) 4. этанол получают ферментативным брожением углеводов – глюкозы или крахмала

2. Спирты. Фенолы Предельные многоатомные спирты этандиол -1, 2 пропантриол -1, 2, 3

2. Спирты. Фенолы Глицерин По физическим свойствам глицерин – бесцветная , сладковатая на вкус, нетоксичная жидкость, с t кип = 2900 С, очень хорошо растворима в воде Химические свойства 1. Так же как одноатомные спирты взаимодействует со щелочными металлами СН 2─О[Н СН 2─ОNа │ СН─О[Н + 2 Nа СН─ОNа + Н 2 │ СН 2─ОН СН 2─ОН

2. Спирты. Фенолы 2. Реакция с органическими и неорганическими кислотами с образованием сложных эфиров (реакция этерификации) 3. Взаимодействие с галогеноводородами СН 2─[ОН СН 2─Cl │ СН ─ОН + Н]Сl СН─ОH + Н 2 O │ СН 2─ОН монохлоргидрин глицерина

2. Спирты. Фенолы 3. Качественная реакция на глицерин ярко-синий раствор

2. Спирты. Фенолы Способы получения глицерина 1. Гидролиз жиров СН 2─О─СО─ R 1 СН 2─ОН │ │ СН─О─СО─ R 2 + 3 Н 2 О СН─ОН + 3 R─СООН │ │ СН 2─О─СО─ R 3 СН 2 ОН Гидролиз протекает под действием кислот, щелочей, а также ферментов.

2. Спирты. Фенолы - производные ароматических углеводородов, содержащие одну или несколько гидроксильных групп у атомов углерода бензольного кольца. С 6 Н 5 ОН
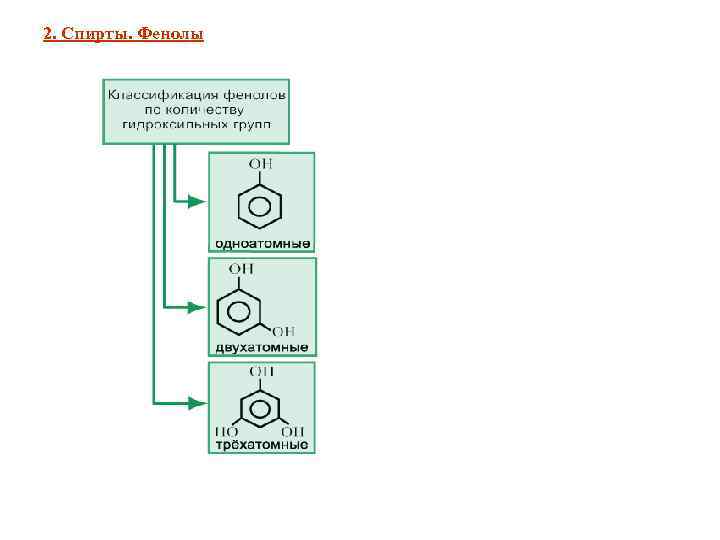
2. Спирты. Фенолы
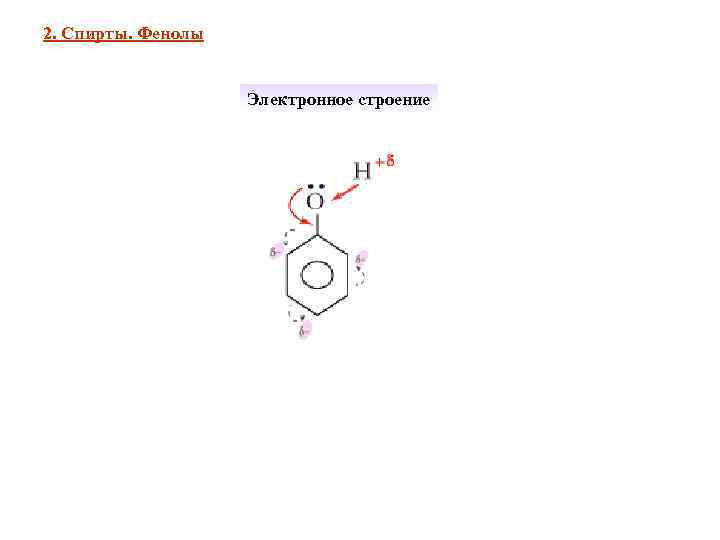
2. Спирты. Фенолы Электронное строение
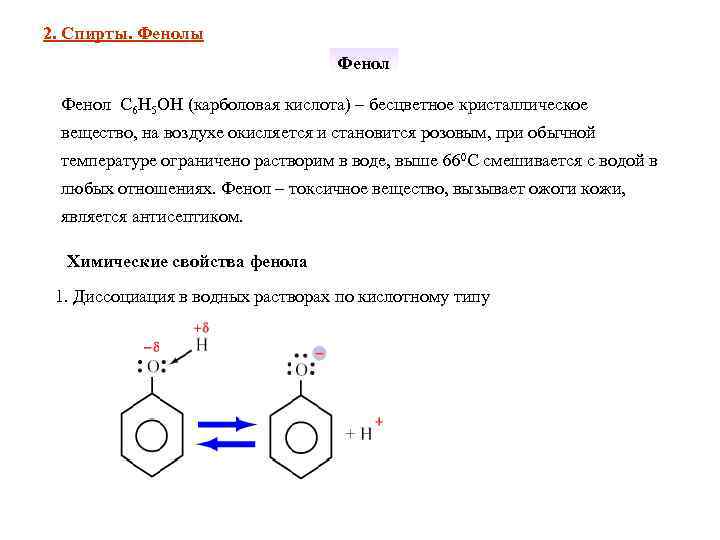
2. Спирты. Фенолы Фенол С 6 Н 5 ОН (карболовая кислота) – бесцветное кристаллическое вещество, на воздухе окисляется и становится розовым, при обычной температуре ограничено растворим в воде, выше 660 С смешивается с водой в любых отношениях. Фенол – токсичное вещество, вызывает ожоги кожи, является антисептиком. Химические свойства фенола 1. Диссоциация в водных растворах по кислотному типу
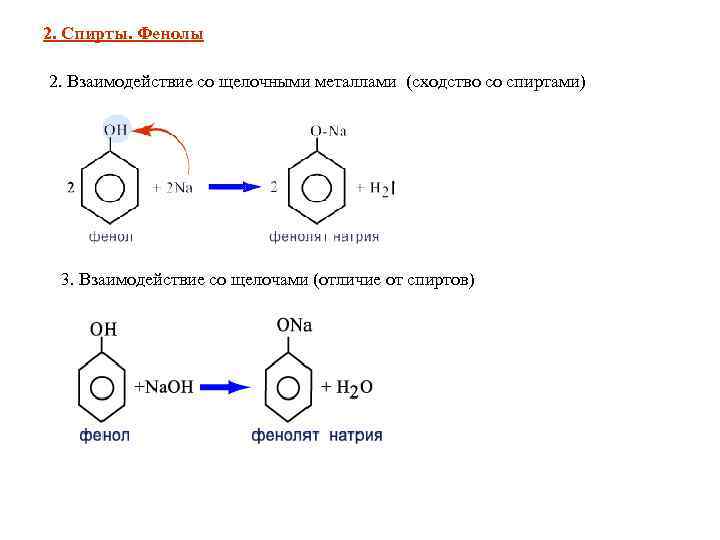
2. Спирты. Фенолы 2. Взаимодействие со щелочными металлами (сходство со спиртами) 3. Взаимодействие со щелочами (отличие от спиртов)
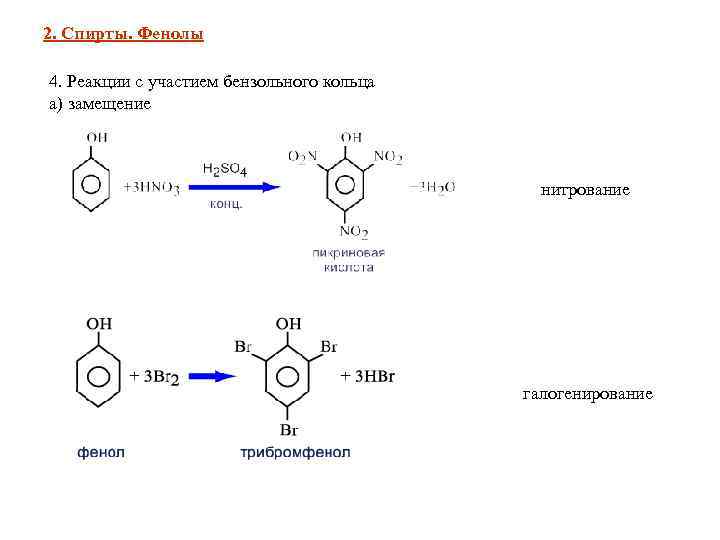
2. Спирты. Фенолы 4. Реакции с участием бензольного кольца а) замещение нитрование галогенирование
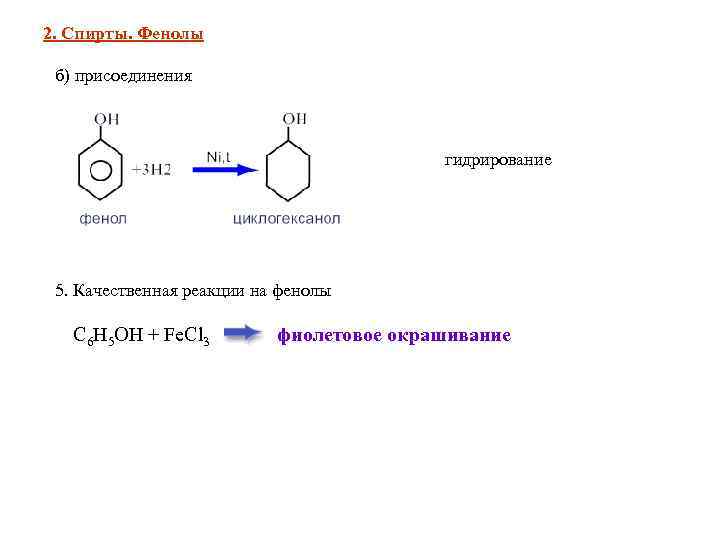
2. Спирты. Фенолы б) присоединения гидрирование 5. Качественная реакции на фенолы С 6 Н 5 ОН + Fe. Cl 3 фиолетовое окрашивание
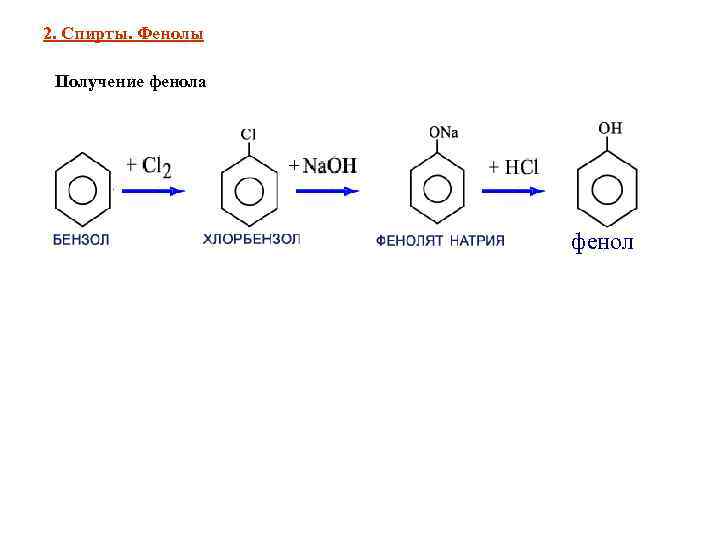
2. Спирты. Фенолы Получение фенола + фенол

3. Альдегиды - органические соединения, молекулы которых содержат альдегидную группу, связанную с углеводородным радикалом
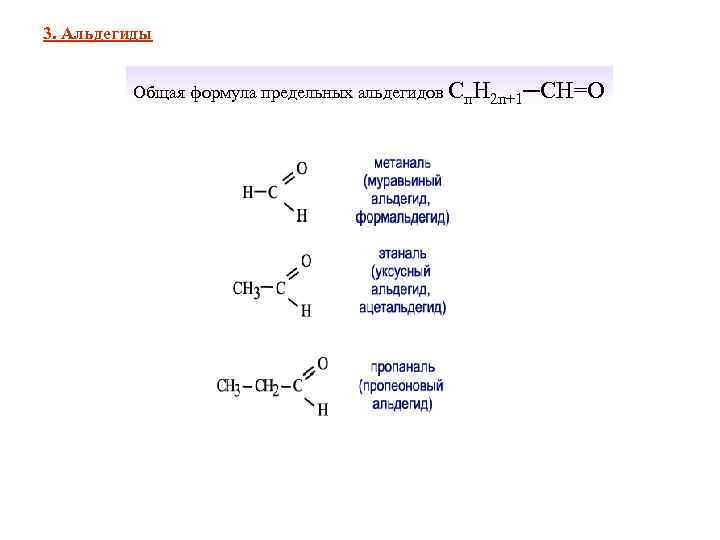
3. Альдегиды Общая формула предельных альдегидов Сп. Н 2 п+1─СН=О
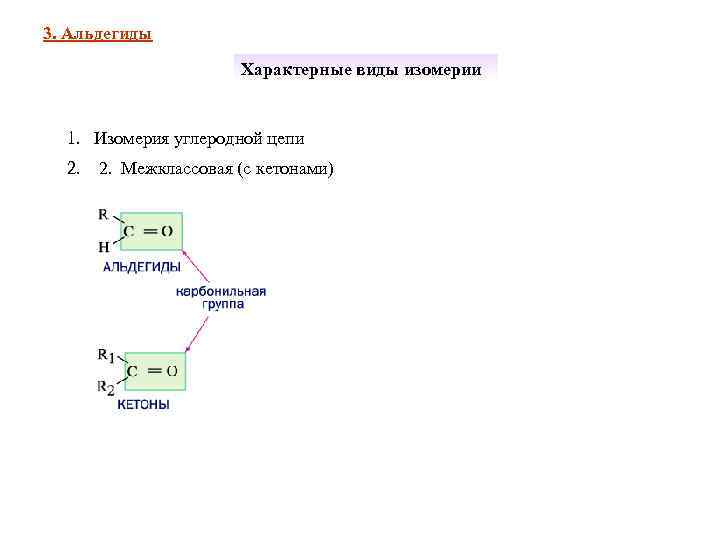
3. Альдегиды Характерные виды изомерии 1. Изомерия углеродной цепи 2. 2. Межклассовая (с кетонами)
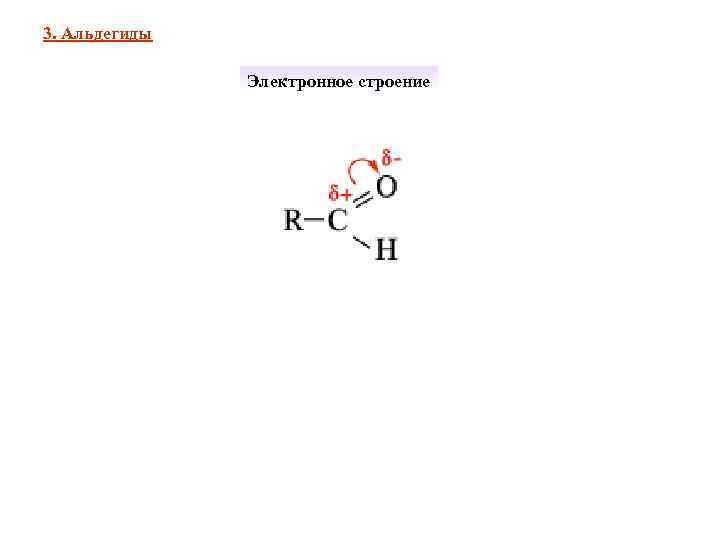
3. Альдегиды Электронное строение

3. Альдегиды Физические свойства альдегидов Низшие альдегиды имеют резкий запах, высшие - от 8 -12 атомов С – душистые вещества. С ↑ числа атомов С растворимость альдегидов в воде уменьшается, все альдегиды растворяются в органических растворителях. Альдегиды раздражают слизистые оболочки глаз и верхних дыхательных путей, вредно влияют на нервную систему.
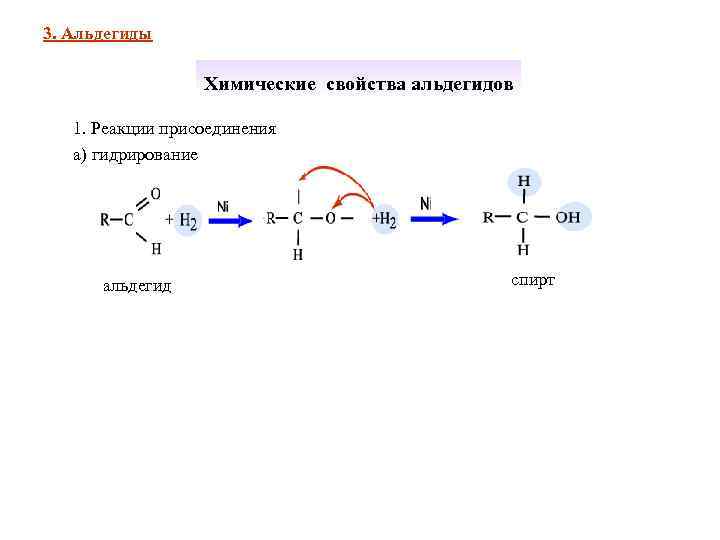
3. Альдегиды Химические свойства альдегидов 1. Реакции присоединения а) гидрирование альдегид спирт

3. Альдегиды 2. Реакции окисления а) реакция «серебряного зеркала» СН 3 СН=О + Ag 2 O СН 3 СООН + 2 Ag↓ (t 0 , NH 4 OH) б) взаимодействие с гидроксидом меди (II) Cu. SO 4 + 2 Na. OH Cu(OH)2↓ + Na 2 SO 4 голубой СН 3 СН=О + Cu(OH)2 СН 3 СООН + Cu 2 O↓ + 2 Н 2 О кирпично-красный Реакции с аммиачным раствором оксида серебра и гидроксидом меди (II) являются качественными реакциями на альдегиды.

3. Альдегиды 3. Реакции полимеризации и поликонденсации n (СН 2 О)п параформальфегид
12. Кислородсодержащие органические соединения.ppt
- Количество слайдов: 40

