7e2d66710c86379c95d866d930016dc2.ppt
- Количество слайдов: 20

ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ УЧРЕЖДЕНИЕ «НАУЧНЫЙ ЦЕНТР ЭКСПЕРТИЗЫ СРЕДСТВ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ» МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ 13. 10. 2016, 16. 15 -17. 45 Нежелательные явления, прерывание и окончание исследования, выход из исследования РОМАНОВ Борис Константинович заместитель генерального директора, доктор медицинских наук © - Романов Б. К. , 2016 1
ИДЕАЛЬНАЯ МОДЕЛЬ Интересы науки, общества и бизнеса Права, безопасность и здоровье испытуемого [ОСТ 42 -511 -99, и др. ] © - Романов Б. К. , 2016 2

ДЕЙСТВУЮЩИЕ НОРМАТИВНЫЕ ТРЕБОВАНИЯ И РЕКОМЕНДАЦИИ 1. Хельсинкская Декларация Всемирной Медицинской Ассоциации 1964 г. 2. Международные гармонизированные трёхсторонние правила GCP (ICH GCP) 1997 г. 3. Федеральный закон от 12 апреля 2010 г. N 61 -ФЗ «Об обращении лекарственных средств» (61 -ФЗ) 4. Приказ МЗ РФ от 1 апреля 2016 г. N 200 н (вступил в силу 4. 09. 2016) «Об утверждении правил надлежащей клинической практики» (Пр. 200 н) 5. Стандарт отрасли ОСТ 42 -511 -99, утвержден МЗ РФ 29 декабря 1998 г. «Правила проведения качественных клинических испытаний в РФ» 6. Руководства по проведению КИ ЛС 2012 г. (Том 1 -2), по экспертизе ЛС 2013 г. (Том 1 -4) ДОКУМЕНТЫ КИ 1. Разрешение на проведение КИ [61 -ФЗ: п. 4 Ст. 38 и Ст. 39 + Пр. 200 н: п. 5] 2. Протокол исследования [61 -ФЗ: п. 47 Ст. 4 + Пр. 200 н: п. 7 + ОСТ: п. 2. 47] 3. Брошюра исследователя [61 -ФЗ: п. 48 Ст. 4 + Пр. 200 н: п. 8 + ОСТ: п. 2. 2 и Раздел 8] 4. Информационный листок пациента [61 -ФЗ: п. 49 Ст. 4 + Пр. 200 н: п. 52, п. 55] 5. Отчет о результатах КИ [61 -ФЗ: п. 7 Ст. 18, п. 11 Ст. 40 + Пр. 200 н: п. 8] 6. Все подлинные документы, данные и записи в любой форме, которые описывают или регистрируют методы, проведение, организацию и (или) результаты КИ, возникающие сложности и способы их преодоления [Пр. 200 н: п. 59 + ОСТ: п. 2. 6 , 2. 39 и 2. 40], в том числе – Информированное согласие [ОСТ: п. 2. 12] и Индивидуальная карта испытуемого [ОСТ: п. 2. 10 ]. © - Романов Б. К. , 2016 3

ПОТЕНЦИАЛЬНЫЕ РИСКИ (ЧТО ПЛОХОГО МОЖЕТ ПРОИЗОЙТИ С ИСПЫТУЕМЫМ ? ) Нежелательные последствия применения ЛП в КИ: 1. Неэффективность или недостаточное действие (Тип F) 2. Передозировка или избыточное действие (Тип А, Тип С) 3. Побочное действие: - нежелательное явление; - нежелательная реакция, в том числе (для вакцин): - поствакцинальное осложнение (ПВО) 4. Неблагоприятные взаимодействия между собой или с пищей. 5. Нарушения применения: - намеренное применение «вне инструкции» (off-label) - намеренное и ненадлежащее применение (missuse) - ошибка применения лекарственного препарата (medication error) - злоупотребления (abuse) 6. Неблагоприятное воздействие на окружающую среду. © - Романов Б. К. , 2016 4

ОСНОВНЫЕ ТЕРМИНЫ И ИХ ОПРЕДЕЛЕНИЯ (1 из 2) Здоровье испытуемых – физическое и психическое благополучие испытуемых, участвующих в клиническом испытании [ОСТ: п. 2. 9] Побочные эффекты лекарств – для незарегистрированного ЛС или при его изучении по новым показаниям, особенно, если терапевтические дозы препарата точно не установлены, к побочным лекарственным эффектам относятся все отрицательные или непредвиденные реакции, связанные с введением любой дозы ЛП. Термин "связанные с введением лекарственного препарата" означает, что существует хотя бы минимальная вероятность причинно - следственной связи между ЛС и нежелательным явлением [ОСТ: п. 2. 41] Нежелательные явления – выявленные у больного или испытуемого любые нежелательные или непредвиденные симптомы (включая патологические изменения лабораторных показателей), жалобы или заболевания, которые связаны во времени с использованием лекарственного (исследуемого) препарата, независимо от наличия причинной связи с его применением [ОСТ: п. 2. 32] Побочное действие – реакция организма, возникшая в связи с применением ЛП в дозах, рекомендуемых в инструкции по его применению, для профилактики, диагностики, лечения заболевания или для реабилитации [61 -ФЗ: п. 50 Ст. 4] Нежелательная реакция - непреднамеренная неблагоприятная реакция организма, которая может быть связана с применением ЛП [61 -ФЗ: п. 50. 1 Ст. 4, введен ФЗ от 22. 12. 2014 N 429 -ФЗ ] © - Романов Б. К. , 2016 5

ОСНОВНЫЕ ТЕРМИНЫ И ИХ ОПРЕДЕЛЕНИЯ (2 из 2) Серьезная нежелательная реакция - нежелательная реакция организма, связанная с применением лекарственного препарата, приведшая к смерти, врожденным аномалиям или порокам развития либо представляющая собой угрозу жизни, требующая госпитализации или приведшая к стойкой утрате трудоспособности и (или) инвалидности[61 -ФЗ: п. 51 Ст. 4] Непредвиденная нежелательная реакция - нежелательная реакция организма, которая связана с применением ЛП в дозах, рекомендуемых в протоколе его клинического исследования, брошюре исследователя, или с применением ЛП в дозах, рекомендуемых в инструкции по его применению для профилактики, диагностики, лечения заболевания или медицинской реабилитации пациента, и сущность, тяжесть или исход которой не соответствует информации о ЛП, содержащейся в протоколе его клинического исследования, брошюре исследователя или в инструкции по применению ЛП [61 -ФЗ: п. 52 Ст. 4, введен ФЗ от 22. 12. 2014 N 429 -ФЗ ] © - Романов Б. К. , 2016 6
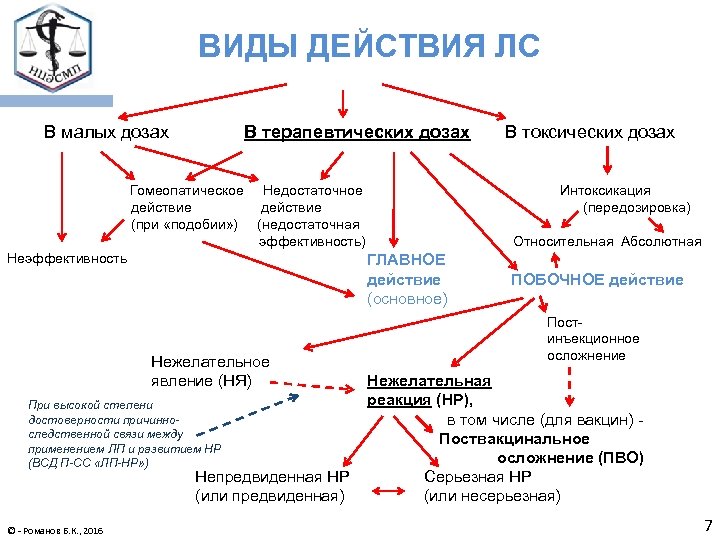
ВИДЫ ДЕЙСТВИЯ ЛС В малых дозах В терапевтических дозах Гомеопатическое действие (при «подобии» ) Недостаточное действие (недостаточная эффективность) Неэффективность При высокой степени достоверности причинноследственной связи между применением ЛП и развитием НР (ВСД П-СС «ЛП-НР» ) Непредвиденная НР (или предвиденная) © - Романов Б. К. , 2016 Интоксикация (передозировка) Относительная Абсолютная ГЛАВНОЕ действие (основное) Нежелательное явление (НЯ) В токсических дозах ПОБОЧНОЕ действие Постинъекционное осложнение Нежелательная реакция (НР), в том числе (для вакцин) Поствакцинальное осложнение (ПВО) Серьезная НР (или несерьезная) 7

ОЦЕНКА ВЗАИМОСВЯЗИ (оценка СД П-СС «ЛП-НЯ» при проведении КИ) СД П-СС 1. Связано Критерии оценки СД П-СС «ЛП – НЯ» ( «Руководство по экспертизе» , 2013, Т. 3) Клинические проявления НЯ, нарушения лабораторных показателей возникают в период приема препарата, не могут быть объяснены наличием существующих заболеваний или влиянием других факторов. Проявления НЯ регрессируют после отмены препарата и возникают вновь при повторном применении препарата 2. Вероятно связано Клинические проявления НЯ, нарушения лабораторных показателей связаны по времени с приемом препарата, не могут быть объяснены наличием существующих заболеваний или влиянием других факторов. Проявления НЯ регрессируют после отмены препарата. Препарат не применялся повторно или не известна реакция на повторное применение препарата 3. Возможно связано Клинические проявления НЯ, изменения лабораторных показателей связаны по времени с приемом препарата, но их можно объяснить наличием сопутствующих заболеваний или влиянием других факторов (например, приемом других препаратов или иных веществ). Информация о реакции на отмену препарата отсутствует 4. Неизвестно Проявления, отнесенные к НЯ, трудно оценивать. Необходимы дополнительные данные для оценки, или же эти данные в настоящее время анализируются 5. Не связано Клин. проявления НЯ, нарушения лаборат. показателей могут быть объяснены наличием существующих заболеваний или влиянием других факторов © - Романов Б. К. , 2016 8
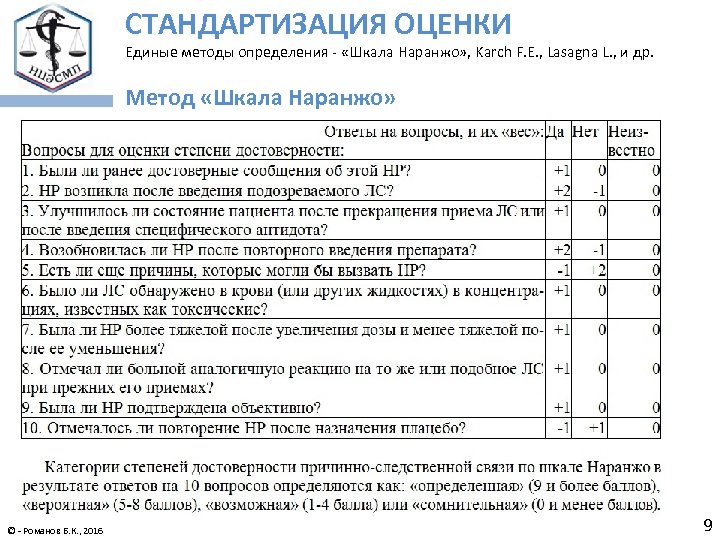
СТАНДАРТИЗАЦИЯ ОЦЕНКИ Единые методы определения - «Шкала Наранжо» , Karch F. E. , Lasagna L. , и др. Метод «Шкала Наранжо» © - Романов Б. К. , 2016 9

ТИПЫ НЕЖЕЛАТЕЛЬНЫХ РЕАКЦИЙ Тип А – избыточные (усиленные) фармакологические эффекты, дозозависимые и предсказуемые. ДЛЯ ВЫЯВЛЕНИЯ ЭТОГО ТИПА – ХОРОШО ПОДХОДЯТ КИ Органотоксичность. Причины относительной передозировки: сопутствующая патология, реакции I-II фазы метаболизма, взаимодействия, . Тип В – дозонезависимые Аллергия, идиосинкразия (иммуннопатии, НР неизвестного генеза). Тип С – НР вследствие длительной терапии. Диагностика затруднительна. Кумуляция, зависимость, подавление выработки эндогенных веществ. Тип D – отсроченные эффекты. Диагностика еще более затруднительна. Канцерогенность, мутагенность, тератогенность. Коды классификации НЯ и НР 1. Med. DRA (Medical Dictionary for Regulatory Activities, Медицинский словарь терминологии регулятивной деятельности), 2. WHO-Art (World Health Organization Adverse Reaction Terminology, Словарь терминов нежелательных реакций ВОЗ). © - Романов Б. К. , 2016 10

БЕЗОПАСНОСТЬ – ОТНОСИТЕЛЬНОСТЬ ХАРАКТЕРИСТИКИ Безопасность лекарственного средства - характеристика лекарственного средства, основанная на сравнительном анализе его эффективности и риска причинения вреда здоровью [61 -ФЗ: п. 23 Ст. 4] Эффективность лекарственного препарата - характеристика степени положительного влияния лекарственного препарата на течение, продолжительность заболевания или его предотвращение, реабилитацию, на сохранение, предотвращение или прерывание беременности [61 -ФЗ: п. 24 Ст. 4] Методы оценки отношения польза/риск 1. Качественные методы: «Метод троек» (Edwards R, 1996). 2. Полуколичественные методы: «TURBO–модель» (Edwards R, 1996). 3. Количественные методы (15): Quantitative Framework for Risk and Benefit Assessment (QFRBA); Benefit-less-risk analysis (BLRA); Quality-adjusted Time Without Symptoms and Toxicity (Q-TWi. ST); Number needed to treat (NNT) and number needed to harm (NNH); Relative value adjusted number needed to treat (RV-NNT); Incremental net health benefit (INHB); Risk-benefit plane (RBP) and risk-benefit acceptability threshold (RBAT); Probabilistic simulation methods (PSM) and Monte Carlo simulation (MCS); Multicriteria decision analysis (MCDA); Risk-benefit contour (RBC); Stated preference method (SPM) or maximum acceptable risk (MAR). Оценка безопасности ЛС при проведении КИ Руководство по экспертизе ЛС, 2014, Том 1, Глава 6. «Структура и содержание отчетов о КИ» , стр. 131 - 173 1. Оценка степени безопасности – изучение величины воздействия (доза ЛС, длительность курса, кол-во испытуемых, включенных в КИ, и получивших хотя бы одну дозу ЛП) 2. Оценка НЯ и др. клинически значимых событий (изменения лабораторных показателей, другие нарушения, приводящие к вмешательству, отмене ЛП, снижению дозы, назначению доп. терапии), сгруппированных по Med. DRA и проанализированных по частоте возникновения, временной взаимосвязи (СД ПСС), взаимосвязи с демографическими характеристиками, дозой и др. 3. Оценка НЯ и др. клинически значимых событий у испытуемых, досрочно прекративших участие в КИ (независимо от приема ЛП) или скончавшихся © - Романов Б. К. , 2016 11

НР - ДЕЙСТВИЯ ИССЛЕДОВАТЕЛЯ (1 из 3) КИ ЛС для МП может быть приостановлено или прекращено, если в процессе его проведения обнаружена опасность для жизни, здоровья пациентов [61 -ФЗ: Ст. 40 п. 6]. В срок, установленный протоколом, исследователь обязан сообщать организатору клинического исследования обо всех серьезных нежелательных реакциях, за исключением тех, которые в протоколе или в брошюре определены как не требующие немедленного сообщения [Пр. 200 н: п. 56]. После первого сообщения о серьезных нежелательных реакциях исследователь в кратчайшие сроки представляет организатору клинического исследования подробный письменный отчет. Первый и последующие отчеты должны идентифицировать участников клинического исследования по присвоенным им уникальным кодам [Пр. 200 н: п. 56]. При сообщениях о смерти участника клинического исследования исследователь обязан по запросу организатора клинического исследования, независимого этического комитета, Министерства и (или) Федеральной службы по надзору в сфере здравоохранения предоставить любую дополнительную информацию относительно данного случая, в том числе протокол вскрытия и посмертный эпикриз [Пр. 200 н: п. 57] © - Романов Б. К. , 2016 12

НР - ДЕЙСТВИЯ ИССЛЕДОВАТЕЛЯ (2 из 3) В случае возникновения опасности для жизни, здоровья участника клинического исследования, исследователь обязан проинформировать об этом руководителя медицинской организации и организатора клинического исследования лекарственного препарата в течение 24 часов [Пр. 200 н: п. 58]. При досрочном прекращении клинического исследования или его приостановлении исследователь и (или) медицинская организация, в которой проводилось клиническое исследования обязаны незамедлительно информировать участников клинического исследования, обеспечить им необходимое лечение и наблюдение, проинформировать организатора клинического исследования, независимый этический комитет с предоставлением подробного письменного объяснения причин приостановления или прекращения клинического исследования [Пр. 200 н: п. 58]. © - Романов Б. К. , 2016 13

НР - ДЕЙСТВИЯ ИССЛЕДОВАТЕЛЯ (3 из 3) Исследователь сообщает в независимый этический комитет [Пр. 200 н: п. 49]: а) об отклонениях от протокола или изменениях протокола, произведенных для устранения угрозы жизни и (или) здоровью участника клинического исследования; б) об изменениях, непосредственно влияющих на проведение клинического исследования и (или) увеличивающих риск участия в клиническом исследовании; в) обо всех нежелательных реакциях, которые являются одновременно серьезными и непредвиденными; г) о новых данных, которые могут свидетельствовать о возрастании риска для участников клинического исследования или могут неблагоприятно повлиять на ход клинического исследования. © - Романов Б. К. , 2016 14

ОБЯЗАННОСТИ МОНИТОРА КИ Проверяет правильность и полноту регистрации в индивидуальной регистрационной карте данных, предусмотренных протоколом, данных об изменениях дозы и (или) терапии, о выявленных нежелательных явлениях и нежелательных реакциях, о пропущенных участником клинического исследования визитах, о невыполненных анализах и обследованиях. Все случаи исключения и выбывания участников клинического исследования из клинического исследования подлежат регистрации и пояснению в индивидуальной регистрационной карте[Пр. 200 н: п. 36, пп. к]. © - Романов Б. К. , 2016 15

ПРИОСТАНОВЛЕНИЕ ИЛИ ПРЕКРАЩЕНИЕ КИ – ДЕЙСТВИЯ РУКОВОДИТЕЛЯ МЕДИЦИНСКОЙ ОРГАНИЗАЦИИ, ОРГАНИЗАТОРА КИ и РЕГУЛЯТОРА Решение о приостановлении клинического исследования принимают руководитель медицинской организации и (или) организатор клинического исследования, решение о прекращении такого исследования принимает уполномоченный федеральный орган исполнительной власти на основании сообщения в письменной форме руководителя медицинской организации или организатора клинического исследования [Пр. 200 н: п. 58]. При досрочном прекращении клинического исследования или его приостановлении исследователь и (или) медицинская организация, в которой проводилось клиническое исследования обязаны незамедлительно информировать участников клинического исследования, обеспечить им необходимое лечение и наблюдение, проинформировать организатора клинического исследования, независимый этический комитет с предоставлением подробного письменного объяснения причин приостановления или прекращения клинического исследования [Пр. 200 н: п. 58]. © - Романов Б. К. , 2016 16

ОБЯЗАННОСТИ ОРГАНИЗАТОРА КИ … уведомляет всех занятых в клиническом исследовании исследователей и медицинские организации о полученных данных, которые могут неблагоприятно отразиться на безопасности участников клинического исследования и (или) повлиять на проведение клинического исследования [Пр. 200 н: п. 32]. Сообщает всем участвующим в клиническом исследовании исследователям, медицинским организациям и Федеральной службе по надзору в сфере здравоохранения обо всех серьезных и непредвиденных нежелательных реакциях, а также представляет в Федеральную службу по надзору в сфере здравоохранения периодические отчеты по безопасности исследуемого препарата в установленном порядке <1> [Пр. 200 н: п. 33]. <1> Приказ Минздравсоцразвития России от 26 августа 2010 г. N 757 н "Об утверждении порядка осуществления мониторинга безопасности лекарственных препаратов для медицинского применения, регистрации побочных действий, серьезных нежелательных реакций, непредвиденных нежелательных реакций применении лекарственных препаратов для медицинского применения" (зарегистрирован Министерством юстиции Российской Федерации 31 августа 2010 г. , регистрационный N 18324). В срок, не превышающий пяти рабочих дней со дня завершения, приостановления или прекращения клинического исследования лекарственного препарата для медицинского применения, сообщение об этом направляется организатором клинического исследования в Министерство [Пр. 200 н: п. 40]. 17 © - Романов Б. К. , 2016

Куда и как отправлять отчетность? В Росздравнадзор – обязательно! 2. CIOMS или ОТЧЕТ 1. Письмо + CD © - Романов Б. К. , 2016 3. Для CIOMS таблица (CSDS) 18

СПРАВОЧНЫЕ МАТЕРИАЛЫ ДЛЯ СЛУШАТЕЛЕЙ q Семинар ФГБУ «НЦЭСМП» Минздрава России q Сайт ФГБУ «НЦЭСМП» Минздрава России q Журналы ФГБУ «НЦЭСМП» Минздрава России www. regmed. ru ЕАЭС – новые нормативные требования: 1. Соглашение о единых принципах и правилах обращения лекарственных средств в рамках ЕАЭС. http: //www. eurasiancommission. org/ru/act/texnreg/deptexreg/konsult. Comitet/Pages/drug_products. aspx 2. Правила надлежащей практики фармаконадзора Евразийского экономического союза http: //www. eurasiancommission. org/ru/act/texnreg/deptexreg/konsult. Comitet/Pages/drug_products. aspx © - Романов Б. К. , 2016 19

Благодарю за внимание! www. regmed. ru © - Романов Б. К. , 2016 20
7e2d66710c86379c95d866d930016dc2.ppt