52a18e8ebbe9c93e2d7fb2fc4b30f467.ppt
- Количество слайдов: 26

федеральное государственное автономное образовательное учреждение высшего образования «Национальный исследовательский Томский политехнический университет» Водоподготовка Энергетический Институт Преподаватели Тайлашева Т. С. , к. т. н. , доцент каф. ПГС и ПГУ Визгавлюст Н. В. , к. т. н. , ст. преп. каф. ПГС и ПГУ

Литература n n n Копылов А. С. Водоподготовка в энергетике: учебное пособие для вузов / А. С. Копылов, В. М. Лавыгин, В. Ф. Очков. – 2 -е изд. , стер. . – Москва: Издательский дом МЭИ, 2006. – 309 с. Соколов Б. А. Вспомогательное оборудование котлов. Водоподготовка: учебное пособие / Б. А. Соколов. – Москва: Академия, 2009. – 64 с. Любимова Л. Л. , Заворин А. С. , Ташлыков А. А. Инженерные расчеты в водоподготовке паровых и водогрейных котлов: учебное пособие. – Томск: Изд. ТПУ, 2009. – 133 с. 2
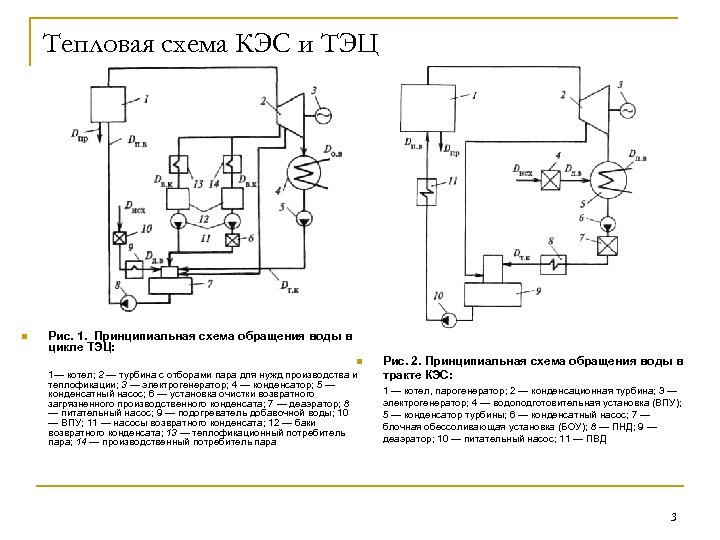
Тепловая схема КЭС и ТЭЦ n Рис. 1. Принципиальная схема обращения воды в цикле ТЭЦ: n 1— котел; 2 — турбина с отборами пара для нужд производства и теплофикации; 3 — электрогенератор; 4 — конденсатор; 5 — конденсатный насос; 6 — установка очистки возвратного загрязненного производственного конденсата; 7 — деаэратор; 8 — питательный насос; 9 — подогреватель добавочной воды; 10 — ВПУ; 11 — насосы возвратного конденсата; 12 — баки возвратного конденсата; 13 — теплофикационный потребитель пара; 14 — производственный потребитель пара Рис. 2. Принципиальная схема обращения воды в тракте КЭС: 1 — котел, парогенератор; 2 — конденсационная турбина; 3 — электрогенератор; 4 — водоподготовительная установка (ВПУ); 5 — конденсатор турбины; 6 — конденсатный насос; 7 — блочная обессоливающая установка (БОУ); 8 — ПНД; 9 — деаэратор; 10 — питательный насос; 11 — ПВД 3

Основные потоки воды n n n Природная (техническая) вода ( Д исх ) - используется в качестве исходного сырья на водоподготовительной установке, а также для других целей на ТЭС и АЭС Добавочная вода ( Д дв ) - направляется в контур для восполнения потерь пара и конденсата после обработки с применением физикохимических методов очистки Турбинный конденсат ( Д вт ), содержащий незначительное количество растворенных и взвешенных примесей, — основная составляющая питательной воды Возвратный конденсат ( Д вк ) от внешних потребителей пара используется после очистки от внесенных загрязнений. Он является составной частью питательной воды Питательная вода ( Д пв ), подаваемая в котлы, парогенераторы или реакторы для замещения испарившейся воды в этих агрегатах, представляет собой главным образом смесь турбинного и возвратного конденсата, добавочной воды, а также конденсата регенеративных подогревателей 4

Основные потоки воды n n Котловая вода, вода парогенератора ( Д кв ) — вода, находящаяся в элементах указанных агрегатов Продувочная вода ( Д пр ) — выводимая из котла, парогенератора или реактора вода на очистку или в дренаж для поддержания в испаряемой (котловой) воде заданной концентрации примесей Охлаждающая или циркуляционная вода ( Д ов ) используется в конденсаторах паровых турбин для конденсации отработавшего пара Подпиточная вода ( Д вп ) подается в тепловые сети для восполнения потерь циркулирующей в них воды 5

Характеристика источников загрязнений контуров ТЭС и АЭС 6

n Согласно Правилам технической эксплуатации электрических станций и сетей (ПТЭ) режим эксплуатации водоподготовительных установок и водно-химический режим должны обеспечить работу электростанций и предприятий тепловых сетей без повреждений и снижения экономичности, вызываемых коррозией внутренних поверхностей водоподготовительного, теплоэнергетического и сетевого оборудования, а также без образования накипи и отложений на теплопередающих поверхностях, отложений в проточной части турбин, шлама в оборудовании и трубопроводах электростанций и тепловых сетей 7

Примеси природных вод и показатели качества воды

Круговорот воды в природе n n В соответствии с основными звеньями круговорота воды в природе различают : - атмосферную (дождь, туман, снег), - поверхностную (реки, озера, пруды, болота), - грунтовую (артезианские скважины), - морскую (моря, океаны). 9

Атмосферная вода n выпадающая на земную поверхность из атмосферы, является наиболее чистой природной водой, но и она содержит, кроме газов (кислорода, азота, углекислоты), органические и неорганические вещества, количество и состав которых зависят от характера атмосферы. 10

Воды поверхностная, грунтовая и морская n Эти воды содержат то или иное количество растворимых и нерастворимых механических примесей. Просачиваясь через верхние слои почвы, вода освобождается от механических примесей, но одновременно обогащается солями, газами и органическими веществами, представляющими собой продукты разложения растительных и животных организмов. 11
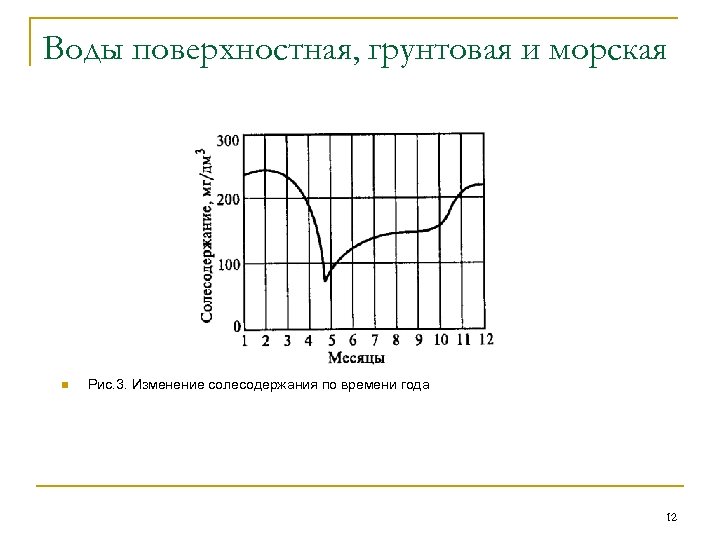
Воды поверхностная, грунтовая и морская n Рис. 3. Изменение солесодержания по времени года 12

Природные воды классифицируются по n • химическому составу: n - минеральные – растворенные в воде содержащиеся в атмосфере газы N 2, O 2, CO 2, а также газы, вносимые сточными водами, различные соли, кислоты, основания. - органические – гумусовые вещества в виде гуминовых кислот, коллоидных соединений фульвокислот, истинно растворенные фульвокислоты. n 13

Природные воды классифицируются • по степени дисперсности: n n n грубодисперсные с размером частиц > 100 нм (мкм); коллоиднодисперсные с размером частиц от 1 до 100 нм; истинно-растворенные (ионно- или молекулярнодисперсные) с размером частиц <1 нм. 14

Грубодисперсные вещества n обусловливают мутность природных вод, являются механическими примесями, состоящими из песка, глины и других частиц минерального и органического происхождения. Эти загрязнения характеризуются весовым количеством, содержащимся в единице объема воды (мг/дм 3, г/дм 3). Удаление грубодисперсных примесей является первой технологической операцией обработки воды. 15

В коллоидном состоянии присутствуют в воде вещества как органического так и минерального происхождения. Органические вещества в виде гуминовых кислот окрашивают воду в желтый цвет и вызывают помутнение воды. Из неорганических веществ в коллоидном состоянии присутствуют в воде соединения железа, кремния и алюминия. n Коллоидные примеси затрудняют работу паровых котлов, повышая склонность котловой воды к вспениванию. Поэтому их необходимо удалить из воды при ее обработке. 16

К истинно-растворенным примесям относятся растворенные в воде соли, кислоты, щелочи и газы. В природных водах присутствуют следующие наиболее распространенные ионы: Ca 2+, Mg 2+, Na+, Cl-, SO 2 -4, HCO 3 -, HSi. O 3 -. Ионы CO 32 -, H+, OH-, NH 4+, NO 2 -, NO 3 -, Fe 2+, Cu 2+ и другие содержатся в природных водах в незначительных количествах. n 17

Главные катионы и анионы примесей Катион Анион Концентрация, мг/кг Na+, K+, Ca 2+, Mg 2+ HCO 3 -, Cl-, SO 42 - От нескольких единиц до десятков тысяч NH 4+, Fe 2+, Mn 2+ HSi. O 3 -, F-, CO 32 - От десятых долей до единиц Ni 2+, Cu 2+, Zn 2+, Al 3+ HS-, I-, NO 2 -, H 2 PO 4 - I II III NO 32 -, Менее десятых долей 18

Характеристики ионизированных примесей воды n 1. Na+, K+ Ионы натрия и калия – группа устойчивых примесей, не образуют труднорастворимых солей, концентрация этих щелочных металлов с увеличением минерализации воды возрастает. Их основные соли Na. Cl, Na 2 SO 4, щелочные Na 2 CO 3, Na. HCO 3, Na. OH. Щелочные компоненты очень опасны, от них обязательно нужно избавиться. 19

Характеристики ионизированных примесей воды n 2. Ca 2+, Mg 2+ Ионы Са 2+ в маломинерализованных водах по количеству занимают первое место. Жесткость воды определяется только концентрацией двух катионов Ca 2+ и Mg 2+. Ионы Ca 2+, Mg 2+ являются основными накипеобразователями Ca. СO 3, Mg. SO 4, Ca. СO 3, Mg. CO 3, Mg(OH)2 – основные соли. С ростом минерализации природных вод относительное содержание ионов Ca 2+ уменьшается, т. к. Ca. СO 3 и Mg. СO 3 при увеличении их концентрации из-за испарения воды переходят в твердую фазу вследствие их малой растворимости. 20

Характеристики ионизированных примесей воды n 3. Ионы Cl- и SO 42 - - относятся к числу устойчивых примесей и не образуют труднорастворимых примесей и не подвергаются гидролизу. Распространены повсеместно. 21

Характеристики ионизированных примесей воды n 4. Анионы угольной кислоты Угольная кислота является двухосновной и имеет две ступени диссоциации: n H 2 CO 3 ↔ H+ + HCO 3 n HCO 3 ↔ H+ + CO 32 В природных водах, кроме так называемой «свободной» углекислоты, находящейся в них в виде растворенного углекислого газа CO 2, и недиссоциированных молекул угольной кислоты H 2 CO 3 содержатся бикарбонатные ионы HCO 3 -, а в некоторых случаях карбонатные ионы CO 32 -. 22

Характеристики ионизированных примесей воды n n n Все формы этой кислоты находятся в Н 2 О в кинетическом равновесии: n 2 НСО 3 - ↔ СО 32 - + Н 2 О + СО 2 Из уравнения следует, что для поддержания в растворе определенной концентрации HCO 3 - требуется, чтобы в воде присутствовало соответствующее этой концентрации количество «свободной» равновесной углекислоты СО 2. А) Если фактически содержащееся в воде количество свободной углекислоты больше «равновесной концентрации» , то избыток ее будет способен вызывать растворение Са. СО 3 при контакте воды, #, с известняками, доломитами и бетонными сооружениями. Такую воду называют «агрессивной» . n СО 2 фак > СО 2 равн n Са. СО 3 + СО 2 + Н 2 О → Са(4 СО 3)2 Б) При недостатке СО 2 по сравнению с равновесной концентрацией будет наблюдаться распад части бикарбонатных ионов, т. е. сдвиг равновесия вправо. Это приведет к образованию дополнительного количества карбонатных ионов СО 32 -, которые реагируют с катионами Са 2+. n СО 2 фак < СО 2 равн n Са 2+ + СО 32 - → Са. СО 3↓(осадок) n Са(4 СО 3)2 → Са. СО 3↓ + СО 2 + Н 2 О Такая вода называется нестабильной в отношении образования карбонатов кальция. 23

Характеристики ионизированных примесей воды n 5 Ионы соединения азота Встречаются в природной воде в виде ионов аммония NH 4+, нитритных ионов NO 2 -, и нитратных ионов NO 3 -. Основным источником этих ионов являются продукты распада различных сложных органических веществ. Ионы аммония NH 4+ попадают со сложными промышленными водами. При достаточном количестве кислорода и особого вида бактерий ионы аммония окисляются в нитритные и нитратные ионы. 24

Характеристики ионизированных примесей воды n 6 Fe. O и Fe 2 O 3 или Fe 2+ и Fe 3+ Встречается в виде двухвалентного (закисного) Fe. O, трехвалентного (окисного) Fe 2 O 3 железа. Эти соединения могут быть в истинно растворенном состоянии, в виде коллоидов и суспензий. Концентрация Fe 2+ и Fe 3+ в исходной воде может увеличиться в процессе транспортировки ее по стальным и чугунным трубам в результате загрязнения воды продуктами коррозии 25

Характеристики ионизированных примесей воды n n 7 Соединения кремния Si. O 2 и HSi. O 3 Кремниевый ангидрид способен присоединять разные количества молекул воды, образуя различные кислоты с общей формулой m. Si. O 2∙n. H 2 O. Кремниевая кислота является двухосновной и имеет две ступени диссоциации: n H 2 Si. O 3 ↔ H+ + HSi. O 3 n HSi. O 3 - ↔ H+ + Si. O 32 Растворимость кремниевой кислоты в природных водах зависит от ряда факторов и в первую очередь от ионного состава воды и величины p. H. 26
52a18e8ebbe9c93e2d7fb2fc4b30f467.ppt