99e0e090b5c5c63845de13426aa33417.ppt
- Количество слайдов: 29

Федеральная служба по надзору в сфере здравоохранения и социального развития «Надлежащая производственная практика (GMP) в России – бремя или благо» Врио руководителя Росздравнадзора, д. ф. н. , профессор Е. А. Тельнова Международная конференция апрель, 2010

Структура отечественных производителей по лекарственным формам - На территории Российской Федерации на 01. 04. 2010 осуществляют деятельность по производству лекарственных средств 460 предприятий (количество выданных лицензий на производство лекарственных средств более 730) - 63 предприятия государственной формы собственности Нестерильные лекарственные формы: твердые, мягкие, жидкие, 272 галеновые 37 Стерильные лекарственные формы: жидкие стерильные, 84 твердые, мягкие, рассыпка 39 Субстанции 66 Препараты крови 44 Медицинские газы 36 МИБП 32 Лекарственные средства на основе сырья природного происхождения (растительное сырье, пиявки, яды змей) 25 Высокотаксичные и опасные лекарственные средства (антибиотики, цитостатики и др. ) 19 Гомеопатические лекарственные средства 10 Центральный ФО – 204 Южный ФО – 40 Северо-западный ФО - 52 Дальневосточный ФО – 8 Сибирский ФО – 51 Уральский ФО – 30 Приволжский ФО – 69 Северокавказский ФО - 6
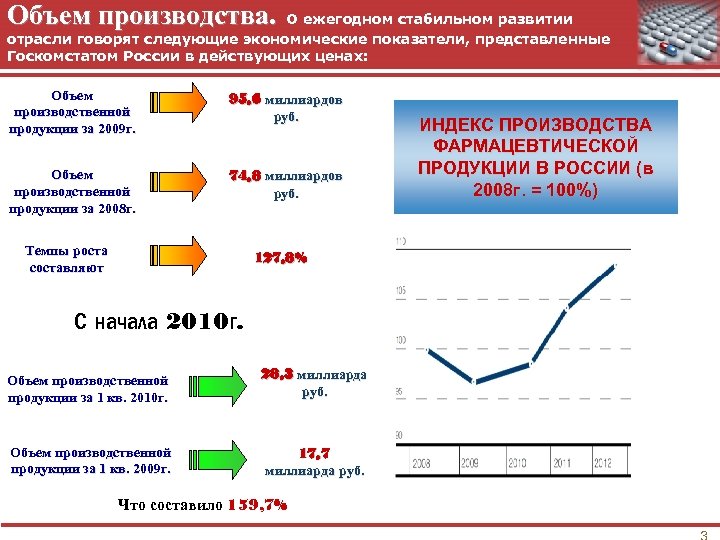
Объем производства. О ежегодном стабильном развитии отрасли говорят следующие экономические показатели, представленные Госкомстатом России в действующих ценах: Объем производственной продукции за 2009 г. 95, 6 миллиардов руб. Объем производственной продукции за 2008 г. 74, 8 миллиардов руб. Темпы роста составляют 127, 8% С начала 2010 г. Объем производственной продукции за 1 кв. 2010 г. 28, 3 миллиарда руб. Объем производственной продукции за 1 кв. 2009 г. 17, 7 миллиарда руб. Что составило 159, 7% ИНДЕКС ПРОИЗВОДСТВА ФАРМАЦЕВТИЧЕСКОЙ ПРОДУКЦИИ В РОССИИ (в 2008 г. = 100%)
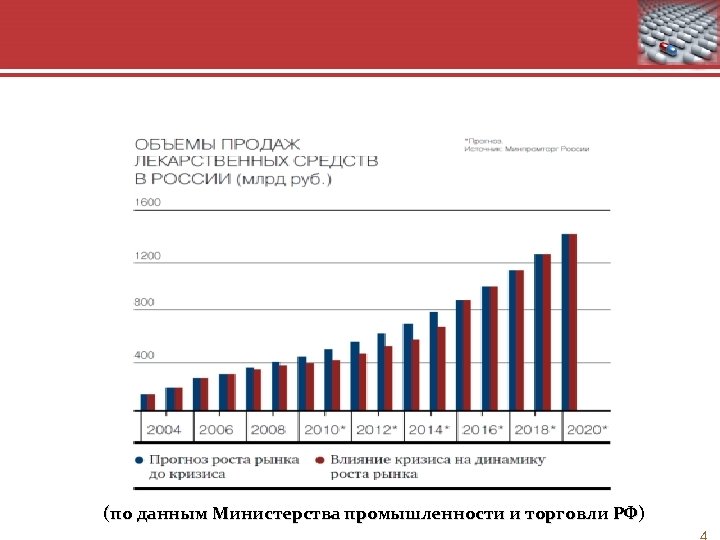
(по данным Министерства промышленности и торговли РФ)

Экспорт и импорт отечественной фармацевтической продукции Экспорт. 2009 г. 338, 0 миллионов $ 2008 г. 337, 4 миллионов $ Темпы роста 99, 8% Цифры по импорту лекарственных средств говорят о стабильности уже сложившегося Российского рынка лекарственных средств: 2009 г. 8 998, 9 миллионов $ 2008 г. 8 543, 5 миллионов $ Темпы роста 94, 9%
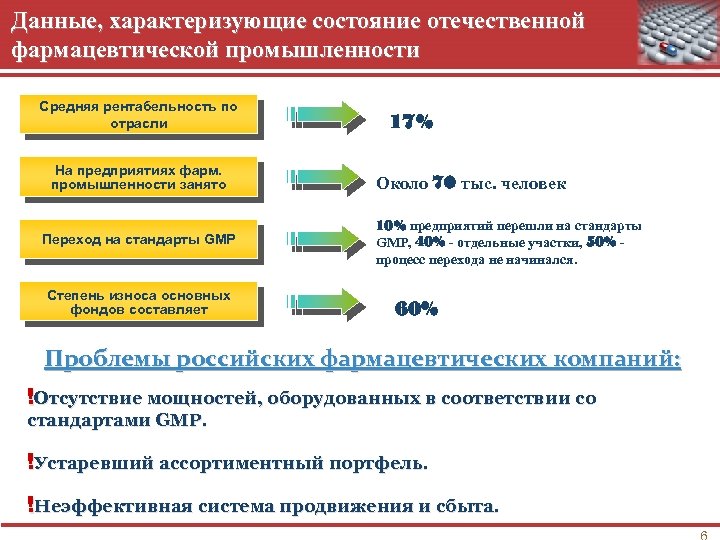
Данные, характеризующие состояние отечественной фармацевтической промышленности Средняя рентабельность по отрасли На предприятиях фарм. промышленности занято Переход на стандарты GMP Степень износа основных фондов составляет 17% Около 70 тыс. человек 10% предприятий перешли на стандарты GMP, 40% - отдельные участки, 50% процесс перехода не начинался. 60% Проблемы российских фармацевтических компаний: !Отсутствие мощностей, оборудованных в соответствии со стандартами GMP. !Устаревший ассортиментный портфель. !Неэффективная система продвижения и сбыта.

Одной из приоритетных задач в области здравоохранения является обеспечение качества лекарственных средств, находящихся в обращении на территории Российской Федерации. При этом уровень требований, предъявляемый к лекарственным средствам, определяет уровень безопасности применения лекарственных средств на территории каждой страны. Система государственного контроля качества лекарственных средств включает в себя: ü оценку эффективности, безопасности и утверждение стандартов качества на лекарственные средства при регистрации; ü оценку качества впервые производимых и впервые ввозимых лекарственных средств при допуске в обращение; ü экспертизу качества лекарственных средств, находящихся в обращении (выборочно); ü ü мониторинг качества, эффективности и безопасности лекарственных средств, находящихся в обращении; инспекционный контроль. Росздравнадзором создана система выявления и изъятия из обращения недоброкачественных и фальсифицированных лекарственных средств. Составляющими данной системы являются: ü территориальные Управления Росздравнадзора; ü испытательные лаборатории; ü единая информационная система; ü системы качества в организациях-производителях лекарственных средств, розничных и оптовых фармацевтических организациях. 5

Проект реформирования системы государственного контроля лекарственных средств находится в стадии реализации, как и ряд других стратегических задач. Начиная с 2009 года, обеспечено бюджетное финансирование государственного выборочного контроля качества социально значимых категорий лекарственных средств, таких как: Cинсулины; Cантибиотики для внутривенного и внутримышечного введения; Cсредства для наркоза; Cинфузионные растворы и растворы для парентерального питания и кровезаменители; Cфармацевтические субстанции, предназначенные для производства лекарственных средств отечественными производителями; Cцитостатики в лекарственных формах для инъекций; Cпрепараты, получаемые из крови и плазмы донорской. 8
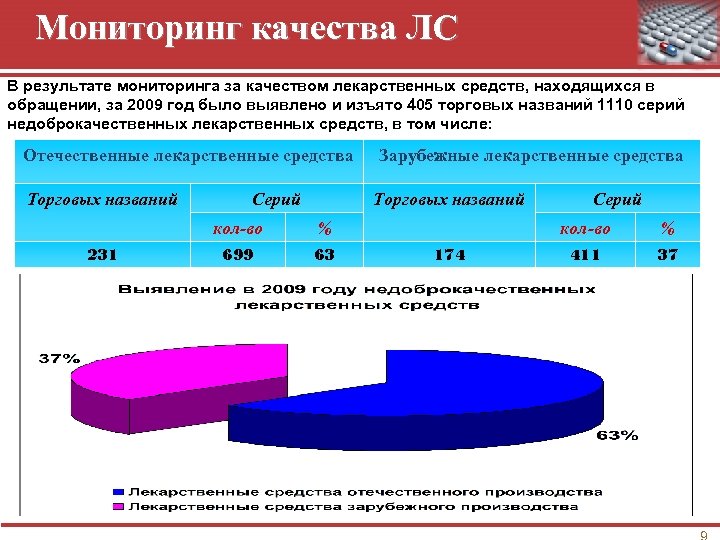
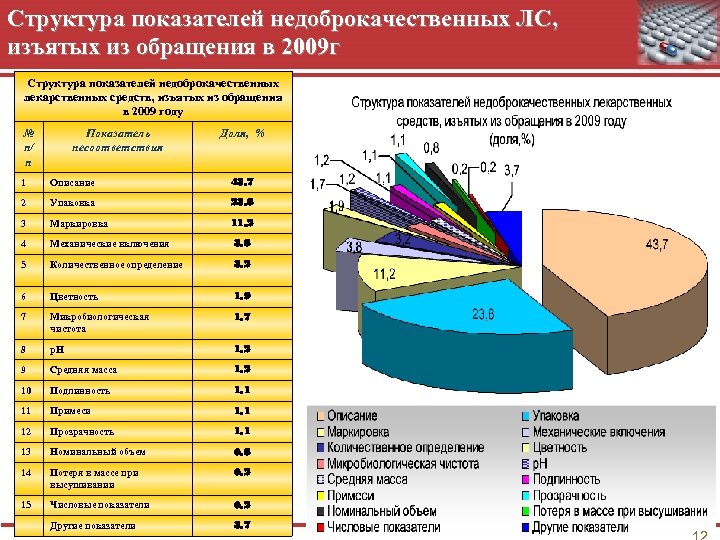
Мониторинг качества ЛС В результате мониторинга за качеством лекарственных средств, находящихся в обращении, за 2009 год было выявлено и изъято 405 торговых названий 1110 серий недоброкачественных лекарственных средств, в том числе: Отечественные лекарственные средства Торговых названий Серий Торговых названий кол-во 231 Зарубежные лекарственные средства % 699 63 Серий кол-во 174 % 411 37
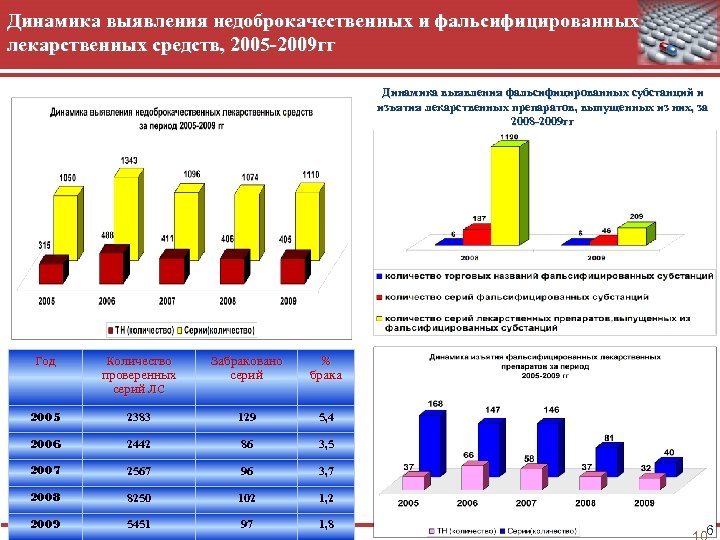
Динамика выявления недоброкачественных и фальсифицированных лекарственных средств, 2005 -2009 гг Динамика выявления фальсифицированных субстанций и изъятия лекарственных препаратов, выпущенных из них, за 2008 -2009 гг Год Количество проверенных серий ЛС Забраковано серий % брака 2005 2383 129 5, 4 2006 2442 86 3, 5 2007 2567 96 3, 7 2008 8250 102 1, 2 2009 5451 97 1, 8 6
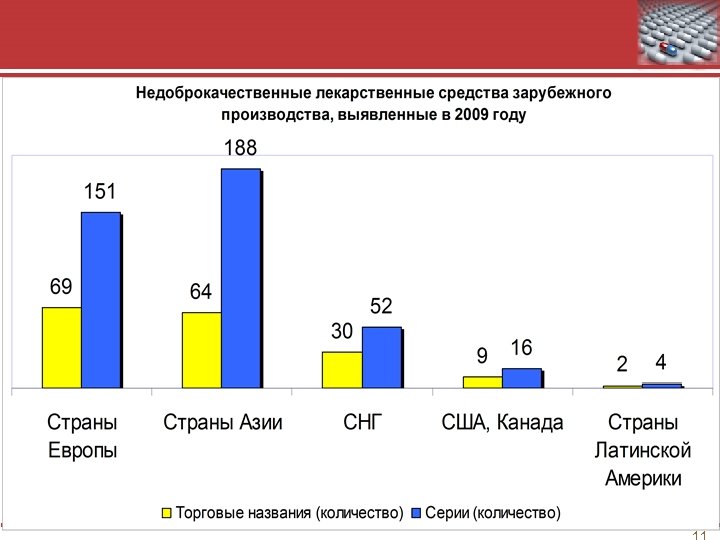
Структура показателей недоброкачественных ЛС, изъятых из обращения в 2009 г Структура показателей недоброкачественных лекарственных средств, изъятых из обращения в 2009 году № п/ п Показатель несоответствия Доля, % 1 Описание 43, 7 2 Упаковка 23, 8 3 Маркировка 11, 2 4 Механические включения 3, 8 5 Количественное определение 3, 2 6 Цветность 1, 9 7 Микробиологическая чистота 1, 7 8 р. Н 1, 2 9 Средняя масса 1, 2 10 Подлинность 1, 1 11 Примеси 1, 1 12 Прозрачность 1, 1 13 Номинальный объем 0, 8 14 Потеря в массе при высушивании 0, 2 15 Числовые показатели 0, 2 Другие показатели 3, 7

Рейтинг отечественных производителей по показателям качества № п/ п 1 Наименование производителя Сотекс Фарм. Фирма ЗАО Кол-во ТН забракован ных ЛС 3 Кол-во серий забракованных ЛС 100 Показатели несоответствия № п / п Наименова ние производит еля 8 Рейтинг отечественных производителей лекарственных средств по объему забракованной продукции за период с 01. 2009 по 31. 12. 2009. Кол-во ТН забрак ованн ых ЛС Кол-во серий забрак ованн ых ЛС Биосинтез ОАО Механические включения, Подлинность (в том числе 98 серий препарата "Милдронат") Йодные технологии и маркетинг ООО 5 34 Описание, Количественное определение, Упаковка, Подлинность, Маркировка, Кислотность, Сухой остаток 3 Ростовская фармфабрика ЗАО 9 29 4 Флора Кавказа ОАО 6 29 Описание, Количественное определение, Спирт, Упаковка, Маркировка, Сухой остаток, Номинальный объем 5 Тульская фармацевтическая фабрика ООО 4 28 Описание, Упаковка 6 Биохимик ОАО 14 23 Описание, Маркировка, Упаковка, Механические включения, Номинальный объем, Средняя масса 7 Дальхимфарм ОАО 10 23 Описание, Прозрачность, Механические включения, Маркировка 22 Описание, Упаковка, Механические включения, Маркировка, Прозрачность, Цветность, Состав, Подлинность, Количественное определение, Родственные примеси 21 Подлинность, Упаковка, Количественное определение суммы капсациноидов, Описание, Номинальный объем Описание, Упаковка 2 Показатели несоответствия 15 9 Гиппократ ООО 5 1 0 Мосхимфар мпрепараты им. Н. А. Сем ашко ОАО 13 20 Описание, Упаковка, Маркировка, Цветность
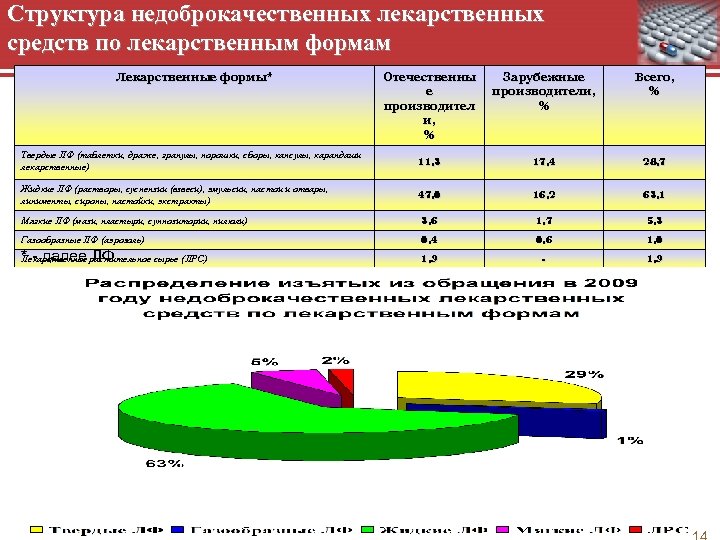
Структура недоброкачественных лекарственных средств по лекарственным формам Лекарственные формы* Отечественны е производител и, % Зарубежные производители, % Всего, % Твердые ЛФ (таблетки, драже, гранулы, порошки, сборы, капсулы, карандаши лекарственные) 11, 3 17, 4 28, 7 Жидкие ЛФ (растворы, суспензии (взвеси), эмульсии, настои и отвары, линименты, сиропы, настойки, экстракты) 47, 0 16, 2 63, 1 Мягкие ЛФ (мази, пластыри, суппозитории, пилюли) 3, 6 1, 7 5, 3 Газообразные ЛФ (аэрозоль) 0, 4 0, 6 1, 0 * - далее ЛФ 1, 9 - 1, 9 Лекарственное растительное сырье (ЛРС)
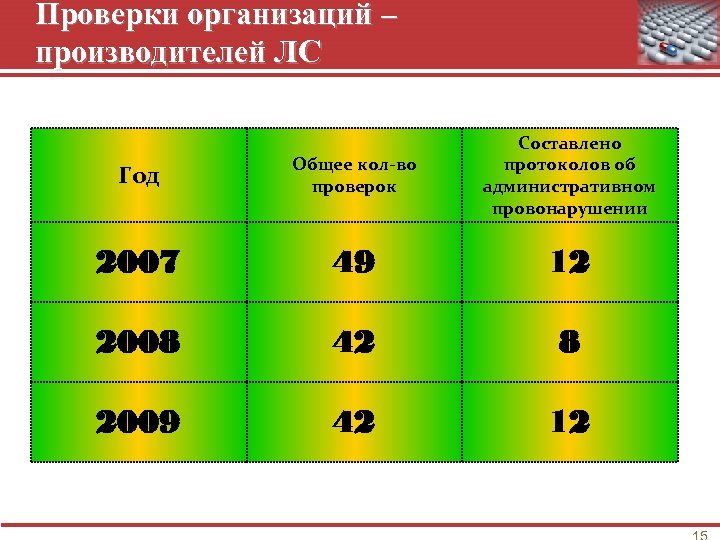
Проверки организаций – производителей ЛС Год Общее кол-во проверок Составлено протоколов об административном провонарушении 2007 49 12 2008 42 8 2009 42 12

Наиболее часто встречающиеся нарушения в организации производства и контроля качества лекарственных средств: G неэффективное функционирование системы обеспечения качеством, что приводит к производству продукции несоответствующего качества; G нарушения правил хранения сырья и исходных материалов, включая размещение сырья и продукции, условия отбора проб и пр. ; G использование фармацевтических субстанций, не предусмотренных нормативной документацией; G несоответствие помещений и оборудования условиям, требуемым для производства заявленных лекарственных средств, а также производство несовместимых лекарственных средств в одних производственных помещениях; G отсутствие данных по валидации чистоты помещений, системы водоподготовки, критических технологических операций и пр.

Установлена взаимосвязь между отклонениями в показателях качества лекарственных средств и нарушениями правил производства лекарственных средств: Показатель качества Нарушения требований и условий, предъявляемых к организации производства и контролю качества лекарственных средств *Описание (внешний вид) *Средняя масса *Упаковка 1. Устаревшее технологическое оборудование (сколы по краям, шероховатости, излишняя пыль). 2. Использование упаковки, не обеспечивающей защиту препарата от внешних воздействий (свет, влажность), или отсутствие вторичной упаковки (механические повреждения). 3. Изучение стабильности лекарственных средств в условиях естественного и стрессового старения (в различных режимах температуры и влажности) осуществляется не должным образом. 4. Несоблюдение технологических стадий производства, нарушение регламентных норм, приводящих к несоответствию продукции при хранении и транспортировке (поверхность таблеток, покрытых оболочкой, с нарушенной целостностью покрытия, сколы). *Примеси (выше установленных норм) *Количественное определение Цветность *Числовые показатели *Растворение *Прозрачность 1. Отсутствие контроля качества в полном объеме (по всем показателям нормативной документации и на всех стадиях производственного цикла). 2. Отсутствие аудита поставщиков (производителей) активных фармацевтических ингредиентов и, как следствие, выбор поставщиков сырья по принципу закупок «ЦЕНАкачество» , вместо «КАЧЕСТВО-цена» . 3. Привлечение к контролю качества контрактных лабораторий, которые не владеют спецификой анализа конкретных препаратов или методиками проведения анализа, как следствие, получение недостоверных результатов испытаний. 4. Нерепрезентативный отбор проб на всех стадиях контроля производственного цикла.
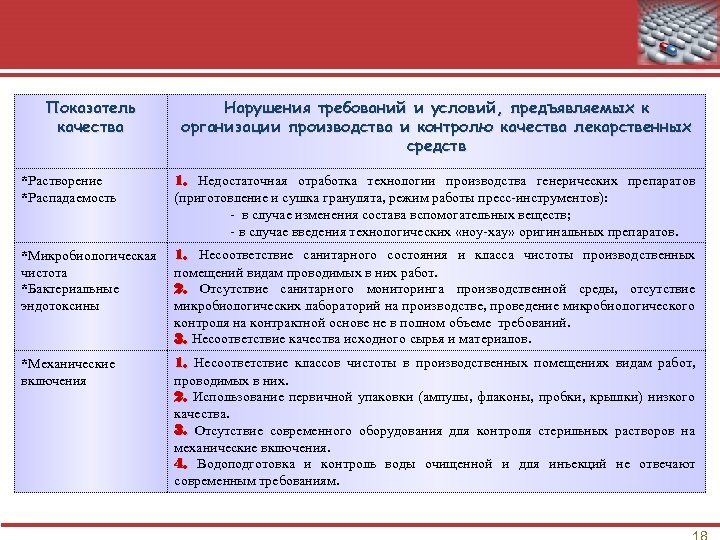
Показатель качества Нарушения требований и условий, предъявляемых к организации производства и контролю качества лекарственных средств *Растворение *Распадаемость 1. Недостаточная отработка технологии производства генерических препаратов (приготовление и сушка гранулята, режим работы пресс-инструментов): - в случае изменения состава вспомогательных веществ; - в случае введения технологических «ноу-хау» оригинальных препаратов. *Микробиологическая чистота *Бактериальные эндотоксины 1. Несоответствие санитарного состояния и класса чистоты производственных помещений видам проводимых в них работ. 2. Отсутствие санитарного мониторинга производственной среды, отсутствие микробиологических лабораторий на производстве, проведение микробиологического контроля на контрактной основе не в полном объеме требований. 3. Несоответствие качества исходного сырья и материалов. *Механические включения 1. Несоответствие классов чистоты в производственных помещениях видам работ, проводимых в них. 2. Использование первичной упаковки (ампулы, флаконы, пробки, крышки) низкого качества. 3. Отсутствие современного оборудования для контроля стерильных растворов на механические включения. 4. Водоподготовка и контроль воды очищенной и для инъекций не отвечают современным требованиям.

Для оценки технического уровня производства и качества лекарственных средств ВОЗ была создана «Система удостоверения качества фармацевтических препаратов» (действующий вариант принят в 1992 году). В настоящее время к системе присоединилось 140 государств Россия не является участником соглашения Для присоединения к системе в стране необходимо наличие трех условий: государственная регистрация лекарственных средств; регулярное государственное инспектирование фармацевтических предприятий; соответствие действующих производств требованиям GMP.

Стандарт отрасли ОСТ 42 -510 -98 PПредставляет собой свод правил по организации производства и контроля качества лекарственных средств; PСтандарт распространяется на все предприятия, выпускающие готовые лекарственные средства, независимо от ведомственной подчиненности и форм собственности.

Министерство здравоохранения Российской Федерации Министерство экономики Российской Федерации ПРИКАЗ от 03. 12. 1999 № 432/512 «О введении в действие Стандарта отрасли ОСТ 42 -510 -98 «Правила организации производства и контроля качества лекарственных средств ( GMP )»

Показатели качества ЛС. D Отсутствует подзаконный нормативный акт, обязывающий предприятия выполнять требования GMP (принят закон, обязывающий предприятия к 2014 г перейти на стандарты GMP). D В России построены предприятия с производственными помещениями по GMP (более 15 площадок), однако, система обеспечения качества ЛС на большинстве предприятий слаба или отсутствует ( «милдронатовый» кризис, использование в производстве фальсифицированных субстанций). D У Росздравнадзора нет права проводить GMP – инспекции зарубежных производственных площадок.

Системные проблемы российской фармацевтической промышленности Ä Отсутствие национальной концепции развития фармацевтической промышленности (разработана); Ä Низкий уровень инноваций и технологий, используемых при разработке и производстве лекарственных средств; Ä Отсутствие механизмов финансирования разработок лекарственных препаратов; Ä Множество разрывов в критических цепях взаимодействия, обеспечивающих создание новых отечественных инновационных брендов; Отсутствие должного уровня кооперации между компаниями; Неравномерное развитие отдельных высокотехнологичных секторов, участвующих в разработках лекарственных средств; Ä Недостаточный уровень Российского патентного законодательства и законоприменительной практики относительно международных стандартов; Ä Непрерывно истощающийся кадровый потенциал отечественной науки и производства; ÄСырьевая зависимость отечественной промышленности.

Обеспечение квалифицированными специалистами Существует острая потребность в подготовке квалифицированных специалистов для современных фармацевтических производств, обладающих знаниями по новейшим технологиям производства лекарств (в основном, ГЛСтаблетирование, капсулирование, ампулирование), современному оборудованию, материалам, а также действующим стандартам производств (GMP и др. ), со знаниями современных норм и правил по регистрации и сертификации. Проблемой является не сколько отсутствие кадров как таковых (формально обучение проводится в большом количестве учебных заведений), а дефицит подготовленных специалистов мирового уровня. В настоящее время лицензию на подготовку кадров по специальности «Фармация» имеют 48 ВУЗов и только два ВУЗа (г. Курск и г. Санкт-Петербург) выпускают инженеров химико-технологического профиля, которые профиля предполагают подготовку специалистов для фармацевтических производств. В 2009 году неудовлетворенность спроса на производственников указывает на то, что «свободных» высококвалифицированных кандидатов на рынке уже нет, и в большинстве случаев единственным способом получить нужного нет специалиста является хэд-хантер.

Выход из ситуации возможен? ! Сценарий I Сотрудничество с государством. Создание государственно-частного партнерства (ГЧП), зарекомендовавшего себя во многих странах. Каждая страна предоставляет имеющиеся у нее ресурсы, в тоже время берет на себя часть потенциальных рисков. ГЧП предполагает: Долевое финансирование (таким образом предприятие получит финансовую поддержку от государства). Сценарий II Необходимо развитие собственного производства не только готовых лекформ, но и сырья. Для чего необходимы: - Значительные инвестиции в модернизацию производства, в т. ч. оборудования. - Финансирование научных разработок. При этом сценарии производитель снижает свою зависимость от импортных субстанций. Плюсы - Снижение зависимости от импортных субстанций Необходимо - Закупка оборудования - Создание дополнительных рабочих мест - Учесть фактор конкурентоспособности - Разработка маркетинговой стратегии реализации субстанций - Финансирование рекламных затрат для вывода новой субстанции на рынок.

Первый шаг сделан !!!! - принят новый закон «ОБ ОБРАЩЕНИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ» № 61 -ФЗ от 12 апреля 2010 г.

На следующем этапе необходимо решение следующих задач: ë серьезная государственная поддержка отечественной промышленности, в т. ч. решение вопроса о реальных преференциях отечественной промышленности; ë подготовка нормативно-правовых актов в развитии нового закона; ë решение проблемы по обеспечению квалифицированными кадрами; ë разработка системы контроля качества лекарственных средств, в том числе открытие сети государственных лабораторий.

Меры по поддержке отечественной фармацевтической отрасли, реализуемые в рамках государственной лекарственной политики, должны быть направлены на поощрение конкуренции, что в конечном счете приведет: к снижению цены, повышению качества лекарственных средств, решению проблем с доступностью лекарственных средств для населения.

99e0e090b5c5c63845de13426aa33417.ppt