Физико-химические методы анализа(часть 2).ppt
- Количество слайдов: 48

![Fe 3++ 5 CNS-→[Fe(CNS)5]2 - желтый красный Ba(OH)2 + CO 2 →Ba. CO 3↓ Fe 3++ 5 CNS-→[Fe(CNS)5]2 - желтый красный Ba(OH)2 + CO 2 →Ba. CO 3↓](https://present5.com/presentation/191862010_437884532/image-2.jpg)
Fe 3++ 5 CNS-→[Fe(CNS)5]2 - желтый красный Ba(OH)2 + CO 2 →Ba. CO 3↓ + H 2 O Сравнительная оценка чувствительности методов анализа Метод 1. 2. 3. 4. 5. 6. 7. Титрометрический Гравиметрический Спектрофотометрический Полярографический, люминесцентный Кинетический Радиохимический Хроматомасс-спектрометрический Чувствительность 10 -1 10 -2 10 -3 -10 -5 10 -4 -10 -6 -10 -8 -10 -9 10 -10 -10 -12 2

1. Фотометрические: - колориметрия; - спектрофотометрия; - турбодиметрия; - нефелометрия. 2. Рефрактометрические 3. Полярометрические 4. Спектральные 1. Экстракция 1. 2. 3. 4. 5. 1. Электроанализ 2. Потенциометрия 3. Кондуктометрия 4. Полярография 2. Хроматография Метод радиактивных индикаторов Термические Радиоактивационные методы Метод ЯМР Масс-спектроскопия 3

Оптические методы. Колориметрия I 0 Ia Ik где It Ir I 0 – поступающий световой поток; Ia – поглощенный световой поток; It – прошедший световой поток; Ir– рассеянный световой поток; Ik – отраженный световой поток. I 0 = It + Ia + Ir + Ik Ir≈ Ik ≈0 I 0 = It + Ia Закон Бугера-Ламберта: Слой вещества одинаковой толщины при прочих равных условиях поглощает одну и ту же часть поступающего светового потока. 4

I Допустим: 100 Тогда: I 0 =100; It 1=50 It 2=25; It 3=12, 5; It 4=6, 25 и т. д. It= I 0∙е-к’b, где k’ – коэффициент поглощения 50 25 12, 5 6, 5 1 2 3 4 b (толщина поглощенного слоя) Следствие из закона Бугера-Ламберта: 1. Отношение не зависит от величины абсолютной интенсивности I 0 2. Изменение толщины поглощающего слоя (b) приводит к изменению It по логарифмическому закону. Допустим: тогда ; 5

Бэр: Уравнение Бугера – Ламберта - Бэра - – молярный коэффициент поглощения (л/моль∙см) С – концентрация (моль/л) А b=3 b=2 b=1 α 2 α 3 Физический смысл С моль/л оптическая плотность при С=1 моль/л и b=1 см 6

1. Влияние концентрации Конц. Синий Со 2+ Разб. Розовый 2. Влияние р. Н – среды Комплекс Fe 3+ с сульфасалицилововой р. Н Состав комплекса кислотой Окраска ~λ, нм при Аmax 1, 8 -2, 5 фиолетовая 400 4 -8 желтая 550 8 -11 красная 640 7
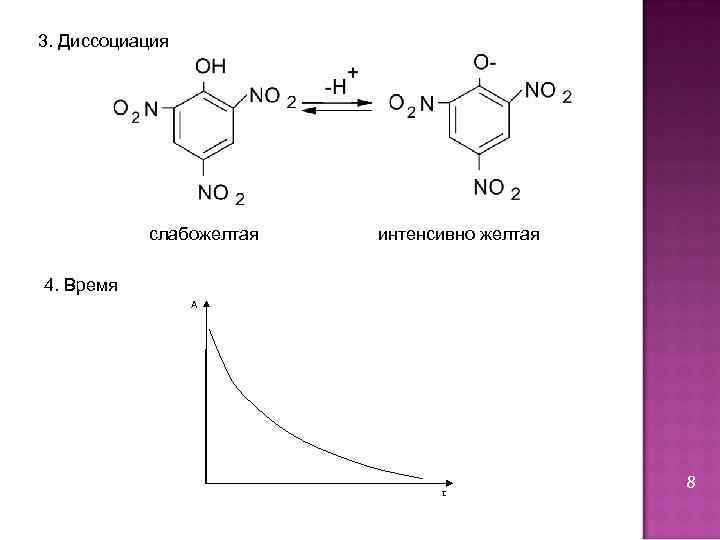
3. Диссоциация слабожелтая интенсивно желтая 4. Время А τ 8
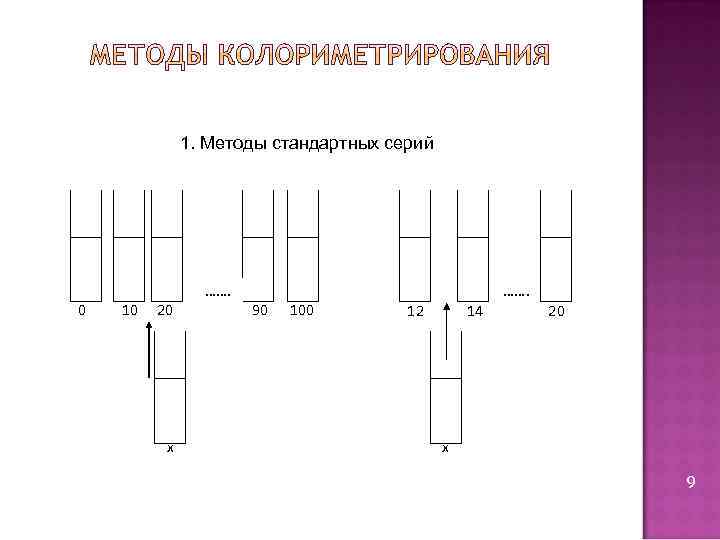
1. Методы стандартных серий 0 10 20 х ……. 90 100 12 14 ……. 20 х 9

2. Метод колориметрического титрования (дублирования) Ах = Аст Сх∙Vx = Сст∙Vст Сх Vx Vст Cст 3. Метод уравнивания , для одного и того же вещества 10

Этот метод анализа, основанный на измерении интенсивности светового потока, рассеянного твердыми частицами суспензии, находящимися во взвешенном состоянии. Уравнение Релея: n и n 1 – коэффициенты преломления среды и твердых частиц; N –общее число твердых частиц; V –средний объем частицы, см 3; λ –длина волны падающего светового потока, нм r– расстояние от кюветы до наблюдателя, см; β–угол, образованный падающим и рассеянным светом. В условиях проведения анализа: n, n 1 , r, β, V, λ – const, тогда: 11

Метод, основанный на измерении интенсивности светового потока прошедшего через слой суспензии. c –концентрация твердых частиц моль/л; b–толщина поглощаемого слоя, см; d –средний диаметр твердых частиц, см; λ –длина световой волны, нм k’ и α– константы, зависящие от природы суспензии и метода измерения; В условиях проведения анализа: α, k’, d, λ – const, тогда: где k - молярный коэффициент мутности. 12

ИНФРАКРАСНАЯ (ИК) СПЕКТРОСКОПИЯ 1800 г. – английский астроном У. Гершель. 1905 г. – американский физик У. Кобленц. ИК волновой диапазон, мкм: 1 -100. В аналитической практике используется: 2, 5 -15 мкм В частотном диапазоне, это: 4000 – 670 см-1. Для нелинейной молекулы, содержащий N атомов, количество основных колебаний можно рассчитать по формуле: 3 N – 6 Для линейной молекулы: 3 N – 5 Для 2 -х атомной молекулы: 3 2 – 5=1 Для 2 -х атомной молекулы частота характеристических колебаний в ИК – спектре может быть рассчитана по следующей формуле: где k – модуль упругости химической связи; m 1 , m 2 - масса атомов; c – скорость света в вакууме. В случае связи С-Н: k = 5∙ 105 дин/см; mс =12; m. H =1; νC-H=3040 см-1 13
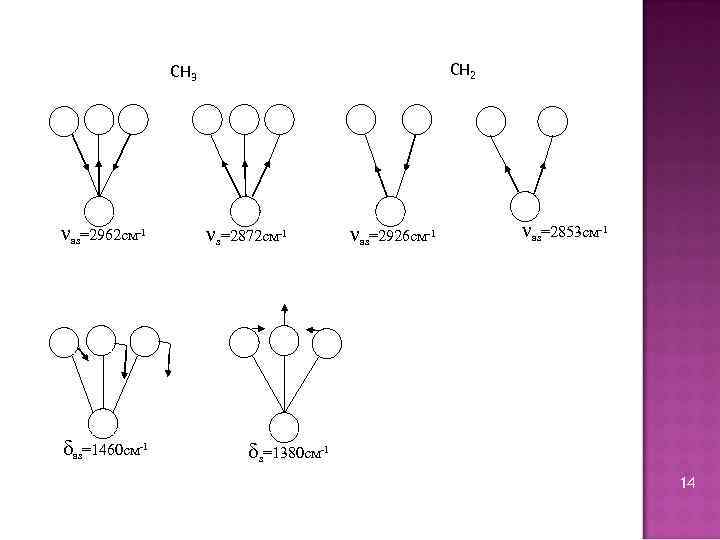
CH 2 CH 3 νas=2962 см-1 δas=1460 см-1 νs=2872 см-1 νas=2926 см-1 νas=2853 см-1 δs=1380 см-1 14 14
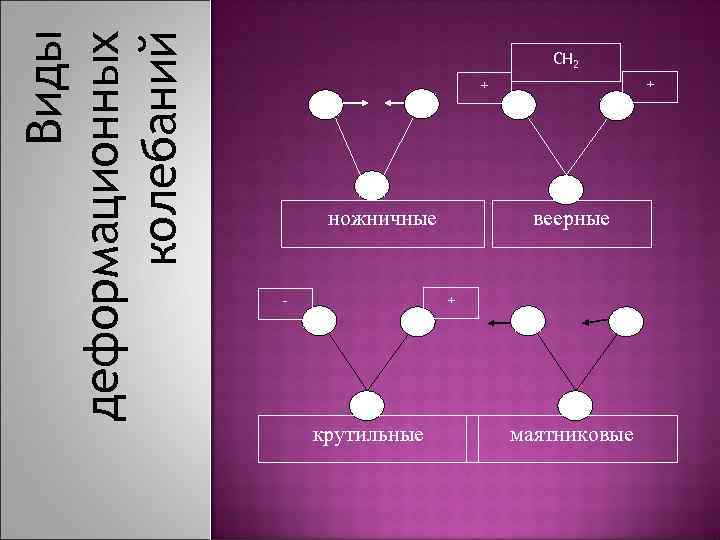
Виды деформационных колебаний CH 2 + + ножничные веерные + - крутильные маятниковые

Энергия поглощаемая атомами при ИК – облучении: где ν, см-1 – частота колебаний; h – const Планка, 6, 6 10 -34 Дж с; υ – квантовое число (0, 1, 2…). Например, υ изменяется от 0 до 1, тогда: - характеристическая частота атомного перехода υn υ3 υ2 υ1 υ0 …………… 16
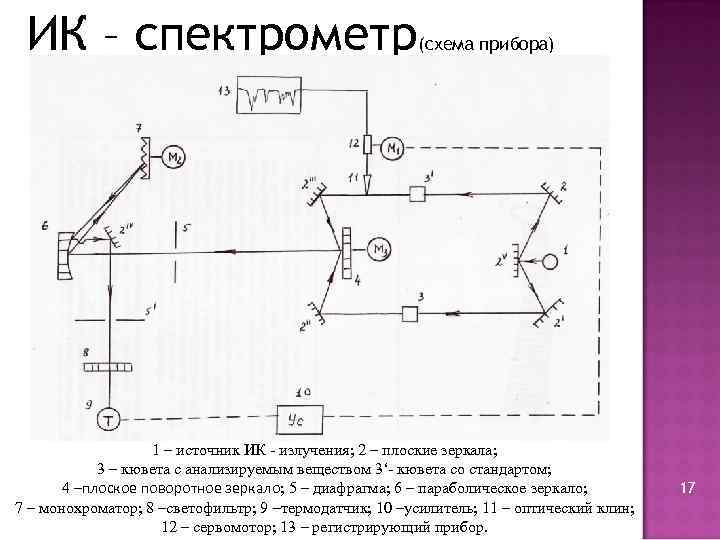
ИК – спектрометр (схема прибора) 1 – источник ИК - излучения; 2 – плоские зеркала; 3 – кювета с анализируемым веществом 3‘- кювета со стандартом; 4 –плоское поворотное зеркало; 5 – диафрагма; 6 – параболическое зеркало; 7 – монохроматор; 8 –светофильтр; 9 –термодатчик; 10 –усилитель; 11 – оптический клин; 12 – сервомотор; 13 – регистрирующий прибор. 17

Глобар – Si. C (T=1400 0 C) Штифт Нернста - Zr. O 2 ; Y 2 O 3 ; Th 2 O 3 (T=1200 0 C) Монохроматоры Дифракционные решетки или призмы из галогенидов щелочных или щелочноземельных металлов Li. F, Ca. F 2, Na. Cl, KBr. 18

Спектральный метод анализа Схема энергетических состояний атомов En …………… E 2 E 1 E 0 Источники возбуждения: Пламя газовой горелки – Т=1700 -4800 0 C; Электрическая дуга - Т=7000 -10000 0 C; Высоковольтная искра - Т=10000 -40000 0 C. Наблюдается линейчатый спектр в волновом диапазоне: λ=100800 нм. При использовании искрового разряда в спектрах образуется большое число линий: Mn – 138; Cu – 530; Fe – 3257. 19
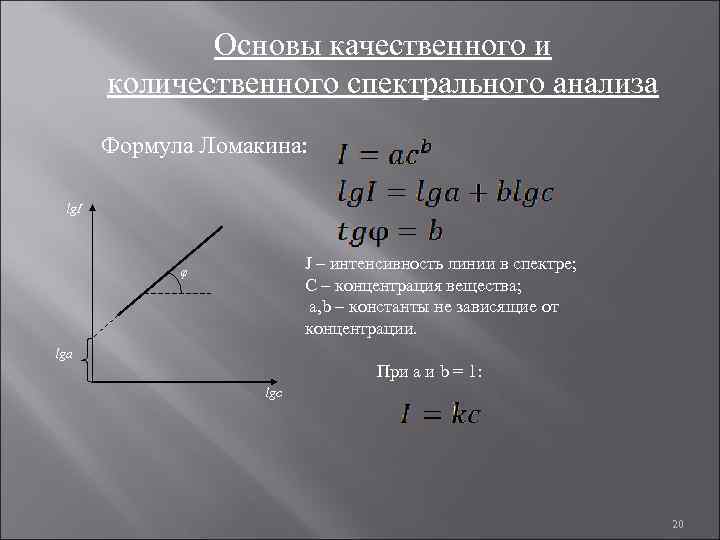
Основы качественного и количественного спектрального анализа Формула Ломакина: lg. I J – интенсивность линии в спектре; C – концентрация вещества; a, b – константы не зависящие от концентрации. φ lga При a и b = 1: lgc 20
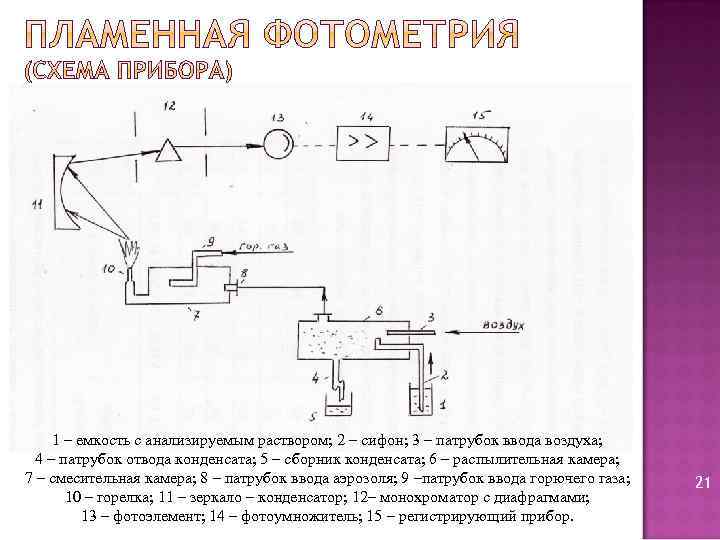
1 – емкость с анализируемым раствором; 2 – сифон; 3 – патрубок ввода воздуха; 4 – патрубок отвода конденсата; 5 – сборник конденсата; 6 – распылительная камера; 7 – смесительная камера; 8 – патрубок ввода аэрозоля; 9 –патрубок ввода горючего газа; 10 – горелка; 11 – зеркало – конденсатор; 12– монохроматор с диафрагмами; 13 – фотоэлемент; 14 – фотоумножитель; 15 – регистрирующий прибор. 21

Источники и методы люминесценции: 1. 2. 3. Хемолюминесценция Катодолюминесценция Триболюминесценция 4. Флуоресценция Основные характеристики люминесценции Выход люминесценции (ρ) – это степень трансформации энергии возбуждения в энергию люминесценции: 1. Основные законы люминесценции: Закон Стокса-Люммеля: ρ 2. Закон Вавилова λ 1 λ 2 λ, нм
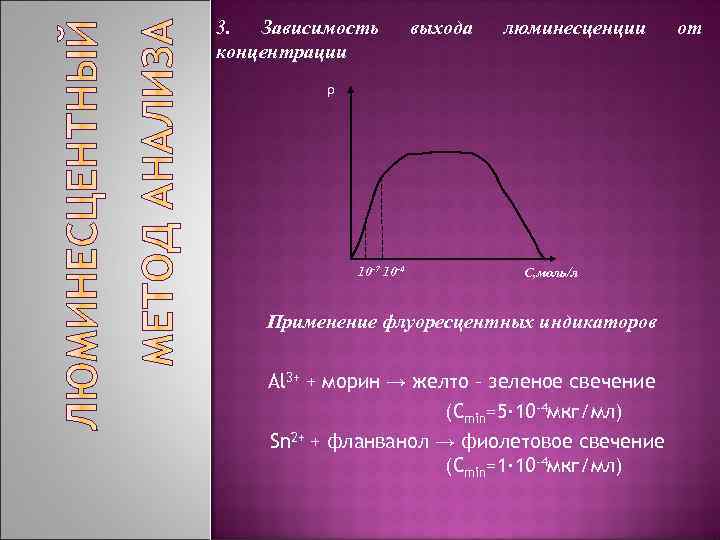
3. Зависимость концентрации выхода люминесценции ρ 10 -7 10 -4 С, моль/л Применение флуоресцентных индикаторов Al 3+ + морин → желто – зеленое свечение (Сmin=5∙ 10 -4 мкг/мл) Sn 2+ + фланванол → фиолетовое свечение (Сmin=1∙ 10 -4 мкг/мл) от

I α Если среда II более плотная, чем I, то (а) а) ∟α >∟β: и наоборот: (∟α <∟β) При ∟β=900 - ∟α<900 II β I α Полное внутреннее отражение ∟β=900 Sinβ =1 б) II β α’ – угол полного внутреннего отражения
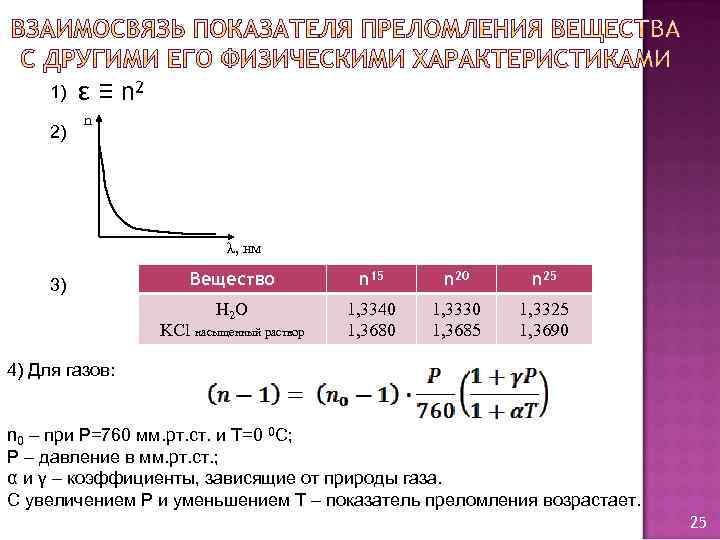
1) 2) ε ≡ n 2 n λ, нм Вещество n 15 n 20 n 25 H 2 O 3) 1, 3340 1, 3680 1, 3330 1, 3685 1, 3325 1, 3690 KCl насыщенный раствор 4) Для газов: n 0 – при Р=760 мм. рт. ст. и Т=0 0 С; P – давление в мм. рт. ст. ; α и γ – коэффициенты, зависящие от природы газа. С увеличением Р и уменьшением Т – показатель преломления возрастает. 25
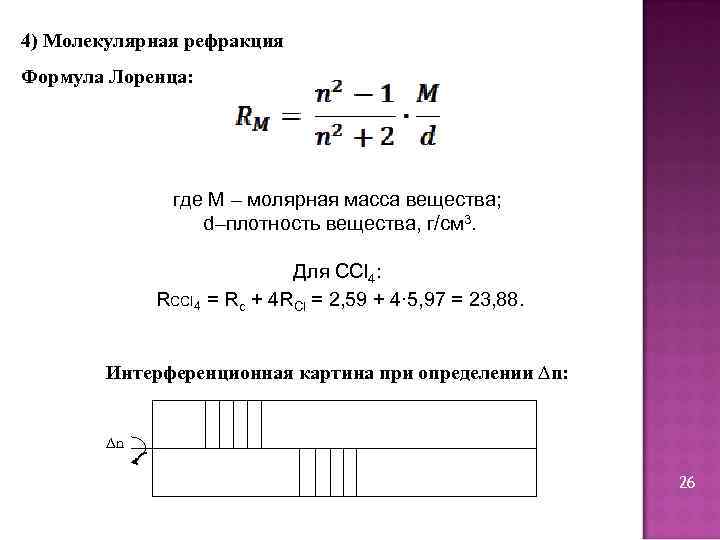
4) Молекулярная рефракция Формула Лоренца: где М – молярная масса вещества; d–плотность вещества, г/см 3. RCCl 4 Для CCl 4: = Rc + 4 RCl = 2, 59 + 4∙ 5, 97 = 23, 88. Интерференционная картина при определении ∆n: ∆n 26

РЕНТГЕНОФЛУОРЕСЦЕНТНЫЙ МЕТОД АНАЛИЗА N M ≡ ≡ α 1 ≡ L K β 1 Закон Мозли: z- порядковый номер элемента в таблице Д. И. Менделеева; λ- длина волны , нм; R – const Ридберга; m – масса покоя электрона; e – элементарный заряд электрона; h – const Планка; c – скорость света в вакууме. Элемент № 28, Ni Элемент № 26, Fe W – выход флуоресценции; W для К-линий кислорода равен 0, 08%; W для К-линий меди равен 0, 40%. 27
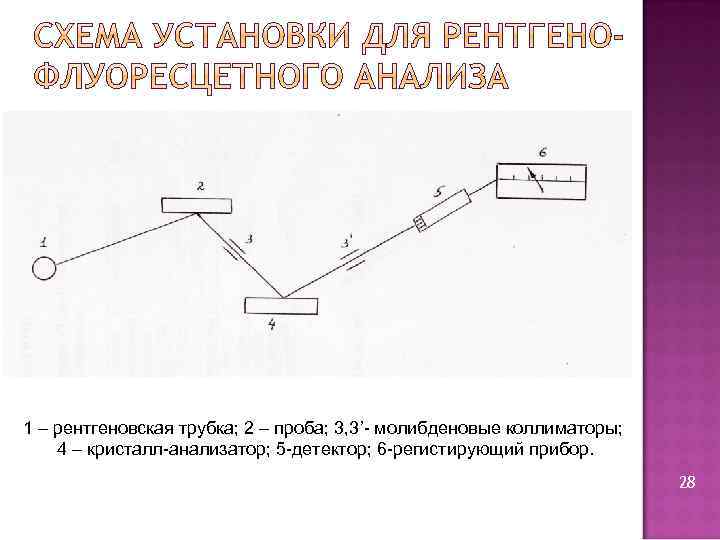
1 – рентгеновская трубка; 2 – проба; 3, 3’- молибденовые коллиматоры; 4 – кристалл-анализатор; 5 -детектор; 6 -регистирующий прибор. 28
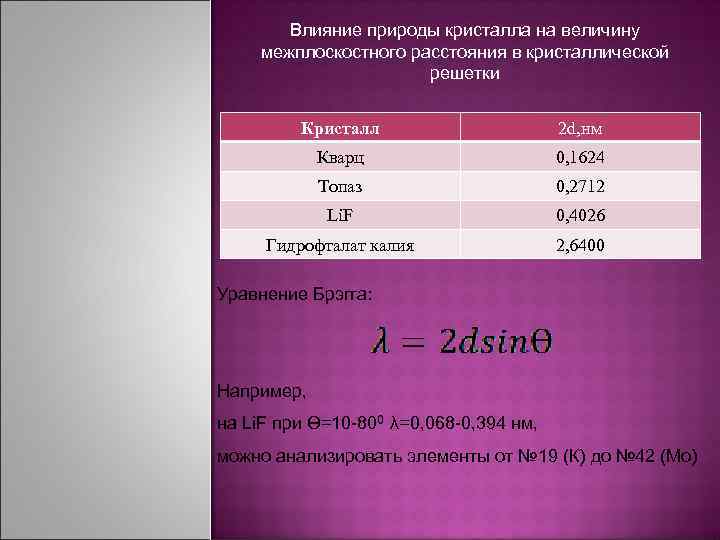
Влияние природы кристалла на величину межплоскостного расстояния в кристаллической решетки Кристалл 2 d, нм Кварц 0, 1624 Топаз 0, 2712 Li. F 0, 4026 Гидрофталат калия 2, 6400 Уравнение Брэгга: Например, на Li. F при ϴ=10 -800 λ=0, 068 -0, 394 нм, можно анализировать элементы от № 19 (К) до № 42 (Mo)

I, мк. А В Полярографический метод анализа Ярослав Гейровский, 1922 г. С А 0 Е 1/2 I- сила тока, мк. А; n – число электронов, принимаемых ионом при восстановлении; D – коэффициент диффузии иона, (см-2∙с-1) m - масса капли ртути, вытекающей из капилляра (катода) за 1 с (1 мг/с); τ – период жизни ртутной капли, (с); c – концентрация определяемого иона, (моль/л)/ Е, В В реальных условиях проведения анализа: 30
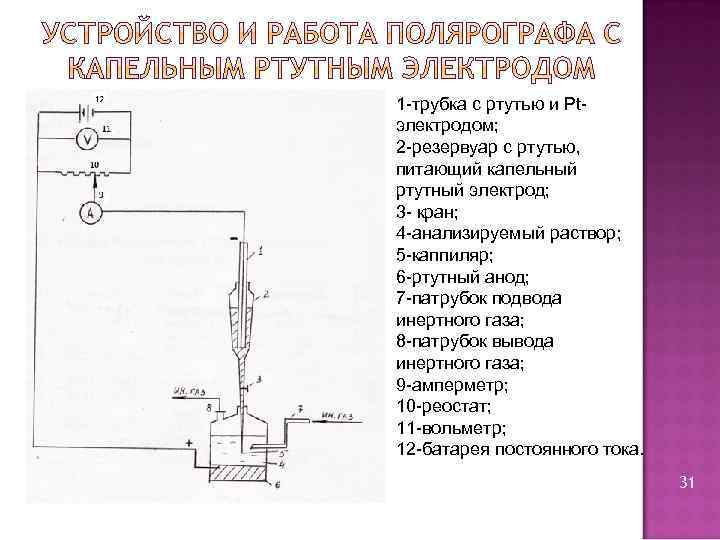
1 -трубка с ртутью и Ptэлектродом; 2 -резервуар с ртутью, питающий капельный ртутный электрод; 3 - кран; 4 -анализируемый раствор; 5 -каппиляр; 6 -ртутный анод; 7 -патрубок подвода инертного газа; 8 -патрубок вывода инертного газа; 9 -амперметр; 10 -реостат; 11 -вольметр; 12 -батарея постоянного тока. 31

Методы для количественного анализа а) калибровочных кривых С 1 h 1 С 2 h 2 …. . Сn hn h, мк. А б) стандарта в) добавок c, моль/л hобщ= h. A+ hст h. A = hобщ – hст CA – концентрация анализируемого раствора, моль/л; Сст - концентрация стандартного раствора в полярографической ячейке, моль/л; Сст’ – концентрация приготовленного стандартного раствора, моль/л. 32

Амперометрическое титрование 1)Pb 2+ +SO 42 -→Pb. SO 4↓ I титрант 2)SO 42 -+ Pb 2+-→Pb. SO 4↓ титрант 3)Pb 2+ +Cr 2 O 72 -→Pb. Cr 2 O 7↓ титрант 3 2 1 V 1, V 2 , V 3 V, мл, титранта 33
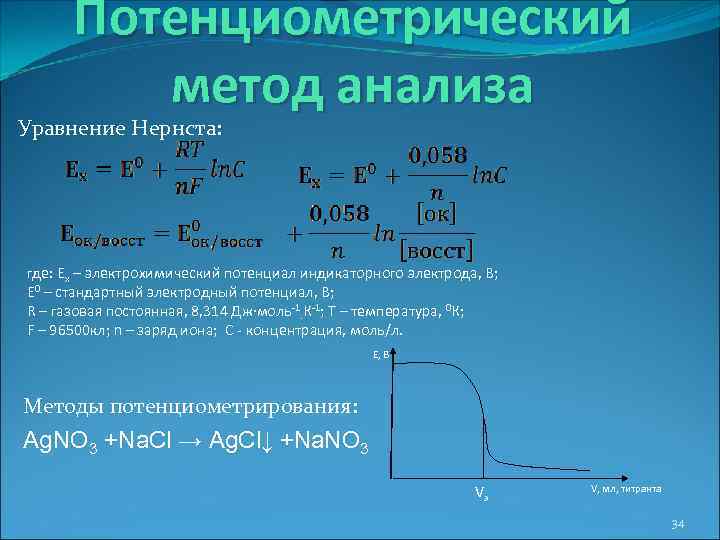
Потенциометрический метод анализа Уравнение Нернста: где: Ex – электрохимический потенциал индикаторного электрода, В; Е 0 – стандартный электродный потенциал, В; R – газовая постоянная, 8, 314 Дж∙моль-1∙К-1; Т – температура, 0 К; F – 96500 кл; n – заряд иона; C - концентрация, моль/л. E, B Методы потенциометрирования: Ag. NO 3 +Na. Cl → Ag. Cl↓ +Na. NO 3 Vэ V, мл, титранта 34
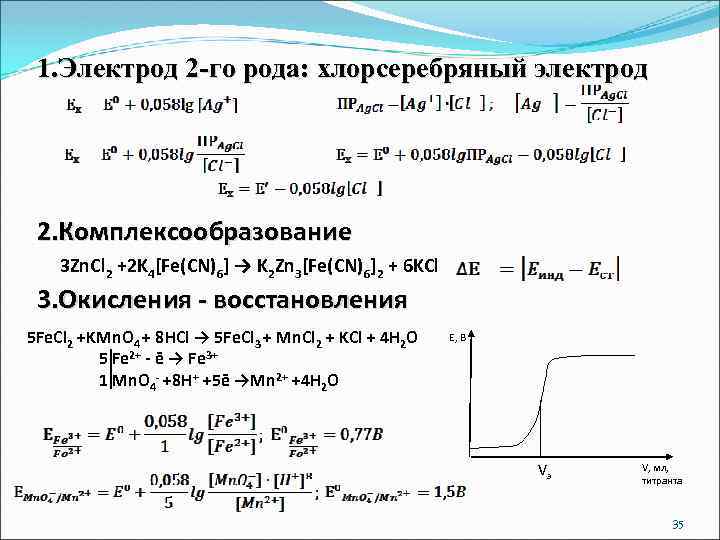
1. Электрод 2 -го рода: хлорсеребряный электрод 2. Комплексообразование 3 Zn. Cl 2 +2 K 4[Fe(CN)6] → K 2 Zn 3[Fe(CN)6]2 + 6 KCl 3. Окисления - восстановления 5 Fe. Cl 2 +KMn. O 4 + 8 HCl → 5 Fe. Cl 3 + Mn. Cl 2 + KCl + 4 H 2 O 5 Fe 2+ - ē → Fe 3+ 1 Mn. O 4 - +8 H+ +5ē →Mn 2+ +4 H 2 O E, B Vэ V, мл, титранта 35

Электроды в потенциометрии Водородный электрод Каломельный электрод Стеклянный электрод 36

ЭЛЕКТРОГРАВИМЕТРИЯ Соосаждение: адсорбционное; окклюзия; изоморфизм; химическое. Pb. Cl 2 +H 2 S → Pb. S↓ + 2 HCl Pb. Cl 2 + Pb. S → [Pb. Cl]2 S ↓ Электролиз водного раствора H 2 SО 4 на Pt – электродах: Катод: 2 Н+ + 2ē → Н 2↑ Анод: H 2 O - 2ē → 2 Н+ +1/2 О 2↑ Электролиз 1 М растворов солей Ag+ , Cu 2+ : Ag выделяется при U=0, 9 B; Cu выделяется при U=1, 4 B Электролиз при совместном присутствии ионов Cu 2+и Zn 2+ Добавляется HNО 3 как деполяризатор: NO 3 - +10 H+ +8ē→NH 4+ + 3 H 2 O Электролиз комплексных соединений: [Ag(CN)2]- 37
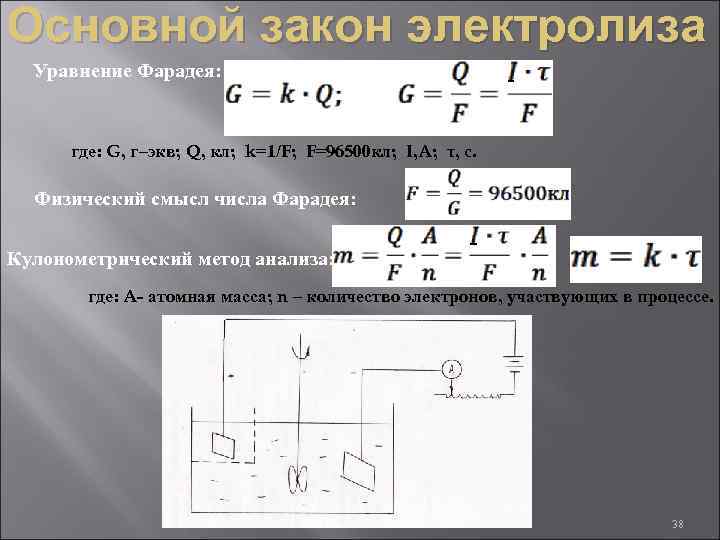
Основной закон электролиза Уравнение Фарадея: где: G, г–экв; Q, кл; k=1/F; F=96500 кл; I, A; τ, c. Физический смысл числа Фарадея: Кулонометрический метод анализа: где: A- атомная масса; n – количество электронов, участвующих в процессе. 38

Кулонометрическое определение содержания K 2 Cr 2 O 7 Содержание кулонометрического ячейки: -K 2 Cr 2 O 7 -Избыток Fe 3+ -цветной индикатор на Fe 3+ +ē→ Fe 2+ Катодный процесс: Кондуктометрический метод анализа 39

Удельная электропроводность 0 некоторых растворов при 18 С Раствор К, H 2 O, дист. 10 -5 HCl, 20% раствор 0, 76 H 2 SO 4 30% раствор 0, 76 Na. Cl, 25% раствор 0, 21 Ca. Cl 2 25% раствор 0, 18 40
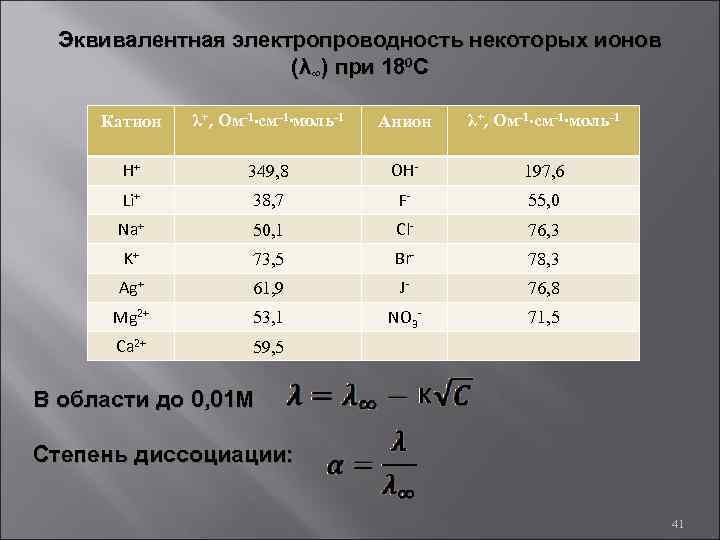
Эквивалентная электропроводность некоторых ионов (λ∞) при 180 С Катион λ+, Ом-1∙см-1∙моль-1 Анион λ+, Ом-1∙см-1∙моль-1 H+ 349, 8 OH- 197, 6 Li+ 38, 7 F- 55, 0 Na+ 50, 1 Cl- 76, 3 K+ 73, 5 Br- 78, 3 Ag+ 61, 9 J- 76, 8 Mg 2+ 53, 1 NO 3 - 71, 5 Ca 2+ 59, 5 В области до 0, 01 М Степень диссоциации: 41
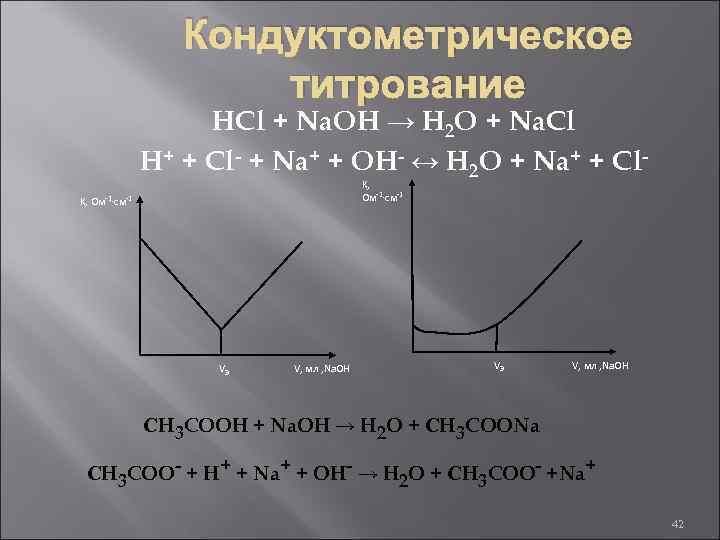
Кондуктометрическое титрование HCl + Na. OH → H 2 O + Na. Cl H+ + Cl- + Na+ + OH- ↔ H 2 O + Na+ + Cl. K, Ом-1∙см-1 VЭ V, мл , Na. OH СH 3 COOH + Na. OH → H 2 O + СH 3 COONa СH 3 COO- + H+ + Na+ + OH- → H 2 O + СH 3 COO- +Na+ 42

Осадительное кондуктометрическое титрование KCl + Ag. NO 3 → Ag. Cl↓ + KNO 3 K+ + Cl- + Ag+ + NO 3 - ↔ Ag. Cl↓ + K+ + NO 3 K, Ом-1∙см-1 VЭ V, мл , Ag. NO 3 VЭ V, мл , Ba(OH)2 Mg. SO 4 + Ba(OH)2 → Mg(OH)2↓ + Ba. SO 4 ↓ сильноразб. р-р 43

Экстракция Интенсификация процесса экстракции с использованием эффекта «высаливания» . UO 2(NO 3)2 + 2 ТБФ ↔ [UO 2(NO 3)2 ∙ 2 ТБФ] UO 2(NO 3)2 ↔ UO 22+ + 2 NO 3 HNO 3 ↔ H+ + NO 3 - Количественные характеристики процесса экстракции. 1. Коэффициент распределения: 2. Константа распределения: 3. Фактор извлечения: СЭ – концентрация компонентов в экстракте; Ср – концентрация компонента в рафинате. * – в состоянии равновесия. mизв – масса извлеченного компонента; mисх – масса компонента в исходной пробе. 4. Коэффициент разделения: 44
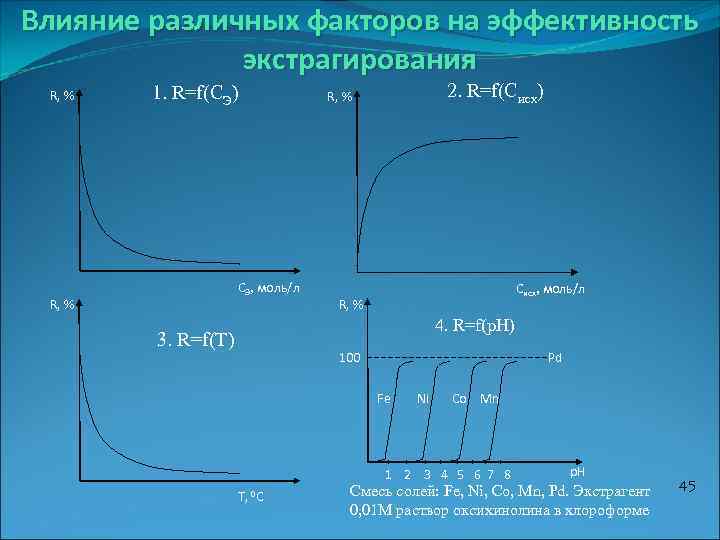
Влияние различных факторов на эффективность экстрагирования R, % 1. R=f(CЭ) CЭ, моль/л R, % 2. R=f(Cисх) R, % Cисх, моль/л R, % 4. R=f(p. H) 3. R=f(T) 100 Pd Fe Ni Co Mn 1 2 3 4 5 6 7 8 T, 0 C p. H Смесь солей: Fe, Ni, Co, Mn, Pd. Экстрагент 0, 01 М раствор оксихинолина в хлороформе 45
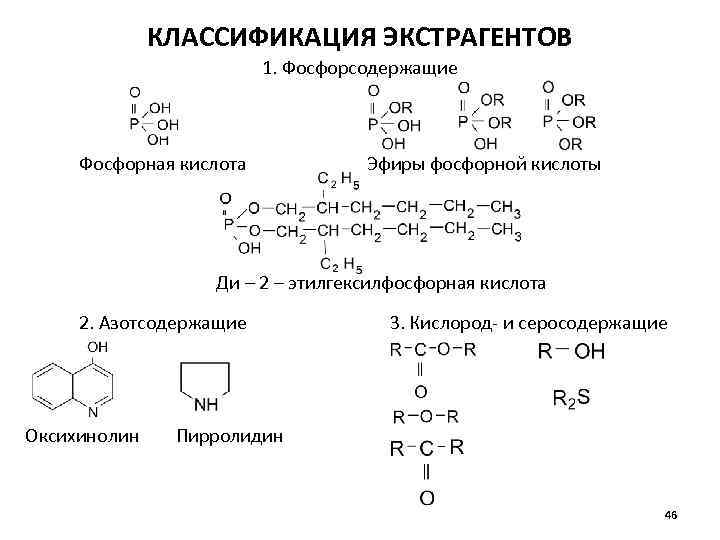
КЛАССИФИКАЦИЯ ЭКСТРАГЕНТОВ 1. Фосфорсодержащие Фосфорная кислота Эфиры фосфорной кислоты Ди – 2 – этилгексилфосфорная кислота 2. Азотсодержащие Оксихинолин 3. Кислород- и серосодержащие Пирролидин 46

4. Ди- и полидентные МЕХАНИЗМЫ ЭКСТРАГИРОВАНИЯ. Сольватационный UO 2(NO 3)2 + 2 ТБФ ↔ [UO 2(NO 3)2 ∙ 2 ТБФ] Ионный Bi(NO 3)2 + 4 HR ↔ [Bi. R 3∙HR] + 3 HNO 3 Изменениe сродства к воде Оксониевый 47
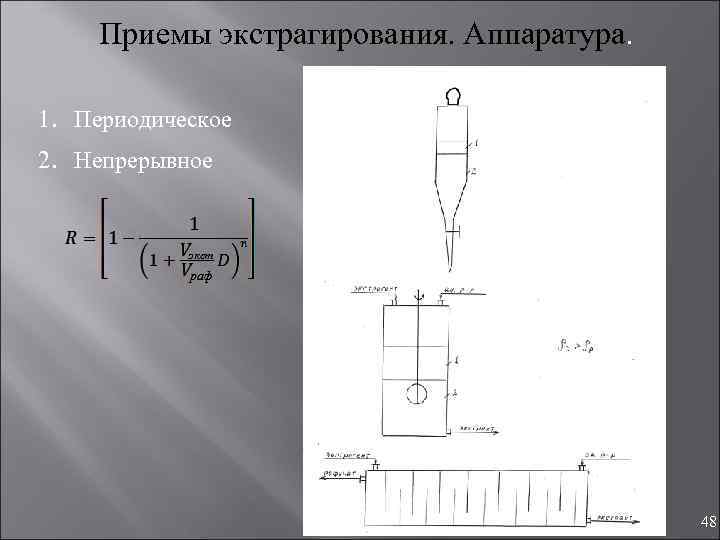
Приемы экстрагирования. Аппаратура. 1. Периодическое 2. Непрерывное 48
Физико-химические методы анализа(часть 2).ppt